(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗОФУРАНА





Изобретение относится к новому способу получения новых соединений формулы 1 где Р и Q - атом водорода, низший алкил или Р и Q вместе низшая алкиленовая группа или дополняют конденсированное бензольное кольцо; R - атсм водорода, низпшй ал D - непосредственная связь, остаток фенилена или сти рилидена, причем имеющие ся в остатке D-двойные связи расположены таким образом, что они находятся в соп яжении с двойными связями одного или нескольких остатков бензофурана. Эти соединения могут быть исполь зованы в качестве оптических вателей. Известен способ получения 2-(п-нит|эофенил) -бензофурана циклизацией 2-(п-нитробензилокси)-бензофуранальдегида в среде метанола в присутствии карбоната калИя в качестве конденсирующего средства при нагревании 1 . Однако этим способом можно получить только 2-(п-нитрофенил)-бензофуран, так как только в этом случае исходное соединение благодаря нитро группе является реакционноепособнь В случае зеилены нитрогруппы другими группами исходное соединение недостаточно реакцибнноспособно, и циклизации с образованием фуранового . кольца не происходит. Целью изобретения является универсальный способ получения новых производных бензофурана. Предлагаемый способ заключаетеи в том, что соединение формулы II . R 0-СН,-1 -,. где 0,Р,(и R имеют вышеуказанные значения;
725559 E фенил, незамещенный или эаме(енный атомом галогена, причем возможные заместители у О не должны содержать атомов водорода, которые так же легко могут быть зайещены атомами металл4, как aVомы водорода Соседней с р м тильной группы, . подв аргают взаимодействию с гидроокиоью амидом или алкоголятом щелочного нли щёлочноземельного металла в среде растворителя формулы III (А1К)у где Atk - низший йлкйл; ; , Ас - остаток низкомолекулярной :карбоноврй кислоты с число атомов углерода от 1 до - четырех или остаток фосфор -----.----- нЬЙкисжзГыЛ ---- Й-ЪснШнс1сггь Кислоты| ;.. V - целое число равное 0,1 или 2, или тетраметилмочевины, N -мётилпиррЪЗТййбна или Шето нитрила при20-15р С. Соответствующая настоящему изоСре тёЙ:й 0 й6вая реакция циклизации осуl e efвл1чётсЖ в сйЛьНО полярном оргайи ч ШШ1Ж -р тв6рЙтелё,хараК1;ёрйзук)ЩИм ся рН от нейтральной до основной области, который ев ободён ;0т присутствия атомов, способных замещаться щелОчным металлом, IB частности, свобо||Ш ШШйсутст6йя атомов водорода. ПрезйДё Всего в качестве рас твор71Теля могут быть исНользованы алкилированййе ЙЙЙЛайидЫ, соответствующие общей формулы Д11, где Atk - низший алкил; А - ofefafoK низкомолёкулйрной карбоновой кислОтbj, coдep жащёй ДОчёт йрех атомб1ЁГ уг лерсща, в ос(эЬёнйости7 Ьстаток муравьиной кислоты и уксуснойк й 5ЛОтЁ1, или ос таток фосфорной кислот1а Т W-ocHOBHOcTb кислоты, т.ё. СКОЛЬКО эКбШалёнтШ) oewoванйя может связать кислот V - значения 0,1 или 2, прёиму . щественнЪ 1или 2, в особе -. нрсти-2, .. -;«-- а Найболёё предпочтительны соединения формулы 111, в которых V принимает значение 2. Среди этих соединений интерес представ л яет;дймётйл(| орм1амид, гексаметилтриамид фосфорной . киcлotьi, диэтилформамид и диметилаце .тамид. .. ., . Растворитель может быть ,иcпoльзp rSFё; йё;i(Э 4iв;идё;:илйs растворителей.-- Г °Ж1к11чШтее° йЖШ Ь- Чзсн«Ш}Ш ег;;кон д йСйрующего средства использукУт сЬё дййенйя щелочных йЛй щелОчноземель(:5S fr 5iJ-:i ;;X i- r44г .. .Д У-Ч;г--. Л--.ч : - --ifL. ,--V:v - -.----ных металлов, например их гидроокиси, амиды или алкогрляты. в качестве алкоголятов используют получаемые из линейных, разветвленных или циклических низших алифатических спиртов, содержащих до 8 атомов углерода, преимущественно из линейных спиртов, содержащих 1-4 атомов углерода. . Наиболее предпочтительно использовать соединения натрия или калия, среди которых особое практическое значение имеют гидроокиси, амиды и алкоголяты этих металлов. Предпочтительно конденсирующее средство используют в эквивалентном количестве или превышающем эквивалентное, особенно в случаях, когда срединения содержат группы, способные гидролизироваться,.или когда реакцию необхОДИМО проводить при повышенных теМпература;х и когда в некоторых случаях часть конденсирующего средства расходуется в результате реакции с растворителем. Если в исходных соединениях для конденсации содержатся чувствительйыё к гиДрЪлизУ группы, например сложноэфирные карбокислотные то, при поВьп.1енныХ температурах выделяют продукт крндёнсации, в котором эти ГРУППЫ полнЪстКюГйдролизованы, например, в зависимости От способа обработки, выделяют свободную карбоновую кислоту или соответствующую соль карбоновой кислоты. Преимущество способа заключается в том, что обычно реакцию можно проводитьв мягких условиях. При проведении реакции нет необходимости Йспользовать температуры выше 160 С. Часто реакцию проводят при комнатной температуре, особенно в случае исйОльзованйГ алкоголята калия или гидроокиси калия. Однако в некоторых случаях предпочтительно или даже необходимо реакционную сМесь, которую целесообразно держать в атмосфере азота, медленно нагревать от 30 до 120 С иifSteM В; те еийё некоторого времени выдерживать при этой температуре. Целевой пройук т получают с количественным выходом. Продукты взаимодействия могут быть выделены из реакционной смеси с помощью обычных.известных методов. Пример 1 , 21,1г iw ,ш-бис-(о-формилфенокси)-дибензила нагревают При температуре кипения с 4,7 г анилина и 0,05 г п-толуолсульфокислоты в 250 лл толуола в течение 2 ч, причем отщепляющуюся в процессер акцйи воду Ьтдёлййт с помощью водоотделителя. Неп(5средствейно после этого реакциойную Смесь охлаждают, отсасывают образовавшийся осадок, промыsaiDT его спиртом и затем сушат в вакууме при 60с.
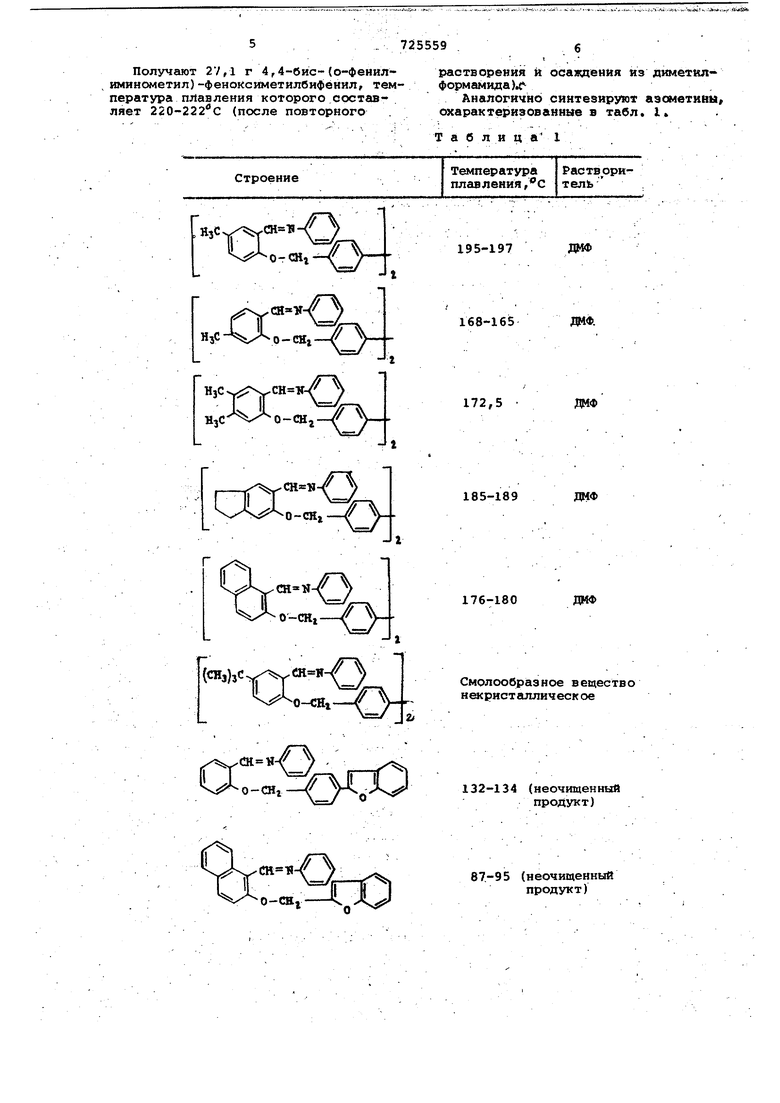
Получают 27,1 г 4,4-б ис-(о-ф енилиминометил)-феноксиметилбифёнил, температура плавления которого составляет 220-222С (после повторного
.# 0-СНг
725559
растворения и осаждения яз диметилФормамида).
Аналогично синтезируют аэометийы охарактеризованные в табл. I
Т а б л и ц а 1
132-134 (неочищенный продукт)
0-CHj
87-95 (неочищенный продукт)
7255598
Продолжение табл. 1
167-169
160-163 Однако в большинстве случаев нет необ :одимости в промежуточном выделе ний или в очистке азоиётинов. Предпо чтительно обработку реакционной смеси njiOHSB од ят отгонкой в вакууме рас Ш&ЖтёЙя, использованного лри получе НИИ аэометина-, с последующей заменой йеЯхбЙящшй дИПОлярным растворителем И нёпосредственньал проведением реакции замыкания цикла, описанной в при мерах 2-6 . Пример 2. 57,2 г 4,4-1бис-о-(фенилиминометил)-феноксиметил -бифёнила, суспендируют в 400 мл диметилформамида. К приготовленной сус пензии прибавляют 12,5 г гидроокиси калия (порошкообразная, 90%-ная). Реакционнук смесь медленно нагревают до 100-120 С; тёмперат5ФУ поддерживают в течение 3 ч, непосредственно пбсле этого реакцйоннуто смесь рхйаждают до комнатной температуры и ртфй 1Ьтррвьшают выделившийся в (Осадок продукт. ЕгЬ сначала промывают димет;ил 1 ормамидом, затем водой до нейтр льной реакциИ прот-плвнйх вбд, после чего продукт сушат в вакууме при , йсазанным спрсобом пРлучайт 36 г неочищенного продукта, соответствующего формуле 4,4-бис-(2-бензофурил)-бифенила, который затем подвергают очистке переосажДением из б1г-хлорнафталина; т.пл, 350 С, Найдено,%: С 87,7; Н 4,80. (368,45) . . Вьтислено,% : С 87,7; Н 4,79, А.акс(абсорбция, ДМФ) 551 мм; « 7,06-10. И р и мер 3. 40,3 г N-jo-tn-(Бензофурил-2-)-бензилокси)-бензилиден -анилина растворяют в 400 мл диметилформгииида. К полученному раствору прибав1лян т 7 г гидроокиси калия (порошкообразная, 85%-ная), реакционную смесь Сначала перемешивают в течение 30 мин при Температуре 60°С и затем в течение 60 миН при температуре 11 . Непосредственно после 9ТОГ6 реакционную смесь охлаждают на ледяной бане примерно до 5 С, после чего отфильтровывают выделившийся в осадок продукт. Полученный продукт ripРмывают сначала метиловым спиртом, а затем водой. ПРсле сушки в вакууме при получают 30,5 г неочищенного продукта, соответствующего 4,4-бис-(2-бензофурил)-фенилу. неочищекНое веществЬ йерекристешлИзовывают из диметилфб13мамида при добавлении активированного угля. Температура плавления полученного продукта составляет 308-309 с. По ансшогий с описанным выше примером синтезировали соединения, указанные в табл. 2,
Таблица 2
100
197г-198 дафКОН
290дафКОЯ
110
350тлNaOH125
125
350ДМАNaOH S350дал 350 ГМТАФК 35о дал 350jyffi 287-293 1451тЯ NaOH К-трет-бутйлаткон кон КОН
725559
11
12
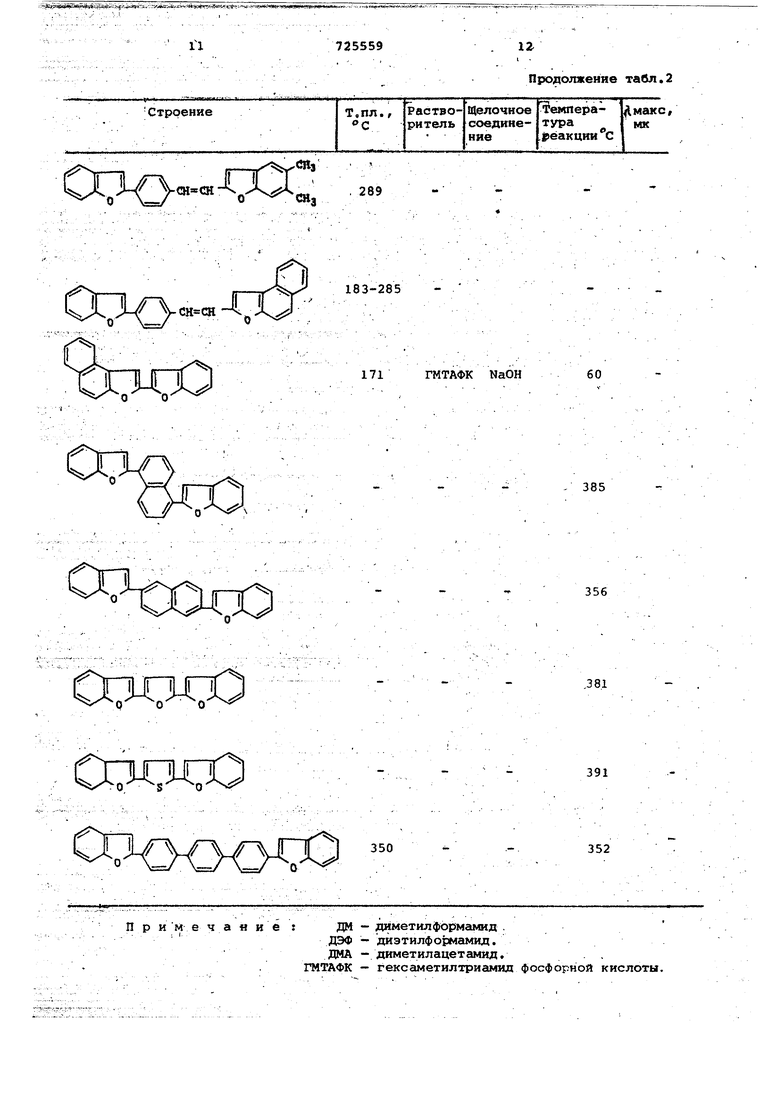
Продолжение табл.2
. 289
183-285
60
171 ГМТАФК NaOH
385
ом: I :urii
356
О SО
о- -оПри м е ч а « и е : ДМ ДЭФ - ДМА ГМТАФК -
381
391
352 диметилформамид . диэтилформамид. диметилацетамид. . . гексаметилтриамид фосфорной кислоты.
Аналогично процесс проводят когда используют в качестве конденсирующего -агента амид натрия и в качестве растворителя тетраметилмочевину, N-метилпйрролидон или ацетонитрил. Формула Изобретения
Способ получения производных бензофурана Формулы
где D,p,q и R
имеют выщеуказаннные значения; .
Е - фенил, незамещенный илиГ9йМещенный атомсм галогена, причем возможйые заместители у D не должны содержать атомов водорода, которые так же легко могут быть замещены атома1ЛИ металла, как атомы водорода соседней с .D метильной группы,
подвергают взаимодействию с гидроокисью, амидом или алкоголятом щелочного или щелочноземельного металла в среде растворителя фо|рмулы где Р и Q - атом водорода, низший ) алкил или Р и О. вместе низшая алкиленовая группа или дополняют бензоль ное кольцо; R - атом водородй, низший алкил; D - непосредственная связь, остаток фенила, бифениле на или стириЛИДена, причем имеющиеся в О4ртатке D двойные связи расположёны таким образом, что они находятся 6 сопряжении с двойными связями одного или нескольких ос татков бензофурана, а ю щ и и с я тем, что со о т л и ч динение формулы R R О-сИг-В (..«) г. ACk - низший алкил Ас - остаток нчзксмолекулярной карбоновой кислоты с числом атся-1ов углерода от 1 до 4, или остаток фосфорной кислоты;W - основность кислоты; V - целое Число, разное 0,1 .. ,или 2, или тетраметилмочевины, N - метил ролидона или ацетонитрила при .. Источники ийфо1 лации нятые во внимание при экспертизе 1. К.В.Ь. Mathyr. 3. Chem. Socr. 0, с . 1954.
Авторы
Даты
1980-03-30—Публикация
1976-01-28—Подача