Предлагаемый способ получения производных имидазола заключается в том, что соединение общей формулы Ttt Z-C-(A))n-W (3) С -С -алкилгде W - атом гашогена, сульйюнат, бензолсульфонат или толуолсульфонат, подвергают взаимодействию с ими дазолом общей формулы или солью имидазола в присутствии инертного растворителя при 50-180 С. Целевой продукт выделяют в свобод ном виде или в виде соли с TaKUNM ки , как соляная, азотная, бромис товодородная, серная, хлорная, фосфо ная, уксусная, щавелевая, яблочная, винная,лимонная, или в виде комплексов с солями металлов. К солям металлов, которые могут быть использованы, относятся соли, образованные катионами таких металлов, как Мд, Са, Ва, Sn, Pb, Си, Zn Cd, Cr, Мп, Fe, Co, Ni и анионами, например хлоридом, бромидом, йодидом сульфатом, бисульфатом, фосфатом,, нитратом. Реакцию взаимодействия проводят с эквимолекулярным или избыточным количеством имидазола ил соли имидазола. В качестве инертног растворителя применяютводу, метанол, этанол, изопропанол или этиленгликоль, а также апротонные раст ворители, такие как диметилсульфокс ацетонитрил,.диметилфррмамид, нитро метан или. ацетон. Пример 1. 1 - р)-(2 , 4-Дихло фенил)-гексил имидазол. К 27,2 г 10,4 моль) имидазола пр 95°С добавляют 31,8 г (0,098 моль) 2-(2,4-дихлорфенил) гексилметансульфоната и смесь перемешивают при 95°С в течение 16 ч. К концу этого периода реакционную смесь охлаждаьэт выливают в 500 мл воды, перемешивают в течение 1 ч, органр ческое вещество отделяют и воддный слой экстр гируют эфиром. Эфир соединяют с органи 1еской фазой и после промывки водой высушивают и концентрируют. 24,4 г (88%). Имидазол иденти фицирован методами ИК, ЯМР и элемен тарного анализа. Его чистота, превы шающая 95%, определена методом газо жидкостной хроматографии. Пример 2. Хлористоводород ный (2,4-дихлорфенил)гексил имидазо.л. Через раствор 30,0 г (0,101 моль (2 , 4-дихлорфенил) гексил ими да.-зола ,в 200 мл эфира барботирует сух газообразный хлористый водород до оявления кислой реакции смеси по акмусу. Образующиеся бесцветные кристаллы фильтруют и получают 24,Ь г хлористоводородной соли. Пример 3. (2 , 4-Дихлорфенил) гексил имидазол-цинкхлорид. А. К раствору 2,0 г (0,0067 моль) 1- р) - ( 2 , 4-ДИ хлорке ни л) га к си л имидазоа в 10 мл абсолютного этанола добавяют по каплям раствор 0,46 г (0,0036 моль) хлористого цинка в 30 мл абсолютного этанола. Реакционную смесь перемешивают при комнатной температуре в течение 10 мин и растворитель отгоняют под вакуумом. Целевой продукт выделяют в виде белого стеклообразного вещества. Б. 2,0 г. (0,0067 моль) l-({V-{2,4-дихлорфенил)гексил имидазола и 0,92 г (0,0067 моль) хлористого цинка смешивают в 40 М.П растворителя ацетон /метанол/ вода (1:1:2)., Пример 4. )-( 2, 4-Ди хлорфенил) гексил имидазол-оксалат. К раствору 4 г (0,0135 моль) 1- fb- (2 , 4-дихлорфенил) гексил имидазола в эфире добавляют по каплям раствор 1,7 г (0,0135 моль) щавелевой кислоты в 10 мл метанола, образующийся белый осадок фил.ьтруют и высушивают в вакууме. Выход 3,37 г, т.пл. 126-128°С. По способу, описанному в примере 1, взаимодействием метансульфоната с имидазолом получают с -заме;ценнь й продукт. Пример 5. (2 ,4-Дихлорбензил)гексил имидазол. Целевой продукт получают способом, описанным в примере 1, его чистота, превышающая 95%, определена методом газожидкостной хроматографии. Пример 6. ( 2 , 4-Дихлорфенил)гептил имидазол. К 10,6 г (0,160 мэ.пь) имидазола добавляют при 95°С 10,9 г (0,042 мэль) сырого 3-(2 ,4-дихлорфенил) гептилметансульфоната. Смесь перемешивают при 95°С в течение 16 ч, охлаждают и выливают в 500 мл воды, перемешивания в течение l ч органический слой отделяют и водный слой экстрагируют эфиром. Эфир созплняют с органическим слоем, пpo -IЫвaют водой, высушивают и растворитель отгоняют. Получают 10,6 г сырого продукта. Пример 7. (2,4-Дихлорфенил)фенетил имидазол. Названное соединение получают способом, описанным в примере 1 , продукт перекристаллизовывают из смеси эфир/ацетон и получают 2,6 г (32%) хлористоводородной соли, т.пл, 197-198с.
Пример 8. (п-Хлорфенил)-п-хлорфенетил имидазол. К 75 глл метанола прибавляют 1,05 г (0,0458 моль) натрия, получают раствор. Затем.к этому раствору добавляют 3,1 г (0,0453 моль) имидазола и растворитель отгоняют досуха. К влгшному твердому остатку добавляют 50 мл Ы,N-диметилформамида. Полученный раствор нагревают до и оставшийся метанол отгоняют. К раствору диметилформамида добавляют 8,.7 г (0,0305 моль) 2-(п-хлорфенил)-п-хлорфенетил-хлорида и смесь нагревают .при в течение 48 ч. Реакционную смесь охлаждают, выливают в ледяную воду и органическое вещество экстрагируют эфиром. Эфирный экстракт охлаждают и обрабатывают газообразным хлористым водородом. Образовавшуюся маслянистую соль отделяют и обрабатывают раствором бикарбоната натрия. Полученную смесь экстрагируют эфиром, эфирный раствор высушивают и растворитель отгоняют, выход 0,6г.
Пример 9. Нитрат ,fj -тетраметилен-IV- (2,4-дихлорфенил) этил имидазола.
Смесь 12 г (0,037 моль) 2,2-тетрамвтилен-2-(2,4-дихлорфенил)зтилметансульфоната, 10 г (0,15 моль) И мдазола и 1 мл диметилформамида нагревают при 140°С в течение 24 ч„ Реакционную смесь выливают в воду и экстрагируют эфиром. Соединенные эфирные экстракты прогиывают водой и высушивают над сульфатом магния. Осушитель отфильтровывают и к эфирному раствору добавляют по каплям концентрированную азотную кислоту. Образующийся белый осадок отделяют фильтрованием и сушат в вакууме. Общий вес полученной соли 3,7 т, т.пл.176-179°С.
Пример 10. 1-(Ь-(2,4-Дихлорфенил)гекснл -4-нитроимидазол. К 1,3 г (0,0307 моль) гидроокиси натрия в 150 лл метанола добавляют 3,5 г (0,0307моль) 4-нитроимида зола, раствор нагревают и метанол отгоняют. К остатку добавляют 10 диметилформамяда и раствор нагревают до для удалэния избытка метанола и воды. Затем раствор охлаждают до те1..1пературы ниже 90 С и добавляют 10,0 г (0,0307 моль) 2-(2, 4-дихлорфекил) гексилметансульфоната. Реакционную смесь нагревают до 145°С в течение 2 ч, затем охлаждают и выпивают в воду. Органическое ве1аество экстрагируют эфиром
После высуаш.вания экстракт перегоняют и получают 11,2 г остатка,Концентрат растирают с гексаном и затем растворяют в 25 мп метанола. Метаноловый раствор медленно вЕлпивают в воду, при этом образуется смолистое твердое вещество. Его отделяют фильтрованием, высушивают и после перекрисгаллизации из смеси ацетон/гексан получают 4,2 г (41%) продукта, т.пл, б7-69с.
0
Пример 11. (2,4-Дихлорфенил)гексил -4,5-дихлоримндазол.
К 100 мл метанола добавляют 1,7 г (0,0735 моль) натрия до полного растворения и вносят 10 г (0,0735 моль)
5 4,5-дихлоримидазола. Смесь перемешивают до исчезновения осадка, затем отгоняют метанол. Влажный остаток добавляют к 50 мл диметилформам да и полученный раствор нагревают
0 до 125 С для удаления метанола и воды. Раствор охлаждают до температуры ниже 100°С и добавляют 2,5 г (0,0735 моль) 2-(2,4-дихлорфенил) гексилметансульфоиата. Реакционную
5 смесь нагревают до 130°С в течение 2 ч, охлаждают, выливают в воду и органическое вещество экстрагируют триждфл (порциями по 200 мл) бензолом,- Соединенные экстракты промывают .дважды (порциями по 50 мл водой,
0 высушивают над безводным сульфатом магния и после концентрирования получают 15,8 г сырого продукта. Его растворяют в эфире и обрабатывают сухим газообразным хлористым водо5родом. Эфирный раствор декантируют с образовавшегося масла и масло растирают дважды (порции по 150 мл) с эфиром. Затем масло обрабатывают 10%-ной гидроокисью натрия и продукт
0 экстрагируют дважды (пориияр. по 200 мл) эфиром. Эфирный раствор высушивают и концентрируют, выход 12,6 г (47%) в виде масла.
П р и f/- е р 12. Йодид 1-1р-(2,45
-дихлорфенил)гексил -3-бутилимидазола.
5,0 г (0,0168 моль) ( 2,4-дихлорфенил) гексил имидазола нагревают в течение 2 ч на водяной бане
0 с 3,1 г (0,0168 моль) 1-йодбутана. Реакционную смесь охлаждают и растирают триждда (порции по 50 мл) с эфиром. Маслянистый остаток высушивают перегонкой и получают 5,3 г (66%)
5 масла.
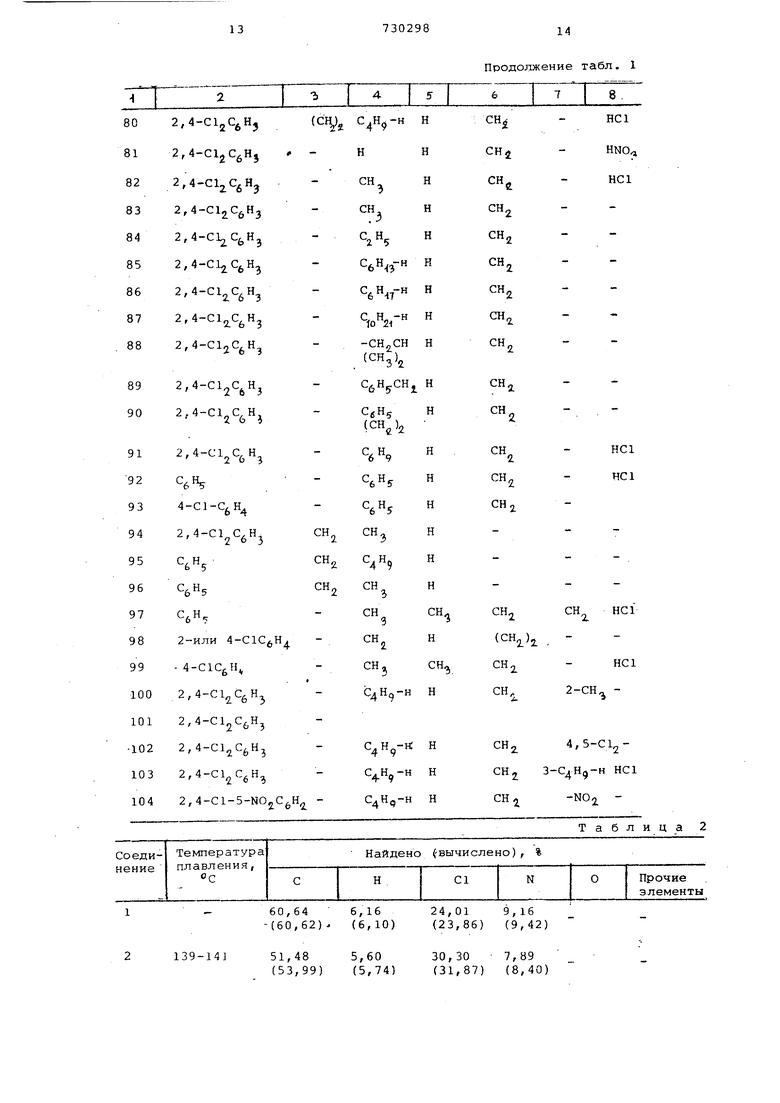
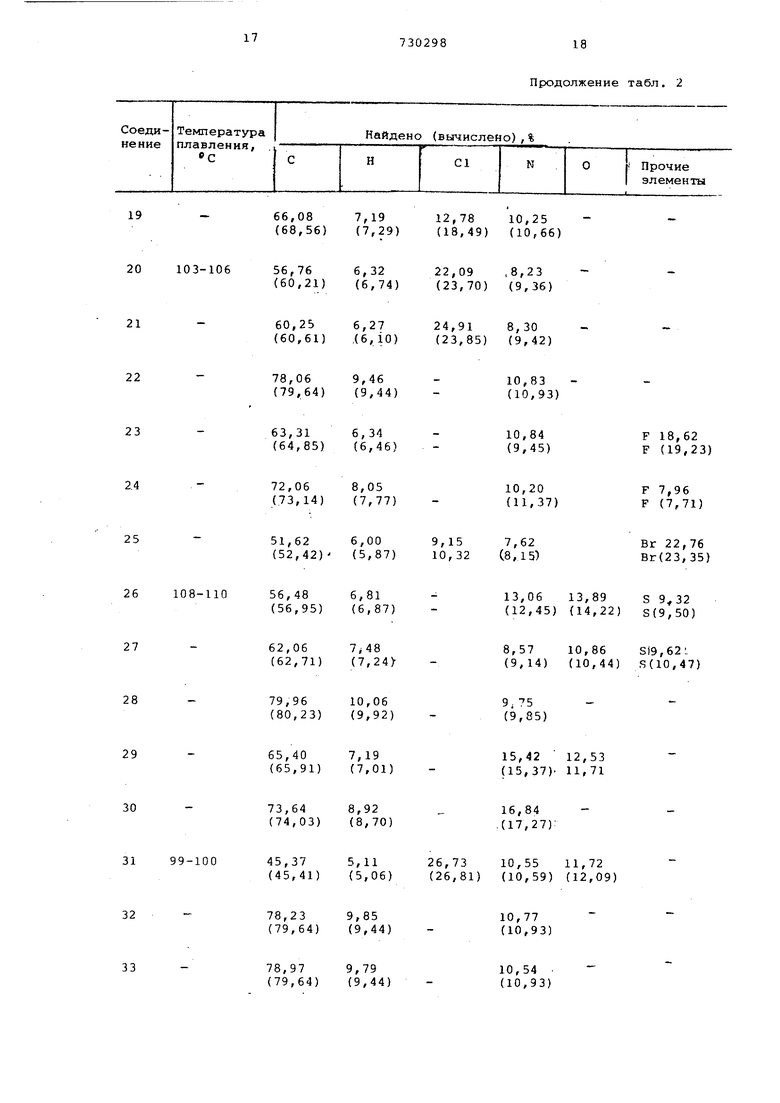
В табл.1 перечислены соединения, полученные пре.длагаер«лми способами, вписанными в приведенных примерах, в табл.2 - их элементарный состав.
f/-Н
Z-(A)n-C -(Ъ)п- -4-(Х)а-МУ
В , . .
Таблица 1
;
4 2,4-Cl,(,ny2,6-(СН) 3,5-(CH,),j . СбИ..С,Н5
39
Продолжение табл. 1. 9
Н
сн,
Н
сн,
ИС1
Н
сн,
Н
сн.
Н
сн
Н
сн,
2- HNO,
сн.
Нс,,
сн,
Н
сн.
Н
Н
сн.













40изо-С.Щ-((СЩ
41«50- CjH742
44
45
46
47
48
zn-ci c H
49
502,4-Cl2C H
512,4-Cl.
522,4-Cl,j.,
сн.
Н
Н
сн,
Н
сн.
сн.
Н
С4 Н, -Н Н
сн,
Н
сн.
сн.
СдН -Н Н
Н
сн.
Н
сн.
HNO.
сн.
-СН2.СН Н СНп
сн.
сн.
RC1
2Н,0НС1
сн.
Продолжение табл. 1
139-14J
51,48 (53,99)
Продолжение табл. 1
Таблица
30,30
7,89
(8,4о; (31,87)
48,75. 4,94 , 29,70 6,86
.57-63 (49,31) (4,97) (29,11) (7,67)
I.i6-l28 3-1,22 5,33 19,20 7,56 14,16
(52,73) (5,21) (18,31) (7,23) (16,53)
221
38,00
3,92 (4,44) (44,06)
61-64
52,35 5,38 (47,79) (4,81)
53-58
49,68 5,16 (49,75) (5,01)
107-113 45,75 4,87
(48,05) (4,84)
45-50
49,77 5,13 (49,96) (5,03)
44-49
40,67 4,81
10 (43,28) (4,36)
11 154-156 53,63 5,74
(53,99) (5,74;
9,21
77,93 (79,29; (9,15)
78,36
9,11 (79,29) (9,15)
14 126-128 68,65 8,47
(68,92) (8,32)
72,998,42
15
(74,40)(8,58)
1
77,368,70
(78,90) (8,83)
1772-73
56,826,26
(60,21)(6,74)
66,807,25
18
(68,56) (7,29)
Продолжение табл. 2
Zn 7,58 Zn(8,95)
5,87
Си 13,00 (6,85) Си (7,77)
21,08- 7,51 5,49 Си 4,70 (18,81) (7,43) (8,49) Cu(8,43)
Со7,60
7,10 28,45 (7.73) (29,37) Со(8,14)
18,96 6,91 10,54 N1 5,23 (15,23) (7,47) (8,53) N1(4,23)
30,12 6,92
Fe 5,70 (29,49) (7,77) Fe (7,74)
16,78 10,14 18,97 Cr 3,2 (11,03) (11,78) (17,29) Cr(6,24)
31,79 8,26 (31,87) (8,39)
11,32 (11,56)
.11,7 (11,56).
12,319,75
(12,71) (10,05)
11,20 7,35 (10,84) (6,17)
11,87 (12,27)
22,248,91
(23,70) (9,36)
14,729,52
(13,49) (10,66)
60,25 6,27 24,91 8,30
21 (60,61) ,(6,10) (23,85) (9,42)
78,06 9,46
22 (79,64) (9,44)
63,31 6,34
23 (64,85) (6,46)
72,06 8,05
51,62 6,00 9,15 7,62
25 (52,42) (5,87) 10,32 (8,15)
26 108-110 56,48 6,81
(56,95) (6,87)
27
62,06 7i48 (62,71) (7,24)79,96 10,06
28 (80,23) (9,92)
65,40 7,19
29 (65,91) (7,01)
30
73,64 (74,03) 3199-10045,375,11 (45,41) (5,06)
78,23
32 (79,64)
78,97
33 (79,64)
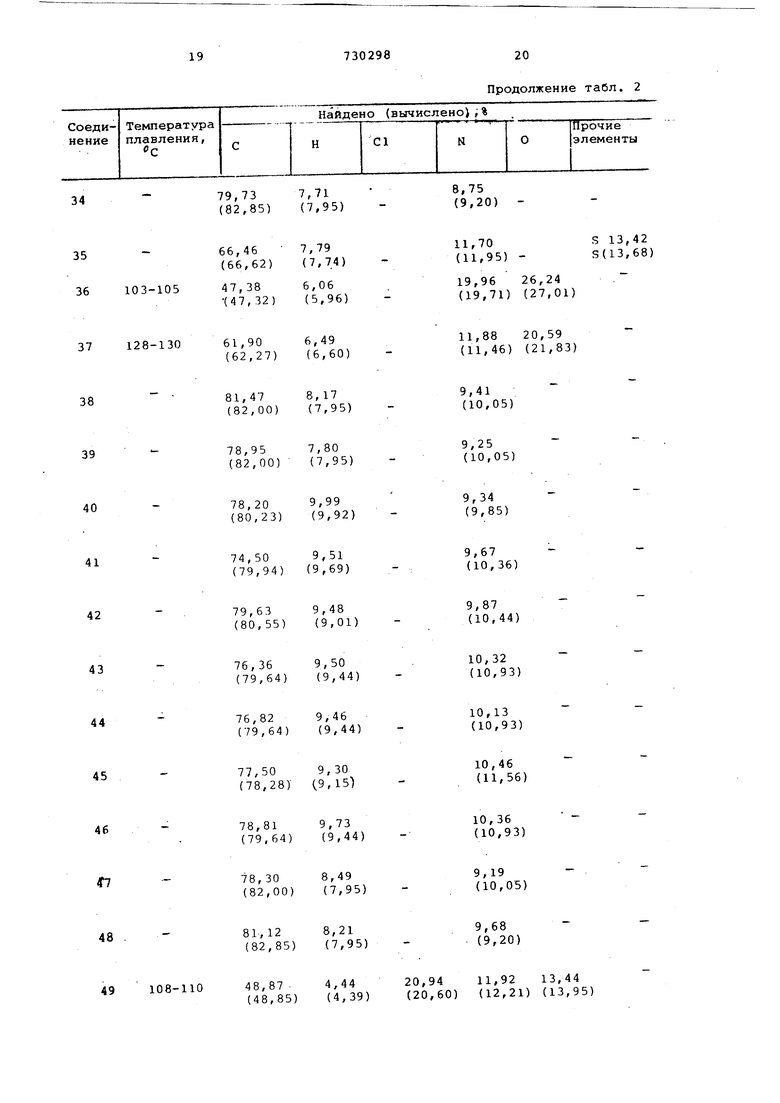
Продолжение табл. 2
10,83 (10,93)
10,84
F 18,62 (9,45) F (19,23)
10,20
F 7,96 (11,37) F (7,71)
Br 22,76 Br(23,35)
13,06 13,89 s 9.32 (12,45) (14,22) S(9,50)
8,57 10,86 St9,62:. (9,14) (10,44) S(10,47)
9,75 (9,85)
15,42 12,53 (15,37). 11,71
8,92
16,84 (8,70) Д17,27):
9,85
10,77 (9,44) (10,93)
10,54
9,79 (9,44) (10,93) 26,7310,55 11,72 (26,81) (10,59) (12,09)
61,90 6,49
128-130
37 (62,27) (6,60)
81,47 8,17
38 (82,00) (7,95)
78,95 7,80
39 (82,00) (7,95)
40
41
79,63 9,48
42 (80,55) (9,01)
9,50
76,36 (9,44) (79,64)
9,46
76,82 (9,44) (79,64)
77,50 9,30
45 (78,28)- (9,15)
78,81 9,73
46 (79,64) (9,44)
78,30 8,49
Т7 (82,00) (7,95)
81,12 8,21
48 (82,85) (7,95)
48,87 4,44
108-110
49 (48,85) (4,39)
Продолжение табл. 2
11,88 20,59 (11,46) (21,83)
9,41 (10,05)
9,25 (10,05)
9,34 (9,85)
9,67 (10,36)
9,87 (10,44)
10,32 (10,93)
10,13 (10,93)
10,46 (11,56)
10,36 (10,93)
9, 19 (10,05)
9,68 (9,20)
20,9411,92 13,44
(20,60) (12,21) (13,95)
51 152-153 57,04 4,58
(57,08) (4,54)
111-112
55
Продолжение табл. 2
26,60 7,17
F 4,50 (26,61) (7,01) F (4,75)
59,93 6,14
66 (60,61) (6,10)
69 197-198
103-105
72
80-82
73
176-179
75
195-197
76
78
248-250
8t) 137-138
109-111
81
(49,42) . (4,49)
Продолжение табл. 2
22,52 9,10 (23,86) (9,43)
36,079,60
(36,47) (9,61)
56,68 4,88
83 (56,49) (4,74)
56,95 5,33
84 (58,01) (5,24)
61,92 6,84 22,27 8,57
85 (62,77) (6,82) (21,88) (8,61)
63,16 7,23 19,54 7,17
86 (64,59) (7,42) (20,07) (7,93)
65,32 8,05
87 (66,00) (7,86)
57,92 6,36
88 (60,60) (6,07)
64,42 5,01
89 (65,27) (4,87)
64,31 5,31
90 (66,19) (5,25)
91 175-177 .54,33 5,39 28,91 7,38
(57,08) (5,35) (29,73) (7,83)
62,62 .6,38 11,98 8,88
83-85
92 (71,70) (6,02) (12,45) (8,94)
71,38 5,41
93 (72,21) (5,35)
55,59 4,96
94 (56,49) (4,74)
76,62 8,67
95 (78,90) (8,83)
76, 58
96 (77,38)
58,926,64 15,61 12,56
165 (раз(65,95) (7,24)(14,98) (11,83) ложение ) .
Продолжение табл. 2
27,37 11,11 (27,79) (10,98)
26,26 10,02 (26,34) (10,41)
18,35 5,84 (18,65) (7,35)
23,16 9,25 (23,90) (9,43)
21,85 8,13 (21,41) (8,46)
20,75 7,71 (20,54) (8,11)
12,81 9,90 (12,54) (9,91)
27,14 11,30 (27,79) (10,98)
12,52 (12,27)
15,08
7,57 (15,04) (7,58)
101 67-69
50,65 4,90 (50,05) (5,23)
102
50,55 4,83 38,62 6,59 (49,21) (4,40) (за,74) (7,65)
47,67 5,98 15,39 5,87
103 (47,42) (5,66) (14,73) (5,82J
4,20
46,60 (4,17) (46,53)
Пример 13. Хлористоводородный 1- 2-циан-2-(2,4-дихлорфенил) гексил имидазол.
.CjMes b. 2-циан-2-( 2 , 4-дихлорфенил) гексилметансульфоната (100 г, 0,29 моль), имидазола (100 г, 1,5 моль) и Ы,Ы-диметилформамида (5 мл) нагревают до 135с при перемешивании в течение суток. Реакционную смесь выливают в воду и экстрагируют эфиром. Соединенные эфирные экстракты сушат над сульфатом магния. Осушитель отфильтровывают и через эфирный раствор пропускают пузырьки сухого газообразного хлористого водорода. Выпавшее в осадок твердое вещество собирают и высушивают, выход 70, 4 г (68%).
Пример 14. Комплексное соединение хлорида цинка с 1- 2-циан-(2,4-дихлорфенил)гексил имидазолом.
Краствору 1- 2-циан-2-(2,4-дихлор енил)гексил имидазола (3 г, 0,01 моль) в этаноле добавляют раствор хлорида цинка (0,63 г, 0,01 моль) в 10 мл абсолютного этанола. Образовавшийся белый осадок отфильтровывают промывают этанолом и после высушлвания получаиот 3,1 г требуемого продукта, т.пл. 196-198°С.
П р Им е р 15. Хлористоводородный 1-.2-Циан-2- (2 , 4-дихлорфенил) децилЗимидазол.
Продолжение табл. 2
19,39 11,63 13,54 (19,70) (11,67) (13,33)
324,39 3 (26,37)
14,37 17,00
(18,31) (14,47) (16,53)
Смесь 2-циан-2-(2,4-дихлорфенил) децйлметансульФоната (41,3 г 0,1 моль), имидазола (27,7 г, 0,4моль) и.Ы,Н-диметилформамида (1,5 мл) нагревают при 130С при перемешивании в течение 24 ч. Реакционную смесь выливают в воду и экстрагируют эфиром. Соединенные эфирные экстракты промывают водой и сушат над сульфатом магния. В эфирный раствор пропускают пузырьк сухого газаобразного хлористого во дорода. Выпавшее в осадок белое твердое вещество собирают 5 и высушивают, выход 11,7 г (28%).
Пример 16. Хлористоводородный 1- 2-циан-2-(4-хлорфенил) пропил имидазол-.
Смесь 2-циан-2-(4-хлорфенил) пропилметансульфоната (бЗ г,. 0,23 моль), имидазола (62,6 г, 0,9 моль) и Ы,К-диметилформамида (3 мл) нагревают при перемешивании и при в течение 24 ч. Реакционную смесь выливают в воду и экстрагируют эфиром. Соединенные эфирные экстракты промывают водой и высушиBcUOT над сульфатом магния. В эфирный раствор пропускают пузырьки сухого газообразного хлористого водорода, выпавшее в осадок твердое вещество собирают и высушивают, выход 38 г (58.6%.
Пример 17.Нитрат 1- 2-циан-2-(2-хлорфенил)-2-(4-хлорфенил)этил 5 имидазола.
Смесь 2-циан-2-(2-хлорфенил-2-(4-хлорфенил)этилметансульфоната (22 г, 0,06 моль), имидазола (16,3 г, 0,24 моль) и К,Ы-диметил-формамида (1 мл) нагревают при и при перемешивании в течение 24 ч. Реакционную смесь выливают в воду и экстрагируют эфиром. Соединенные эфирные экстракты промывают водой и высушивают над сульфатом магния, В эфирный раствор выливают при энергичном перемешивании избыток концентрированной азотной кислоты. Обра- зующийся осадок отфильтровывают, промывают эфиром и высушивают, выход 10,8 г (44,4%) .
Пример 18. Нитрат 1 2-циан-2-(2,4-дихлорфенип)-4-фенил бутил имидазол.
Смесь 2-циан-2-(2,4-дихлорфенйл)-4-фенилбутилметансульфоната (25 г, 0,063 моль), имидазола (17 г, 0,25 моль) и Ы,Н-диметилформамида (1 мл) нагревают при перемешивании и ISO-C в течение 4 ч. Реакционную смесь выливают в воду и экстрагируют эфиром. Соединенные эфирные экстракты промывают водой и высушивают над сульфатом магния., В эфирный раствор выливают при энергичном перемешивани избыток концентрированной азотной кислоты. Образующийся осадок отфильтровывают, промывают эфиром и сушат, выход 17. 5 г (64%) .
Пример 19, 1- 2-Циан-2-(2-пиридил.) -2-фенила тил имидазол.
Смесь, состоящую из 2-циан-2-(2-пиридил)-2-этилметансульфоната
Z-C--(.
СдНд-н
.Н,
3 с
СдНц-Н
з-сн,
СдНц-н
4-СН СЛ1дСдН -н4-ГСбНд СдНд-н
С4Н,-н 2-CF,C,H4 СдНд-н
4-СьН5. ,
(11 Г; 0,037 моль) иг идазола (10 г, 0,15 моль) и Ы,М-д1-5метилформамида (1 мл) нагревают при 140°С в течение. 24 ч при перемешивании. Реакционную смесь выливают в воду и экстрагируют эфиром. Смешанные экстракты эфира промьдвают водой и высушивают над сульфатом натрия. После отгонки растворителя получают 3,4 г (34%) целевого поодукта.
Пример 20. 1- 6-Циан-60-(2,4-дихлорфенил)децил имидазол.
Смесь б-цианЧб (2,4-дихлорфенил) децилбромида (14,2 г, 0,036 моль), имидазола (10 г, 0.,15 моль) и 5 мл N,N-димeтилфopмaмидa нагревают при
5 120°С в течение 24 ч. Реакционную смесь В1лливают в воду и экстрагируют эфиром. Соединенные экстракты высушиваЮт над сульфатом магния и отфильтровывают.В эфирный раствор пропускают пузырьки сухого газообразного хлористого водорода до прекращения образования маслянистого осадка. Затем растворитель декантируют, маслянистый остаток растворяют в ацетоне и нейтрализуют разбавленным
5 раствором гидроокиси аммония. Очищенное свободное основание экстрагируют эфиром и высушивают над сульфатом магния. После отгонки растворителя получают целевой продукт, выход
0 6,5 г (47,8%) .
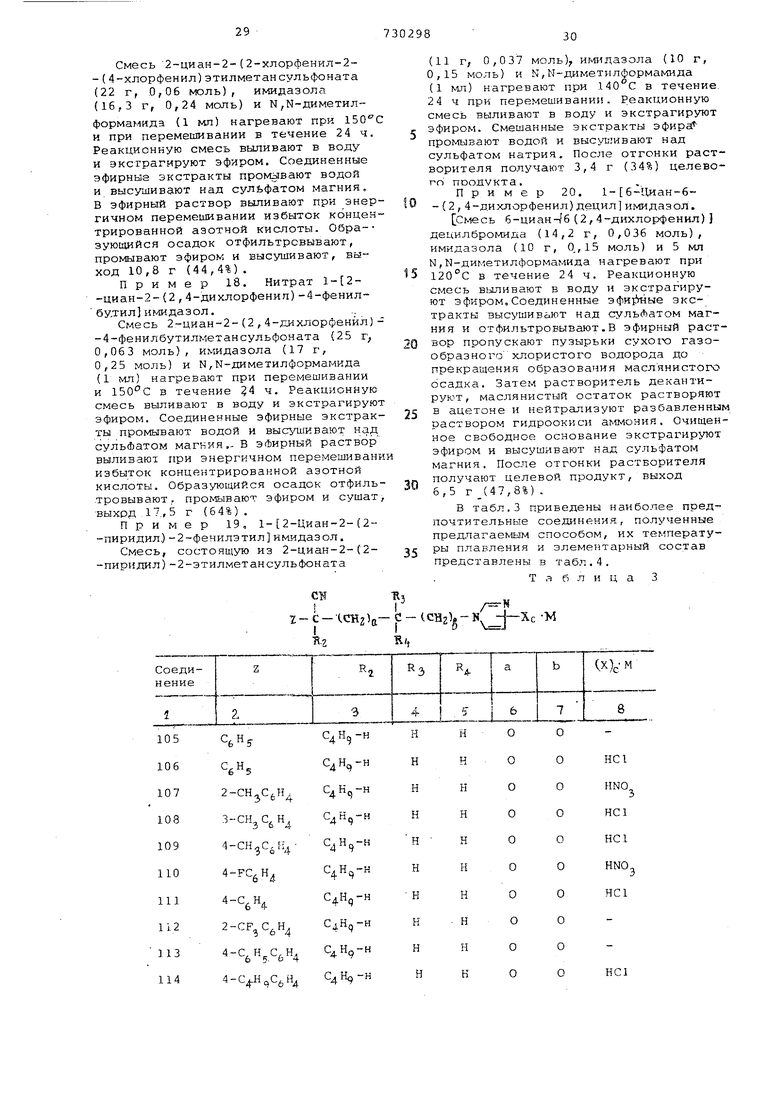
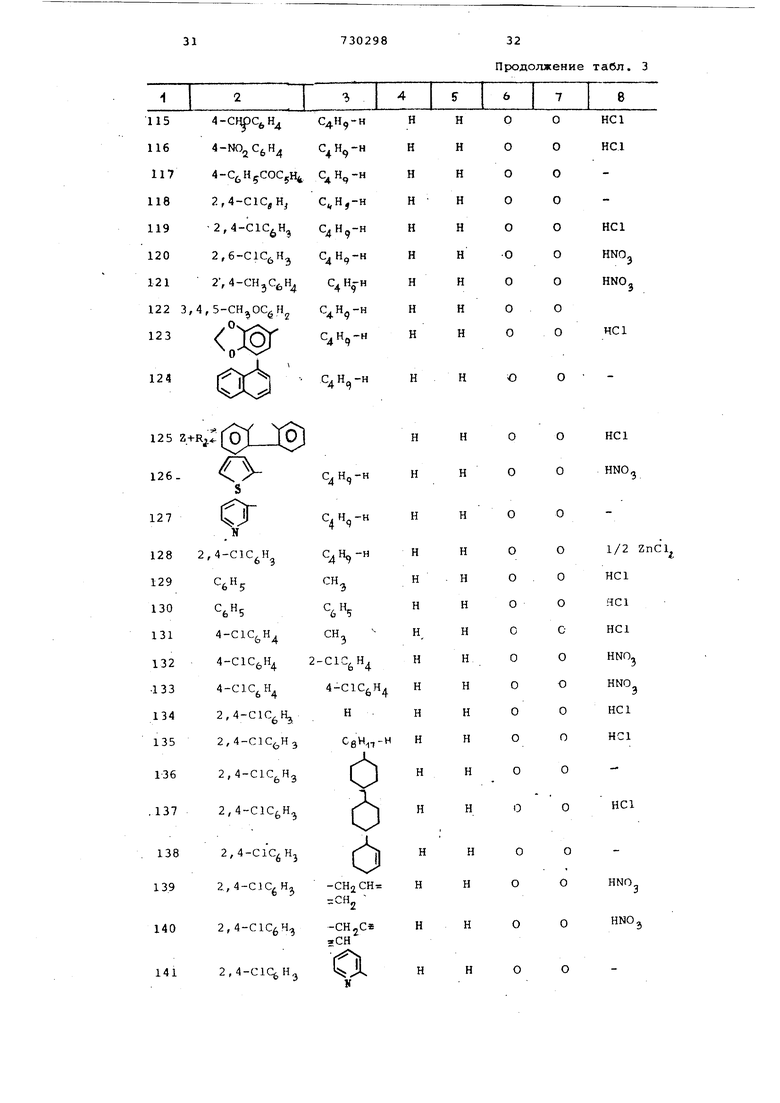
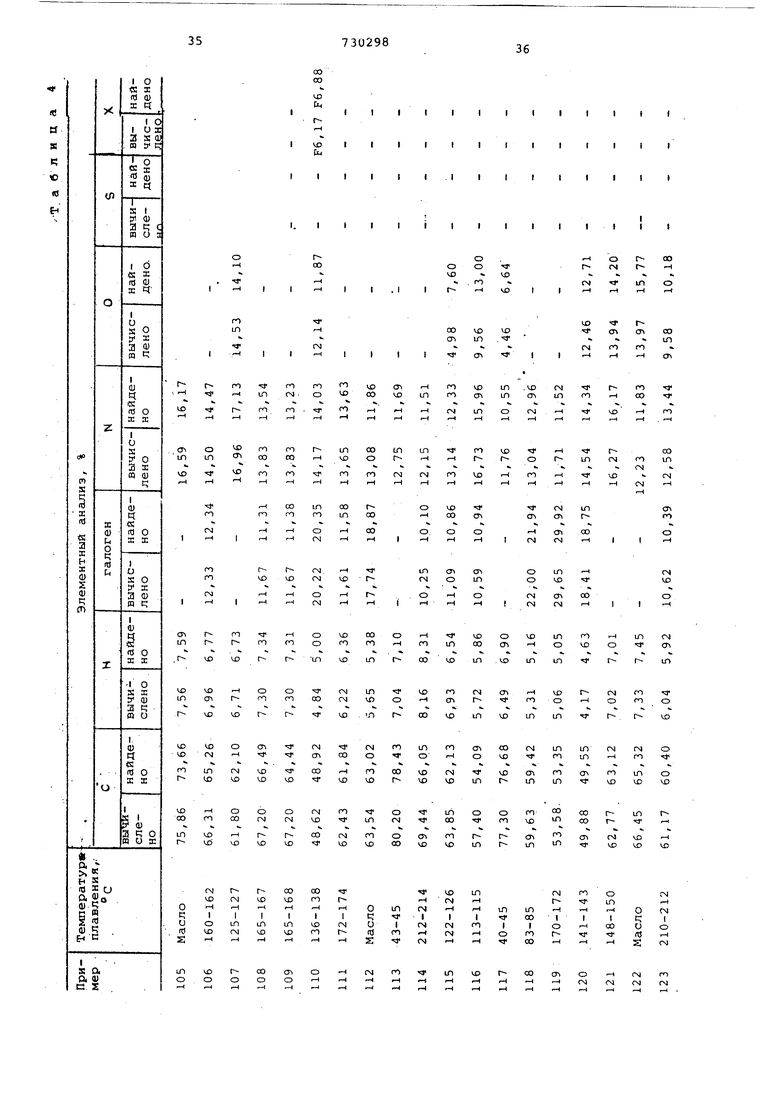
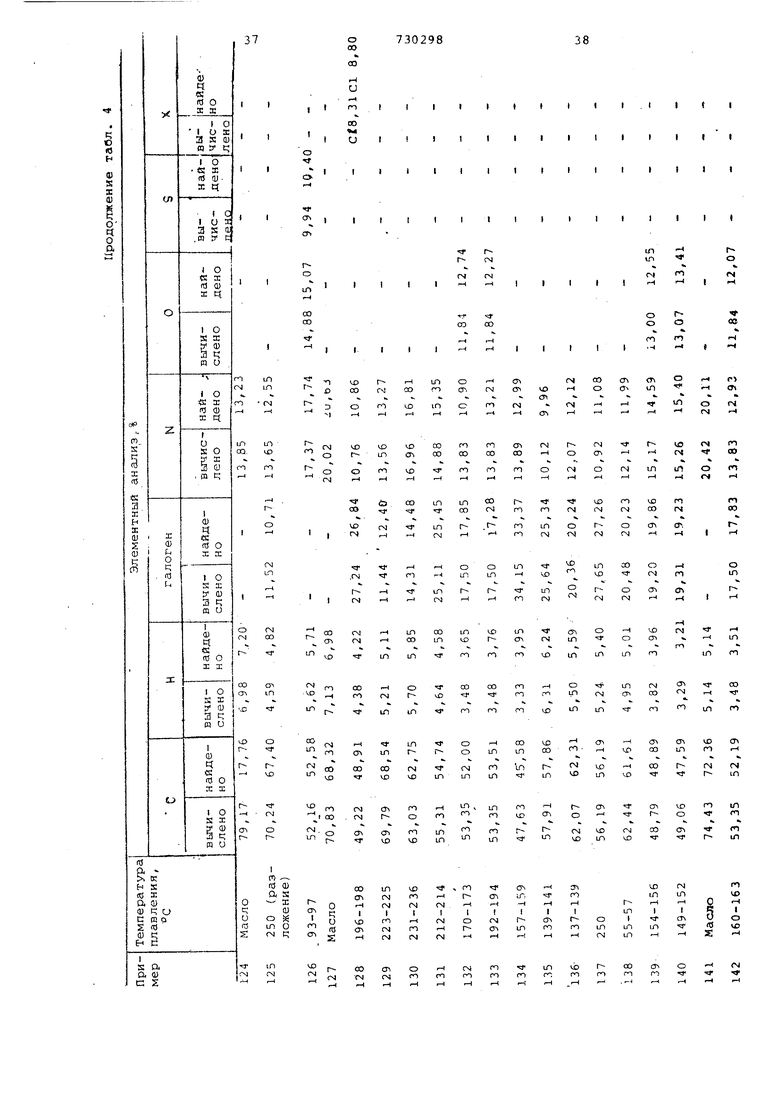
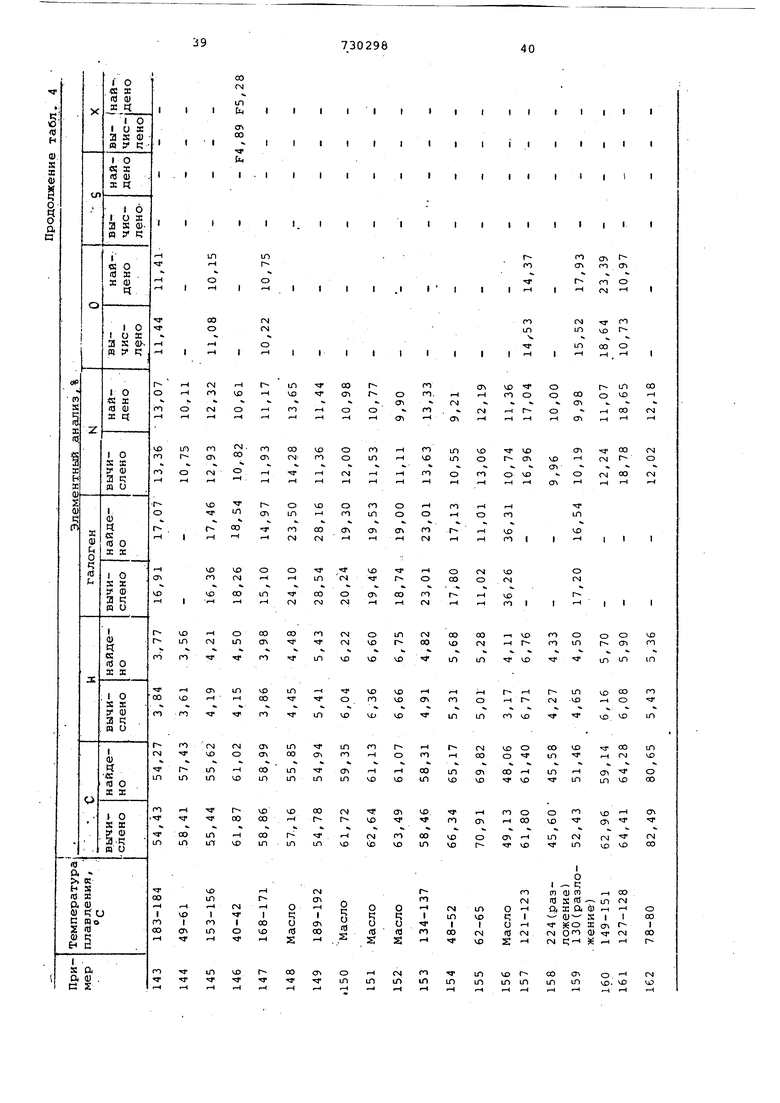
В табл.3 приведены наиболее предпочтительные соединения, полученные предлагаемым способом, vix температуры плавления и элементарный состав
5 представлены в табл,4.
Таблица 3
-М
CHz
R,
.-Н
2,4-С1С И СН
C6«5
Сб«5
Сб«5
сн. 4-С1С Н
2-С1С Н4
4-С1С Н4 4-С1С Н4 4-С1С,Н 2,А-С1С Н
2,
2,4-С1С Нз
2,4-С1С Н
2,4-ClC Hj
-СН2СН
2, 4-ClC Hj
.,с
2,4-С1СбЧ «сн
а
2,4-ClC Hj
Продолжение табл. 3
о
о
н
НС1
о
о о
н
HNO,
о
н
о
о
1/2 ZnCl,
о о о с о о о о
о о о
н н н н н н н н
НС1
ЯС1
НС1
о о о о о
HNO
HNO
HCl
HCl
6 6
о о
о
н н
HCl
о
О
н о о
HNO, н о о
HNO,
о о
н
о
о 1422,4-CiqH,j 1432,4-ClC H -CHjC Н 1442,3-ClC f 1452 4-С1С,Нз -снгСН2.-/ 1462,4-ClCgR1472,4-ClC H 1482,4-ClC H 1492,4-ClC Hg 1502,4-ClC H5 1512,4-ClC H 1522,4-С1СбНз 1532,4-С1-СьНз 1542,4-ClCfeH 1554-Cl-Cj H 1562,4-Cl-C H 157C H 1582,4-Cl-C H 1592,4-С1-С Нз 160C Hj 161C Hj 162C Hg
Продолжение табл. 3 -СИ2-Т Сд Н -н СдН оо 0о HNO, (1)0(1) 1о НС1 2(1)0(1) 3(2)0(1) 4(2)0(2) ОО( I m I I I I ,
ICJI I1
со
I I I I I I Формула изобретения Способ получения производных имидазола общей формулы О (А))д где Z означает С (-С 4. зри л, замещенный 1-3 заместителями, такими ка фтор, хлор, бром, йод, нитрогруппа цианогруппа, метоксигруппа, С -С -алкил, амйно- или метилтиогруппа; R - водород или цианогруппа; R2 означает водород, С |-С -диклоалкил, Cj-Qj, -алкенил, Cg.-Cg-диклоалкенил, -алкинил, CT-Ц -аралкил, фенил или -ар кил или фенил, замещенные l-З замес тителями, такими как фтор или хлор Z и Rj взятые вместе, могут о6разовать группу фенили R,, RJ и К являются атомами 9 означает -алводорода, то К; гсу кил, С5-С2-циклоалкил, С .-С. -алкенил- С1;--Сд-циклоалкенил , С; -С -алкинил, C-j-C -аралкил, фенил или С-,-С -аралкил или фенил, замещенные 1-3 заместителями, такими как фтор или хлор, или их солей, или их комплексов с солями металлов, о т л и ч а ющ и и с я тем, что соединение общей формулы Z-C-(A)-C-(BV-W Кг i, где ЧУ .- атом галогена, -алкилсульфонат, бензол сульфонат или толуолсульфонат, подвергают взаимодействию с имидазолом общей формулы
Ri и R4 независимо Друг от друга означают водород, -алкил или фенил;
А и В - двухвалентные С - алкиленовые группы;
X означает атом галогена,С.-С.-алкил или нитрогруппу;
а.принимает значения от О до 2;
п принимает значения от О до 1;
ti принимает значения от О до 1;
если Z обозначает незамещенный
Н
25
или солью имидазола при 50-180С и целевой продукт выделяют в свободном виде или в виде соли, или комплексов с солями металлов. 30 Источники информации,
принятые во внимание при экспертизе

Авторы
Даты
1980-04-25—Публикация
1977-01-04—Подача