1
Изобретение относится к усовершенствованному способу получения аминоантрахинонов каталитическим гидрированием нитро антрахинонов.
Аминоантрахиноны используются в 5 качестве промежуточных продуктов при производстве дисперсных красителей для синтетических волокон.
Известен способ получения аминоантрахинонов гидрированием питроант- 10 рахинонов в присутствии 5% Ра на угле в концентрированной серной кислоте при 40-70°С и 1 атм Hj М
В этих условиях 1-нитроантрахинон и 1-нитро-2-метилантрахинон гидриру- 15 ются до соотвётствуюишх аминов с выходом 32 и 80% соответственно, а 1-нитроантрахинон-2-карбоновая кислота не гидрируется вообще. Практическое применение способа невозможно,20 из-за использования серной кислоты как растворителя, отравление катализатора, низкого выхода целевого продукта.
Известен также способ получения 25 1-аминоантрахинона гидрированием 1-нитроантрахинона в присутствии скелетного Ni в среде инертных растворителей (углеводородов, эфиров, спир% тов, кетонов). Процесс ведут при 30
100°С и давлении Н j. 1 атм с выходом целевого продукта 96% 2 .
Недостатками способа являются невозможность гидрирования замещенных нитроантрахинонов, отравление катализатора, его пирофорность, одноразовое его использование, низкий выход целевого продукта.
Наиболее близким по технической сущности к предлагаемому является способ получения аминоантрахинонов гидрированием нитроантрахинонов в инертных орга,нических растворителях (углеводородах, эфирах1 в присутствии платиновых металлов (0,05-10% на норителях (например, активированном угле) или N1 скелетного при 60200°С (лучше 80-160°С) и парциальном , давлении Н до 16 атм (предпочтительно 0,5-10 атм) З .
Недостаткг1ми этого способа являются наличие рецикла, низкий выход целевых продукт.ов, низкая чистота продуктов, образование продуктов восстановления аминоантрахинонов, гидроксиламиноантрахинонов и гидроксиаминоантрахинонов, близких по Фкзико-химическим свойствам к целевому , продукту, в связи с чем требуется особо тонкая очистка, а также неврз- .
можность получения чистых целевых продуктов без вторичной переработки
Цель изобретения - увеличение выхода и упрощение процесса.
Указанная цель достигается тем, что в качестве катализатора используют паллсщиевый комплекс полимерного лиганда, содержащего NH-группы в основной цепи, общей формулы PdL где L - полимерный лиганд, содержаний NH-группы в основной цепи; , предпочтительно в среде инертного к реакционной системе растворителя - спирта, эфира, амина .амида (либо их смесей с водой) - растворяющего исходный и конечный продукт реакции.
Указанные катализаторы представлют собой комплексы Pd с полимерными лигандами, содержащими NH-группы в основной цепи общей формулы PdLn, где L - полимерный лиганд, содержащий аминогруппы; . В качестве полимерных лигандов могут быть использрва.ны полиэтиленполиамины, полйэтйлёнимин, силохром СХ-1,5, модифицированный 5-аминопропилтриэ оксисиланом, с концентрацией аминоалкильных групп 0,21 мг-экв/г (в дальнейшем аминоаэросил).Мольное соотношение Pd : полимерный лига1нд, предпочтительно, от 0,1 до 1.
В зависимости от растворимости катализатора способ может осуществляться как в гомогенной, так и в г етерогенной среде.
Перед проведением процесса катализаторы активируют обработкой NaBH Предвосстановление может проводиться как непосредственно перед опытом, в реак1;оре, так и задолго {более чем за 5 мес) до опыта, на воздухе, Предвосстановленные катализаторы стабильны на воздухе и не теряют своей активности в течение .более «leM 5 мес. при .
Каталитическое гидрирование нитроантрахинонов ведут при 20°С и давлении Н 1 атм. Выход соответствующих аминоантрахинонов количественный - 100% при степени конверсии 100%. С целью более интенсивного протекания процесса без потери селективности температура может быть повышена вплоть до 80°С, а давление - до 15 атм..
После завершения процесса гидрирования целевой продукт может вселяться двояким образом. В случае применения гетерогенного катализатора реакционную смесь фильтруют, фильтрат упаривают при пониженном давлении и температурах не выше температуры сублимации продукта при этом давлении.
. В случае использования гомогенно го катализатора реакционную смесь
разбавляют алифатическим спиртом до осаждения катализатора, жидкую фазу отделяют декантацией или фильтрованием и целевой продукт выделяют далее аналогично вышеописанному.
Состав и растворимость используе NBJX катализаторов приведены в табл.1.
Таблица 1
Анионит АН-10,14
Анионит АН-10,7
Анионит АВ-170,1
Полйэтиленимин0,2
2°
Полиэтиленполиамины0,2
Аминоаэросил0,2
Предлагаемый способ иллюстрируется примерами. Используется техни ческий 1-нитроантрахинон с т.пл.
5 21В°С (лит.т.пл.230с) - образец 1 и 1-нитроантрахинОН, очищенный перекристаллизацией с т.пл. - образец ll.
Пример 1. В реактор помещают 0,3 г катализатора П (0,003 г Pd) 10 мл этанола и обрабатывают 0,02 г NaBH4 при 42°С, после чего вводят 0,1265 г 1-нитроантрахинона (образец I ) и гидрируют при и 1 атм Hg. Удельная активность 0,55 моль Н2/г-ат Pd-мин. После прекращения поглощения Н2 катализатор отфильтровывают, фильтрат упаривают при 10 мм и 20С. Выход 1-аминоантрахинона - 0,11 г. Т.пл. - 240243°С с возгонкой.
Пример 2. В реактор помещают 0,202 г катализатора VI (0,002 г Pd, 5 мл раствора), 10 мл. этанола и при 42°С обрабатывают 0,005 г NaBH4, после чего вводят 0,1265 г (5 -Ю моль) 1-нитрЬантрахинона (образец /7). Удельная активность 5,5 моль 112/г-ат fd-мин, выход 1-аминоаноантрахчнона 100%. Т.пл. - 256°С.
Пример 3. В колбу помещают 0,202 г катализатора (0,002 г Pd, :5 мл водного раствора), 10 мл этанола и при обрабатывают О.,005 г NaBH. После полного разложения NaBH, раствор переносят на воздухе
В реактор, вводят 0,1265 г Х.5.--10 моль) 1-нитроантрахинона. Удельная активность 5,4 моль Н /г-ат Pd-мин. Выход 1-aNmHoaHTpaхинона 100%.
Пример 4. В колбу помещают 0,3 г катализатора И (0,003 г Pd-) , 10 мл этанола и при 40.С обрабатывают 0,02 г NaBH4. После полного разложения NaBH раствор фильтруют, катализатор промывают водой, ацетоном, эфиро 1 и сушат на воздухе. Высушенный катализатор (0,27 г) помещают в реактор, приливают 10 мл этанола, вводят 0,1265 г (5-Ю мол 1-нитроантрахинона (образец II). Удельная активность 1,35 моль Н,/г-ат Pd-мин. Выход 1-аминоантрахинона 100%.
Пример 5. в реактор помещают 0,202 г катализатора VI (0,002 f Pd, 5 МП водного раствора), 10 мл этанола и при 42°С обрабатывают 0,005 г NaBH4, после чего вводят j 0,1265 г (5.) 1-нитроантрахинона (образец) и гидрируют при 42 с и давлении Hg 1 атм. По прекращению поглощения водорода в реакционную систему вводят 10 мл этанола. Q Жидкую фазу отделяют фильтрованием, фильтрат упаривают при 20°С и остаточном давлении 10 мм. Получгцот О 1165 г 1-аминоагнтрахинона с т.пл. . Выход 100%.
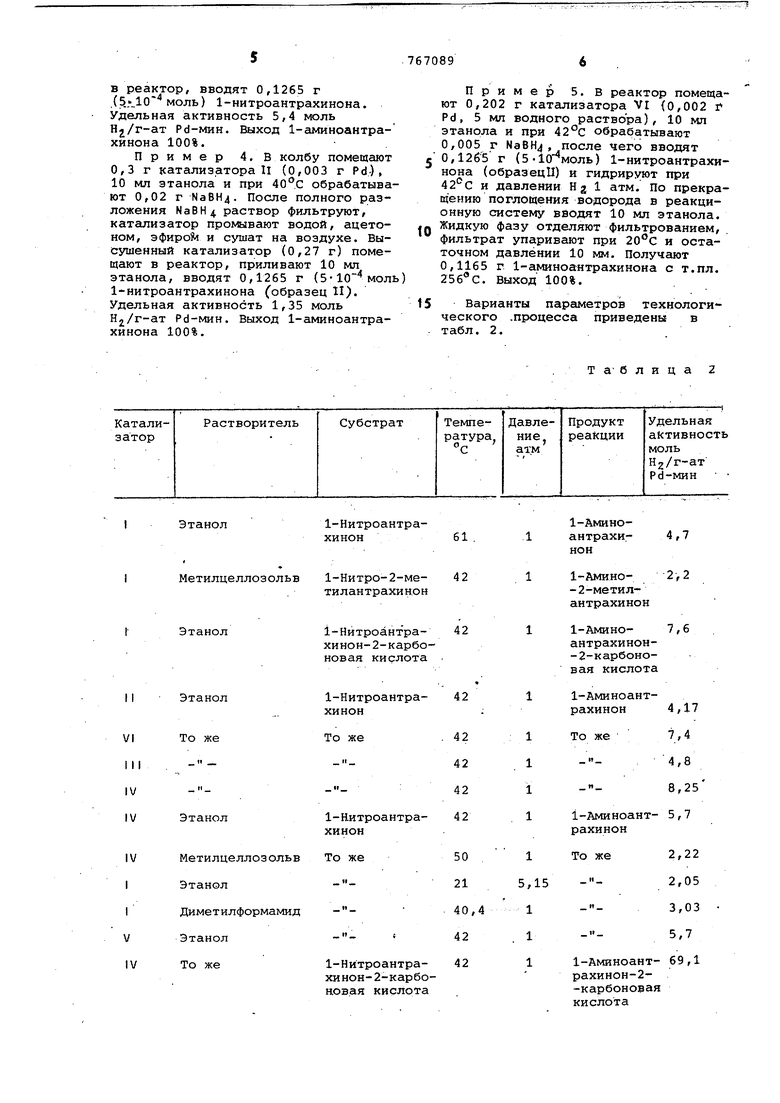
5 Варианты параметров технологического .процесса приведены в табл. 2.
Т а б л и ц а


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения аминоантрахинонов | 1980 |
|
SU943228A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 1-АМИНОНАФТАЛИН-5-СУЛЬФАМИДОВ | 1989 |
|
SU1648056A3 |
| Способ получения 1-окси-4-амино-АНТРАХиНОНОВ | 1979 |
|
SU808494A1 |
| Способ получения аминоантрахинонов | 1973 |
|
SU567399A3 |
| Способ получения циклоалифатических кетоаминов или их солей | 1979 |
|
SU886735A3 |
| СПОСОБ СИНТЕЗА МЕТАЛЛ-УГЛЕРОДНОГО КАТАЛИЗАТОРА И ПРОЦЕСС ВОССТАНОВЛЕНИЯ НИТРОСОЕДИНЕНИЙ | 2013 |
|
RU2581166C2 |
| Способ получения циклоалифатических кетоаминов или их солей | 1980 |
|
SU984404A3 |
| Способ получения циклогексанкарбоновых кислот | 1986 |
|
SU1387354A1 |
| Способ получения цис-алкенов | 1988 |
|
SU1664777A1 |
| Способ получения диметилвинилкарбинола | 1987 |
|
SU1476834A1 |

1-НитроантраЭтанолхинон
Метилцеллозольв 1-Нитро-2-ме- 42
тилантрахинон
1-НитроантраЭтанолхинон-2-карбоновая кислота
1-НитроантраЭтанолхинон
То же
То же ti
II
|| :
1-НитроантраЭтанолхинон
Метилцеллозольв
То же
Этанол
Диме т илформамид
Этанол
1-НитроантраТо же хинон-2-карбоновая кислота
61
1-Амино- 7,6 антрахинон-2-карбоновая кислота
1-Аминоантрахинон 4,17
74
1 1 1 1
То же 4,8
8,25
п
1-Аминоант- 5,7 рахинон
2,22 2,05 3,03 5,7
рахинон-2-карбоновая
кислота
1-Нитроантрахинон
Катализатбр VII представляет собой палладиевый комплекс поливинилового спирта; выход 1-аминоантрахинона 20%, 1-амино-9,10-диоксиантрацена - 80%.
Катализатор VlH палладиевый комплекс с найлоном-б6, выход 1-аминоантрахинона 20%, 1-амино-9,10-диоксиантрацена - 70%, амино-4-оксиантрахинона следы.. Формула изобретения Способ получения амииоантрахинон гидрированием иитроантрахинонов в Ш1 1Ш Р Ш еШШ р«етвс1рй ё ;йрйеутстбии катализатора на основ метёшла Vlll группы, отличающий С я тем, что, с целью увели ЧГёТайя ВШсОда и упрощения процесса в качёотве катализатора используют палладиевый комплекс полимерного лиганда, содержащего NH-группы в основной цепи, общей формулы Pdl, где L - полимерный лигакд содержаПродолжение табл. 2
21 10,8 1-Аминоантрахинон 45,0 щий NH-группы в основной цепи; . Источники информации, п ринятые ВО внимание при экспертизе 1. Чуреина В.М., Литвин Е.Ф., Фрейдлин Л.Х., Зинченко Р.И. Изв. АН СССР, серия Химия, 1969, 2550. I 2. Патент ФРГ 2348102, кл. С 07 С 97/24, опублик. -1973. 3. Патент Швейцарии № 577958, кл. С 07 С 97/24, опублик. 1976 (прототип).
Авторы
Даты
1980-09-30—Публикация
1979-01-16—Подача