





| название | год | авторы | номер документа |
|---|---|---|---|
| Циклические аналоги каллидина и других пахикининов,обладающие пролонгированным гипотензивным действием в сочетании с низкой или полностью отсутствующей миотропной активностью | 1978 |
|
SU1219587A1 |
| Циклический аналог брадикинина,обладающий пролонгированным гипотензивным действием | 1980 |
|
SU892871A1 |
| Способ получения основных эфиров енолов или их солей | 1975 |
|
SU614743A3 |
| Способ получения пептидов или их солей или амидов или сложных бензиловых эфиров | 1973 |
|
SU651691A3 |
| Способ получения пептидов с последовательностью актг-человека,содержащих в -конечном положении аминооксикислоту | 1973 |
|
SU490284A3 |
| Цистеинсодержащие пептиды для синтеза пептидных гормонов окситоцина и вазопрессина | 1974 |
|
SU523083A1 |
| Способ получения производных соматостатина | 1974 |
|
SU586837A3 |
| Способ получения производных 3-оксииминометилцефалоспорина или их солей | 1972 |
|
SU525429A3 |
| Способ получения 5-замещенных 10,11,-дигидро-5н-дибензо( @ , @ ) циклогептен-5,10-иминов | 1978 |
|
SU895288A3 |
| Способ получения бензилпиримидинов или их солей | 1974 |
|
SU577987A3 |

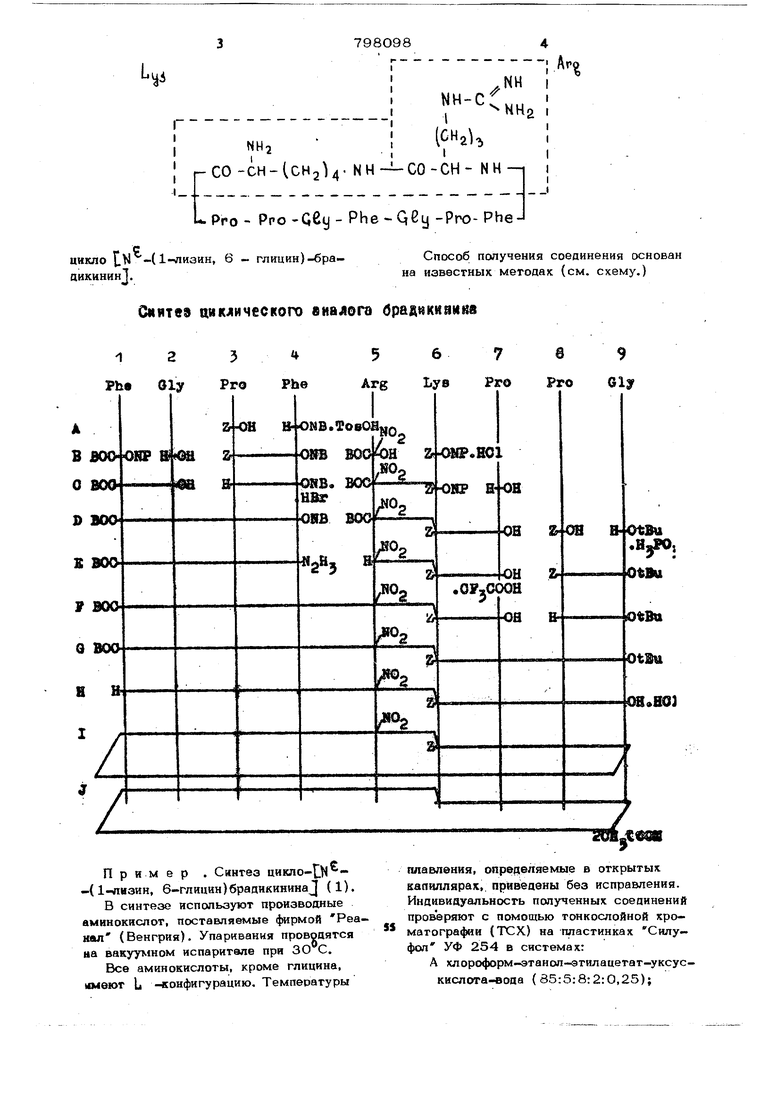
цикло LM -(1- пизин, 6 - глицин)-брацикинин.
Сиитеэ циклического в на дога браднккаинв
Пример . Синтез цикло-,( 1-лизин, 6-глицин)браяикинина (1).
В синтезе используют производные аминокислот, поставляемые фирмой Реанал (Венгрия). Упаривания проводятся на вакуумном испарителе при ЗО С.
Все аминокислоты, кроме глицина, имеют L -конфигурацию. Температуры
Способ получения соединения основан на известных методах (см. схему.)
т
«Ф«
плавления, определяемые в открытых капиллярах,, ариведены без исправления. Индивидуальность полученных соединений проверяют с помощью тонкослойной хроматографии (тех) на пластинках Силуфол УФ 254 в системах:
А хлороформ-этанол-этилацетат-уксускислота-вода (85:5:8:2:0,25); Б хлороформ этанол-«-бутанол-9ТИЛ1ацетат-чвода (10:6:4:3:1); В )слороформ-метанол- еода (40:30:5); Г бутанол-уксусная кислота-вода (4:1:1); Д этилацетат-пиридин-уксусная кислота-вода (5:5:1:3) и электрофореза на бумаге PN 16 в IN или 5 уксусной кислоте. Эпектрофоретв- ческую подвижность определяют по отношению к гистидину. Пятна веществ обнаруживают при облучении хроматограм ультрафиолетовым светом, а также опрыс киванием кингидрином или при помощи реагента хлора.ензидина. Для идентифи- кации соединений используют протонный магнитныйрезонанс (ПМР) при 60 мГц, спектры снимают на приборе Pefkin ЕВгяеР R 12 А. Аминокислотный анализ выполняют на анализаторе Bio CAL-200 после гидролиза пептида в запаянной ампуле при НО в течение 24 ч.. Трет-Бутиповый эфир бенз{шокстсар-. бонилпролилглицина (Е 8-9). К раствору 1О,0 г (4О ммоль)бензил оксикарбонилпролина в 50 мл диК етилфор мамида, добавляют 4,45 мл (40 ммопь) N-метилморфолина и при (по каплям) охлажденный раствор 5,30 мл (40 ммоль) изобутилового эфира хлоругоп ной кислоты в 10 мл диметилформамида. Реакционную смесь перемешивают ЗО мин при -15 С и добавляют к ней охлансденную суспензию 10,6 г (50 ммоль) фосфита трет-бутилового эфира глицина в 1ОО мл диметилформамиаа и 0,56 мл (50 ммоль) W -метилморфолина. Смесь перемешивают 30 мин при -15 С и ос- тавляют на 15 ч при -ЮС. Растворитель упаривают в вакууме, остаток растворяют в смеси 100 мл этилацетата и 100 мл воды, этилацетатный слой промывают 10%-«ыми растворами бикарбоната калия и бисульфата калия и водой, су- шат над сульфатом магния, фильтруют и упаривают. Продукт выкристаллизовывают из полученного масла обработкой последнего смесью эфира с гексаном (1:1). (70 Т,Ш1 71-72 С 49,0° (с 2, диметилформамид). Выход 9,2 г (63%). R 0,55 (А); 0,64 (Б) и 0,68 (В), Трет-Бутиловый эфир пропипгляцвна (Р8-9). 5,0 г (13,8 ммоль) Е 8-9 раствора ют в 50 мл этанола и гидрируют в Присутствии палладиевой черни в течение 5 ч Катализатор отфильтровывают, маточник упаривают, остаток растворяют в смеси 7 ЯЯ6 сухого эфира с гексаном (1:2) и снова упаривают досуха. Получают бесцветное кристаллическое вещество. Выхоп 2,8 г (89%). Т. пл. 56-57 C/ti | f - 38,6 (с 1, диметилформамид). .gO,83 (IN уксусная кислота). Rr 0,28 (В); ОД5 (Г) и 0,70 (Д). П -Нитрофениловый эфир с -бензилоксикарбонил-6 -(трет-бутоксикарбоннл(0--н{1троаргинил)лиаиыа (С-5-6). К раствору 12,8 г (34,3 ммоль) трет-бутоксикарбонш1-СО -ннтро) аргинина и 3,8О мл (34,3 ммоль) N -метилморфолина в 10О мл диметилформамида при добавляют 4,63 мл (34,3 ммоль) изобутилового эфира хлоругольной кислоты, а затем 10,0 г (22,8 ммопь) порошка хлористоводородной сопи R -нитрофенилового эфира 0& бензилоксикарбониллизина. Смесь перемешивают 30 мин при -10 С, затем в течение 2 ч по каплям добавляют раствор 2,55 мл (22,8 Л4моль) N -метилморфолина в 5О мл днмётилформамида. Перемешивание продолжают в течение 30 мин при -20 С, затем добавляют 1,33 мл (12,1 ммоль) 1% -диметиламиноэтиламина. Смесь вновь перемешивают ЗО мин, упаривают растворитель, остаток растворяют в смеси 1ОО мл этилацетата и 100 мл воды. Эгилацетатный слой отделяют и промывают 10%-41ыми растворами бикарбоната калия и бисульфата калия (дважды) и водой. Сушат над сульфатом магния, фильтруют, упаривают. Получают желтоватое аморфное вещество. Выход 13,5 г (86,5%). 1 0,80 (А) и 0,90 (r)./oi/JJ- 20,9 (с 1, диметилфорйамид). РО-Бензил оксикарбонил- -(трет- у- тилоксикарбрнил-() аргинил) -лизилиролин (). В раствор 10,0 г (14,2 ммоль) С 5-6 в 1ОО мл диметилформамида вводят 2,46 г (21,4 ммоль) мелкорастертого пролина и 1,66 мл (1,49 ммоль) N -метилморфолина и смесь перемешивают на магнитной мешалке 20 ч. Затем растворитель упаривают, остаток растворяют в смеси ЮОмл этилацетата и 1ОО мл раствора бисульфата калия, водный слой отделяют, этилацетатный слой экстрагируют 10%-ным растворе бисульфата каия, а затем 10%-«ым раствором бикарбоната калия. Водный слой отделяют, нейтрализуют 1О%-«ым раствором бисульфата калия, доводят рН до 2 и экстра-, гируют продукт атилацетатом (2х1ООмл). Экстракт сушат над сульфатом маг-ния, фильтруют и упаривают. Получеиот бесцвет ное аморфное вещество. Выход 7,9 г (82,0%). /oi/ - 23,1 (с 1, аиметилформамид). f 0,54 (А) и 0.81 (Г). Трифторацетат об -бензилоксикарбо- НИЛ -((О-нитроаргиннл)лизилпролина (Е 5-7). 5,0 г {7,37 ммопь) D 5-7 растворяют в смеси трифторуксусно кислоты с хлористым метиленом (1:1) при О С. Выдерживают 20 мин при комнатной тем пературе, затем упаривают при комнатной температуре досуха. Остаток раствор$пот с сухим эфиром, образовавшееся твердое вещество отфильтровывают и промывают сухим эфиром. Выход бесцветного аморфного вещества 5,0 г (98%). О.49 (5 Ц уксусная кислота),/о /Q-11,1 (с 1, диметилформамид). R 0,57 (В); 0,70 (Д). Трет-Бутоксикарбон клфен ипап аи ипгл ицнн (С 1-2). 6,4 г (16,6 ммопь) Г -нитрофенилово го эфира трет-бутоксикарбонилфенилалани на; 1,13 г (15 ммоль) глицина и 1,67м (15 ммоль) W -метнлморфолина растворя ют в смеси 200 мл дйметилформамица и 20 мл воды. Полученный раствор выдерживают 2О ч при комнатной температуре упаривают и оставшееся масло растворяют в смеси 8О мл 1О%-ного водного раствсфа бикарбоната калия и 5О мл этилацетата. Этилацетатный слой отделяю а водный слой экстрагируют 50 мл эфира и 1О%-ным водным раствором бисульфата калия, доводят рН до 2.. Полученный раствор экстрагируют этилацетатом (2x50 мл), экстракт промывают 5О мл воды сушат над безводным сульфатом ма кия, фильтруют и упаривают досуха. Полу чают бесцветное кристаллическое вещество. Выход 4,0 г (82,7%). После перекристаллизации из этилацетата Т. пл, 165°С (с разложением),о (с 1, диметилформамид), R 0,85 (А); О О,90 (Б) и 0,88 (В). - {итробенаиловый эфир трет утоксикарбонилфенилаланилглицилпролилфенилаланина (с 1-4). К раствору 2,8О г (8,7 ммоль) С 1-2 в 50 мл сухого диметилформамида добавляют 1,84 г (10 ммоль) пентафтор фенола, смесь охлаждают ао -2О С и добавляют к ней 1,9О г (9,2 ммоль) дициклогексилкарбодиу1мида .встряхивают до растворения последнего и выдерживают 30 мин при О С. Затем добавляют 4,15 г (8,7 ммоль) гиаробромида П - итробензилового эфира пролилфениланина (С 3-4) и 0,97 мл (8,7 ммоль) -метилморфолина. Выдерживают при комнатной температуре, контролируя рН среды с помощью индикаторной бумаги, и в процессе реакции по каплям добав- ляют N -метилморфолин, для поддерживания рН около 8. Спустя 3 ч после введения аминокомпоненты смесь упаривают, к остатку добавляют 1ОО мл хлористого метилена, осадок отфильтровывают, фильтрат промывают последовательно 10%-ными {«створами бикарбоната калия, бисульфата калия и водой. Сушат над безводным сульфатом магния, фильтруют и упаривают. Полученное масло кристаллизуют растирая с сухим эфиром. Выход 5,4 г (88,4%). Т. пл. 125ISS C/O /jf- 45,б (с 1,диметилформамид). К± 0,88 (А); 0,91 (В) и 0,91 (ГТ. Гидразит трет-бутоксикарбонилфенил-. аланилглицилпролилфенилаланина (Е 1-4). 3,0 г (4,27 ммаль) Е 1-4 и 1,Омл гидразингидрата нагревают 1 ч в ЗО мл этанола тфи 7О С. Фильтруют, к фильтрату добавляют 5О мл воды и смесь выдерживают 20 ч при -1О С, осадок отф«5льтровывают и кристаллы на фильтре промывают 30 мл 5О%.-«ого водного этанола, затем водой до нейтральной реакции фильтрата. Сушат над пятиокисью фосфора. Выход 2,ЗО г (92,8%). Т, пл. 140-160°С/0 / -59,80 (с 1,диметилформамид). К.Ч О,93 (А); О,92 (В) и 0, (Г). (Х--Бензилоксикарбонил-Е -(трет-бутоксикарбонилфенилаланилглицилпролилфенилаланил- со-«итро)аргинил)лизилпролин (Г 1-7). К раствору 2,1 г (3,62 ммоль) Е 1-4 в 5О мл диметилформамида, охлажденному до -ЗО С при перемешивании, добавляют охлажденную (-70 С) смесь 3,5 мл (15,7 ммоль) 4,5 и раствора сухого хлористого водорода в тетрагидрофуране и 2О мл этилацетата. Затем при -ЗО С по каплям добавляют охлажденный раствор 0,45 мл (3,87 ммоль) трет-бутилнитрита в 10мл этилацетата. Выдерживают 30 мин при -25 С, затем добавляют 1,76 мл (15,8 ммоль) W .-метнлморфол11на, после чего вводят раствор 2,68 г ( 3,87 ммоль) Е 5-7 и О,44 мл N -метилморфолина в 5О мл диметилформамида. Смесь выдерживают 3 сут при , упаривают, остаток растворяют а СМРСИ ЮО мл хлористого метилена и IОО мл воды. Слой хлор(к;то10 мг тилЧ11 отделяют, промЫйа- ют послецовательно 10%-ными растворами бикарбоната калия, бисульфата калия и воаой (по 1ОО мл), сушат над безводным сульфатом магния, фильтруют и упаривают. Получают мчсло, из которого при расти- . рании со смесью эфира с этилацетатом (1:1) выкристаллизовывается проаукт. Выход 3,50 г (85,8%). Т. пл. 140177®C./oi/о- 44,1 (с 1, диметипформаМИД). R.J 0,53 (А); 0,84 (Б) и О,87(Г) Трет-Бутиловый эфир об -бензилоксикар бонил- -(трет-бутоксикарбонилфенилала- нилглицилпролилфенилаланил-(со-нитро)-аргинил)лизилпролилпролилглицина(51-9) К охлажденному цо раствору 2,70 г (2,40 ммоль) F 1-7 в 4О мл диметилформамида добавляют 2,19 г (2,89 ммоль) комплекса дициклогекси- карбодиимида с пентафторфенолом и 1,1 г (4,8 ммоль) трет-бутилового эфира про- лилглицина (F 8-9). Смесь выдерживают 2О ч при комнатной температуре, упаривают остаток растворяют в 50 мл хлористого метилена, фил ьтруют, фильтрат промывают 50 мл 10%-ного раствора бисульфат калия и 5О мл воды. Сушат над безводным сульфатом магния, фильтруют и упаривают. Остаток дважды растворяют в минимальном объеме хлористого метилена и осаждают эфиром. Выход 2,8 г (87,2%), Т. пл 15О-193 С с разложением/0(/ -60,3 (с 1, диметилформамид). Rj 0,57 (А); 0,68(Б) и 0,6О(Г). Гидрохлорид 06 -бензилоксикарбонил- -(трет-бутоксикарбонилфенилаланилглицилпролилфенилаланил- (UJ-нитро)аргинил)- 1иаилпрсм1илпролилглицина (Н 1-9). 1,8 г (1,346 ммоль) G 1-9 при растворяют в 2О мл смеси трифторуксусной кислоты с хлористым метиленом (1:1) выдерживают 20 мин при комнатной температуре и упаривают при О С. Остаток кристаллируют растиранием с 5О мл сухого эфира, отфильтровывают и растворяют 45 в 10 мл сухого диметипформамида. К раствору добавляют О,33 мл (1,5 ммопь) 4,5 н раствора безводного хлористого водорода в тетрагидрофуране и продукт осаждают 100 мл сухого эфира. Выход 1,55 г so ,(95%)/Of/2pO 77,8°. Т. пл. 140-192 С R{ 0,73 (В) и 0,74 (Д). ЦиклоГо -бензилоксикарбонил- Е фв- нилаланилглицилпролилфенилаланил-((0 - -нитро)аргинил)лизилпролилпролилглицил О 1-9). К раствору 1,1 г (0,91 ммоль) Н 1-9 в 2 л сухого диметилформамида 79 S10при перемешивании в атмосфер сухого аргона при О С добавляют 1,5 г (1,98 ммоль) комплекса дициклогексилкарбодиимида с пентафторфенолом (1:3) (комплекс Р ). Смесь перемешивают в атмосфере аргона при комнатной температуре, в течение 6 ч. Затем добавляют раствор О,19 мл (1,38 ммоль) триэтиламина в 300 мл диметилформаМида. Полученнную смесь выдерживают при комнатной температуре 2 сут и упаривают при 28 С. Маслянистый остаток закристаллизовы- вают растиранием с сухим эфиром, фильтРУ т и осадок на фильтре просывают эфиР м. затем водой. Полученный продукт чистят на колонке (2х10О см) с силикагелем (средний размер частиц 20 мк) (фирмы Хемапол, ЧССР). Для элюирования используют систему хлороформ:эганол:н-бутанол:этилацетат (1О:6:4:3). Фракции, содержащие предполагаемый циклопептид, собирают и чистят вновь на колонке с силикагелем (3x250 см, средний размер jacTHU 20 мк), используя систему Б в качестве элюента. Собирают фракции по 20 мл и регистрируют поглощение при 280 нм (Увикорд 11) фракции с 55 по 66 объединяют и упаривают, остаток обрабатывают эфиром. Получают 1О2 мг (9,73%) кристаллического вещества. Т. пл. 163-165 С, Хроматографически чистый (проверен по ТСХ на пластинках МЕРК в 6 системах). 0,47 (Б). Молекулярный вес найдено 1024 (определен криоскопически, используя расплав мочевины), вычислено по формуле 1163, 313./Qi/2j5- 64,1 диметилформамид). 0,37 (Л); 0,43 (Б); 0,89 (В); 0,96 (Д) и 0,37 (Г). , Цикло (6 -фенилаланилглицилпролилфе); ннлаланиларгинил)лизилпролилпролилглицин)диацетат (цикло-Гм( 1-лизил 6-Рлицин)-брадикинин1)3 1-9 зо мг (0,043 ммол1) D 1-9 раство в 5 мл уксусной кислоты и гидриру т 2О ч в присутствии палладиевой черни. Катализатор отфильтровывают, и фильтрат лиофилизуют. Остаток раствора нн ют в 10 мл и вновь лиофилизуют. Растворяют в 10 мл воды, фильтруют через мем- мембранный фильтр Сынпор и вновь , лиофилизуют/ Получают белый рыхлый порошок. Хроматографически гомогенный „76 (с О,65, вода). Выход 45,7 мг (96%). ,0,65 (1 N уксусная кислота). R 0,69 (Д). Аминокислотный пролил 2,83, глицин 1,90, фенилаланин 1,93; лизин 1,00; аргинин 1,23, При триптическом расщеплении арепарата образуется только одно вещество ( IN уксусная кислота), что является покааательством циклического строения пептида. Результаты испытаний биологической активности циклического брацикинина (ЦАБ). Опреаелено1П vivO влияние ЦАБ на кровяное давление у наркотиаированнык крыс; П влияние ЦАБ на сократительную способность матки и подвздошной кишки крыс;4п влияние ЦАБ на васкулярную проницаемость в экспериментах на наркотизированных морскик свинках. В качестве стандартного соединения используют синтетичеср:ий препарат брааикннина производства фирмы ReanaB. 1.Определение влияния на кровяное давление крыс. Экспер(1менты проводят на крьюах обоих полов весом Животных наркотизируют 25%-«ым уретаном 0,5 МЛ/1ОО г. Кровяное давление и леряют с помощью ртутного манометра на закопченой ленте кимографа. ЦАБ- вводят в виде инъекций объемом ОД мл/20 в дозах 0,6-50 мкг/кг. 2.Определение миотропного действия. В экспе риментах используются крысы-сам ки весом 20О-220 г. Регистрируют изото нические сокращения изолированных органо (матки и подвздошной кишки) в определен ном режиме температуры и аэрации. Используют метод кумулятивных сокращений. Проверяют концентрации ЦАБ в диапа зоне 1О -10 моль/л. Рассматривают также влияние ЦАБ в этих концентрациях (с предварительной экспозицией их 3 мин на миотропные эффекты брадикннина (БК) Регистрацию проводят на модифицированном приборе ВИ 6-5МА. 3. Влияние на васкулярную проницаемость. Эксперименты проводят на наркотизированных, морских свинках мужского пола весом 350-400 г. В бедрюнную вену вводят 0,5%-ный раствор красите(;|я (Evans ЪВие) в концентрации 2 мл/кг и спустя 6 мин вводят под кожу ЦАБ в объеме 0,1 мл. Для контроля аналогично вводят стандартное соединение БК и физиологический раствор в объеме 0,1 мл. Через 30 мин животных декаптируют и На снятие слое абдоминальной кожи измеряют два перпендикуляныч диаметра появляющихся синих пятен. Исследуют концентрации ЦАБ от 0,0001 до 1 мг/мл. В этих же концентрациях проверяют влияние ЦАБ на увеличение васкулярной проницаемости, вызванной БК в стандартной концентрации. Результаты. ЦАБ в отличие от БК обладает выра- женым и пролонгированным действием. Пороговая концентрация ЦАБ 5 мкг/кг (у брадикинина 0,5 мкг/кг). В концентрации 5О мкг/кг ЦАБ вызывает эквипрессорный эффект с БК, но со значительной его пролонгацией. В случае ЦАБ эффект понижения кровяного давления на 30- 40% мм рт. ст. продол кается 1-2 ч с последующим восстановлением уровня на 4О-5О% от исходного после 2-3 ч от начала введения (4мг. 1). В опытах ч П vHrOHa изолированной матке -и подвздошной кишке крысы установлено, что у ЦАБ в концентрациях 1О -iCfS моль/л отсутствует миотроп- нов действие, свойственное природному БК. В этих концентрациях ЦАБ также не влияет на миотропное действие БК. Эффект увеличения васкулярной проницаемости у ЦАБ ниже, чем у БК; реакции сравнимы при концентрациях 1 и 25 мкг/кг соответственно (фиг. 2). Таким образом, циклический брадики- НИН по сравнению с природным брадикшнином обладает более выраженной селек- тивностью и продолжительностью гипотензивного эффекта. Формула изобретения Циклический аналог брадикинина, формулы;
облапаюший способностью созаавать пролонгированный авпрессорный эффект в эксперименте П V4VO , а также увёличи. вать васкулярную проницаемость в эксперимент -if) .
Источники информации, принятые во внимание при экспертизе
1, Дзизинекий.А. А. и Гомааков О. А. Киннны в физиологии и патологии сердечно-сосудистой системы. Новосибирск, 1976.
ia.fma.
Мир, 1969, т. 2, с. 112-7.

Авторы
Даты
1981-01-23—Публикация
1977-12-14—Подача