, 1
Изобретение относится к способу полученных новых биологически активных химических соединений, а швенно 7-зсилешенных аминогщетги1И1до-1-оксаде j тиацефалоспоринов, котО1яле могут, найти.применение в медицине.
Известен способ получения 1-сяссадеТиацефалоспоринов общей
-10
1 «vti м
ц.-снев н
5.,.Л oBj о
COBgCHj15
где Аг т 2-тиенил, 3-тиенил, фенил, п-оксифенил или ялгканоилоксифенил, группы СОВ - независимо дауг от друга свободная или завдодён-,20 ная карбоксильнёш группа ;: у - .ат{ водорода или метокс группа,
или их солей, ацилированием соответствующего производного 7-а1««ю-3- 25 -t1гметилтетразол-5-илтиометИл)-1-оксадетиа- 3-цефем- 4-царбоновой кис-; поты соответствующим производным фв илмалоновой кислоты или ее моногалоидангидридсял из. ,30
Эти соединения облаДгиот биологически активными свойствами.
целью изобретения является синтез новых производиых 1-оксадетиацефалоспоринов, расширякшщх арсенал средств воздействия на ашвс организм.
Эта цель достигается основаннь на известной |)еакции способом получения 7-эа1« «ев ис мданоацетамидо- -оксадетй€щефалоспоринов общей формулы (I) $
в,««яи-в«««ш4-т % й
«Z
4ввНtfHj
где Жл озявчает группу
: а
V4
О
где R фенил или монозамещенный ок СИ-, карбамоилокси- или em,f токси4 руш10й фенил,
где R-1 - низоюй влкил
-HJK
группу
«6
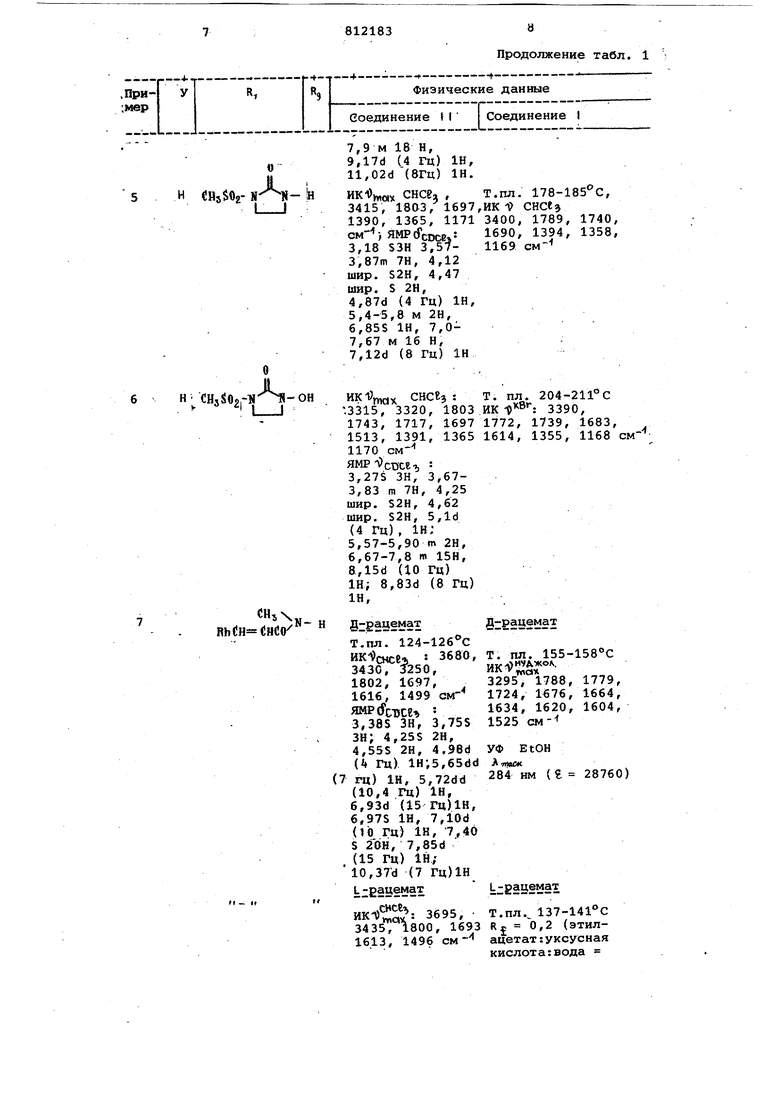
Й4 где Rjj. и R 5 низший алкил и R .атом всадорода, группу где R 7 эил, I -Ы-COR группу где Rft - низпшй алкил и R, - фенил (низший)алкеНИЛ, или R фенил, замещенный двумя ац токсигруппами. окситиопира нил или 8-низший алкил-3-низшая алкокси-5-оксо-5,8 -ДИГКДрОПИрИДО-/2,3-С/-ПИР дазинил, атсм водорода или метоксигруппа, который заключается в том, что в со (II) динении общей формулы Ч fi.ONH- СНЙОКН -4-f I I н, ,CBjS jf где R. R и у имеют указанные выше значения и Z - защитная фенил(низший) алкил-. или дифенил (низший) алкил- группа, удаляют защитную группу , Удаление может быть осуществлено например, гидролизом, восстановлени сольволизом или фотохимической реак цией. Оксадетиацефалоспорины по изобре тению являются активными прот.ивобй ;Териальными средствами против rpciMотрицательиых штаммов и штамйов, ст .ких к другим цефалоспоринам и пенид линам. Соединения формулы (I), включая его некоторые сложные эфиры и фарма цевтически допустимые соли, п эигодны для предотвращения или лечения различных человеческих и ветеринарных инфекционных болезней, вызванны бактериями. Соединения формулы (I) можно вводить как таковые или в сме сях. Кроме того , соединения можно вводить в кснкбинадиях с фармацевти ески ДОПУСТИМКВ1И носителями, раз бавителями, вспсялогательными вещест вами и другими соответствующими лекарствс1ми. Фармацевтические композиции по изобретению могут содержать от 0,01 до 99% по весу соединения формульа (t) в качестве активного ингредиента. Соединения формулы (I) обычно вводят людям и животным суточными .дозами от 250 мг до 5 г, хотя зто количество можно менять в зависимос ти от дели, состояния больного, чув ствительности бактерий, способа и частоты введения. Пример 1. Раствор дифенилметил-7о -метокси-7|V {О-с -фенил-М-{4-этилт2,З-диоксо-1-пиперазинилкарбонил)-глицидиламино - 3-(1-метил-1Н-тетразол-5-илтиометил)-1-оксадетиа-З-цефем-4-карбоксилата (25 ,.1мг) в дихлорметане охлаждают до 0°С. Анизол (0,05 мл)трифторуксусную кислоту (0,1 мл) добавляют к раствору, который перемешивают в течение 30 мин при 0°С и испаряют досуха под пониженным давлением. Остаток растирают с эфиром с получением 7oL-метокси-7р- о-о1-фенил-N- (4-этил-2 , 3-диоксопиперазинилкарбонил)-глициламино -3-(1-метил-1Н-тетразол-5-илтиометил)-1-оксадетиа-3-цефем-4-карбоновой кислоты (13,8 мг) в качестве бесцветного порошка. Выход 69,2%. т. пл. 152-156 с, ИК анализ: V В 1785, 1713, 1680 см-: При м ер 2. Тем же самым способен, что и в примере 1, дифенилметил-7- о-о1,- (п-оксифенил) -N- (1,3-диметилуреидокарбонил) -глициламино}-3-(1-метил-1Н-тетразол-5-илтиометил)-1-оксадетиа-3-цефем-4-карбоксилат обрабатывают с получением 7- о-dL- (п-оксифенил) -N- (1,3-диметилуреидокарбонйл)-глициламино -3-(1-метил-1Н-тетраэЬл-5-илтиометил)-1-оксадеTiaa 3-1|ефем 4 карбоновой кислоты. Т. r vr50 -;i80c. ИК aiiahrf3: :rtrer4 3400, 2940, 1784, 1682 1j&v32 civf . ,8+2,1 (С 0,522 в 1%HOfci |УгаН60-5) . . П p И м e p 3. Тем же самым способом-, что и в примере 1, дифенилметил-7-1;0-№-(3,4-диацетоксибензоил)-фенилглициламино -3-(1-метил- 1Н-тетразол-5-илтиометил)-1-оксадетиа-3-цефем-4-карбоксилат обрабатывают с получением 7-fO-N - (3,4-диацетоксибвн3оил )-фенилглициламино -3- (1 -метил-1 Н-тетразол-5-илтиометил)-1-оксадетиа-З-цефем-4-карбоновой кислоты, анализ: М 1780, 1700, 16 анализ: М 1780, 1700, 1660 см R« 0,78 (Этилацетат:уксусная кислота:вода 3:1:1), 0,58 (хлороформ:метанол Rf 1:1) R 0,24 (хлороформ: метанол :)- . Примеры 4-9. Тем же способом, что. в примере 1, были получены следующие соединения, физико-химйчес-, кие данные которых приведены в . табл. 1. Пример 10. Тем же самым способом, что и в примере 1, дифенилметил-7- {о- о(. (п-ацетоксифенил) -NT (4-этил-2,З-диоксо-1-пиперазинил-карбонил)-глициламино -3-(1-метил-1Н-тетразол-З-илтиометил)-1-оксадетиа.-3-цефем-4-кар6оксилат (60 «) вып обработан с получением 7-f D- «L - (п- , -ацетоксифе.нил) - М - (4 -этил- -дйоксо-1-йипераэинилкарбЬнил)-гл1|цияам91но}-3-(1-метил-1Н-тетразол-5-илтно- . метил)-1-оксадетиа-3-цефем-4-карбоновой кислоты (43 мг}.
Т. пл. 165-170°С (d). ИК анализ:A S,aii 3270(Вг), 1685/ 1756(Sh), 1710, 1975 см
П р и мер 11, Тем же самым способом, что ив примере 1, дифеиилметил -7 А-мет6кси- О - oL - (п -гидфоКсифенил)-N-(трет-бутилоксикарбонял)-оксадетиа-3 цефем-4-карбоксилатбьш обработан с получением 7о{.-метокси-7р- D-oL-(п-гидроксифенил)-глициламино -3-(1 метил-1Й-тетраэол-5-илтис «етил)-1-оксадетиа-3-цефем-4-карбоиовой кислоты трифторацетата. ИК аиализ :i ., 3200, 2600, 1770, 1660-1700 СМ-;
Пример 12. Тем же самим слоббом, что и в примере 1, дифенилметил-7-eL -метокси-7р- fo-oL (h-карбглюилоксифенил)-N-(4-этил-2,3-диоксо-1-пиперазииилкарбонил)-глициламиио}-3-(1-метил-1Н-тетразол-&-илтиометил) -1 -оксадетиа- 3 -цефем- 4 -карбокси.-т лат (30 Mf) был обработан с получением 7 а1-метокси-7 }Ь - fo- з1-(п-карбамоилоксифенил)-N-(4-этил-2,3-диоксо-1-пиперазинилкарбонил)-глициламиHoJ-3- (1-метил-1Н-тетразол-5-илтио- метил7-1-оксадетиа-3-цефем-4ткарбоиовой кислоты (22 мг). ИК анализ:ljj i 3290 (Вт), 1780, 1730 (Sh), 1700, 1670 (Sh) СМ- .
Пример 13. Тем же сгмым способом, что и в примере 1, дифенмл №тил-7- о - ot - ( -карбамоилоксифеиил) -N - (4-метил-2,3-диоксо-1-пипераэиR-CONHCHCOHH
н илкарбонил} -глициламиноЗ -3- (1-метил-1Н-тетразол-5-илтиометил)-1-оксадетиа- 3-Цвфем-4-карбоксилат (85 мг) был обработан с получением 7- 0-й1-(п-карбамошюксифенил) -N-(4-метш1-2,З-диоксо-1-пиперазинилкарбонил)-глициламино -3-(1-метил-1Н-хетразол-5-илтис «етил)-1-оксадетиа-З-цефем-4-карбоновой кислоты (54 мг) в качестве пудры.
Г. пл. 173-176 С..
0
ЙК анализti&;j;gj .3295, 1783, 1740, , 1710, 1682 .-
; Пример 14. Дифенатшетил-. . - (п-карбамоилоксифенил) -Н- (4-этил-2,З-диоксо-1-пиперазинилкар-: бонш1)-глициламинрЛ-3-(1-метил-1Н5-тетразол-5-илтис втил)-1-оксадетиа-З-цефем-4-карбоксилат (50 мг) был обработан тем же спосюбоМг что ив примере 1, с получением 7- в-«А-(п- -карбамоилоксифевил) -М-(4-этил0-2;З-диоксо-1-пиперазинилкарбонил)-глициламино -З- (1-метил-1Н-тетразол -5-илтиометил)-1-оксадетиа-3-цефем-4-карбоновой кислоты (33 мг) в качестве порошка., .
5 &ЛХОД 83%.„
ИК анализ-Оп,,. 3270, 1775, 1720(Sh), 1700, 1655 ст«-1
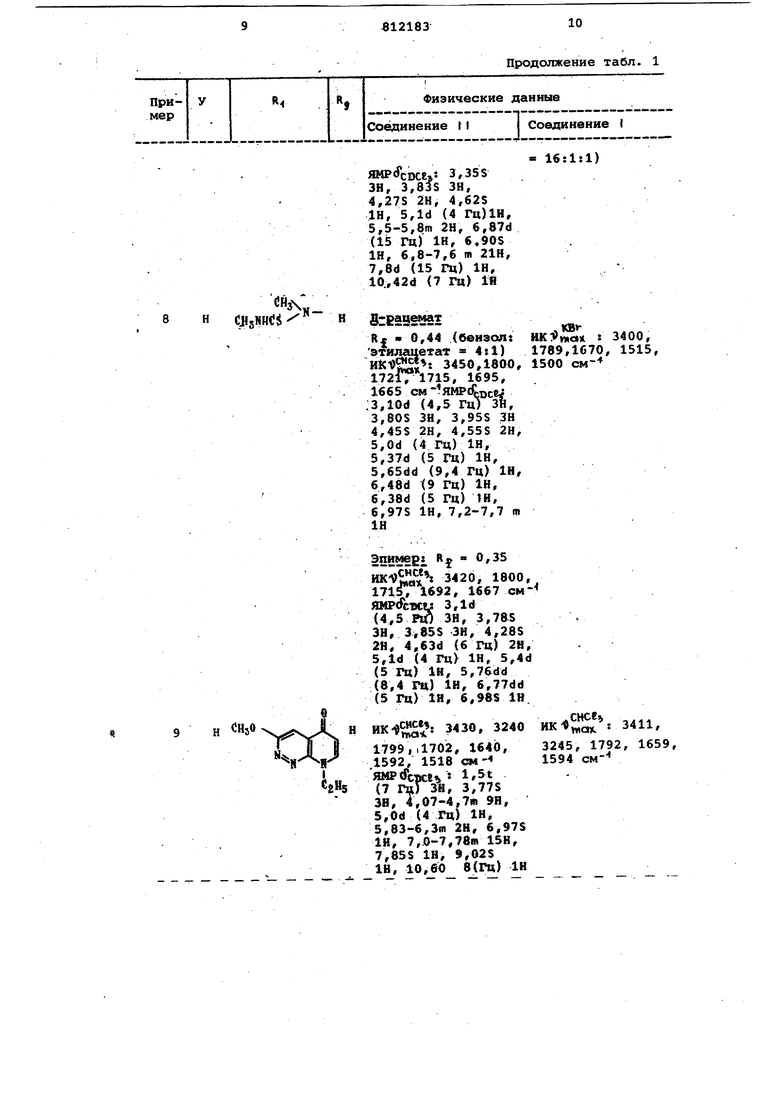
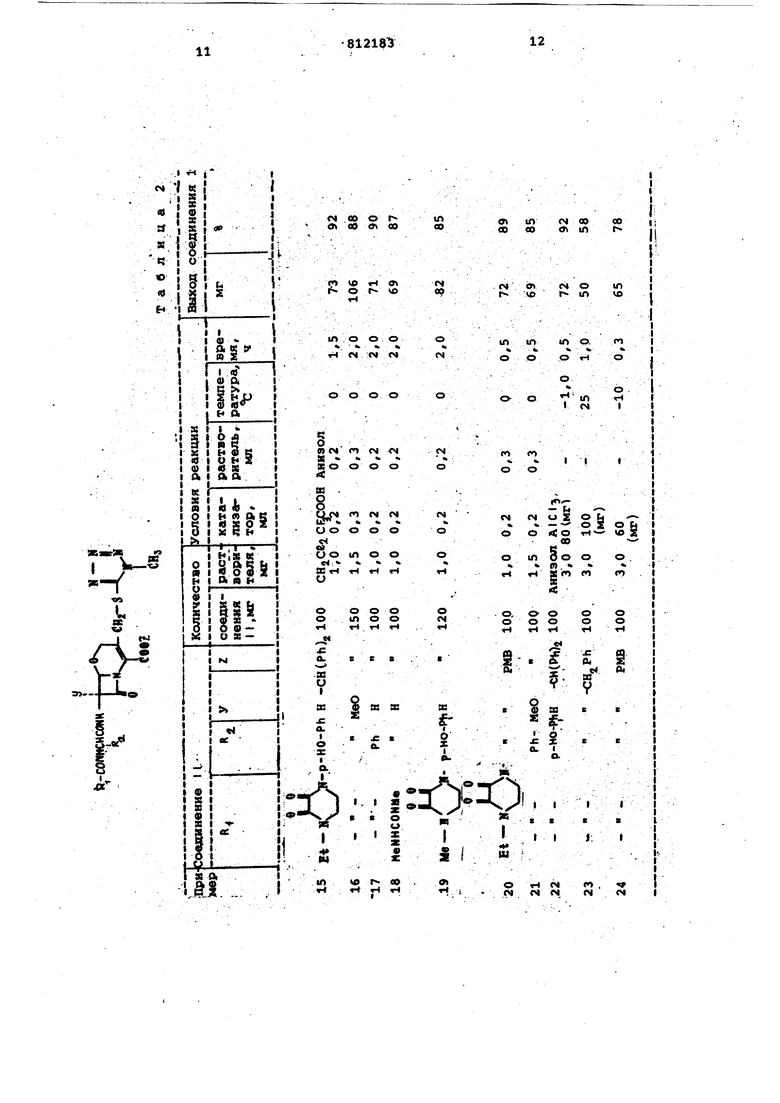
Пример 15-24. Соединение (11) гидролизуется под действиал
0 условий, описанных в табл. 2, с по- . лучением соединения (1).
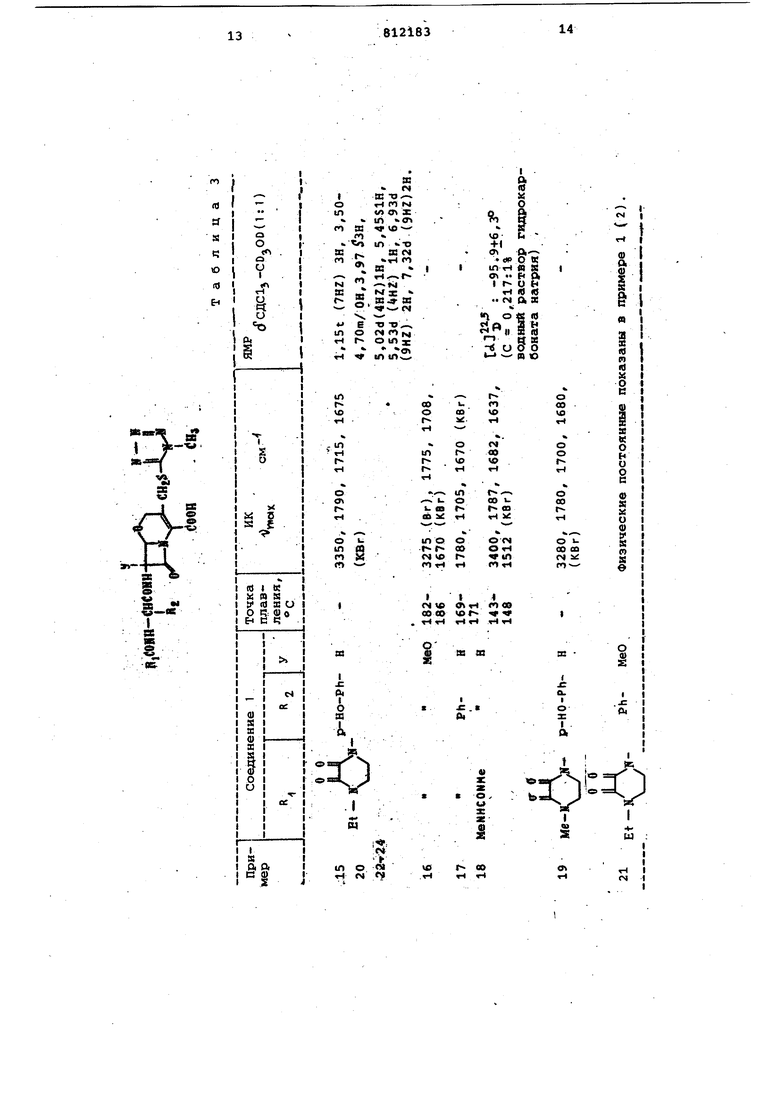
Физические постоянные соединений (1) показаны в табл. 3.
5
Используемые сокращения: Me - метил, .
Et - ЭТИЛ,
Ph - фенИл,
p-OH-Ph - п- Оксифенил,
0
РМВ - пг-метоксибензил.
N«,14
,
,-.Л.,4 О cow
си.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 7-замещенныхАМиНОАцЕТАМидО-1-ОКСАдЕТиАцЕфАл-ОСпОРиНОВ | 1978 |
|
SU799665A3 |
| Способ получения 7-замещенных аминоацетамидооксадетиацефалоспоринов | 1977 |
|
SU786901A3 |
| Способ получения 7-метокси -1-оксадетиацефалоспоринов | 1978 |
|
SU860704A1 |
| Способ получения 7-замещенных амино-АцЕТАМидООКСАдЕТиАцЕфАлОСпОРиНОВ | 1978 |
|
SU831079A3 |
| Способ получения ацилуреидоцефалоспоринов или их солей или эфиров | 1975 |
|
SU541438A3 |
| Способ получения 1-оксадетиацефалоспоринов или их солей | 1977 |
|
SU1056903A3 |
| Способ получения производных цефалоспорина | 1982 |
|
SU1119608A3 |
| Способ получения производных цефалоспорина | 1979 |
|
SU1118289A3 |
| Способ получения производных цефалоспорина | 1981 |
|
SU1047392A3 |
| Способ получения уреидозамещенных цефалоспорановых соединений или их солей | 1975 |
|
SU583761A3 |

а
3410, Т.пл. 185-190 С,
1602, 1707, 1668,ИК I 3410,
16в5, 1512 см- 1779, 1665, 1603
3,82 1522 см-
за, 4,28 шир.
52Й, 4,5г
ЦВ1Р. $26, 5,02d
(4 Гц) IH, 5,75
dd (9, 4 Гц), 1Н
(8 Гц) 1Н;
6,95.,10И CHsSOz-N- H-1Н
V
CHjSO i
он
N- н
(К
(7 гц) 1Н, 5,72dd
Продолжение табл. 1
Т.пл, 178-185 с,
ИК 1 CHCe
3400, 1789, 1740,
1690, 1394, 1358, 1169 см-
ИК ГМСПС. СНСКз :
Т. пл. 204-211°С ИК 3390, 3315, 3320, 1803 1743, 1717, 1697 1772, 1739, 1683, 1614, 1355, 1168 см1513, 1391, 1365 1170 смЯМРЛ ст)се-ь : 3,275 ЗН, 3,673,83 га 7Н, 4,25 шир. 52Н, 4,62 шир. 52Н, 5,Id (4 Гц), 1Н; 5,57-5,90 m 2Н, 6,67-7,8 m 15Н, 8,15d (10 Гц) 1И; 8,83d (8 Гц) 1Н,
Д-рацемат
g gaugMaT Т.пл. 124-126 с
Т. пл. 155-158°С
ИК СНСвз, 3680, HK HVAxov 3430, 3250,
3295, 1788,1779, 1802, 1697, 1616, 1499 см1724, 1€76,1664,
® р свсе%
1634, 1620,1604, 1525 CM-f
3,385 ЗН, 3,755 ЗН; 4,255 2Н, 4,555 2Н, 4,98d
УФ EtOH (Ц Гц) lH;5,65dd
Л««ЙС
284 нм ( 28760) (10,4 Гц) 1Н, 6,93d (15 Гц)1Н, 6,975 1Н, 7,iOd (to Гц) 1Н, 7,40 5 20Н, 7,85d ,(15 Гц) 1Н; 10,37d (7 Гц)1Н
и цацемат
Т.пл. 137-141°С R 0,2 (этилацетат ;уксусная кислота:вода 8 Н CjIsWHl
CHjO
Ч
«2И5
Продолжение табл. 1
ЯМРЙсвсЕ : 3,355 ЗН, 3,835 ЗН, 4,275 2Н, 1Н, 5,Id (4 Гц)1Н, 5,5-5,8.т 2Н, 6,87d (15 Гц) 1Н, 6.905 1Н, 6,8-7,6 m 21Н, 7,8d {15 Гц) 1Н, 10,424 (7 Гц) ifl
3nKMeg R « 0,35
3420, 1800, 1715; 1692, 1667 см 3,ld (4,5 ЙЮ ЗН, 3,7а5 ЗН, 3,855 ЗН, 4,285 211/ 4,e3d (6 Гц) 2Н, 5,Id (4 Гц 1Н, 5,4d (5 Гц) 1Н, 5,76dd (8,4 ГЦ) 1Н, 6,77dd (5 Гц) 1Н, 6,985 1Н.
. 3430, 3240
1799, .1702, 1640, 1592, 1518 СМ-
ЯШ delicti (7 ГцГзв, 3,775
ЗН, i,07-4.7« 9Н, 5,0d (4 Гц) 1Н, 5,83-6,3я1 2Н, 6,975 1Н, 7,0-7,78т 15Н, 7,855 1Н, 9,025 1Н, 10,60 8(Гц) 1Н SrBasssaz R{ о е,44 (бензола : 3400, этялаиетат 4il) 1789,1670, 1515, 3450,1800, 1500 см- 1721Л1715, 1695, 1665 см ЛИРАпсе 3,10d (4,5 Гц) ЗН, 3,805 ЗН, 3,955 ЗН 4,455 2Н, 4,553 2Н, 5,0d (4 Гц) 1Н, 5,37d (5 Гц) 1Н, 5,65dd (9,4 Гц) 1Н, 6,48d (9 Гц) 1Н, 6,38d (5 Гц) ГН, 6,975 1Н, 7,2-7,7 m 1Н
I i СЧ I «}
C .00 01
О 00 o 00
( vo -i a r о r- «
x
ГЧ 00
n 1Л 00 CO
ri in r
CM да
f4 о
in h- vo
ЛО
г in
-OSФормула изобретения
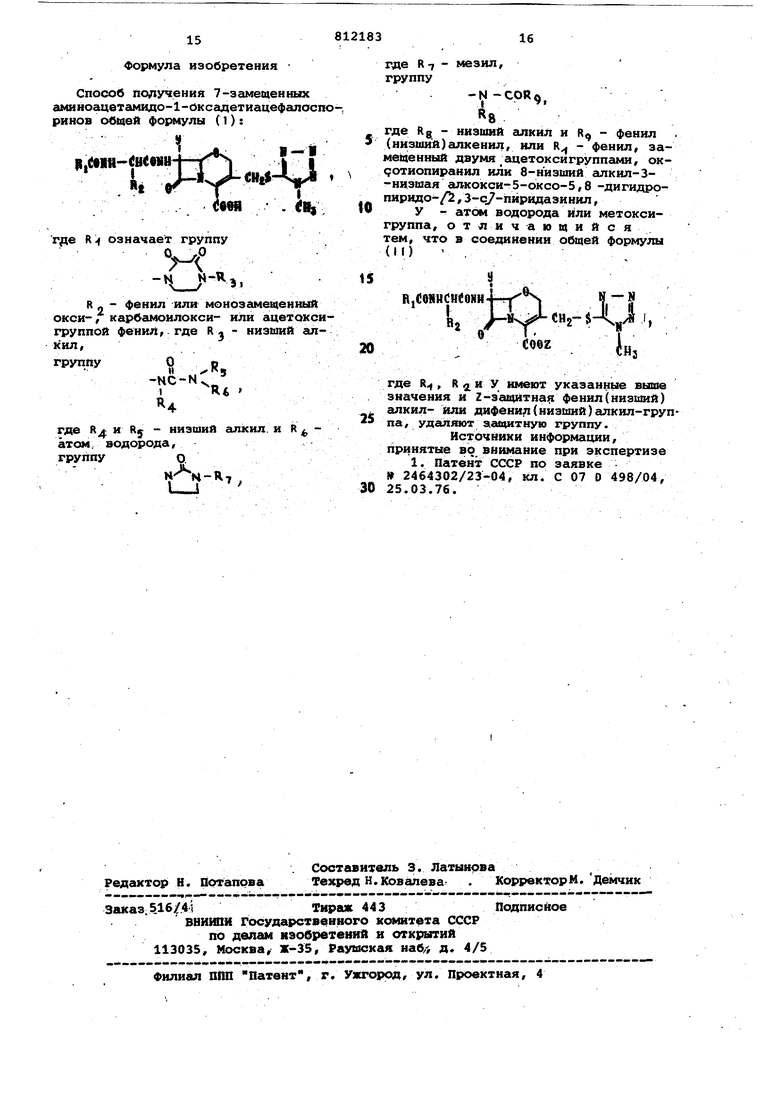
Способ получения 7-заме1ценньпс аминоацвтамидо-1-оксадетиацефалоспоринов обцей формулы (1):
- И
t
где R означает группу ,9
-N N-R
аи
к л фенил или монозамеценный ОКСИ-, карбамоилокси- или а цетоксигруппой фенил,, где Rj низший алкил,
группу
-NC-N.
I RA Ч
где R и RJ - низший алкил и R атом; водорода, группу о.
,
где RT - мезил, группу
-N-COR,
где Rg - низший сшкиЛ и R) - фенил (низший)алкеНИЛ, или R - фенил, заме4денный двумя ацеток си группами, ок(;отиопиранил или 8-низший алкил-3-низшая алкокси-5-оксо-5,8-Дигидропиридо-/,3-с7-пиридазинил,
У - атом водорода или метоксигруппа, отличающийся, тем, что в соединении общей формулы (И) .
Rj(oeHdHteM«4-rf ®N
иг ,
20 cm . L
где R , R 2 X У, имеют указанные выше значения и г- заюйтная фенил (низший) алкил- или дифенил(низший)алкил-группа, удаляют ааЕцитную группу.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1981-03-07—Публикация
1978-09-05—Подача