Изобретение относится к ветеринарии, в частности к производству антибиотиков. Известны способы получения антибиотиков, например А-4696, путем выращивания в аэробных условиях культуры Aetinoplahes sp. АТСС 23342 на среде, содержащей источники углерода азота и минеральные соли 1 . 20-Деоксинаразин и 20-деоксй-эпи-17-наразин являются новыми полиэфирными антибиотиками. Они наиболее тесно связаны с известным полиэфирным противомикробным наразином 2 и -13} . Способ получения деоксинаразиново го антибиотического комплекса заключается в том, что вырадивают Strepto myces aureofaclens NRRZ 11181 в куль туральной среде, содержащей ycBcLHBaемые источники углерода, азота и неорганических солей, в условиях аэроб ной ферментации при погружении и при достижении необходимой величины антибиотической активности, антибиоти.ческий комплекс извлекают из культургшьной жидкости в виде кислот и их фармацевтически приемлемых солей. Деоксинаразиновые антибиотики подавляют рост болезнетворных организмов, патогенных для животных и растений. В соответствии с одним из аспектов изобретения деоксинаразиновые антибиотики являются антикоккидиальными веществами. Кроме того, деоксинаразиновые антибиотики увеличивают усваиваемость пищи жвачными животными. Деоксинаразиновый антибиотический комплекс включает 20-деоксинаразин и 20-деокси-эпи-Д7-наразин i получаемые при брожении в виде смеси. 20-Деоксинаразин и 20-де6кси-Э11и-17-наразин выделяют и разделяют в виде индивидуальных .веществ в соответствии с приведенным ниже описанием. Деоксинаразиновый комплекс также содержит незначительное количество-веществ, которые удаляются в соответствии с описанной ниже методикой. Деоксинаразиновый антибиотический комплекс растворим в большинстве органических растворителей, но нерастворим в воде.
38164924
20-Леоксинаразин обладает той жераэин. Структура 20-деоксинараэкна
абсолютной конфигурацией/ что и на- представлена в виде
он
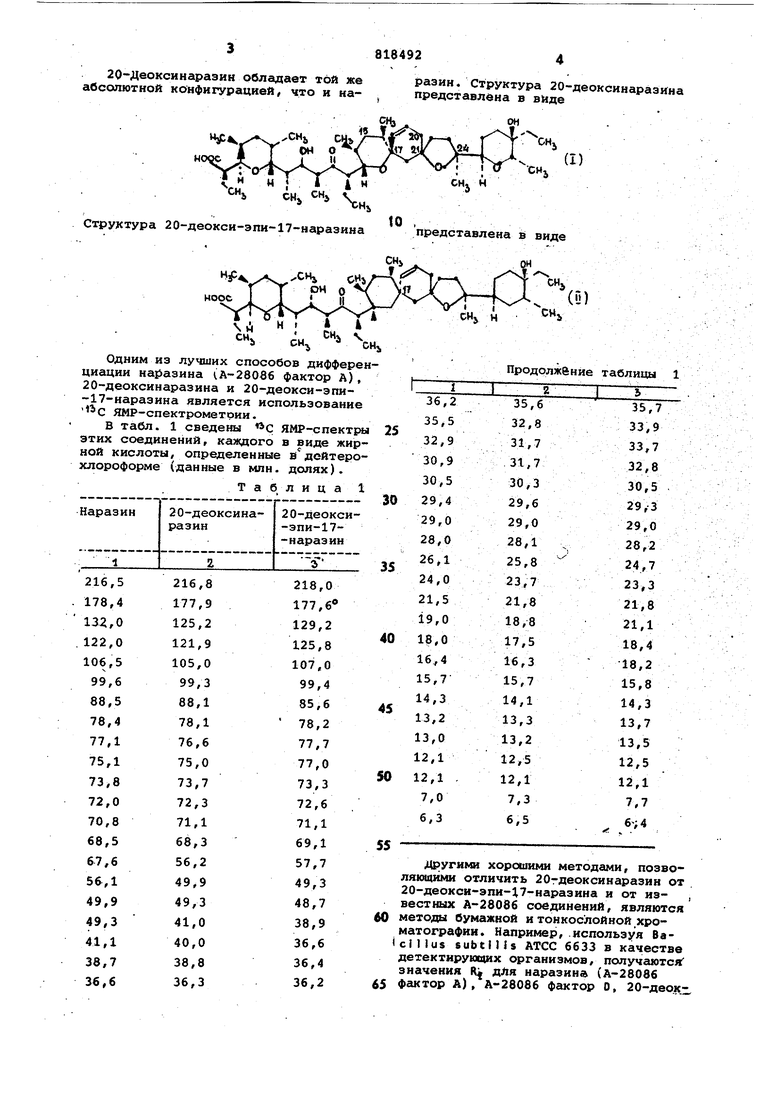
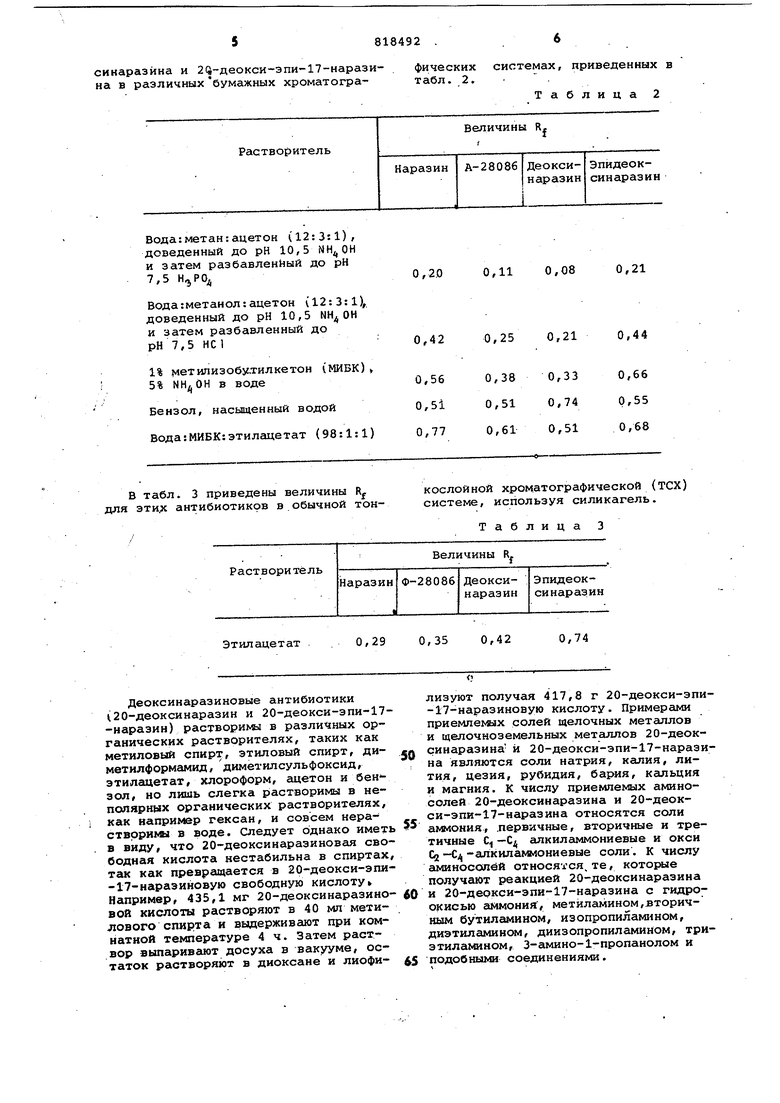
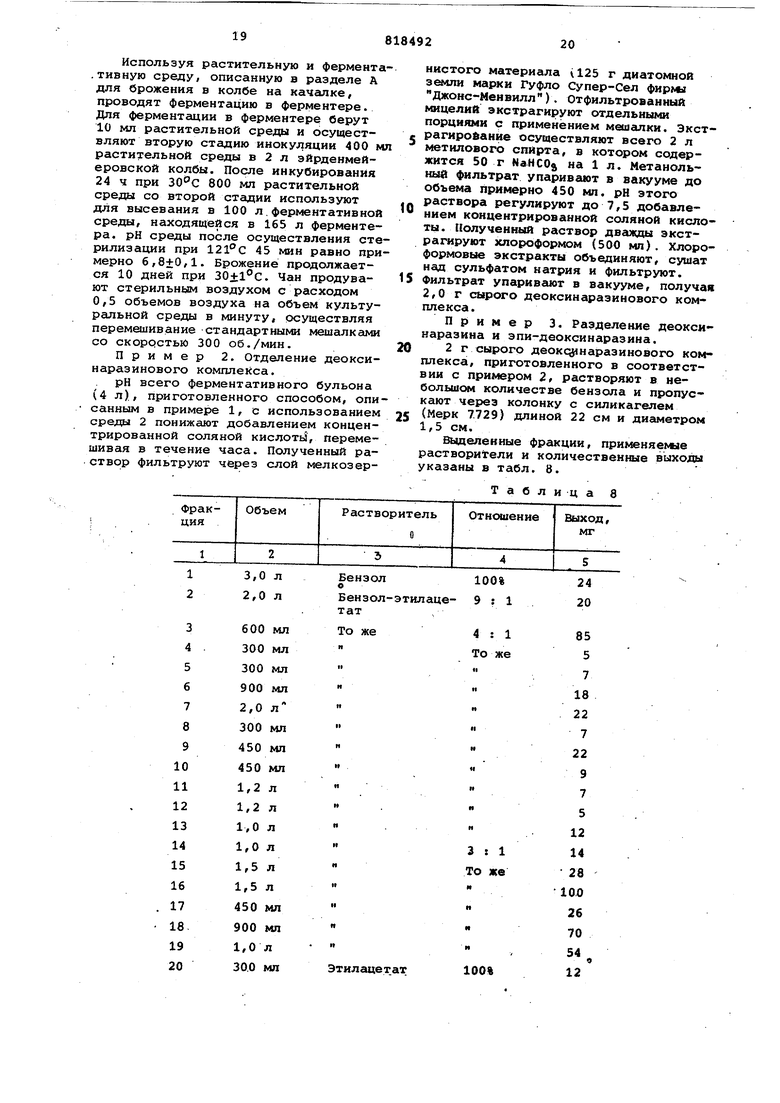
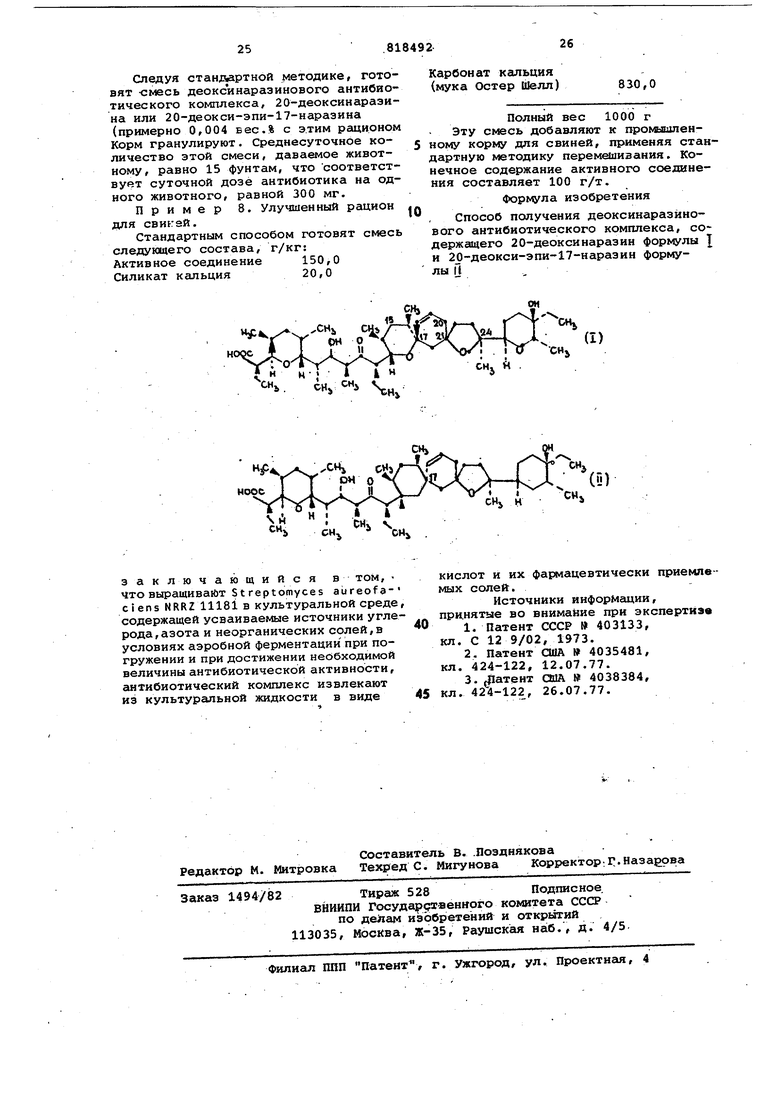
сикаразина и 2(5-деокси-эпи-17-наразина в различных бумажных хроматографических системах, приведенных в табл. 2.
Таблица 2








| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения антибиотического комплекса а-28086 | 1975 |
|
SU576966A3 |
| Способ получения антибиотика | 1974 |
|
SU509246A3 |
| Способ получения гликопептидных антибиотиков А82846А, А82846В и А82846С или их солей, штамм актиномицета NocaRDIa оRIеNтаLIS NRRL 18098-продуцент гликопептидных антибиотиков А82846А, А82846В и А82846С, Штамм актиномицета NocaRDIa оRIеNтаLIS NRRL 18099-продуцент гликопептидных антибиотиков А82846А, А82846В и А82846С и штамм актиномицета NocaRDIa оRIеNтоLIS NRRL 18100-продуцент гликопептидных антибиотиков А82846А, А82846В и А82846С. | 1987 |
|
SU1724015A3 |
| Способ получения полиэфирного антибиотика А 80190 | 1985 |
|
SU1531861A3 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИЧЕСКОГО КОМПЛЕКСА | 1972 |
|
SU352469A1 |
| Б П Т Б Алчп '>&-,'Ю^У'^:''ЛЧ1 | 1973 |
|
SU404186A1 |
| Способ получения антибиотика | 1978 |
|
SU738517A3 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА | 1990 |
|
RU2029783C1 |
| Способ получения антибиотика | 1972 |
|
SU442605A1 |
| ШТАММ LACTOCOCCUS LACTIS SUBSP.LACTIS F-119 - ПРОДУЦЕНТ АНТИБИОТИЧЕСКОГО КОМПЛЕКСА LGS И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИЧЕСКОГО КОМПЛЕКСА LGS С ЕГО ИСПОЛЬЗОВАНИЕМ | 2007 |
|
RU2374320C2 |

Вода:метан:ацетон (12:3:1),
доведенный до рН 10,5
и затем разбавленный до рН
7,5
Вода:метанол:ацетон {12:3:1),
доведенный до рН 10,5
и затем разбавленный до
рН 7,5 НС1
1% метипизоб5г,тилкетон (МИБК)
В табл. 3 приведены величины R для ЭТИ.Х антибиотиков в обычной тонЭтилацетатДеоксинаразиновые антибиотики 20-деоксинаразин и 20-деокси-эпи-17 -наразин) растворимы в различных органических растворителях, таких как метиловый спирт, этиловый спирт, диметилформамид, диметилсульфоксид, этилацетат, хлороформ, ацетон и , но лишь слегка растворимы в неполярных органических растворителях, как например гексан, и совсем нерастворимы в воде. Следует однако имет в виду, что 20-деоксинаразиновая сво бодная кислота нестабильна в спиртах так как превращается в 20-деокси-эпи -17-нараэиновую свободную кислоту Например, 435,1 мг 20-деоксинаразино вой кислоты растворяют в 40 мл метилового спирта и выдерживают при комнатной температуре 4 ч. Затем раствор выпаривают досуха в вакууме, остаток растворяют в диоксане и лиофи0,11 0,08 0,21
0,25 0,21 0,44
кослойной хроматографической (ТСХ) системе, используя силикагель.
Таблица 3
0,29 0,35
0,74
0,42 лизуют получая 417,8 г 20-деокси-эпи-17-наразиновую кислоту. Примерами приемлемых солей щелочных металлов и щелочноземельных металлов 20-деоксинаразина и 20-деокси-эпи-17-наразина являются соли натрия, калия, лития, цезия, рубидия, бария, кальция и магния. К числу приемлемых аминосолей 20-деоксинаразина и 20-деокси-эпи-17-наразина относятся соли аммония, .первичные, вторичные и третичные С -Ц алкиламмониевые и окси Cj -С -алкиламмониевые соли. К числу аминосопёй относятся,те, которые получают реакцией 20-деоксинаразина и 20-деокси-эпи-17-наразина с гидроокисью аммония , метиламином,вторичным бутиламином, изопропиламином, диэтиламином, диизопропиламином, триэтиламином, З-амино-1-пропанолом и подобными соединениями. Катионные соли щелочных и щелочно земельных металлов 20-деоксинараэина и 20-деокси-эпи-17-нараэина получают в соответствии с методикой, обычно используемой для приготовления катионных солей. Например, антибиотик в виде свободной кислоты растворяют в подходящем растворителе, таком как ещетон или водный диоксан. К этому раствору добавляют другой раствор, содержащий стехиометрическое количество требуемого неорганического осно вания. Полученную в результате соль выделяют обычными способами, такими как фильтрование или выпаривание растворителя. Аналогичным способом могут быть приготовлены соли органических аминов. Например, к раствору антибиотика в приемлемом растворителе, таком как ацетон, может быть добавлен газо образный или жидкий амин и затем испарением удаляется растворитель и избыток амина. Предпочтительной методикой получения требуемой соли одного из деоксинаразинового антибиотика является соответствующий начальный выбор процедуры выделения, например регулирование рН бульона добавлением соответ ствующего основания или добавлением к экстрагирующему растворителю соответствующей катионной соли. При лечении животного форма антибиотика не имеет значения. В большин стве случаев под влиянием условий, существующих внутри организма животного, происходит изменение первоначальной формы лекарства. Следователь но, для методики лечения не имеет;, зна чения, что лекарство вводится в соле вой .форме. Однако солевой форме може отдаваться предпочтение, исходя из с ображений экономики, удобства и токсичности. Новые антибиотики .получгиот культивированием штамма Streptomyces аиreofасiens, производящего деоксина разин, при глубоких аэробных условия в подходящей культуральной среде до тех пор, пока не будет получена существенная антибиотическая активност Антибиотики извлекаются с помощью ра личных методов вьщеления и очистки, обычно применяелллх и известных в технике. Организм, используемый для получения деоксинаразиновых антибиотиков получается путем мутации Streptomyce aureofaciensvNRRZ 8092 (3) под дайствием М-мет 1л-Ы-нитро-М-нитрЬзогуанадина. Культура, применимая для по лучения деоксинаразиновых антибиотиков, сдается на хранение и входит в коллекцию чистых культур Северного регионального исследовательского цен тра Министерства сельского хозяйства США, сельскохозяйственной исследовательской службы в Пеории, штате Иллинойс 61604 под номером HRRZ 11181. Для выращивания Streptomyces aureofaciens NRRZ 11181 предпочтительным углеводным источником является тапиоковый декстрин, хотя также могут применяться глюкоза, кукуруза, крахмал, плодовый сахар, манноза, солодовый сахар, молочный сахар и подобные соединения. Другими источниками углерода могут служить кукурузное масло, масло земляного ореха, масло соевых бобов и рыбий жир. Предпочтительным источником азота является фермент гидролизуемого казеина, хотя также могут применяться пептоны, мука соевых бобов, мука из семян хлопчатника, аминокислоты, такие как глутаминовая кислота и т. п. К числу питательных неорганических солей, которые могут быть включены в культуральную среду, относятся обычные раЬтворимые соли, способные образовывать ионы натрия, м§гния, кальция, аммония, а также хлоридный, карбонатный сульфатный, нитратный и тому подобные ионы. В состав культуральной среды должны также быть включены микроэлементы, необходимые для роста и развития организмов. При осуществлении процесса брожения в крупных масштабах может оказаться необходимым добавлять небольшие количества (0,2 мл/л) противопенного агента, такого как полипропиленгликоль, если вспенивание представляет серьезную проблему. Выход антибйотика увеличивается при добавлении малых количеств масла, такого как масло соевых бобов. Для получения значительных количеств деоксинаразиновых антибиотиков предпочтительно осуществлять глубинную аэробную ферментацию в ферментерах. Меньшие количества этих антибиотиков могут быть приготовлены во встряхиваемой колбе. -Поскольку временная задержка при производстве антибиотиков обычно связана с инокуляцией больших ферментеров споровыми формами организмов, желательно применять растительную посевную культуру. Растительный инокулят готовят засеванием : малого объема культуральной среды cnopoBi iMH формами мицелиальных фрагментов организма с целью получения свежей активно растущей культуры организма. Затем растительный посевной материал переводят в большие чаны. В качестве культуральной среды для выращивания растительного инокулума может использоваться та же среда, что применяется.при более крупномасштабном брожении, но могут использоваться также и другие среды. Деоксинаразин-вьщеляющий организм может расти в пределах от примерно 20 до . Оптимальный температурный диапазон получения деоксинаразинов ограничен значениями примерно от 7 до . Через среду продувают стерильный воздух, эффективный рост организма достигается т-огда, когда в ферментер подают примерно 0,1 объема воздуха на объем культуральной среды в минуту. Для эффективного получения антибиотиков объем подаваемого возду ха при производстве в ферментере дол жен быть больше 0,25 объема культурапьнои среды в минуту. Высокие концентрации растворенного кислорода не подавляют образования антибиотиков. За получением антибиотиков необхо димо следить по ходу процесса брожения, отбирая пробы бульона или зчстрактов твердых грибниц для определения антибиотической активности. Для испытания предлагаемых антибиотиков применяется организм Bacillus subtilis АТСС 6633. Биоанализ удобно проводить с помощью дисковых бумажных проб на агаровых средах. Начальный рН незасеянной культуральной среды меняется в зависимости от применяемой среды. Обычно рН должен быть в пределах от 6,0 до 7,5, рН в конце брожения обычно несколько выше, в пределах 6,5-8,0. Обычно антибиотическая активность обнаруживается на второй день ферментации. Максимум антибиотической активности обычно достигается примерно на 4-10-й день. При получении деоксинаразиновых антибиотиков глубинным аэробным брожением они могут быть извлечены из ферментативной среды способами, обыч но используемыми в технологии брожения. Получаемые при брожении антибио тики присутствуют как в миЦелиальной массе, так и в отфильтрованном бульоне. Максимальное извлечение деоксинаразиновых антибиотиков достигается следовательно, совместным осуществле нием таких способов.как фильтрование экстракция и адсорбционная хроматография. В качестве растворителя для выделения деоксинаразиновых антибиотиков либо из.всего, либо из фильтро вального ферментативного бульона пре почтительно использовать этиловый эфир уксусной кислоты, хотя удовлетворительные, результаты получают при применении других, обычно используе№1Х растворителей-. Особенно предпочтительным способо выделения деоксинаразиновых антибиотиков является понижение рН всего ферментативного бульона примерно до 3,0. При этой величине рН деоксинара зиновые антибиотики удобно отделять с .мицелиальной массой, используя метод фильтрования. Другим выгодным мо ментом этого способа является добавление бикарбоната, такого как бикарбонат натрия, ко всему бульону в количестве примерно 1 г/л. Используя данный способ, деоксинаразиновые антибиотики удобно отделять от мицелиальной массы в виде соли. Для отделения антибиотиков от мицелиальной массы предпочтительно использовать в качестве растворителя метиловый спирт, однако также могут применять- ся и другие низшие спирты и кетоны. Для извлечения деоксинаразиновых антибиотиков может с успехом использоваться также азеотропная перегонка. В соответствии с этим способом органический растворитель, который образует соответствующую азеотропную смесь с водой, добавляют к водному ферментативному бульону. Полученную смесь растворителя и бульона подвергают азеотропной перегонке для того, чтобы удалить, по крайней мере, половину воды из бульона и получить смесь воды с растворителем, в которой в органическом растворителе растворены деоксинаразиновые антибиотики. Нерастворимые побочные продукты могут быть отделены соответствующими способами, такими как фильтрование или центрифугирование. Затем деоксанаразйновые антибиотики извлекаются из органического растворителя, используя хорошо известные методы, такие .как выпаривание растворителя, осаждение добавлением нерастворителя или экстракция. , В качестве примеров органических растворителей, образующих азеотропные смеси с водой для осуществления такой процедуры извлечения, могут быть указаны такие соединения, как бутиловый, С1МИЛОВЫЙ, гексиловый и бензиловый спирты, бутиловый эфир уксусной кислоты, амиловый эфир уксусной кислоты, 1,2-дихлорэтан, 3-пентанон, 2-гексанон, бензол, циклогексанон, толуол, ксилол и подобные соединения. При осуществлении процессов брожения в крупных масштабах извлечение особо предпочтительно проводить методом азеотропной перегонки. Вода и растворитель, отогнанные из азеотропной смеси, могут быть разделены из-вестными методами и затем рециркулироваться для повторного применения. Отделенная таким способом вода не содержит загрязнителей и не требует осуществления процесса обработки сточных вод. Дополнительная очистка деоксинаразиновых антибиотиков включает дополнительную экстракцию и адсорбцию. В качестве адсорбента предпочтительно применять такие материалы, как силикагель, уголь,флоризнл и подобные материалы. С другой стороны, возможно применение твердой культуральной массы, содержгицей компоненты среды и мицелий, без осуществления. . экстракции или разделения в качестве источника деоксинаразинового антибиотического комплекса, но желательно после удаления воды. Например, после Юстижения деоксинаразиновой антибиотической активности культуральная среда может сушиться путем лиофилизации или на вальцовой суишлке и прямо добавляться к питательной смеси. В соответствии с другим аспектом изобретения после достижения активности культуральной среды отделяют мицелий и сушат его, получая продукт который может непосредственно использоваться в качестве пищевой добавки. При отделении мицелия для такого применения добавки карбоната кальция (примерно 10 г/л) облегчает фильтрование и дает высушенный продукт более высокого кач1гства. 20-Деоксинаразин и 20-деокси-эпи-17-наразин разделяют и вццеляют в виде индивидуальных соединений, применяя хорошо известные методы, такие как хроматография на колонках, тонко слойная хроматография, противоточное распределение и подобные способы. Например, для разделения 20-деоксинаразина и 20-деокси-эпи-17-наразин применяется хроматография на колонке с силикагелем с использованием для элюирогания колонки различных смесей растворителей. Применяя смесь из таких растворителей, как бензол и зтиловый эфир уксусной кислоты, в колон ку с силикагелем сначала элюируют 20-деокси-эпи-17-наразин, а затем 20-деоксинаразин. Тонкослойная хрома тография на колонке с силикагелем с применением чистого этилового эфира уксусной кислоты является удобным способом для контроля за процессом элюирования. Деоксинаразиновые антибиотикиг являются противомикробными агентами. В тавл. 4 представлена относитель ная микробиологическая активность 20-деокси-эпи-17-наразина (свободной кислоты) при применении стандартного диско-диффузионного метода. Таблиц а.4 StaphyIOCOCCUS aureus3055 - 16,9 13,8 -« - 3074 19,5 15,4 - - 19,0 17,2 Streptococcus pyogenes (группа А) 12,0 10,0 (группа D) 17,0 14,6 Dtplococcus pneumonia 16,0 13,0 Устойчивые к пенициллину. Устойчивые к метициллину. в соответствии с одним из аспектов изобретения Деоксинаразиновые антибиотики подавляют рост анаэробных бактерий. В табл. 5 представлены минимальные подавлйгадне концентрации (МПК) 20-деокси-эпи-17-наразина (свободной кислоты) относительно различных анаэробных бактерий. МПК определены стандартным анализом разбавления агара. Конечные значения соответствуют 24-х ч инкубационному периоду. Таблица 5 Actinomyces israeJil w. 8558 Clostridlum perfriffgens 8116 Clostridium septicum 112816 Eubacterium aerofaciens 123516 Peptococcus asaccharojitlcus 1302 .g Peptococcus prevo i 12814 Peptos t reptococcus anaerobius 1428 4 Peptostreptococcus intermedi us 12644 Propionibacterium acnes 792 Bacteroides fragiBisill128 Активность против микоплазмы явяется другим центам аспектом антиикробной активности деоксинараэиновых антибиотиков. Вяд микоплазки известный как плевро-легоч|1оподобный (ПЛПО) организм, является также боезнетворным для челов ека и различных животных. Вещества, активные против Ш1ТО организмов, особенно неободимы в птицеводстве. В табл. 6 сведены значения миниальных подавляющих концентраций (МПК) 20-деокси-эпи-17-наразина (свободной кислоты) против указанных идов микоплазкея, определенных in vitro на бульонных разбавлениях. Таблица 6 МПК, Организм мкг/мп М. gal IIsepticum Н. hyorhinIS Н. synovlae Деоксинаразмновые антибиотики являются также противовирусными препаратами. Например, 20-деокси-эпи-17-наразин активен против риновирусного типа 3, вакци:шого вируса, герпе свируса и вируса анфлюенца Л. В соответствии с одним из аспектов изобретения деоксинарзиновый антибиотик может вводиться млекопитающим перорально, местно или парентерально для подавления вирусов. Для профилактики илч лечения заболеваний применяются обычно дозы, которые меняются примерно от 1 до 5 мг/кг тела млекопитающего в зависимости от типа вируса и от того, применяется ли лекарство профилактически или терапевтически. Более того, растворы, содержащие деоксинаразиновый антибиотик, предпочтительно вместе с поверхностно-активным веществом могут применять ся для дезактивации in vitro мест обитания, где присутствуют вирусы, та кие как полио или герпес. Для подавления вирусов эффективны растворы, содержащие примерно 1-1500 мкг/мл деоксинаразинового антибиотика. Острая токсичность 20-деокси-эпи-17-наразина
Зараженные контрольные
20-Деоксинаразин
(100 млн. долей)
Две клети с четырьмя курами в каждой.. для
обработки.
Максимально возможное число, равное 4,00
Для профилактики или лечения кокцидиоза домашним птицам предпочтительно ежедневно перорально вводят зффективнбе количество деоксинаразинового антибиотика. Деоксинаразиновый антибиотик может быть в различных формах, но -наиболее удобно использовать его вместе с физиологически приемлемыми носителями, предпочтительно с пищей, заглатываемой птицами. Хотя следует учитывать различные факторы при определении подходящей,концентрации деоксинаразинового антибиотика, вводимое количество обычно Нс1ХОДИТСЯ в
пределах 0,003-0,03% от веса нелечебиого корма и предпочтительно в пределах 0,004-0,02%.
Изобретение относится также к антик окциди ал ьным пищевым композициям для домашней птицы, включающим корм
37,5 114
4,00
185 0,13
/
для домашней птищя и примерно 35 160 г деоксинаразинового антибиотика на тонну.
Способность улучшить эффективность усваивания пищи животными является ругим важным свойством деоксинаразиновых антибкотиков. Например, указанные антибиотики улучшгцот усваиваемость пищи жвачнйми животными, которые обладают развитой функцией рубца.
Деоксинаразиновые антибиотики обычно эффективно увеличивают выход пропионатов-и, следовательно, улучшгиот ус аиваеМость пищи при введении жвачным животным перорально, в количестве примерно 0,05-5,0 мг/кг в день. Наиболее впечатляющие результаты остигаются при введении антибиотиков
в количестве примерно 0,1-2,5 мг/кг в (свободной кислоты) и 20-деоксинарааина (натриевой соли) при внутривенном введении мышам,, выражаемся в виде Lugo равна 201 мг/кг и 5 мг/кг соответственно. Антикокцидиальная активность является важным СВОЙСТВСЛ4 деоксинаразиновых .антибиотиков; 20-Део1 синаразин (соль натрия) и 20-Жёокси-эпи-17-наразин (в виде свободной кислоты) являются активными и соединениями в количествах уже 0,2 частей на тысячу, против Etmeria tenella, простейшего организма, большей частью ассоциирующего с кокцидиозом. Опыты на молодых цыплятах показывают, что деоксингфазиновые антибиотики обладают антикокцидиальной активностью in vivo. 20-Деоксинаразин (натриевая соль), вводимой в количестве 100 млн. долей в пищу цыплят, зараженных Eimeria tenel)а, предотвращает смертность, улучшает прирост и уменьшает шсло поражений у цыплят. Результаты эксперимента представлены в т-абл. 7. Таблица 7 день. Предпочтительным способом введения антибиотиков является их смешение с кормом для животного. Однако ВОЗМОЖНО и иное их введение, например в форме таблеток, киселей, пилюль, или капсул. Составление этих различных дозированных форм может осуществляться способами, хорошо известными в ветеринарном фармацевтическом производстве. Каждая индивидуальная дозированная единица должна содержать такое количество соединени которое непосредственно связано с по ходящей суточной дозой для больного животного. Изобретение относится также к пищевым композициям, предназначенным для откармливаемых пород жвачных животных, таких как крупный рогатый скот и овцы. Эти пищевые композиции включают корм для крупного рогатого скота и 1-30 г деоксинаразинового ан тибиотикана тонну корма. Дизентерия у свиней является обыч ным заболеванием в ОНА и других стра нах, ежегодно вызывающая повсеместный падеж скота на свиноводческих фе мах. Профилактику и лечение дизентер у свиней предпочтительно осуществлят включением эффективного количества деоксинаразинового антибиотика в пищевой рацион. Деоксинаразиновые антибиотики обычно эффективны для предотвращения или лечения дизентерии у свиней, если они вводятся свиньям пероргшьно в количестве примерно 35 150 г активного соединения на тонну корма. Особенно предпочтительным количеством является примерно 100 г активного соединения на тонну. 1аибо лее приемлемым способом введения антибиотиков животным является добавка препарата в корм скоту, хотя он может вводиться также ины1«ш способами, например в виде таблеток, капсул, ки селей или пилюль. Каждая дозированная единица должна содержат-ь такое количество антибиотика, которое непо средственно связано с требуемой суточной дозой для животного, подвергаемого лечению. V Изобретение касается также пищевых композиций для свиней, включающих рацион для свиньи и эффективное количество деоксинаразинового антибиотика. Как указывалось ранее, эффективное количество антибиотика обычно находится в пределах примерно 35-150 г деоксинаразинового антибиотика на тонну корма. Деоксинаразиновые антибиотики являются противовирусными препаратами и активны против анаэробных бактерий, таких как Clostrldlum perfringens. Следовательно, Деоксинаразиновые антибиотики целесообразно использовать для лечения и профилактики воспаления тонких кишок у кур, свиней, крупного рогатого скота и овец, а также при лечении воспаления брюшины у жвачных животных. Некоторое Деоксинаразиновые соединения (20-деоксинаразин и его соли) проявляют ионосвязывакщие и ионотранспортирующие свойства и, следовательно, являются ионоформами. Эти соеди-, нения могут применяться в том случае, когда желательно осуществить селективное удаление определенного катиона. Примерами такого применения являются удаление и извлечение ионов серебра из фотографических растворов, удаление токсичных катионов из промышленных сточных вод перед тем, как такие воды попадают в окружающую среду, и обессоливание морской воды. Деоксинаразиновое соединение может использоваться в качестве одного из компонентов ионоспецифического электрода. Эти соединения изменяют катионную проницаемость прир(у1ных и искусственных мембран. Следовательно, деоксинаразиновое соединение может применяться в качестве компонента мембраны, используемой для селективного перемещения катионов . против градиента концантраций. Одним из возможных применений этого свойства является извлечение тяжелых и благородных металлов в промышленных масштабах. 20-Деоксинаразин и его соли являются также активными ингибиторами энзима АТФ-аза, АТФ-аза-фермент, чувствительный к щелочным металлам, был найден в клеточных мембранах. Он вовлечен в энергетические расходы для активного транспорта. Под активным транспортом подразумевается ряд процессов с затратой энергии, с помощью которых поддерживается состав внутриклеточных и зкстрацеллюлярных жидкостей. Ингибиторы . уменьшают энергию, требуемую для. активного транспорта. В опытах вне организма (in vitro) показано, что 20-деоксинаразин; (натриевая соль) подавляет катионтранспортирующую АТФ-азу в печеночной митохондрии при половинной эффективной концентрации 0,065 мгк/мл. 20-Деоксинаразин и его соли являются также эффективными препаратами, тонизирующими деятельность сердца. В экспериментах на изолированном предсердии морской свинки 20-деоксинаразин, например, увеличивает сокращение сердца. Следовательно, изобретение включает также способ увеличе- . ния усилия сокращения сердечной мышцы теплокровного млекопитающего, в соответствии с которым вводится эффективная нетоксичнаядоза 20-деоксинаразина доза фармацевтически приемлемой его соли. Эффективная нетоксичная доза находится в пределах примерно 30-500 мкг/кг живого веса. Предпочтительный диапа:;рн доз ограничен значениями примерно 30 100 мкг/кг веса. Для рассматриваемого способа антибиотик вводится парентерально, например внутривен но. Приемлемым способом введения является капельный метод, при котором антибиотик включают в стандартный внутривенный раствор, такой как раствор глюкозы. 20-Деоксинаразин предпочтительно вводят в дозах ниже примерно 100 мкг/кг до тех пор, пока не наблюдается требуемое усилие силы сокращения. Затем количество вводимого 20-деоксинаразина может регулироваться скоростью подачи так, чтобы обеспечить требуемую реакцию. Как и в случае клинического применения дру гих инотропных препаратов, доза 20 деоксинаразина может меняться для данного клинического случая в зависи мости от таких факторов как индивидуальная, восприимчивость к 20-деокси наразину, характера сердечных наруше ний, т. е. степени повреждения сердечной мышцы, возраста и общего физического состояния больного. Предлагаемый способ получения антибиотического комплекса, включающий применение положительного инотропного агента 20-деоксинаразина, может использоваться в ряде клинических ситуаций, широко классифицируемых ка кардиогенный шок. К ним относятся, например, инфаркт миокарда, послеопе рационный кардиогенный шок и прогрес сирующая сердечная недостаточность. Пример 1.А. Ферментсщия во встряхиваемой колбе. Готовят культуру S t reptomy.ces aureofaciens NRRZ 11181 и сохраняют ее на скошенном агаре, имеющем следующий состав, г: КаНРОд MgSO;, - УНдО МНдМОо,, УНпО ZnSO . 7НвО Глюкоза До 1 л Деиониаирова:нная вода рН (нерегулируемое) Скошенный агар засевают Streptomyces aureofaciens NRRZ 11181 и зараженный сколенный агар инкубируют при 30°С до 7 дней. Созревшую культу ру покрывают стерильно,й говяжьей сывороткой и стерильной петлей удаляют споры. Полученную говяжьесывороточну суспензию спор и мицелиальных фраг ментов лиофилизируют в максимум шес ти гранулах. Одна гранула, приготовленная таким образом, применяется для инокуля ции 50 мл растительной среды следующего состава, г: Глюкоза20 Соевая мука15 Жидкость после замочки кукурузы СаСО. Водопроводная вода рН регулируют до 6,5 добавлением . гидроокиси натрия. Зараженную растительную среду в ленмейеровской колбе объемом мл инкубируют при 30°С приблизиьно 24-28 ч на качалке со скорою вращения 250 об./мин. Инкубироную растительную среду, приготовную в соответствия с описанием мл), используют для инокуляции МП одной из ферментативных сред. Среда 1 имеет следующий состав, г: Тапиоковый декстрин 60 Энзимом гидролизованный казеин 6 Ферментативный гидролизат казеина 2 СаСОп,2 MgSOi,7H,.0О,Б Меласса портвейна с патокой15 Очищенное соевое масло 0,5 мл/л Водопроводная вода До 1 л рН (нерегулируемый) 6,6 Стадекс 11, А. Е. Стели, г. штата Иллинойс. Амбер вне. Лабораторий Амбера, г. Джуни 1атата Висконтин. Sf .Д Амин А фирм Шефилд Кемикл г. Норидж штата Нью-Йорк. Среда 2 имеет следующий состав, г: Тапиоковый декстрин Глюкоза Энзимом гидролизованный казеин Ферментативный гидролизат казеина Дрожжевой зкстракт .СаСОо, . 7Н„0 Меласса портвейна с патокой 15 Очий енное соевое масло 5,0 мл/л Водопроводная вода До 1 л рН (нерегулируемое) 6,4 XX, XXX Соответствуют значениям, указанным в примечании к среде 1. Среда 3 имеет следукнций состав, г: Соевая мука,25 Глюкоза .20 СаСО-ь.2,0 МадбО ЮНдО1,0 Очищенное соевое масло 20 мл Метйлолеат20 мл Ре50ц ,6 MnCJ . «tHttO0,3 Аскорбиновая кислота 0,018 Деирнизиро анная вода до 1 л рН (нерегулируемое)6,5 Брожение щ оводят 10 дней при С на качалке со скоростью вращения об./мин. Б. Брожение в ферментере.
Используя растительную и фермента.тивную среду, описанную в разделе А для брожения в колбе на качалке, проводят ферментацию в ферментере. Для ферментации в ферментер берут 10 мл растительной среды и осуществляют вторую стадию инокуляции 400 м растительной среды в 2 л эйрденмейеровской колбы. После инкубирования 24 ч при 800 мл растительной среды со второй стадии используют для высевания в 100 л,ферментативной среды, находящейся в 165 л ферментера. рН среды после осуществления стерилизации при 121°С 45 мин равно примерно 6,8+0,1. Брожение продолжается 10 дней при 30±1°С. Чан продувают стерильным воздухом с расходом 0,5 объемов воздуха на объем культуральной среды в минуту, осуществляя перемешивание стандартными мешалками со скоростью 300 об./мин.
Пример 2. Отделение деоксинаразинового комплекса.
рН всего ферментативного бульона (4 л)., приготовленного способом, описанным в примере 1, с использованием среды 2 понижают добавлением концентрированной соляной КИСЛОТЫ , Перемешивая в течение часа. Полученный раствор фильтруют через слой мелкозер600 мл 300 мл 300 мл 900 мл 2,0 л 300 мл 450 мл 450 мл 1,2 л 1,2 л 1,0 л 1,0 л 1,5 л 1,5 л 450 мл 900 мл 1,0 л 30.0 мл
нистого материала (125 г диатомной земли марки Гуфло Супер-Сел фирмл Джонс-Менвилл). Отфильтрованный мицелий экстрагируют отдельными порциями с применением мешалки. Экстf рагиробание осуществляют всего 2 л метилово1чэ спирта, в котором содержится 50 г NaHCOft на 1 л. Метанольный фильтрат упаривают в вакууме до объема примерно 450 мл. рН этого раствора регулируют до 7,5 добавле0нием концентрированной соляной кислоты. Юлученный раствор дважды экстрагируют хлороформом (500 мл). Хлороформовые экстракты объединяют, сушат над сульфатом натрия и фильтруют. 5 Фильтрат упаривгиот в вакууме, получая 2,0 г сырого деоксинаразинового комплекса.
П р и м е р 3. Разделение деоксинаразина и эпи-деоксинаразина.
2 г сырого деоксинаразинового ком0плекса, приготовленного в соответствии с примером 2, растворяют в небольшом количестве бензола и пропускают через колонку с силикагелем (Мерк 7.729} длиной 22 см к дигшетром
5 1,5 см.
Вьшеленные фракции, применяемое растворители и количественные выходы указаны в табл. 8.
Таблица8
4 : 1
85 5 7
То же То же
18
22
7
22 9 7 5
12
3 : 1
14
28 То же
100
26
70
54 ,
12
100%
Этилацет.ат Полученный после су рования и упаривани Фракции контролируют методом тонкослойной хроматографии с использованием в качестве растворителя этилацетат. Фракции 16-17 (126 мг) содержат 20-деокси-эпи-17-наразин, а фракции 18-23 - смесь 20-деоксинаразина и 20-деокси-эпи-17-наразина. Смесь 20-деоксинаразина и 20-деокси-эпи-17-наразин а, присутствующую в фракциях 18-23, подвергают хроматографическому разделению по методу препаративной тонкослойной хроматографии. В качестве растворителя используют этиловый эфир уксусной кислоты. Смесь (105 мг на одной пластине и 130 мг на другой) растворяют в малом количестве дихлорметана и вносят на силикагельный (Мерк) препаративный лист. После проявления листа два раздельных материала наблюдают в ультрафиолетовом свете. Каждую из областей, занятую двумя веществами, удёшяют с листа и экстрагируют смесью дихлорметана и метилового спирта (4:1). В этой системе деоксинаразин представляет собой более медленно движущийся компонент по сравнению с двумя другими. Из листа, содержащего 105 мг материала, выделяют 7,5 мг 20-деокси-эпи-17-наразина и 27 мг диоксинаразина. С листа, содержащего 130 мг смеси, получают 4,0 мг 20-деок си-эпи-17-наразина и 56 мг 20-деоксинаразина. Пример 4. Другой способ выделения 2Р-деоксинаразина. Весь ферментативный бульон (95 мл) регулируют до рН 3 добавлением соляной кислоты с последующим перемешиванием в течение часа. Добавляют филь |тровый мелкозернистый порошок (марки 1Гуфло-Супер-Сел, 3%) после чего фильтруют бульон. Отделенную мицелиальйую фильтровую лепешку дважды экстрагируют примерно 45 мл ацетона, который содержит 50 г бикарбоната натрия в литре. Ацетоновые экстракты объединяют и концентрируют в вакууме, получая примерно 10 л водяного раствора. рН этого раствора регулируют до 8,0 добавлением 5Н соляной кислоты и полученный раствор трижды экстра гируют половинными объемами ди5слормен 1д сульфатом натрия, фильтльтрата досуха в вакууме. тана. Дихлорметановые экстракты объединяют и упаривают в вакууме, получая маслянистый остаток. Этот остаток растворяют в 500 мл верхней фазы смеси растворителей гексан-метиловый спирт-вода (10:7:1). Верхнюю фазу экстрагируют шесть раз 300 мл порциями нижней фазы. Экстракты объединяьзт и концентрируют в вакууме, получая остаток. Этот остаток растворяют в диоксане, диоксановый раствор лиофилизуют получая 19,4 г деоксинаразинового комплекса. Несколько образцов, полученных аналогичным способом, объединяют (40 г), растворяют в толуоле и вводят в колонку с силикагелем в жидкостной хроматограф (препаративный жидкостной хроматограф/система 500). Колонку элюируют смесью растворителей толуол-этилацетат (9:1) со скоростью 250 мл/мин, собирая фракции объемом 250 мл. Состав фракций контролируют методом тонкослойной хроматографии. Фракции 37-52 объединяют и концентрируют в вакууме, получая остаток, который растворяют в диоксане и лиофилизуют. В результате получают 7,8 г очищенного материала, обогащенного 20-деоксинаразином. Этот материал повторно пропусзкают через хроматограф (препаративнойжидкостной системы 500 Уотерса, аналогичный описанному выше). После элюирования 50 фракций системой толуол;этилацетат (9:1) элюирующий растворитель заменяют на 100% этилв ® Фракции 51-53 объединяют и упарийают в вакууме, получая остаток, который растворяют в диоксане и лиофилизуют. В результате получают 1,12 г 20-деоксинаразина в виде его натриевой соли. Пример 5. Получение 20-деоксинаразировой свободной кислоты. 200 мг натриевой соли 20-деоксинаразина растворяют в этиловом эфире уксусной кислоты (10 мл), раствор прокываютО,1 Н соляной кислотой (10 мл) и затем дважды водой (5 мл). Полученный органический слой упаривают досуха, получая остаток, который повторно растворяют в диоксане и лиофилизуют, давая 139,6 мг 20-деоксинаразиновой кислоты в виде белого твердого материала.
Пример 6. Рацион для цыплят для подавления кокцидиоза.
Измельченная желтая кукуруза
Соевая мука, экстрагированная растворителем, лущеная, тонко измельченная 50% белка
Животный жир (говяжье сало)
Высушенная рыбная мука с бардой
{60% протеина)
Барда из кукурузы
Дикальцийфосфат, пищевой сорт Карбонат кальция
Смесь витаминов (витамины А, О, , К
и В холин, никотиновая кислота,
паигогеновая кислота, рибофлавин,
биотин, глюкоза в качестве наполнител
Соль поваренная
(MnSO , ZnO, К& , FeSO , CaCOj )
2-Амино-4-оксимасляная кислота .(оксианалог метионина)
Следуя стандартной технологии смешения корма, деоксинаразиновый JJOMплекс, 20-деоксинаразин или 20-деокси-эпи-17-наразин (примерно 0,01 вес.% смешивают с указанным выше рационом. 40 Цыплята, которые получают такой рацион с водой ad Cibitum защищены от кокцидиоз а.
Пример 7. Улучшенный рацион для крупного рогатого скота.
Готовят сбалансированный рацион для крупного рогатого скота, приведенный в табл. 10.
Таблица 10
По приведенному в табл. 9 рецепту готовят сбалансированный высококалорийный рацион,предназначенный для кормления цыплят с целью получения быстр.ого привеса.
Т а блица 9
454
280,6 59
45,4 36,3 16,3 7,3
4,5
2,72
0,91
0,91
50
Содержание в расчете на фунт: 40 2000000 ед. витамина А, 227200 ед. витамина Д, и 385,7 г соевого корма с добавкой 1% масла. Сушенная кукурузная дробина с бардой, содержащей 2000Q ед. альфа65 токоферилацетата на фунт.
Следуя стандартной методике, готовят :месь деоксинаразинового антиСиотического комплекса, 20-деоксинараэина или 20-деокси-эпи-17-нараэина (примерно 0,004 вес. с этим рационом Корм гранулируют. Среднесуточное количество этой смеси, даваемое животному, равно 15 фунтам, что соответствует суточной дозе антибиотика на одного животного, равной 300 мг.
Пример 8. Улучшенный рацион для свикей.
Стандартным способом готовят смесь следующего состава, г/кг: Активное соединение150,0
Силикат кальция20,0
сн
заключающийся в том, что выращивайт Streptomyces aureof ciens NRRZ1118i в культуральной среде содержащей усваиваемые источники углерода, азота и неорганических солей,в условиях аэробной ферментации при погружении и при достижении необходимой величины антибиотической активности, антибиотический комплекс извлекают из культуральной жидкости в виде
Карбонат кальция (мука Остер Шелл)
830,0
Полный вес 1000 г Эту смесь добавляют к промышленному корму для свиней, применяя стандартную методику перемешивания. Конечное содержание активного соединения составляет 100 г/т.
Форко ла изобретения
Способ получения деоксинаразинового антибиотического комплекса, содержащего 20-деоксинаразин формулы и 20-деокси-эпи-17-наразин формулы П
СН,
кислот и их фармацевтически приемлемых солей.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1981-03-30—Публикация
1978-10-19—Подача