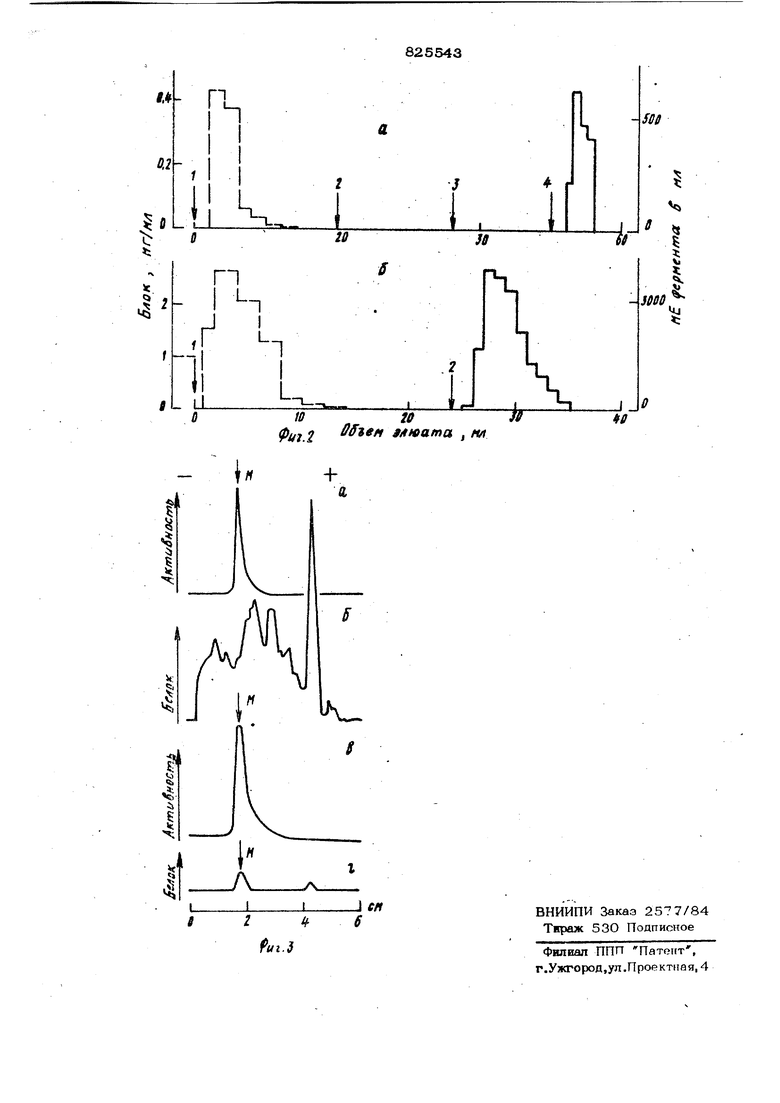
очюценного фермента с высоким выходом из исходных неочищенных, препаратов. Поставленная цель достигается свойствами модифицированной 4-(4-аминоанилино)-5- метокси -1,2-бензохиноном , сефарозы общей формулы R-NH- V-NHгде R - остаток сефарозы. На фиг. 1 представлена схема синтез модифицированной 4-{4- аминоанилино)5-метокси-1,2-бенаохиноном сефарозы; на фиг, 2 .аффинная гфоматография менадио федуктазы; на фиг. 3 - анализ методом диск-электрофореза в полиакрич ламндном геле препаратов менадионре дуктааы опыта, показанного на фиг. 26.; Опыть {см, фиг. 1 и2) вьшолнены на колонке с объемом сорбента 2,6 мл при , скорость прохождения растворов через колонку 0,3-О,4 мл/мин. Пунктирной линией показан белок и сплошной - содержание менадионредуктааы. А. Сорбент (W). 1 - неочищенный Щ}епарат менадионредуктазы, 2i2 мг белка с удельной активностыо / 4,2 мкмоль/(мин мг), 1,15 М фосфатны буфер,рН 7,5 с 0,5 М HfeCC , 2-1/15Л1 фосфатный буфер, рН 6,О,-О,5 MHoiCe, 3-12 мМ НАДФН,; 1/15 М фосфатный буфер, рН 6,О; О,5 MNaCe, 4-10 мМ НАДФН; 1/15 М фосфатный буфер, рН 6,О; 0,5 MNaCE. Б.Сорбент (ИК ).1 - неочищенный препарат менадионредуктазы 17,8 мг белка с удельной активностью . .и1,2 мкмоль/(мин мг); 1,15 М фосфатны буфер,jiH 7,5; ММаСе; 2-1О мМ НАЛФН; 1/15 М фосфатный буфер, рн 6,0; о,б TviKdce. А и Б - неочищенный исходный препа рат менадионредуктазы (см, фиг, З); В и Г - Щ)епарат после хроматографи на сорбенте (VMI ); М - положение менадионредуктазьи Предлагаемое соединение получают на основе СКВ/г. - активированной сефаро зы 4 В и активированной СИ - сефарсвы 4В СзЗ путем нижеуказанных превращений (см, фиг. 1), где соединешш (J) и (V) представляют соответетвенно активированную сефарозу 4В и активированную СН - сефарозу 4В, а вертикальная черта обознаяает полимерную матрицу сефарозы. Как вытекает из схемы, синтез нового соединения проводят в несколько этапов. Реакции присоединения первичного амина к активированной сефарозе проводят известным способом Л., получение анилино-производных 4,5-диметокси-1,2-бензохинона (реакции (2) и (4)) также осуществляют известным путем 4, .Модифицированные 4-( 4-амйноанилино)-5-метокси-1,2-бензохиноноМ сефарозы несут ковалентно связанную структуру 4-анилино-5-метокси-1,2-бензохинона, который является субстратом менадионредуктазы. Этот хинон отецифически взаимодействует с менедионредуктазой с образованием фермент-суб .i-. страктного комплекса, что обеспечивает высокую селективность извлече- . ния фермента из смеси белков. Балласт ные белки не | сорбируются на этом сорбенте и выходят из хроматографической колонки. Таким образом, модифицированная, сефароза представляет собой аффинный сорбент менадионредуктааы, применение которого прзволяет выделить менадионредуктдау из с меси белков и обеспечить высокий вь1ход фермента. Пример, Модификация CNB активированной сефарозы 4В. а) 3 г -активированной сефарозы 4В подвергают набуханию в 1 мМ НС В « Суспензию промывают 6ОО мл 1 мМ НС и 5О мл 0,1 М боратного буфера, рН 8,О, содержащего 0,5 МНоСВ на стеклянном фильтре под вакуумом, создаваемым водоструйным насосом. Сефарозу переносят в колбу, содержащую 2О мл 0,13 М И-фенилендиамина, растворенного в боратном буфере. Суспензию вьздерживают 1 ч 45 мин в условиях осторо кного перё , мещения при 23С после чего переносят на фильтр и промывают бООмл HjCXGOO мл ,5 М раствора НаСв в боратном буфере, рН8,О. Промытая, сефароза имеет белый цвет с легким синеватым оттенком. б) К обработанной сефарозе добавляют 21 мл 18 мМ 4,5-диметокси-1,2-бензохинона,( приготовленного на боратном буфере (О,1 М, рН 8,0). Суспензию выдерживают при помещивании 1ч4О мин, после чего промывают 5ОО мл воды, 50 мл боратного буфера и 15О мл фосфатного буфера О,07 М, рН 7,5, содержашего в растворе 0,5 MNqCe. Промытый продукт в массе обладает краснофиолетовой ояраской, у которого в электронном спектре обнаруживается типичный максимум аминохинона при 51О им. В тцэисут- ствии восстановителей, (тетраборгидрвда натрия и др.) максимум исчезает. Продукт при добавлении восст.ановителей обесцвечивается. После отмывки восстановителя при .стоянии на воздухе продукт восстанавливает свою враснофиолетовую окраску и максимум в видимой области спектра. Все эти свойства присуиш автооксидабельным дифенолам и их аминохинону.что полностью соответствует указанному в описании результату модификации. Продукт модификации сефарозы, полученный ПС (а) и (б)-обеспечивается также в присутствии менадионредуктазы и НАДН (восстановленного никотинамиааденнукпеотида). Последний не восстанавливает аминохиноны в отсутствие менадиокредуктазы. Таким образом, на образование аминохинона указывает также высокоспецифическая ферментативн : реакция, Модификация активированной СН-сефарозы 4В. а)2,2 г активированной СН-сефароаы 4В подвергают набуханию и отмывке. как было описано выше для CNB.j -активированной сефарозы 4В. Сефарозу встряхивают на протяжении 1 ч при 25С с 15 мл О,О9 М раство И-фенилендиамина в боратном буфере, рН 8,0. После этого щэоизводят отмывк получившегося продукта 4ОО мл я 5О мл боратного буфера. Отмытый продукт имеет бель1й цвет с легким синеватым оттенком. б)К продукту, полученному по п. а добавляют 11 мл 18 мМ раствора 4,5диметокси-1,2-бензохинона в боратном буфере, рН 8,0. Суспензию встряхивают 1 ч ЗО мин при , после чего о- мывают на стеклянном филыре 50О мл К продукту добавляют 0,05 М трис буфер, рН 8,0 и вьщерживают при встряхивании 2 ч. Производят отмывку продукта дистиллированной водой, 4ОО м Получившийся продукт обладает краснофиолетовой окраской. Его спектральные характеристики идентичньг таковым для продукта модификации CNB.,- активироаан сефароаы 4В. Продукт обесцвечивается при восстановлении, в том числе и при .специфическом ферментативном восстановлении, как было описано вьпде. Окрас ка восстанавливается до исходной при стоянии на воздухе. П р и м е р 2. Аффинная хроматогра. фия менадионредуктазы. 8 3 Сорбент, приготовленный, как описанвыше, упаковывают в колонку высотой около 2,4 см. На колонку наносят в объеме 0,5-1 мл исходный раствор, неочищенного фермента-менадионредуктагзы, (остальные условия хроматографиисм. фиг. 2).Элюат, т.е. раствор, прошедший через колонку, собщрают фракциями в объеме 1-2 мл, как это показано на гийтрграм- мах фиг. 2. Во всех 4ракциях определяют белок и испытывают на активность менадионредуктазы. Результаты изложены в пояснении к фиг. 2 и 3 и таблице. Как видно из эксперимента, связывание менадионредуктазы с сорбентом высоко специфично. Балластные белки появляются вслед за свободным объемом колонки. Менадионредуктаза остается связанной с сорбентом и её люнруют ; добавлением другого субстрата НАДФН. Таким образом, модифшщрованные сефарозы удерживают менадионредуктазу, но не связьшают другие прямесе. Например, в опыте, показанном на фиг. 2 до введения НАДФН, выз14ваюшего спе- . пифическую десорбцию менадиоаредуктазы, через колонку объемом 2,6 мл было) пропущено 5О мл разных растворов. Последние отличались разным значением рН и высоким содержанием Noice. При такой обработке колонки вымывают все белки, не обладаюище способностью аффинного связывания с сорбентом. На фиг. 3 приведен пример электр форетического анализа исходного, неочищенного препар&та менадиощ)едуктазы и фермента после хроматографии на со{ бенте (VI4 ), Как видно из этого 1фи- мера, происходит одномоментная очистка фермента из сложной смеси белков до двух белковых фракций. Дналогичные результаты получены для сорбента (IV ). В таблице даны количественные результаты хроматографии менадионредуктазы, из которых видно, что фермент г повышает свою активность в 102 раза и выход его составляет 83 %. Приведенные выше примеры в сово«упность характеризуют высокую сорбшюнную, специфичность модифицированных 4( 4-амш1оанилино)-5-метокси-1,2бензохиноном сефароз и г, . -доказывают аффинную природу связывания менадион- редуктазы с этими сорбентами. Применение предлагаемых вьпие модифицированных сорбещ-ов обеспечивает быстрое, однсу этапное получение очищенного фермента с высоким его выходом.
Количественная оценка аффшшой ;фоматографии менадионредуктаэы
на сорбенте ( ) (Данные экслерименга фиг. 26) Определения активности вьшолнкш cS «4-4% при 6-8 наблюдениях


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения сорбента для аффинной хроматографии | 1984 |
|
SU1217461A1 |
| Способ очистки протеолитических ферментов | 1976 |
|
SU644796A1 |
| Биоспецифический сорбент для аффинной хроматографии трипсина | 1978 |
|
SU777041A1 |
| Способ очистки протеолитических ферментов | 1978 |
|
SU942427A1 |
| Способ получения белкового антигена фасциол | 1983 |
|
SU1159579A1 |
| АФФИННЫЙ СОРБЕНТ ДЛЯ УДАЛЕНИЯ ФАКТОРА НЕКРОЗА ОПУХОЛИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2123860C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ТРОФОБЛАСТИЧЕСКОГО БЕТА-1-ГЛИКОПРОТЕИНА | 2007 |
|
RU2325171C1 |
| Способ получения глицеролкиназы | 1987 |
|
SU1433980A1 |
| Способ очистки протеиназ цистеинового типа | 1986 |
|
SU1377292A1 |
| СПОСОБ ПОЛУЧЕНИЯ АФФИННОГО СОРБЕНТА ДЛЯ УДАЛЕНИЯ ФАКТОРА НЕКРОЗА ОПУХОЛИ ИЗ РАСТВОРОВ И БИОСУБСТРАТОВ | 2001 |
|
RU2184569C1 |

Исходнь1й ме-
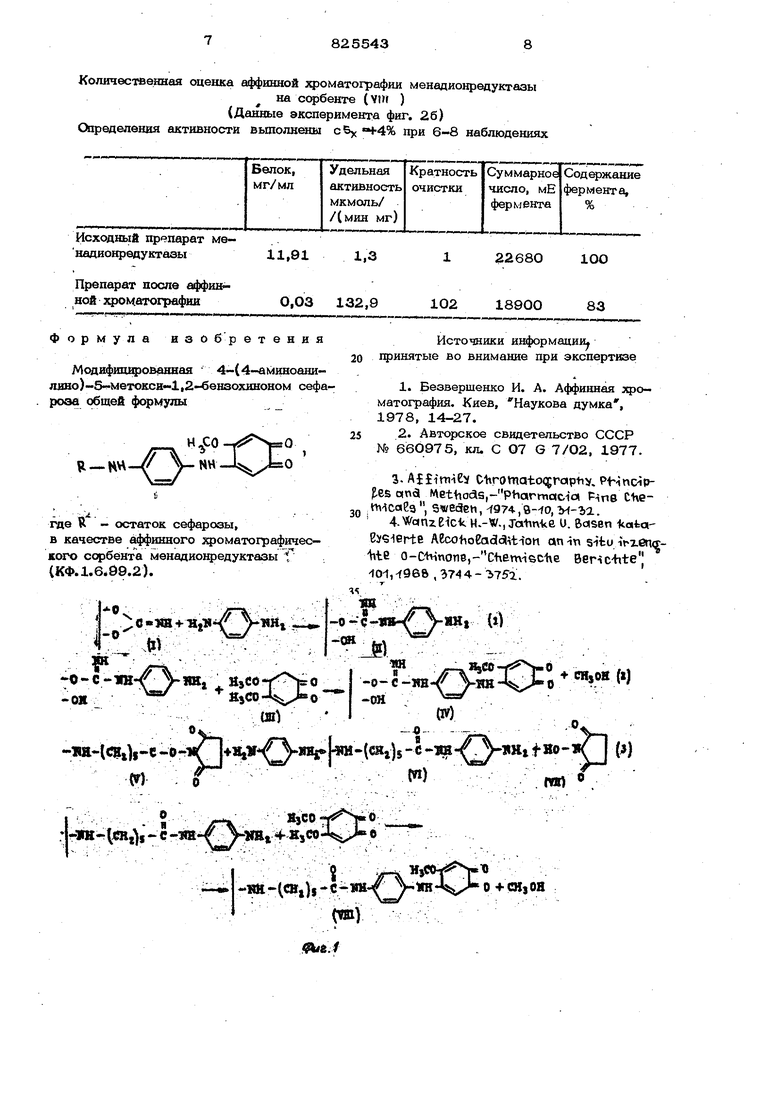
Формула изобретения
Моаифишфованная 4-(4-aм шoaш линo)-5 мeтoкcи-l,2- eнзoxинoнoм сефарова общей формулы
где R - остаток сафароаы, в качестве аффинного :фоматографичес- кого сорбента менадионредуктазы f (КФ. 1..2).
Источники информации
20 гринятые во внимание при экспертизе
NO 660975, кл. С О7 G 7/О2, 1977.
im 4-HsW-4(
- . - 9 -Htt-(CBj)f-C-lM
(Ш)
Авторы
Даты
1981-04-30—Публикация
1979-05-03—Подача