Изобретение относится к новым химическим соединениям - производным 2-арил-З-(2-аминоэтил)-бензофуранов, которые обладаютнейротропным действием. Указанное свойство дает возможность предположить использование этих соединений в медицине. Известен карбидин- (3,6-диметил1 2,3 ,,,9а-гексагидро-3-карболин) , обладающий нейтролептической и антидепрессивной активностью. Целью изобретения является расширение арсенала средств воздействия на живой организм. Эта цель достигается новой химической структурой общей (Формулы (I) (СНг)гН fHX)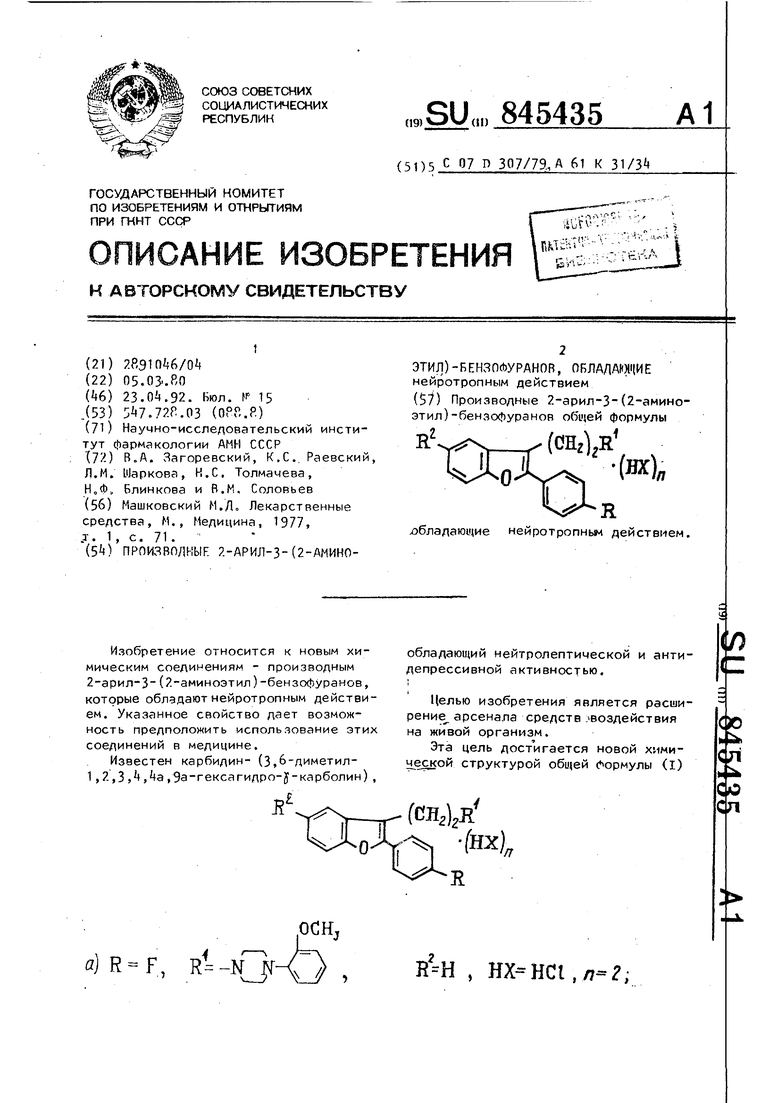





Производные 2-арил-3-
a)R F, Rl-NJf4D , . ,
ОСИ, F, R--Nnv-V}
- -«/ шялааа 12
Е, R-,N3 R, )
Г., .Г, H-HN-O;
..„«
н, rf-:B.
Н , -(
//) R -Н., R--N О .
AJ -F, R N
л .R-F О ;
r-Л )
А Б.-F
/v) E-F,
s.;
,ft-TX
oj K-F,
v-,V
/T) 3 -F, .., ,
I
/ E,-H-, .,.B%i Соединения формулы I получают взаимодействием 2-арил-З-(2-хлорэтил) бензофурана общей формулы II: (II) ,5 .
--Ш с о ;
,HX-HCl , /7-/;
Hdl ,
HCt, /7-f; HCt, n ТГГ4-3. #
nut, 11
HCl, л-/; HCl , Ct,
TrrSf/
Jitl p
KMlCt, /7-f:
,HI-HCt,
ir-NB.,Hi-HooacH-dHCooH,
i.- у
Я-J
r-H . Б1-НС1,
г -i где R и имеют указанные значения. с азотистым основанием общей формулы IIR, где к имеет указанные значения при кипячении с последуюьним выделением целевого продукта в виде соли. Процесс предпочтительно проводят в среде инертного органииеского растпорителя;течение 5 ч получают 1,7. г (1л), Топл. 2б1-.6.с (из абсолютного спир та) , выход . НайденоД,: С 63,1; Н 5,8; С1 8,2; F 4,6; N 6,7. Z7.Hz4ClFN20a, Н 5,8; Cl8, Вычислено,о: С 63, F 4,5; N 6,7. П р и м е р f, Хлоргидрат 2-(-1фторфенил)3(2-циклогексиламиноэтил бенаофурана (le). Аналогично примеру 5 из 2,6 г 2 ({-фторфенил) -3 хлорэтилбензофуран и 3 мл ци логексиламина в 10 мл ксилола получают 1,Р) г (le , ,т.пл. 7.1 ,5°С (из абсолютного спирта), выход 5ог;„ Найдено, Ж: С 70,9; 11,6,8; С1 9,4; F 5 ,1 ; М 3 ,8, СггЛг5 -КОВычислено,%: С 70,7; 11 6,7; С19,5 Е 5,1; N 3,8. П р и м е р 7о Хлоргидрат 2 фенил 3 (2-11иклогексиламиноэтил) -бензофурана (iw), Акглогично примеру-5 из 2,85 г 2 фенил-3 хлорэтилбензофурана и 3 мл ци(логексиламина в 10 мл ксилола получают 1,8 г () , т.пло 2i4l 2i2 C (из абсолютного спирта), выход-(5 ,3 i7,5: С1 9„9 ., Хлоргидрат 2--фенил 3 (2 Г1Иперидинозтил) -бензофурана (Т-з) . Аналогично примеру 5 из 4,1 г 2-фенил 3 Хлорэтилбензофураг а и 3 мл пиперидина в 1П мл-:ксияола по лучают 3 г (1з) , т.пЛо (из абсолютного спирта), выход . НайденоД: С 73,6; И 7,1 ; С1 1П,6: N 4,3„ C jH24ClNO. Вычислено, %: С 73,8; И С1 10,4; N 4,1с П р и м е р 9 Хлоргидрат 2-фени 3 (- МОрфолиноэтил)бензофурана (1и Аналогично примеру 5 из З, г 2фенил-3 5 лорэтилбензофурана получают 3,2 г (Т.и), Топл, 2i( (из абсолютного спирта), выход НайденоД: С 70,0; И 6,4; С1 10,3; N 4,1„ C.g HjeClNOa. Вычислено.X: С 69.9 Н 6,4; С1 10,3; N 4,1 , П р и м е р 10, Хлоргидрат 7.-(h фторфенил)-3-(2-пиперидиноэтил)-бензофурана (1к) . Аналогично примеру 5 из 3,5 г 2-(4 фторфенил)-3-хлорэтилбензофура на м 3 мл пиперидина в 10 мл ксилола в присутствии каталитического количества и од ид а натрия при к -1пяцении в течение 3,5 ч получают 1,9 г (li). т,пл. 2-47 2 8 Г, (из абсолн.тного спир та). вь1ход 8i},2;;;: Найдено.% С 70.1 ; И 6,4; С1 10.1; F 5,2: 3,9. C jH aClFNO. Вычислено f 70 ,1 ; } 6 , 4 ; Cl 9,9; F 5,3; N 3,9, fl n и M e p 1 ,. Хлосгид|5ат 2-(и-Фторфенил)3(2-морфолиноэтил е1 3офурана 11л). Аналогично примеру 10 -из 3,7 г 2 (-фторфенил) -З хлорэтилбенза У мл мo фoлиi a зн. т.пл, 2Г 1--2б2° : (1л ого спирта), выход 5 Найдено ,;: С 64 , -: ; . г -1 . т -3 q ,J -, .,} . : i -J - ; Вычислено,;: С 66,4; 11 5,8; N 3,9 р 12, Дихлоргидрат Смесь. 1 г П-фенилгидроксиламииа хлоргидрата и 2 г азабутирона в 2П мл раствора хлористого водоро;, абсолютном спирте кипятят 2 ч пьпао иий осадок хлористого аммония ог(;)ильтровывают ; спиртовый раствор уг:аривают, 1садок, остави1ийся после упаривания спиртового раствора, поMeii3;oT з 5П мл воды, водный раствор под1нелачивают 5 мл 1 П ,-ного раствора едкого натра,, Водно ,-1целочной раствор экстрагируют эфиром, Зфирнь1Й экстракт )ивают над сульсЬатам магния, сульфат магния отфильтровыBaiOT,-, Из эфирного фильтрата подк1-;с лзнием раствором хлористого водорода 3 абсолютном эфире получают 1,52 г (1м), т.пл. 2 2-2чЗо (из абсолютного спирта), выход 63,. Майдено,: С 63,5- Н 6,5; С1 F А,5; N 6,4, Cj- njtOb.FNxO. Г4ьгчислено,//: С 63,.; Н 6,2; С1 16.,2; F 4.,3; N 6,i
9
П р и м е р 13. Лихлоргидрат .(4-фторФенил) - 3 (.-пергидропирролоP , .-аЗ пиперазино) -этил-5-нитробензофурана (1н) ,
Смесь 0,5. г 4-нитрофенилгидроксиламина хлоргидрата и 0,4 г азабутирона в 20 мл 255 -ного спиртового раствора хлористого водорода кипятя 12ч, Охлаждают, выпавший осадок отфильтровывают, промьччают водой, спиртом. Получают П,Р г (1н), т„пл, С (из абсолютного спирта) , выход k,5%,
Найдено, С 55,4
Н 5,7
С1 13,9; F 3,8; N 8,4; Р,0 (по Фише; Р,0 РУ). 3,3,
Сг5ЧзС127 4. Вычислено,,: С 55,2; К 5.6;
С1- 14,2; F 3,8; N 8,4; 3,6.
Пример 1-fо Трималеат (iфторфенил)-3 С(-Т1еРидропирроло 1,2-а2 пиперазино}-этил1--5 аминобензофурана (1о).
К раствору 1,3 г 2-(-1-фторфенил)3 пергидропирроло 1 , 2-а -пиперазмно этиJlJ 5 нитробензофурана в 25 мл метилового спирта прибавляют 1.2 мл гидразингидрата п присутствии каталитического количества скелетного никеля о Смесь перемешивают при комнатной температуре 2 ч (до исчезновения пятна R 0,6 при тонкослойной хроматографии на окиси алюминия IV степени активност -, хлороформ). Катализатор отфильтровывают, промывают метанолом; метанольнь1Й раствор упаривают, остаток раствор(ют в 50 мл эфира, промывают водой. Эфирный раствор высушивают над сульфатом магния о Сульфат магния отфильтровывают, эфир упаривают. Остаток - 1,1 масла растворяютг в 8 мл абсолютного спирта, нагревают и к горячему спиртовому раствору приливают горячий раствор П,7 малеиновой кислоты в .6 мл абсолютного спирта., Выпавший осадок отфильтровывают, получают 1,4 г (Ю), т.пл. 153-15 °С (из абсолютного спирта) 5 выход kl,:%,
Найдено,,: С 58,1; Н 5,2; F 2,6.
С rj.
Вычислено,%: С 57,8; Н 5,3; F 2,6
Пример 15о Лихлоргидрат 2(4-фторфенил) 3- (4--метилпиперазино1-этил)-бензофурана (in).
Аналогично примеру 10 из 3,5 г 2(4-фторфенил)-З-хлорэтилбензофурана и 5 мл N-метилпиперазина в 20 мл
10
абсолютного ксилола получают 2,7 г (in), ТоПЛ. 7-73 (разлс, из абсолютного спирта), выход 51,5%.
Найдено,%: N 6,8; С1 17,3; F 4,6,
С2, }4,,Cl2.FN-,0(
Вычислено,о: N 6,8; ГЛ 17,2; F 4,6,.
Пример 16,. Л.ихлоргидрат .фенил-З(метилпиперазино-1-этил)5 нитробензофурана (ip).
Аналогично примеру 10 из 1,1 г 2--фенил-3 хлорзтил-5 митро6ензофурана и 3 мл N-метилпиперазина в 15 мл абсолютного ксилола получают 1 г (IP), т,пл. .70°С (разя., из спирта), выход 5,%.
Найдено,;; С 53,8; Н 6,1 ; С1 15,0; N 9,0; ЬгО (по Фишеру) 6,7.
т
C,}i2gВычислено,: С 53,9; Н 6,1; 15,1; N 9,0; 6,6.
СI Нейротропную активность и токсичность соединений формулы (I) опре25деляли в опытах на белых мышах весом Ifi-. г. Исследуемые вещества растворяли в твине-РП и вводили внутрибрюлинно. Эффекты регистрировали в разных сериях опытов спустя
30 мин после введения веществ.
Для характермсти1 1-1 нейротропной активности соединений использовали следующие методы; продолжительность тиопенталнатриевого наркоза тиопен35 тал-натрия 30 мг/кг внутривенно), температура тела (изменение более чем на 1°С), спонтанная двигательная активность способность вызывать миорелаксацию (по методу вращающегося стержня), предупреждать кора эоловые (коразол подкожно 110 мг/кг) судороги и фазу тонической экстен- i зии при электрошоке.
Токсичность определяли при внут45 рибрюшинном введении веществ белым мышам и наблюдении за ними в течение суток Эффект учитывали по числу погибших мышей в группе из трех
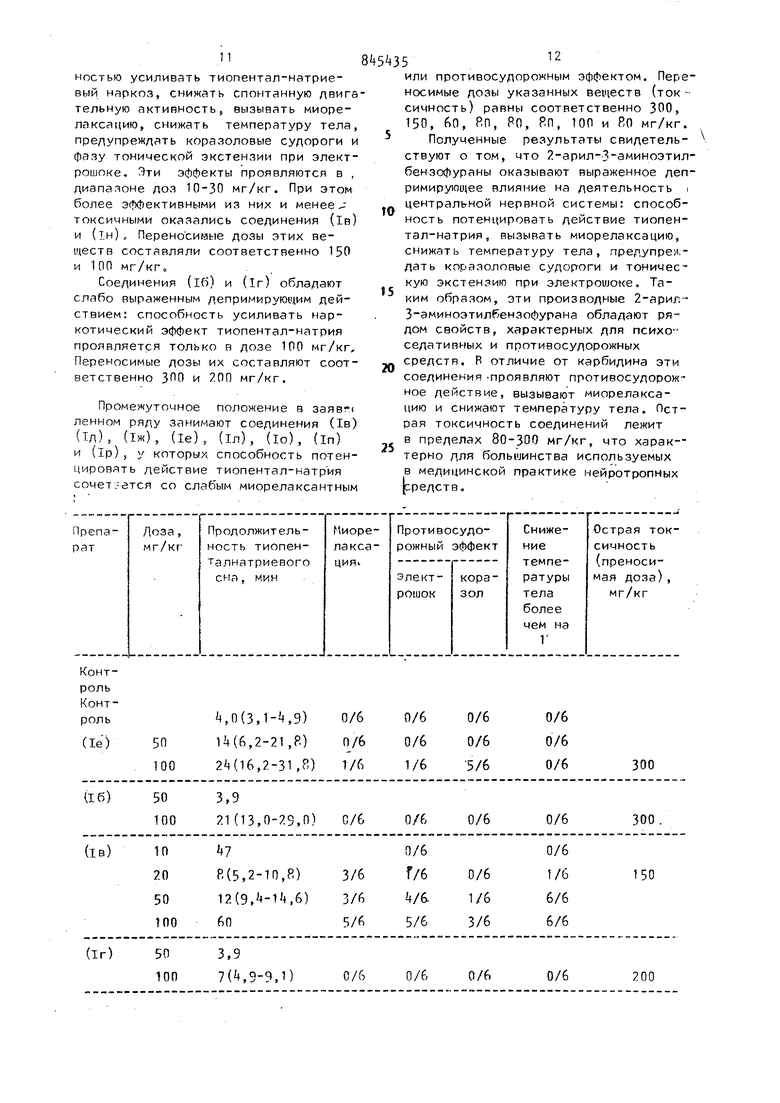
Результаты опытов представлены в 50 таблицеS из которой видно, что все соединения формулы () обладают центральным нейротропным действием депримирующего типа, отличаясь между con бой величиной эффекта и спектром фармакологической активности.
55
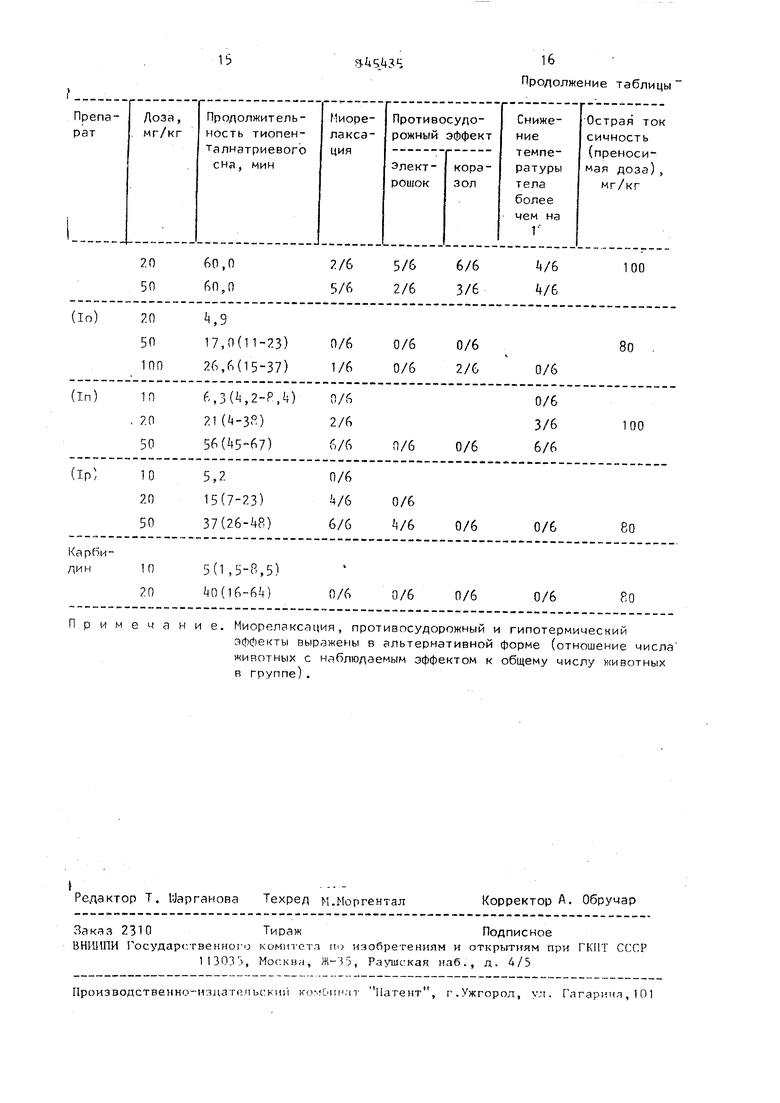
Волее широкий спектр фармакологической активности выявлек у веществ (IB)., (1з), (1и), (IK), (IM), (IH). Указанные соединения обладают способностью усиливать тиопентал-натриевый наркоз, снижать спонтанную лвига тельную активность, вызывать миорелакса1 ию, снижать температуру тела, предупреждать коразоловые судороги и фазу тонической экстензии при электрошоке. Эти эффекты проявляются в , диапазоне доз 10-30 мг/кг. При этом более эффективными из них и менее токсичными оказались соединения (1в) и (IH)е Переносимые дозы этих веществ составляли соответственно 150 и 100 мг/кг. Соединения (l6) и (1г) обладают слабо выраженным депримирующим действием: способность усиливать наркотический эффект тиопентал-натрия проявляется только в дозе 100 мг/кг, Переносимые дозы их составляют соответственно 300 и 200 мг/кг. Промежуточное положение в заяв-.( ленном ряду занимают соединения (1в) (Тд), (1ж), (1е), (1л), do), (In) и (IP)5 у которых способность потенцировать действие тиопентал-натрия сочет.-ется со слабым миорелаксантным 5 или противосудорожным эффектом. Переносимые дозы указанных вегцеств (токсичность) равны соответственно 300, 150, , Во, РО, RO, 100 и ЯО мг/кг. Полученные результаты свидетельствуют о том, что 2-арил--3 аминоэтилбензофураны оказывают выраженное депримирующее влияние на деятельность i центральной нервной системы: способность потенцировать действие тиопентал-натрия, вызывать миорелаксацию, снижать температуру тела, предупрея;дать коразоловые судор-оги и тоническую экстензию при электрошоке. Таким образом, эти производные 2-арил3-аминоэтил6ензофурана обладают рядом свойств, характерных для психеседативных и противосудорожных средств. Р отличие от карбидина эти соединения проявляют противосудорож ное действие, вызывают миорелаксацию и снижают температуру тела. Пстрая токсичность соединений лежит в пределах 80-300 мг/кг, что харак-терно для большинства используемых в медицинской практике нейротропных средств.
(in,) 50 5,00/6
100 37(19,0-55,0) 2/6
(le)
to 3,20 U1,P(11,.-1R,) S/6 0/6 0/6
50 6o,n3/6 0/6 0/6
20- k,l
50 16,7. (lil,,) 0/6
10,7
0/G
2012,7(Я,,2/6
3056(3, 0-7., 0) 5/6 6/6
5060,0
3,6n/6
10 20
11,2(6,8-15,6)1/6
,8(16,0-43,6)3/6
100
6n,n4/6
.nn 4,8n/60/60/6 15,0(9,3-20,7)3/61/60/6 29,5(15,1-43,9)5/63/61/6 40(20,5-59,5)6/64/63/6 6n,06/66/66/6
(тл) 10 4,9
2П 17,0(5,0-29,0) 0/6 0/6 0/6 50 42(21-63) 2/6 0/6 3/6 (IM) 107,3(,2-10,4)0/6 2034,0(23,0-45,0)1/6 3042,0(19,0-65,0)2/6 5060,06/6 (in 56,174,1-9,1)0 1012,8(3,1-16,5)1/6
0/6
0/6 1/6 0/6
150
80
0/6
0/6
0/6
0/6
1/6
2/6 it/6 4/6
50 6/6 6/6 6/6 h/6
4/6
0/6
250 0/6
6/6
50
0/6
80 4/6 2/6 0/6 3/6 3/6 6/6 0/6 0/6 3/6 1/6 0/6 3/6 2/6 1/6 80 6/6 6/6 0/6 0 0/6 2/0 1/6
13 Примечание.
16
g-iSt ;-:
Прололжение таблицы Миорелаксация, противосудорожный и гипотермический эффекты выражены в альтернативной форме (отношение числа животных с наблюдаемым эффектом к общему числу животных в группе).
| Машковский М.Д„ Лекарственные средства, М., Медицина, 1977, .1 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Контрольный стрелочный замок | 1920 |
|
SU71A1 |
Авторы
Даты
1992-04-23—Публикация
1980-03-05—Подача