Изобретение относится к новым замещенным адамантана, в частности к оксипроизводным ди-(адамантил)амина, которые проявляют антикаталептическую активность и поэтому могут быть использованы в фармакологических препаратах.
Известны различные замещенные оксиадамантанов, например 1-окси-4-N-дизамещенные адамантана, в которых заместителями по аминогруппе могут быть алкил, ацетил, циклогексил, бензоил или совместно с азотом представляют пиперидил, 2-пирролидонил, и эти соединения проявляют различную активность (сердечно-сосудистую, психотропную).
Известны также замещенные адамантана, проявляющие антикаталептическую активность, 2,2,6,6-тетраметил-1-оксил-4- пиперидилацетамидо-1'(или 2'-)адамантаны.
Целью изобретения является выявление новых оксипроизводных адамантана с антикаталептической активностью.
Поставленная цель достигается новыми оксипроизводными ди-(адамантил)амина формул I, II и III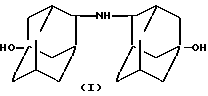

 проявляющими антикаталептическую активность.
проявляющими антикаталептическую активность.
Эти соединения получают известным путем, например взаимодействием хлоргидрата ди-(2-адамантил)амина со смесью азотной и серной кислот при температуре 0-30оС (соединение формулы I) или конденсацией 1-окси-4-адамантанона с 2- или 1-аминоадамантаном в присутствии муравьиной кислоты (соединения формул II и III).
П р и м е р 1. К смеси, содержащей 30 мл 98-100%-ной серной кислоты и 3 мл 65%-ной азотной кислоты, при перемешивании и температуре 0-15оС добавляют постепенно 3 г хлоргидрата ди-(2-адамантил)амина, перемешивают 3 ч при комнатной температуре и выливают реакционную массу на лед, после чего подщелачивают концентрированным раствором щелочи (NaOH) до щелочной реакции и экстрагируют хлороформом основание амина. Экстракт сушат над сульфатом магния, растворитель отгоняют и получают 2,3 г бис-(1-окси-4-адамантил)амина формулы I c выходом 75,4% т.пл. 240-245оС (сухой ацетон).
Найдено, C 75,28; H 9,63; N 4,66.
C20H31NO2.
Вычислено, C 75,65; H 9,84; N 4,42.
Основание растворяют в абсолютном этаноле, добавляют спирт, насыщенный хлористым водородом, и сухим эфиром высаживают хлоргидрат бис-(1-окси-4-адамантил)амина, т.пл. 292-298оС.
Найдено, Cl 9,82.
C20H31NO2 ˙ HCl.
Вычислено, Cl 10,02.
П р и м е р 2. Смесь 8,6 г 5-окси-4-адамантанона, 6,3 г мочевины и 7 мл 85% -ной муравьиной кислоты кипятят 5 ч при 130-140оС, добавляя в течение этого времени еще 2 мл муравьиной кислоты. Охлажденную массу подщелачивают раствором 8 г КОН в 8 мл воды, кипятят 4 ч, добавляют концентрированную соляную кислоту до кислой реакции, кипятят полчаса и экстрагируют эфиром исходный оксикетон (0,3 г). Водный слой насыщают бикарбонатом натрия и многократно экстрагируют хлороформом, экстракт сушат сульфатом магния, растворитель отгоняют и получают 5,5 г амина формулы I с выходом 70% т.пл. 240-245оС.
Найдено, C 75,77; H 9,72; N 4,61.
C20H31NO2.
Вычислено, C 75,66; H 9,84; N 4,42.
П р и м е р 3. Смесь 2,2 г 1-окси-4-адамантанона, 4 г 2-аминоадамантана и 2,6 мл 100% -ной НСООН кипятят 8 ч при 150оС, добавляют 10 мл 10% НСl, кипятят еще полчаса и экстрагируют толуолом исходный оксикетон. Водный слой насыщают бикарбонатом натрия, фильтруют, осадок промывают водой, сушат, растворяют в этиловом спирте, высаживают эфиром, отфильтровывают, сушат и получают 3 г основания амина формулы II с выходом 75% т.пл. 227-229оС.
Найдено, C 79,43; H 10,38.
C20H31NO.
Вычислено, C 79,68; H 10,36.
Солянокислая соль плавится при 316-318оС (хлороформ).
Найдено, Cl 10,57.
C20H31NO ˙ HCl.
Вычислено, Cl 10,49.
П р и м е р 4. Смесь 4 г 1-аминоадамантана, 4,4 г 1-окси-4-адамантанона и 4 мл 100% -ной НСООН кипятят 8 ч при 130-150оС, добавляют 20 мл 10%-ной НСl, кипятят еще полчаса и экстрагируют толуолом исходный оксикетон. Водный слой насыщают бикарбонатом натрия, осадок отфильтровывают, сушат и перекристаллизовывают из сухого ацетона. Выход амина формулы III 67,5% (5,4 г), т.пл.183-185оС.
Найдено, C 79,66; H 10,41.
C20H31NO.
Вычислено, C 79,68; H 10,36.
Фармакологическую активность определяли в опытах на крысах по способности соединений формул I, II и III предупреждать развитие каталепсии, вызванной галоперидолом. Исследуемые препараты вводили внутрибрюшинно в водном растворе или в эмульсии Твин-80 за 30 мин до введения нейролептика.
ЭД0,5, (в/бр) мг/кг: для соединения формулы I 4,74; II 6,46; III 15,14.
ЛД50 (по методу Литчфильда и Уилкоксона), мг/кг: для соединений I, II и III соответственно > 3000, > 3000, > 3000. Заяв- ляемые соединения имеют токсичность в 3 раза ниже, чем мидантан.
| название | год | авторы | номер документа |
|---|---|---|---|
| Замещенные N-адамантиланилины, проявляющие психостимулирующую и антикаталептическую активность | 1980 |
|
SU860446A1 |
| ЗАМЕЩЕННЫЕ N-АДАМАНТИЛАНИЛИНЫ, ПРОЯВЛЯЮЩИЕ ПСИХОСТИМУЛИРУЮЩУЮ И АНТИКАТАЛЕПТИЧЕСКУЮ АКТИВНОСТЬ | 1981 |
|
SU1018361A1 |
| Способ получения 1-окси-4-амино- или 4- -замещенных адамантана | 1977 |
|
SU740752A1 |
| Способ получения 2-( ациламино)-адамантанов | 1973 |
|
SU449582A1 |
| Хлоргидрат N-(2-адамантил)-N-фторанилина, обладающий иммуностимулирующей активностью и повышающий физическую работоспособность | 1979 |
|
SU782313A1 |
| Способ получения -(1-или 2-адамантил) пиперазина | 1970 |
|
SU326863A1 |
| Производные 1-оксиадамантана, проявляющие антикаталептическую активность | 1974 |
|
SU535085A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ГИДРОКСИАДАМАНТАН-4-ОНА (ЛЕКАРСТВЕННОЕ СРЕДСТВО "КЕМАНТАН") | 1994 |
|
RU2104994C1 |
| АМИНОПРОИЗВОДНЫЕ АДАМАНТАНА, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА | 2008 |
|
RU2401263C2 |
| Хлоргидраты N-адамантильных производных-1-(оксифенил)-2-аминоэтанола, обладающие местноанестезирующей и противоаритмической активностью | 1979 |
|
SU803349A1 |
Оксипроизводные ди-(адамантил)амина следующих формул:
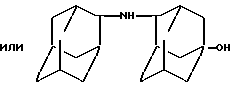
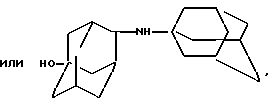
обладающие антикаталептической активностью.
| Лаврова Л.Н | |||
| и др | |||
| Некоторые аминоспирты ряда адамантана и их производные, ЖОрХ, т.XIi, вып.II, с.2369-2374, 1976. |
Авторы
Даты
1995-07-25—Публикация
1978-05-26—Подача