(5) СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА С-15003 Р-
1
Изобретение относится к микробиологии и касается производства антибиотиков.
Предложенный антибиотик новый и способ его получения в патентной и научно-технической литературе не описан.
Целью изобретения является получение антибиотика..
Эта цель достигается тем, что штамм
Nocardia sp.NC-15003 ( AJCC-31281, 3FO-13726) выращивают в питательной среде, содержащей источники углерода и азота, с добавлением лейцина или его производных.
Штамм Nocardia sp. NC-15003, продуцирующий антибиотик, был выделен из почвы и других образцов.
Штамм NC-15003 депонирован в исследовательском институте ферментации Agency of Industrial Science and Technol ogy (PERM) под номером 3992, в институте ферментации, Осака (JFO) под номером JFO 13726 и в американской коллекции разновидностей культур (АТСС), Мэриленд, США под номером 31281.
Культурально-морфологические признаки. Вегетативный мицелий растет 6 хорошо, гифы достигают 0,8-1,2 мкм, в диаметре, в некоторых случаях их можно разделить на фрагменты. Воздушный мицелий накладывается на вегетативный мицелий, часто образует
10 монолиты (50-200X200-1000 мкм), на которых продолжается дальнейший рост. Воздушный мицелий представляет собой волнообразные, прямые или петлеобразные спирали. Микроскопическое исследование старых культур показывает что лишь в нескольких случаях в цепях образуются конидии как клетки, тогда как клеточные суспензии, полученные с поверхностей таких культур
20 содержат много удлиненных эллипсоидальных (0,8-1,2 мкм X ,8-6,8 мкм) и эллипсоидальных (0,8-1,2 х.:1,02,0 мкм) телец, похожих на артроспорц
Сахарозо-нитратный агар : рост умеренный , цвет дыни до янтарнорыжевато-коричневого, образует тела похожие на монолиты. Воздушный мицелий скудный, белый. Растворимый hигмeнт отсутствует или бледный желтовато-рыжевато-коричневый, Глицерино-нитратный аГар : субстратный мицелий - рост умеренный, цвета слоновой кости, образует тела похожие на .монолиты. Воздушный мицелий умеренный, белого цвета. Раст зоримый пигмент отсутствует. Глюкозо-аспарагиновый агар : рос умеренный, цвета календулы до яркожелтого. Воздушный мицелий скудный, белого цвета. Растворимый пигмент ярко-желтый Глицериново-аспарагиновый агар : рост умеренный, цвета слоновой кости образует тела, похожие на монолиты. Воздушный мицелий скудный, белый. Растворимый пигмент отсутствует. Крахмальный агар : рост умеренный, цвета светлой слоновой кости до светло-пшеничного, образует тела похожие на монолиты. Воздушный мице ЛИЙ обильный; светлой слоновой кости. Растворимый пигмент отсутствует . Агзр на овсяной нуке : рост умеренный, цвета от светлой слоновой кости до колониального желтого, об разует тела, похожие на ГЮНолиты. Воздушный мицелий скудный, от белог до светло-желтого, Растворимый пигмент отсутствует, Тирозиновый агар : рост умеренный, от светлой слоновой до цвета светло-желтой дыни, образует тела, похожие на монолит. Воздушный мицелий умеренный, от белого до цве та светлой слоновой кости. Раствори мый пигмент цвета верблюда. Физиологические признаки. Температурный интервал роста 12-38 С. Температурный интервал, в котором наблюдается хороший воздушный рост, составляет 20-35 С. Желатин разжижа ет. Крахмал гидролизует. Нитраты восстанавливает. Молоко пептонизирует, но не коагулирует. Казеин рас щепляет. Меланоидные пигменты на агаре с пептоном и дрожжевым экстрактом не продуцирует, на тирозиновом агаре продуцирует. Тирозин разлагает, Ксантин и гипоксантин не ра лагает. Толерантность к.лиаоциму по ложительная. Толерантность к хлорис тому натрию - 2%. Очень хорошо растет на фруктозе, маннозе, хорошо растет на глюкозе, маннитоле, сахарозе, растворимом крахмале. Усваивает ксилозу, арабинозу, галактозу, рамнозу, трегалозу, раффинозу, мелибиозу, слабо усваивает мальтозу, глицерин, не усваивает i-инозитол, D-сорбитол, лактозу. Лейцин в качестве добавки можно применять в форме производного. Примерами производного являются алкильные сложные эфиры С -С, например, метиловый эфир, этиловый эфир лейцина, амиды, такие как амид С -С алкиламиды (например N-метиламид,Nэтиламид) лейцина, его кетокислоты (например L-кетоизокапроновая кислота) или их соли например гидрохлориды . Желательно с С-форма лейцина. Применимыми являются также свободная форма лейцина и его производные и смесь производных. Количество добавляемого к среде вещества составляет 0,0.1 - 1% вес/объем, предпочтительно 0,1-, 0,5. Время добавления любое на протяжении продуцирования антибиотика P-, предпочтительно добавлять в начале стадии культивирования. Среда для культивирования антибиотика может содержать источники углерода и азота, неорганические вещества, следы питательных веществ. В качестве источников углерода используют глюкозу, лактозу, сахарозу, мальтозу, декстин, крахмал, глицерин, маннитол, сорбитол, жиры и масла (например, масло из бобов,сои, свиное сало , куриный жир). В качестве источников азота используют мясной экстракт, дрожжевой экстракт, сухие дрожжи, соевую муку, жидкость от замоченного зерна, пептонмуку хлопковых семян, мелассу, мочевину, соли аммония (например сульфат аммония, хлорид аммония, нитрат аммония) и нитрат солей (например нитрат-натрия, нитрат калия). Среда также может содержать соли натрия, калия, кальция, магния-, соли железа, марганца; цинка, кобальта, никеля, соли фосфорной кислоты, борной кислоты. Среда может содержать в качестве добавок витамины (например В , Bg никотиновую кислоту, Вц,С, Е), нуклеи новые кислоты (например пурин, пирими, дин и их производные) .
Для установления нужного значения рН среды добавляют неорганические или органические кислоты, щелочи, буферные растворы. В качестве , антивспенивающих веществ добавляют подходящие количества масел, жиров, поверхностно-активных веществ.
Культивирование проводят в любых стационарных, со встряхиванием, аэробным погружением и других условиях для выращивания культур. Для получения высоких выходов предпочтительным является аэробное погружение культуры.
Инкубирование осуществляют при температуре 20-35 С при начальном рН 5.5-8,5, предпочтительным является интервал 23-30С и рН 6,5-7,5.
82tl 6
Время инкубирования может быть 8-240 ч.
Получают антибиотик следующим образом.
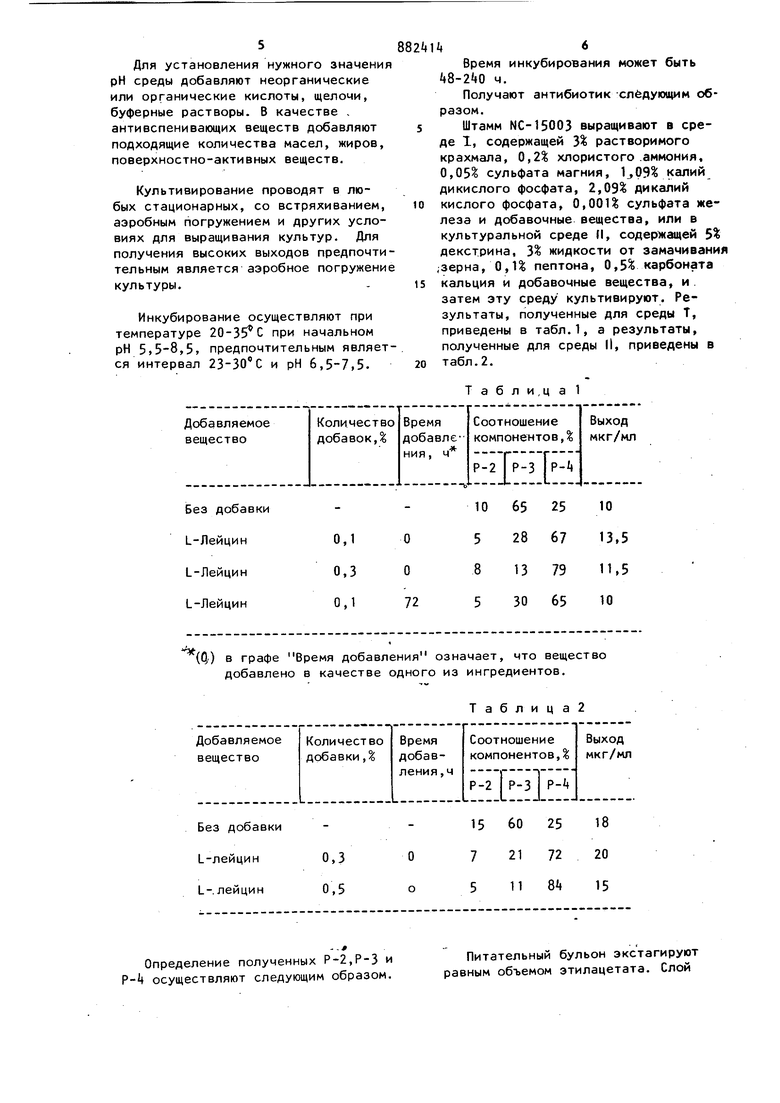
5 Штамм NC-15003 выращивают в среде 1, содержащей 3% растворимого крахмала, 0,2 хлористого .аммония, 0,05 сульфата магния, Ij09% калий дикислого фосфата, 2,09% дикалий 10 кислого фосфата, 0,001% сульфата железа и добавочные вещества, или в культуральной среде (I, содержащей 5% декстрина, 3% жидкости от замачивания .зерна, 0,1% пептона, 0,5% карбоната 15 кальция и добавочные вещества, и . затем эту среду культивируют. Результаты, полученные для среды Т, приведены в табл.1, а результаты, полученные для среды ||, приведены в табл.2.
20
Т а б л и,ц а 1






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения антибиотика @ -15003 @ -3 | 1978 |
|
SU1036251A3 |
| Способ получения антибиотика | 1977 |
|
SU741804A3 |
| Способ получения алкалоидов метанзинола, метанацина и пропионата метанзинола | 1977 |
|
SU938746A3 |
| Способ получения 2-кето-L-гулоновой кислоты | 1988 |
|
SU1788967A3 |
| Способ получения антибиотика @ -19393 @ и/или @ -19393 @ | 1980 |
|
SU1075984A3 |
| Способ получения антибиотика G-6302 | 1978 |
|
SU1003761A3 |
| Способ получения 2-кето-D-глюкаровой кислоты | 1986 |
|
SU1753949A3 |
| Способ получения производных 1-сульфо-2-оксоазетидинона или их солей, или сложных эфиров | 1983 |
|
SU1480763A3 |
| Способ получения бициклического соединения или его фармацевтически приемлемых солей | 1981 |
|
SU1271372A3 |
| Способ получения алкиловых эфиров сахароаскорбиновой кислоты | 1989 |
|
SU1729292A3 |

-че
(Q.) в графе Время добавления означает, что вещество добавлено в качестве одного из ингредиентов.
Определение полученных Р-2,Р-3 и Р-4 осуществляют следующим образом.
Таблица2
Питательный бульон экстагируют равным объемом этилацетата. Слой раствсэрителя концентрируют и сушат, затем растворяют этилацетатом для получения 1/100 объема исходного бульон Продукты определяют тонкослойной хром тографией на силикагеле, используя насыщенный водный раствор этилацетатом. Получаемое количество и соотношение компонентов определяют по величине поглощения на длинноволокновом ТСХ-многоточечном измерительном приборе модели С5-910 на основе интеграл-плотностей каждого пятна на хроматограмме при 25 мм. Отношение компонентов представлено в процентах вес/вес в общих продуктах, Р-2, Р-3, Р-. Как показано в табл. 1 и 2 штамм NC-15003 продуцирует антибиотик Р-А в количестве б5-8А% от общего количества в присутствии специфических добавок, и 25 или меньше в отсутствие таких добавок. Поэтому выделение Р- из питательного бульона является в первом случае более эффективным, чем во втором. Так как P-t, полученный таким способом в ферментационной жидкой среде, является липофильным нейтраль ным веществом, его обычно выделяют из питательного бульона в соответствии со способами выделения и очистки которые обычно используют для выделения таких микробных метаболитов, Р-А легко экстрагируется из питатель ного фильтра несмешивающимися с водой органическими растворителями, та кими как сложные эфиры жирных кислот например этилацетат и амилацетат, спирты, например бутанол, талоидированные углеводороды, например хлоро форм, кетрны, например метилизобутилкетон. Экстрагирование Р- проводят при рН, близком к нейтральному, и предпочтительно экстрагируют этил ацетатом, рН которого равен 7- Экст ракт промывают водой и концентрирую при пониженном давлении. Затем к ко центрату добавляют неполярный растворитель, например петролейный эфир или гексан, и выделяют в виде осадка т сырой продукт, содержащий акти ное соединение. Полученный сырой продукт подвергают при желании обыч ным способам очистки. Так, в качест 8 обычного способа очистки может быть использована адсорбционная хроматография. Для этой цели используют один из обычно применяемых адсорбентов, например силикагель, окись алюминия, «макропористые неионные смолы, ад-сорбенты и т.А,. Р- в сыром продукте отделяют на таком силикагельном хроматографе,например, с помощью петролейного эфира и гексана и . элюирование осуществляют, добавляя такой полярный растворитель, как этилацетат, ацетон, этанол или метанол, или галоидированНый водород, как дихлорметан или хлороформ с добавкой полярного растворителя, такого как спирт, например метанола или этанола, кетона, например, ацетона или метилэтилкетона, или тому подобных. Таким образом можно элюировать, выделить и получить P-t. Если в качестве средств очистки используют адсорбент как макропористую смолу, то элюирование проводят смесью воды с низшим спиртом, низшим кетоном или сложным эфиром. Например, низшим спиртом может быть метанол, этанол, пропанол или бутанол, низшим кетоном может быть, например ацетон метилэТилкетон, В качестве сложного эфира может быть этилацетат, бутилацетат. Сырой продукт (1 растворяют в 60 смеси метанол вода и адсорбируют на колонке Dialon НР-1. Колонку промывают 701 смесью метанол-вода. Затем осуществляют элюирование - смесью метанол-вода. Фракции, содержащие Р-4, собир ют и концентрируют при повышенном давлении. К сухому продукту добавляют 5-8 объемов этилацетата и полученную смесь оставляют выстаиваться, после чего выделяют кристаллы Р-. Выход антибиотика достигает около б5 или более, при этом легко выделяется из питательного бульона. Поэтому предлагаемый способ является преимущественным для промышленного получения Р-4. Физико-химические свойства Рприведены в табл.3.
Антибиотик
Формула
Точка плавления, °С
Удельное вращение
110
Idl
Элементарный анализ
Найдено, %
Элементарный анализ
Рассчитано,%
Ультрафиолетовый спектр поглощения НМ (6)
(в метаноле)
Инфракрасный спектр поглощения КВг, см
ЯМР-спектр частиц на млн, 100 МгГ в СД«з
Масс-спектр (т/е) Растворимость
Цветовая реакция
8821411 10
Таблица 3
С-15003 Р-
,196
177-180 Й2 i 10 с 0,522 CHClj)
С 60,65
Н 7,05
N 4,25
С 5,23
С 61 ,05
Н 6,99
N (4,32
о
С1 5,6
233 (29900) ( плечо ) 252(275590;
280(5712)288(5680)
,1730,1670,1580,
,1385,,1255,
ПВО,1150,1100,1080, 1038
1,03 (д) (6Н) 587,, А70, 450
Нерастворим в петролейном эфире, гексане, воде. Умеренно растворим в бензоле, эфире. Растворим в хлороформе, этилацетате, ацетоне, этаноле, метаноле, пиридине, тетрагидрофуране, диметилсульфоксиде
Драгендорф : положительная Бельштейн : положительная
Антибактериологичёская активность По способу бумажных дисков определяют ингибирующие концентрации штамм выращенного на триптикинозно-соевом агаре (BBL), против микроорганизмов, перечисленных далее. Так, диски фильтровальной бумаги, пропитаные каждый 0,02 (л раствора концентрации 300 мкг/мл , помещают на пластины, инокулированные соответственно микроорганизмами, перечисленными ниже, для определения минимальной ингибирующей концентрации. Полученные результаты показали, что антибиотики не обладают активностью против следующих микроорганизмов : Escherichla coli, Proteus vulgaris, Proteus mirabllis, Pseudomonas aeruginosa,Staphylococcu ureus, ВасП lus subtil is Bacillus cereus, Klebsiella pneumoniae, Serratia marcescens, Mycobacteriurn avium.
С другой стороны, на агаровых пластинках, содержащих испытываемую среду (3,5 г динатрийфосфата, 0,5 г монокалийфосфата, 5 г дрожжевого экстракта (Difco), 10 г глюкозы, 15 г агара, 1000 мл дистиллированной воды, рН ) было определено ингибирование роста Talaromyces avellaneus. В этом опыте минимальная ингибирующая концентрация составляет 1-1,5 мкг/мл для Р-. Далее культивируют в качестве исследуемого организма дикий штамм Tetrahymenpyrlformis w на опытной среде, состощей из 20 г протеоза-пептона (DIfco) 1 г дрожжевого экстракта, 2 г глюкоз 1000 мл дистиллированной воды и 10 мл 1 М фосфатного буфера рН 7,0 jпри в течение kk 48 ч и определяют методом последовательных разбавлений активность ингибирования роста антибиотиков против этого конкретного микроорганизма. Оказалось, что ингибирование роста наблюдается при концентрации 0,5 мкг/мл для С-15003 Р-.
P-k обладает активностью против следующих микроорганизмов : Faslcladium levieri, Helminthosporiu sigmoideum var, irregulare, Pyricularla oryzae, Cochlicborus miyabeanus, Sclerotinia sclerotiorum Pellicularia sasakii, Trichophyton . rubrum, Rhodotorula rubra и Cryptococcus neoformans.
Антиопухолевая активность. Было исследовано терапевтическое действие Р- вводимого внутрибрюшинно в течение 9 последовательных дней, против лейкемии Р388 у мышей (1x10 клеток/животное, трансплантированных внутрибрюшинно)). Результаты показали, что в единицах степени продления продолжительности жизни эти соединения обладают антиопухолевой активностью порядка 200 при уровне дозы 0,00625 мг/кг в день.
Токсичность. В тестовых испытаниях на острую токсичность, прове5денных на мышах в качестве подопытных животных, которые предусматривали внутрибрюшинные инъекции Р-Ц, все исследованные антибиотики продемонстрировали величину ЛД|оо 050,625 мг/кг и ЛДо 0,313 мг/кг.
Антибиотик P-k обладает высокой ингибирующей активностью против грибковых организмов и простейшых и поэтому представляет ценность в качестве фунгицидного агента или агента против простейших. Кроме того, так как P-k демонстрирует продлевающее продолжительность жизни действие у млекопитающих, у которых 0 есть опухоль (например мышей ) можно также ожидать, что это соединение сможет найти применение в качестве антиопухолевого лекарства.
Как фунгицид или агент против , простейших Р-4 можно использовать для оценки бактериальной экологии в почве, активном иле, жидкости животных организмов и т.д. Так, если нужно выделить ценные бактерии из обр зцов почвы или если нужно оценить
0 действие бактерий независимо от грибковых или простейших организмов при работе и исследовании активных илистых систем, используемых для очистки сточных вод,то можно использовать
5 антибиотик для получения селективного роста бактериальной флоры, сопровождающегося подавлением роста загрязняющих грибковых или простейших организмов в образце. В этом
0 случае образец добавляют к жидкой или твердой среде и на 1 мл среды добавляют 0,1 мл раствора 10100 мкг/мл антибиотика в смеси метанол-вода, после чего образец
5 инкубируют.
Р- можно также использовать в . качестве бактерицидного агента для борьбы с болезчями растений, вызванными микроорганизмами, упомянутыми выше. Как случай типичного применен Р- используют в виде 1 -ного метанольного водного раствора, содержа щего 0,5 мкг/мл - 5 мкг/мл антибиот Так, например, Р-4 можно использовать для контроля за красновато-коричневой листовой гнилью, бластом, гельминтоспориозной пятнистостью листьев и листовым заболеванием рисовых растений. Пример 1. АО мл засеянной культуральной среды (1,0% глюкозы, 2,0% бактотриптона, 1,2% бактодрожжевого экстракта, рН 7,0 ) вылив ют в колбу Эрленмейера объемом 200 мл. После стерилизации в среду 1.нкубируют Nocardia sp. С-15003 (JFO 13726 : АТСС 31281 : FERM 3992 Инокулянт инкубируют при 28°с во вращающемся шейкере (200 об/мин) для получения засеянной культуры. Эту засеянную культуру трижды промы вают стерилизованной дистиллированной водой и промывные клетки выделя ют до исходного количества стерилизованной дистиллированной водой. 1 мл полученного вещества инокул руют в основную культуральную среду растворимого крахмала, 0,2 хлористого аммония,0,05 сульфата магния, 0,09% монокалийфосфата, 2,09 дикалийфосфата 0,001% сульфата железа, 0,3% L-лейцина , и основную культуральную среду выдерживают при 28 8 дней во вращающемся шейкере (200 об/мин). Общее количество полученного С-15003 составляет 12 мкм/м и 80% его составляет .уР-. П р и м е р 2, Готовят тот же по культуры, что и в примере 1, и 500 мл засеянной культуры выливают в колбу Сакагуши объемом 2000 мл После стерилизации питательной сред среду инокулируют тем же штаммом, что и в примере 1. Инокулированную среду культивируют при А8 ч с вращательно-поступательным движением (110 ход/мин) до получения засеянной культуры. 100 л засеянной культуры ( 2,0% глюкозы, 3,0% растворимого крахмала, 1,0% жидкости замоченного зерна, 1,0% соевой муки, 0,5% полипептона, 0,3% хлористо натрия, 0,5% карбоната кальция, рН 7,0} готовят и выливают в 200литровый ферментер из нержавеющей стали. После того как ферментер стерилизуют при 12ГС 20 мин и охла Ц14 дают, в него инокулируют 500 мл засеянной культуры. Содержимое культивируют при 28 С 8 ч при скорости аэрации 100 л/мин, скорости перемешивания 200 об/мин. Питательный бульон (Юл) помещают в 100 литров питательной среды (5% декстрина, 3% жидкости от замачивания зерна, 0,1% пептона, 0,5 Lлейцина, 0,5% карбоната кальция, рН ) в 200-литровом ферментере из нержавеющей стали, ферментацию проводят k дня при при скорости аэрации 100 л/мин и скорости перемешивания 150 об/мин. Полное количество полученного C-1S003 составляет 12 мкг/мл, и Р-Ц С-15003 составляет около 85%(вес/ве4. ПримерЗ. К95л жидкой питательной среды, полученной в примере 2, добавляют 50 л ацетона. Полученную смесь перемешивают 30 мин. К полученной смеси добавляют 2 кг hyflo-supercell и полученную смесь хорошо перемешивают. Полученную смесь отфильтровывают на фильтре под давлением, в результате чего получают 13,5 л фильтрата. К полученному фильтрату добавляют 50 л воды и 90 л этилацетата, полученную смесь пере мешивают и экстрагируют. Процедуру повторяют дважды. Полученные слои этилацетата объединяют и дважды промывают 80-литровыми порциями воды. К слою добавляют 1 кг безводного сульфата натрия, высушивают и концентрируют до 200 мл. К полученному концентрату добавляют петролейный эфир, и образовавшийся осадок выделяют фильтрованием, в результате чего получают 35 г продукта. К полученному таким образом сырому продукту добавляют 50 мл этилацетата и полученную смесь перемешивают. Нерастворимую часть выделяют фильтрованием и к фильтрату добавляют 10 г силикагеля. После перемешивания полученной смеси этилацетат отгоняют при пониженном давлении. Остаток помещают в верхнюю часть колонки с силикагелем ( 500 мл). Злюирование . проводят последовательно 500 мл г-гексана, 500 мл смеси и - гексан: этилацетат (3:1) , 2000 мл смеси н-гексан: этилацетат (.1:1) и 2000 мл насыщенного водного раствора этилацетата. При этом элюат собирают в 50-миллилитровые фракции. По 1 мл от каждой фракции концентрируют досуха и к-полученному концентрату добавляют 0,1 мл этилацетата до получения смеси. Смесь дает пятно на расстояни 2,5 см от нижнего края пластины силикагель - стекло и проявляется окол 17 см растворителем (вода, насыщенная этилацетатом). После проявления проводят определение ультрафиолетовы излучением (2537 А). Активные фракци Rf 0,9 собирают и концентрируют при ПОНИ« АНОМ давлении мл. К этом добавляют 20 мл петролей ного эфира,я,|Ч| результате чего получают 1,0:8 кристаллов. Сырые кристаллы ращворяют в 20 мл теплого этилацетата. Ирсле охлаждения выделяют 920 мг. кристаллов Р-. Температура правления 178-18(3 С(Р-, 9 вес/вес). При-мер. В 400 мл 501 метан ла растворяют 20 г сырого продукта, полученного в примере 3. Колонку 2,5 см в диаметре набивают 1000 мл, диайона НР-10 и готовят 3000 мл смеси метанол-вода. Приготовленный таким образом раствор образца пропускают через колонку и промывают, используя 1000 мл 60%-ного метанола и последовательно проводят . градиентное элюирование 7500 мл смеси метанол-вода , 7500 мл смеси метанол - вода. Элюат собирают в 75 мл фракции и каждую фрак цию исследуют тонкослойной хроматогр фией на силикагеле, описанной в примере 3. фракции NN 182-190 собирают и кон центрируют. К полученному концентрату добавляют 500 мл воды и 1000 мл 16 этилацетата. Прлу. раствор встряхивают в разделительной воронке и водный слой отделяют, после двухкратного промывания 300 мл воды этилацетатный слой высушивают над безводным сульфатом натрия, концентрируют и оставляют выстаиваться. В результате получают кристаллы, которые собирают фильтрованием и высушивают. Получают 950 кг P-k. Температура плавления 177-179 С (Р-, 92 вес/вес). П р и м е р 5. Используя методику примера 1, но вместо L-лейцина применяя метиловый сложный эфир лейцина. N-метиламид лейцина, оС - кетой зокаггроновую кислоту или гидрохлорид лейцина, получают тот же результат, а именно получают специфически требуемый Р-. Предложенный способ позволяет получить новый антибиотик С-15003 Р- Формула изобретения Способ получения антибиотика С-15003 Р-4 отличающийся тем, что штамм Nocardia ар NC-15003 (АТСС-31281, JFO 13726) выращивают в питательной среде, содержащей источники углерода и азота с добавлением лейцина или его производных . Источники информации, принятые во внимание при экспертизе Предложенный антибиотик новый и способ его получения в патентной и научно-технической литературе не описан .
Авторы
Даты
1981-11-15—Публикация
1978-11-16—Подача