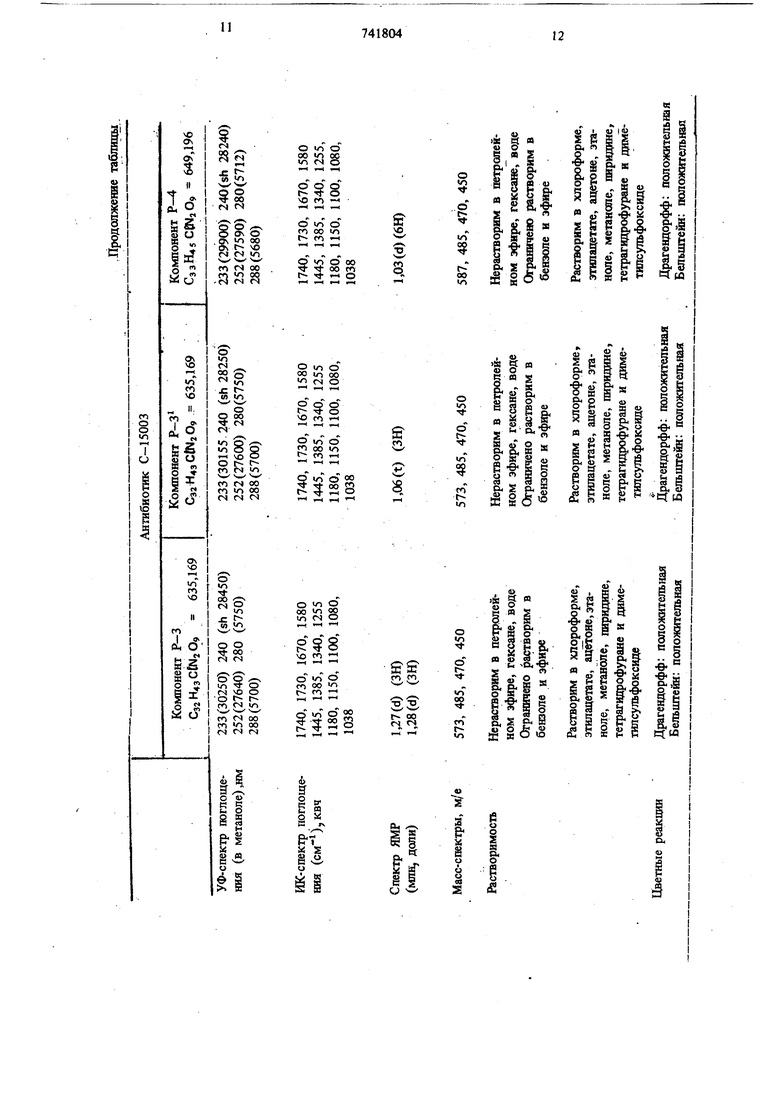
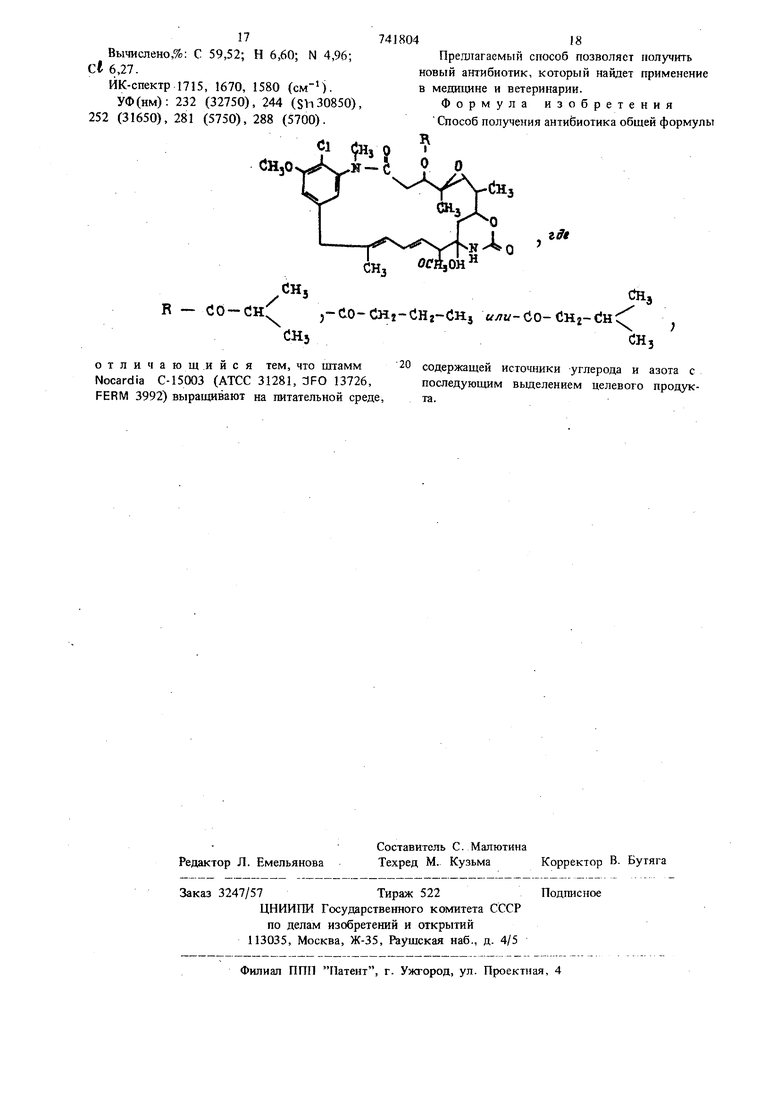
(54) СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА Изобретение относится к области микробиологии и касается получения нового антибиотика. Предложенный антибиотик новый и способ .,-CO-CH2-C R - СО-СН Эта цель достигается тем, что штамм No- cardia С-15003 (АТСС 31281; YFO 13726, PERM 3992) выращивают на питательной среде, содержащей источники углерода н азота, с последующим выделением целевого продукта. В качестве щтамма микроорганизма, производящего антибиотик используют щтамм Noего получения в патентной и научно-технической литературе не описан. Целью изобретения является получение антибиотика общей формулы Hj е/ли-Со-СНг-С Н cardia С-15003, который выделен из почвы. Штамм Nocardia С-15003 хранится в институте исследования ферментации в отдеяении промышленной науки и технологии (FER М) под номером 3992, в Институте ферментации, Осака ( 1FO) под номером 13726 и в Американской коллекции типовых культур (АТСС), Мэриленд, США под номером 31281. 37 Культурально- морфологические признаки Вегетативный мицелий развивается как на плотной, так и в жидкой питательной среде. Гифы имеют в диаметре 0,8-1,2 мм, часто образуются метелкоподобные тела (5-200 х X 200-1000 мм), на которых происходит дальнейший воздуигаый рост, в некоторых случаях они могут быть разделены на фрагменты. Штамм хорошо растет на различных токсономических средах, в. старых культурах в цепях встречаются конидальноподобные клетки. Суспензия клеток, полученных из поверхностей таких культур содержит удлиненные эллипсовдапьные (0,8-1,2 мм - 4,8-6,8 мм) и эллипсоидальные (0,8-1,2 X 1,0-2,0 мм) тела, подобные артроспорам, имеюшие гладкие поверхности. Штамм хорошо растет на различных питательных средах. Сахаро-нитратный агар. Рост умеренный. Субстратный мицелий жел тый до коричневого, образуются метелкоподобные тела. Воздушный мицелий скудный, белый. Растворимый пигмент отсутствует или светлый, желтовато-коричневый. Глицериново-нитратный агар. Рост умеренный. Субстратный мицелий цвета слоновой кости. Образуются метелкоподобные тела. Воздушный мицелий умеренный, белый. Растворимый пигмент отсутствует. Глюкозо-аспарагиновый агар. Рост умеренный. Субстратный мицелий от золотистого до ярко-желтого. Воздушный мице лий скудный, белый. Растворимый пигмент ярк желтого цвета. Глицерино-аспарагиновый агар. Рост умеренный .Субстратный мицелий цв та слоновой кости, образуются метелкопоДобные тела. Воздушный мицелий скудный, белый Растворимый пигмент отсутствует. Крахмальный агар. Рост умеренный. Субстратный мицелий цвета слоновой кости до желтого, образуются метелкоподобные тела. Воздушный мицелий скудный белый. Растворимый пигмент отсутствует. Агар с малатом кальция. Рост умеренный, субстратный мицелий цв та слоновой кости, образуются метелкоподобн тела. Воздушный мицелий умеренно белый, до цвета слоновой кости. Растворимый пигмент отсутствует. Агар с дрожжевым солодовым экстрактом. Рост умеренный. Субстратный мицелий ко .ричневатый до ярко-желтого, образуются мётел коподобные тела. Воздушный мицелий умеренный, белый, д цвета слоновой кости. Растворимый пигмент отсутствует. Овсяно-солодовый агар. Рост умеренный, субстратр1ый мицелий цвеа слоновой кости до желтого, образуются етелкоподобные тела. Воздушный мицелий скудый, белый,до светло-желтого. Растворимый игмент отсутствует. Пептонный агар с дрожжевым экстрактом и железом. Рост умеренный. Субстратный мицелий коониальный желтый. Воздуцшого мицелия нет, Растворимый пигмент колониальный, желтый. Тирозиновый агар. Рост умеренный. Субстратный мицелий цвета слоновой кости, образуются метелкоподобные тела. Воздушный мицелий умеренный, белый,до цвета слоновой кости. Растворимый пигмент коричневого цвета. Физико-биохимические признаки. Растет при температуре 12-38 С, хорошей рост воздушного мицелия наблюдается при 20-35 С. Желатину разжижает, Крахмал гидролизует. Нитраты восстанавливает. Молоко пептонизирует, но не коагулирует. Козеин разлагает. Меланоидные пигменты на пептонном агаре с экстрактом дрожжей и железом не производит, на тирозиновом агаре производит. Тирозин разлагает. Ксантин и гипоксантин не разлагает. Хорошо растет и усваивает О-ксилозу, D-rnsuкозу, маннозу, фруктозу, сахарозу, трегалозу, усваивает L-арабинозу, D-галактозу, L-рамнозу, мелибиозу, растворимый крахмал. Слабо растет на мальтозе, раффинозе, глицирине. Не усваивает лактозу, инозитол, D-сорбитол, Среда, применяемая для культивирования антибиотика может быть как плотной, так и жидкой, и содержать источники углерода и азота, которые штамм может ассимилировать и переваривать. Кроме того, среда Содер;.лт неорганические продукты и микроэлемент1. В качестве источников углерода используют глюкозу, лактозу, сахарозу, мальтозу, декстрин, крахмал, глицерин, мзннит, сорбит, жиры и масла (например соевое масло, свиное сало, куриный жир). Источником азота может быть, например, мясной экстракт, дрожжевой экстракт, сухие дрожжи, соевое молоко, жидкость от замачивания зерна, пептон, мука из хлопковых семян, истошенная меласса, мочевина, соли аммония, например сульфат аммония, хлорид аммония, нитрат аммония, ацетат аммония. Среда может также содержать соли натрия, калия, кальция, магния, железа, марганца, цинка, кобальта, никеля, соли фосфорной и борной кислот и соли органических кислот, такие как штетаты и пропионаты. Среда в качестве добавок может содержать различные аминокислоты, например глутаминовую и аспарагиновую кислоты,аланин,глицин, лизин, метионин, прелин), пептиды, витамины, например Bj, 82, никотиновую кислоту Bi2, С, Е), нуклеиновые кислоты (например пурин, пиримидин и их производные),Для установления рН среды туда добавляют неорганическую или органическую кислоту, щелочь, буфер. В качестве противовспенивающих агентов могут быть добавлены подходящие количества масел, жиров, поверхностно-активных веществ Культивирование проводят в любых условиях: стационарно, при встряхивании, погруженых, аэробных и др. Условия культивирования зависят от условий и состава среды, штамма, методик культивирования и других факторов; предпочтительно проводят инкубацию при 20-3 при первоначальном рН около 7,0. Предпочтительной является температура при первоначальном рН 6,5-7,5. Инкубацию продолжают до тех пор, пока со держание антибиотика не станет максимальным. Для культивирования при встряхивании или аэроб ного погружного культивирования в жидкой сред требуется 48-144 ч. Антибиотик накапливается в ферментационном бульоне как внеклеточно, так и внутриклеточно. Его определяют с помощью тонкослойной хроматографии. Ферментативный бульон разделяют на клетки и фильтрат с помощью фильтрования или цент рифугирования. Фильтрат экстрагируют таким же образом этилацетата. К клеткам прибавляют такое же количество 70%-ной смеси ацетонвода, как и фильтрата, а после одночасового перемешивания при 2(fC суспензию фильтруют. Из фильтрата удаляют ацетон и полученный водный раствор экстрагируют этилацетатом. Каждый из экстрактов концентрируют до 0,01 объема и подвергают тонкослойной хроматографии на стеклянной пластине с силикагелем. Система растворителей: хлороформ-метанол 9:1. Активность .определяют по интенсивности пятен, определяемой при облучении УФ-излучением при 2537 А. Антибиотик выделяют и очищают с помощью адсорбентов, таких как активированньш уголь, макропористые неионные смолы, силикагель, окись алюминия или экстракцией растворителем. Растворителями, пригодными для экстракции фильтрата, могут быть несмешивающиеся с водой органические растворители, такие как слож ные эфиры жирных кислот, например этилацетат и амилацетат, спирты, например бутанол, галоидированные углеводороды, например хлороформ, и кеитоны, например метилизобугалкетон. Экстракцию проводят при значении рН, близком к нейтральному, предпочтительно устанавлшаают рН культуральной жидкости, равным 7, и экстрагируют этилацетатом. Экстракт промьшают водой и концентрируют при пониженном давлении. Затем к концентрату прибавляют такой неполярный растворитель, как петролейный эфир или гексан, и собирают сьфой продукт,содержащий активное соединение. Очистку проводят адсорбционной хроматографией, предпочтительно используют силикагель. Проявление проводят, начиная с петролейного эфира и гексана, а элюирование антибиотика осуществляют при добавлении полярного растворителя, такого как этилацетат, ацетон, этанол или метанол. При использовании силикагеля (0,05 - 0,2 мм) в качестве носителя проводят хроматографию на колонке с серийным увеличением отношения гексана к зтилацетату. Отбирают образец элюата и исследуют с помощью тонкослойной хроматографии и фракции, содержащие антибиотик, объединяют и концентрируют при пониженном давлении. Затем к концентрату прибавляют петролейный эфир или гексая, в результате чего получают сырой продукт. Так как этот продукт содержит 1фимеси, продотгасают его очистку. Очищают его с помощью второй колонки с силикагелем, используя систему растворителей. Проявляющая система состоит из галоидированного углеводорода, такого как хлористый метилен или хлороформ, с добавкой полярного растворителя, такого как спирт, нащшмер метанол или этанол, кетона, как ацетон или метнлэтилкетон. Таким путем вьщеляют . Прт использовании макроскопической адсорбирующей смолы в качестве очищающего средства для сырся-о продукта, элюирование антибиотика осуществляют смесью воды с низшим спиртом, низщим кетовом или сложным, эфи: ром. Низшим спиртом может быть метанол, этднол, пропаноп нлн бутанол, а низишм кетоном может быть, например, ацетон или метилзтилкетон. Сложным эфиром - этилацетат.Сырой продукт растворяют в 60%-ной омеси метанол - вода и адсорбируют на колонке,Дайон нР-10. Колонку цромывают 70%-ной смесью метанол - вода, а затем проводят элюирование 90%-ной смесью метанол - вода. Таким путем антибиотик элюируют из колонки. Фракции, содержащие антибиотик, объединяют и к(нщ«1трируют 1ФИ пониженном давлении. К сухому продукту добавляют 5-8 объемов этилацетата и смесь оставляют стоять до отделения кристаллов антибиотика. Эти кристаллы антибиотика содержат шосолько активных компонентов С 15003, Р-3 н Р. Их затем отделяют друг от Щ)уга с помощью адсорбента. Используя оншосагель или макропористую неиониую адсор&фующую смолу и растворители,-можно элюнровать необходимый компонент. Напри1мер, при использовании силикагеля проявление тфоводят гексаном, этилацетатом или хлороформом-метанолом, в результате чего активные компоненты С 15003, Р-4, Р-З и Р-3, выделяют в таком порядке. После определения тонкослойной хроматографией фракции, соответствующие С-15003, Р-4, Р-3 и Р-3 соответственпо кшцентрируют при пониженном давлении и к концентратам прибавляют этилацетат. Активные компоненты могут быть получены в виде кристаллов. При использовании макропористой неионной адсорбирующей смолы Может быть применен градиент элюирования с изменением соотношения спирта, кетона или сложного зфира и воды. Например, с помощью метода градиента элюирования, включающего использование 60%гной смеси метанол-вода и 95%-ной смеси метанолвода с добавкой 5% хлористого натрия, Р-3, Р-3 и Р-4 поглощаются в указанном порядке. После отбора образцов и определения с помощью тонкослойной хроматографии каждую группу активных фракций концетрирую при пониженном давлении и кристаллизуют из этилацетата. Выделенные кристаллы содержат этилацетат как кристаллизационный растворитель и после сушки над пятиокисью фосфора при 70° С в течение 8 ч показывают физические и icимичecкиe свойства, данные которых приведены в таблице.
о lO 00 «о V-1 СЧ
§8
чо fo -
о 10 о ел ОО 1Л Г ел --н
о П о оо
00 го
( ч- -I о
о ю о
ОО ю ОО in (SI о
о
о о о
ю л
о 1л о гп оо «о f fi -1
g 1л С)
S528
1Л
t
с оо
1Л
о
О
5:
i л
о in о
йй§
,-, 1Г-« --1
ЧО f - - г-Ч -I
сГ О С5
rf) 00 С fO
С 00
С5 Л о i
.-ч - -о
о t
го гe{«v







6
g
I 5
§ 1
&t
l§
4
1г
i
a.
u
&
s .iii .и1гиГ)И(Г1нк обладает актнвностыо им(нбщюпиния роста против микроорганизмов, Koiopi.io вызывают болезни растений. Антибиотик и его компоненты обладают противоопухолевой активностью 200. при 0,00625 мг/кг/день. В испытании на острую токсичносгь на мыш при внутрибрюшинном введении LDjo составляет 0313 мг/кг. Антибиотик обладает сильной ингибирующей активностью против грибков и простейхиих и является ценным для борьбы с грибками и про тейшими. Антибиотик может быть использован для лечения болезней растений, вызванных микроорганизмами. Пример 1 . Штамм Nocardia С-15003 (QFO 13726, FERM 3992, АТСС 31281) , выращенный на среде (агар с дрожжевым и солодовым экстрактом), используют для инокулирования ферментера емкостью 200 обл., содержащег 40 об.ч. засеваемой культуральной среды (2% глюкозы, 3% растворимогр крахмала, 1% сырой соевой муки, 1% жидкости от замачивания зерна, 0,5% попипептона, 0,3% NaCI, 0,5% СаСОз, рН 7,0). Инокулированную среду инкубируют при 28С в течение 48 ч для получения посевно культуры. 0,5 об. ч. полученной посевной культуры переносят в ферментер, содержащей 40 об ферментационной среды, состоящей из 5% декетрина, 3% жидкости от замачивания семян куку рузы, 0,1% полипептона и 0,5% СаСОз, рН 7,0; культивируют при 28°С в течение 90 ч, получая инокулят (посевную культуру). Посевная культура имеет титр 25 мг/мл. Пример 2. Порцию из 10 об. ч. посевной культуры, полученной в примере 1, переносят в ферментер емкостью 2000 об. ч., содержащий 500 об. ч. посевной культуральной среды И инкубируют при 28 с в течение 48 ч. Перекосят 500 об. ч. полученной культуры в танк из нержавеющей стали емкостью 50000 об. ч., содержащий 30000 об. ч. посевной культуральной среды и культивируют при 28° С в условиях аэрации для получения посевной культуры. Эту культуру используют для посева в танк емкость 200000 об. ч., содержащий 100000 об.ч. ферментационной среды, подобной той, что использовали в примере 1, при степени инокулирования 10%. Засеянную среду инкубируют при 28° С в условиях аэрации. Полученная культура имеет титр 25 мг/мл. Пример 3. К 95000 об. ч. культуры, полученной в примере 2, добавляют 2000 г Гифлосуперселя и после тщательного перемешивания смесь фильтруют. Затем фильтрат экстрагируют 30000 об. ч. этилацетата. Эту процедуру повторяют снова. Объединяют этилацетатные слои, дважды промывают 30000 об.ч. воды. при HOpOMeniHHaFnui с 5l)f) об. ч. белюлного сульфата натрия н кониеигрн 1уют при 1гониженном давлении до объема 20() об.ч. К концентрату прибавляют петролсйиьгй эфир и отфильтровывают нерастворимые продукты; фильтрат переменшвают с 10 об. ч. силикагеля и отгоняют этилацетат при пониженном давлении. Остаток помещают в верхнюю часть колонки с силикагелем (400 об. ч.)- Элюйрование осуществляют с помощью 500 об. ч. гексана, 500 об. ч. смеси гексан-этнлацетат (3:1), 500 об. ч. смеси гексан-этилацетат (1:1), 500 об. ч. смеси гексан-этилацетат (1:3), 500 об. ч. зтиладетата и 1000 об. ч. смеси этилацетата с метанолом (50:1), собирая. элюат фракциями по 100 об. ч. Одну часть каждой фракции концентрируют досуха и к концентрату добавляют 0,1 об. ч. этилацетата, получая смесь. Смесь наносят в виде пятна на расстоянии 2,5 см от нижнего края стеклянной пластины с силикагелем и проявляют примерно 17 см в системе растворителей этилацетат-метанол (19:1). После проявления проводят определение в ультрафиолетовом свете. Объединяют активные фракции № 23-№ 28 с Rf 0,6-0,65 и концентрируют их при пониженном давлении примерно до 20 об. ч. К этому концентрату прибавляют 150 об. ч. петролеиного эфира для по.пучения 15 об. ч. продукта. Пример 4. Экстрагируют при перемешивании 32000 об. ч.влажных клеток, прлученных в примере 3, 50000 об. ч. 70%-ного раствора ацетона в воде. Затем фильтруют на фильтре, работающем под давлением. Снова повторяют экстракцию и фильтрование. Объединяют фильтраты и отгоняют ацетон при пониженном давлении. Приученную водную систему пропускают через колонку с 5000 об. ч. Дайона нР -10. Колонку промывают водой и 50%-ным водным метанолом, после чего элюируют 15000 об. ч. 90%-ного метанола в воде. Элюат концентрируют при пониженном давлении до 3000 об. ч. и встряхивают с таким же количеством воды и этилацетата, вновь повторяют процедуру. Объединяют этилацетатные соли, промывают водой, сущат при добавлении безводного сульфата натрия и концентрируют при пониженном добавлении до 200 об. ч. После прибавления петролейного эфира отфильтровывают осадок. Полученный продукт очищают на колонке с силнкагелем, собирая 8,0 об. ч. сырого продукта. Пример 5. В 10 об. ч. этилацетата растворяют 1,5 об. ч. сырого продукта, полученного в примере 3, и хорощо перемещивают раствор с 4 об. ч. сштакагеля. Отгоняют этипацетат при пониженном давлении. Остаток наносят на верхнюю часть колонки с 300 об. ч. силикагеля и колонку промывают сначала 500 об. ч. хлороформа, а затем элюнруют 500 об. ч. смеси хлореформ-метанол (50:1), 500 г смеси хлороформ-метанол (20:1) и 500 г смеси хлороформ метанол (10:1). Элюат собирают.фракциями по 25 об. ч. Кот1ентрируют при пониженном давлении 0,5 об. ч. каждой фракции. К концентрату прибавляют 0,05 об. ч. этилацетата и смесь используют как образец щш тонкослойной хроматографии на силикагеле (проявляющая система :хлороформ-метанол 9:1). Фракции № 39 и 40 при 2537А в зоне Rf 0,50-0,60 собирают и концентрируют при пониженном давлении. К остатку прибавляют 2 об. ч. этилацетата и оставляют смесь стоять, в результате чего получают 0,150 об. ч. кристаллов антибиотика. Растворяют кристаллы антибиотика в. 15 об. метанола, затем прибавляют 0,300 г хлористого натрия и 15 об. ч. воды. Набивают колонку 200 об. ч. Дайона рН-10 и калибруют 600 об.ч. 50%-ного раствора метанола в воде, содержащего 50% хлористого натрия. Образец приготовленного выще раствора пропускают через колон ку и проводят элюирование, используя 1500 об. ч. 60%-ного метанола в воде, содержа щего 5% хлористого натрия и 1500 об. ч. 95% ного метанола в воде. Элюат собирают фракциями по 15 об. ч. и каждую фракцию исследуют с помощью тонкослойной хроматографии на силикагеле. Фракция 145-153 содержат компоненты С-15003 Р-3, фракции 167-180 содержат С-15003 Р-3 и Р-4, а фракции 185-190 содержат С-15003 Р-4. Каждую группу фракций концентрируют и растворяют, добавляя 50 об. ч. воды и 100 об. ч. зтилацетата. Раствор встряхивают в делительной воронке и отделяют водный слой. После промывки дважды 50 об. ч. воды этилацетатный слой сушат над безводным сульфатом натрия, концентрируют и оставляют стоять По описанной выше методике получают кристал лы из каждой группы фракций. Кристаллы собирают фильтрованием, сушат и получают, об. ч.: С-15003 Р-40,070 С-15003 Р-З, Р-40,018 С-15003 Р-4 Смесь кристаллов С-15003 Р-З и Р-4 (0,018 ч растворяют в 03 об.ч. этилацетата, наносят в виде пятна на линию на расстоянии 2,5 см о нижнего края стеклянной пластинки с силикагелем, затем проявляют смесью этилацетата с метанолом (19:1). После проявления примерно 18 см выскабливают полосу абсорбции при Rf 0,68 (Р-4) и Rf 0,65 (Р-/), каждую независимо экстрагируют этилацетатом, содержащим незначительное количество воды. Полученный зтилацетатный экстракт промывают водой, сушат над безводным сульфатом натрия, концентрируют при пониженном давлении и оставляют стоять. Получают 0,010 об. ч. кристаллов С-15003 Р-4 и 0,003 об. ч. кристаллов С-15003 Р-З из фракции Rf 0,68 и Rf 0,б5 соответственно. Пример 6. Инокулируют 1000 об. ч. культуры примера 2 в танк из нержавеющей стали, содержащий 100000 об. ч. посевной культуральной среды; засеянную среду инкубируют при 28°С в условиях аэрации и перемешивают в течение 48 ч. Затем получе1шую культуру переносят в танк емкостью 2000000 об. ч., содержащий 1000000 об. ч. ферментационной среды, подобной той, которая была использована в примере 1. Культивирование проводят при 28° С в условиях аэрации и перемешившши при внутреннем давлении 1 кг/см в течение 90 ч. Полученная культура имеет титр 20 мг/мл. К 90000 об. ч. полученной культуры добавляют 900000 об. ч. ацетона и после перемешивания в течение 1 ч прибавляют 20000 об. ч. Гифлосуперселя. Смесь затем перемешивают и фильтруют на фильтре, работающем под давлением. К 1700000 об. ч. полученного фильтрата прибавляют 500000 об. ч. воды и смесь экстрагируют 1000000 об. ч. этилацетата. Этилацетатный слой промывают водой, сушат, прибавляя безводный сульфат натрия и концентрируют при пониженном давлений . К концентрату добавляют птеролейный эфир и собирают полученный осадок фильтрованием к. сушат. Собирают 65 об. ч. сырого продукта. После этого сырой продукт очищают и получают 9,5 об. ч. С-15003 Р-3, 0300 об.ч. С-15003 Р-Зк 2,5 об.ч. С-15003 Р-4. Пример 7. Растворяют в 1 об.ч. тетрагидрофурана 0,015 об. ч. кристаллов антибиотика С-15003, полученных в примере 5, после чего охлаждают раствор до 5° С и прибавляют 0,012 г литийалюминийгидрида. Смесь оставляют стоять на 2 ч. Затем прибавляют 0,5 об. ч. 1%:ного водного раствора серной кислсть, реакционную смесь экстрагируют 2 об, ч. этилацетата. Этилацетатный слой промывают водой, сугиат, добав:гюя безводный сульфат натрия и концентрируют при пониженном давлении. Проводат тонкослойную хроматографию на силикагеле с концентратом, выскабливают зону с Rf 0,25 0,3 и экстрагируют этилацетатом с незначительным количеством воды. Экстракт промывают водой, сушат над безводным сульфатом и концентрируют при пониженном давлении, после чего отделяют кристаллы. Кристаллы отфильтровывают и сушат. Получают 0,010 об.ч. С-15003, плавящегося при 174°С. Элементарный анализ: Найдено,%: С 59,65; Н 6,58; N 5,02; СС 6,51;. CjeHsvCINjOg
17
Вычислено,%: С 59,52; Н 6,60; N 4,96; С1 6,27.
ЙК-спектр 1715. 1670, 1580 (см ).
УФ(нм): 232 (32750), 244 (S1i 30850), 252 (31650), 281 (5750), 288 (5700).
R - СО-СН
j-do-CHi-CHz-CH, t 7i/-Со-Снг-dH
(JHj отличающ.ийся тем, что штамм20 Nocardia С-15003 (АТСС 31281, 3FO 13726, FERM 3992) выращивают на питательной среде,
74180418
Предлагаемый способ позволяет получить новый антибиотик, который найдет применение в медивдне и ветеринарии.
Формула изобретения Способ получения антибиотика общей формулы
zfft
СН,
СНз содержащей источники углерода и азота с последующим выделением целевого продукга.
Авторы
Даты
1980-06-15—Публикация
1977-10-07—Подача