(54) СПОСОБ 1ЮЛУЧЕНИЯ АНТИБИОТИЧЕСКОГО Изобретение относится к микробиологической промьшшенности и касается получения антибиотиков. Предлагаемый антибиотический комп леке новый и способ его получения в научно-технической и патентной литературе не описан. Цель изобретения - получение антибиотического комплекса. Поставленная цель достигается тем что штамм Streptomyces 1елеЬгаг1и5 АТСС 17920 культивируют в глубинных условиях аэробно в питательной среде содержащей источники углерода, азо та и минеральные соли при температуре 37-43°С в течение 4-7 дней, затем В14целяют целевой продукт в свободном виде или в виде его солей и при необ ходимости разделяют комплекс на соетавные антибио- ические компоненты О W, Ч и С и переводят их в соли. Новый антибиотический комплекс ха рактеризуется наличием секи компонен тов, из которых каждый отличается активностью, свойственной антибиотику.. Этот комплекс, в качестве свободного основания растворим в воде и диметилсульфоксиде, слабо растворим в метаноле и нерастворим в большинКОМПЛЕКСАстае других органических растворителей, таких как ацетон, высшие спирты, дИоксан, зтилацетат, дизтиловый эфир/ ацетонитрил, метил-изобутил кетон и растворители, относящиеся к классу углеводородов. Свободное основание комплекса ycf тойчиво при пониженных температурах и температуре 37°С. Антибиотический комплекс тенебримицин содержит семь различных фак торов (компонентов : тенебримйцин Г , тенебримицнн Т; тенебримиции il , тенебримйцин UJ , тенебримйцин (V , тенебримйцин н тенебримйцин-Ё.. В комплексе, получаемом Нри обычных условиях, тенебримйцин I тенебршлицин и тенебримйцин ill присутствуют в незначительных количествах, Тенебримйцин Г входит в состав в количестве 45-50% и тенебримйцин J содержится в комплексе а количестве около 30%, тенебримщии (у присутствует в количестве около 15-20%, атенебримйцин 7) около 10%. Тенебримйцин Т| является белым твердым ве.|цествЬм. Электрометрическое титрование в водной покаэывает наличие способных титроваться группировок, имеющих значения рН около 5,7 6,7 7,7 и8,7. Удельное вращение, определяемое в свете линии D натрия при 25С, обусловленное данным фактором, равна +159°, если концентрация антибиотика равна 1%, считая на весовое количество приходящееся на единицу объема в водном растворе.. Данные микроорганизма свидетельствук1Т о том, что тенебримицин имеет приблизительно следующий процентный состав: С 46,47; Н 7,99; N 13,05 О 32,29. Молекулярный вес, по результатам титрования, составляет около 539. Эмпирическая формула .
Инфракрасный спектр поглощения тенебримицина JT в среде, содержащей минеральное масло, показывает следующие различимые полосы в составе спектров инфракрасного поглощения в пределах от 2 до 15 мк: 3,02 3,14, 60,5 J 6,23; 7,4) 8,5; е,75 9,17, 9,65; 10,11; 11,15; 11,7 12,6 мк.
Тенебримицин 1 образует ацетильное производное, имеющее удельное вращение cl D около-1-130° при концентрации соединения 1%, считая на весовое .количество, приходящееся на единицу .объема в водном растворе. У производного не имеется оставшихся группировок, способных титроваться. Элемен.тарный состав, определенный по методу микроорганизма, показывает, что к структуре тенебромицина 1 присоединяются четыре ацетильные группировки. Тенебримицин W является основнкям веществом, содержеицим группировки, способные титроваться, имеющим значения показателя рК. а около 5,3 6,8; 7,8 и 9,0, судя по данным электрометрического титрования, в воде, Удельное вращение тенебримицина у , определенное в 1%-ном водном растворе при 25°С, равно +114° Процентный состав тенебримицина iV по данным микроанализа; С 41,91;Н 7,53, . N 15,16 Молекулярный вес, определенный по данным титрования - около 544. Эдтирическая формула для тенебримицина iy
6°
Инфракрасный спектр поглощения тенебримицина N -в среде минерального масла показывает различные полосы поглощени я в рределах 2-15 мк составляют: 3,05. 3,17; 5,85; 6,27; 7,46 8,75; 9,7; 10;5; 11-,1 и 12,85 мк.
Тетра-ацетильное производное тенебримицина 5 является твердым, кристаллическим веществом с точкой плавления около 265-267 С. Удельное вращение в том случае, если концентрация производного равна 1% в водном растворе.
Электрометрическое титрование тенебримицина 2 свидетельствует о наличии способных титроваться группировок, имеющих значение рка около 5,5
7,0; 8,0 и 9,1. Удельное вращение в свете D линии натрия в однопроцентном водном растворе данного фактора определяемое при 25с, +118°. Элементарные составы, определенные по мето Ду микроорганизма, таковы: С 43,21; Н 7,86; N 13,69. Молекулярный вес равен 483. Эмпирическая формула для тенебримицина V CjgHjYN j-O-Q. НлО.
Спектр инфракрасного поглощения .тенебримицина в среде, содержащей минеральное масло, имеет следующие различные полосы в пределах 2-15 мк, 3,05; 3,19; 6,32; 7,45 8,75; 9,7; 11,35 и 12,25.мк.
Подобно тенебримицину , тенебримицин ( образует кристаллическое тетра-ацетильное производное. Производное плавится с разложением при температуре около и характеризуется удельным вращением d) около +190°, при концентрации 0,42% в водном растворе.
Тенебримицин имеет способные титроваться группировки, характеризуемые значениями рКа около 5,6; 7,,2 и 9,3, определенными в водном растворе путем электрометрического титрования. Молекулярный вес 467. Удельное вращение в свете D линии в однопроцентном водном растворе тенебримицина Y1 при температуре 25°С равно, примерно +127. Микроанализы свидетельствуют о приблизительном процентном составе: С 44,3; Н 8,1 N 14,3 32,8. Эмпирическая формула C a j-yNyOg .
Спектр инфракрасного поглощения тенебримицина VI показывает различные полосы поглсяцения в пределах 2-15 мк; 3,05; 3,19; 6,35; 7,47; 8,75, 9,8; 12,3 и 12,95 мк.
Показатель удельного вращения тетра-ацетил производного тенебримицина Vj в 1%-ном водном растворе составляет около+95° при определении пр 25С.
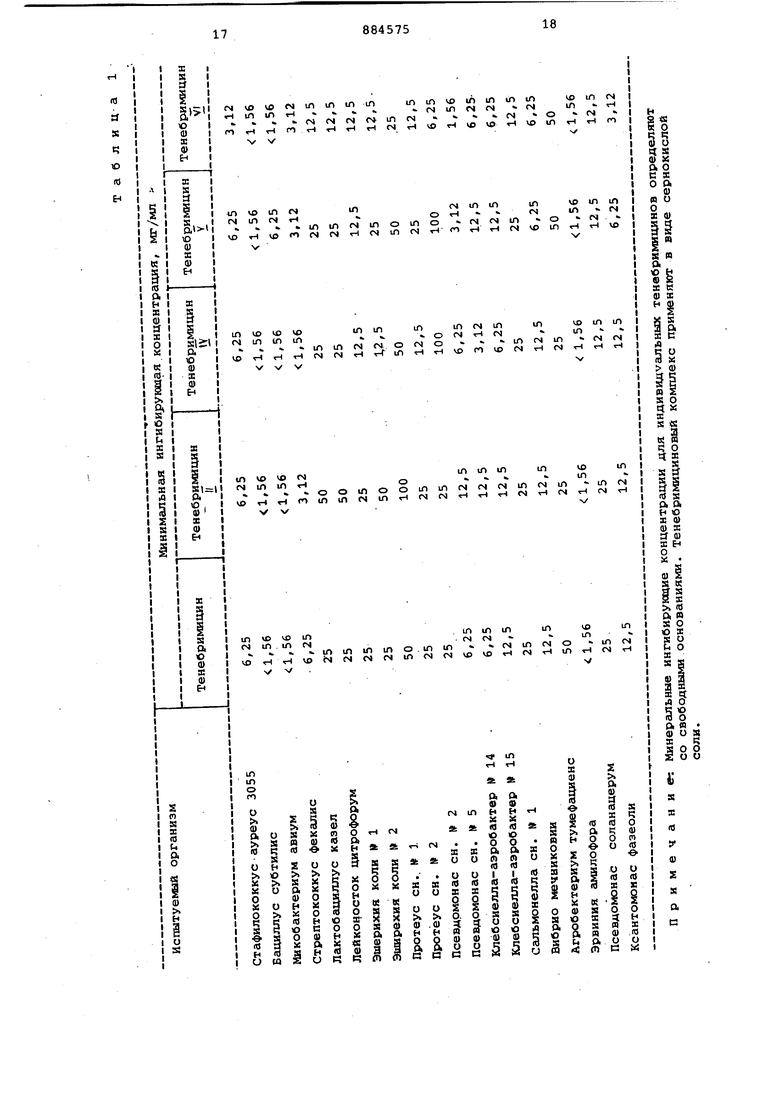
Соли, являющиеся продуктами присоединения кислот к тенебримицину ил отдельным компонентам, входящим в состав антибиотика, можно получить с помощью обычных методов. Для образования соли применяют или органические или неорганические кислоты. Удобный метод получения таких солей заключается в добавлении раствора, кислоты, служащей для образования соли к водному раствору антибиотика. В случае нерастворимых солей, являющихся продуктами присоединения кислоты, соль осаждается из раствора и легко отделяется с помощью обычных те снических приемов, таких как фильтрование или центрифугирование. В том случае, когда желаемая соль, являющаяся продуктом присоединения кислоты, быстро не осаждается, то процессу осаждения можно способствовать ил концешгрируя раствор до меньшего объема или добавляя к воде смешиваю щийся с ней растворитель, такой как ацетон или подобный ему. Соль, являкядаяся продуктом присоединения кислоты, можно перевести в форму св бодного основания путем пропускания водного раствора соли над анионообменной смолой в гидроксильном цикле Различные факторы, образующие те небримициновый комплекс можно отлич |0дин от другого,а также от других анти биотиков, обладающих сходными свойс вами с помощью технических приемов мажной хроматографии. Хроматографию Проводят по обычному нисходящему методу при температуре 22,8tO,. С 73Ф+1Ф; , на бумаге фирмы Ватман № 1, имеющей размеры 19,,3 см. Антибиотический комплекс тенебри мицина, а также индивидуальные, образующие упомянутый комплекс, обладают ингибирующим действием по отношению к росту микроорганизмов, патогенных для жизнедеятельности жи вотных и растений. Концентрация ком плекса и индивидуальных тенебримицинов, при которых проявляется тормозящее действие в части развития ряда организмов, показано в табл.1. Минимальные ингибирующие концентрации определяют по методу разбавлени агара. Острая токсичность тенебримицион ного комплекса и сравнительно менее распространенных его составных частей определяют на мышах. Значения доз вызывающих гибель подопытных животных в 50% случаев для тенебримидинсульфата, составляют около 300 мг/кг для случая внутреннего введения, и около 350 мг/кг при введении в брюшную полость. Все мыши выживают в случае дозировок при под кожном введении в количестве 750 мг/кг или при скармливании 5600 мг/кг. Не отмечается значительного раздражения при внесении в один глаз каждой из четырех крыс одной капли 50%-нрго водного раствора суль фата тенебримицина по три разав день в течение 5 дней. Получгшзт следующие значения 1050 выраженные в мг/кг свободного основания для ИНдивидуальных тенебримицинов при внут ривенном введении для мышей; тенебримицин И около 385, тенебримицин l3f около 220, тенебримицин Y около 140 и тенебримицин YJ около 120. Новый антибиотический комплекс получают в результате культивирования подходящего штамма антиномицетного организма при аэробных условиях на пригодной для культивирования ере де до тех пор, пока такая среда не будет обладать значительной активностью, характерной для антибиоти|Ка. Тенебримицин можно извлечь, применяя для этой цели различные методы вьаделения и очистки, известьые в производстве антибиотиков, Комплекс антибиотика может применяться, как таковой или же его можно поавергать дополнительным операциям для очистки с целью выделения различных его индивидуальных компонентов с более высокой степенью чистоты. Штамм представляет собой образующую спираль, устойчивые к воздействию тепла, аэробные по отношению к микроаэрофильным S t г ер t оту се s споры, имеющие продолговатые глащкие стенки, они ингибируются при искусственном освещении сравнительно небольшой интенсивности. Штамм Stгерtomyces tепеЬгаг(us внаделен из образца почвы посредством суспендирования отдельных порций почвы в стерильной дистиллированной воде с последующим переносом суспензий на питательную среду, образованную агаром. Засеянные пластинки с питаю1дей средой в виде агара инкубируют при 25-35°С до тех пор, пока не обеспечивался рост. К концу периода инкубирования колонии организмов, вырабатывающих антибиотик, переносят с помощью стерильной платиновой петли на скошенный агар, затем инкубируют с целью обеспечения достаточных количеств прививочного материала для производства антибиотика. Штамм организма, применяемого для производства комплексного антибиотика, помещена на постоянное хранение Б коллекцию культур американского типа в Вашингтоне (Федеративный округ Колумбия США, культуре присвоен № АТСС 17920. Морфология о При выращивании на пептоновом агаре по Чапеку разветвленные формы спор образуются в виде беспорядочных пучков и гроздьев на воздушном мицелии. Изолированные споры наблюдаются редко. Мицелий в целом, неповраясденном виде, легко отделяется от субстрата. Цепочки созревших спор обычно образуют 5-6 открытых спиралей. Споры имеют продолговатую форму, доходящую до цилиндрической. При исследовании под электронным микроскопом споры кажутся гладкими, имеют размеры от 0,7 до 1,3 и от 2,О до 2,1 мк. На среде по Беннату наблюдаются утолщения. Агар Чапека: характеристика роста; редкий,разбросанный; воздушный мицеллий .редкий; светлый, оранжевожелтый; спорообразование удовлетворительное; субстратный., мицелий; светлый, оранжево-желтый, растворимый пигмент слегка розовый. Пептон по Чапеку: обильный рост; возушный мицелий обильный, светлый, елтовато-коричневый с белыми участками обильное спорулирование; субстатный мицелий светлый, красноватосерый, растворимый пигмент; сероватородовый.
Агар, содержащий кальциевую соль, яблочной кислоты; рост умеренный, воздушный мицелий умеренный, светлый оранжево-желтый, спорообразование умеренное, субстратный серовато-розовый растворимый пигмент серовато-розовый Агар тирозиновый: рост ограниченный, скудный, воздушный мицелий скудный,светлый оранжево-желтый, сзпорулирование незначительное; субстратный мицелий светлый, оранжево-желтый, растворимый пигмеНт отсутствует. I Агар, содержащий неорганическ ие соли и крахмал: рост умеренный, воздушный мицелий умеренный, коричневато-розовый с белыми участками, спорообразование обильное; противоположный цвет светло-желтый, растворимый пигмент светло-желтый.
Агар, содержащий глюкозу и аспарагин, рост умеренный, воздушный мице,лий умеренный, светло-желтый с белыми участками, спорообразование умеренное субстратный мицелий светло-желтый рас воримый пигмент отсутствует.
Томатная паста - овсяная мука: рост обильный, воздушный мицелий обильный,светлый желтовато-коричневый, спорообразование обильное, субстратный мицелий темно-серый, красновато-коричневый растворимый пигмент темный, пурпурно-красный.
Дрожжевой экстракт: рост обильный воздушный мицелий обильный, светлый, оранжево-желтый с белыми участками,спорообразование обильное, субстратный мицелий умеренно-желтый растворимый пигмент отсутствует.
Питательный агар: рост редкий, разбросанный, воздушный мицелий редкий, белый, спорообразование редкое, субстратный мицелий сероватозеленовато-желтый, растворимый пигмент отсутствует.
Агар по Беннету: рост умеренный, воздушный мицелийумеренный белый, спорулирование умеренное, субстратньай мицелий светло-желтый, раство..римый пигмент отсутствует.
Действие на молоко: толстое желтое кольцо роста на поверхности. Наблюдается коагуляция и пептонизация. Нитраты восстанавливает, сероводород не образует, желатин полностью разжижает через 14 дней.
Требования в отношении температуры при выращивании на пептоновом агаре по Чапеку:
20° - рост отсутствует;
26 рост, удовлетворительный, воздушный мицелий отсутствует;
30 рост и образование воздушного мицелия умеренные, однако спорообразование отсутствует)
37 рост, образование воздушного мицелия и спорообразование все обильное)
43 рост, образование воздушного мицелия и спорулирование обильно ;
50 рост, образование воздушного мицелия и спорулирование - все обильное;
55 рост скудный, ограниченный;
60 рост отсутствует.
Споры, образованные из суспензии спор, нагреваемой при 75°С в течение 15 мин остаются жизнеспособными. В случае нагревания суспензии спор до в течение 15 мин жизнеспособных спор -не остается.
Красный растворимый пигмент вырабатывается лишь в присутствии иона трехвалентного железа, причем интенсивность пигментации пропорциональна концентрации иона трехвалентного железа в заданных пределах, Физиологические свойства: усваивает рибозу, фруктозу, маннозу, глюкозу, мальтозу, сукрозу, трегалозу, инозитол, салицин. Не усваивает арабинозу, рамнозу, ксилозу, лактозу, раффинозу, целлюлозу, инсулин, маннитол, oL -сорбитол.
Штамм Streptomyces tenebrarius АТСС 1720 культивируют с помощью обыных приемов в условиях погруженной аэробной культуры в среде, содержащей ассимилируемые источники углерода, азота и неорганических солей.
Штамм растет хорошо при темпера туре рт 30 до . Оптимгшьнбй является температура 37-43°С. Организмы .чувствительны к действию света и пло;,Хо растут при освещении. Через среду для выращивания культуры продувают стерильный воздух. Объем воздуха, используемый в процессе ферментации в резервуарах составляет свыше 0,1 об/мин на 1 объем средь: для выращивания культуры.
Концентрация, характеризующая активность антибиотика в ферментационной среде может быть легко прослежена по мере хода ферментации посредством отбора и испытания проб ореды для выращивания на их активность в отношении ингибирования роста организмов , которые должны тормозиться в своем развитии в присутствии тенебримицина. Для этой цели применяются два организма: Klebsiella pneumoniae и Мicobacter1um butyг i cum.
Максимальный уровень производства активности антибиотика достигает примерно через 4-7 дней после иноКу лирования среды для выращивания культур в случаях применения культур,выращиваемых в аэробных условиях погружения или же в стекляннрй посуде, содержимое которой перемешивается при встряхивании. Несколько более длительное время затрачивается при использовании поверхности культуры. Мицелий и нерастворившиеся остат ки удаляют из ферментационного буль на с помощью обычных средств, таки как фильтрование или центрифугирова ние. Характеризующее антибиотик активное начало содержится в профиль рованном бульоне и может быть извле чено из него путем применения адсор ционной техники. К числу абсорбенто которые могут быть применены с наибольшим успехом относятся катионнообменные смолы, например IRC-50. Извлекают тенебримицин и фермен тационного бульона следующим образом Бульон отфильтровывают с применение средства, способствующего фильтрова нию, после того, как показатель кон центрации водородных ионов рН смеси снижен приблизительно до рН 2 посредс вом добавления кислоты, такой каксерная кислота, фосфорная кислота, хлористоводородная кислота и подобные им. После этого значение рН фильтрата доводят примерно до рН 5, путем добавления концентрированной щелочи и смесь снова фильтруют. Пол ченный фильтрат пропускают через ионообменную колонку, заполненную ионообменной смолой, такой как IRC 50 в аммонийном цикле. Затем колонку промывают дистиллированной водой и активное действующее начгшо, характеризующее антибиотик, извлекают с сшсорбента посредством вьиншвания разбавленной кислотой.. Фракции, содержащие активное действукядее начало, объединяют и концентрируют приблизительно до 1/20 от первоначального объема. Значение показателя рН концентрата повышают примерно до рН 11 путем добавления концентрированной щелочи, после чего щелочный концентрат выливают примерно в шестикратный объем ацетона, хорошо перемешивают и охлаждают. Выделяющийся осадок, не обладающий активностью в микробиологическом отношении, устраняют с помощью фильтрования. Значение показателя рН фильтрата понижают приблизительно до рН 3,5 путем добавления 20%-Ной серной кислоты при тщательном перемешивании. Тенебримицин в виде комплекса осаждается в форме сернокислой соли, в то время как керуломицин, попутно образующийся в процессе ферментации, остается во всплывающем слое, который отбрасывается. Сернокислую соль тенебримицина растворяют в минимальном количестве воды и водный раствор пропускают через колонку с Доуэксом 1x1. Водный раствор сульфата тенебримицина доводят в колонке дистиллированной водой, после чего жидкость, вытекающую из коло.нки, собирают в виде отдельных фракций. Активные фракции объединяют и концентрируют до консистенции густого сиропа, заteM высушивают с целью получения тенебримицина в виде срободного основания. Основные факторы, образующие комплекс тенебримицина можно получить, если это желательно, в. виде раздельных антибиотиков посредством дополнительного фракционирования на колонках, заполненных ионообменной смолой тенебримицина. Для проведения фракционирования тенебримицин применяют в виде соли, являющейся продуктом присоединения кислоты. Пригодной солью является в данном случае сульфат Раствор сульфата тенебримицина удобно получать посредством приготовления 20%-ного водного раствора тенебримицина с последующей установкой показателярН раствора приблизительно до рН 4,5 путем добавления серной кислоты. Окрашенные примеси можно удалить с помощью перемешивания приготовленного раствора примерно с 5% (весовое количество по отношению к объемному активированного угля, например Дарко G-60. Эффективное обеспечение обычно достигают в результате перемешивания смеси, содержащей автивированный уголь в течение приблизительно часа. После этого смесь фильтруют и фильтрат, который содержит сульфат тенебримицина помещают в колонку, заполненную ионообменной смолой марки IRC-50 в аммонийном цикле. Колонку промывают водой, после чего индивидуальные антибиотики, образующие комплекс тенебримицина фракционировано отмывают с адсорбента с помощью 0,1-н. раствора гидрата окиси аммония. Процесс элюирования происходит медленно, и для получения необходимого эффекта фракционирования комплекса обычно необходимо очень большое число фракций. Так, например, полное и законченное фракционирование примерно 250 г тенебримицина требует получения около 700 фракций, каждая из которых содержится примерно в 900 мл жидкости, .отмываемой с адсорбента. Первые из числа полученных активных фракций содержат тенебримицин 1,1 и l . За ними следуют серии активных фракций, в которых содержится в качестве единственного антибиотика тенебримицин U Прежде чем будут открыты фракции, содержащие тенебримицин 3 , вслед за элюированием тенебримицина ц отходит ряд фракций, не обладающих активностью. Первые фракции, содержащие тенебри цин JV , содержат следы, тенебримицина ш . Тенебримицин 7 получают из колонки в составе активных фракций, за которыми следует тенебримицин 1 . Для получения тенебримицина W колонку дополнительно элюируют более концентрированным раствором гидрата окиси аммония, после того как весь тенебримицин V извлечен из колонки. По ходящей жидкостью для отмывки с аб бента тенебримицина V/ служит 0,3 раствор гидрата окиси аммония. Пример. Ферментация S.te brarius штамма АТСС 17920. Спорулированную культуру S.tene brarius АТСС 17920 получают посред ством выращивания организма на модифицированной среде Беннета в виде скошенного агара, имеющего след щий состав, г: Декстрин 10 Дрожжевой экстракт (Дифко) 1 Гидролизованный казеин 2 Экстракт из мяса крупного рогат го скота(Дифко) 1 0,01 агар 20 Деионизированная вода в количестве, необходимом для до-ведения объема смеси до 1000 мл Значение показателя концентраци водородных ионов рН доводят до рН до автоклавирования. Скошенную среду засевают спорам St, tenebrarius АТСС № 17920 и кул тивируют в отсутствии видимого све та в течение пяти дней при 37 С, Культуру, выращенную на скошенной де покрывают водой и наклонную по верхность осторожно соскабливают, удаляя споры с целью получения вод ной суспензии, содержащей споры,По лученную указанным образом суспенз спор применяют для инокулирования среды, имеющей такой состав, %: Декстроза 0,05 Питательная соевая мука, содержащая 35-45% диспергирующегося протеина 1,5 Декстрин 700 (картофельный) Декстрин с низким содержанием хлоридов 1 Хлористый калий 0,1 N Z-амин А О , 3 КН2.РО 0,05 MgSO.. 0,5 СтС1|2 -2Н О 0,025 Деионизированная вода 100 мл Инокулированную вегетативную ср ду инкубирурт при температуре окол 37°С в течение 16 ч на аппарате дл перемешивания путем встряхивания одновременном вращении со скорост 250 об/мин при размахе колебаний мм. Для инокулирования резервуара д посева емкостью 44 л, содержащего ную среду следующего состава: Декстроза 1 Соевая крупа 1,5 ,05 MgSO 0,5 Хлористый 0,1 СаС1;2 -2H-j O 0,025 Средство против вспенивания 0, применяют порцию вегетативной кул туры объемом 50 мл. Среду, находя уюся в резервуаре для посева стериизуют при 120С в течение 30 мин. нокулированную среду в резервуаре ля посева инкубируют при 37°С в ечение 12 ч. Перемешивание со скоостью 370 об/мин начинают немедленно после инокулирования. В продолжении всего периода инкубирования осуществляют аэрацию при скорости подачи воздуха 0,22 . К концу периода инкубации содержимое резервуара для посева используют для инокулирования ферментатора емкостью 1,14 0,95 м, содержащего среду следующего состава,%: Декстроза 4 Соевое масло рафинированное 3 Соевая мука 3 Хлористый аммоний 0,5 Хлористый кальций О,3 Сернокислый магний 0,2 Азотнокислый аммоний 0,1 NZ-амин-А О,5 Средство против образования - пены 0,2% Депонизированная вода До инокулирования ферментационную среду стерилизуют 30 мин при . Ферментацию проводят при З7с. Аэрацию осуществляют при скорости подачи воздуха 0,48 в течение го периода выращивания, начиная от инокулированияи кончая сбором выращенной культурыо Перемешивание начинают при скорости вращения мешалки 120 об/мин. Через 12 ч число оборотов мешалки увеличивают до 180. Процесс ферментации продолжают5 дней. Бульон, содержащий культуру,, после проведения ферментации фильтруют для удаления мицелия и других нерастворившихС.Я твердых веществ . Профильтрованный бульон содержит активность антибиотика при концентрации около 680 ед. в мл, П р и м е р 2. Изолирование комплекса тейебримицина. Значение показателя концентрации водородных ионов у 880 л ферментационного бульона, содержащего антибиотик и полученного, как указано в примере 1, понижают приблизительно до рН 2 путем добавления приблизительно 10-15 л 20%-ного водного раствора серной кислоты. К подкисленному бульону добавляют 45 кг средства, способствующего фильтрованию, тщательно перемешивают смесь и фильтруют. Отжатый осадок, оставшийся на фильтре промывгиот водой и промывные воды добавляют к фильтрату. Значение показателя рН фильтрата доводят до рН 5,5 посредством добавления 50%-ного водного раствора гидрата натрия. Добавляют примерно 4 кг средства, способствующего фильтрованию, смесь тщательно перемешивают и фильтруют. Полученный фильтр пропускают: через колонку, имеющую размеры 10,2 cMxIjB м, заполненную ионообменной смолой марки IRC-50. Колонка имеет слой смолы высотой 111,7-114,3 см и действует по аммонийному циклу. После того, как весь фильтрат пропустят через колонку, е последнюю промывают дистиллированной водой в количестве около 200 л. Активно действующее начало, характеризуемое свойствами антибиотика затем отМывают с адсорбента в течение 12-15 ч «л примерно л и 0,1 н. раствора серной кислоты. Элюат собирают в виде фракций по 10 л каждая. Присущая антибиотику активность в составе элюата становится распознаваемой в случае снижения величины водородного по- казателя рН до 4 или несколько менее. По мере продолжения отмывки, водородный показатель элюата продолжает-снижаться до тех пор, пока его значение не достигнет уровня около рН 1,5. 20 Фракции, содержащие активное начало антибиотика объединяют и концентрируют при уменьшенном давлении приблизительно до 1/20 от первоначального объема .. 25
Значение водородного показателя рН концентрированного элюата доводят до рН 11 посредством добавления 50%-ного водного раствора гидрата окиси натрия, после чего подщелоченный кон- п центрат добавляют к 6 объемам ацетона. Полученную смесь охлаждают и отставляют в сторону для TOiO, чтобы дать отделиться осадку, лишенному активности, свойственной антибиотику, jc Затем смесь фильтруют и плотную массу отжатую на фильтре, и состоящую из неактивного осадка, отбрасывают.
Значение водородного показателя рН устанавливают до 3,5 посредством добавления,при тщательном перемешивании, 0 20%-ного водного раствора серной Кислоты. Во время такой обработки комп,лекс тенебримицина осаждается в виде сульфата. Практически полное осаждение достигается, когда рН раствора 45 достигнет значения около 4 или несколько менее. Смесь фильтруют и фильтрат , содержащий церуломицин, попутно образующийся в процессе ферментации, отбрасывают.50
Отжатый на фильтре осгщок, являюийся сульфатом тенебримицина, растворяют в минимальном количестве воды и охлаждают. Все твердые вещества, растворяющиеся более или менее трудно, г отбрасывают, наряду со всеми твердыи веществами, выпадающими в виде осадка или кристаллизующимися при охлаждении, прозрачный раствор сульфата тенебримицина пропускают через насадку из ионообменной смолы марки 60 Доуэкс 1x1 размером 10,2смх2,1 м. Раствор антибиотика выводят из колонны с применением 40-50 л дистиллиованной воды. Жидкость, выходящую з колонны собирают отдельными фрак- 65
циями по 10 л. Активные фракции объединяют, концентрируют в вакууме до консистенции густого сиропа, который .после высушивания на противне дает сухой тенебримицин.
Примерз. Сульфат тенебримицина получают путем добавления концентрированной серной кислоты к 20%-ному водному раствору, содержащему 258 г комплекса тенебримицина в виде свободного основания с таким расчетом, чтобы значение водородного показателя рН среды стало равным 4,5. Полученный таким путем раствор сульфата тенебримицина обесцвечивают , перемешивая его примерно один час с 5% (весовое количество по отношению к объемному активировного угля марки Дарко 6-60. Затем раствор фильтруют и фильтрат пропускают через колонку размером 9х х105 см заполненную примерно 7 л ионообменной смолы марки IRC-50 и работающую в аммонийном цикле. После того, как фильтрат, содержащий соль антибиотика, пропустят через колонку, ее прошзвают приблизительн 17 л деионизированной воды. Въ1мава ние активной части антибиотика, задержанной в колонке начинают с помощью 0,1 н. раствора гидрата окиси аммония, подаваемого со скоростью около 20 мл в мин. Элюат собирают отдельными фракциями приблизительно по 900 мл, причем каждую фракцию проверяют на микробиологическую активность. Фракции, содержащие одина ковый фактор антибиотика объединяют и высушивают из замороженного состояния с . ;целью получения индивидуальных высушенных тенебримицинов. Индивидуальные тенебримнцины распределяются, в зависимости от активности фракций йледующим образом (табл.2).
П р и м е р 4.;Получение гелиантатов тенебримицинов.
Готовый раствор 2 г тенебримицина U в 22 мл воды и водородный показатель раствора доводят до значения рН 5 посредством добавления 50%-ной серной кислоты. Затем к раствору антибиотика добавляют горячий 10%-ный водный раствор метил-оранжа. Гелиантат тенебримицина il выделяют в виде осг1дка -и отделяют фильтрованием. Твердую соль тщательно промывают горячей водой и высушивают в вакууме. В итоге получают 3,5 г тенебримицин М гелиантата.
П р и м е р 5. Окончательная очиска факторов тенебримицина.
Готовят гелиантат тенебримицина в соответствии с методикой, аналогичной описаннойв примере 4. Четыре грамма приготовленной таким путем соли суспендируют приблизительJHO в 200 мл воды, значение водородiHoro показателя которой доведено до
ipH 2 за счет добавления серной кислоты. Смесь перемешивают около 4 ч, после чего фильтруют ее через воронку с фильтрующей пористой стеклянной пластинкой средней степени пористости с целью удален{|я гелиантовой кислоты. Фильтрат обесцвечивгиот путем пропускания через тонкий слой активированного угля, после чего пропускают через колонку размером 1x32 см, наполненную ионообменной смолой Доуэкс 1x2 и работающую в гидроксильном цикле. Фильтрат замещают в колонке с помсяцью дистиллированной воды с целью завершения отмывки активного действующего начала антибиотика. Выходящую из колонки жидкость собирают отдельными фракциями, объединяя вместе активные фракции
В заключение производят высушивание в замороженном состоянии. Полученный остаток представляет сухой антибиотик. Остаток, растворяют приблизительно в 15 мл воды и полученный раствор пропускают через колонку размером 1х х25 см, заполненную ионообменной смолой, Био Рад смола Аб 11А8. Это смола задерживающего действия. Активную составную часть, обладающую свойствами антибиотика, вымывают из колонки дистилированной водой. Активные фракции снова объединяют и высушивают в замороженном состоянии. Вы)ход тенебримицина высшей степени очистки - около ТОО мг.
Предлагаемый способ позволяет получить новый антибиотический комплекс, который найдет применение в медицинеJ
«3
а s
R Ю
Id ЕЧ
Таблица 2








| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения антибиотического комплекса а-28086 | 1975 |
|
SU576966A3 |
| Способ получения антибиотического комплекса а-35512 | 1977 |
|
SU751332A3 |
| Способ получения антибиотического комплекса тенебримицина | 1979 |
|
SU776566A3 |
| Способ получения антибиотика в 508 | 1977 |
|
SU715034A3 |
| Способ получения антибиотиков А51568-фактора А и А51568-фактора В | 1983 |
|
SU1194285A3 |
| Способ получения метаболита "а 27 106 | 1974 |
|
SU539538A3 |
| Способ получения антибиотического комплекса | 1977 |
|
SU786914A3 |
| Штамм @ @ @ @ @ . @ . | 1977 |
|
SU713170A1 |
| Штамм @ @ 12/3а-продуцент аклациномицинов @ и @ | 1982 |
|
SU1069433A1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА А204 | 1971 |
|
SU296323A1 |

Фракция
1-34 35-53 54-77 78-153
154-172
173-249
250-256
257-634
635-668
669-698
л;
с этого момента элюат изменен до р,3-н. гидрата окиси аммония.
Формула изобретения Способ получения антибиотичесого комплекса,содержащего тенебримицин И, Ш , , и Vi и их солей заключающийся в том, что штамМ Streptomyces tenebrarius АТСС 17920 культивируют в глубинных условиях аэробно в питательной среде, содерПрисутствующий антибиотик
Не активны
Тенебримицин I Д
Тенебримицин П
Не активны
Тенебримицин l
Тенебримицина Ш
Тенебримицин ij
Не активны
Тенебримицин V
Не активны
Тенебримицин
жащей источники углерода, азота и минеральные соли при температуре 3743°С в течение 4-7 дней, затем выделяют целевой продукт в свободном ви30 Яе или в виде его солей, при необходи-мости разделяют комплекс на составные антибиотические компоненты П , iTl , ij , V и VJ и переводят их в соли.
Авторы
Даты
1981-11-23—Публикация
1967-05-10—Подача