Изобретение относится к способу получения новых оптически активных норпиненовых соединений общей формулыгде Ч, - -0-COCHf или, взятый вместе с R , образует двойную связ Rj -0-СОСН или взятый вместе с R, образует двойную связь. Получаемые соединения являются пол продуктами при получении биологичес активных производньпс гексагидродибензопиранона- цис- и транс -1-окси-3- (1,1 -диметилгептил) -6,6-диметил;-6,6а,7,8,1О,Юа-гексагидро-ЭН-дийе 30 (b.d )пиран 9-онов (л ir). 1-Окси-З-замещенные-6,6-диметил-6,6а,7,8,10,10а-гексагидро-9Н-дибензоСЬ,j)пиран-9-оны, в том чис ле 3-(1,1-диметилгептил)ьное производное, обладают сильным воздействием на центральную нервную систему и могут быть использованы как антидепрессанты и обезболивающие средств Наиболее перспективно использова ние не рацематов, а индивидуальных оптических изомеров названных соеди нений 1 - З . Известен способ получения соединения (П) путем взаимодействия 5-(1,1-диметилгептил)резорцинола с диэтил-ot ацетилглютаратом, циклизации полученного лактонового эфира под действием гидрида металла, кета лизации кетогруппы в полученном кетолактоне, обработки полученного кеталя метилмагнийбромидом, замести тельной циклизации полученного производного с отщеплением соли магния и восстановления двойной связи действием лития в среде жидкого аммиака при -78°С з. Изрес ный способ многостадиен и сложен. Цель изобретения - разработка способа получения новмх соединений класса норпиненов, пригодных I качестве полупродуктов при получёнии 292 биологически активных производных гексагидродибензопиранона (Пд,). Поставленная цель достигается тем, что согласно способу получения оптически активных норпиненовых соединений общей формулы (1), где - 3 nMSioT указанные вьппе значения, оптически активно 6,6-диметилнорпинон-энол-ацетат формулы 0-С-(1Н5. подвергают взаимодействию с двухтрехкратным мольным избытком тетраацетата свинца в среде-бензола в атмосфере инертного газа при температуре кипения реакционной смеси. При этом, с целью получения соединений (I), где R, - ацетокси; Rj и R образуют двойную связь (ta), процесс ведут в течение 1-3 ч, с целью получения соединений (I), где Rj ацетокси; R, и Rj образуют двои ную связь (IS), процесс ведут в течение 16-2П ч. Оптически активные соединения формулы (III) могут быть легко .получены по методике 4 из оптически активных j и Е- изомеров -пинена. Представляющие практический интерес соединения (На ,б) могут быть получены взаимодействием соединений (Г) с 5-(1,1-диметилгептил)резорцинолом в хлороформе в присутствии П-толуолсульфокислоты и нагреванием полученного продукта в присутствии (т-толуолсульфокислоты или хлорида олова. Примеры показывают возможность использования соединений (I) как полупродуктов при получении обладающих биологической активностью соединений (Ilq) и (US). Способ получения соединений (Па) и (Ilf) с использованием соединений (I) обеспечивает значительное упрощение технологии в сравнении с известным способом 09 , Пример 1. ()-6,6-Лиметил-2,4-диацетокси-2-норпинен D(-)- IS. К перемешиваемому в атмосфере газообразного азота раствору 18,0 г 3 . (-)-норпинон-энол-ацетата в 250 мл сухого бензола добавляют 48,8 г тетраацетата свинца., который предварительно высушивают в вакууме над пятиокисью фосфора и гидроокисью калия. Реакционную смесь нагревают с обратным холодильником и перемеши вают в течение 18 ч. Затем реакционную смесь охлаждают до комнатной температуры, фильтруют и фильтрат промывают 10%-ным. раствором ната натрия и водой, сушат, раство ритель отгоняют при пониженном давлении и получают 23,5 г сырого продукта в виде прозрачной жидкост Полученный таким образом продукт перегоняют и получают 9,3 г (iS) йыход 39%, т.кип. 115-119°С/5 мм, Wi - 89,7° (с ПО СН ). НЯМР-спектр ЧСНС,), S ; 5,25 (т, 2Н); 2,4 (т, 4Н); 2,1 (д, ЗН); 2,0 (9, ЗН); 1,35 (б, ЗН); 1,0 (S, ЗН). ИК-спектр (СНСе,), см : 1730, 1763, иарбонил. Масс-спектр, т/е: 196 (М -СН„ С О). Пример 2. (+)-6,6-Диметил.-2,2-диацетокси-З-норпинен (+)- 1а К перемешиваемому в атмосфере г зообразного азота раствору 18,0 г (-)-норпинон-енол-ацетата в 250 мл сухого бензола добавляют 48,8 г тетраацетата свинца, который предварительно высушивают в вакууме над пятиокисью фосфора и гидроокись калия. Реакционную смесь нагревают с обратным холодильником в течение 2 ч. Затем смесь охлаждают до комнатной температуры, промывают водны раствбром бикарбоната натрия и водо сушат, растворитель отгоняют при пониженном давлении и получают продукт в виде масла. Затем масло перегоняют и получают 9,8 г (Id), выход 41%, т.кип. 102-103°С/5 мм, И + 33,2°(с 1,0, снсе,). Найдено, %: С 65,77; Н 7,32; СОСН 36,56. 1 19 4 Вычислено, %: С 65,53; Н 7,61; СОНО 36,12. Н ЯМР- спектр (спев, ),S : 6,4 (m, 2Н); 3,15 (m, 1H); 2,3 (m ЗН); 2,1 (g, 6Н), 1,4 (s, ЗН); 1,1( Масс-спектр, m/e: 196 (). ИК-спектр (CHCgj), см : 1750 карбонил. 9. ..4 Пример 3. Получение (+)-4(1 1-диметилгептил)-2,6-диоксифeнилJ-6,6-димeтил-2-нopпинaнoнa. Раствор 1,19 г (-)-6,6-дйметил-2,4-диацетокси-2-норпинена и 1,18 г 5-(1,1гдиметилфенил)резорцина в 50 мл хлороформа, содержащего 0,95 г Яцоногидрата пара--толуолсульфокислоты, выдерживают при 25 С в течение 4 ч. Реакционную смесь разбавляют 100 мл диэтилового эфира и полученный раствор промывают водным раствором бикарбоната натрия, водйй и сушат, растворитель отгоняют при пониженном давлении и получают продукт в виде полукристаллической массы. Образованный таким образом продукт растирают с 25 мл Н-гексана и фильтруют, получают 1,30 г (-ь)-4- 4-( 1, 1-диметилгептил)-2,6-диоксифенил -6,6-диметил-2-норпинанона. Т.пл. 171-174с. « р° + 55,8° (с 1,0, снсе). Найдено, %: С 77,59; Н 9,83. 21 н 3Вычислено, % С 77,38; Н 9,74. н ЯМР-спектр (CJCe, +ВМ90с} в), S : 8,05 (9, 2Н фенольный ОН) ; 6,35 (, 2Н); 4,05 (t, 1Н); 3,65 (т, 1Н); 2,45 (пц 5Н); 1,35 (д, ЗН); :,15 ;(|т1, 19Н); 0,95 (5, ЗН) . ИК-спектр (КБг ), см 1668, карбонил. I Масс-спектр, м/е: 372 (М ). По такой же методике 1, г (+) 5, 6-диме тил- 2,2-диаце то к си- 3норпинена превращают в ()(1,1-диметилгептил)-2,2-диоксифенил -6,6-диметил-2-норминанЬн с такими же физическими свойствами, как у полученного продукта. Получение (-)-цис 1 окси-3-(1,1-диметилгептил)-6,6-диметил-6,60,7, 8,10,10р-гексагидро-9Н-дибензо(6,е}) пиран-9-она Г(-)-110. Раствор S72 мг (+)-4-{;4-(1,1-диметилгептил) -2,6-диоксифенил -6,6-диетил-2-норпинанона в 25 мл хлороорма, содержащего 190 мг моногидрата Пара-толуолсульфокислоты, нагревают с обратным холодильником при перемешивании в течение 24 ч. Затем реакционную смесь охлаждают до комнатной температуры, разбавляют 25 мл воды и несколько раз экстрагируют по 25 мл ди этилового эфира. Эфирные экстракты соединяют вместе, промывают 10%-ным воднь раствором бикарбоната
натрия и водой, сушат, растворитель отгоняют при пониженном давлении и получают 380 мг продукта в виде белой пены. Полученный таким образом сырой продукт хроматографируют на колонке с насадкой из промышленного силикагеля Волн АктивитиП, элюирование ведут 5%-ным раствором диэтилового эфира в бензоле. После выпаривания растворителя из соответствующих фракций по чают 228 мг (-)-цис-1-окси-3-(1,1метилгептил)-6,6-диметил-6, 6ci, 7,8, 10,1 Оа-гексагидро-9Н-дибензо (Ь ,ij )-пиран-9-она, т.пл. 139,5-141°С; 7 -50® (,о снсе,). Масс-спектр, «я/е: Найдено 372, 2665; Вычислено, 372, 2664. Получение (-)-Тро(нс-1-окси-3-(1,1-диметилгептил)-6,6-диметил-6,6а, 7,8,10,10а-гексагидро-9Н-дибензо/Ь,3)пиран-9-она С(+)ПК . К раствору 372 мг (+)(1,1-диме тилгептил)-2,6-диок сифе нил -6,6-диметил-2-норпинанона в 25 иг хлороформа добавляют в одну порцию 1,0 мл хлористого олова. Реакционную смесь перемешивают при 25 С в течение 16 ч, затем добавляют ее к 50 г льда. Водную реакционную ; смесь экстрагируют несколько раз по 25 мл диэтилового эфира, эфирные экстракты соединяют вместе, промывают 2 н. раствором соляной кислоты затем 5%-ным водным раствором бикар
боната натрия. Затем органический слой промывают водой, сушат, растворитель отгоняют при пониженном давлении и получают 378 мг продукта в виде сырой пены. Затем эту пену хроматографируют в колонке с силикагелем Волм АктивитиП, элюирование ведут бензолом. После отгонки растворителя из фракций, в которых по .данным тонкослойной хроматографии содержится один компонент, получают 305 мг (-)--гранс-1-окси-3(1,1-диметилгептил)-6,6-диметил-6, 6с|, 7, 8,10,10а-гексагидро- Н-дибензо (Ь ,(j)-пиран-9-она, ei I, -52,3® (,0 СНСЕ ) . Масс-спектр, (7)/е: найдено 372, 2667, С,, вычислено 372, 2664. После отгонки растворителя из элюатов тонкослойная хроматография показывает наличие другого компонента, а именно 55 мг (-)-4ис-1-окси-3-(1,1-диметилгептил)-6,6-диметил6,60,7,8,10,10а-гексагидро-9Н-дибензоСЬ,)-пиран-9-она, oi -50 (с 1,0; CHCe). Таким образом, изобретение позволяет получать с выходом 39-41% оптически активные соединения (1), которые могут быть использованы в каче стве полупродуктов для синтеза биологически активных производных гексагидродибензопиранона формулы (tt) по значительно упрощенной технологии по сравнению с известным способом.


СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХ НОРПИНЕНОВЫХ СОЕДИНЕНИЙ общей формулы В,. .o-fj-dHs II где R, - ацетокси или, взятый вместе с R, образует двойную связь,; Rj - оцетокси или, взятый вместе со с R а ., образует двойную связь, отличающийся тем, что, оптически активный 6,6-диметилнорпинон-энол-ацетат формулы н н подвергают взаимодействию с двух-трехкратным мольным избытком тетраацетата свинца в среде бензола в атмос фере инертного газа при температуре кипения реакционной смеси.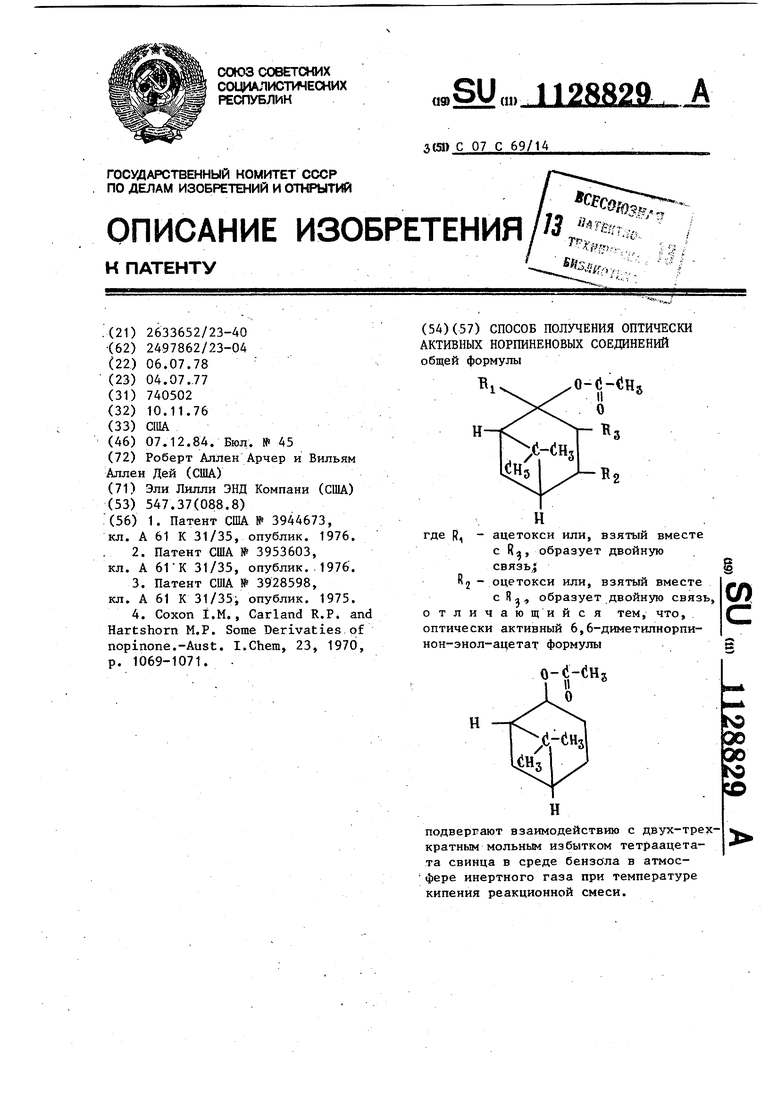
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Патент США № 3944673, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент США № 3953603, кл | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| and Hartshorn M.P | |||
| Some Derivaties of nopinone.-Aust | |||
| I.Chem, 23, 1970, p | |||
| ИСКРОВОЙ ГЕНЕРАТОР КОРОТКИХ ВОЛН | 1924 |
|
SU1069A1 |
Авторы
Даты
1984-12-07—Публикация
1978-07-06—Подача