валина, N-метилизолейцина и N-метил-аллоизолейцина.
Процентное содержание различных компонентов продукта, обозначенных А, В, С и D, определяют после разделения их методом жидкостной хроматографии при высоком давлении в инвертированной фазе и измеряют при помощи интегратора. Процентные содержания различных компонентов определяют по отношению к суммарной площади пиков четырех компонентов в зависимости от их остаточного поглощения в УФ-области при 25 нм. Процентное содержание каждого из пептидных компонентов лежит в пределах: А 2-5; В 10-16 С 32-39; D .
Компонент А при частичном гидролизе в щелочной среде дает три молекулы лактона, образующиеся при разрыве эфирных связей и последующей циклизации в лактон о -гидроксиизовалерил-N-метилвалина. При полном гидролизе в кислой среде происходит разрыв и эфирных, и аминных связей. Результатом такого гидролиза является получение трех молекул N-метилвалина и трех молекул о -гидроксиизовалериановой кислоты. Компонент В при частичном гидроли- -j водят
зе в щелочной среде дает две молекулы лактона, образующегося при циклизации о -гидроксиизовалери л-N-метилвалина и одну молекулу лактона, образующегося при циклизации cii-гидроксиизовалерил-М-мети/1-изолейцина 91ли -аллоизолейцина. При полном гидролизе в кислой среде компонента В получают три молекулы гидроксиизовалериановой кислоты, две молекулы N-метилвалина и одну молекулу гидроксиизовалерил-М-метилизолейцина или N-метил-аллоизолейцина.
Компонент С при щелочном гидролизе дает одну молекулу лактона, образующегося при циклизации 0 1-гидроксиизс5валерил-Н-метилвалина и две молекулы лактона, образующегося при циклизации 0 -гидроксиизовалерил-N-метилизолейцина или N-метил-алоизолейцина. При полном гидролизе в кислой среде получают три молекулы о -гидроксиизовалериановой кислоты, одну молекулу N-метилвалина и две молекулы N-метилизолейцина или N-метил-аллоизолейцина.
Компонент D при частичном гидролизе в щелочной среде дает три молекулы лактона, образующегося при циклизации о -гидроксиизовалерил-М-метилизолейцина или N-метил-аллоизолейцина. При полном гидролизе в кислой среде компонент D дает три молекулы ск -гидроксиизовалериановой кислоты и три молекулы N-метилизолейцина или N-метил-аллоизолейцина.
При гидролизе всего биологически активного продукта по предлагаемому способу получаюто -гидроксиизовалериановую кислоту, N-метилвалин, N-метилизолейцин (в эритро-форме) и N-метил-аллоизолейцин (в трио-форме), при этом N-метил-аллоизолейцин не может быть отнесен ни к одному конкретному компоненту.
Способ осуществляют следующим образом.
Проводят аэробную ферментацию штамма Fusarium eguiseti № 213107 в глубоких сосудах при 29±5°С и рН в пределах при перемешивании, продолжительность каждой стадии 36-iS ч, собирают в конце ферментации мицелий, извлекают его хлорсодержащим раство-. рйтелем - трихлорэтиленом, отделяют органическую фазу, отгоняют растворитель досуха, в остаток вводят углеводород {пентан или гексан), проВОДНЫМ спиртом с противотоке: водный раствор спирта представляет собой смесь метанола и воды, после чего отделяют спиртовую фазу, концентрируют ее, осаждают продукт пептидного характера и очищают его с применением хроматографии на колонке с окисью алюминия.
П.р и м е р 1. Идентификация штамма.
Ферментационная среда № 1, г: сахароза 25; глюкоза 25; нитрат аммония 10; сульфат магния 2,5 однозамещенный фосфат калия 5- рН после стерилизации 5- Компактный мицелий имеет пушистую нитевидную структуру и оранжевую окраску. При переворачивании чашки Петри культура принимает желто-оранжевую окраску (цвет персика) , переходящую в охристый оранжевый цвет у более развитой культуры
Зерновая среда.
Мицелий дает ровную, пушистую культуру, располагающуюся в виде характерных колец. Пигментация слабая, обратная сторона при развитии культуры приобретает темно-желтую окраску.
Среда сне, г: карбоксиметилцеллюлоза 15; нитрат аммония 1; однозамеэкстракцию углеводородной фазы щенный фосфат калия 1; сульфат магния 0,5; экстракт дрожжей 1; дистиллированная вода 1000. Эта среда может быть дополнена посредством добавления к ней сухих фрагментов культуры Phragmites communis. Мицелий редкий очень ровный, незаметный, не имеющий окраски. Воздействие света на споруляцию грибков. При воздействии белого света, который дают белые флуоресцентные источники света, интенсивностью 1000 л в течение 12 ч ежедневно, отмечают образование макроконидий в среде на основе CMC и в среде, дополненной культурой Phragmites. При использовании источника света Вуда (длина волны излучения ЗбО,Зб5 нм), расположенного на расстоянии 33 см от испытуемых культур, макроконидии образуются в больших количествах по истечении -6 дней. Окраска культуральных сред, культивированных под воздействием источника света Вуда, несколько ослаблена по сравнению .с окраской сред, полученных при культивировании под воздействием белого света. Культура. Fusariurn eguiseti №21310 может-быть получена на классических средах, используемых для получения культур вида Fusariurn. Насреде,содержащей tO г/л овсяной муки, среде на основе картофеля (50 г картофельной пульпы, 10 г глюкозы и 20 г агара на 1 л воды),. солодово-агаровой среде (2), агаризованной на 2, конидиогенез наблюдается редко с образованием ненормальных конидий, со смешением несозревших макроконидий С микроконидиями. Появление окраски в виде концентрических зон наблюдается в большей степени при культивировании под воздействием света, чем для культур, полученных в темноте (на среде на основе картофеля). Куль тура на овсяной муке дает компактные ровные, гетерогенные, слабо окрашенные мицелии. Конидиогенез в этом слу чае не наблюдается. Морфологическая характеристика ма роконидий. Макроконидии имеют удлиненную сер повидную форму, конечные клетки имею форму раскрытого клюва, промежуточны клетки несколько расширены, основная клетка имеет форму ступни. Размеры значительно меняются и зависят от ус 6 ловий культивирования: длина 25 60 мкм, ширина - мкм. Окрашенные конидии имеют стеклообразный вид. Ко.личество перегородок в молодых культурах А. Микроконидиофоры П.ПОХО различимы и появляются редко, дают разветвление в виде кисточки. Характеристика хламидоспор. Промежуточные хламидоспоры, одиночные или в виде цепей, имеют форму глобул с более плотными стенками диаметром мкм. Они образуются в более зрелых культурах при культивировании более 20 дней. Приготовление подложек. Скошенный агар, Из содержимого ампулы с лиофилизированным мицелием извлекают 2 мл стерилизованной воды. Полученную суспензию используют для высевания культуры в четырех пробирках, содержащих по 10 мл скошенного агара, имеющего следующий состав, г: овсяные хлопья 30; глюкоза 10; агар 20; дистиллированная вода 1000; условия стерилизации 20 мин при 120С, первоначальный рН 6,6, рН после стерилизации 5,8. . Среду культивируют 6-8 дней в термостате при 28 С, после чего подвергают облучению солнечным светом в течение недели в лабораторных условиях при комнатной температуре. Чашка Ру. Из воздушного мицелия, полученного на скошенном агаре, извлекают 10 мл стерилизованной воды. Полученную суспензию применяют для высевания в 5 чашках Ру, содержащих 200 мл агаровой композиции состава, идентичного приведенному. Среду культивируют 68 дней в термостате при 28 С, после чего подвергают облучению солнечным светом в течение недели в лабораторных условиях. Получение прививочного материала. Первая стадия. Из культуры, полученной в чашке Ру, получают суспензию мицелия в 100 мл стерилизованной воды путем снятия культуры со всей поверхности. Полученную суспензию используют для высевания культуры в колбе, содержащей Ц л среды следующего состава, г/л: сахароза 25,0; глюкоза 25; нитрат аммония 10,0; однозамещенный фосфат калия сульфат магния 2,5; водопроводная вода 1,0 л. Условия стерилизации 30 мин пои , первоначальный рН 5,5, рН после стерилизации А,75- Аэробное культивирование проводят при 28°С. в устройстве, обес печивающем барботирование стерилизованным воздухом с перемешиванием k8 ч (среднее значение 72 ч) . Вторая стадия. Посев культуры () производят исходя из одной -литровой колбы пре парата, полученного на первой стадии и 75 л среды следующего состава, г/л сахароза kO; целероза 5; нитрат аммо ния 10; однозамещенный фосфат калия 5; сульфат магния 2,5; водопроводная вода 1,0 л. Условия проведения стери лизации 30 мин при 120 С, рН после стерилизации 5,6. Условия ферментации: аэрация 3,5 м /ч, перемешивание 70 раз в мин, температура продолжительность 36 ч. Во время про ведения ферментации проводят контрол стерильности, измерения рН, микроскопические исследования и количественный анализ остаточных Сахаров с соблюдением стерильных условий. Третья стадия. Используют прививочный материал, полученный на второй стадии, для посева на 1200 л питательной среды, имеющей состав, идентичный описанному (посев 6,25)- Условия проведения ферментации: аэрация 70 м /ч, перемешивание 50 раз в мин, температура + 29-1 °С,, продолжительность ч. Во время проведения ферментации проводят те же контрбльные исследования, что и на предыдущей стадии . Производство. 1200 л прививочного материала, по лученного на третьей стадии, переносят для посева в 7 м питательной ер ды, имеющей следующий состав, г/л: сахароза 50; целероза 5,0; нитрат аммония 10,0; однозамещенный фосфат калия 3,0; сульфат магния 2,5; сульфат цинка 0, карбонат кальция 2,0 водопроводная вода 1,0 л; условия пр ведения стерилизации 30 мин при +20 рН после стерилизации 6,5-Условия фе ментации: аэрация 250 , перемеши вание 20 раз в мин, температура + 29 41 °С, продолжительность 0 ч. Во вре мя проведения ферментации осуществляют те же контрольные исследования, что и на предыдущих стадиях, Значение рН, близкое к 3 на 2А ч, медленн повышают и стабилизируют около значе ния 5,3-5,5 к концу ферментации. Мицелии отделяют от ферментационного русла фильтрованием под давлением и сушат в вентилируемом сушильном шкафу. Таким способом получают после измельчения в среднем 120 кг сухого мицелия. Экстракция. Экстракция неочищенного продукта. На 100 кг мицелия. Из измельченного мицелия извлекают 400 л трихлорэтилена, перемешивают 2 ч и сушат. Полученный остаток промывают 100 л трихлорэтилена и проводят вторичную экстракцию 300 л трихлорэтилена при перемешивании 1 ч, после чего опять сушат. Остаток промывают 100 л трихлорэтилена, объединяют экстракты, концентрируют их при пониженном давлении до получения густой массы. На 10 кг полученной массы. Массу растворяют в 90 л гексана, осветляют фильтрованием и экстрагируют из гексанового раствора водным раствором метанола в противотоке (cor став водного раствора вода:спирт 80:20 по объему); первая экстракция 50 л смеси, вторая 25 л, третья 12,5 л и четвертая 10 л. Метанольные экстракты объединяют и концентрируют досуха при пониженном давлении. Хроматография на кислотной окиси алюминия. Получение окиси алюминия. 1 кг окиси алюминия переводят в суспензию в 5 л дистиллированной воды и при слабом перемешивании добавляют концентрированную соляную кислоту в количестве, необходимом для поддержания рН ,0 в течение 2Ц ч. Суспензию фильтруют через нейлоновый фильтр и обильно промывают дистиллированной водой, после чего промывают ацетоном для удаления остатков воды сушат окись алюминия в сушильном и шкафу при в течение одлой ночи. Хроматография. На 20 кг метанольного экстракта. Метанольный экстракт растворяют в 80 л хлористого метилена, осветляют раствор фильтрованием и подвергают хроматографическому разделению в хлористом .метилене на стеклянной колонке высотой 0,8 м, заполненной 0 кг окиси алюминия таким образом, чтобы расход раствора в хлористом метилене составлял 15 л/ч. Окись алюминия промывают 80 л хлористого метилена при том же часовом расходе. Выделение активного вещества. Отмытое хлористым метиленом вещество концентрируют при пониженном давлении до получения густой массы, которую затем растворяют в 200 л эти лового спирта и осветляют фильтрованием. Раствор в этиловом спирте охлаждают до- k С и добавляют при медленном перемешивании 8 ч, поддерживая при этом температуру и при перемешиваний 20, ч, после чего отделяют выделившиеся кристаллы фильтрованием. Полученный остаток промывают смесью метанол:вода 1:2, предварительно охлажденной, затем 50 л дистил-15 ния лированной воды. Кристаллический деп сипептид сушат в сушильном шкафу при пониженном давлении и 40С до по стоянного веса. Депсипептид получают в виде кристаллического порошка белого или светло-желтого цвета, без запаха, имеющего горький вкус. Он очень плохо растворим в воде и легко растворяется в хлороформе, метиловом и этиловом спирте при 95°С. Температура плавления безводного продукта, определенная методом Кофлера, равна 121i5 С, удельное вращениеСо ,-80°±5°С 5, метанол. Общее содержание азбта 6,2±0,3%. Идентификация компонентов методом тонкослойной хроматографии. Приготовление носителя. Из расчета на 5 хроматографически пластинок 20-20 см готовят гомогенну смесь из 4 г целлюлозы Мп 300,8 г це люлозы Ип 300 G .и б5 мл воды, после чего наносят полученную суспензию на тщательно обезжиренные пластинки в . виде слоя толщиной 0,25 мм. Обработа ные таким способом хроматографические пластинки сушат на воздухе при 110 С 2 ч, охлаждайт и погружают в вертикальном положении в смесь формамид:ацетон 1: на глубину около 2 см от края. После этого их сушат 1 мин на открытом воздухе для удаления ацетона. Растворитель для хроматографии. Используют гептан, насыщенный фор мамидом (пересыщенный раствор). Готовят раствор в метаноле из рас чета 10 мг вещества на 1 л. (О мл раствора помещают на рассто нии I см от края пластинки, н обраб танного формалином. После распространения раствора на расстояние около 10 см пластинку сушат 1 ч при и опрыскивают Э 10 0,5%-ным раствором иода в хлороформе. При этом образуются четыре пятна желтого цвета, два из которых, наиболее интенсивные, соответствуют Rf около 0,55 и 0,5, одно, менее интенсивное, Rf около 0,35, и одно очень слабое Rf около 0,3Разделение дипсипептида на компоненты методом жидкостной хроматографии при высоком давлении (ЖХВД). Относительные содержания, компонен-тов А, В, С и D определены для различных промышленных образцов после разделения их методом ЖХВД и измереплощадей пиков с помощью интегратора. Относительные содержания компонентов в процентах рассчитаны относительно суммы площадей пиков всех четырех компонентов при предположении , что остаточное поглощение в УФ-области при 25 нм остается одинак.овым для всех компонентов. Условия проведения разделения: носитель фаза Bonsapak с 18 (Waters Associates) длина 30 см, внутренний диаметр 3,9 мм. Элюент метанол:вода 8:2 по объему. Скорость пропускания 1,5 мл/мин. Рабочие растворы: 10 мг . вещества на 1 л метанола, дозирование по 10 мл. Детектирование: УФ-область, длина волны 25 нм. Чувствительность D 0,02 от всей шкалы. Измерение площадей с применением интегратора ICAP 5. Следующие результаты соответствуют среднему составу для различных образцов депсипептидного продукта,%: А 3,9; В 15,3; С 38,1; D k2,7. Наличие продукта подтверждается также приводимыми ИК-спектрами. Пример 2. Фармацевтические композиции на основе депсипептида. Створоженный раствор в изо-пропилмиристате, г: экстракт депсипептида Fusarlum eguiseti 0,050; эссенция Нероли 0,050; эвкалиптол 0,050; сахарин О , 001 25; изо-пропилмиристат 2,5 мл; флюген 12-7,5 мл. Водная суспензия, г: экстракт депсипептида Fusarium eguiseti 0,050; полио.ксиэтиленсорбитанмоноолеат твин 80 0,010; хлористый натрий GJ80; эссенция Нероли 0,050.; эвкапмптол 0,05; сахаринат натрия 0,010, дистиллированная вода 20. В обоих случаях продукт распределяют с помощью дозировочного шприца емкостью 0,080 г на доз, что соответствует 200 мг активного препарата на дозу.
1твороженный раствор, г: экстракт депсипептида Fusarium eguiseti 0,015; ароматизирующий агент 0,0075; изо-пропилмиристат 0,75 мл, фреон 122,25 мл. Сосуд оборудован клапаном на 25 мкл и содержит 3 мл раствора. При каждом срабатывании клапана получается доза депсипептида в 125 мкг.
Створоженный раствор, г: экстракт депсипептида Fusarium ego i set 0,030 ароматизирующий агент 0,015; изо-про пилмиристат 0,750 ел, фреон 122,23 МЛ- Этот рецепт дает возможност иметь 250 мкг депсипептида в каждой дозе при общем количестве доз 120. Маслообразный раствор, г: экстрак депсипептида Fusarium eguiseti 0,05; сахарин 0,0015; ароматизирующий аген 0,05; изо-пропилмиристат 6 мл, сосуд оборудован дозатором, позволяющим по лучать дозу в 30 мкл при каждом нажа тии . Водная суспензия, мг: экстракт депсипептида Fusarium eguiseti 50; полиоксиэтиленсорбитанмоноолеат 15; хлористый натрий 120; двузамещенный фосфат натрия 17,25; двузамещенный фосфат калия 3; хлористый кальций 1,5; хлористый магний 1,5; мышьяковистый меркаптид натрия 0,0375; вода 15- Суспензию помещают в сосуд емкостью 15 мл, оборудованный дозато ром, обеспечивающим получение дозы в 75 мкл при каждом впрыскивании. Каждое впрыскивание содержит 250 мкг активного вещества. Водный раствор для инъекций: депсипептид Fusarium eguiseti 100 мг, кремофор EL 0,10 г, хлористый натрий 0,8 г, вода 100 мл. Пример 3- Фармакологическое изучение экстракта депсипептида. Изучение гуморального иммуностимулирования у мышей по отношению к эритроцитам баранов (GRM). Иммунизация. Каждой мыши СД швейцарской породы 5 весом 20 г, вводят пороговую имуннуюдозу в 10 миллионов эритроцитов барана внутривенно. Кровь барана предварительно обрабатывают раствором Эльзевира. Эритроци ты- трижды промывают физиологической сывороткой, а затем переводят в суспензию в этой же среде для проведени прививки. Каждая группа иммунизированных мышей состоит из 8 особей. Обработкаживотных. В каждом эксперименте имеют одну группу контрольных животных и две
группы животных, прошедших специальную обработку. Мышей подвергают обработке, спустя различное время после иммунизации различными способами: внутривенно или внутрибрюшинно. Культуру псевдодифтерийнрй палочки Согупеbacterium Parvum готовят в виде суспензии в физиологической сыворотке. Депсипептид растворяют в пропиленгликоле, исходя из концентрации мг/мл, после чего указанный концентрированный раствор разбавляют физиологической сывороткой в соотношении 1:20 для мышей, получавших дозу 50 мкг депсипептида, и в соотношении 1:100 для мышей, получавших 10 мкг депсипептида. Взятие пробы. В определенные дни у мышей берут пробу крови посредством ретроорбитальпункции. Сыворотки хранят при ной для предотвращения разложения. Для каждой данной группы исследованных животных изучают характеристики индивидуальных сывороток, а также характеристики объединенной сыворотки.. Анализ антител. Определение степени гемагглютинации. Методика микрогемагглютинации на пластинках. К 0,75 мл суспензии эритроцитов барана, нанесенных на тампон Майера с титром мл (0, им 0,700) добавляют 0,025 мл сыворотки, разбавленной в отношении 2:2, на том же самом.тампоне. Пластинки оставляют на 2 ч при комнатной температуре, затем в течение ночи при С, Гемагглютинацию наблюдают при помощи увеличительного зеркала. Степень гемаглютинации определяют по наибольшему разбавлению сыворотки, при котором наблюдается свободная гемагглютинация. Степень определяют в качестве логарифма при основании 2 от степени разбавления, так при разбавлении 1, степень гемагглютинации 6. Свободная гемагглютинация может быть сосчитана только при значении степени более или равным 4, при меньших значениях этого показателя счет становится слишком затрудненным. Определение показателя гемолиза. Методика микрогемолйза на пластинках. К 0,025 мл суспензии эритроцитов барана на тампоне Майера (10 на мл) добавляют 0,025 мл эликсина морской свинки Mericux, разбавленHord в соотношении 1/100 на тампоне Майера, и 0,025 мл сыворотки, раз13Sбавленной в соотношении 2:2. Пластинки помещают на 1 ч в сушильный шкаф при ЗУС, после этого на 2 ч при С и проводят расчет при помощи оптических приспособлений. Гемолитический показатель определяют для наиболее сильного разбавления сыворотки, при котором еще происходит полное растворение осадка эритроцитов крови барана. Этот показатель определяют таким же способом, что и показатель степени гемагглютинации. Обработка результатов. Вычисляют средние значения индивидуальных показателей(± стандартное отклонение), а также показатели объединенной сыворотки для каждой группы в зависимости от времени взятия пробы. Функциональные изменения для группы, не подвергнутой специальной обработке, определяют из оценки разности средних показателей и разности показателей по группам. При расчетах используют билатеральное т -распределение Стьюдента или метод х в тех случаях, когда метод Стьюдента не может применяться. Изучение пороговых явлений. Изучено большое количество различных доз эритроцитов крови барана для нахождения порогового значения гуморального ответа у мышей швейцарской породы и для обнаружения сверхпорогового эффекта. 10 эритроцитов дают возможность для изучения кинетики в имевшихся условиях проведения эксперимента. Кинетические изучения ответа у контрольных животных. Изучены несколько групп животных, иммунизированных введением 10 эритроцитов. Показатели гемагглютинации. Появление антител-гемагглютинантов наблюдают у некоторых групп животных на -е сут после иммунизации, э У некоторых только на сут, при этом результаты, имеющие сильный разброс на -е сут, имеют тенденцию к сближению на 11-е сут. Показатели при этом не превышают k.
Показатели гемолиза.
Появление гемолитических антител практически не наблюдается до .сут результаты имеют тенденцию к сближению в более поздней стадии проведения эксперимента.
Изучение, сравнительного иммуностимулятора.
внедрение меченного предшествующего вещества.
Эталонные условия.
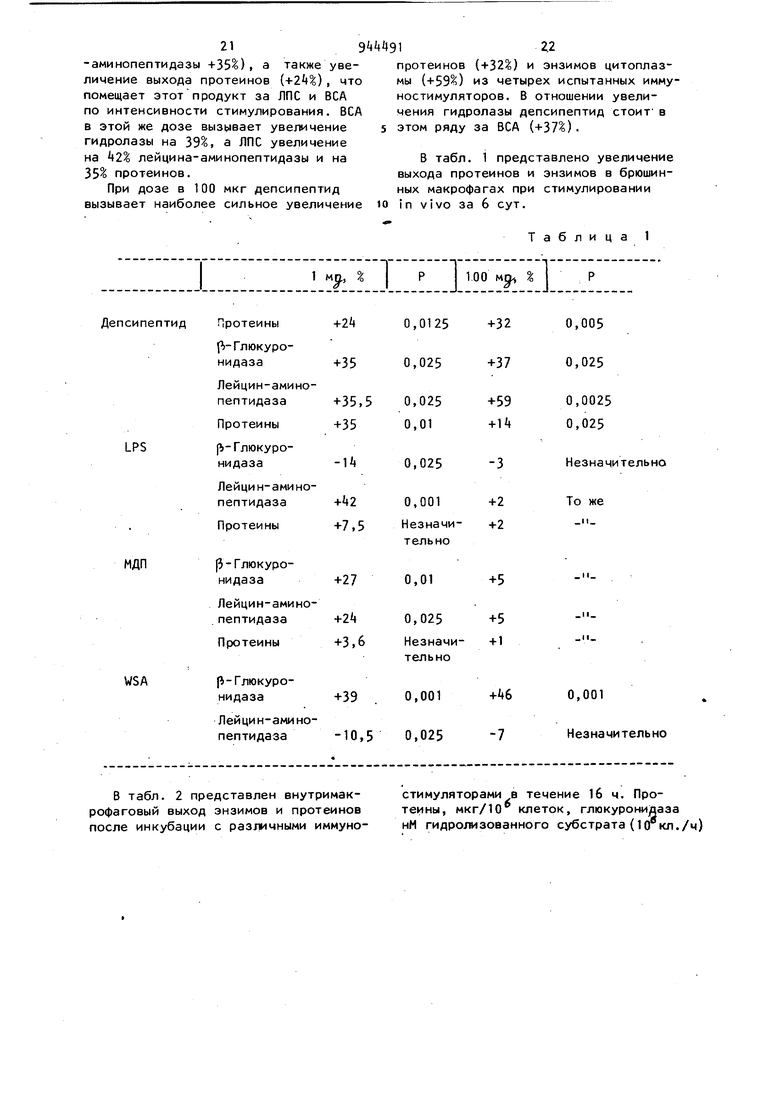
Определение оптимальной дозы митогена производят из кривых зависит, мостей эффект/доза для начала наступления платоактивности на этих кривых. Концентрации митогена, при которых достигается наибольший стимулирующий эффект при условиях проведения испытаний, следующие, мкг/мл: фитогемаглютинин в растворе 100 мкг/мл физиологической сыворотки (ПГА) 1; липопоIВведение культуры Corynebacterium parvum на 3-6-й день иммунизации способствует проявлению иммунного эффекта. Изучение предварительной фазы сверхпорогового эффекта (4-е сут) позволяет обнаружить образование гемолитических и гемагглютинантных антител у животных, подвергавшихся воздействию стимулятора. Наблюдения на более поздней стадии ( сут) подтверждают полученные результаты. Разброс результатов объясняется гетерогенностью использованного при опытах швейцарского штамма. Изучение активности предлагаемого депсипептида. Депсипептид, введенный в течение 3 сут, с 3-х по 6-е сутки до проведения иммунизации, вызывает увеличение количества гемагглютинирующих и гемолитических антител, а также появление гемолитических антител на Ц-е сутки иммунного испытания, при этом дозы в 10 ив 50 мкг/день на мышь дают аналогичные результаты. Стимулирование, полученное при применении депсипептида в предлагаемых условиях аналогично стимулированию, достигаемому, при применении культуры G. parvum внутрибрюшинно в дозах 500 мкг/день на мышь с точки зрения кинетики протекания процесса. При этом сравнимый эффект получают при применении депсипептида в активных дозах, меньших в 10-50 раз. Изучение лимфобласттрансформации. При ТТЛ-дозировании дипсепептида воспроизводят условия 2j в отношении оптимальной концентрации метогена, при этом испытуемый продукт остается в контакте в течение всего времени превращения, при этом происходит наиболее полное и воспроизводимое внедрение предшествующего вещества, а биологический эффект продукта может быть представлен через ингибирование Э лисахарид культуры Escherichia Со Ii 026 б растворе в концентрации 1 мкг/мл в физиологической сыворотке (ЛПС) 5- Лимфоциты, превращаемый ПГА представляют собой только клетки Т, а ЛПС концентрируется только в клетках В. Кинетические исследования позволяют определить наступление максимальной стимулирующей акти ности ПГА на 66-й ч, а ЛПС на 8-й При указанной дозировке ПГА предста ляет собой лучший митоген, внедрени в этом случае в два раза большее, чем в случае ЛПС, а результаты, пол ченные с его использованием, более воспроизводимы. Из полученных резул татов следует, что экстракт депсипе тида Fusarium eguiseti не является митогенным агентом и ингибирует внед рение тритий-замещенного тимидина, вызываемое митогенными агентами. Изучение иммунного эффекта депсипептида. Стимулирующее или тормозящее воздействие указанного препарата изучено по отношению к гуморальному и клеточному эффекту. Гуморальный эффект изучают при введении ЛПС, который вызывает увеличение клеток в спинномозговом веществе. Клеточный эффект изучают при введении оксазолона. Эффект, вызываемый этим продуктом , сосредоточен преимущественно е клетках. Изучение клеток, продуцирующих антитрла. Количество клеток, продуцирующих антитела,в колонии лимфоцитов, определяют количественно посредством изу чения гемолитических пластинок в полужидкой среде, содержащей меченые эритроциты. Эксперимент проводят с использованием прямых гемолитических пластинок, и отмечаются клетки, продуцирующие IQ.M. в чашку Петри, содержащую слой 3 -ного агара, вливают второй агаровый слой (0,6), содержащий 110 лимфоцитов и эритроцитов, объединенных на 30. Полученную среду выдерживают 1 ч при 37 С, после чего в нее добавляют алексин морских свинок 1/10 и вновь оставляют на час при 37° С. Изучение гемолитических пластинок проводят с применением бинокулярной лупы и результаты выражают в расчете на 10 лимфоцитов или на орган. Мечеными считаются эритроциты крови барана, чувствительные одно16временно по отношению к оксазалону и к ЛПС. Иммуно-цитохимическое изучение клеточных суспензий, розеток и клеток, продуцирующих антител. Изучение общего лимфоцитоза в лимфатическом узле в селезенке. Для авторадиографического изучения клеточные суспензии выдерживают 30 мин при 37 С с тритий-замещенными тимидином с дозой излучения 20 мкюри/мл, после чего их подвергают обработке для определения поверхностного имуноглобулина. Клетки наносят на глютаральдегид, обрабатывают диаминобензидином, согласно способу Грэхома и Карновски, (1966), для обнаружения пероксидазы, после чего обрабатывают осмиевой кислотой и заключают в пластмассу (эпон). Результаты. Изучение иммунного ответа с использованием оксазалона. Изучение числа клеток. На 5 день увеличение числа клеток превышает 50%, при этом наиболее важные результаты наблюдают при внутрибрюшинном введении. На 9 день увеличение количества клеток становится менее заметным. Количество клеток, содержащих тритий-замещенный тимидин, сравнимо у контрольных животных и у животных, прошедших обработку и составляет величину порядка -6 на 100. Изучение числа клеток, узнающих антиген. На 5 день наблюдается очень сильное увеличение числа клеток, узнающих антиген (257 на 100), приводящее-одновременно к увеличению числа клеток в лимфатическом узле и увеличению количества клеток, узнающих антиген, из расчета на 10 клеток. Эти изменения не наблюдают на 9 день. Изучение количества клеток, образующих гемолитические пластинки. Заметное увеличение числа, клеток, образующих гемолитические пластинки, на 5 день приводит к росту числа клеток, в то время как на 9 день увеличивается количество клеток, образующих гемолитические пластинки из расчета на 10 клеток. Изучени.е количеств антител. На 5 день количество антител остается постоянным, однако на 9 день количество гемагглютинантных и гемолитических антител увеличивается, в особенности- это касается гемолитических антител. Изучение числа клеток на 1 г поверхности . Количество клеток на 1 г поверхности рассчитывают на полутонких сре зах для начальной клеточной суспензии , при этом процентное отношение у контрольных животных и у животных, прошедших обработку, составляет 35 на 100. Иммуноцитологическое исследование под электронным микроскопом. Природа клеток, образующих розетки и пластинки одна и та же у контрольных животных, и у животных, прошедших обработку. Речь идет о розетках лимфоцитов на 1 г поверхности и клетках Т, которые на девятый день имеются в количестве 0-50 на 100, 8случае гемолитических пластинок речь идет о плазмоцитах. Изучение иммунного ответа на ЛПС. Изучение количества клеток. Отмечают заметное увеличение на 9день в случае депсипептида. Изучение числа клеток, узнающих антиген. Воздействие не наблюдается, или ж вызывает уменьшение в том случае, когда результаты рассчитываются на 10клеток -или на орган. Указанное уменьшение становится особенно замет ным на 9 день. Изучение числа клеток, образующих гемолитические пластинки. Полученные результаты не позволяю говорить о наличии какого-либо действия в сторону уменьшения или увели чения . Изучение количества антител. Наблюдает.ся тенденция к уменьшению количества гемагглютинантных ант тел, в то время как количество гемолитических антител имеет тенденцию.к заметному увеличению на 5 день. Иммуноцитологическое исследование под электронным микроскопом. . Клетки, образующие розетки, и кле ки, образующие пластинки, как в случае контрольных животных, так и в слу чае животных, прошедших обработку, в основном представляют собой плазмоци ты. В этом случае наблюдают количест во лимфоцитов на 1 г поверхности (в случае розеток). Среди иммуноцитов н наблюдается Т клеток. Депсипептид действует следующим образом. Ответ на оксазалон стимулируется. Заметное увеличение числа клеток в лимфатических узлах, достигает максимума на 5 день (50-80 на 100). Количество клеток, узнающих антиген, увеличивается во всех случаях. Увеличение числа антител всегда незначительно, в особенности на 9 день. Ответ на ЛПС может быть скорее тормозящим. Увеличение числа клеток в селезенке не наблюдается, число клеток, узнающих антиген, не изменяется или же скорее уменьшается, изменение числа клеток, образующих пластинки, является слишком случайным, а число антител либо уменьшается (гемагглютинантные антитела), либо остается неизменным (гемолитические антитела) . Влияние депсипептида на имунный ответ. Материал. Депсипептид переводят в раствор из расчета 100 мкг на 50 мл физиологического раствора для тех опытов, где максимальная концентрация 2 мкг/мл. В случае использования больших концентраций применяют суспензии, полученные перемешиванием 3 ч при комнатной температуре. Животные. Гуморальная иммунная способность - мыши-самцы С 57 В 6, лимфобласттрансформация - мыши СВА, самцы, активация макрофага + крысы ФИШЕР/1 со, самки. Антиген. Очищенный (фракция по Кону) бычий серумальбумин Армор фармацевтикал Компани (Чикаго). Каждой мыши вводят 300 мкг этого антигена в задние подошвенные подушечки. Вспомогательные средства. Добавки для сравнения Difco - полная добавка по Фрейнду, неполная добавка поФрейнду. Депсипептид применяют из расчета 10 мкг на мышь для испытания гуморальной иммунной способности, в день О и 5мг на мышь для вызывания иммунизации . Методы. Иммунизация. День 0. Иммунизация 20 мышей по 10 мкг/мышь депсипептида. При этом каждая мышь получает 0,2 мл смеси, состоящей из двух объемов фосфатной вытяжки БСА и депсипептида и трех объемов неполного реактива ло Фрейнду.Десять мышей получают ту же смесь, но без депсипептида, и десять мышей получают антиген с полным реактивом по Фрейнду. День 21. Паловину мышей каждой серии умертвляют для измерения количест19ва антител, действующих против БСА посредством пассивной гемагглютинации. Второй половине животных делаю инъекцию для вызывания эффекта в ви половинной от первоначальной дозы (0,1 мл вместо 0,2 мл). День 35. Умертвляют оставшихся м шей для определения пассивной гемаг глютинации и определения таким способом числа антител, специфических отношению к БСА. Исследования клеток. Митогенная способность депсипепти да. 0, селезеночных лимфоцитов мышей СВА в 0,1 мл РПМИ помещают на культуру на 3 дня при при содержании COg. с различными концентрациями депсипептида. Группам мышей вводят ПГА при разбавлении (1/200, Соп А в дозе 10 мкг/мл вЛПС в дозе 100 мкг/мл, 4 ч спустя после выдержи вания к каждой культуре добавляют 1 мкюри тритий-замещенного тимидина В конечной фазе выдерживания клетки фильтруют через фильтр Whatman GF/C и дважды промывают 10 мл физиологического раствора. Третий-замещенный тимидин, фиксированный на АДН остается на фильтре и изучается его радиоактивность с помощью счетчика fb-излучения. Показатель превращения определяют как отношение тимидина, входящего в присутствии изучаемого соединения, к тимидину, входящему в лимфоциты в отсутствии какого-либо ми то гена., Макрофаговая стимуляция. Брюшинные макрофаги не стимулированных крыс Фишера, взятые при промы вании брюшной полости и изолированные на культуре, нанесенной на пласт массу NUNCLON, культивируют в течени ночи совместно с дозами депсипептида лежащими в пределах от 1 пг до 1 нг на 1 мл. Затем определяют содержание протеинов с выходом лизo-fi-глюкopoни дазы и лейцинаминопептидезы цитоплаз мы в клетках, растворимых в 0,05 Triton Х-100. ЛПС культуры Escherichia и мурамилдипепсид (МДП) является сравнительными эталонами. Потенцирующее воздействие на не специфическую клеточную иммунность. Лимфоциты: митогенная способность В то время как по отношению к селезеночным лимфоцитам мышей фитогемагглютинин (ФГА) при обычном разбавлении 1/200, и конкавалин А(КонА при дозе 10 мкг/мл дают показатель 120 превращения около 50, а ЛПС культуры Escherichia при дозе 100 мкг/мл имеет показатель И,8, предлагаемый депсипептид ингибирует внедрение тритийзамещенного тимидина (что соответствует показателю менее 1,0) при всех испытанных концентрациях (от 0,1 пг до 100 мг/мл). Подобное ингибирование ядерного метаболизма при применении очень малых доз депсипептида служит признаком очень большой активности указанного продукта в механизме, в котором принимают участие уничтоженные клетки или даже по отношению к модификации метаболизма и к клеточной проницаемости. Депсипептид сам по себе не является митогеном и этот стимулирующий по отношению к лимфоцитам эффект не может быть предположен на основании представлений о классических митогенах. Активирование макрофагов. Зп V i tro. Энзиматическое дозирование: депси-пептид вызывает значительное увеличение макрофаговой гидролазы при дозе от 1 пг до 10 нг/мл. Выход протеина значительно увеличивается при дозе 10-100 мг/r-tn. Начиная с дозы в 100 нг/мл, депсипептид становится токсичным, на что указывает падение выхода протеинов и внутриклеточных экзимов макрофага, наблюдаемое при дозе, равной или превышающей данную концентрацию. On V iVO Депсипептид заметно стимулирует метаболизм макрофагов. on vivo за 6 дней до промывания брюиины животных делают инъекцию депсипептида при дозе 1-100 мкг внутрибрюшинно, в виде раствора в 1 мл физиологического раствора ЛПС, МДП, ВСА служат эталоном. Клетки, отобранные в результате брюшинного промывания, выдерживают 2ч для удаления несросшихся клеток, а популяцию сросшихся клеток, состоящую на 30% из макрофага, дополнительно культивируются еще ч. При этом клетки растворяют и определяют выход протеинов и энзимов при дозах, приведенных для изучения in vitro. Dn vivo энзиматическое дозирование: при дозе 1 мкг депсипептид вызывает увеличение лизоэнзимов (при испытаниях на р-глюкуронидазе +35%) и цитоплазмическое (так. для лейцин-аминопептидазы +35), а также увеличение выхода протеинов (), что помещает этот продукт за ЛПС и ВСА по интенсивности стимулирования. ВСА в этой же дозе вызывает увеличение гидролазы на 39, а ЛПС увеличение на 42% лейцина-аминопептидазы и на 35 протеинов.
При дозе в 100 мкг депсипептид вызывает наиболее сильное увеличение
протеинов (+32) и энзимов цитоплазмы (+59) из четырех испытанных иммуностимуляторов. В отношении увеличения гидролазы депсипептид стоит в этом ряду за ВСА (+37%)
В табл. i представлено увеличение выхода протеинов и энзимов в брюшинных макрофагах при стимулировании in vivo за 6 сут.













| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L., продуцирующий моноклональные антитела к бактериям рода BRUceLLa | 1988 |
|
SU1604849A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L. - продуцент моноклональных антител к бактериям рода BRUceLLa | 1988 |
|
SU1604848A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L. - продуцент моноклональных антител к бактериям рода BRUceLLa | 1990 |
|
SU1752764A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L. - продуцент моноклональных антител к холерному энтеротоксину биотипа эльтор | 1990 |
|
SU1742325A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS - продуцент моноклональных антител к Са @ /MG @ - зависимой эндонуклеазе клеточных ядер лимфоцитов селезенки человека | 1987 |
|
SU1497214A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS - продуцент моноклональных антител к Са @ /М @ - зависимой эндонуклеазе клеточных ядер лимфоцитов селезенки человека | 1987 |
|
SU1497213A1 |
| ИММУНОМОДУЛЯТОР | 1993 |
|
RU2108100C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНЫХ Mus. musculus L - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К О-АНТИГЕНУ ХОЛЕРНЫХ ВИБРИОНОВ О1 СЕРОГРУППЫ | 2010 |
|
RU2425874C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ФЕТАЛЬНЫЙ ГЕМОГЛОБИН И БАКТЕРИАЛЬНЫЙ ЭНДОТОКСИН И, НЕОБЯЗАТЕЛЬНО, ДОПОЛНИТЕЛЬНЫЕ КОМПОНЕНТЫ ПЕЧЕНИ ПЛОДА | 2004 |
|
RU2366449C2 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ MUS MUSCULUS L. - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К ПРЕПАРАТУ БЕЛКОВ БРУЦЕЛЛ С МОЛЕКУЛЯРНЫМ ВЕСОМ 18 И 38 КД | 1996 |
|
RU2113475C1 |

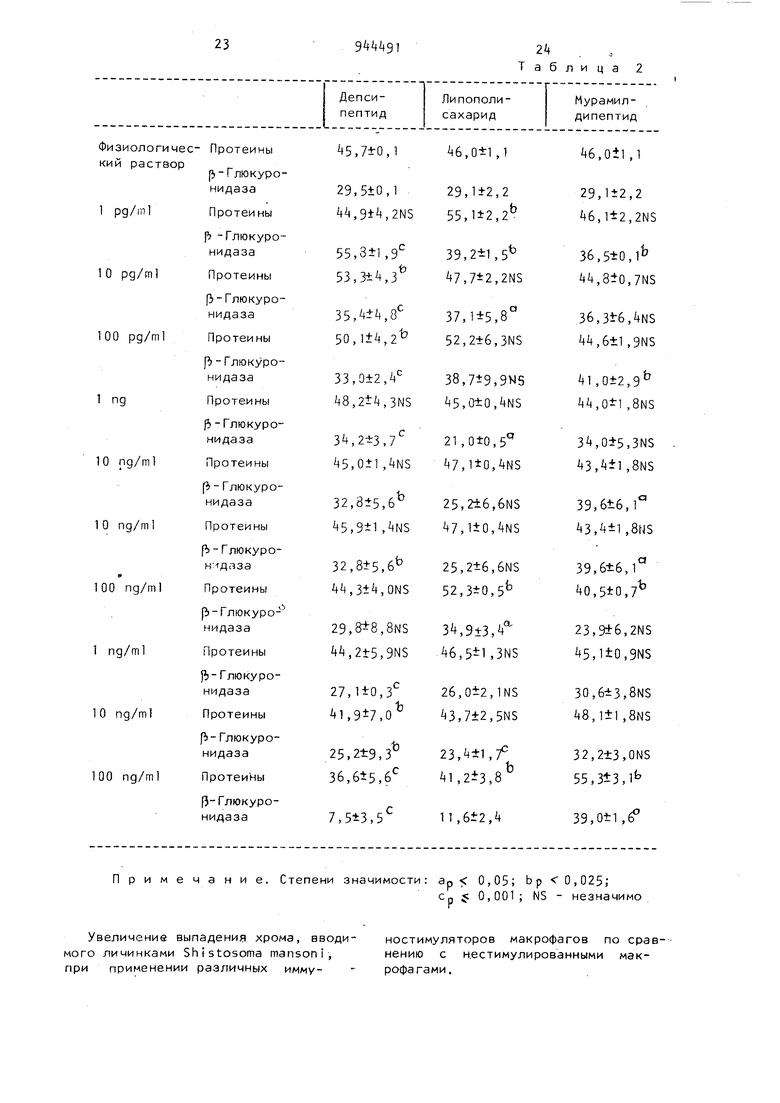
В табл. 2 представлен внутримакрофаговый выход энзимов и протеинов после инкубации с различными иммуностимуляторами в течение 16 ч. Протеины, мкг/10 клеток, глюкуронидаза нМ гидролизованного субстрата(1 (гкл./ч)
23 Примечание. Степени значимости:
Увеличение выпадения хрома, вводимого личинками Shistosofna mansoni, при применении различных иммуЭ + Э
Таблица 2
ностимуляторов макрофагов по сравнению с кестимулированными макрофагами. ар 0,05; Ьр 0,025; Ср {: 0,001; NS - незначимо Цитотоксическая способность: депсипептид исследован в отношении его воздействия in vivo на цитотоксичность брюшинных макрофагов крыс в отношении личинок Shistosoma mansoni. Клетки, стимулированные in vitro или in vivo, помещают вместе с личинками Shistosoma mansoni мечеными хромом-5 для обнаружения возможной цитотоксиВещества
Депсипептид +0,5(незначительно) ЛПС
МДПВСА
Депсипептид вызывает лишь незначительное увеличение выпадения хрома-51, являющегося радиактивной меткой для шистосомул, в той же степени, что и МДП, в то время как ЛПС и ВСА дают макрофаги, значительно более токсичные по отношению к личинкам, по сравнению с- макрофагами животных, которые существуют только в физиологическом растворе. Таким образом, дeпcипептид не обладает воздействием in vivo на макрофаги,если испытания проводятся по отношению к шистосомам, меченым хромом-51. 19,67.13,1 I8,21t3,9 2i, 2,k Изучение влияния циклодепсипептида на время выживания мышей, зараженных 55 лейкемией Л1210. Циклодепсипептид представляет Собой иммуностимулятор in vivo по от+15 (незначительно) +10(незначительно)
(р 0,005) +10 (незначительно)
льно) +30% (р 0,025)
Питотоксическая способность. Только ЛПС Е.соП, кроме депсипептида, не вызывает in vitro значительного увеличения цитотоксичности макрофагов по отношению к шистосомулам, меченым хромом-51. Стимулирующие дозы депсипептида вызывают только небольшое увеличение содержания радиоактивной метки.
Общее количество хрома, обнаруженное в шистосомулах, инкубированных в течение 16 ч с нормальными стимулированными в течение 2 ч макрофагами , и с различными дозами депсипептида представлены в табл. i.
Таблица ческой способности, измеряемой количеством хрома, выпадающего в культуральную среду вследствие поражения клеток на поверхности шистосомул. Для этого измеряют радиоактивность питательной среды в процентах от общей радиоактивности, имевшейся в начале опыта. Результаты представлены в табл. 3, Таблица 3 100 мкг 21,71±3,5 23.k(±2,7 ношению к макрофагам, также как и БЦГ. Представляется интересным сравнить оба этих вещества. В качестве модели используют мыши, зараженные лейкемией Л1210 и прошедшие предва27рительную обработку циьспофосфамидом для того, чтобы иметь возможность оценить влияние обоих этих веществ на остаточное заболевание. Материалы и методы. В качестве животных используют мыши БДФ в возрасте около недель {CSEAL-Орлеан). Животные, проходят обработку согласно способу13 В день О всем животным делают инъек ции IV по 10 живущих клеток с лейкомией Л1210. В день 1 проводят рас пределение животных на четыре группы по 10 животных, делают инъекцию физиологической сыворотки (внутрибрюшинно), а животным остальных трех групп вводят внутрибрюшинно циклофос фамид в дооптимальной дозе 80 мг/кг Животные, прошедшие обработку циклофосфамидом, далее подвергаются обработке. На 6-й день животные одной из групп, прошедших обработку циклоЦиклофосфамид в дозе, меньшей оптимальной, заметно увеличивает срок выживания животных по сравнению с животными контрольной группы, не про шедшими обработки. Комбинация циклофосфамид-БЦГ дает только статически незначимое увеличение продолжительности выживания животных, а то время как комбинация циклофосфамид-депсипе тид вызывает статистически значимое увеличение времени выживания животных, прошедших обработку. Вследствие этого нельзя отметить какую-либо существенную разницу между двумя типами терапевтических комбинаций: цикло фосфамид-БЦГ и циклофосфамид-депсипептид, Депсипептид увеличивает выживаемость у мышей, которым предварительн 128 фосфамидом, получают инъекцию iV 0,1 мл физиологической сыворотки. Они служат в качестве эталона при изучении выживания мышей, обработанных циклофосфамидом. Животные группы БЦГ получают инъекцию IV по 1 мг/мышь БЦГ из Института Пастера в объеме 1 мл. Они служат в качестве контрольных при изучении активной иммунотерапии после введения циклофосфамида, в этих условиях БЦГ является активным. Животным одной из групп проводят инъекцию депсипептида по 50 мкг/мышь внутрибрюшинно в объеме 0,5 мл. Они служат в качестве образца для .изучениявыживания мышей, прошедших обработку продуктом по предлагаемому способу. Результаты. Результаты опытов приведены в табл. 5Таблица 5 ВВОДЯТ по 10 клеток Л1210 и которые проходят обработку циклофосфамидом. Результаты, полученные при применении депсипептида, аналогичны результатам, полученным с БЦГ. Однако опыты проводят на группах, содержащих тольг .ко по 10 животных, что не дает возможности установить статистически значимые с точки зрения статистического анализа различия. Значимость различий между различными группами исследовалось с применением т -распредепения Стьюдента: А -В р 0,02; В - С незначимое; В - D р « 0,06; С - О незначимое. Влияние депсипептида на пролиферацию лимфоцитов и макрофагов. Для исследования in vitro пролиферации лимфоцитов под воздействием митогенов Т используют способ,описан ный Дж. В. Хадденом и сотрудниками. Тот же способ используют для изучения пролиферации макрофагов и актива ции макрофагов в отношении их способ ности к разрушению клеток. В этих испытаниях используют лимфоциты человека, взятые из крови, отобранной в периферической кровеносной системе. Пролиферация лимфоцитов под воздействием фитогемагглютинина определяют в зависимости от степени внедрения тритий-замещенного тимидина. Депсипептид Fusarium eguis ti изучают в присутствии дооптимальных, оптимальных и сверхоптимальных количеств фитогемагглютинина, что соответствует 0,001, 0,01 и 0,1 ед/м соответственно. Пролиферация лимфоци тов, вызываемая лимфокином (ММФ) определяют по степени внедрения тритий замещенного тимидина, спустя 3 и 5дней культивации. Активирование способности макрофагов к лизису клеток Lister а вызываемая лимфокином (МАФ), спустя 5 дней культивирования в присутствии или в отсутствии МАФ изучают при периоде контакта, равном 6ч (Haddeu Dmmunopharmacology, с. , 1977). Степень фагоцитоза определяют после 20 мин контакта с клетками Lister а monocytogenes. При этом подсчитывают количество мак рофагов, содержащих бактерии,и количество бактерий в клетке макрофага. Бактерицидную активность макрофагов определяют в зависимости от числа клеток, содержащих бактерии и от чис ла бактерий в каждой клетке, спустя. 6 ч после 20-МИН контакта. Депсипептид используют в дозах 5 мкг. При этом установлено, что депсипепти в широком диапазоне концентраций (510 - 0,5 мкг) увеличивает внедрение тритий-замещенного тимидина в стимулируемые лейкоциты как при- оптимальных дозах фитогемагглютинина, так и при дозах, меньших оптимальной Более высокие дозы, напротив, весьма значительно уменьшают внедрение тритий-замещенного тимидина, проявляя тем самым цитостатическое воздействие продукта. Аналогичный эффект получен с применением лейкемических. клеток человека и макрофагов, активированных оптимальной дозой ММФ. Определение острой токсичности. Среднюю летальную дозу депсипепти да определяют на группах, состоящих S I из 1 о гетероксенных мышей породы СД или на группах крыс породы Вистар, которым вводят испытуемый продукт либо в виде суспензии в водном растворителе, либо в виде раствора в изо-пропилмиристате. Продукт вводят либо перорально, либо внутрибрюшинно, либо внутривенно в постепенно увеличиваемых дозах. За животными наблюдают в течение 8 дней и ведут при этом подсчет умерших животных. Среднюю летальную дозу определяют графически согласно методу Литчфилда и Уилкинсона. При этом получены следующие результаты. Водная суспензия. У мышей внутрикостно ЛД-50 5000 мг/кг, внутрибрюшинно ЛД 67 мг/кг, внутривенно ЛД-50 17 мг/кг, у крыс: внутрикостно ЛД-50 5000 мг/кг, внутрибрюшинно ЛД-50 67 мг/кг, внутривенно ЛД-50.11 мг/кг, В растворе изо-пропилмиристата. У мышей при внутрибрюшинном введении: для самок ЛД-50 182 мг/кг, у самцов ЛД-50 1б9 мг/кг. При внутривенном введении: для самцов ЛД-50 +1 мг/кг, для самок ЛД-50 1 мг/кг. При применении в растворе изо-прот пилмиристата циклодепсипептид обладает значительно пониженной токсичностью. Формула изобретения Способ получения биологически активного вещества, обладающего иммуностимулирующим действием, путем культивирования штамма продуцента в питательной среде с последующим отделением мицелия, экстракцией его органическим растворителем, повторной экстракцией, отделением экстракта и очисткой целевого продукта, о т л и чающийся тем, что, с целью повышения иммуностимулирующей активности, в качестве продуцента используют штамм Fusarium eguiseti (Corda) Saccardo H° 213107, культивирование проводят при и рН среды 5,+-6,5 в три последовательные стадии продолжительиостью ч, мицелий многоступенчато экстрагируют трихлорэтиленом из расчета 1-9 объемов трихлорэтилена к объему мице/ 1я, полученные экстракты объединяют, выпаривают при пониженном давлении, полученный осадок обрабатывают гексаном и повторную экстракцию проводят 20%-ным водным раствором метанола.
31Э Э 32
Источники информации,2.Дэникл Р. П. иХолиан С.К. Proceed
принятые во внимание при экспертизе Nat. Dead. Sc i (USA) 73, 1976,3599.

Авторы
Даты
1982-07-15—Публикация
1978-11-30—Подача