где R и R имеют указанные значения подвергают взаимодействию с 3-аминопропантиолом в среде инертного растворителя при нагревании с последующе переэтерификацией при необходимости и заменой одного значения Rна другое, и целевой продукт вьщеляют в свободном виде или в виде кислотноаддитивной соли. Пример 1. 2-Метил-З-циано- 2-тиенил)акрилат. Раствор пиперидина (1,0 мл в диоксане 10,0 мл) добавляют осторожно к перемешанному раствору 2-тиофен-карбоксальдегида (33,65 г, 0,3 моль) и метилцианоацетата (29,7 г, 0,3 моль) в диоксане (40 мл), После отстаивания в течение 12 i при комнатной температуре получают кристаллический осадок, ког торый фильтруют, промывают холодным диоксаном и сушат в вакууме. Выход 49,3 г (85% от теоретического), т.плЛ04--106с. Вычислено,: С 59,9; Н 3,7; N 7, С 1Ц.Ю.,5 Найдено, % : С 56,1; Н 3,8; N 7, Примеры 2-4. Аналогично примеру 1 получают следующие соединения : 2-Этил-3 циано-(2-тиенил)акрилат выход 76%, т.пл . 94-95 С, Вычислено.%: С 57,9; К 4,4; N 6, Найдено,. % : С 57,6; Н 4,3; N 6, 2%, т.пл.114-115 С, i : С 61,2; Н 5,6; . 5, t;,,ll,, Найдено, % : С 61,2; Н 5,4; N 5, 2-Метил-3-циано(З-метилтиен-2-ил акриллт, выход 92%, т.пл.135-136°С. Вычислено,%: С 57,9; Н 4.4; N6, CJUXO.S Найдено, % : С 57 , 9 Н 4 , 3 N6, При г-л ер 5 . 2-;1етил-3-циано - ;2-т;-енил) пропионат . 2-Метил- 3-циа1-ю- (2-тиенил) акрила (29 г., 0,15 моль) подвергают раство ремию в 300 Nti смеси, состоящей из метанола и воды в объемном соотноше НИИ . К 1 полученному раствору добавляют 3 капли молярного водного раствора Г 1/4роокиси натрия с последующим ДО7 бавлением боргидрида натрия (1,8 г, 0,048 моль) и полученную таким обра3o i суспензию перемешивают в течение 12 ч при комнатной температуре. Реа ционную смесь далее нейтрализуют с HcnoirbSOBaHnervi молярного водного ра тлора уксусной кислоты и летучие ком покенты выпариваю при по - иженном давлении, Остаток подвергают суспен дированию в воде и затем экстрагиру ют толуолом. Полугенный экстракт сушат с помогдьо с :ульс,ата натрия и толуол подвергают выпариванию в вакууме с получением в результате продукта-сырца, который очищают путем дистилляции с получением 10,6 г продукта (36% от теоретического), т,кип.172с при 12 мм рт.ст. Вычислено,%: С 55,4; Н 4,6;N 7,2 CgH-NOiS Найдено, % : С 55,4; Н 4,8;N 7,0. Примеры 6и7. Аналогично примерку 5 получают следующие соединения : 2-Этил-З-циано-(2-тиенил)пропионат, выход 52% от теоретического, т.кип.112-114с при 0,25 мм рт.ст. Вычислено, % : С 57,4; Н 5,3; N6,7 . Найдено, % : С 57,7; Н 5, 6,6. 2-Трет-бутил-З-циано-(2-тиенил)пропионат, выход 81% от теоретического, продукт представляет собой масло. Пример 8. 2-Метил-З-циано-(З-метилдиен-2-ил)пропионат. 2-Метил-З-циано-(З-метилтиен-2-ил)акрилат (75,0 г, 0,36 моль) подвергают суспендированию в 1 л метанола и гидрогенизации в четырех порциях в установке Парра при 50 С и давлении 4,23 атм с использованием 0,25 г катализатора - 10% палладия на актив рованном угле на каждую из порций. В результате дистилляции продукта, оставшегося после удаления катализатора и растворителя, получают чистое соединение в виде масла палево-желтого цвета в количестве 70,4 г (93% от теоретического),т - кип.119 С при о,5 мм рт.ст . Вычислено,%: С 57,4; Н 5,3;N 6,7 C,H,5 OaSa Найдено, % : С 51,5; Н 5,5;N 6,7. Пример 9. 2-Метил-(5 , 6-диГИДРО-4К-1,3-тиазин-2-ил)-3-(2-тиенил) пропионат . Суспензию 3-аминопропантиол гидрохлорида (4,7 г, 0,037 моль) в метиленхлориде (150 лл) , содержащую 2-метил-З-циано-(2-тиенил)пропионат 6,5 г, 0,033 моль) и триэтиламин 3,7 г, 0,037 моль) подвергают перемешиванию при температуре дефлегмирования в атмосфере азота в течение 17 ч. После фильтрации реакционной смеси растворитель выпаривают при пониженном давлении с образованием в результате маслообразного остатка, который подвергают суспендированию в воде и далее экстрагируют с помощью простого эфира. Экстракт простого эфира сушат с помощью сульфата натрия, далее простой эфир выпаривают и остаток подвергают дистилляции при пониженном давлении с получением в результате целевого продукта, представляющего собой жидкость палено-желтого цвета. Выход 3,4 г (38% от теоретического), T.KHn. .при 0,4 мм рт.ст. Вычислено,%: С 53,5; Н 5,6;N 5,2 C a ffiNO Sa. , % : СГ 53,8; Н 5,6;N 4,8 П ри м е р ы 10-12. Аналогично примеру 9 получают следующие соединения:, 2-Этил-З- (5 ,6- ДИГИДРО-4Н-1, 3-тиазин-2-ил)-(2-тиенил)пропионат, выход 8%, т.кип.144-154С при .0 , 2 мм рт. ст. Вычислено,%: С 55,1; Н 6,1;N 4,9 C,,.7NOi,Si Найдено, % : С 55,5; Н 6,1;N 5,2 . 2-Трет-бутил-З-(5,6-дигидро-4Н-1,З-тиазин-2-ил)-(2-тиенил)пропионат, масло, выход 38% от теоретического . Вычислено,%: С 57,8; Н 6,8;N 4,5 .O,S 2. Найдено, % : С 58,1; Н 6,3;N 4,5 2-Метил-З-(5,6-дигидро-4Н-1,3-тиазин-2-ил)-(3-метил-тиен-2-ил)про пионат, выход 48% от теоретического т.кип. 1бЗ-1б4с при 0,4 мм рт.ст. Вычислено,%: С 55,1; Н 6,1;N 4,9 Qi -17 02 Si Найдено у % : С 55,8; Н 6,4 ; N 5,2 Пример 13. 2-Н.-пропил-3(5,6-ДИГИДРО-4Н-1,З-тиазин-2-ил)(2-тиенил)пропионат. Калий в количестве 0,1 г растворя ют ц н.-пропаноле (6,0 г), а далее разбавляют безводным толуолом в коли честве 75 мл. К полученному раствору добавляют 2-метил-З-(5,6-дкгидpo-4H-, З-тиаэин-2-ил)-(2-тиенил)пропи онат в количестве 5,4 г (0,02 моль) полученный как в примере 9, и 30 г молекулярного сита 4А , которое пред варительно выдерживают при . Полученную таким образом суспензию интенсивно перемешивают при температуре- дефлегмирования в течение 16 ч После удаления молекулярного сита компоненты растворителя выпаривают при пониженном давлении. Полученный остаток подвергают хроматографированию на колонке, заполненной силикагелем с использованием простого диэтилового эфира в качестве элюента с получением целевого продукта в виде масла, выход 1,8 г (30% от теоретического) . Вычислено,%: С 56,5; Н 6,4;N 4,7 Найдено, % : С 56,8; Н 6,6;N 4,8 Примеры 14 и 15. Аналогич но примеру 13 получают следующие соединения: 2-Н.-бутил-3- С5.6-д Гидро-4Н-1,3 -тиазин-2-ил)- (2-тиенил)пропионат, выход32% от теоретического,продукт представляют собой масло. Вычислено,%: С 57,8; Н 6,8;N 4,5 С,,И XO.S Найдено, % : С58,1; Н 6,8;N 4,7 2-Циклопропилметил-3-(5,б-дигидро-4Н-1,З-тиазин-2-ил)-(2-тиенил)пропионат, выход 48% от теоретического, продукт представляет собой масло. Вычислено,%: С 58,2; Н 6,2;N 4,5 Найдено, % : С 58,1; Н 6,2;N 4,5. Пример 16. 2-Метил-З-циано-(2-фурил)акрилат. Раствор пиперидина (1,0 мл) в диокеане (10,0 мп) добавляют осторожно к перемешанному раствору фурфурола (28,8 г, 0,3 моль) в диоксане (40 мл) После перемешивания при комнатной температуре в течение 12 ч реакционкую смесь разбавляют водой (100 мл) и экстрагируют толуолом. Полученный таким образом экстракт сушат безводным сульфатом натрия и толуол выпаривают в вакууме с получением в результате продукта-сырца в виде красного твердого вещества. Продукт-сырец кристаллизуют из смеси толуолгексан с получением чистого целевого продукта в виде кристаллов красного цвета. Выход 37,3 г (70% от теоретического), т.пл. 90-9lc. Вычислено,%: С 61,0; Н 4,0;N 7,9 Найдено, % : С 61,1,; Н 1,2;N 8,2 Пример 17. 2-Метил-З-циано-(2-фурил)пропионат. 2-Метил-З-циано- (.2-фурил) акрилат в количестве 26,4 г (0,149 моль) растворяют в 300 мл смеси, состоящей из метанола и воды в объемном соотношении 80:20. Далее добавляют 3 капли молярного водного раствора гидроокиси натрия с последующим добавлением боргидрида натрия в количестве 1,8 г (0,048 моль).. Полученную таким образом суспензию перемешивают при комнатной температ -ре в течение 12 ч и нейтрализуют молярным водным раствором уксусной кислоты. Летучие компоненты реакционной смеси отделяют выпариванием при пониженном давлении и остаток суспендируют в воде и экстрагируют в толуоле. Полученный экстракт сушат сульфатом натрия и толуол выпаривают в вакууме с получением продукта-сырца в виде масла красного цвета. Это красное масло частично очищают путем хроматографирования на колонке, заполненной силикагелем с использованием в качестве элюента смеси, состоящей из толуола и метанола в объемном соотношении 9:1, и полученный таким образом частично очищенный продукт дистиллируют при пониженном давлении с получением в результате чистого целевого продукта в виде жидкости палево-желтого цвета. Выход 12,2 г (46% от теоретического), т.кип. 52С при 0,2 мм рт.ст.
Вычислено,%s С 60,3; Н 5,1;N 7,8
Найдено, % : С 59,0; Н 5,0;N 8,1
Пример 18. 2-Метил-3,-г-(5,б-дигидро 4Н-1,З-тиазин-2-ил)-(2-фурил)пропионат.
Суспензию 3-аминопропантиол гидрохлорида (7,33 г, 0,0575 моль) в безводном метиленхлориде (100 мл), содержащую метил-2-циано-З-(2-фурил)пропионат в количестве 10,1 г (0,0523 моль) и триэтиламин в количестве 5,8 г (0,0575 .моль), перемешивают при температуре дефлегмирования в атмосфе1 е азота в течение 17 ч После фильтрации этой реакционной смеси растворитель выпаривают при пониженном давлении с получением в результате маслообразного остатка, который далее суспендируют в воде и экстрагируют эфиром. Экстракт эфира сушат сульфатом натрия, эфир выпаривают и остаток подвергают дистилляции при пониженном давлении с получением в результате целевого продукта, в виде жидкости палево-желтого цвета. Выход 5,8 г .(44% от теоретического), т.кип. 158° С при О,4 мм рт.ст.
Вычислено,%: С 56,9; Н 6,8;N 5,5 С,Л,ЛОз5
Найдено,% : С 57,4; Н 6,0;N 6,1
Активность по отношению к паразитам и псгстицидная активность предлагаемых соединений определена с помощью следующих тестов.
Тест 1. Соединения подвергались испытаниям с помощью противогелькшнтного экрана, который обладает высокой чувствительностью по отношенигю к Нематодам, встречающимся у жвачных животных, и позволяет выделить известные антигельминты у жвачньох. Этот экран включает в себя определение эффективности соединений при лечении крыс, зараженных крысиными аскаридами .ippostrongylu5 hrasilrens1s.
Белые caivoibi крыс вида SpragueDawley весом примерно по 50 г подвергались заражению N.bra si 1iensis путем подкожного ввода в область затылка 1 мл воды, содержащей около 200 личинок N.brasi1iensis. Крысы далее выдерживались в течение 9 дне для развития инфекции.
Каждое соединение, подвергаемое испытаниям, развешивалось по 50 мг в стеклянные бутылочки с притертой npoкой. После приготовления соединения для испытаний оно подвергалось растиранию в ступке с б куб.см пшеничного масла, добавляемого в качестве носителя. В том случае, если соединение, подвергаемое испытаниям, не суспендировалось должньп- образом или не переходило в раствор при растирании в ступке, смесь подвергалась ультразвуковым колебаниям, и в резултате тепла, образующегося при этом, достигался требуемый эффект. Полученные формирования соединений, подвергаемых -испытаниям в носителе пшеничном масле, вводились ь еду для крыс объемом 200 г. Используя емкост с круглым основанием и электрический смеситель, соединение, подвергаемое испытаниям, пшеничное масло и пища, подвергались тщательному перемешиванию. Приготовленная таким .образом пища далее помещалась в пластиковые мешочки с ярлыками для заполнения кормушек.
На девятый день после заражения крыс они случайным образом распределялись по пластиковым ящикам. Две крысы использовались Б качестве обрабатываемой группы для каждой из серий различных доз-каждого из соединений, подвергаемых испытаниям. Были также включены 5-10 не обработанных контрольных экземпляров. Специальные .самоподающие питатели (кормушки),содержащие обработанную и необработанную пищу, доставлялись в каждую пластиковую коробку вместе с карточной идентификации. Спустя 5 дней после приема обработанной пищи 1 :рысы помещались в специальные обзорные ящики за 24 ч перед вскрытием. Крысы были умерш лены с использованием двуокиси углерода (сухой лед. Примерно от 10 до 15 дюймо Kanofi кишки извлекалось, сжималось тяжелыми стеклянными пластинами и количество маленьких красных паразитических аскаридов подсчитывалось визуально.
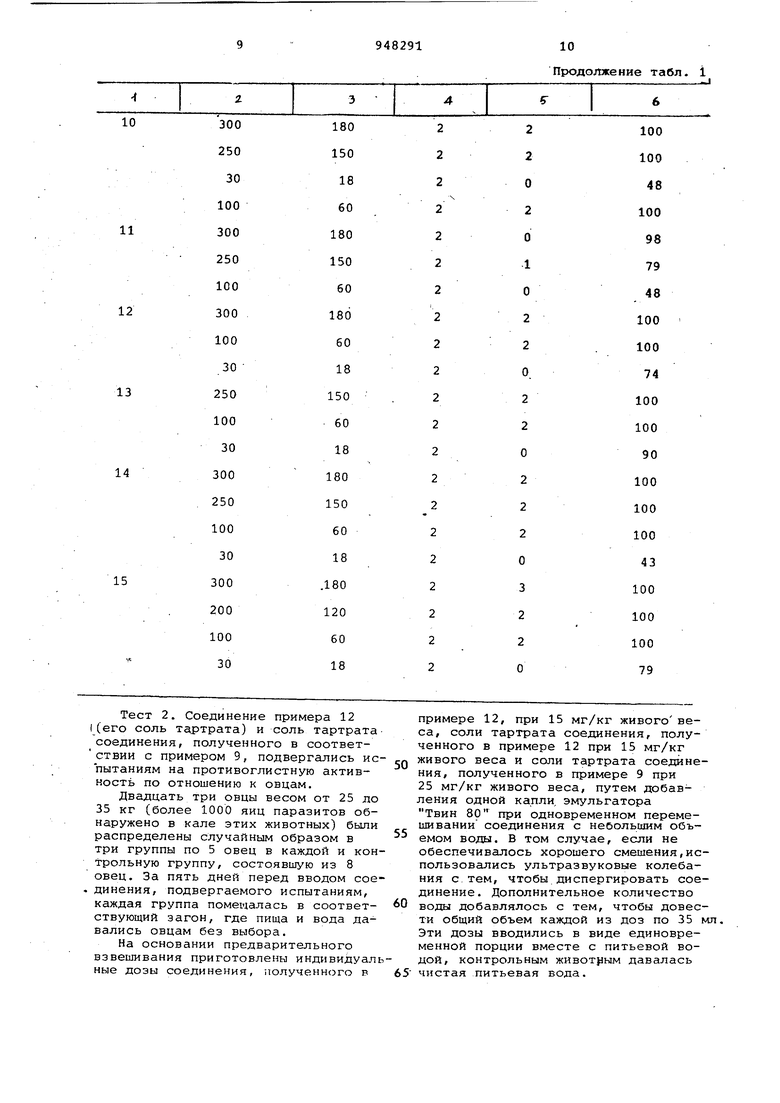
Результаты испытаний на антигельр-жптную активность представлены в табл.1.
Таблица 1





18
30
Тест 2. Соединение примера 12 (его соль тартрата) и соль тартрата соединения, полученного в соответствии с примером 9, подвергались ис пытаниям на противоглистную активность по отношению к овцам.
Двадцать три овцы весом от 25 ло 35 кг (более 1000 яиц паразитов обнаружено в кале этих животных) были распределены случайным образом в три группы по 5 овец в каждой и контрольную группу, состоявшую из 8 овец. За пять дней перед вводом соединения, подвергаемого испытаниям, каждая группа помещалась в соответствующий загон, где пища и вода давались овцам без выбора.
На основании предварительного взвешивания приготовлены индивидуалЕт ные дозы соединения, полученного в
Продолжение табл. 1
примере 12, при 15 мг/кг живого веса, соли тартрата соединения, полученного в примере 12 при 15 мг/кг живого веса и соли тартрата соединения, полученного в примере 9 при 25 мг/кг живого веса, путем добавения одной капли, эмульгатора
Твин 80 при одновременном перемешивании соединения с небольшим объемом воды. В том случае, если не обеспечивалось хорошего смешения,использовались ультразвуковые колебания с тем, чтобы диспергировать соединение. Дополнительное количество воды добавлялось с тем, чтобы довести общий объем каждой из доз по 35 мл. Эти дозы вводились в виде единовременной порции вместе с питьевой водой, контрольным жИвот})ым давалась чистая питьевая вода.
Ка пятый день после обработки из всех овец выводилась пища после утреннего кормления. Спустя 36 ч производилось вскрытие каждой из овец. Abomasum, малая кишка и cecum ободочная кишка каждой из овец извлекались и их содержимое промывалось через экран-сито размером 0,25 мм. Aboraasum и малая кишка каж,цой из овец подвергались искусственному перевариванию в течение 12 ч и еще раз
84,9 79,0
97,0 98,3 100 59, 1 95,1 0
Тест 3. Соединение, полученное в соответствии с примером 12, в виде его соли тгртрата, и соединение, полученное в соответствии с примером 9, подвергались испытаниям с целью определения их противогельминтной активности у свиней в соответствии со следующей процедурой.
Поросята весом от 28 до 45 кг в количестве 10 штук, содержание яичек в кале которых превышало 500, помещались в индивидуальные загоны, в которых им давался свиной рацион, обеспечивающий их рост, и вода в течение трех дней периода аклиматизации и четырех дней периода теста. Эти поросята были случайным образом распределены в три группы по два поросенка в каждой, а в контрольную группу входили четыре поросенка.
Индивидуальные дозы соединений, подвергаемых испытаниям, были приготовлены из расчета 20 мг/кг живого веса. Каждая индивидуальная доза соединения, полученного в соответствии с примером 12, подвергалась смешению с рав:чым весовым количеством пшеничного масла и по/Лещалась в
t po iЬiвaлиcь через экран размером 0,25 мм. Все промывки помещались в 10%--нь й раствор форма/шна, с использованием обычных процедур производился сбор всех паразитов, их идентификация, подсчет, табулирование и расчет снижения инфекции у обработанных животных по сравнению с контрольными ,
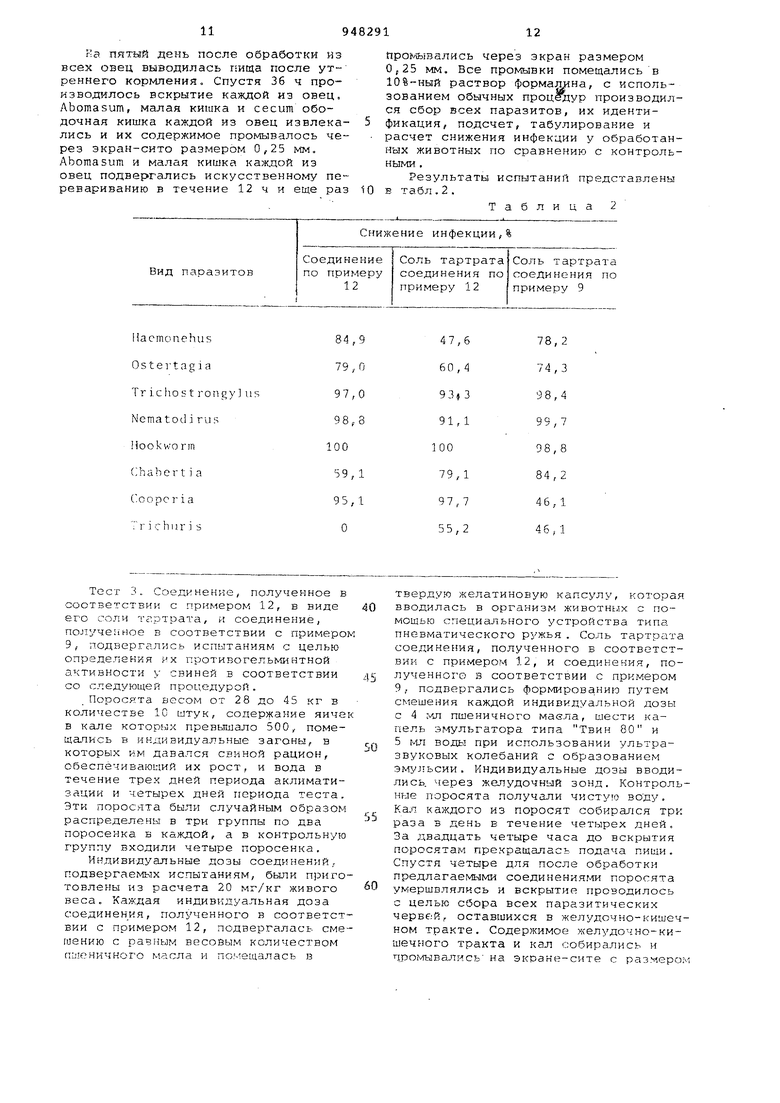
Результаты испытаний представлены в табл.2.
Таблица 2
78,2
47,6 74,3 60, 4 98,4 91,1 99,7 98,8 00 79,1 84, 2 46,1 97,7 46,1 55,2
твердую желатиновую капсулу, которая вводилась в организм ЖИВОТНЕЛХ с помошью специального устройства типа пневматического ружья . Соль тартрата соединения, полученного в соответствии с примером 12, и соединения, полученного 3 соответствии с примером 9, подвергались формированию путем смешения каждой индивидуальной дозы с 4 ул пшеничного мавла, шести капель эмульгатора типа Твин 80 и 5 tvui водьз при использовании ультразвуковых колебаний с образованием эм: льсии. Индивидуальные дозы вводились, через желудочный зонд. Контрольные поросята получали чистую воду. Кал кажццого из поросят собирался три раза в день в течение четырех дней. За двадцать четыре часа до вскрытия поросятам прекращалась подача пищи. Спустя четыре для после обработки предлагаег фами соединениями поросята умершвлялись и вскрытие проводилось с целью сбора всех паразитических червей, оставшихся в желудочно-кишечном тракте. Содержимое желудочно-кишечного тракта и кал собирались и п роivTb вались на экране-сите с раэмеро
отверстий 0,42 мм. Каждая из промывок хранилась в 10%-нйм растворе формгшина.аждое вскрытие или промывка кала подвергалось анализу с целью идентификации и подсчета всех паразити.ческих червей, прошедких последующую обработку или оставшихся при вскрытии.
. Результаты испытаний представленц в табл.3 и 4.
Таблица 3
Авторы
Даты
1982-07-30—Публикация
1980-05-21—Подача