(5) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИЗОЦИАНУРОВОЙ КИСЛОТЫ
. Изобретение относится к способу получения новых производных изоциан ровой кислоты, обладающих цитостаг 1тической активностью, которые могут найти применение в медицине.
Известна реакция раскрытия эпоксидного цикла, в частности глицидола, нуклеофильными реагентами, такими как вода, спирты, меркаптан ны СП.
Цель изобретения - псУлучение новых производных изоциануровой кислоть1, обладающих ценными цитостатйческими свойствами.
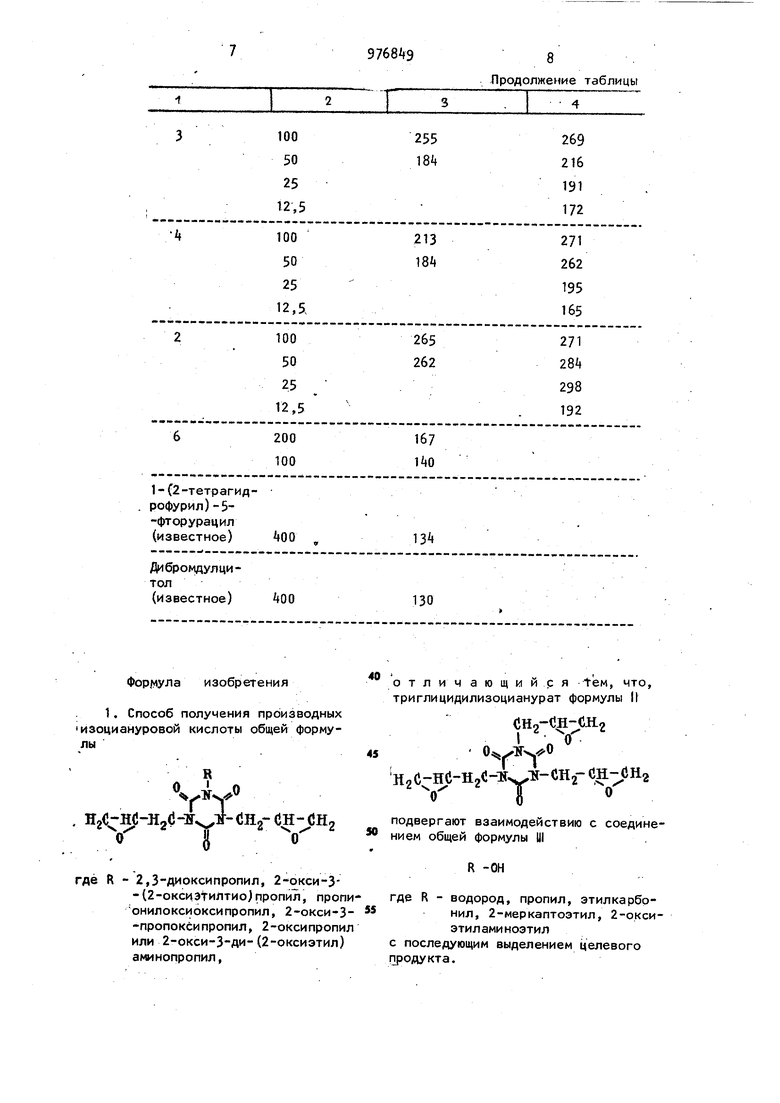
Поставленная цель достигается тем, что согласно способу получения производных изоциануровой кислоты обшей формулы
R
JH2C-HC-H2 -ir s -CH2-CH- dH2
VQо
где R-2 3-дисэксипропил , 2-окси-3-(2-оксиэтилтио}пропил, пропионилоксиоксипропил, 2-окси-З-пропоксипропил, 2-оксипропил или 2-окси-3-ди-(2-оксиэтил) . аминопропил, триглицидилизоцианурат формулы
еы -сн-оно о
ОуЗГуО (п;
1ГгС-ЛЙ-Н2 1-ИххТ« -СН2 :Р 2 ,
подвергают вза 1модействию с соединением общей формулы
R-OH
III
где R - водород, пропил, этилкарбонил, 2-меркаптозтил, 2-оксиэтиламиноэтил,
с последующим выделением целевого
продукта. При этом способ предпочтительно, осуществляют при 70 С, если R - водород. Кроме того, процесс проводят при комнатной.температуре в этаноле в присутствии боргидрида натрия, если К - водород. Причем процесс предпочтительно про водят при кипячении в органическом растворителе, если R - пропил. Кроме того, процесс проводят при кипячении в органическом растворите ле в присутствии молекулярного сита если R - этилкарбонил. При этом процесс проводят при ки пячении в органическом растворителе в присутствии основания, если R - меркаптоэтил. Причем реакцию проводят при 60°С в органическом растворителе, если R - 2-окси-З-ди-(2-оксиэтил)аминопропил. Пример. Получение .диглици дил-2,3-диоксипропилизоцианурата. 100 гci-триглицидилизоцианурата перемешивают в 1000 мл воды при рН в течение 3 ч при 70°С. Нераство рившийся исходный продукт отфильтро вывагот после охлаждения раствора и раствор упаривают досуха осторожно в вакууме масляного насоса. Смесь содержит 9,1 эпоксидного ки(лорода и состоит из смеси диглицидил-2, -диоксипропилизоцианурата и глицидил-ди{2,-з-диоксипропил )изоцианурата.. Смесь хроматографируют на колонке диаметром 3 см, содержащей 170 г силикагеля с размером частиц 0,ОбЗ0,2 мм. В качестве, элюента используют смесь метиленхлоридаи этилаце тата (32), содержащую 5 метанола. I При хроматографировании 38 г про дукта выделяют 18 фракций по 100 мл Фракции 10-18 дают 21 г целевого пр дукта. .. Процент эпоксидного кислорода , 10,3 (теоретически 10,1), бесцветный сироп. Показатель преломления 1,5093. П р и м е р 2. Получение диглици .дил- 2-окси-З-(2-оксиэтилтиопропил) изоцианурата, 29,7 г (0,1 моль) oL-триглицидилизоцианурата, 8,0 г (0,1 моль) меркаптоэтанола и 1,5 мл триэтиламина 8 500 мл метиленхлорида кипятят с братным холодильником в течение ч. Затем экстрагируют водой (3 раа по 60 мл) путем встряхивания, суат над сульфатом натрия и. упариват . Продукт внocяt в 200 мл метанола отсасывают выпавший исходный триглицидили.зоцианурат. Метанольную фазу упариеают и получают16.г смеси. змоно- и диглицидилового соединеия . Процент эпоксидного кислорода 6,1. Реакционную смесь хроматографиуют на Колонке диаметром 4 см, соержащей 230 г силикагеля No. 60, В качестве элюента используют смесь етиленхлорида, этилацетата и метаола (3:2:1). Вь1ход АИГЛИЦИДИЛОВОГО соединенЯЯ 10,5 г. Процент эпоксидного кислороа 8,2 (теоретически 8,5). Показатель реломления Пд 1 ,5207. .П. р и мер 3-. Получение диглицидил (пропионилоксиоксипропил)изоциануата. 20 г (О ,0б7 моль) о -триглицидилизоцианурата, 50 г (0,67 моль) пропионовой кислоты и 10 г молекулярного КИСЛОТЫ и сита 3 А в 300 мл толуола кипятят с обратным холодильником в течение ,5 ч. Затем фильтруют и упаривают. Выход сырого продукта 23,5 г. Смесь вносят в 150 мл метанола, отфильтровывают выпавший триглицидилизоцианурат и упаривают метанольный фильтрат. После фракционирова- ния на колонке с силикагелем No.60 получают 17,2 г целевого продукта в виде бесцветного сиропа. Процент эпоксидного кислорода 8,1 (теоретически 8,2). П р и м е р 4. Получение диглицидил(2-окси-3-пропоксипропил)изоцианурата . 29,7 г (0,1 моль) ot-триглицидилизоцианурата и 30 г (0,5 моль) н-пропанола в 500 мл.толуола с обратным холодильником в течение 6 ч при перемешивании. Затем раствор упаривают и вносят в 200 мл метанола. Выпавший триглицидилизоцианурат отфильтровывают и упаривают метакольный фильтрат. Выход сырого -продукта 15 г (в |виде маслянистого сиро.па)., Смесь хроматографируют на колонке диаметром 5 см и высотой 50 см содержащей 250 г силикагеля No.60. В качестве элюента берут метиленхлорид и этилацетат (3:2), Выход диглицидиловог о соединения 12 г. Процент эпоксидного кислорола 8,9 (теоретически 9,.0). Согласно данным тонкослойной хроматрграммы,ц елевой продукт имеет значения ,35 (метиленхлорид:этилаце ат-3:2). Пример 5. Получение диглициг дил-2-оксипропилизоцианурата. 5,9 г (0,02 моль) сС-триглицидилйзоцианурата растворяют в 200 мл смеси этанола и воды (7:3). Затем добавляют 0,76 г (0,02 моль) боргид рида натрия и перемешивают при комнатной температуре в течение 5ч. Мутный раствор подкисляют разбавленной соляной кислотой, фильтруют и за тем экстрагируют 3 раза метиленхлори дом по 200 мл, метиленхлоридные экс;тракты сушат и упаривают. . Выход сырого продукта ,8 г. Процент эпоксидного кислорода 8,5 (тер.ретически 10,7). Сырую реакционную смесь, хроматогр фируют на колонке диаметром 5 сми в :сотой 5 см, содержащей силикагель Ч4о..60. В качестве элюента берут смесь метиленхлорида, этилацетата и метанола (3.2:1). Выход диглицидилового эфира 3,7 г. Процент эпоксидного кислорода 10,6 (терретически 10,7). Согласно данным тонкослойной хроматограммы целевый продукт имеет, значение Rf 0,5 (метиленхлорид: этилацетат:метанол-3:2:1).. k36 П p и м e p 6. Получение дигдйцидил (2-оксй-З-диоксидиэтиламинопропил)изоцианурата. 29,7 (0,1 моль) oi-триглицидилизоцианурата и 10,6 г (0,1 моЛь)диЭтано ламина в среде 500 мл толуола нагревают при в течение 6 ч, защищая от влаги. Толуол отгоняют и остаток обрабатывают аналогично примеру k, Целевой продукт имеет значение Rf 0,6 (растворитель:метиленхлоридметанол-ам;1иак в соотношении k7k7: 6). Процент эпоксидного кислорода 7,7 (теоретически 7,9). Выход 13 г. . Цитостатическая активность известных и предлагаемых соединений оценивается на мышах. Соединения вводятся животным в виде водного раствора для иньекций, которыи готовится непосредственно перед применением. Мыши заражаются опухо,.яью Р 388 (лейкемия) (ГЧО клеток/ мышь). Длительность жизни зараженных животных определяется в контрольной ...ч группе (i.). Подопытным группам зараженных нышеи вводят испытуемые вещества в г трех различных дозах. Для каждой подопытной группы определяется средняя продолжительность жизни (т). Средняя продолжительность жизни животных подопытных групп с даг вотными контрольных групп сравнивается для определения степени продления жизни в % Т/С, которая свидетельствует об активности применяемого Q опыте соединения, В таблице указаны значения Т/С в зависимости от концентрации испытуемых веществ.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных уразола | 1982 |
|
SU1074405A3 |
| Способ получения производных уразола | 1982 |
|
SU1118287A3 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДОВ КАРБОНОВЫХ ИЛИ СУЛЬФОНОВЫХ КИСЛОТ ИЛИ ИХ ФИЗИОЛОГИЧЕСКИ СОВМЕСТИМЫХ СОЛЕЙ | 1990 |
|
RU2072986C1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛБЕНЗАЗЕПИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ АНТИГИСТАМИННАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2126802C1 |
| Способ получения карбапенемов | 1984 |
|
SU1395142A3 |
| 4-АРИЛ-1-ФЕНИЛАЛКИЛ-1,2,3,6-ТЕТРАГИДРОПИРИДИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ ВЕЩЕСТВА | 1996 |
|
RU2163237C2 |
| ПРОИЗВОДНЫЕ КСАНТИНА В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ИНДИВИДУАЛЬНЫХ ИЗОМЕРОВ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ АНТАГОНИСТОВ АДЕНОЗИНА | 1992 |
|
RU2057752C1 |
| 1,2,4-ЗАМЕЩЕННЫЕ ПИПЕРИДИНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ ПИПЕРИДОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ НОВЫХ СОЕДИНЕНИЙ | 1992 |
|
RU2114829C1 |
| Способ получения производных 2-пенем-3-карбоновой кислоты в виде свободной кислоты или ее защищенных производных,или ее солей | 1979 |
|
SU925252A3 |
| Способ получения производных 2-тиацефемов | 1984 |
|
SU1340591A3 |

100
50
25 12,5
100
50
25 12,5
226 17 167
300
197 17V
R - 2,3 диоксипропил, 2-окси-З
-(2-оксиэтилтио)пропил, пропионилоксиоксипропил, 2-окси-З-пропоксипропил, 2-оксипропил или 2-окси-3 Аи-(2-оксиэтил) аминопропил.
8 Продолжение таблицы
R -ОН
где R - водород, пропил, этилкарбо НИЛ, 2-меркаптоэтил, 2-оксиэтил аминоэтил
с последующим выделением целевого
продукта.
щ и и с я тем, что процесс проводят при , если R - водород.
. Способ по п.1, о т л и ч а ющ и и с я тем, что процесс проврдят при кипячении в органическом растворителе, если R - пропил.
Источники информации, принятые .80 внимание при экспертизе

Авторы
Даты
1982-11-23—Публикация
1980-10-03—Подача