(S) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИНДОЛИЗИНА








| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных индолизина или их солей | 1981 |
|
SU1109051A3 |
| Способ получения производных индолизина или их солей | 1977 |
|
SU715025A3 |
| Способ получения производных индолизина или их солей | 1977 |
|
SU674674A3 |
| СПОСОБ ПОЛУЧЕНИЯ АМИПОЗАМЕЩЕННЫХ ТРЕТИЧНЫХ БУТАНОЛОВ | 1970 |
|
SU429584A3 |
| СПОСОБ ПОЛУЧЕНИЯ САЛИЦИЛАНИЛИДА | 1970 |
|
SU281285A1 |
| Способ лечения фасциолеза овец | 1988 |
|
SU1590072A1 |
| Способ получения производных индолизина | 1980 |
|
SU1058505A3 |
| ДИГАЛОИДПРОПЕНОВЫЕ СОЕДИНЕНИЯ, ИНСЕКТИЦИДНО-АКАРИЦИДНЫЕ СРЕДСТВА, СОДЕРЖАЩИЕ ИХ, И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2144526C1 |
| ПРОИЗВОДНЫЕ БЕНЗОФУРАНА, БЕНЗОТИОФЕНА, ИНДОЛА ИЛИ ИНДОЛИЗИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИАРИТМИЧЕСКИМ ДЕЙСТВИЕМ | 1991 |
|
RU2095357C1 |
| Способ получения проивзодных пенициллановой кислоты или их солей | 1974 |
|
SU609468A3 |

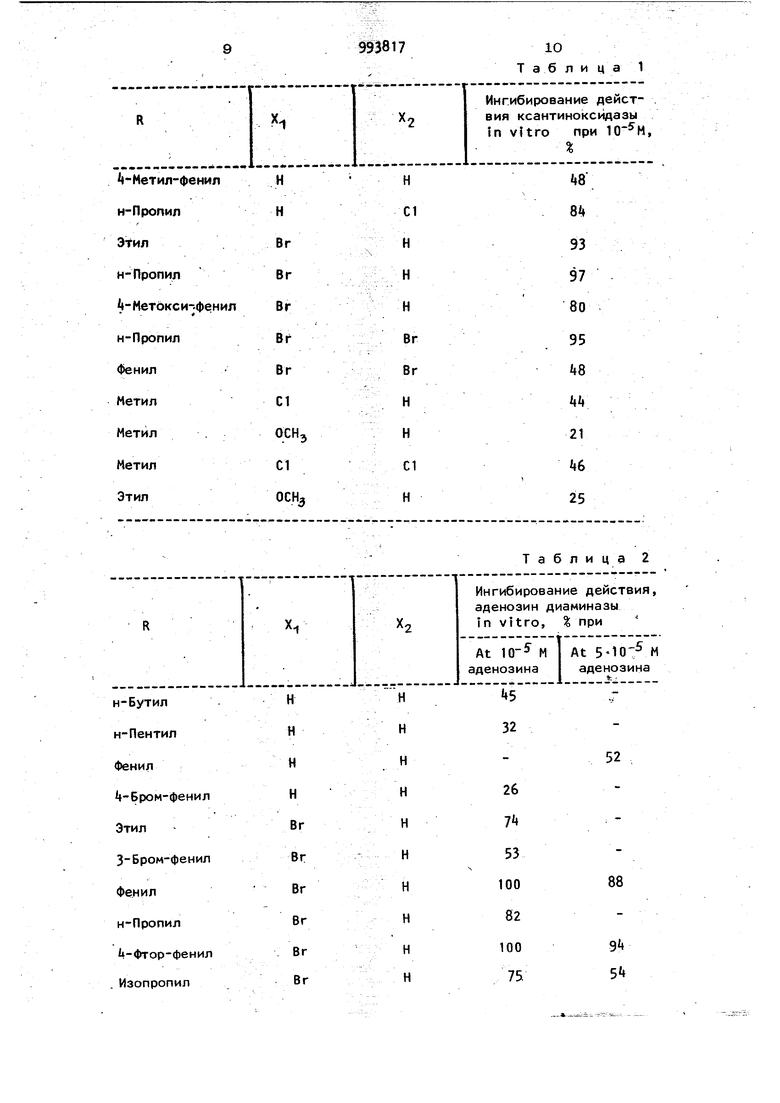
Изобретение относится к получению производных индолизина, обладающих биологической активностью, которые могут найти применение в медицине. Известна реакция галогенирования, преимущественно бромом, в среде органического растворителя в присутствии ацетата щелочного металла, в частности ацетата натрия Cl3. Цель изобретения - получение новых соединений, обладающих ценными фармакологическими свойствами. ПосТ вленная цель достигается тем что согласно способу получения производных индолизина общей формулы Т Бг .К О 2 . где R - прямой или разветвленный ал,кил C-f-Cfl, фенил, 3 хлор- -метилфенил, 3,дихлорфенил или фенил, заме щенный одним атомом хлора, фтора или брома или одним метилом или метокси, Х-, и Х2 - одинаковые или различные, . водород, хлор, бром или метокси, производное бензоилиндолизина общей формулыгде R, Х и 2 имеют указанные значе-. ния, подвергают взаимодействию с бромом в среде растворителя в присутствии щелочного металла. , В качестве растворителя используют диоксан, а в качестве ацетата щелочного металла ацетат натрия. В качестве другого растворителя можно использовать уксусную кислоту. Однако этот растворитель следует использовать только тогда, когда исходным соединением формулы (П).является однозамещенное по бензоильному ос399татку атомом хлора, брома или метоксигруппой соединение. Установлено, что производные индо лизина обладают ценными фармакологическими свойствами, а именно: они яв ляются ингибиторами по отношению к действию ксантиноксидазы и аденозиндеаминазы, а также uricosuric. Кроме того, эти соединения усиливают-сердечно-сосудистое действие катехолами на. Поэтому соединения (I) могут использоваться для лечения физиологических нарушений, вызываемых избытком мочевой кислоты и расстройствами сие темы иммунизац.ии. Примером физиологических нарушений, вызываемых избытком мочевой кис лоты является подагра или подагра tophaceous. При лечении таких на|цуше НИИ ежедневная доза соединений (|) для пациента весом 60 кг составляет, например, 300 мг. Физиологическими нарушениями, вызываемыми расстройствами системы иммунизации, которые можно лечить с помощью соединений (1), является преду преждение отторжения органов при трансплантации. Для оценки фармакологического дей ствия соединений (I) проведены пробы для оценки ин1 ибирующего действия на ксантин оксидазу и аденозин диаминазу - in vitro в абсорбционной ячейке УФ-спектрофотометра; /;ля оценки урикозурного действия и ингибирующего эффекта на действие аденозин диаминазы проведены опыты in vitro. Ингибирование действия ксантин ок сидазы. Опыт проводят с ксэнтин оксидазой найденной в молоке. Активность ферментной пробы измеряют по образованию мочевой кислоты гипоксантина в . присутствии кислорода и фосфатного буферного раствора. В абсорбционную ячейку помещают 1,5 мл 0,1 М фосфатного буферного раствора (,), насыщенного кислородом, 0,3 мл 1 М раствора тетраацетата этилендиамина; 0,8 мл воды, 0,01 мл раствора промышленной ксантиноксидазы с известкой концентрацией фермента, 0,01 л молярного этанольного раствора испытуемого соединения. Содержимое абсорбционной ячейки термостатируют 2 мин, затем начинают ферментативную реакцию, вводя в абсорбционную ячейку 0,3 мл 10 М раствора гипоксантина. За ходом реакции следят спектрофотометрически, записывая скорость окисления гипоксантина при 293 нм и 37°С. Регистрация оптической плотности проводится автоматически. Те же измерения проводят на контрольном растворе, содержащем все названные ингредиенты, за исключением испытуемого соединения. Таким образом, снимают кривые изменения оптической плотности во времени для растворов, содержащих и не содержащих ингибитор. Определяют наклон обеих кривых и выражают в молях мочевой кислоты, образующейся за 1 мин. В табл. 1 даны результаты экспериментальных и расчетных данных ингибирования действия ксантин оксидазы под действием по предлагаемому спосо УУрикозурное действие. Урикозурное действие оценивают на людях после орального введения 30 мл 2-этил-З- (3,5-Дибром- -окси-бензоил)-индолизина. Содержание мочевой кислоты в моче возросло на в течение ч после введения препарата. Среднее увеличение за 2h ч составило 22. Объем мочи за 2k ч существенно не изменился. Урицемия снизилась на 9% к 5-му числу, и к этому времени испытуемое соединение находилось на самом.высоком плазматическом уровне. Ингибирование действия аденозин диаминазы. Опыт in Vi tго. Опыт проводят с аденозин диаминазой, полученной из кишечника теленка. В абсорбционную ячейку помещают 2,7 мл 0,1 М фосфатного буферного раствора (,), 0,3 мл 5-10 М раствора аденозина в фосфатном буферном растворе (конечная концентрация аденозина ЮАили ), 0,01 мл 3 -10 М этанольного раствора исследуемого соединения (примерно 10 милличастей). Сддержимое абсорбционной ячейки термостатируют 2 мин, затем начинают ферментативную реакцию, вводя 0,03 мл раствора промышленной аденозин диаминазы с известной концентрацией Фермента. Реакция протекает при 30°С, за ходом которой следят спектрофотометрически, записывая уменьшение поглощения при 2б5 нм за счет перехода аденозина о инозин в присутствии аденозин диаминазы. 599 Ферментативную реакцию схематически можно представить уравнением аденозин диаминаза Аденозин + Hob ИНОЗИН 1 NN3. Те же измерения проводят на контрольном растворе, содержащем те же ингредиенты (за исключением исследуемого соединения), затем строят кривые снижения поглощения во времени, полученные для растворов, содержащего ингиби тор, и контрольного. Определяют наклон обеих кривых и выражают в молях инозина, образующегося за 1 мин. Затем рассчитывают процент ингибирования активности аденозин диаминазы в присутствии соединения данного изобретения. Результаты представлены в табл. 2 Сравнительные опыты, проведенные с 2-этил-З-(-оксибензоил)-бензофураном и 2-фенил-З-(3 5 Дибpoм- -oкcи-бeнзoил)-бeнзoфypaнoм, показали, что эти соединения обеспечивают только ингибирование действия аденозин диаминазы при 10 М аденозина соответственно. Соединения 2-этил-, 2-изопропили 2-н-бутил-3 (3,5-Дибром- -окси-бензоил)-бензофуранов, а также 2-этил-З-(3.5 ДИйод- -окси-бензоил) -бензофу ра на не ингибируют действие аденозин диаминазы при аденозина. При концентрации М 1-бром-2-фенил и 1-бром-2-(4-фтор-фенил)-3 -(З-бром- -окси-бензоил)-индолизина обеспечивается соответственно ингибирование действия аденозин диаминазы Во и 961 in vitro. Ингибирование действия аденозин диаминазы двумя соединениями также испытано на неповрежденных клетках путем выращивания асцитных клеток (Кребс и) в присутствии , аденозина при концентрации 5-10 М и измерении количества образующегося инозина и гипоксантина . Диаминиррвание аденозина за счет асцитных клеток ингибировалось на 50% в присутствии 2-10- М 1-бром-2-фенил-3-{3-бром- -оксибензол)-индолизина и 1-бром-2(«-фтор-фенил)-3-(3-бром-|-окси-бензоил)-индолизина. Опыт in vitro. Опыт проводят для определения влияния аденин аразинозида (Ара-А) и предлагаемых соединений на появление пораженных лишаем участков кожи и 76 смертность мышей, зараженных HSV-1(KOS) Athymic, лишенных волосяного покрова (пи/пи). Мышей возрастом 2025 дней внутримышечно заражают HSV-l(KOS) при (бляшкообразующих единиц) на мышь. Ара-А и предлагаемое соединение наносят на кожу при концентрации % в диметилсульфоксиде раза в день на 0,1, 2,3 и день. Определяют число мышей с эпидермальным поражением (некроз не менее 5 10 мм длиной) на общее число живых мышей. Результаты исследования показывают, что предлагаемое соединение усиливает противовирусное действие аденин аразинозида. Токсичность. Для определения острой токсичности опыты проводят на мышах с предлагаемыми соединениями. При внутривенном введении 20 мг/кг 1-бром-2-фенил- или 1-бром-2-(-фтор-фенил) -3- (3 бром-+-окси-бензоил) -индолизина через И дней не наблюдали смертельных случаев. . Внутрикишечное введение 1500 мг/кг 1-бром-2-изопропил- или 2-этил-3-(3,5-дибром- -окси-бензоил)-индолизина дало те же результаты. Предлагаемое соединение обладает ингибирующим действием, которое они оказывают на аденозин диаминазу, о чем упоминалось выше. Так как таким действием обладают и некоторые известные соединения, например коформицин и 2-деоксйкоформицин, обладающие противопаразитимескими свойствами, то вполне возможно, что предлагаемые соединения также обладают противопаразитическими свойствами, является чрезвычайно важным для терапии. При терапевтическом использовании предлагаемого соединения его можно вводить в форме фармацевтических и ветеринарных композиций в дозированной форме. П р и М е р 1. 1-Бром-2-этил-3-( окси-бензоил)-индолизин. К смеси 5,3 г (0,02 М) 2-этил-З1 -окси-бензоил)-индолизина по каплям в течение 3,75 ч добавляют 5,6 г (0, М) тригидрата ацетата натрия и 50 мл уксусной кислоты, а также 3,25 г (0,021 М) брома в 50 мл уксусной кисоты при 20-22°С. Перемешивают 0,75ч, затем добавляют 150 мл воды. Смесь еремешивают еще 1 м и выпавший осадок отфильтровывают -на вакуумном фильтре. Этот остаток превращают в пасту в 50 мл, а затем в 100 мл бензола, в результате чего пoлyчaюf 6,53 г твердого вещества. Его перекристаллизовывают из 90 мл метанола. Таким образом получают k,k г Т-бром-2-этил-3(-окси-бензоил)-индо лизина. Выход 63,9. Т. пл. 160-161,5°С. В табл. 3 показаны соединения, по лученные согласно Примеру 1. П р и м е р 2. 1-Бром-2-этил-3(3 -бром- -окси-бензоил)-индолизин. К смеси 1,3 г (0,00 М) 2-этил-З-(З-бром- -окси-бензоил)-индолизияа 0,6 г (0,09м) безводного ацетата натрия и 10 мл уксусной кислоты по каплям в течение 3 3/ ч при перемешивании приливают 0,6 г (0,ООА М) брома в 10 мл уксусной кислоты при 20-22°С. Раствор перемешивают еще в течение 5 мин, а затем.выливают в 50 мл воды. Выпавший осадок отфильтровывают на вакуумном фильтре, промывают до нейтральной реакции. Таким образом, получают 1,4 г вещества, из которого после перекристаллизации из 20 мл хлороформа получают 0,7 г 1-бром-2-этил-3(3-бром-4-окси-бензоил)-индолизина. Выход 5%. Т. пл. 213-21 °С.. В табл. даны соединения, полученные согласно примеру 2. П р и м е р 3- 1-Бром-2-этил-3(3, -дибром-4-оксй-бензоил)-индолизин. К раствору k,2 г (0,01 М) 2-этил-3-(3,5-Дибром-4-окси-бензоил-индоли зина в 100 мл диоксана добавляют 1,6 (0,02 м) безводного ацетата натрия. При интенсивном перемешивании по кап лям добавляют раствор 1,6 г:(О,01 М) брома в 20 мл диоксана. Температуру поддерживают 20-22°G. После перемешивания раствора в течение 1 ч продукт реакции выливают в 250 мл воды. Выпавший желтовато-зеленый осадок отфильтровывают и промывают до нейтрал ной реакции фильтрата. После просуши вания под,вакуумом получают 5,2 г сы рого продукта, который перекристалли зовывают из 50 мл дихлорэтана. 99 Д Таким образом, после обработки активированным углем получают ,2 г 1-бром-2-этил-3(3,5 Дибром- -окси бензоил)-индолизина. Выход 83,6. Т. пл. 1Э5°С. В табл. 5 даны соединения ,полученные согласно примеру 3П р и м е р 4. 1-Бром-2-этил-3(3 5-Дибром- -окси-бензоил)-индолизин. к смеси 5,3 г (0,02 М) 2(этил-3-) -оксибензил-индолизина, 17,7 г (0,13 М) тригидрата ацетата натрия и 50 мл уксусной кислоты по каплям в течение 3 ч добавляют 10,55 г (О,066 М) брома в 50 мл уксусной кислоты, температура 20-22°С. Перемешивают 18 ч, осадок отфильтровывают на вакуумном фильтре и промывают уксусной кислотой и водой. К фильтрату добавляют 50 мл воды и раствор вновь фильтруют. Два осадка соединяют и перекристалл изовывают из четыреххлористого углерода. Таким образом получают 7,9 г 1-бром-2-этил-3-(3,5-Дибром- -окси-бензоил)-индолизина. Выход 79%. П р и м е р 5- 1-Бром-2-метил-3-(3,5-Дихлор- -окси-бензоил)-индолизин. к раствору 3,2 г (0,01 М) 2-метил-3- (3,5-Дихлор-1-окси-бензоил)-индолизина в 100 мл диоксана добавляют 1,6 г (0,02 м) безводного ацетата натрия. При интенсивном перемешивании по каплям при 20°С приливают 1,6 г (0,01 М) брома. Во время операции температура 20-22°С. После перемешивания смеси в течение 1 ч продукт реакции выливают.в 250 мл воды. Образовавшийся желтовато-зеленый осадок фильтруют и промывают водой до нейтральной реакции фильтрата. После высушивания под вакуумом сырой продукт перекристаллизовывают из смеси дихлорэтан/гептан-80/20. Таким образом, после обработки активированным углем получает 1,7 г 1 бром-2-метил-3-(3,5-Дихлор- -окси-бензоил)-индолизина. Выход k2,6%, Т. пл. 240°С. В табл. 6 даны соединения, полученные согласно примеру 59
993817
lO Таблица1
n
Соединение
1-Бром-2-метил-ЗС Окси-бензоил )-индолизин
1-Бром-2-н-бутил-3- (А-окси-бензоил)-индолизина
1-Бром-2-н-пентил-3 ( -окси-бензоил)-индолизин
1-Бром-2-н-гексил-3-(-окси-бензоил)-индолизин
1-Бром-2-н-гептил-3-(4-окси-бензоил)-индолизин
1-Бром-2-н-октилгЗ- (f-окси-бензоил)-индолиЗИН .
1-Вром-2-фенил-3- (-окси-бензо ил)-индолизин
1-Бром-2- (-метил-фенил-3-)-океи-бензил
индолизин
1-Брсм-2- (4-бром-фенил)-3-( -окси-бензоил)-индолизин
993817 Продолжение табл. 2
Таблица 3 Т. пл. , с
238-239 (дихлорэтан)
160-162 (бензол)
155-157 (дихлорэтан)
1б2-1бЗ (дихлорэтан)
(бензол)
132-138 (дихлорэтан)
210 (диоксан)
197-198 (дихлорэтан)
220-225 (бензол)
13
Соединение
1-Бром-2-(3 бром-фенил)-3( оксибензоил)-индолизин
1-Бром-2-(3 хлор-4-метил-фенил)-3 -(-окси-бензоил)-индолизин
1-Бром-2- (3 ЛДихлор-фенил)-3- { -окси-бензоил)-индолизи)б
Соединение
1 - Бром-2-метил-3 (3 6ром- -окси-бенз-индолизин
1-Бром-2-н-проп ил-3(3-бром- -окси-бе -индолизин
I.
1-,Бром-2-изопропил-3- (3-бpoм- -oкcи-бeнзoил) - индолизин
1 - Бром-2-н-бут ил- 3 (3-бром- i-окси-бензоил)-индолизин
1-Бром-2-н-пентил-3-(З-бром-Ц-окси-бензоил)-индолизин
1-Бром-2-н-гексил-3-(З-бром- -окси-бензоил)-индолизин
1-Бром-2-н-гептил-3-(3-бром- -окси-бензоил)-индолизин
1-Бром-2-н-оксил-3-(3 бром- -окси-бензоил)-индолизин
1-Бром-2-пентил-3- (3 бром- -оке и-бензоил)-индолизин
1-Бром-2- («-метил-фенил)-3- (3-бром-окси-бензоил)-индолизин
1-Бром-2- ( -метокси-фенил)-3- (3-бром- 4-океи-бензоил)-индолизин
1-Бром-2- (-фтор-фенил)-3- (З-бром- -океи-бензоил)индолизин
1-Бром-2- (4-хлор-фенил)-3- (Збром- -окси-бензоил)-индолизина
U
ЭЭ3817 Продолжение табл. 3
Т. пл., С
225 (четыреххлористый углерод)
210 (бензол) 2«0 (дихлорэтан)
Таблица J
Т пл., °С
2j5-2 6 (дихлорэтан) 189-191 (бензол) 130-132 {бензол) 183-18 (бензол) lyt-US (дихлорэтан). 175-177 (дихлорэтан) 165-166 (дихлорэтан) 161,5-163 (дихлорэтан) 18,5-186 (бензол) 231 (дихлорэтан) (дихлорэтан) 196 (бензол) 228-230 (бензол)
-K jeygV
Соединение
1-Бром-2-( -бром-фенил)-3(3 бром- -окси-бензоил)-индолизин
1-Бром-2-(Збром-фенил)-2-(Збром-А-окси-бензоил)-индолизин
1-Бром-2-(2-бром-фенил)3(Збром-4-окси-бензоил)-индолизин
1-Бром-2-(3 хлор- -метил-фенил)-3-(Збром-А-окси-бензоил)-индолизин
1-Бррм-2-(3,Дихлор-фенил)-3 -(3 бром-4-окси-бензоил)-индолизин
1-Бром-2-метил-3(3 хлор- -оксм бензоил)индолизин
1-Бром-2-этил-3 (3 хлор-4-окси-окси-беизоил -индолизин
1-Бром-2-н-пропил-З(3 хлор- -окси-бензоил)-индолизин
1-Бром-2-изопропил-3 {3Хлор- -окси-бвнзоил-индолизин
1-Бром-2-н- утил-3(3 хлор- -окси-бензоил)-индолизин
1-Бром-2-фенил 3-(3 хлор-4-окси-безоил)-индолизин
1-Бром-2-(4-хлор-фенил)-3-(З-хлор- -окси-бензоил)-индолизин
1-Бром-2-(3 бром-фенил)-3(Зхлор-А-окси-бензоил)-индолизин
1-Бром-2-{4-бром-фенил)-3-(3-хлор-4-окси-бензоил)-индолизин
1-Бром-2-метил-3-( З-метокси- -оксибензоил) индолизин
1-Бром-2-этил-3-(3-метокси-Ц-окси-бензоил)индолизин
Продолжение табл. Т. пл., °С
(дихлорэтан)
185-186 (четыреххлори углерод)
213-21i (бензол) 201-202 (дихлорэтан) 207-209 (бензол)
228 (диоксан)
.
191-192 (дихлорэтан) I80-t8l (изопропанол) (бензол)
177-178 (дихлорэтан) 198-193 (бензол) 212-213 (дихлорэтан) 126-128 (беизол) 231-232 (дихлорэтан) 155(метанол)
1бО(метанол)
Соединение
1-Бром-2-метил-3 (3,5 Дибром- -окси-бензоил)-индолизин
1-Бром-2-н-пропил-3(3,5 Дибром- -окси-бензоил)-индолизин .
1-Бром-2-изопропил-3-(3,5-Дйбром- -окси-бензоил)-индолизин
1-Бром-2-н-бутил-3(3,5-Дибром-.1-окси-бензоил)индолизин
1-Бром-2-н-пентил-3 {3.5 Дибром- -окси-бензоил}-индолизйн
1-Бром-2-н-гексил-3(3,5 Дибром- -окси-бензоил)-индолизин
1-Бррм-2-н-гептил-3(3,5 Дибром-А-окси-бензоил)-индолизин
1-Бром-2-н-оксил-3- (3,5 Дибром- -окси-бензоил)-индолизин
1 -Бром-2-(|)ёнил-3- (3,5-Дибрс -|-окси-бензоил)гиндолизина
1-Бром-2- ( -метилфёнил)-3 (3,5 дибром-А-окси-бензоил)-индолизин
1-Бром-2- (4-метокси-фен14л )-3 -дибром-4-окси-бензоил)-индолизин
1-Бром-2- (t-фтор-фенил )-3- (3.5-Дибром-|-окси-бензоил)-индолизин
1 -Бром-2- С -хлор-фенил )-3- (3Л5-Дибром- -окси-бензоил)-индолизин
1-Бром-2- (-бром-фенил )-3 (3 5 Дибpoм-4-oкcи-бeнзoил )-индолизин
1-Бром-2- (3-бром-фенил )-3- (3,5-Дибром-4-окси-бензоил )-индолизин
1-Бром-2- (г-бром-фенил )-3,5 Дибром-4-оксибензоил )-индолизин
Таблица 5 Т. пл., С.
(дихлорэтан)
183-IB (бензол)
188-183 (CCit) .
162-163 (гептан)
(четыреххлористый угрерод)
152-153. (бензол) 167-168 (бензол) 153-15 (бензол) 211-212 (бензол)
1 8-150 (циклогексан) (четыреххлористый углерод)
16/-168 (изопропанол)
191-192 (бензол)
203-20 (четыррххлористый углерод)
203-20 (четыреххлористый углерод)
269-270 (дихлорэтан)
17б-177 (четыреххлористый углерод )
Соединение
1-5ром-2- (3 хлор-4-метил-фенил )-3- (3,5-дибром- -окси-бензоил )-индолизин
1 - Бром-2 (3, -дихлор-фенил) -3 ( 3,5-Дибром-k-окси-бензоил)-индолизин
Соединение
1-Бром-27ЭТИл-3-(3,5-Дихлор-4-окси-бензоил)-индолизин
1-Бром-2-фенил-3- (З ,5 Дихлор-4-окси-бензоил)-индолизин
Продолжение табл. 5 .Т. пл., °С
2 Й-215,5 (дихлорэтан) 2k (бензол)
Таблица 6
т-fJ IТ. пл. С
17
236 /дихлорэтан/гептан-90/1 О
Авторы
Даты
1983-01-30—Публикация
1980-07-03—Подача