Изобретение относится к области органической химии, а именно к одновременному получению и разделению в ходе синтеза химических продуктов орто- и пара-броманилинов, находящих применение в химико-фармацевтической, а также анилинокрасочной промышленности.
Существующие методы получения о- и п-броманилинов предусматривают раздельный синтез изомеров. Так, п-броманилин в промышленном масштабе получают через анилин, ацетанилид, который бромируют, а затем подвергают гидролизу. О-броманилин при этом способе не получается [1].
Исходя из бензола система синтеза выглядит следующим образом.
Схема синтеза п-броманилина из бензола: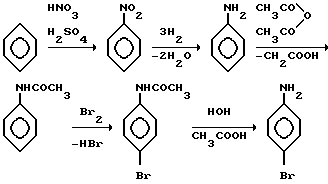
Схема синтеза о-броманилина из бензола: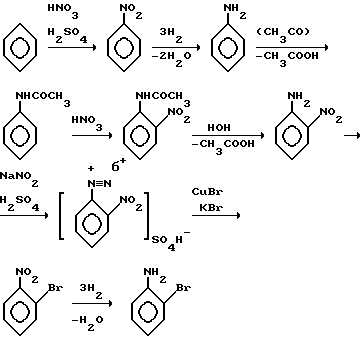
Аналогично из п-нитроанилина получают п-броманилин [2].
Наиболее близким к предложенному является способ постадийного получения о- и п-галоиданилинов из галоидбензолов, которые нитруют нитрующей смесью с получением смеси п- и нитрогалоидбензолов, которую разделяют дробной кристаллизацией и/или ректификацией в вакууме. При этом вначале выделяется п-изомер, а затем из маточника о-изомер. Указанные изомеры восстанавливают и отделяют перегонкой с паром [5].
Приведенные методы синтеза не позволяют получать одновременно оба изомера. Кроме того, они многостадийны, трудоемки по времени выполнения и неэкономичны, т. к. требуют для синтеза значительного ассортимента и количеств исходных полупродуктов.
Задачей изобретения является одновременное менее сложное и экономически более доступное получение и разделение в ходе синтеза о- и п-броманилинов из бромбензола, являющегося продуктом химического производства АООТ "Галоген", г. Пермь.
Предлагаемый способ малостадиен, менее трудоемкий и более экономичен, поскольку требует органического ассортимента и количеств исходных полупродуктов.
Предлагаемый согласно изобретению способ одновременного получения п- и о-броманилинов включает стадии нитрования галоидбензола, в качестве которого используют бромбензол, с получением смеси о- и п-нитрогалоидбензолов, выделение из последней части п-изомера кристаллизацией из изопропанола или метанола, который восстанавливают, восстановление оставшейся части смеси изомеров и разделение п- и о-броманилинов перегонкой с водяным паром.
Отличием предложенного способа получения п- и о-бромбензолов является использование в качестве галоидбензола бромбензола, выделение из смеси п- и о-бромбензолов части п-изомера кристаллизацией из изопропанола или метанола, который восстанавливают, а оставшуюся смесь изомеров также подвергают восстановлению с последующим разделением п- и о-броманилинов перегонкой с водяным паром.
Для сравнения приведены схема синтеза о- и п-броманилинов из бромбензола: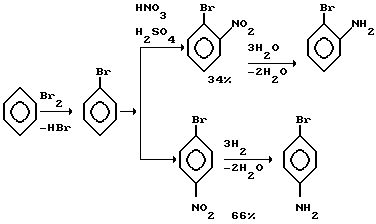
Согласно предлагаемому методу получения о- и п-броманилинов, исходный бромбензол нитруют на холоду нитрующей смесью [4] и количественно получают смесь п- и о-бромнитробензолов в соотношении 2:1 (по аналогии с нитрованием хлорбензола). Из смеси кристаллизацией из изопропилового спирта или метанола выкристаллизовывают большую часть п-изомера, выделяющегося при этом в чистом виде. Путем восстановления он далее переводится в п-броманилин.
Оставшуюся в маточнике смесь о- и п-бромнитробензолов (обогащенную о-изомером) после частичной отгонки растворителя подвергают восстановлению и полученные о- и п-броманилины из реакционной смеси выделяют перегонкой с водяным паром с их разделением в ходе перегонки.
Пример. Нитрорирование бромбензола (1-я стадия).
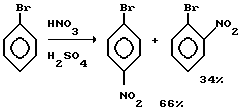
В трехгорлую колбу объемом 500 мл с охлажденной до 0oC нитрующей смесью [3] , состоящей из 30 мл HNO3 (d=1,4) и 30 мл H2SO4 (d=1,84) при энергичном перемешивании добавляют 20 мл (30 г) (0,19 М) охлажденного бромбензола, так, чтобы температура реакции не поднималась выше 5oC. Оптимальный температурный режим проведения реакции 2-5oC. После добавления всего количества бромбензола продолжают перемешивание реакционной массы 25-30 мин при этой же температуре, затем еще полчаса при нагревании на водяной бане при температуре не более 40oC. Далее реакционную смесь выливают в стакан с литром ледяной воды. Выпавший осадок смеси п- и о-изомеров отфильтровывают и промывают на фильтре небольшим количеством холодной воды. Осадок переносят на бумагу, высушивают (сушка на воздухе). Выход 38,4 г, т.е. практически количественный.
Выделение п-бромнитробензола (2-я стадия).
Высушенный осадок смеси о- и п-бромнитробензолов растворяют при кипячении в изопропиловом спирте (ИПС) (примерно 50 мл ИПМ на 10 г осадка) и выдерживают на холоду 2-2,5-ч. Выпавшие кристаллы п-бромнитробензола отфильтровывают и промывают на фильтре из расчета 2 мл ИПС на 10 г осадка. Из смеси при кристаллизации выделяется 20,3 г чистого п-бромнитробензола, о чем свидетельствует температура его плавления, равная 127-128oC [4]. ПМР-спектр подтверждает структуру и чистоту полученного продукта. В области 7,65 ± 0,05 и 8,06 ± 0,05 м.д. наблюдаются два дуплета, характерные для пара-замещенных соединений.
Более дешевым и, следовательно, более доступным растворителем с целью выделения п-изомера при кристаллизации смеси является метанол. Однако в этом случае с целью выделения чистого п-бромнитробензола необходима повторная перекристаллизация осадка п-изомера, выделенного первоначально из смеси изомеров. Маточники после обоих кристаллизаций объединяются, отгоняется метанол и остаток, представляющий собой смесь изомеров, обогащенный о-изомером, подвергается восстановлению.
После двух вышеописанных перекристаллизаций из первоначального количества смеси изомеров выделяется свыше 40% чистого п-бромнитробензола. ПМР-спектр подтверждает его структуру и чистоту.
Получение и разделение смеси о- и п-броманилинов (3-я стадия).
Восстановление нитрогруппы до амино - можно осуществить любым из разработанных для этого процесса способом [1]. В нижеприведенной схеме восстановление проводится экономически наиболее доступным методом, описанным в [2] :
4ArNO2 + 9Fe + 4H2O _→ 4ArNH2 + 3Fe3O4
В трехгорлую круглодонную колбу на 500 мл, снабженную обратным холодильником, мешалкой, термометром и помещенную в водяную баню, помещают 41 мл ИПС, 41 мл воды, 2,6 г хлористого аммония и 15 г (0,26 М) железного порошка. При энергичном перемешивании массу нагревают до кипения и небольшими порциями добавляют 18,1 (0,09 М) смеси о- и п-бромнитробензолов. По окончании добавления смеси реакционную массу кипятят еще 1 ч, затем фильтруют горячей. Из фильтрата отгоняют ИПС, добавляют 33 мл воды, в делительной воронке отделяют нижний маслянистый слой.
Далее смесь подвергают перегонке с водяным паром. При перегонке происходит разделение о- и п-броманилинов. Разделение изомеров основано на том, что они не растворяются и имеют различное агрегатное состояние в воде комнатной температуры: п-броманилин - кристаллический, о-броманилин - жидкий маслянистый продукт. Отгон собирают в литровый стакан с водой комнатной температуры. Внутри на середине стакана располагается под углом примерно 30o металлическая сетка (d= 1 мм) с расположенной на ней фильтровальной бумагой. Внизу сетка свободна, и ячейки, примыкающие к стеклу стакана, несколько увеличены. о-Броманилин, перегоняющийся в первую очередь, в виде маслянистых капель скатывается по сетке и через отверстия попадает вниз стакана. п-Броманилин, перегоняющийся с водяным паром вслед за о-изомером, попадая в воду, кристаллизуется и оседает на сетке.
После окончания перегонки п-броманилин с сетки вытряхивают на бумагу и высушивают на воздухе. Т.пл.= 63-64oC [5]. Общий выход п-броманилина (с учетом восстановления п-бромнитробензола) - 16,34 г (50% в расчете на исходный бромбензол). о-Броманилин отделяют от воды, высушивают и подвергают перегонке под вакуумом, отбирая при 20 мм рт.ст. фракцию, кипящую при 120-130oC. Выход о-броманилина 6,5 г (20% в расчете на исходный бромбензол).
Структура и чистота полученных изомеров подтверждена ПМР-спектрами. Так, для о-броманилина в области 3,84-0,05 м.д. наблюдается характерный уширенный сигнал поглощения протонов аминогруппы, а в области (6,13-7,70)± 0,05 м.д. - мультиплет протонов ароматического ядра. Интегральная интенсивность линий ПМР соответствует данной структуре. Для п-броманилина в области 3,44 ± 0,05 м. д. наблюдается характерный уширенный сигнал поглощения протонов аминогруппы, а в области 6,40 ± 0,05 и 7,13 ± 0,05 м.д. наблюдаются два дуплета, характерные для паразамещенных ароматических соединений.
Изобретение относится к способу получения ароматических аминов, а именно к способу получения и выделения из смеси продуктов, полученных нитрованием бромбензола, части чистого п-бромнитробензола кристаллизацией из изопропанола или метанола с последующим его восстановлением, восстановлением оставшейся смеси изомеров с получением полученной смеси п- и о-броманилинов перегонкой с водяным паром.
Способ одновременного получения о- и п-броманилинов, включающий стадии нитрования галоидбензола с получением смеси о- и п-нитрогалоидбензолов, выделения из указанной смеси п-изомера кристаллизацией, восстановления и перегонки с водяным паром, отличающийся тем, что в качестве галоидбензола используют бромбензол, из смеси о- и п-нитробромбензолов выделяют часть п-изомера кристаллизацией из изопропанола или метанола, который восстанавливают, и далее подвергают восстановлению оставшуюся смесь изомеров с последующим разделением п- и о-броманилинов перегонкой с водяным паром.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Краткая химическая энциклопедия | |||
| Судно | 1925 |
|
SU1961A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Препаративная органическая химия | |||
| Автоматический сцепной прибор американского типа | 1925 |
|
SU1959A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Топчиев А.В | |||
| Нитрование углеводородов и других органических соединений | |||
| Приспособление для строгания деревянных полов, устраняющее работу на коленях | 1925 |
|
SU1956A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Бельштейн | |||
| Прибор для записи продолжительности рабочих операций | 1924 |
|
SU1929A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Беркман Б.Е | |||
| Промышленный синтез ароматических нитросоединений и аминов | |||
| - М.: Химия, 1964, с.52 - 54, 94 - 110, 208 - 210. | |||
Авторы
Даты
1998-04-27—Публикация
1995-12-19—Подача