Это изобретение относится к некоторым дигалотриазолопиримидина, некоторые из которых являются новыми, способам их получения, композициям, содержащим такие соединения, и их использованию в качестве фунгицидов.
Chemical Abstracts (1964), 61:2941 раскрывают получение 5,7-дихлоро-6-метил-1,2,4-триазоло [1,5-а] пиримидина нагреванием 5,7-дигидрокси-6-метил-1,2,4-триазоло [1,5-а] пиримидина с хлорокисью фосфора в течение 4 часов при 100oC. Однако нет указания на то, что какое-либо из этих соединений обладает биологической активностью.
Европейская заявка заявителя N 92204097.7 (EP-A-0550113), находящаяся на рассмотрении, раскрывает соединения общей формулы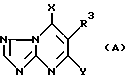
в которой R3 представляет возможно замещенную арильную группу и X и Y оба представляют атом хлора или атом брома,
как промежуточные соединения в получении некоторых фунгицидно активных производных триазолопиримидина общей формулы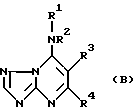
в которой R1 представляет возможно замещенную алкильную, алкенильную, алкинильную, алкадиенильную, циклоалкильную, бициклоалкильную или гетероциклильную группу R2 представляет атом водорода или алкильную группу; или R1 и R2 вместе с атомом азота представляют возможно замещенное гетероциклическое кольцо; R3 имеет значение, определенное выше, и R4 представляет водород или атом галогена или группу -NR5R6, где R5 представляет атом водорода или группу: амино, алкильную, циклоалкильную или бициклоалкильную и R6 представляет атом водорода или алкильную группу.
Однако в этом документе нет указания на то, что соединения формулы A сами обладают какой-либо фунгицидной активностью.
Теперь выявлено, что некоторые соединения формулы A и некоторые другие новые производные дигалотриазолопиримидина проявляют сами по себе фунгицидную активность.
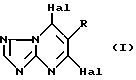
В соответствии с изобретением предлагается фунгицидная композиция, которая содержит носитель, и, в качестве активного ингредиента соединение общей формулы I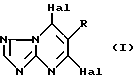
в которой R представляет возможно замещенную алкильную группу или группу алкокси с прямой или разветвленной цепью, или возможно замещенную циклоалкильную, арильную, арилокси или гетероциклильную группу; Hal представляет атом фтора, хлора, брома или йода.
Когда соединения в композициях этого изобретения содержат циклоалкильную группу, она может содержать от 3 до 8, желательно от 3 до 6 атомов углерода. Арильной группой может быть любая ароматическая углеводородная группа, лучше фенильная или нафтильная группа. Гетероциклильной группой может быть любая насыщенная или ненасыщенная кольцевая система, содержащая по меньшей мере один гетероатом, при этом 3-6 членные кольца предпочтительны и особенно 5- и 6-членные кольца. Лучше, если это азото-, кислородо- или серосодержащие кольца, такие, как пиридинил, пиримидинил, пирролидинил, фурил, пиралил, морфолинил и тиенил.
Если любые из вышеперечисленных заместителей указаны как возможно (необязательно) замещенные группами заместителя, которые могут присутствовать, могут быть одна любая или несколько из групп, используемых обычно в получении пестицидных соединений и/или модификации таких соединений, чтобы повлиять на их структуру/активность, устойчивость, проницаемость или другое свойство. Конкретные примеры таких заместителей включают, например, атомы галогена, нитро, циано, тиоциана, цианато, гидроксильные, алкильные, галоалкильные, алкокси, галоалкокси, амино, алкиламино, диалкиламино, формильные, алкоксикарбонильные, карбоксильные, алканоильные, алкилтио, алкилсульфинильные, алкилсульфонильные, галосульфонильные, карбамоильные, алкиламидо, фенильные, фенилокси, бензильные и бензилокси, гетероциклильные, особенно фурильные, и циклоалкильные, в частности, циклопропильные группы. Обычно может присутствовать 0-3 заместителя.
Если какие-либо из упомянутых заместителей представляют или содержат алкильную группу, она может быть линейной или разветвленной и может содержать до 12, лучше до 6, еще лучше до 4 атомов углерода. Если любой из указанных заместителей представляет или содержит арильную или циклоалкильную часть, арильная или циклоалкильная часть может сама быть замещена одним или несколькими атомами галогена, нитро, циано, алкильными, галоалкильными, алкокси или галоалкокси группами. В случае циклоалкильных и гетероциклильных групп возможные заместители также включают группы, которые вместе с двумя соседними атомами углерода циклоалкильной или гетероциклильной группы образуют насыщенное или ненасыщенное углеводородное кольцо. Другими словами, насыщенное или ненасыщенное углеводородное кольцо может быть конденсировано с циклоалкильной иди гетероциклильной группой.
Лучше, если R представляет C1-12алкильную, C1-C12 алкокси, C3-8циклоалкильную, фенильную, фенокси или нафтильную группу или 3-6-членное гетероциклическое кольцо, причем каждая группа или кольцо могут замещаться одним или несколькими заместителями, выбранными из: атомов галогена, нитро, циано, гидрокси, C1-4алкильной, C1-4галоалкильной, C1-4алкокси, C1-4галоалкокси, амино, C1-4алкиламино, ди-C1-4алкидамино, формильной, C1-4алкоксикарбонильной, карбоксильной, галосульфонильной, фенильной, фенокси, бензильной и бензилокси групп или в случае, если R представляет C1-8циклоалкильную группу или 3-6-членное гетероциклическое кольцо, возможно орто-конденсированную с бензольным кольцом.
Еще лучше, если R представляет C1-6алкил, C1-6алкокси, C3-8циклоалкил, фенил, фенокси или нафтильную группу или 3-6-членное гетероциклическое кольцо, причем каждая группа или кольцо могут замещаться одним или несколькими заместителями, выбранными из атомов галогена, C1-4алкила, C1-4галоалкила, C1-4алкокси, C1-4галоалкокси, галосульфониловых, фениловых, фенокси и бензилокси групп.
Наиболее предпочтительной подгруппой соединений формулы I является подгруппа, в которой R представляет пропильную, бутильную, этокси, циклопентильную, циклогексильную, фторофенильную, хлорофенильную, бромофенильную, дихлорофенильную, хлорофторфенильную, метилфенильную, пропилфенильную, бутилфенильную, диметилфенильную, трифтордетилфенильную, метоксифенильную, этоксифенильную, диметоксифенильную, диэтоксифенильную, триметоксифенильную, трифторметоксифенильную, хлорсульфонилфенильную, бифенилильную, феноксифенильную, бензилоксифенильную, фторофенокси, хлорофенокси, метилфенокси, диметилфенокси, нафтильную или тиенильную группу; и Hal представляет атом хлора или брома.
Предлагается также способ получения композиции, который включает соединение соединения формулы I, как указано выше, с по меньшей мере одним носителем. Такая композиция может включать одно соединение или смесь нескольких соединений настоящего изобретения.
Композиция по изобретению предпочтительно содержит от 0,5 до 95 вес.% активного ингредиента.
Носителем в композиции по изобретению может быть любой материал, с которым составляется активный ингредиент, чтобы облегчить применение в обрабатываемом очаге (локусе), который, например, является растением, семенами или почвой, или чтобы облегчить хранение, транспортировку или обращение. Носитель может быть твердым или жидким, включая материал, который в обычных условиях газообразен, но может сжиматься до образования жидкости, при этом используется любой из обычно применяемых носителей в получении фунгицидных композиций.
Подходящие твердые носители включают природные и синтетические глины и силикаты, например, природные кремнеземы, такие, как диатомовые земли; силикаты магния, например, тальки; магний-алюминиевые силикаты, например, аттапульгиты и вермикулиты; силикаты алюминия, например, каолиниты, монтмориллониты и слюды; карбонат кальция; сульфат кальция; сульфат аммония; синтетические гидрированные оксиды кремния и синтетические силикаты кальция или алюминия; элементы, например, уголь и сера; природные и синтетические смолы, например, кумароновые смолы, поливинилхлорид, и стиреновые полимеры и сополимеры; твердые полихлорфенолы; битумы; воски, например, пчелиный воск, парафиновый воск, и хлорированные минеральные воски; и твердые удобрения, например, суперфосфаты.
Подходящие жидкие носители включают воду; спирты, например, изопропанол и гликоли; кетоны, например, ацетон, метил-этиловый кетон, метилизобутиловый кетон и циклогексанон; эфиры; ароматические или алифатические углеводороды, например, бензол, толуол и ксилол; петролейные фракции, например, керосин и легкие минеральные масла; хлорированные углеводороды, например, тетрахлорметан, перхлорэтилен и трихлорэтан. Приемлемы также смеси различных жидкостей.
Фунгицидные композиции часто формируются и транспортируются в концентрированной форме, которая потом разбавляется пользователем непосредственно перед применением. Наличие небольших количеств носителя, который представляет собой ПАВ, облегчает этот способ разбавления. Поэтому лучше, чтобы хотя бы одним носителем в композиции по изобретению было ПАВ. Например, композиция может содержать по меньшей мере два носителя, по меньшей мере один из которых является ПАВ.
ПАВ может быть эмульгирующим, диспергирующим или смачивающим агентом; оно может быть неионным или ионным. Примеры подходящих ПАВ включают натриевые или кальциевые соли полиакриловых кислот и сульфокислоты лигнина; продукты конденсации жирных кислот или алифатические амиды или амины, содержащие по меньшей мере 12 атомов углерода в молекуле с этиленоксидом и/или пропиленоксидом; эфиры жирных кислот и глицерина, сорбита, сахарозы или пентаэритрита, их конденсаты этиленоксидом или/и пропиленоксидом; продукты конденсации спиртов жирного ряда или алкил фенолов, например, n-октилфенол или n-октилкрезол, этиленоксидом и/или пропиленоксидом; сульфаты или сульфонаты этих продуктов конденсации; соли щелочных или щелочноземельных металлов, предпочтительно, соли натрия, эфиры серной или сульфо-кислоты, содержащие по меньшей мере 10 атомов углерода в молекуле, например, натрий лаурил сульфат, вторалкил сульфаты натрия, натриевые соли сульфированного касторового масла и натрий алкилированные сульфонаты, такие, как додецилбензолсульфонат; и полимеры этиленоксида и сополимеры этиленоксида и пропиленоксида.
Композиции изобретения могут быть сформулированы, например, как смачиваемые порошки, дусты, гранулы, растворы, эмульгирующиеся концентраты, эмульсии, суспензионные концентраты и аэрозоли. Смачиваемые порошки обычно содержат 25, 50 или 75 вес.% активного ингредиента и в дополнение к твердому инертному носителю содержат обычно 3-10 вес.% диспергирующего агента и при необходимости 0-10 вес. % стабилизатора или/и других добавок, таких, как пенетранты или связующие вещества. Дусты обычно формируются в виде пылевого концентрата с составом, аналогичным составу смачиваемого порошка, но без дисперсанта, и могут разбавляться на поле другим твердым носителем, чтобы получить композицию, содержащую 0,5-10 вес.% активного ингредиента. Размер гранул составляет обычно 10-100 BS меш (1,676-0,152 мм), и они производятся технологией аггломерации или пропитки. Обычно гранулы содержат 0,5-75 вес.% активного ингредиента и 0-10 вес.% добавок, таких, как стабилизаторы, ПАВ, модификаторы медленного высвобождения и связующие агенты. Так называемые сухие текучие порошки состоят из относительно небольших гранул с относительно высокой концентрацией активного ингредиента. Эмульгирующиеся концентраты обычно содержат в дополнение к растворителю и при необходимости со-растворителю, 1-50 вес. %/об. активного ингредиента, 2-20 вес.%/об. эмульгаторов и 0-20 вес.%/об. других добавок, таких, как стабилизаторы, пенетранты и ингибиторы коррозии. В состав суспензионных концентратов, чтобы получить стабильный не осаждающийся текучий продукт, входят 10-75 вес.% активного ингредиента, 0,5-15 вес. % диспергирующих агентов, 0,1-10 вес.% суспендирующих агентов, таких, как защитные коллоиды и тиксотропные агенты, 0-10 вес.% других присадок, таких, как препятствующие образованию пены, ингибиторы коррозии, стабилизаторы, пенетранты и загустители, и вода или органическая жидкость, в которой активный ингредиент практически нерастворим; некоторые твердые органические вещества или неорганические соли могут присутствовать растворенными в препарате, чтобы воспрепятствовать осаждению или в качестве антифризов для воды.
Водные дисперсии и эмульсии, например, композиции, полученные разбавлением смачиваемого порошка или концентрата по изобретению водой, также входят в объем изобретения. Указанные эмульсии могут быть типа вода-в-масле или масло-в-воде и могут иметь консистенцию майонеза.
Композиции изобретения могут содержать и другие ингредиенты, например, другие соединения, обладающие гербицидными, инсектицидными или фунгицидными свойствами.
Особый интерес в увеличении срока защитной активности соединений изобретения представляет использование носителя, который обеспечит медленное высвобождение фунгицидных соединений в среду растения, нуждающегося в защите. Такие препараты с медленным высвобождением могут вводиться в почву у корней виноградной лозы или могут включать адгезивный компонент, позволяющий применять их непосредственно на стебель лозы.
Некоторые из соединений формулы I, как определено выше, являются новыми. Соответственно, изобретение предусматривает также и соединение общей формулы I, как ранее указывалось с оговорками, что
(i) если R представляет арильную группу возможно замещенную, обе группы Hal не представляют атом хлора или атом брома, и
(ii) если R представляет метильную группу, обе группы Hal не представляют атом хлора.
Далее настоящее изобретение предлагает способ получения соединения формулы I, как определено выше, который включает
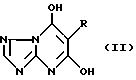
а) реакцию соединения общей формулы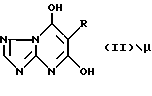
в которой R - как определено выше,
с хлорирующим или бромирующим агентом, чтобы получить соединение формулы I, в котором Hal представляет атом хлора или брома;
b) при желании, реакцию соединения формулы I, полученного на стадии (a), с фторирующим агентом, чтобы получить соединение формулы I, в котором Hal представляет атом фтора; и
c) при желании, реакцию соединения формулы I, полученного на стадии (a), с NH3, и затем с дийодометаном в присутствии диазотирующего агента, чтобы получить соединение формулы I, в которой по меньшей мере один Hal представляет атом йода.
Способ стадии (a) можно проводить в присутствии растворителя. Подходящие растворители включают галогенированные углеводороды такие, как дихлорметан. Кроме того, избыток хлорирующего или бромирующего агента может служить растворителем. Подходящие хлорирующие агенты включают оксихлорид, трихлорид и пентахлорид фосфора. Подходящие бромирующие агенты включают оксибромид, трибромид и пентабромид фосфора. Реакция проводится при температуре в диапазоне от 0oC до температуры рефлюкса реакционной смеси, предпочтительная температура реакции составляет от 20oC до температуры рефлюкса реакционной смеси.
Способ стадии (b) проводится в присутствии растворителя. Подходящие растворители включают сульфолан, диметилформамид или смесь ацетонитрила и краун-эфира. Если в качестве растворителя используется сульфолан или диметилформамид, в качестве сорастворителя хорошо использовать толуол, с целью дегидратирования фторирующего агента. Реакция обычно проводится при температуре в диапазоне от комнатной температуры (около 15oC) до температуры флегмы реакционной смеси, предпочтительная температура реакции составляет от 40oC до температуры флегмации реакционной смеси. Подходящие фторирующие агенты включают фториды щелочных металлов, особенно фторид калия, пентафторид сурьмы и трифторид диэтиламиносеры.
Реакция с NH3 в способе стадии (c) проводится в присутствии растворителя. Подходящие растворители включают эфиры, такие, как диоксан, диэтиловый эфир и тетрагидрофуран, галогенированные углеводороды, такие, как дихдорметан, и, особенно, толуол. Реакция хорошо осуществляется при температуре в диапазоне от 20oC до температуры флегмы реакционной смеси, предпочтительная температура реакции составляет от 40oC до температуры флегмы реакционной смеси. Желательно также, чтобы реакция проводилась в присутствии основания, и избыток NH3 может служить основанием. Диазотирующим агентом, используемым в стадии (c), может быть любой алкиловый эфир азотистой кислоты, при этом лучше брать изопентил нитрит. Если используется алкиловый эфир азотной кислоты, он может служить сорастворителем с дийодометаном. Эта реакция проводится при температуре от 60oC до 120oC, а лучше от 70oC до 110oC. Обе стадии в способе стадии (c) можно проводить в одном реакторе.
Соединения формулы II можно получить реакцией 3-амино-1,2,4-триазола с соответствующим эфиром малоновой кислоты в щелочных условиях по способу Y. Makisumi, Chem.Pharm. Bull. 9, 801, (1961).
Далее изобретение предлагает использование в качестве фунгицида соединения общей формулы I, как указано выше, или композиции, как указано выше, и способ борьбы с грибками в очаге (локусе), который включает обработку очага, который может быть, например, растениями, подверженными воздействию грибков, семенами таких растений или средой, в которой растут эти растения, или будут расти, таким соединением или композицией. Культуры, которые можно защищать от грибков, включают виноградную лозу, зерновые, такие, как пшеница, овес, яблони и томаты. Срок защиты обычно зависит от отдельного выбранного соединения и от многих внешних факторов, таких, как климат, воздействие которого обычно смягчается использованием подходящего препарата.
Далее изобретение иллюстрируется следующими примерами.
Пример 1.
Получение 5,7-дихлоро-6-(2-хлорфенил)-1,2,4-триазоло[1,5-a]пиримидина
(R = 2-хлорфенил; Hal=Cl)
Смешивали 5,7-дигидрокси-6-(2-хлорфенил)-1,2,4-триазоло [1,5-а] -пиримидина (6,2 г, 0,026 М) и 30 мл оксихлорида фосфора, и полученная суспензия выдерживалась при to флегмы 3 часа. Избыток оксихлорида фосфора отгоняли от полученного чистого раствора и полученное вязкое масло растворяли в 50 мл дихлорметана. Для разложения следовых примесей оксихлорида фосфора в растворе дихлорметана медленно добавляли 50 мл ледяной воды. Затем органический слой отделяли, высушивали сульфатом натрия и растворитель отгоняли в вакууме с получением 6,62 г 5,7-дихлоро-6-(2-хлорфенил)-1,2,4-триазоло-[1,5а]-пиримидина, в виде желтоватых кристаллов, т. пл. 153oC.
Выход: 85% от теоретического.
Пример 2. Получение 5,7-дибромо-6-(2-хлорфенил)-1,2,4-триазоло [1,5а]-пиримидина
(R = 2-хлорфенил; Hal=Br)
5,7-Дигидрокси-6-(2-хлорфенил)-1,2,4-триазоло[1,5а] -пиримидин (15 г, 0,057 М) добавлялся небольшими порциями при температуре около 100oC к расплавленному оксибромиду фосфора (избыток, 40 г). После энергичной первоначальной реакции получалось чистое, очень вязкое масло, которое оставляли при 120oC на 2 часа. Смесь охлаждали до комнатной температуры и полученное "стекло" порциями добавляли к смеси воды и дихлорметана. Органический слой отделяли сульфатом натрия и растворитель отгоняли в вакууме с получением 19,93 г 5,7-дибромо-6-(2-хлорфенил)-1,2,4-триазоло [1,5a]-пиримидина в виде желтоватых кристаллов, т. пл. 212oC.
Выход: 90% от теоретического.
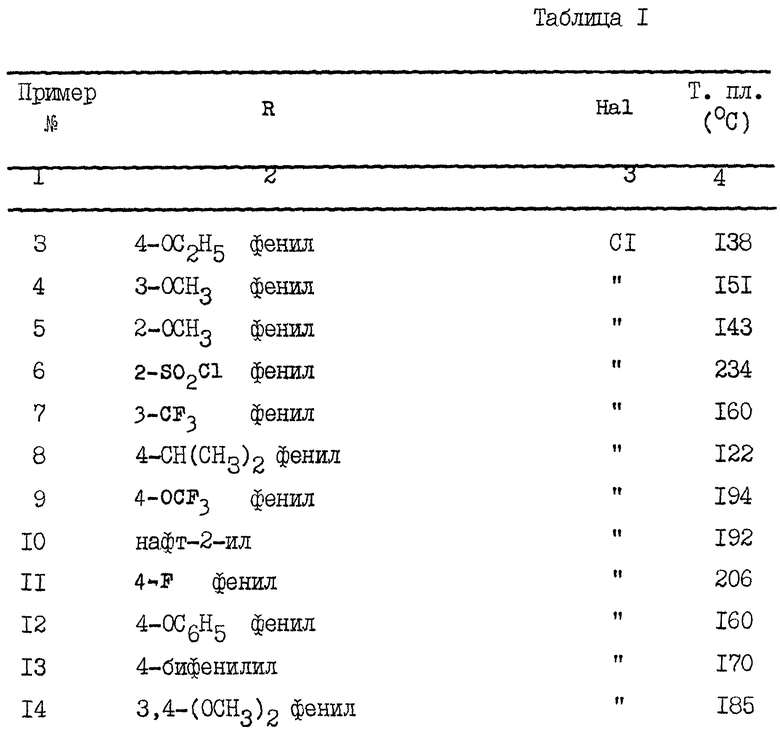
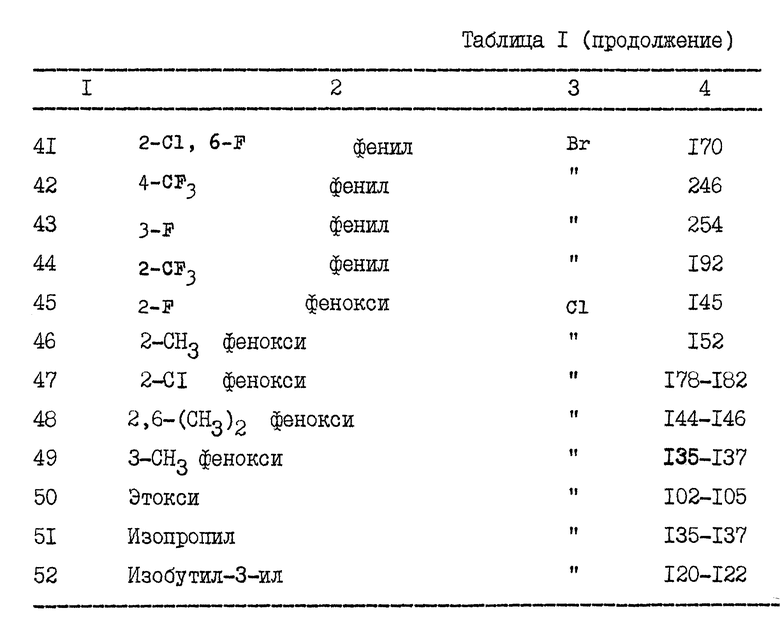
Примеры 3 - 52.
Способами, аналогичными описанным в примере 1 выше, были получены другие соединения по изобретению, указанные в табл. 1 в конце описания. В этой таблице соединения указаны со ссылкой на формулу I.
Пример 53.
Фунгицидная активность соединений по изобретению исследовалась следующими тестами.
(а) Антиспорулянтная активность против ложной мучнистой росы винограда (Plasmopara viticola; PVA).
Тест на непосредственное уничтожение спор с использованием распыления на листья. Нижнюю поверхность листьев всей виноградной лозы (Cabernet Sauvignon) инокулировали распылением водной суспензии, содержащей 2,5 • 104 зооспорангий/мл за два дня до обработки испытуемым соединением. Инокулированные растения выдерживались 24 часа в помещении с высокой влажность, затем 24 часа при тепличной температуре и влажности. На нижние поверхности инфицированных листьев распыляли раствор активного материала в воде/ацетоне 1:1, содержащем 0,04 " TWEEN 20 " (Тов. знак; ПАВ - полиоксиэтиленовый эфир сорбитана). Растения обрабатывали с использованием автоматической линии распыления и сопла. Концентрация соединения составила 1000 част/милл. в объем распыления - 700 л/га. После распыления растения возвращали в нормальные тепличные условия на 96 часов и затем переносили в помещение с высокой влажностью на 24 часа для инициирования споруляции до оценки результатов. Оценка проводилась на основе процентного показателя площади листа, покрытого спорами в сравнении с контрольными растениями.
(b) Прямая защита против фитофтороза томатов (Phytophthora infestans; PIP).
Тест на прямую защиту с распылением на листья. На верхние поверхности листьев томатов с двумя выпущенными листочками распылялось испытуемое соединение с дозировкой 1000 част/милл. с использованием распылителя, как описано в (a). После соответствующего периода в 24 часа в нормальных тепличных условиях верхние поверхности листьев инокулировались распылением водной суспензии, содержащей 2 • 105 зооспор/мл. Инокулированные растения выдерживались 24 часа в помещении с высокой влажностью и 5 дней в условиях помещения для роста. Оценка, основывалась на процентном показателе пораженной площади листа в сравнении с контрольными листьями.
(c) Прямая защита против ложной мучнистой росы винограда. (Plasmopara viti cola; PVP).
Тест является прямым тестом с использованием распыления на листья. На нижнюю поверхность листьев всего растения винограда (Cabernet Sauvignon) распылялось тестуемое соединение с дозировкой 1000 част/милл. с использованием автоматической линии распыления, как описано в (a), и после последующего периода в 24 часа в нормальных тепличных условиях нижние поверхности листьев инокулировались распылением водной суспензии, содержащей 2,5 • 104 зооспорангий/мл. Инокулированные растения выдерживались 24 часа в помещении с высокой влажностью, 5 дней в нормальных тепличных условиях, и затем возвращались на 24 часа в условия высокой влажности. Оценка проводилась по процентному показателю площади листа, покрытой спорами в сравнении с площадью на контрольных листьях.
(d) Активность против ранней гнили томатов (Alternaria solani; AS)
Этот тест определяет контактную профилактическую активность тестуемого соединения, применяемого в форме распыления на листья. Ростки томатов (Outdoor Girl) выращивались до стадии, на которой распускается второй истинный лист. Растения обрабатывали с использованием автоматической линии распыления, как описано в (a). Тестуемые соединения применялись как растворы или суспензии в смеси ацетона и воды (50:50 об/об.), содержащей 0,04 ПАВ ("TWEEN 20" - Тов. знак). Через день после обработки ростки инокулировались распылением на верхние поверхности листьев суспензии A. Solani conidia, содержащей 104 спор/мл. 4 дня после инокуляции растения выдерживались влажными во влажном помещении при 21oC. Заболевание оценивалось через 4 дня после инокуляции на основе процентного показателя площади поверхности листа, охваченного поражением.
(d) Прямая защитная активность против серой плесени бобов (Botrytis cinerea; BCB).
Тест определяет прямую защиту распылением на листья. Верхние поверхности листьев растений бобов (The Sutton ) подвергались распылению тестуемым соединением с дозировкой 1000 част/ милл. с использованием автоматической распылительной установки, как описано в (a). Через 24 часа после распыления листья инокулировались водной суспензией, содержащей 105 конидий/мл. 4 дня после инокуляции растения выдерживались влажными во влажном помещении при температуре 21oC. Заболевание оценивалось через 4 дня после инокуляции на основе процентного показателя площади поверхности листа, охваченного поражением.
(f) Активность против пятнистости пшеницы (Leptosphaeria nodorum; LN)
Тест является прямым терапевтическим тестом, применяющим распыление на листья. Листья пшеницы (Norman) на стадии одного листа инокулировались распылением водной суспензии, содержащей 1 • 106 спор/мл. Инокулированные растения выдерживались 24 часа в помещении с высокой влажностью до обработки. На растения распылялся раствор тестуемого соединения с дозировкой 1000 част/милл, с использованием автоматизированной распыляющей установит, как описано в (a). После, высыхания растения выдерживались 6-8 дней при 22oC и умеренной влажности, затем оценивались. Оценка основывалась на плотности поражений на лист в сравнении с листьями контрольных растений.
(g) Активность против бурой ржавчины пшеницы (Puccinia recondita; PR).
Тест является прямым защитным с распылением на листья. Ростки пшеницы (Avalon) выращивались до стадии 1-1,5 листа. Затем на растения распыляли тестуемое соединение с дозировкой 1000 част/милл. с использованием автоматической распылительной установки, как описано в (a). Тестуемые соединения применяли как растворы или суспензии в смеси ацетона и воды (50:50 об/об.), содержащей 0,04 ПАВ ("TWEEN 20 " - Тов. знак). Через 18-24 часа после обработки ростки инокулировались распылением на растения со всех сторон водной споровой суспензией, содержащей около 105 спор/мл. 18 часов после инокуляции растения выдерживались в условиях высокой влажности при температуре 20-22oC. После этого растения содержались в тепличных условиях, близких к окружающей среде, то есть в умеренной относительной влажности и при температуре 20oC. Заболевание оценивалось через 10 дней после инокуляции на основе процентного показателя площади растения, покрытого споруляционными пустулами, в сравнении с контрольными растениями.
(h) Активность против настоящей мучнистой росы овса (Erysiphe graminis f.sp hordei; EG).
Тест является прямым терапевтическим тестом, применяющим распыление на листья. Листья ростков овса (Golden Promise) инокулировались нанесением пыли конидий мучнистой росы за день до обработки тестуемым соединенном. Инокулированные растения выдерживались всю ночь при обычной тепличной температуре и влажности до проведения обработки. На растения распылялось тестуемое соединение с дозировкой 1000 част/милл. с использованием автоматической распыляющей установки, как описано в (a). После высыхания растения возвращались в помещение при 20-25oC и умеренной влажности на срок до 7 дней, затем проводилась оценка. Оценка основывалась на процентном показателе площади листа, покрытого споруляцией в сравнении с листьями на контрольных растениях.
(i) Активность против пирикуляриоза риса (Pyricularia oryzae; PO).
Это прямой терапевтический тест с применением распыления на листья. На листья рисовых ростков (Aichiaishi - около 30 ростков на горшочек) распылялась водная суспензия, содержащая 105 спор/мл за 20-24 часа до обработки тестуемым соединением. Инокулированные растения выдерживались всю ночь в высокой влажности и затем им давали высохнуть до распыления тестуемого соединения с дозировкой 1000 част/милл. с использованием автоматической распылительной установки, как описано в (a). После обработки растения выдерживались в помещении, специальном для выращивания риса при 25-30oC и высокой влажности. Оценка проводилась спустя 4-5 дней после обработки и основывалась на плотности некротических поражений на лист в сравнении с контрольными растениями.
(j) Активность против глазковой пятнистости пшеницы in vitro (Pseudocercosporella herpotrichoides; PHI).
Этот тест определяет in vitro активность соединений против грибка, вызывающего пятнистость пшеницы. Тестуемое соединение растворяется или суспендируется в ацетоне и добавляется в 4 мл аликвоты разбавленного наполовину бульона картофельной декстрозы, помещенные в чашки Петри с 25 клетками с получением окончательной концентрации в 50 част/милл. соединения и 2,5% ацетона. Каждая клетка инокулировалась кусочком агара/мицелия диаметром в 6 мм, взятого из 14-дневной культуры P. herpotrichoides. Чашки инкубировались при 20oC 12 дней до определения мицелиального роста.
(k) Активность против Fusarium in vitro (Fusarium culmorum; FSI).
Этот тест определяет in vitro активность соединений против видов Fusarium, которые вызывают гниение стебля и корней. Тестуемое соединение растворялось или суспендировалось в ацетоне и добавлялось к расплавленному агару картофельной декстрозы в половинной концентрации с получением окончательной концентрации в 50 част/милл. соединения и 2,5% ацетона. После застывания агара чашки инокулировались кусочками агара и мицелия диаметром в 6 мм, взятыми от 7-дневной культуры Fusarium sp. Чашки инкубировались при 20oC 5 дней и определялся радиальный рост от кусочков.
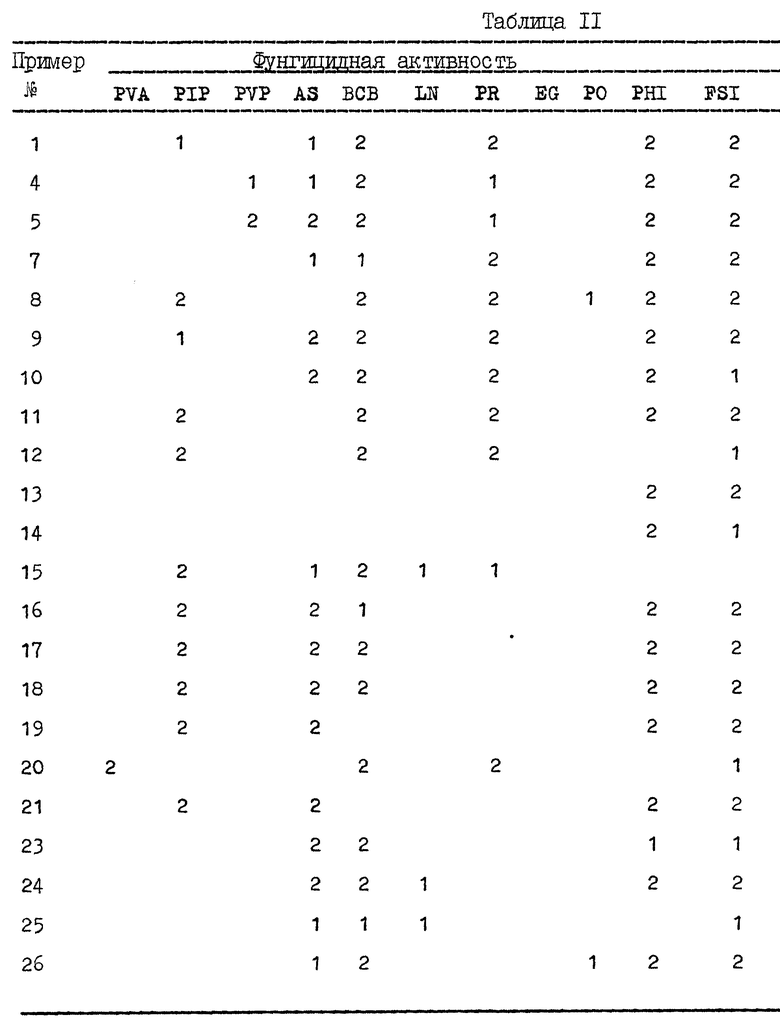
Степень подавления заболевания во всех вышеописанных тестах выражалась в процентном показателе в сравнении либо с необработанными контрольными объектами, либо контрольными объектами, с распылением разбавителем по критериям:
0 - подавление заболевания менее чем на 50%,
1 - подавление заболевания на 50- 80%,
2 - подавление заболевания более чем на 80%.
Результаты этих тестов изложены в табл. II в конце описания.
Пример 54.
(a) Антиспорулянтная активность против мучнистой росы винограда (Plasmopara viticola; PVA).
Тест является прямым антиспорулянтным тестом с применением распыления на листья. Нижняя поверхность листа виноградных лоз (Gabernet Suavignon) высотой приблизительно в 8 см инокулируется водной суспензией, содержащей 5 • 104 зооспорангий/мл. Инокулированные растения выдерживаются 24 часа при 21oC в помещении с высокой влажностью, затем 24 часа в теплице при 20oC и относительной влажности 40%. На нижнюю поверхность инфицированных листьев распыляется раствор тестуемого соединения в 1:1 воде/ацетоне, содержащий 0,04% "TWEEN 20". Растения распыляются из разбрызгивателя с двумя соплами. Концентрация соединения составляет 600 част/милл. и объем распыления - 750 л/га. После высыхания растения возвращаются в таблицу при 20oC и 40% относительной влажности на 96 часов и затем переносятся в помещение с высокой влажностью на 24 часа для индуцирования споруляции. Оценка основывается на процентном показателе площади листа, покрытого спорами в сравнении со спорами на контрольных листьях.
(b) Прямая защитная активность против фитофтороза томатов (Phytophthora infestans; PIP).
Это прямой защитный тест, использующий распыление на листья. На растения томатов с двумя распустившимися листами (First in the Field) распыляется тестуемое соединение с дозировкой 600 част/милл., как описано в (a). После высыхания растения выдерживаются 24 часа в теплице при 20oC и 40% относительной влажности. Затем верхние поверхности листьев инокулируются водной суспензией, содержащей 2 • 105 зооспорангий/мл. Инокулированные растения выдерживаются 24 часа при 18oC в помещении с высокой влажностью и затем 5 дней в камере роста при 15oC и 80% относительной влажности с 14 часами светового дня. Оценка основана на процентном показателе пораженной площади листа в сравнении с площадью на контрольных листьях.
(c) Активность против раннего фитофтороза томатов (Alternaria solani; AS).
Это прямой профилактический тест, применяющий распыление на листву. Ростки томатов (Outdoor Girl) на стадии развертывания второго листка подвергаются распылению тестуемым соединением с дозировкой 600 част/милл., как описано в (a). После высыхания растения выдерживаются 24 часа в теплице при 20oC и 40% относительной влажности с последующей инокуляцией верхних поверхностей листьев водной суспензией конидий A. solani, содержащей 1 • 104 конидий/мл. После 4 дней нахождения в помещении с высокой влажностью при 21oC проводится оценка заболевания по процентному показателю площади поверхности листа, охваченной поражением в сравнении с контрольными растениями.
(d) Прямая защитная активность против серой плесени (Botrytis cinerea; BCB).
Это прямой защитный тест с использованием распыления на листву. Растения бобов (The Sutton ) с двумя парами листьев подвергались распылению тестуемым соединением с дозировкой 600 част/милл., как описано в (a). После высыхания растения выдерживались 24 часа в теплице при 20oC и 40% относительной влажности. Затем верхняя поверхность листьев инокулировалась водной суспензией, содержащей 1 • 106 конидий/мл. Растения выдерживались 4 дня при 20oC в помещении с высокой влажностью. Оценка проводилась по процентному показателю площади листа, затронутой заболеванием в сравнении с площадью на контрольных листьях.
(e) Активность против пятнистости пшеницы (Leptosphaeria nodorum; LN).
Это прямой терапевтический тест с применением распыления на листву. Ростки пшеницы (Norman) на стадии одного листа, инокулируются водной суспензией, содержащей 1,5 • 106 конидий/мл. Инокулированные растения выдерживаются 24 часа при 20oC в помещении с высокой влажностью с последующим распылением тестуемого соединения, как описано в (a). После высыхания растения содержатся 6-8 дней в теплице при 22oC и 70% относительной влажности. Оценка проводится по плотности поражений на лист в сравнении с поражениями листьев контрольных растений.
(f) Активность против глазковой пятнистости in vitro пшеницы (Pseudocercosporella herpotrichoides; PHI).
Этот тест определяет in vitro активность соединений против грибка, вызывающего глазковую пятнистость пшеницы. Тестуемое соединение растворяется или суспендируется в ацетоне и добавляется в 4-миллилитровые аликвоты бульона картофельной декстрозы с половинной концентрацией, помещенные в чашки Петри с 25 секциями с получением окончательной концентрации тестуемого соединения с 10 част/милл и ацетона 0.825% Грибковый инокулят состоит из фрагментов мицелия, P.herpotrichoides, выращенного в бульоне картофельной декстрозы с половинной концентрацией во встряхиваемых колбах, и он добавлялся к бульону в количестве 5 • 104 фрагментов мицелия/мл бульона. Чашки Петри инкубировались при 20oC 10 дней до оценки мицелиального роста.
(g) Активность против Rhizoctonia in vitro (Rhizoctonia solani; RSI).
Тест определяет in vitro активность соединений против Rhizoctonia solani, которое вызывает гниение корня и стеблей. Тестуемое соединение растворяется или суспендируется в ацетоне и добавляется в 4- миллилитровые аликвоты бульона картофельной декстрозы с половинной концентрацией, разлитые в чашки Петри с 25 секциями с получением окончательной концентрации соединения в 10 част/милл и ацетона 0,825%. Грибковый инокулят состоит из мицелиальных фрагментов R. solani, выращенных в бульоне картофельной декстрозы с половинной концентрацией в колбах для культур, и добавляется к бульону в количестве 5 • 104 фрагментов/мл бульона. Чашки Петри инкубируются при 20oC 10 дней до определения роста мицелия.
(h) Активность против парши яблони in vitro (Venturia inaequalis; VII).
Этот тест определяет in vitro активность соединений против Venturia inaequalis, которая вызывает паршу яблонь. Тестуемое соединение растворяется или суспендируется в ацетоне и добавляется в 4-миллилитровые аликвоты бульона картофельной декстрозы с половинной концентрацией, разлитые в чашки Петри с 25 секциями с получением окончательной концентрации соединения в 10 част/милл. и ацетона 0,825%. Грибковый инокулят состоит из мицелиальных фрагментов и спор V. inaequalis, выращенных на солодовом агаре и добавленных к бульону в количестве 5 • 104 стадий/мл бульона. Чашки Петри инкубируются при 20oC 20 дней до оценки роста, мицелия. Степень подавления заболевания во всех вышеуказанных тестах выражена как показатель в сравнении с необработанными контрольными объектами или с контрольными объектами, обработанными разбавителем, в соответствии с критериями:
0 = подавление заболевания меньше чем на 50,
1 = подавление заболевания на 50-80%,
2 = подавление заболевания более чем на 89%.
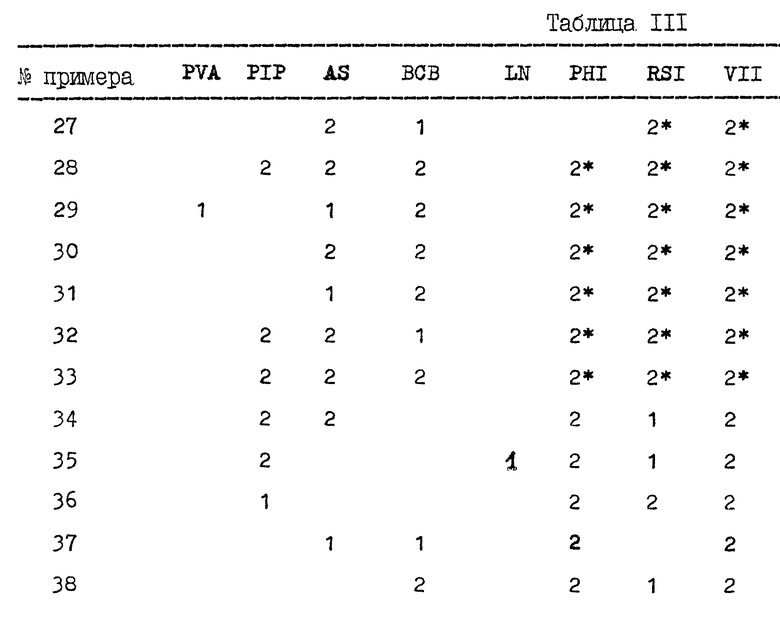
Результаты эти тестов изложены в табл. III в конце описания.
Пример 55.
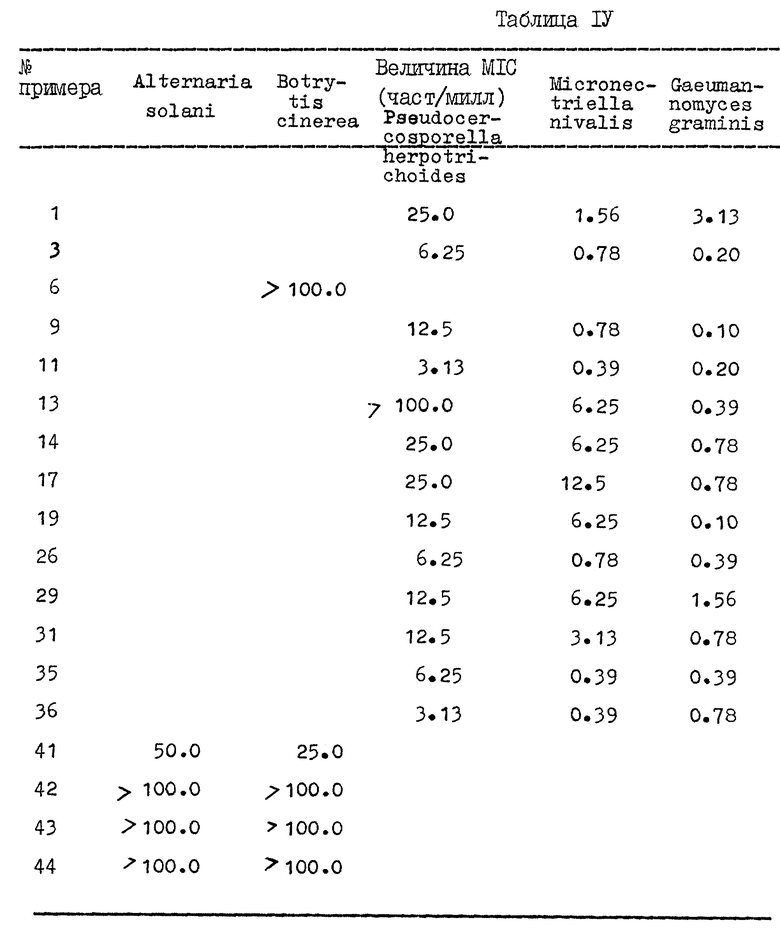
Определение MIC величин (Минимальная концентрация подавления соединений против различных фитопатогенных грибков.
Величины MIC определялись тестами серийного разбавления с использованием микротитровальных планшетов с 48 лунками. Разбавление тестуемых соединений в питательном растворе и распределение в лунки осуществлялось роботом-процессором TECAN RSP 5000.
Соединения разбавлялись до следующих концентраций: 100, 50, 25, 12,5, 6,25, 3,13, 1,56, 0,78, 0,39, 0,20, 0,10 и 0,05 μг/мл.
Для получения питательного раствора V8 сок (Тов. знак) нейтрализовался карбонатом кальция и центрифугировался. Всплывающий (супернатантный) слой разбавлялся дистиллированной водой (1:5) до окончательной концентрации.
Грибки (Alternaria solani, Botrytis cinerea, Pseudocercosporella herpotrichoides, Micronectriella nivalis, Gaeumannomyces graminis) добавлялись в лунки каплей споровой суспензии. Затем микротитровальные планшеты инкубировались при 20oC 6- 8 дней. Величина MIC низшей концентрации в серии разбавлений без роста мицелия определялась визуальным осмотром планшетов.
Результаты этих тестов изложены в табл. IV в конце описания.
Пример 56.
Определение минимальной концентрации подавления тестуемых соединений в тесте серийного разбавления с фитопатогенными грибками Alternaria solani, Botrytis cinerea, Rhizoctonia solani.
Тест серийного разбавления проводился с использованием микротитровальных планшетов с 24 или 48 лунками на планшет. Тестуемые соединения использовались в виде 1000 μг/мл водной суспензии, содержащей 20% ацетона, которая затем стерильно фильтровалась через 0,2 μ фильтр. Разбавление стерильной фунгицидной суспензии питательным раствором и последующее закапывание в лунки проводилось с использованием робота-процессора TECAN RSP5000. Диапазон тестуемых концентраций был от 100 μг/мл до 0,05 μг/мл. Делалось 12 разбавлений. Питательный раствор выбирался в соответствии с питательными потребностями патогена.
Инокулят добавлялся каплей (50 μл) споровой суспензии (5 • 108) мл в лунки.
Оценка
После 6-12 дней инкубации при подходящих температурах величина MIC определялась визуальной оценкой. Наинизшая концентрация в ряде разбавления без роста мицелия была определена как MIC величина. Результаты изложены в табл. V в конце описания.
Пример 57.
Полевое испытание на Cercospora arachidicola арахиса.
15 семян арахиса были посажены в горшочки, наполненные почвенным субстратом. Когда растения выпустили 4 истинные листа (приблизительно 12-14 дней после посева) они обрабатывались из ручного распылителя фунгицидами и тестуемыми соединениями. Тестуемые соединения применялись с концентрацией 500 μг/мл в смеси, содержащей 10% ацетон и 0,05% Tritor X 155 в воде. Общее количество распылительной смеси соответствовало 1000 л/га. На обработку использовалось 6 горшочков. Через 2 дня после обработки горшочки выставлялись в поле рядом с растениями арахиса, на которых грибок Cercospora arachidicola образовал участки споруляций. Оценка проводилась через 15 дней после обработки определением процента заражений площади листа. Процентная эффективность рассчитывалась с использованием формулы Эббота.
Полевое испытание на Puccinia arachidis на арахисе.
15 семян арахиса были посажены в горшочки, наполненные почвенным субстратом. Когда растения выпустили 4 истинные листа, они обрабатывались из ручного распылителя фунгицидами и тестуемыми соединениями. Тестуемые соединения применялись с концентрацией 500 μг/мл в смеси, содержащей 10% ацетон и 0,05% Triton X 155 в воде. Общее количество распылительной смеси соответствовало 1000 л/га. На обработку делалось 6 повторов. Через 2 дня после обработки горшочки выставлялись в поле рядом с растениями, на листьях которых грибок Puccinia arachidis образовал спорулирующие пустулы. Оценка проводилась через 19 дней после обработки определением процентного показателя зараженной площади листа. Процентная эффективность рассчитывалась с использованием формулы Эббота.
Результаты изложены в табл.VI.
Примеры композиций.
Пример A.
Суспензионный концентрат (SC).
Активный компонент - Соединение N 37 100,0 г
Анионный ПАВ - Morwet® D4251) 25,0 г
Диспергирующий агент - Pluronic® PE 105002) 5,0 г
Биоцид - Proxel® CXL3) 1,5 г
Пеногаситель - Rhodorsil® 4264) 2,0 г
Гетерополисахарид - Rhodopol® 234) 3,0 г
Антифриз - Propylene glicol 50.0
Вода - 866,5 г
Распределение по размеру частиц - Размер частиц [мкм]
x10 - 0,78
x50 - 1,95
x90 - 4,52
Плотность пр 20oC: 1,053 г/мл
Внешний вид: гомогенная, светло-бежевая суспензия;
SC хорошо диспергируемая в воде.
Пример Б.
Смачиваемый порошок
Активный компонент - Соед. примера N 37 200,0 г
Анионный ПАВ - Tensiofix® LX Spezial5) 90,0 г
Анионный ПАВ - Tensiofox® BCZ5) 30,0 г
Носитель/наполнитель - Kaolin 680,0 г
Распределение по размеру частиц: - Размер частиц [мкм]
x10 - 1,66
x50 - 6,54
x90 - 17,15
Внешний вид: гомогенный свободно-текущий светло-бежевый порошок, хорошо смачиваемый и диспергируемый в воде.
1) Продукт закуплен у фирмы S.A. Witko, Франция
2) Продукт закуплен у фирмы BASF AG, Германия
3) Продукт закуплен у фирмы Zeneca GmbH, Германия
4) Продукт закуплен у фирмы  Германия
Германия
5) Продукт закуплен у фирмы Omnichem.




Изобретение относится к фунгицидной композиции, новым производным триазолопиримидина, способу их получения и способу борьбы с грибками. Описывается фунгицидная композиция, включающая активный компонент - производное триазолопиримидина и носитель. В качестве указанного производного она содержит эффективное количество триазолопиримидинового соединения общей формулы I, в которой R представляет собой C1-C6-алкильную, C1-C6-алкоксигруппу, C3-C8-циклоалкильную группу; фенил, замещенный 1-3 заместителями, выбранными из атомов галогена, C1-C4-алкила, C1-C4-галогеналкила, C1-C4-алкокси, C1-C4-галогеналкокси, галогенсульфонила, фенила, фенокси и бензилоксигрупп; C1-C4-алкокси, фенилоксигруппу, замещенную атомом галогена или C1-C4-алкилом; нафтил или тиенил; Hal - атом Сl или Вr. Описывается способ получения производных триазолопиримидина формулы I, заключающийся в том, что соединение общей формулы II, где значение R определено пп. 5 и 6 формулы, подвергают взаимодействию с хлорирующим или бромирующим агентом. Способ борьбы с грибками включает обработку соединением формулы I. 3 с. и 7 з.п. ф-лы, 6 табл.
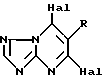
в которой R представляет собой C1-C6-алкильную, C1-C6-алкоксигруппу, C3-C8-циклоалкильную группу; фенил, замещенный 1 - 3 заместителями, выбранными из атомов галогена, C1-C4-алкила, C1-C4-галогеналкила, C1-C4-алкокси, C1-C4-галогеналкокси, галогенсульфонила, фенила, фенокси и бензилоксигрупп; фенилоксигруппу, замещенную атомом галогена или C1-C4-алкилом; нафтил или тиенил;
Hal - атом Cl или Br.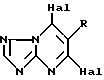
в которой R представляет собой C1-C6-алкильную, C1-C6-алкоксигруппу, C3-C8-циклоалкильную группу; фенилоксигруппу, замещенную атом галогена или C1-C4-алкилом; или тиенил;
Hal - атом Cl или Br, при условии, что когда заместитель R представляет собой метильную группу, то обе группы заместителя Hal не являются атомами хлора.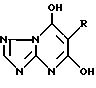
в котором заместитель R принимает значения, определенные в пп.5 и 6,
реагирует с хлорирующим или бромирующим агентом.
| Способ получения производных пиразолпиримидина | 1987 |
|
SU1528322A3 |
| Способ получения триазолсульфонамидов | 1987 |
|
SU1644719A3 |
| Способ получения производных триазолопиримидина или их солей с метансульфокислотой | 1984 |
|
SU1347865A3 |
| Гербицидное и рострегулирующее средство | 1987 |
|
SU1658808A3 |
| Способ борьбы с ростом нежелательных растений | 1989 |
|
SU1823786A3 |
| Прибор для автоматического бесконтактного измерения толщины листовых материалов | 1960 |
|
SU141317A1 |
| DE 3533050, 1987 | |||
| Плита и система крепления для плит | 1999 |
|
RU2223371C2 |
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
| Прибор для автоматического бесконтактного измерения толщины листовых материалов | 1960 |
|
SU141317A1 |
| Кассета для красящей ленты | 1973 |
|
SU550113A3 |
Авторы
Даты
1999-05-20—Публикация
1994-03-03—Подача