Изобретение относится к способу получения 13α- 1,3,5-10-триен-19-норандростан-3-ол-17-она (13α-эстрона) и его метилового эфира, формулы: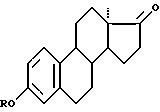
где R = H, Me,
являющихся полупродуктами в синтезе активных 13 α -19-нор-17-кетостероидов [1] , пригодных в качестве антигестагенов и посткоитальных контрацептивов [2, 3, 4].
Известен способ получения 13α-эстрона и его метилового эфира непосредственно из 13β-эпимеров с выходами до 31%, заключающийся в облучении их диоксановых растворов ртутной лампой с использованием излучения с длиной волны 313 нм в течение 28 дней с последующим разделением смеси 13α- и 13β- изомеров действием реактива Жерара [5]. К недостаткам указанного метода относятся нетехнологичность, низкий выход целевых продуктов и трудности в их выделении.
Известны также способы получения метилового эфира 13 α -эстрона в несколько стадий.
Один из них заключается в изомеризации предварительно получаемого 17-оксима метилового эфира 13β-эстрона при 12 часовом кипячении в смеси уксусного ангидрида и пиридина в инертной атмосфере с последующим гидролизом образовавшихся 17-моно- и диацетиламидопроизводных метилового эфира 13α- 1,3,510-триен-19-норандростан-3-ол-17-она, которые выделяются хроматографически на силикагеле [6]. Выход метилового эфира 13α-эстрона составляет 65%. Этот способ также имеет недостатки: необходимость получения и выделения промежуточных продуктов (оксима, моно- и диацетиламидопроизводных), продолжительность и сложность синтетической процедуры.
Другой способ состоит в изомеризации 17-оксима метилового эфира 13β-эстрона (в свою очередь получаемого из исходного 17-кетона) действием порошка никеля в условиях кипячения в смеси уксусной кислоты и октана [7]. Выход 13α-эстрона составляет 67% на исходный оксим. К недостаткам этого метода можно отнести необходимость введения дополнительной стадии получения промежуточного оксима и как следствие уменьшение выхода целевого продукта.
Задачей изобретения является упрощение синтеза путем устранения промежуточных реакций при переходе от производных 13β-эстрона к 13α- эпимерам; снижение времени проведения реакции за счет уменьшения количества стадий процесса; увеличение выхода целевых продуктов.
Поставленная задача решается тем, что синтез указанных соединений проводят в одну стадию и в качестве реагентов используют эстрон (или его метиловый эфир) и 1,2-фенилендиамин или его 4-моно- и 4,5-дизамещенные при кипячении в уксусной кислоте или ее водных растворах в присутствии кислорода воздуха. При этом выход целевых продуктов повышается до 87%.
Способ получения предлагаемого соединения представлен следующей схемой реакции: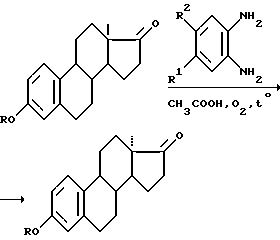
Химическая структура полученных соединений была доказана с использованием спектральных методов (ЯМР 1H, 13C) и сравнением с литературными данными.
Пример 1. Получение 13α- 1,3,510-триен-19-норандростан-3-ол-17-она .
В раствор 2.70 г (0.01 М) 13β- 1,3,510-триен-19-норандростан-3-ол-17-она в 50 мл ледяной уксусной кислоты добавляют 1.10 г (0.01 М) 1,2-фенилендиамина. Реакционную смесь кипятят с обратным холодильником 3 ч, охлаждают и оставляют стоять на ночь. Выпавший белый осадок отфильтровывают и сушат при 80oC 4 ч. Получают 2.00 г технического 13α- 1,3,510-триен-19-норандростан-3-ол-17-она с т. пл. 165 - 170oC. Исходную реакционную смесь выливают в воду, экстрагируют хлороформом и хроматографируют на колонке с силикагелем (элюент - хлорформ). Получают 0.30 г 13α- 1,3,510-триен-19-норандростан-3-ол-17-она с т. пл. 169 - 172oC и 0.25 г исходного стероида (Rf = 0.56, Rf = 0.47 (хлороформ - этанол = 24 : 1) соответственно). Кристаллизация объединенных порций 13α- стероида из смеси метанол - хлороформ = 7 : 5 дает продукт массой 2.20 г с т. пл. 174 - 175oC (лит. т. пл. 173 - 174oC [5]). Общий выход составляет 85.2%. ЯМР 1H (ДМСО-D6), δ, м.д.: 0.97 (18-CH3, 3H), 6.44.. . 7.04 (Ar, 3H), 8.9 (OH, 1H); ЯМР 13C (ДМСО-D6), δ, м.д.: 24.44 (18-CH3), 154.79 (3-C), 220.32 (17-C).
Результатыопытовпополучению13α-1,3,510-триен-19-норандростан-3-ол-17-она (13α-эстрона) в различных условиях с использованием как 1,2-фенилендиамина, так и его замещенных приведены в табл.1. Из данных табл.1. следует: а) высокий выход 13α-эстрона достигается при использовании всех предложенных диаминов, но наибольший выход получен в случае 4-метил и 4,5-диметил-1,2-фенилендиаминов; б) увеличение времени реакции свыше 3 ч не приводит к увеличению выхода целевого продукта; в) наиболее высокий выход целевого стероида получен при использовании ледяной уксусной кислоты.
Пример 2. Получение метилового эфира 13α- 1,3,510-триен-19-норандростан-3-ол-17-она.
В раствор 2.85 (0.01 М) метилового эфира 13β- 1,3,510-триен-19-норандростан-3-ол-17-она в 50 мл ледяной уксусной кислоты добавляют 1.10 г (0.01 М) 1,2-фенилендиамина. Реакционную смесь кипятят с обратным холодильником 3 ч, охлаждают и оставляют стоять на ночь. Выпавший белый осадок отфильтровывают и сушат при 80oC 4 ч. Получают 2.00 г технического метилового эфира 13α- 1,3,510-триен-19-норандростан-3-ол-17-она с т. пл. 125 - 129oC. Исходную реакционную смесь выливают в воду, экстрагируют хлороформом и хроматографируют на колонке с силикагелем (элюент - хлороформ). Получают 0.55 г метилового эфира 13α- 1,3,510-триен-19-норандростан-3-ол-17-она с т.п. 127 - 129oC и 0.20 г исходного стероида (Rf = 0.56, Rf = 0.47 (хлороформ - этанол = 24 : 1) соответственно). Кристаллизация объединенных порций 13α- стероида из метанола дает продукт массой 2.30 г с т.п. 131 - 132oC (лит. т. пл. 130 - 133oC [6] ). Общий выход составляет 82.4%. ЯМР 1H (CDCL3), δ, м.д.: 1.05 (18-CH3, 3H), 3.76 (3-OCH3, 3H), 6.59...7.20 (Ar, 3H); ЯМР 13C (CDCL3), δ, м.д.: 25ю04 (18-CH3), 55.10 (3-OCH3), 157.41 (3-C), 221.61 (17-C).
Результаты опытов по получению метилового эфира 13α- 1,3,510-триен-19-норандростан-3-ол-17-она (метилового эфира 13α эстрона) в различных условиях с использованием как 1,2-фенилендиамина, так и его замещенных приведены в табл. 2. Из данных табл. 2 следует: а) высокий выход метилового эфира 13α- эстрона достигается при использовании всех предложенных диаминов, но наибольший выход получен при использовании 4-метил- и 4,5-диметил-1,2-фенилендиаминов; б) увеличение времени реакции свыше 3-4 ч не приводит к увеличению выхода целевого продукта; в) наиболее высокий выход целевого стероида получен при использовании ледяной уксусной кислоты.
Источники информации.
1. Teutsoh. G., Belanger A..- Tetrahedron be-tters.- 1979.-P. 2051.
2. Neef G., Beler S., Elger W., Henderson D., Wieoher-t R..- SteroicLB.- 1984.- Vol.44.- N 4.- p.349-72.
3. Пат. 129499 EP, МКИ C 07 J 41/00. 13 α -Alkylgonanes and phartnaoeu-tioal oomposi-tionB containing them / Neef G., Sauer G., Wieohert R., Beier S. , Elger W. , Henderson D., Rohde R. (ФРГ); Sobering A.-G. (ФРГ). 3321826; Заявлено 15.06.1983; Опубл. 27.12.1984.-34 с.
4. Заявка4216004 ФРГ, МКИ A 61 K 31/565. Use of oompetitive progesterone antagonists as female oontraoeptives /Sohering A. -G. (ФРГ).- Заявлено 12.05.1992; Опубл. 18.11.1993.-7 с.
5. H. WerIi, K. Sohaffner Mitteilung Zur UV.- Bestrahiung von 17-oxo- Steroiden.- Helvetioa Chimioa Aota.- 1962.- Vol.45.- N 43-44.- P. 385-9.
6. Boar R.B., Jetuah F.K., Meghie J.F., Robinson M.S., Barton D.H.R. An improved synthesis of 13-epi-AndroBtanes and 13-epi-Oestranes.- J.Chem.Soo. Perkin Trans.l..- 1977.- N 19.- p.2163-5.
7. Jean Boivin, Anne-Marie Schiano, Samir Z.Zard A novel and praotioal aooes to 13-epi-17-ketosteroids. - Tetrahedron betters.- 1992.- Vol.33.- N 51.-P. 7849-52.
| название | год | авторы | номер документа |
|---|---|---|---|
| 15,15-ДИАЛКИЛСТЕРОИДНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2147306C1 |
| 20-АМИНОЗАМЕЩЕННЫЕ СТЕРОИДЫ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ | 1995 |
|
RU2146680C1 |
| 16α,17α-ЦИКЛОГЕКСА-17β-(2'-ГИДРОКСИЭТИЛ)-13β-МЕТИЛГОНА-1,3,5(10)-ТРИЕН-3-ОЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2601423C1 |
| СТЕРОИДЫ, СПОСОБ ПОЛУЧЕНИЯ СТЕРОИДОВ, СПОСОБ ПОЛУЧЕНИЯ 16-МЕТИЛЕНСТЕРОИДОВ, СОЕДИНЕНИЯ | 1992 |
|
RU2099346C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТЕРОИДНЫХ СОЕДИНЕНИЙ | 1971 |
|
SU293345A1 |
| ТМ. Кл. С 07с 169/08УДК 547.689.6.07(088.8) | 1973 |
|
SU379088A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 17α -ГИДРОКСИ-3-ОКСОАНДРОСТ-4-ЕН- 17β -КАРБОНОВЫХ КИСЛОТ | 1985 |
|
SU1314641A1 |
| Способ получения стероидных /16 @ ,17 @ /-циклогексен-21-карбоновых кислот или их эфиров | 1980 |
|
SU1055334A3 |
| 14,17-C-МОСТИКОВЫЕ СТЕРОИДЫ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1995 |
|
RU2169153C2 |
| [N'-(Изо)хинолилметилен]гидразиды 3-метокси-13,17-секоэстра-1,3,5(10)-триен-17-овой кислоты | 2023 |
|
RU2801166C1 |

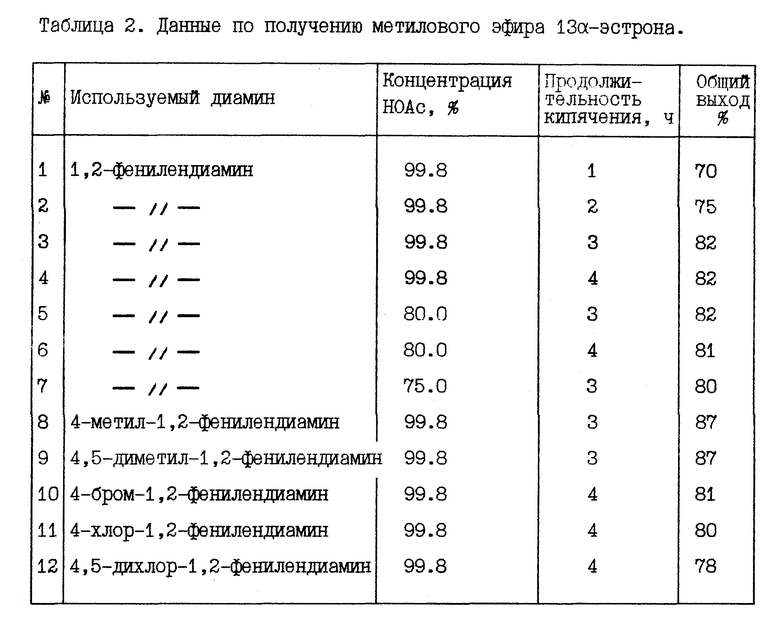
Изобретениекасаетсяполучения13α-1,3,510-триен-19-норандростан-3-ол-17-она (13α-эстрона) и его метилового эфира формулы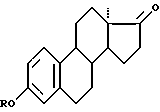
где R = Н, Ме,
являющихся полупродуктами в синтезе активных 13α-19-норстероидов. Новизна способа получения заключается в использовании в качестве реагентов 3-замещенного 13β-1,3,510-триен-19-норандростан-3-ол-17-она и 1,2-фенилендиамина или его 4-моно- и 4,5-дизамещенных производных и проведении реакции в уксусной кислоте или ее водных при кипячении растворах, в присутствии кислорода воздуха. Процесс представлен на схеме: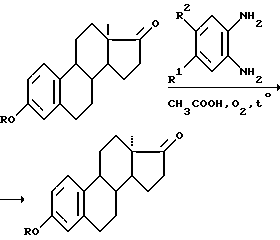
Предлагаемый способ отличается от известных ранее одностадийностью, сокращением времени реакции, высоким общим выходом целевых продуктов. 1 з.п. ф-лы, 2 табл.
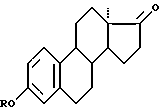
где R - H, Me,
отличающийся тем, что соединение формулы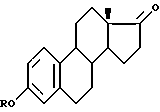
где R - H, Me,
вводят в реакцию с соединением формулы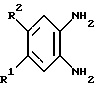
где R1-H, Me, Cl, Br, OMe;
R2-H, Me, Cl,
в уксусной кислоте или ее водных растворах при кипячении в присутствии кислорода воздуха в течение 1 - 4 ч с последующим выделением целевых продуктов известными методами.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Teutseli G., Balanger A | |||
| Tetrahedron Letters , 1979, p.2051 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Neef G., Beier S., Elger W., Henderson D., Wiechert R | |||
| Steroids | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| EP, 0129499, 1984 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| DE, 4216004, A1, 1993 | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| H.Werli, K.Schaffner Mitteilung Zur UV | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Baar R.B., Jetuah F.K., Meghie J.F., Rolinson M.S., Barton D.H.R., An improved synthesis of 13-epi-Androstanes and 13-epi-Oestrannes | |||
| J | |||
| Chem Soc., Perkin Trans | |||
| J., 1977, N19, p.2163-5 | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Jean Boivin, Anne-Marie Schiano, Samir Z.Zard | |||
| Насос | 1917 |
|
SU13A1 |
| Tetraheedron letters | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
Авторы
Даты
1999-04-20—Публикация
1995-04-06—Подача