Изобретение относится к катализаторам для процессов удаления из воды растворенных в ней нитритов и/или нитратов путем их восстановления в присутствии водорода (процессы гидроденитрификации воды).
Проблема денитрификации вод (особенно питьевых) имеет большое экологическое значение и приобретает особую остроту в настоящее время. Это обусловлено интенсивным использованием в сельском хозяйстве азотсодержащих минеральных удобрений, проникающих в грунтовые воды, в естественные и искусственные водоемы. Концентрация нитратов в этих водах значительно возросла за последние годы и достигла к настоящему времени во многих регионах критического уровня. Наибольшую опасность, для человека представляют не столько нитраты, сколько нитритные формы солей, которые образуются в результате восстановительных реакций и других химических превращений, происходящих в воде в естественных условиях. Нитриты подавляют процессы переноса кислорода в крови и при этом способны превращаться в канцерогенные нитрозамины. Для того, чтобы защитить здоровье человечества Международная Организация Здоровья (WHO) разрабатывает и упорядочивает допустимые нормы содержания нитрат/нитритов в воде на основе научно обоснованного решения этой проблемы.
Нитрат/нитриты являются стабильными, хорошо растворимыми солями, плохо адсорбируемыми и неспособными к соосаждению. Названные свойства этих солей создают принципиальные трудности для их удаления из вод такими традиционными методами обработки водных сред, как умягчение путем известкования с последующей фильтрацией.
Известны биологические методы денитрификации (см., например, J.Envir. Engn. , 1997, 4, 371-; A.Kapoor, T.Viraraghavan, Nitrate removal from drinking water). Однако эти методы характеризуются существенными недостатками, поскольку это весьма медленные и трудноуправляемые процессы, при этом не обеспечивающие полной очистки. Следует выделить два существенно негативных фактора, присущих технологии прямой биологической денитрификации воды: (1) очищаемая вода должна быть тщательно перемешена с вводимыми в нее биологическими культурами и (2) в воду должны быть введены органические соединения (как источник энергии для функционирования биологической реакции денитрификации), что само по себе создает новые проблемы в процессах денитрификации вод.
Известны различные физико-химические процессы денитрификации вод, такие как, например, ионо-обменные технологии, осмотические методы разделения, методы электродиализа ( см. там же: J.Envir.Engn., 1997). Однако применение этих методов требует больших финансовых затрат и связано с использованием больших масс твердых компонентов, подлежащих удалению из очищаемых вод. Регенерация отработанных ионо-обменных смол, связанная с использованием концентрированных растворов хлорида или бикарбоната натрия, требует организации производства больших количеств рассола. Применение осмотических мембран сопровождается появлением таких эксплуатационных затруднений, как их засорение, уплотнение (рост сопротивления) и потеря фильтрующей способности мембран. Процессы электродиализа все еще находятся в начальной стадии развития и их стоимость весьма велика.
Химический процесс восстановления нитратов и/или нитритов из вод с помощью Fe(OH)2 сопровождается образованием больших количеств железосодержащего шлама. Восстановление нитрат/нитритов в воде методом электролиза описано в патенте США N 4956057. Однако и эти методы дорогостоящи и нетехнологичны.
Денитрификация воды методом каталитического восстановления нитратов и/или нитритов является единственным процессом, который позволяет обеспечить 100%-ую очистку воды от этих примесей. Процесс базируется на использовании металлсодержащих катализаторов на носителе, на которых при участии водорода растворенные в воде нитрат/нитриты восстанавливаются до азота, что и обеспечивает денитрификацию водной среды. Такой способ описан в изобретении авторов K. D.Vorlop и др., запатентованном в Германии - патент N DE 3830850 A1,1988, МКИ C 02 F 1/70 и в США - патент N US 5122496, 1992, НКИ 502./245. Данное техническое решение является наиболее близким к заявляемому предлагаемому изобретению и выбирается за прототип.
В прототипе запатентован металлсодержащий катализатор на порошкообразном носителе, находящийся в очищаемой водной среде в суспендированном состоянии. Такой катализатор характеризуется существенными недостатками. Во-первых, управление процессом на порошковом суспендированном катализаторе существенно затруднено. Во-вторых, порошковая форма катализатора требует применения реакторной аппаратуры, оборудованной перемешивающими устройствами, необходимыми для образования суспендированной реакционной среды и преодоления лимитирующих интенсивность денитрификации диффузионных затруднений. В-третьих, порошковый суспендированный катализатор связан с необходимостью введения в технологический процесс стадий фильтрационного освобождения от него очищаемых водных сред. Существование в схеме стадий фильтрования требует значительных энергетических затрат и обуславливает технологически невыгодный периодический режим работы. Кроме этого, чтобы повысить селективность гидрирования нитратов до азота и уменьшить образование ионов аммония (компонента не токсичного, однако присутствие которого в питьевых водах крайне нежелательно), при применении описанного прототипа приходится наряду с Pd/Cu-катализатором (в соотношении 4:1) вводить дополнительно Pd-содержащий катализатор, который обеспечивает полноту восстановления нитритов.
Целью настоящего предлагаемого изобретения является устранение названных недостатков.
Эта цель достигается в результате использования для процесса денитрификации вод металлсодержащего катализатора на неорганическом носителе, изготовленном из стекловолокнистых материалов, диаметр волокон которых находится в интервале 1-10 мкм имеющих пористую структуру с площадью внутренней поверхности 2-100 м2/г, применяемых в форме тканых изделий и нетканых блоков, содержащих в своем составе металл из ряда палладий, родий и/или из палладия, модифицированного металлами из группы медь, олово, индий, серебро, цинк при общем содержании металла в волокнистом носителе в интервале 0,01-1,0 мас.%
Каталитическое восстановление нитрат/нитритов в воде при участии водорода может быть записано в обобщенном виде следующими уравнениями химических реакций:
2NO3 - +5H2 ---> 4N2 + 4H2O + 2OH-;
NO2 - + H2 ---> N2 + 2OH-;
NO2 - + 3H2 ---> NH4 + + 2OH-.
Кислород, растворенный в воде, восстанавливается на том же катализаторе водородом до начала реакций денитрификации
O2 + 2H2 ---> 2H2O.
Гидроксильные ионы, образующиеся в ходе процесса в эквивалентных концентрациях, нейтрализуются кислотами (HCl или CO2)
H+ + OH- ---> H2O;
CO2 + OH- ---> HCO3 -.
Важно отметить, что катализатор, предлагаемый в данном изобретении, должен быть сформирован таким образом, чтобы реакции восстановления реализовались в водной среде без применения порошковых суспендируемых носителей. Решение этой задачи и преодоление всех недостатков, присущих порошковым суспендированным катализаторам (см. вышеприведенный анализ катализатора по патенту-прототипу), оказалось возможным для катализатора, защищаемого данным предполагаемым изобретением, характеризуемого следующими отличающими его от прототипа признаками:
1. Предлагаемый катализатор формируется на основе стекловолокнистого носителя.
2. Диаметр элементарных волокон стекловолокнистого носителя лежит в интервале 1 -10 мкм.
3. Волокно стекловолокнистого носителя характеризуется низкопористой структурой с площадью внутренней поверхности 2-100 м2/г.
4. Стекловолокнистый носитель содержит в себе активные металлы из ряда палладий, родий и/или из композиций палладия по крайней мере с одним металлическим промотором, выбранным из группы металлов, включающей медь, олово, индии, серебро, цинк, при общем содержании активного металла в интервале 0,01- 1,0 мас.%.
5. Катализатор на основе стекловолокнистого носителя, изготавливаемый из тканых и нетканых материалов.
6. Катализатор на основе стекловолокнистого носителя размещается в реакторе (а) в виде ковриков, расстилаемых на колесниках, (б) в форме рулонной скрутки, запрессованной в трубки реактора, или (в) в виде полотнищ, закрепленных на элементах перемешивающих устройств реактора.
Активность предлагаемых в данном изобретении катализаторов в отношении реакций денитрификаии вод зависит от метода приготовления катализатора, от структуры используемого стекловолокнистого носителя, от природы активных металлических компонент, а также от их распределения на носителе. Как показали исследования (см. примеры), процесс денитрификации воды в соответствии с предлагаемым техническим решением эффективно протекает на стекловолокнистых катализаторах. Анализируя этот положительный (по сравнению с прототипом) результат, можно выделить следующие химические и физические причины, обеспечившие достижение качественного скачка в параметрах процесса денитрификации:
а) оказалось, что вводимый в стекловолокнистый носитель металл (в частности, палладий) приобретает особое состояние по уровню каталитической активности, что позволяет снизить его содержание, приблизительно, на порядок;
в) малость размеров элементарного волокна (1-10 мкм) в стекловолокнистом носителе предлагаемого катализатора обеспечивает интенсификацию процесса за счет снижения диффузионных затруднений;
г) применение предлагаемого катализатора на стекловолокнистом носителе (как альтернатива порошковому катализатору в изобретении-прототипе) позволяет исключить из технологической схемы сложную и дорогостоющую операцию фильтрационной очистки и перевести процесс на непрерывный режим.
В качестве каталитически активных металлов, вводимых в стекловолокнистый носитель, использованы палладий и родий. Однако для этих целей могут быть использованы и другие переходные металлы. Процесс денитрификации воды эффективно протекает на палладированном стекловолокнистом носителе, в котором в качестве промотирующего элемента введены металлы, выбранные из группы Сu, Sn, In, Ag, Zn, однако и другие элементы могут быть использованы в предлагаемом катализаторе в качестве промоторов.
Выбор оптимального катализатора при его освоении в производственных условиях должен определяться требованиями к уровню интенсивности процесса, степени очистки, а также экономическими оценками эффективности технологической схемы.
Каталитически активные металлы могут вводиться в стекловолокнистый носитель различными способами. В российском патенте RU N 2069584, 1996, МКИ В 01 J 23/38 (авторов Барелко и др.) упомянут способ, основанный на введении каталитически активного металла в стадии формирования расплавленной стекломассы. Приготовление катализаторов, данные испытаний которых приведены в таблицах, проводилось в операциях ионного обмена, т.е. путем пропитки стекловолокинстого носителя в растворах солей вводимого металла (в частности, в растворах солей хлористого палладия).
Предлагаемый катализатор может быть использован в процессах денитрификацин вод при содержании в них нитрат/нитритов в широком диапазоне концентраций. Оптимизация процесса удаления нитрат/нитритов на предлагаемом катализаторе проводится в зависимости от начальной концентрации нитрат/нитритов, от значения pH обрабатываемой среды, от скорости подачи водорода и от температуры процесса.
Растворимость водорода в воде при 10-35oC составляет приблизительно 2 мл/л при атмосферном давлении, при этом с увеличением давления растворимость возрастает линейно. Таким образом, в случаях денитрификации сильно загрязненных вод, требующих повышенного расхода водорода, процесс на предлагаемом катализаторе можно вести под увеличенным давлением. Насыщение воды водородом может осуществляться любыми известными способами (например, с использованием газосатурирующих устройств). Однако отметим, что для оптимальной эффективности процесса важно тонкое распыление вводимого в реактор водорода и предотвращение процесса укрупнения пузырей при барботаже водорода через обрабатываемую воду. Для реализации этого требования могут быть использованы специальные диспергирующие мембраны. Процесс денитрификации на предлагаемом катализаторе идет активно при температурах 5-30oC, наиболее предпочтительный интервал 10-25oC.
В ходе процесса необходимо регулирование pH среды, чтобы обеспечить нейтрализацию гидроксил-ионов.
В проведенных исследованиях показана возможность осуществления денитрификации на предлагаемом катализаторе для широкого круга различных водных сред: грунтовых вод, сточных вод, питьевых вод, а также минеральных вод и фруктовых соков. Таким образом, используемый в описании изобретения термин "вода" охватывает широкий спектр водных сред.
Для представления более детальной информации о процессе денитрификации с использованием предлагаемого катализатора и иллюстрации преимуществ этого катализатора ниже дается описание ряда характерных примеров. Эксперименты, нашедшие отражение в примерах 1-18, проведены с образцами предлагаемых катализаторов, характеризующимися следующими параметрами:
- стекловолокнистый материал, использованный в качестве носителя, относится к классу силикатных стекол с содержанием SiO2 в интервале 50-98 мас.%.
- диаметр элементарного волокна стекловолокнистого носителя находился в интервале 5-7 мкм;
- площадь внутренней поверхности стекловолокнистого носителя варьировалась в интервале 2-500 м2/г;
- в качестве активного металла, вводимого в носитель, использован Pd при варьировании его содержания от 0,025 до 0,2 мас.%.
В специальных опытах (не сведенных в таблицы) установлены оптимальные диапазоны параметров предлагаемых катализаторов:
- стекловолокнистый носитель изготавливается из класса силикатных стекол с содержанием SiO2 50-98 мас.%;
- диаметр элементарного волокна 1-10 мкм;
- площадь внутренней поверхности 2-100 м2/г;
- активный металл выбирается из ряда Pd, Rd, при этом в качестве промотора может быть выбран металл из ряда Cu, Sn, In, Ag, Zn;
- общее содержание активного металла в стекловолокнистом носителе находится в интервале 0,01-1,0 мас.%.
Пример 1 (удаление нитритов из воды).
Процесс денитрификации проводился в лабораторном реакторе периодического действия, объемом 500 мл, с перемешивающим устройством и системой управления температурным режимом процесса.
Элемент предлагаемого в изобретении стекловолокнистого катализатора (в форме тканого или нетканого изделия) монтировался на специальном каркасе в виде вращающейся корзины, закрепленной на валу перемешивающего устройства.
Подача водорода в реактор осуществлялась с помощью специальной системы, содержащей устройства управления газовым потоком и давлением в реакторе.
Расход водорода поддерживался на уровне не ниже 100 мл/мин, чтобы обеспечить требуемый уровень сатурации, давление варьировалось в интервале 2,3-4,3 атм, температура процесса поддерживалась на уровне 21-25oC, частота вращения корзины с исследуемым катализатором соответствовала 300 - 400 об/мин.
Образец N 1 (описываемый в данном примере) представлял собой стекловолокнистый тканый элемент, характеризуемый величиной активной поверхности носителя 2 м2/г и содержащий Pd в количестве 0,2 мас.%. Этот элемент, имеющий массу 4,7 г, закреплялся на каркасе вращающейся корзины в реакторе. Запуск реакции производился путем введения в среду концентрированного раствора нитрита натрия. Начальные условия процесса: 400 мл раствора, 100 мг нитрита, pH - 6,5-6,8 (устанавливалось дозированным добавлением соляной кислоты). Кинетика процесса денитрификации измерялась путем спектрофотометрического анализа проб, периодически отбираемых из реактора, с использованием стандартных методов: NO3 - в полосе 220 нм с использованием аналитической процедуры восстановления кадмием в полосе 500 нм; NO2 - - с сульфатом железа в полосе 425 нм; NH4 +- с реактивом Несслера в полосе 575 HM(Standard methods for examination of water and wastewater, 18ed, 1992, Amer.Public Helth Assn. Washington, D.C.). Через 8 часов работы нитрит полностью удалялся из обрабатываемой среды.
Активность катализатора (характерная скорость превращения) измерялась путем определения темпа уменьшения концентрации нитритов в воде. После окончания эксперимента (исчезновение в пробе нитрита) проводился спектрофотометрический анализ конечного продукта на остаточное содержание аммония (по вышеуказанным стандартным методикам ). Этот анализ давал информацию о степени селективности процесса денитрификации до образования свободного азота. Все полученные результаты представлены в соответствующих графах таблицы 1.
Примеры 2-8 (удаление нитритов из воды).
Примерами 2-8 иллюстрируется влияние на процесс денитрификации, проводимый на предлагаемых катализаторах, таких параметров, как содержание и стекловолокнистом носителе активного металла, степени развитости внутренней поверхности, температуры процесса и давления в реакторе.
Опыты проводились на реакционной установке, описанной в примере 1. Все параметры по начальным условиям и по конечным результатам сведены в таблице 1.
Пример 9 (удаление нитратов из воды).
Пример 9 иллюстрирует процесс денитрификации воды на предлагаемых катализаторах для случая загрязнения воды нитратами. Опыты проводились на реакционной установке, описанной в примере 1. Каталитический элемент массой 8,7 г в форме стеклотканого изделия с содержанием палладия 0,2 мас.% и внутренней поверхностью 2 м2/г устанавливался на вращающейся корзине в реакторе таким же образом, как описано в примере 1. Все измерения кинетики процесса проводились с привлечением указанных выше стандартных аналитических методов путем периодического отбора проб из реактора. Полное удаление нитратов из воды достигалось в течение 10-11 часов. Все параметры по начальным условиям и конечным результатам процесса денитрификации сведены в таблице 2.
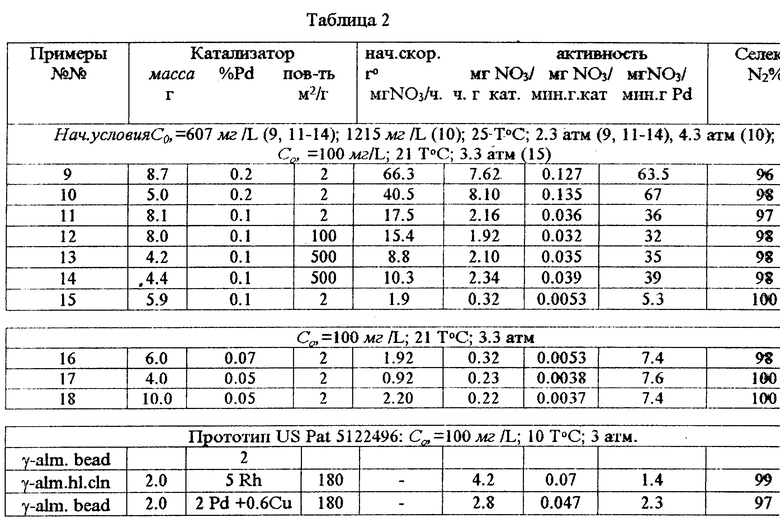
Примеры 10-18 (удаление нитратов из воды). Примеры 10-18 иллюстрируют влияние на процесс денитрификации, проводимый на предлагаемых катализаторах, таких параметров, как содержание в стекловолокнистом носителе активного металла, степени развитости внутренней поверхности, температуры процесса и давления в реакции.
Опыты проводились на реакционной установке, описанной в примере 9. Все параметры по начальным условиям и конечным результатам сведены в таблице 2.
Для оценки эффективности процесса денитрификации, реализуемого на предлагаемых катализаторах, в обеих таблицах приведены данные, характеризующие процесс денитрификации на катализаторе-прототипе. Как видно, эффективность (активность и селективность) предлагаемого катализатора существенно выше как в расчете на единичную массу палладия, так и на массу катализатора. Все другие преимущества предлагаемого катализатора по сравнению с прототипом уже были рассмотрены выше.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ДЛЯ ГИДРИРОВАНИЯ АРОМАТИЧЕСКИХ НИТРОСОЕДИНЕНИЙ | 1999 |
|
RU2156654C1 |
| КАТАЛИЗАТОР ДЛЯ КОНВЕРСИИ АММИАКА | 1999 |
|
RU2160157C1 |
| КАТАЛИЗАТОР ДЛЯ СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ АЦЕТИЛЕНОВЫХ И/ИЛИ ДИЕНОВЫХ УГЛЕВОДОРОДОВ | 1999 |
|
RU2164814C1 |
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ ДИОКСИДА СЕРЫ В ТРИОКСИД СЕРЫ | 1999 |
|
RU2158633C1 |
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2411993C1 |
| НАНОКАТАЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2411994C2 |
| СПОСОБ ДЕНИТРИФИКАЦИИ ВОДЫ | 2001 |
|
RU2240986C2 |
| КАТАЛИЗАТОР ДЛЯ ГИДРИРОВАНИЯ РАСТИТЕЛЬНЫХ МАСЕЛ И ЖИРОВ | 1999 |
|
RU2158632C1 |
| НОСИТЕЛЬ И КАТАЛИЗАТОР ДЛЯ ГЕТЕРОГЕННЫХ РЕАКЦИЙ | 1998 |
|
RU2143948C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНЕСЕННОГО КАТАЛИЗАТОРА И СПОСОБ СОПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ С МОНООКСИДОМ УГЛЕРОДА НА НАНЕСЕННОМ КАТАЛИЗАТОРЕ | 2008 |
|
RU2385185C1 |

Изобретение относится к катализаторам для процессов очистки воды от растворенных в ней нитратов и/или нитритов путем их восстановления в присутствии водорода. Катализатор для гидроденитрификации воды состоит из неорганического носителя, изготовленного из силикатных стекловолокнистых материалов, содержащих 55 - 98% оксида кремния с диаметром волокон 1-10 мкм, имеющих пористую структуру с площадью внутренней поверхности 2-100 м2/г, применяемых в форме тканых изделий и нетканных блоков, и металл из ряда палладий, родий и/или из палладия, модифицированного металлами из группы медь, олово, индий, серебро, цинк, при общем содержании металла в волокнистом носителе 0,01-1,0 мас. %. Изобретение позволяет усовершенствовать процесс гидроденитрификации воды по сравнению с известными способами и повысить его эффективность. 5 з. п.ф-лы, 2 табл.
| DE 3830850 A1, 22.03.90 | |||
| US 5122496 A, 16.01.92 | |||
| RU 95111443 A1, 20.06.97 | |||
| КАТАЛИЗАТОР ДЛЯ ХИМИЧЕСКИХ ПРОЦЕССОВ, НАПРИМЕР КОНВЕРСИИ АММИАКА, ОКИСЛЕНИЯ УГЛЕВОДОРОДОВ, ДИОКСИДА СЕРЫ, ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ | 1994 |
|
RU2069584C1 |
| US 4990266 A, 05.02.91 | |||
| US 5069800 A, 03.12.91 | |||
| US 5662809 A, 02.09.97 | |||
| DE 3906781 A1, 06.09.90 | |||
| DE 4207959 A1, 16.09.93 | |||
| DE 4323085 A1, 12.01.95 | |||
| DE 4437864 A1, 25.04.96 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| ПРОВОДКА КАЧЕНИЯ ДЛЯ СОРТОВОГО ПРОКАТА | 0 |
|
SU359074A1 |
| DE 19512955 A1, 17.10.96. | |||
Авторы
Даты
1999-07-20—Публикация
1998-07-29—Подача