Изобретение относится к области синтеза химических соединений, конкретно к синтезу металлокомплексов макрогетероциклических соединений.
Известны биядерные металлокомплексы 6,11:19,24:32,37:45, 50-тетраимино-5,52: 13,18: 20,31: 39,44-тетранитрилооктабензо (c, g, e, p, u, y, D, H) (1,10,19,28)-тетраазациклогексатриаконтина с Co (II), Cu (II), Ni (II), обладающие полупровордниковыми свойствами и способные возгоняться в вакууме [Смирнов Р.П., Андреянов В.В., Воробьев Ю.Г., Шорин В.А., Федоров М.И. Синтез и электрические свойства биядерного кобальтсодержащего макрогетероциклического соединения. Изв. вузов, Химия и хим. технология, 1984, т. 27, N 10, с. 1239 - 1241].
Использование соединений подобного строения в качестве биологически активных объектов ограничено в связи с их недостаточной растворимостью в органических растворителях.
Задачей предлагаемого изобретения является синтез биметаллического металлокомплекса макрогетероциклического соединения, растворимого в спиртах и обладающего бактериостатическим действием на кишечную палочку и стафилоккок.

Структура InClCoO2 (МГЦС) подтверждается способом синтеза, а также данными элементного анализа, колебательной и электронной спектроскопии.
InClCoO2 (МГЦС) синтезирован темплатным способом на основе диамино-β-изоиндиго [Неустроева Н. Р. , Воробьев Ю. Г. , Смирнов Р.П. Диамино-β-изоиндиго и его производные. Ивановск. гос. хим.-технолог. академ., Иваново, 1994, Деп. в ВИНИТИ г. Москва 04.07.94, 1650-В-94]. Предлагаемое соединение относится к металлокомплексам азамакрогетероциклических соединений симметричного строения с ковалентным типом связи металл - лиганд. Структурным отличием его от наиболее близкого аналога металлокомплекса 54,56: 58,60-дикобальт(II)диоксо-6,11: 19,24: 32,37: 45,50-тетраимино- 5,52:13,18: 20,31: 39,44-тетранитрилооктабензо[c, g, e,p,u,y,D,H] (1,10,19,28)-тетраазациклогексатриаконтина является то, что в состав макрогетероциклического лиганда молекулы InClCoO2 (МГЦС) входят различные по природе металлы: In (III) и Co (III) с соответствующими экстралигандами.
Предлагаемое изобретение иллюстрируется следующими примерами.
Синтез InClCoO2 (МГЦС)
Пример 1. InClCoO2 (МГЦС). 1 г диамино-β-изоиндиго (0,004 г-моль), 0,3 г ацетата кобальта (0,0009 г-моль) и 0,5 г хлорида индия (0,001 г-моль) в 100 мл осушенного этиленгликоля перемешивают 15 минут в атмосфере аргона. Затем реакционную смесь нагревают до кипения и продолжают перемешивание при этой температуре в течение 20 часов, поддерживая атмосферу инертного газа. Образовавшийся осадок отфильтровывают, промывают небольшим количеством 5%-ного раствора HCl, затем 5%-ного раствора аммиака и водой до нейтральной реакции, ацетоном в аппарате Сокслета. Сушат при 100oC. Полученный продукт подвергают хроматографической очистке на колонке, заполненной оксидом алюминия γ-формы. В качестве элюента используют смесь хлороформ-пиридин (8 : 1). Выход: 50%. Разлагается при 445oC, Rf = 0,75 (силуфол, смесь пиридин-хлороформ-1:5).
InClCoO2 (МГЦС) представляет собой мелкокристаллическое вещество темно-зеленого цвета. Растворяется в пиридине, диметилформамиде, хуже в спиртах. При растворении в концентрированных кислотах разрушается.
Данные элементного анализа удовлетворяют брутто-формуле InClCoO2 (МГЦС):
C64H32N12InClCoO2.
Найдено, %: C 63,0; H 2,8; N 13,6; M 10,8; Hal 10,5.
Вычислено, %: C 62,53; H 2,61; N 13,68; M 10,9; Hal 10,33.
Электронные спектры InClCoO2 (МГЦС): регистрировали на спектрофотометре Specord M-40 - для раствора в диметилформамиде марки "ХЧ" в области 400 - 800 нм при температуре 298 К (фиг. 1).
В электронном спектре InClCoO2 (МГЦС) наблюдается четыре полосы поглощения в видимой области. Полосы поглощения в области 406, 450 нм характеризуют π-π*-электронные переходы в системе сопряжения отдельных фрагментов диамино-β-изоиндиго, входящих в состав макрогетероциклического лиганда, а полосы в области 605, 563 нм отвечают π-π*-электронным переходам, обусловленным наличием единой замкнутой π-системы сопряжения макрокольца лиганда.
Регистрацию инфракрасных спектров InClCoO2 (МГЦС) проводили на спектрофотометре Specord - 75 IR в области 4000 - 400 см-1 с образца, запрессованного в виде таблетки с оптически активным бромидом калия (фиг. 2).
Перемешивание всех колебаний в молекулах биядерных МГЦС, присущее, как известно, высокосопряженным структурам [Казицина Л.А., Куплетская Н.Б. Применение УФ-, ИК- и ЯМР-спектроскопии в органической химии. - М.: Высшая школа, 1971, 264 с.], приводит к тому, что в их спектрах практически нет полос характеристических колебаний. Сравнительно независимыми являются валентные и неплоские деформационные колебания связей C-H изоиндольных фрагментов, к которым относятся полосы поглощения в области 3000 - 3100 см-1 и 720 - 730 см-1 соответственно, а также деформационные колебания связей C-H (1050 - 1200 см-1) и валентные колебания C=C связей бензольного кольца в области 1600, 1580, 1500 см-1. Отсутствие полос в области 3300 - 3400 см-1, характеризующих относительно независимые колебания связей N-H первичных концевых аминогрупп и внутрициклических иминогрупп, подтверждает замкнутый характер лиганда в молекуле InClCoO2 (МГЦС) и их полное замещение ионами соответствующих металлов: In (III), Co (III). Наличие связей M-N подтверждается полосой в области 400 - 500 см-1 [Казицина Л.А., Куплетская Н.Б. Применение УФ-, ИК- и ЯМР-спектроскопии в органической химии. - М.: Высшая школа, 1971, 264 с.].
Определение биологической активности InClCoO2 (МГЦС).
Испытания для определения биологически активных свойств InClCoO2 (МГЦС) проводили по методике сравнительной оценки задержки колониеобразования тест-культур, а также по определению зон лизиса данных культур под влиянием испытуемого вещества.
В качестве тест-культур использовали штаммы Escherichia coli M-17 и Staphylococcus aureus (lec+). Исходно готовили насыщенный раствор вещества в этиловом спирте, который затем вносили в объеме 10 мл в 100 мл расплавленного мясопептонного агара. Полученную таким образом питательную среду, содержащую испытуемое вещество, разливали в чашки Петри по 20 мл. Смыв суточной культуры исследуемых штаммов микроорганизмов готовили по стандарту мутности [Хитаршвили Р. П. , Осидзе Д.Ф., Биценко В.А. Методическое руководство по приготовлению и контролю бактериологических питательных сред, Тбилиси, 1977, 158 с. ] , используя для разведения физиологический раствор и затем раститровывали до конечного разведения 10 - 6, т.е. концентрация микроорганизмов в 1 мл данного разведения была десятки клеток микроорганизмов. Из этого разведения выполняли посев по 0,1 мл взвеси тест-культур на чашки Петри, содержащие исследуемое соединение, и на контрольные чашки без введенного вещества. Посевы термостатировали при температуре 370,2oC. Оценка антимикробной активности проводилась по результатам колониеобразования через 24 часа.
Постановка второй серии экспериментов заключалась в следующем: из МПА (мясопептонный агар) газоном засевали испытуемую тест-культуру микроорганизмов. После посева чашки выдерживали для устранения избыточной влаги в агар в течение 30 минут, на который затем с соблюдением правил асептики накладывали диски из фильтровальной бумаги, пропитанные исследуемым раствором. Диски предварительно стерилизовали в сухожаровом шкафу, пропитывали спиртовым раствором вещества, а спирт впоследствии удаляли подсушиванием дисков в стерильных условиях. Таким образом полностью устраняли негативное влияние растворителя на испытуемые тест-культуры, которое могло бы исказить получаемые результаты и привести к неправильной их трактовке.
В ходе проведенных экспериментов обнаружено достоверное различие между контролем и экспериментом для испытуемых тест-культур, характеризующееся изменением диаметра выросших колоний (фиг. 3).
При измерении диаметра колоний E. coli в эксперименте с добавлением исследуемого вещества было обнаружено уменьшение диаметра колоний на 30% (опыт с добавлением испытуемого вещества - D = 1,98 ± 0,02 мм, контроль D = 2,83 ± 0,03 мм). В аналогичном эксперименте с использованием Staphylococcus aureus уменьшение диаметра колоний было на 27,5% (опыт - D = 1,24 ± 0,001 мм, контроль - D = 1,71 ± 0,09 мм).
В результате эксперимента были получены следующие данные: для E. coli зона задержки роста - 1,5 ± 0,02 мм, для Sth. aureus - 1,0 ± 0,01 мм.
Итак, биологическое воздействие исследуемого вещества выражается в наличии бактериостатического влияния на тест-культуры, причем в несколько большем отношении для Escherichia coli M-17, чем для Staphylococcus aureus.
Особый интерес в эксперименте с Staphylococcus aureus вызвал факт образования вторичного фронта роста культуры внутри зоны задержки роста, который можно расценивать, как частичное преодоление бактериостатического воздействия исследуемого вещества клетками Staphylococcus aureus с последующей активизацией их развития.
Полученные данные позволяют сделать выводы о биологической активности предлагаемого соединения на внутрипопуляционное влияние передачи информации между клетками, вынужденными в адаптационный период изменить обычный режим развития колонии.
Для определения токсичности InClCoO2 (МГЦС) по методике [Беспамятнов Г. Т. , Кротов Ю.А. Предельно допустимые концентрации химических веществ в окружающей среде. Справочник. -Л.: Химия, 1985, 350 с.] определена временно допустимая концентрация данного соединения в воздухе рабочей зоны (ВДК р.з. ), которая составила: ВДК р.з. = 0,87 мг/м3.


Предложено новое биметаллическое металлмакрогетероциклическое соединение: 54,56-индий(III)хлор: 58,60-кобальт(II)оксо-6,11: 19,24: 32, 37: 45,50-тетраимино-5,52:13,18:20,31:39,44-тетранитрилооктабензо [c,g, e,p,u,y, D,H](1,10,19,28)-тетраазациклогексатриаконтин формулы I
обладающее бактериостатическим действием на стафилоккок и кишечную палочку. Описан его синтез. Доказательство структуры подтверждено данными элементного анализа, электронной и ИК-спектроскопии. 3 ил.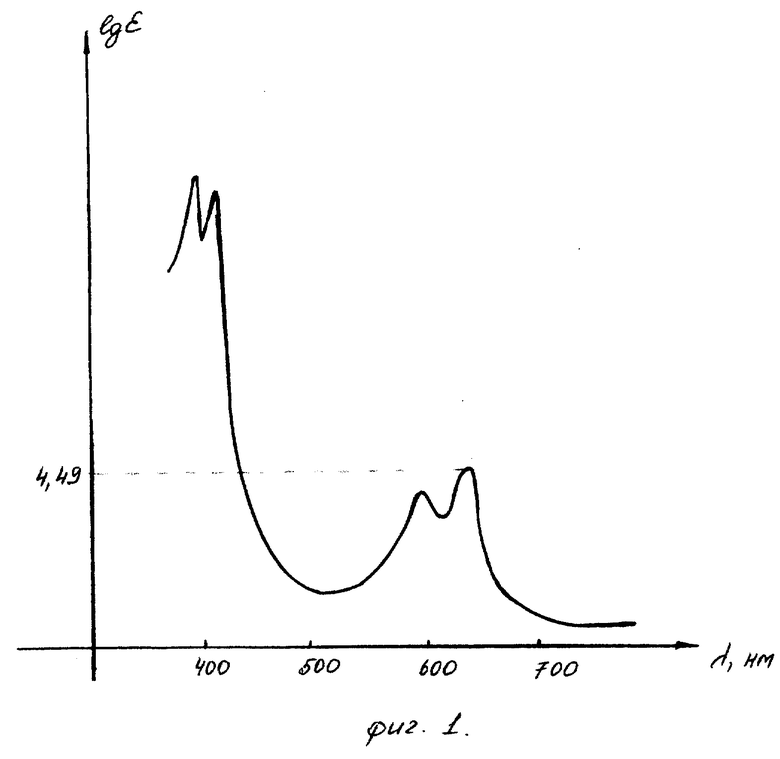
54,56-Индий(III)хлор: 58,60-кобальт (II) оксо-6,11:19,24:32,37:45,50-тетраимино-5,52: 13,18:20,31:39,44-тетранитрилооктабензо [c, g, e, p, u, y, D, H] (1,10,19,28)-тетраазациклогексатриаконтин формулы
обладающий бактериостатическим действием на стафилоккок и кишечную палочку.
| Неустроева Н.Р., Воробьев Ю.Г., Смирнов Р.П | |||
| Диамино-изоиндиго и его производные, Ивановск | |||
| гос.хим.-технолог | |||
| Академ | |||
| - Иваново, 1994, Деп | |||
| В ВИНИИТИ, М., 1994, 1650 - В- 94 | |||
| Удерживающее устройство навесного привода конвертора | 1977 |
|
SU687133A1 |
| Способ получения гептенов | 1969 |
|
SU488397A3 |
| Способ получения анионита | 1973 |
|
SU519423A1 |
| Смирнов Р.П | |||
| Андреянов В.В., Воробьев Ю.Г., Шорин В.А., Федоров М.И | |||
| Синтез и электрические свойства биядерного кобальтсодержащего макрогетероциклического соединения, Изв.вузов, Химия и хим.технология, 1984, т.27, N 10, с.1239-1241 | |||
| Гэрбэлэу Н.В., Арион В.Б | |||
| Темплатный синтез макрогетероциклических соединений | |||
| Кишинев: Штиинца, 1990, с.30-102 | |||
| Хитаршвили Р.П., Осидзе Д.Ф., Биценко В.А | |||
| Методическое руководство бактериологических питательных сред - Тбилиси, 1977, 158 с. | |||
Авторы
Даты
1999-08-27—Публикация
1995-08-31—Подача