Изобретение относится к технологии химической промышленности, конкретно - способ получения гидроксохлоридов алюминия особой чистоты, применяемых как коагулянт для очистки питьевой воды и промстоков, а также как связующее вещество в производстве керамики и огнеупоров и тампонировании скважин нефте- и газодобычи. Особо чистый продукт пентагидроксохлорид применяется в косметическом и фармацевтическом производствах.
Известные способы предлагают получать основные хлориды алюминия растворением оксида или гидроксида алюминия в соляной кислоте или хлориде алюминия.
В НИОХИМе разработан способ получения гидроксохлорида алюминия путем растворения в соляной кислоте активированного гидроксида алюминия. Технический гидроксид алюминия высушивают и подвергают термической обработке и затем растворяют в хлориде алюминия при температуре 95-98oC. Раствор гидроксохлорида алюминия отделяют от нерастворимого остатка, осадок растворяют в соляной кислоте с целью получения хлорида алюминия.
Высокая себестоимость применяемых оксида и гидроксида алюминия в производстве получения основных хлоридов алюминия, необходимость в дополнительной обработке нерастворимого осадка соляной кислотой при температуре 95-100oC, дополнительные затраты на соляную кислоту и условия работы с кислотой являются существенными недостатками.
При небольших мощностях производства имеют преимущество способы с анодным растворением металлического алюминия (авторское свидетельство N 132624, СССР; патент N 1398820, Франция). В качестве анодного материала можно использовать алюминиевые обрезки, стружку, опилки и другие отходы металла, имеющиеся на машиностроительных предприятиях.
Способ получения основных хлоридов алюминия описан в патенте N 2791486 (Англия). Часть ионов хлора замещают гидроксильными группами путем пропускания раствора хлорида алюминия через слабо или среднеосновную анионообменную смолу. Длительность контакта составляет 0,5 часа. При этом получают моно- и дегидрооксизамещенные хлориды алюминия. Необходимая степень основности продукта определяется концентрацией исходного раствора, природой и количеством ионообменника, времени контакта. Использование слабоосновных смол и ограничение степени прохождения второй стадии гидролиза не исключают образования гидроксида алюминия на зернах ионита и в его порах, что затрудняет реализацию способа в промышленных условиях.
Достаточно надежен процесс получения стабильных растворов основных хлоридов алюминия на ионообменных мембранах при прохождении электрического тока. Обычно применяют трехкамерный аппарат, где со стороны анода находится катионитовая мембрана, а со стороны катода - анионитовая. В анодную камеру подают хлорид алюминия, в катодную - раствор гидроксида натрия. При прохождении электрического тока раствор хлорида алюминия в средней камере обогащается ионами алюминия со стороны анода и гидроксид-ионами - со стороны катода (патент N 49-24353, Япония). Установив дополнительную катионитовую мембрану, преодолевают проникновение хлора к аноду. Особо чистые основные хлориды алюминия получают электродиализом хлорида алюминия, обработанного щелочными реагентами (патент N 55-36711, Япония).
Основные хлориды алюминия получают и бездиафрагменным электролизом водных растворов хлорида алюминия (до 25% AlCl3) с нерастворимым анодом (графит, платина, платинированный титан и др.) (патент N 4203812, США). Катод может быть изготовлен из железа, нержавеющей стали или титана. Электролиз осуществляют в интервале температур 50-80oC. На аноде выделяется хлор, а на катоде - водород. Рабочий диапазон плотностей тока колеблется в довольно широких пределах (200-400 A/м2). В основных растворах возможна пассивация катода высокоосновными нерастворимыми солями и гидроксидом алюминия. Большие трудности при использовании этого метода связаны с утилизацией анодного хлора и стабильностью анода.
По наиболее близкому предлагаемому способу (А.К. Запольский, А.А. Баран Коагулянты и флокулянты в процессах очистки воды. Л.: Химия, 1987) основные хлориды алюминия получают из обескремненного алюминатного раствора с концентрацией 70 г/л Al2O3 путем быстрой карбонизации газом (CO2) в течение одного часа при температуре 20-30oC. Осадок Al(OH)3 отделяют от источника, промывают водой и растворяют в соляной кислоте при нагревании. Этот способ требует очистки и охлаждения большого количества газа. Низкая концентрация газа и приводит к снижению коэффициента использования газа и нестабильному процессу получения аморфного гидроксида алюминия.
Сущность изобретения заключается в том, что разработан способ получения гидроксохлоридов алюминия по бикарбонатной технологии. По данной технологии используются растворы основного глиноземного производства:
1. Содовый раствор после передела карбонизации с содержанием:
Al2O3 - 2-5 г/л;
Na2Oт - 80-110 г/л.
2. Глубокообескремненный алюминатный раствор с содержанием:
Al2O3 - 80-100 г/л;
Na2Oт - 90-110 г/л.
3. Вода, соответствующая ГОСТу 2874-82.
4. Двадцатипроцентная соляная кислота.
Для получения бикарбонатного раствора используют содовый раствор после передела карбонизации основного глиноземного производства, который газируется промышленным газом с содержанием CO2 до 5% до содержания Na2Oбкб 25-30 г/л, по реакции:
Na2O•CO2 + CO2 + H2O ---> Na2O•2CO2•H2O
Глубокообескремненный алюминатный раствор смешивается с бикарбонатным раствором в соотношении 1:7 с условием создания бикарбонатной среды в полученной пульпе не менее 2,0 г/л Na2Oбкб, температура раствора при их смешении и полученной пульпы не должна превышать 30oC, pH среды в пульпе 11.2-11,8.
В результате получается гидроалюмокарбонат натрия состава:
Al2O3•2CO2•Na2O•2H2O
Данное соединение получается при взаимодействии алюминатного и бикарбонатного растворов по уравнениям:
Na2O•H2O + Na2O•2CO2•H2O = 2H2O + 2Na2O•CO2 (1)
Na2O•Al2O3 + 2Na2O•2CO2•H2O = Al2O3•2CO2•Na2O•2H2O + 2Na2O•CO2 (2)
Избыток бикарбонатной щелочи в пульпе и температура растворов не более 30oC позволяют стабилизировать в гидроалюмокарбонате натрия гидроксид алюминия в аморфном состоянии. Содержание Al2O3 в гидроалюмокарбонате натрия 50-100 г/л. Получение гидроалюмокарбоната натрия без избытка бикарбонатной щелочи, повышение температуры растворов более 30oC приводит к образованию байерита, что нежелательно при приготовлении гидроксохлоридов алюминия.
Гидроалюмокарбонат натрия разлагают водой, соответствующей ГОСТу 2874-82, с температурой не более 30oC до pH среды 6-7, в результате чего получают гель аморфного гидроксида алюминия и содовый раствор.
t ≤ 30oC
Nа2O•CO2•Al2O3•2H2O + nH2O ---> Na2O•CO2 + Al2O3•nH2O
Для обработки гидроалюмокарбоната натрия водой достаточно двух декантаций. Первая декантация берется в соотношении Т:Ж = 1:10, вторая - Т:Ж = 1: 20. Крепкая промвода от первой декантации с содержанием Al2O3 1-2 г/л и Na2Oт 60-80 г/л возвращается в основное производство глиноземного цеха в виде содового раствора. Слабая промвода после второй декантации с содержанием Na2Oт 1-2 г/л направляется на шламовое поле и циркулирует в схеме водооборота завода.
Гель гидроксида алюминия с содержанием Na2O3 0,2-0,3% отправляется на растворение в двадцатипроцентной соляной кислоте при комнатной температуре в течение 30-40 минут.
Раствор гидроксохлоридов с концентрацией Al2O3 5-10% направляется на концентрирование и затарку.
Гель гидроксида алюминия представляет собой полупрозрачную желеобразную массу с содержанием Al2O3 50-100 г/л. Характерной особенностью данного продукта является то, что он полностью взаимодействует с малым количеством соляной кислоты без остатка твердого осадка при комнатной температуре. Данный продукт реагирует с соляной кислотой в любом соотношении, что позволяет получать гидроксохлориды заданной основности с модулем кислотности 1,0-2,0.
Технологическая схема.
Схема по производству гидроксохлоридов работает в периодическом режиме.
Для приготовления бикарбонатного раствора используется содовый раствор основного производства, который газируется в карбонизаторе 1. Полученный бикарбонатный раствор фильтруется на фильтре ЛВАЖ 2, осадок отправляется на производство галлия, а бикарбонатный раствор - на охлаждение в мешалку 4.
Отфильтрованный алюминатный раствор основного производства закачивается для охлаждения в мешалку 3.
Вода, соответствующая ГОСТу 2874-82, получается очисткой промышленной воды коагулянтом гидроксохлоридом алюминия в сгустителе 5, сливается в бак 6, охлаждается, твердая фаза со сгустителя отправляется на шламовое поле.
Выделение гидроалюмокарбоната натрия производится при интенсивном смешении подаваемых в соотношении 1:7 алюминатного и бикарбонатного растворов в мешалке 7. Приготовленный гидроалюмокарбонат натрия обрабатывается водой с выделением аморфного геля гидроксида алюминия и соды в мешалке 7 и перекачивается в заполненный водой сгуститель 8. При этом осуществляется первая отмывка геля гидроксида алюминия от соды. Сгущенная пульпа геля гидроксида алюминия со сгустителя направляется в репульпатор 9, обрабатывается водой и фильтруется на фильтре ЛВАЖ 10. Крепкая промвода слива со сгустителя 8 и фильтрат с ЛВАЖ 10 возвращаются в основное глиноземное производство, кек с фильтра 10 сбрасывается в репульпатор 11, где обрабатывается водой, пульпа из репульпатора 11 откачивается на вторую отмывку вновь на сгуститель 8. Сгущенная пульпа геля гидроксида алюминия со сгустителя 8 направляется в репульпатор 9, обрабатывается водой и фильтруется на фильтре ЛВАЖ 10, слив слабой промводы со сгустителя 8 и фильтрат с фильтра ЛВАЖ 10 отправляются на шламовое поле, а кек геля гидроксида алюминия собирается в сборник 12 и через объемный дозатор 13 направляется в реактор 14 на приготовление гидроксохлоридов алюминия. В реактор 14 из расходного бака 15 через мерник-дозатор 16 подается двадцатипроцентная соляная кислота. После завершения процесса растворения геля гидроксида алюминия коагулянт из реактора 14 отправляется на концентрирование и затарку в емкости.
Технический эффект.
Получение гидроксохлоридов алюминия по данной технологии позволяет:
1. вести процесс получения бикарбонатного раствора газацией содового раствора после карбонизации основного глиноземного производства промышленным газом с содержанием CO2 до 5%;
2. использовать растворы основного глиноземного производства; получить особо чистый продукт в виде полупрозрачной активной гели гидроксида алюминия, т.к. исходными компонентами являются глубокообескремненный алюминатный раствор, бикарбонатный раствор и вода, соответствующая ГОСТу 2874-82,
3. растворение гидроксида алюминия двадцатипроцентной соляной кислотой вести нацело при комнатной температуре в течение 30-40 минут;
4. исключить твердый остаток при растворении;
5. получить гидроксохлориды алюминия с заданной основностью от 5/6 до 1/3 с модулем кислотности 1,0-2,0;
6. исключить из процесса опасные или вредные сбросы;
7. увеличить срок службы технологического оборудования в связи с низкой кислотностью продукта.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АКТИВНОГО ГИДРОКСИДА АЛЮМИНИЯ | 2000 |
|
RU2175951C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОДИСПЕРСНОГО ГИДРОКСИДА АЛЮМИНИЯ | 2007 |
|
RU2355638C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСОХЛОРИДА АЛЮМИНИЯ | 1999 |
|
RU2157340C1 |
| УСТАНОВКА ДЛЯ ПОЛУЧЕНИЯ ГИДРОКСОХЛОРИДА АЛЮМИНИЯ | 2019 |
|
RU2715542C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЛИНОЗЕМА И ГАЛЛИЯ ИЗ БОКСИТА | 1999 |
|
RU2174955C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГАЛЛИЯ ИЗ ПОТАШНОГО МАТОЧНОГО РАСТВОРА | 1997 |
|
RU2116369C1 |
| СПОСОБ ПЕРЕРАБОТКИ АЛЮМИНИЙСОДЕРЖАЩЕГО СЫРЬЯ | 2000 |
|
RU2197429C2 |
| СПОСОБ ПОЛУЧЕНИЯ МАЛОЩЕЛОЧНОГО ГЛИНОЗЕМА | 1992 |
|
RU2047561C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛЛИЯ | 1997 |
|
RU2118391C1 |
| СПОСОБ ПЕРЕРАБОТКИ КРАСНОГО ШЛАМА ДЛЯ ПОЛУЧЕНИЯ ОКСИДА СКАНДИЯ | 2024 |
|
RU2840984C1 |
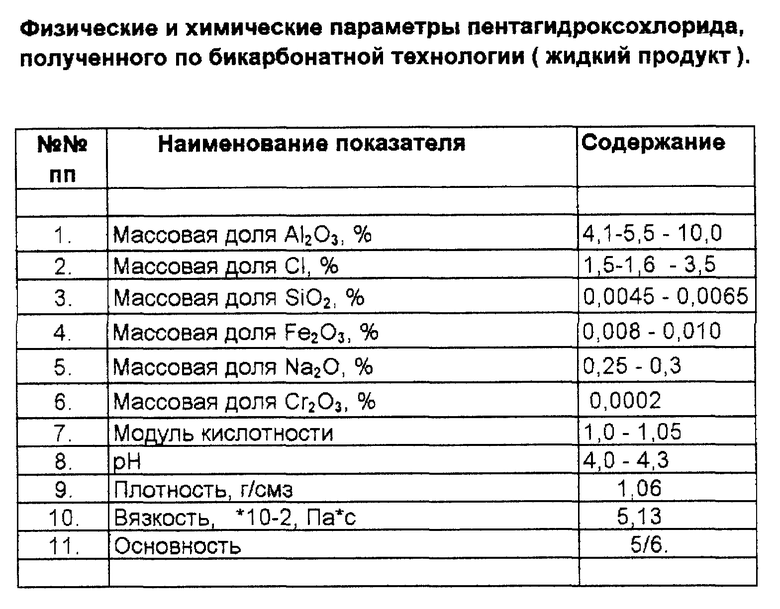
Изобретение относится к технологии химической промышленности, а именно к способам получения основных хлоридов, т.е. гидроксихлоридов, в частности пентагидрооксихлорида алюминия особой чистоты, применяемых как коагулянты для очистки питьевой воды и промстоков, а также как связующее вещество в производстве керамики, огнеупоров и тампонировании скважин нефте- и газодобычи. Особо чистый продукт пентагидрооксихлорида алюминия применяется в косметическом и фармацевтическом производстве. Способ включает получение гидрооксихлоридов алюминия особой чистоты по бикарбонатной технологии с заданной основностью и модулем кислотности 1,0-2,0 из аморфного полупрозрачного геля гидроксида алюминия с содержанием Al2O3 - 50-100 г/л, полученного из гидроалюмокарбоната натрия в результате нейтрализации, в соотношении 1:7, при температуре не более 30oС, рН 11,2-11,8, очищенного алюминатного раствора бикарбонатным раствором, полученным газацией солового раствора после карбонизации основного глиноземного производства промышленным газом с содержанием СО2 не более 5%, разложенного очищенной промышленной водой с температурой не более 30oС до рН - 6-7, растворенного в соляной кислоте в заданном соотношении, при температуре 20-30oС. Способ позволяет получить особо чистые гидрооксихлориды алюминия с заданной основностью от 5/6 до 1/3 и с модулем кислотности 1,0-2,0. 1 табл., 1 ил.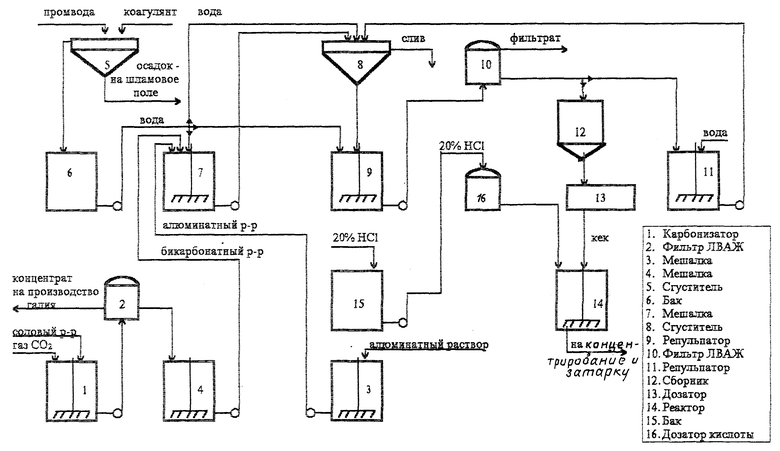
Способ получения гидроксохлоридов алюминия, включающий получение гидроксида алюминия, растворение его соляной кислотой, отличающийся тем, что процесс получения аморфного реактивно - активного геля гидроксида алюминия проводят нейтрализацией алюминатного раствора бикарбонатным раствором, полученным газацией садового раствора глиноземного производства промышленным газом, содержащим до 5% СО2, с последующим разложением получаемого алюмокарбоната натрия промышленной водой, процесс же взаимодействия соляной кислоты с гелем полученного гидроксида алюминия ведут при комнатной температуре и получают продут с кислотным модулем 1,0-2,0.
| Запольский А.К., Баран А.А | |||
| Коагулянты и флокулянты в процессах очистки воды | |||
| - Л.: Химия, 1987, с.90-95 | |||
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО ХЛОРИДА АЛЮМИНИЯ | 1993 |
|
RU2093466C1 |
| УСТРОЙСТВО для ПОДАЧИ КИСЛОРОДА в КОНВЕРТЕР | 0 |
|
SU383736A1 |
| Учебное пособие по электротехнике | 1986 |
|
SU1410087A1 |
| GB 1460966 A, 06.01.77 | |||
| US 4944933 A, 31.07.90 | |||
| US 5182094 A, 26.01.93 | |||
| Способ соединения сваркой патрубков с днищем реактора | 2020 |
|
RU2740128C1 |
Авторы
Даты
1999-10-10—Публикация
1997-11-03—Подача