Изобретение относится к органической и аналитической химии и может найти применение в медицине и биологии.
Стероидные соединения играют важную роль в процессах жизнедеятельности человека и животных. Одним из стероидных гормонов является прогестерон - соединение формулы I: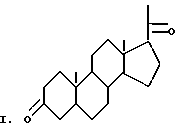
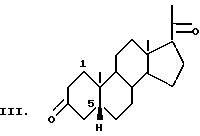
Важное участие в биохимических процессах принимают его метаболиты. Среди метаболитов прогестерона известны 5α- и 5β-прегнан-3,20-дионы (соединения общей формулы II и III соответственно):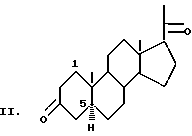
(Sigma 2000. Реактивы для биохимии и исследований в области естественных наук, с.348, 829) [1].
Известно, что 5α- и 5β-прегнан-3,20-дионы выполняют ряд функций, связанных с репродукцией живых организмов (Hodges Y.K. et all Biol.Reprod., 1997, v.56, 3, p.640) [2].
Однако данные метаболиты содержатся в крови в очень низких концентрациях. Для определения соединений, содержащихся в биологических жидкостях в нанограммовых и донанограммовых количествах, необходимо иметь меченые аналоги определяемых соединений. Меченые аналоги 5α- и 5β-прегнан-3,20-дионов не известны.
Техническим результатом, достигаемым при реализации настоящего изобретения, является получение новых высокомеченных тритием соединений и их использование для определения содержания метаболитов прогестерона в плазме крови.
Указанный технический результат достигается тем, что получены высокомеченные тритием 5α- [4,5-3Н] прегнан-3,20-дион и 5β-[4,5-3H]прегнан-3,20-дион.
Указанный технический результат достигается также тем, что способ определения содержания в плазме крови метаболитов прогестерона, 5α- прегнан-3,20-диона и 5β-прегнан-3,20-диона заключается в том, что в анализируемую пробу плазмы крови вводят меченые аналоги определяемых метаболитов, обрабатывают пробу органическим растворителем, затем подвергают селективной деструкции перешедшие в экстракт прогестерон и другие ненасыщенные стероиды, которые сопутствуют определяемым, после чего оставшиеся в обработанном экстракте определяемые метаболиты и их меченые аналоги переводят в дансильные производные, содержание которых в обработанном экстракте определяют методом ВЭЖХ с использованием детекторов флюоресценции или поглощения и радиоактивности, а по полученным данным производят расчет содержания определяемых метаболитов в плазме крови.
В качестве меченых аналогов метаболитов прогестерона в пробу плазмы крови вводят 5α- [4,5-3H]прегнан-3,20-дион и 5β-[4,5-3H]прегнан-3,20-дион.
Для обработки анализируемой пробы плазмы крови в качестве органического растворителя используют хлороформ, а прекращают обработку после перехода в экстракт не менее 50% добавленных в пробу меченых аналогов определяемых метаболитов.
Селективную деструкцию проводят путем выдерживания экстракта в присутствии перекиси водорода в щелочной среде.
Щелочную среду создают добавлением в экстракт карбоната калия.
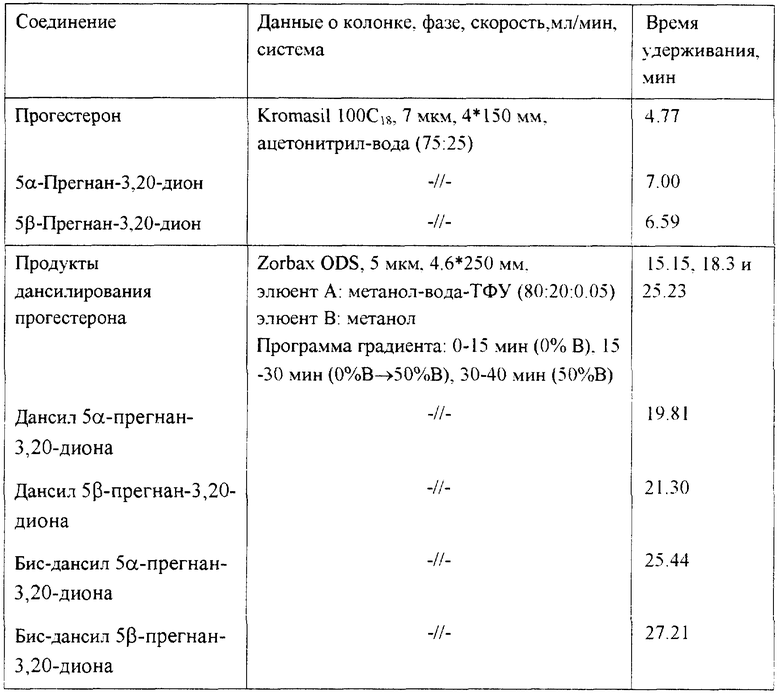
На фиг.1 приведена хроматограмма реакционной смеси после восстановления С4= С5 связи в прогестероне газообразным тритием, с использованием детектора по УФ-поглощению (UV) и детектора по радиоактивности (Rad).
На фиг. 2 представлена хроматограмма продуктов дансилирования прогестерона. Детектор по флуоресценции.
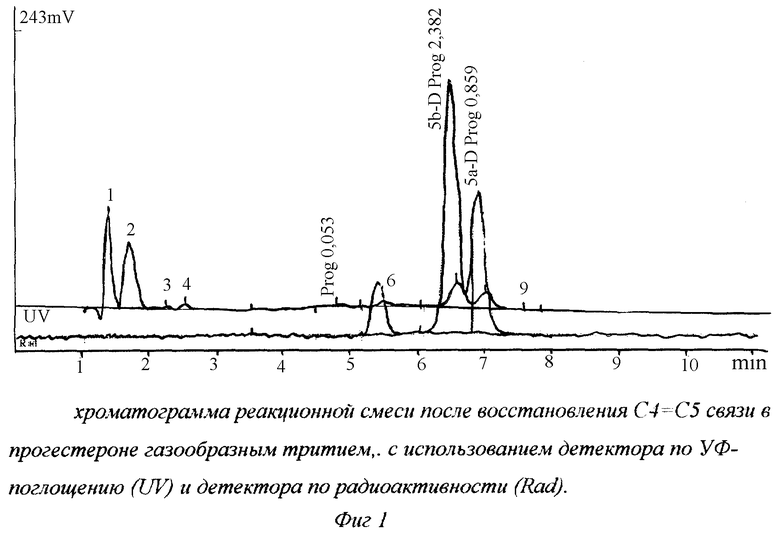
На фиг.3 представлена хроматограмма продуктов дансилирования смеси прогестерона, 5α- и 5β-прегнан-3,20-дионов. Детектор по флюоресценции.
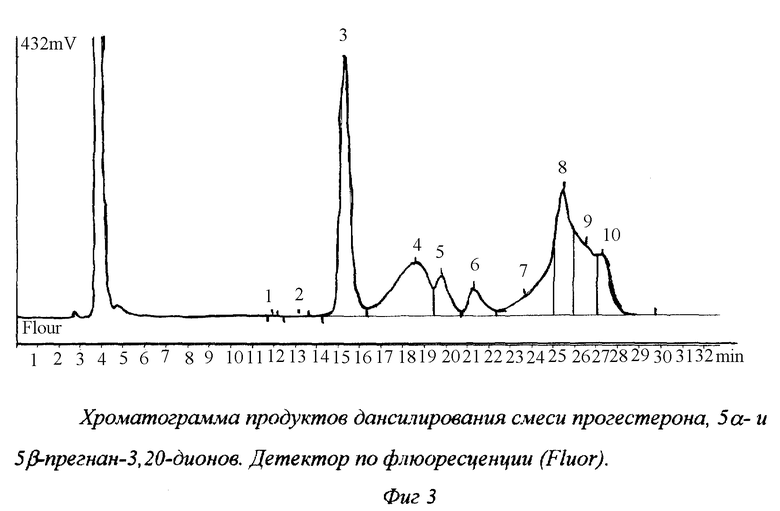
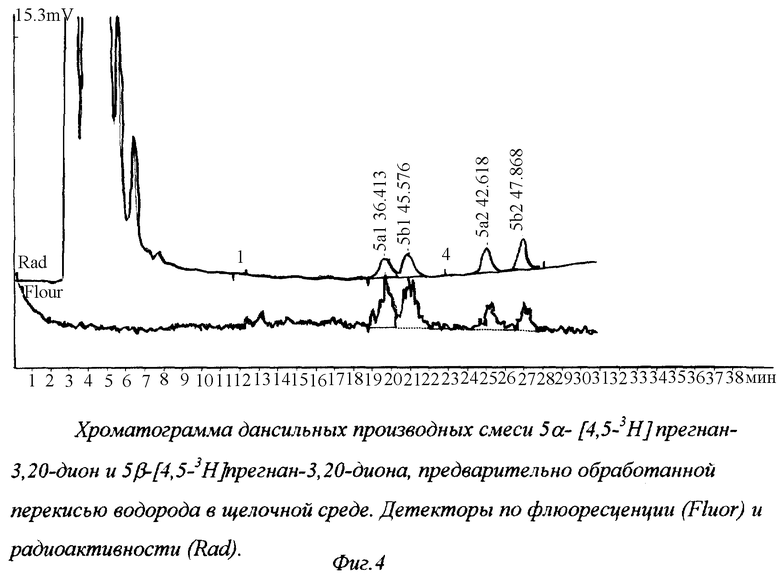
На фиг. 4 представлена хроматограмма дансильных производных смеси 5α- [4,5-3H] прегнан-3,20-дион и 5β-[4,5-3H] прегнан-3,20-диона, предварительно обработанной перекисью водорода в щелочной среде.
Детектор по флюоресценции и радиоактивности.
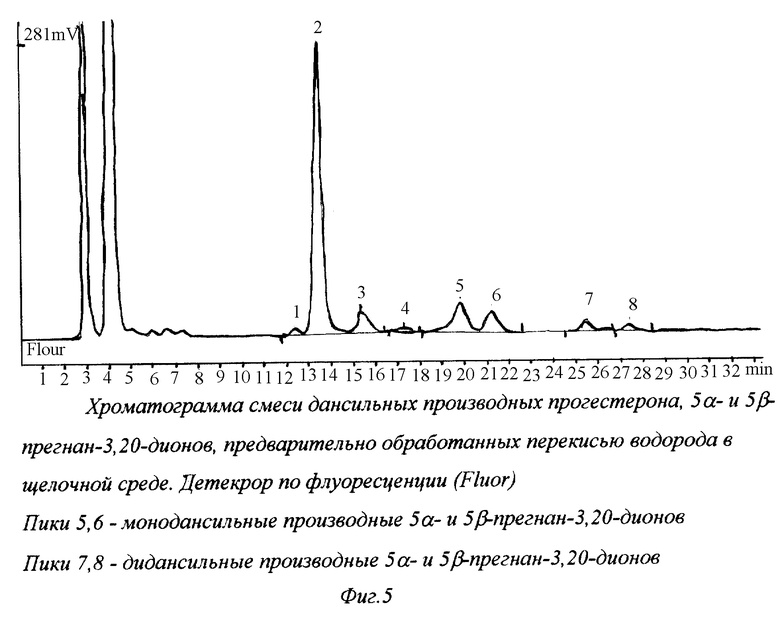
На фиг.5 представлена хроматограмма смеси дансильных производных прогестерона, 5α- и 5β-прегнан-3,20-дионов, предварительно обработанных перекисью водорода в щелочной среде.
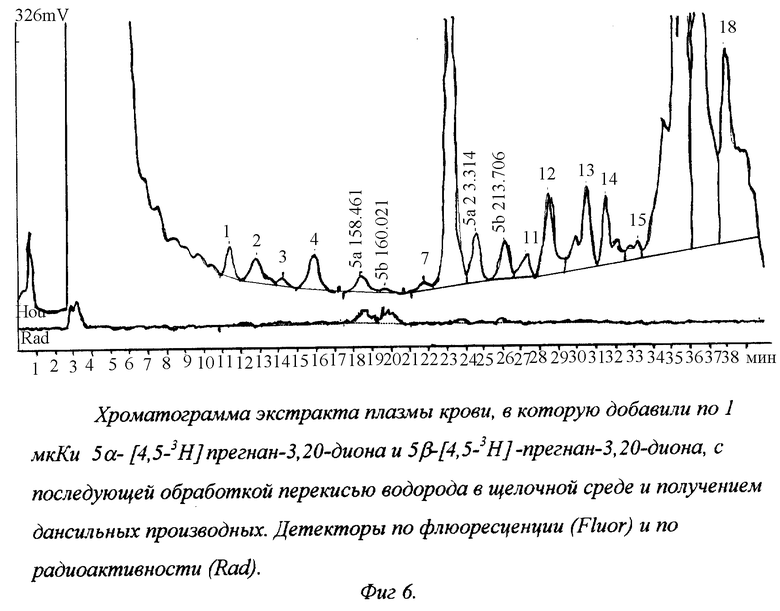
На фиг. 6 представлена хроматограмма экстракта плазмы крови, в которую добавили по 1 мкКu 5α- [4,5-3H]прегнан-3,20-диона и 5β-[4,5-3Н] -прегнан-3,20-диона, с последующей обработкой перекисью водорода в щелочной среде и получением дансильных производных. Детекторы по флюоресценции и по радиоактивности.
Собственные исследования показали, что при обработке плазмы крови хлороформом в него переходят прогестерон и его метаболиты, в том числе определяемые способом согласно определению - 5α- и 5β-прегнан-3,20-диона (соединения общей формулы II и III). Для того чтобы стало возможным определять в этой смеси только эти два метаболита прогестерона, способом согласно изобретению предусмотрена процедура деструкции содержащихся в хлороформенном экстракте самого прогестерона и иных его ненасыщенных метаболитов. Для этого на них воздействуют перекисью водорода в щелочной среде. Оказалось, что такая обработка приводит к селективной деструкции мешающих определению прогестерона и ряда его ненасыщенных метаболитов, но сохраняет метаболиты, определяемые способом согласно изобретению - соединения формулы II и III.
Однако определение этих двух соединений методом ВЭЖХ затруднено отсутствием в их молекулах фрагментов с высоким оптическим поглощением, поэтому рекомендовано получить из них их дансильные производные, которые анализируют методом ВЭЖХ, а полученные данные используют для расчета содержания соединений формулы II и III в анализируемой плазме крови.
Удобство работы с дансильными производными заключается в том, что при использовании флюоресцентного детектора можно надежно анализировать пробы, содержащие 1 нг определяемых метаболитов в виде их дансильных производных на мл биологической жидкости, в то время как при использовании соответствующего меченого аналога с молярной радиоактивностью порядка 1.2-1.8 ПБк/моль для достоверного получения пика по радиоактивности при использовании ВЭЖХ необходимо 5 нг вещества на мл раствора.
Ниже приведены примеры, иллюстрирующие изобретение.
Пример 1. Синтез меченных тритием 5α- и 5β-прегнан-3,20-дионов.
В реакционную ампулу поместили раствор 4 мг прогестерона в 0,4 мл метанола, 20 мг 5% Pd/СаСО3, заморозили жидким азотом и вакуумировали до давления 0,1 Па. В ампулу напустили газообразный тритий до давления 400 гПа и вели реакцию при комнатной температуре при перемешивании 1 ч. Затем ампулу вновь заморозили жидким азотом и избыточный тритий удалили вакуумированием. Содержимое ампулы отфильтровали, катализатор промыли этанолом (3х1 мл), фильтраты объединили. Лабильный тритий удалили трехкратным упариванием реакционной смеси с метанолом (3х3 мл). Остаток очистили методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Характеристики полученных препаратов:
5α- [4,5-3H] прегнан-3,20-дион - молярная радиоактивность - 51 Ku/ммоль, выход - 21,5%;
5β-[4,5-3H] пpeгнaн-3,20-диoн - молярная радиоактивность - 38 Ku/ммоль, выход - 60%;
Радиохимическая чистота 5α- [4,5-3Н] прегнан-3,20-диона и 5β-[4,5-3H] прегнан-3,20-диона составила 97-98%.
Пример 2. Синтез дансильных производных прогестерона, 5α- прегнан-3,20-диона, 5β-прегнан-3,20-диона.
1 мкг прогестерона или 5α- прегнан-3,20-диона или 5β-прегнан-3,20-диона или их смесей растворили в 80 мкл метанола, добавили 10 мкл уксусной кислоты, 10 мкл раствора дансилгидразина (10 мг/мл) в ацетонитриле и выдерживали 1,5 ч при комнатной температуре в темноте, после чего реакционную смесь анализировали методом ВЭЖХ.
Анализ хроматограмм, приведенных на фиг.2-4, свидетельствует о том, что дансильные производные прогестерона могут мешать точному определению концентрации 5α- прегнан-3,20-диона и 5β-прегнан-3,20-диона в реакционной смеси. Кроме того, в биологических жидкостях могут содержаться другие ненасыщенные соединения, которые могут исказить реальное количество определяемых метаболитов в исходной смеси.
Пример 3. Синтез дансильных производных, 5α- прегнан-3,20-диона, 5β-прегнан-3,20-диона после предварительной обработки их смеси с прогестероном перекисью водорода в щелочной среде.
Смесь прогестерона, 5α- прегнан-3,20-диона и 5β-прегнан-3,20-диона (по 1 мкг) растворили в 200 мкл метанола, добавили 20 мкл водного раствора К2СО3 (57 мг/мл) и 10 мкл 50%-ного раствора Н2О2 и выдерживали при комнатной температуре 2 ч. Затем смесь упаривали и дансилировали. Результаты приведены на фиг.5 и в таблице.
Пример 4. Определение 5α- и 5β-дигидропрогестеронов в нанограммовых количествах в плазме крови.
В 1,5 мл плазмы крови ввели по 0,1 МБк 5α- [3Н] и 5β-[3H]-дигидропрогестеронов и экстрагировали хлороформом 3 раза по 1 мл. Экстракцию завершили после перехода в органический слой 50% введенной в плазму метки. Предварительными опытами установили оптимальность использования хлороформа для экстракции из плазмы крови определяемых метаболитов и их меченых аналогов. С одной стороны, хлороформ обеспечивает переход в органический слой более 50% метки. С другой стороны, он экстрагирует минимальное количество подобных веществ, мешающих определению 5α- и 5β-прегнан-3,20-дионов.
После завершения экстракции хлороформ упарили, а оставшийся осадок растворили в 200 мкл метанола. В полученный метанольный раствор добавили 20 мкл водного раствора К2СО3 (60 мг/мл) и 10 мкл 50%-ного раствора Н2О2. Смесь выдержали 2 ч при комнатной температуре, затем ее упарили, осадок растворили в 80 мкл метанола, добавили 10 мкл уксусной кислоты, 10 мкл раствора дансилгидразина (10 мг/мл) в ацетонитриле и выдержали 2 ч при комнатной температуре. Затем реакционную массу растворили в 50 мкл воды и анализировали методом ВЭЖХ (см. фиг.6).
Расчет концентрации определяемых метаболитов прогестерона (нг/мл) по методу радиоактивного разбавления проводится по следующему уравнению: C=M/V, где С - концентрация стероида;
V - объем взятой пробы [мл],
М - содержание стероида в пробе [нг]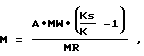
где А - активность стероида, добавленного в пробу [мкКu],
MW - молекулярный вес стероида,
Ks - отношение площади пика по радиоактивности к площади пика по оптическому поглощению при использовании метода ВЭЖХ для меченого аналога данного стероида.
К - отношение площади пика по радиоактивности к площади пика по оптическому поглощению при использовании метода ВЭЖХ для смеси немеченого стероида, находящегося в пробе, и меченого аналога данного стероида, который был добавлен в пробу;
MR - молярная радиоактивность меченого аналога данного стероида, который был добавлен в пробу [Ки/ммоль].
Таким образом, синтезированы новые высокомеченные тритием аналоги двух известных метаболитов прогестерона. Способ согласно изобретению позволяет определять эти метаболиты в плазме крови с использованием новых меченых соединений.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ ТАФЦИН И СПОСОБ ОПРЕДЕЛЕНИЯ ТАФЦИНА В БИОЛОГИЧЕСКИХ ОБРАЗЦАХ | 2001 |
|
RU2206556C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ ЦИКЛОСПОРИН А | 1998 |
|
RU2144017C1 |
| N-[Н]АЦЕТИЛ-D-ГЛЮКОЗАМИН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2190620C1 |
| КРАТНОМЕЧЕННАЯ ТРИТИЕМ ПО ДВОЙНЫМ СВЯЗЯМ 15-ГИДРОКСИ-5Z,-8Z,11Z, 13Е-ЭЙКОЗАТЕТРАЕНОВАЯ КИСЛОТА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2073665C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [МЕТИЛ-H]МЕТИЛТОЗИЛАТ | 2008 |
|
RU2353613C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [H]-РАПАМИЦИН | 2003 |
|
RU2233285C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ (2-ПРОПИЛЕН-4,6-ДИМЕТИЛ-8-ОКСИМЕТИЛ)ОКТИЛ-(3'-ОКСИ-4',5',6'-ТРИМЕТИЛ-6'-ЕН )ГЕПТИЛКЕТОН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2143431C1 |
| ВЫСОКОМЕЧЕННЫЕ ТРИТИЕМ ПРОИЗВОДНЫЕ СИАЛОВОЙ КИСЛОТЫ | 2001 |
|
RU2190621C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [H]-(E)-N-[(4-ГИДРОКСИ-3-МЕТОКСИФЕНИЛ)МЕТИЛ]-8-МЕТИЛ-6-НОНЕНАМИД | 2004 |
|
RU2268256C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [Н]-5-ХЛОРО-8-ГИДРОКСИХИНОЛИН | 2005 |
|
RU2284322C1 |

Изобретение относится к органической и аналитической химии, к медицине и биологии. Синтезированы высокомеченные тритием 5α-[4,5-3Н]прегнан-3,20-дион и 5β-[4,5-3H]прегнан-3,20-дион, которые использованы для определения этих метаболитов прогестерона в плазме крови. В анализируемую пробу плазмы крови вносят меченные тритием аналоги определяемых метаболитов прогестерона. В хлороформенный экстракт, помимо определяемых двух метаболитов, переходят иные метаболиты прогестерона и прогестерон, которые мешают определению. Их разрушают выдерживанием экстракта в присутствии перекиси водорода в щелочной среде. Оставшиеся в экстракте после этой обработки определяемые метаболиты переводят в дансильные производные, которые позволяют определять нанограммовые количества этих стероидов при анализе методом ВЭЖХ. По результатам определения содержания дансильных производных вычисляют содержание определяемых метаболитов в анализируемой плазме крови. Изобретение позволяет определять указанные метаболиты в плазме крови при их очень низкой концентрации. 2 с. и 4 з.п. ф-лы, 6 ил., 1 табл.
| Реактивы для биохимии и исследований в области естественных наук | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Телефонная трансляция с местной цепью для уничтожения обратного действия микрофона | 1924 |
|
SU348A1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1988 |
|
RU2039560C1 |
| Способ определения стероидных гормонов в биологических объектах | 1984 |
|
SU1273334A1 |
| Способ определения альдостеронсвязывающей способности белков плазмы крови | 1980 |
|
SU922636A1 |
Авторы
Даты
2002-06-10—Публикация
2001-03-26—Подача