Изобретение относится к области ароматических сульфонов, конкретно к способу получения 4,4'-дихлордифенилсульфона (ДХДФС), являющегося мономером в синтезе термостойких полиариленсульфоновых полимеров.
Известен способ получения ДХДФС путем взаимодействия хлорбензола с хлорсульфоновой кислотой (ХСК) при 10-30oС в течение 2-3 ч [Заявка Японии 58-206553, МКИ С 07 С 147/06, 1983].
Способ не обеспечивает хорошего выхода сульфона и основным продуктом реакции является 4-хлорбензолсульфохлорид (ХБСХ).
По другому способу целевой продукт получают реакцией хлорбензола с ХСК при 55-60oC с последующим сульфонилированием хлорбензола, образующимся ХБСХ в присутствии хлорного железа при 145-155oС [Заявка Великобритании 2135666, МКИ С 07 С 143/70, 1984].
Недостатком способа является прежде всего сложность технологии очистки мономера от катализатора.
Известен способ получения ДХДФС в отсутствии металлсодержащего катализатора взаимодействием смеси эквимольных количеств хлорбензола, ХБСХ и 4-хлорбензолсульфокислоты (ХБСК) при 145-155oC [Патент США 3673259, МКИ С 07 С 147/06, 1972]. Целевой продукт высаживают водой и отделяют от водного раствора ХБСК.
Недостатком способа является необходимость утилизации. ХБСК путем ее обезвоживания перед направлением в рецикл на стадию синтеза ДХДФС. Существующие методы регенерации ХБСК требуют больших энергетических затрат и не обеспечивают очистку кислоты, что приводит к накоплению примесей в системе и вследствие этого снижению качества товарного продукта.
Наиболее близким к предлагаемому по технологической сущности является способ получения ДХДФС, включающий взаимодействие хлорбензола с ХСК при 0-60oС, добавление к полученной реакционной массе хлорбензола в мольном соотношении к исходному хлорбензолу 0,7-1,3:1 и отгон азеотропа воды с хлорбензолом с возвратом хлорбензола в реакционную массу, добавление ХБСХ в мольном соотношении к исходному хлорбензолу 0,50-0,90:1 и выдержку при 150-200oС до завершения реакции, выделение ДХДФС и перевод образующейся ХБСК в аммонийную соль и далее в ХБСХ действием ХСК в органическом растворителе при 70oС, ХБСХ отделяют от солей и направляют в рецикл на стадию синтеза ДХДФС [Патент России 2135466, МКИ 6 С 07 С 317/14, 1998].
Выход целевого продукта составляет 85-90%.
Недостатками этого способа являются относительная сложность технологии получения ДХДФС, а также образование больших количеств неорганических солевых отходов.
Задачей предлагаемого изобретения является упрощение способа получения ДХДФС за счет уменьшения количества технологических стадий, а также исключение образования неорганических солевых отходов.
Это достигается тем, что получение ДХДФС осуществляют взаимодействием ХСК с избытком хлорбензола при температуре 20-60oC, добавлением к полученной смеси ХБСХ и выдержкой при 145-165oC до прекращения выделения хлористого водорода, превращением образующейся ХБСК в ХБСХ действием избытка ХСК на реакционную массу при 20-80oС с последующим выделением ДХДФС и плава ХБСХ, содержащего до 35 мас.% ДХДФС.
Взаимодействие ХСК с избытком хлорбензола осуществляют путем смешения реагентов при 20-30oС с последующей выдержкой при 20-60oC до завершения реакции.
К полученной реакционной массе прибавляют ХБСХ в мольном соотношении к исходному хлорбензолу 0,39-0,49:1 и выдерживают при 145-165oС до прекращения выделения хлористого водорода.
В качестве ХБСХ может использоваться плав ХБСХ, содержащий до 35 мас.% ДХДФС, полученный на предыдущей операции.
К полученной реакционной массе прибавляют ХСК при мольном соотношении к исходному хлорбензолу 0,74-1,24: 1 и выдерживают при 20-80oC до завершения реакции.
Взаимодействие ХСК с реакционной массой можно осуществлять в хлорорганическом растворителе, выбранном из группы: хлороформ, тетрахлорметан, трихлорэтан, трихлорэтилен, тетрахлорэтан, тетрахлорэтилен.
Выделение продуктов реакции осуществляют кристаллизацией из хлорорганического растворителя, выбранного из указанной группы с предварительным разложением избытка ХСК водой и удалением кислых примесей из органического слоя водной промывкой.
Процесс получения ДХДФС может быть описан схемой, приведенной в конце текста.
Отличительной особенностью предлагаемого способа является проведение взаимодействия ХСК с избытком хлорбензола, добавление ХБСХ к полученной реакционной массе без предварительной ее осушки, превращение ХБСК в ХБСХ действием ХСК на реакционную массу без предварительного выделения ХБСК, выделение продуктов реакции кристаллизацией из хлорорганического растворителя с предварительным разложением избытка ХСК водой и удалением кислых примесей из органического слоя водной промывкой.
Указанные мольные соотношения реагентов являются оптимальными, поскольку их изменение приводит к снижению эффективности технологического процесса из-за образования нежелательных примесей и невозможности поддержания необходимого температурного режима на стадии синтеза ДХДФС.
Проведение процесса при температурах ниже указанных приводит к снижению конверсии хлорбензола. При более высоких температурах возрастает количество побочных продуктов, в том числе изомеров ДХДФС и смолообразных примесей, ухудшающих цветность целевого сульфона.
Предложенный ряд растворителей по своим физико-химическим свойствам хорошо подходит для разделения целевых продуктов кристаллизацией. Они инертны по отношению к исходным и конечным продуктам при указанном температурном интервале.
На стадии синтеза ХБСХ применение данных растворителей способствует более равномерному нагреву реакционной массы и исключает локальный перегрев на стенках реактора.
Экспериментальные данные
Сульфирование хлорбензола до ХБСК при 20-60oС проходит практически со 100% конверсией ХСК. В качестве побочного продукта образуется в незначительном количестве ДХДФС.
В таблицах 1 и 2 приведены условия конденсации с получением целевого сульфона и хлородегидроксилирования ХБСК с получением ХБСХ.
Ниже приведены примеры, иллюстрирующие предполагаемое изобретение.
Пример 1
В реактор, снабженный мешалкой, термометром, обратным холодильником и капельной воронкой, загружают 39 г (0,347 моля) хлорбензола и прибавляют из капельной воронки при 20-30oC 20 г (0,172 моля) ХСК. Реакционную массу нагревают до 50-60oC и выдерживают при перемешивании до прекращения выделения хлористого водорода. Затем добавляют 36,3 г (0,172 моля) ХБСХ, нагревают до 160oC и выдерживают, перемешивая, при 155-165oC до прекращения выделения хлористого водорода, охлаждают реакционную массу до 60-70oC и добавляют трихлорэтилен (ТХЭ) и 40 г (0,344 моля) ХСК. Выдерживают реакционную смесь, перемешивая, при 65-75oC в течение 7 ч и промывают водой от серной кислоты и кислых примесей. Из органического слоя отгоняют воду в виде азеотропа с ТХЭ, охлаждают до 5-7oC и выдерживают раствор несколько часов до прекращения выпадения осадка ДХДФС. Кристаллы сульфона отфильтровывают и сушат при 60-80oС/200-300 мм рт. ст. Получают 35,2 г технического продукта, который содержит 93 мас.% ДХДФС и 6,5 мас.% ХБСХ.
Из маточника отгоняют ТХЭ и получают 43 г плава ХБСХ, который содержит 68 мас. % ХБСХ и 30,5 мас.% ДХДФС. Плав без очистки может быть направлен в рецикл на синтез ДХДФС.
Выход ДХДФС с учетом его содержания в плаве ХБСХ составляет 45,8 г (93%), ХБСХ с учетом его содержания в техническом ДХДФС - 31,5 г (87%).
Перекристаллизацией технического ДХДФС из ТХЭ получают 28,2 г целевого продукта с т.пл. 147-148oС, содержанием основного вещества 99,2%.
В качестве растворителя в процессе можно использовать соединения из группы: хлороформ, тетрахлорметан, трихлорэтан тетрахлорэтан, тетрахлорэтилен.
Пример 2
К реакционной массе стадии синтеза ХБСК, полученной по методике примера 1 из 39 г хлорбензола и 20 г ХСК, прибавляют 43 г плава ХБСХ, полученного согласно примеру 1 и содержащего 28,6 г (0,135 моля) ХБСХ и 12,6 г (0,044 моля) ДХДФС. Получают 34 г технического продукта, который содержит 92,5% ДХДФС и 7% ХБСХ и 41,4 г плава ХБСХ, который содержит 64,5% ХБСХ и 32,5% ДХДФС.
Выход ДХДФС с учетом его содержания в плаве ХБСХ составляет 44,9 г (87%) и ХБСХ - 29,1 г (80%).
Пример 3
В реактор загружают 39 г (0,347 моля) хлорбензола, прибавляют при 20-30oС 20 г (0,172 моля) ХСК в течение 2-3 ч и выдерживают при этой температуре до завершения реакции. Затем добавляют 36,3 г (0,172 моля) ХБСХ, нагревают до 150oС, выдерживают при 150-155oС до прекращения выделения хлористого водорода. Охлаждают реакционную массу до 60-70oС и добавляют 50 г (0,429 моля) ХСК. Выдерживают реакционную смесь при 65-75oС до завершения реакции. Прибавляют ТХЭ и промывают водой от серной кислоты и кислых примесей. Выделение целевых продуктов проводят аналогично примеру 1. Получают 42,1 (85%) ДХДФС и 29,4 г (81%) ХБСК.
Пример 4
В условиях примера 3 после синтеза ДХДФС прибавляют 30 г (0,258 моля) ХСК и выдерживают реакционную смесь при 75-80oС до завершения реакции. Выделение продуктов проводят аналогично примеру 1. Получают 44,9 г (91%) ДХДФС и 28,3 г (78%) ХБСК.
Таким образом, предлагаемый способ по сравнению с прототипом включает на одну химическую стадию меньше (отсутствует стадия получения аммонийной соли ХБСК), существенно упрощает процесс выделения целевых продуктов и полностью исключает образование неорганических солевых отходов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 4,4'-ДИХЛОРДИФЕНИЛСУЛЬФОНА | 2001 |
|
RU2212403C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4,4'-ДИХЛОРДИФЕНИЛСУЛЬФОНА | 1998 |
|
RU2135466C1 |
| Способ получения смеси 4,4 -дихлордифенилсульфона и -хлорбензолсульфохлорида | 1975 |
|
SU763332A1 |
| СПОСОБ ПОЛУЧЕНИЯ АРОМАТИЧЕСКИХ ХЛОРСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 1998 |
|
RU2152381C1 |
| Способ получения 4,4 -дихлордифенилсульфона | 1977 |
|
SU765262A1 |
| Способ получения полиэфирсульфона | 2024 |
|
RU2839480C1 |
| Способ получения 3,3",4,4" -тетрааминодифенилсульфона | 1969 |
|
SU370845A1 |
| Способ получения ароматических полисульфонов | 2023 |
|
RU2815713C1 |
| Способ получения ароматических сополиариленэфирсульфонов | 2017 |
|
RU2669790C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТАЛИМИДА | 2001 |
|
RU2185376C1 |
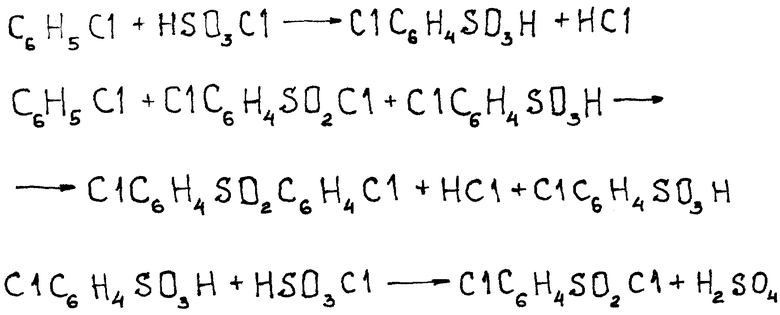

Изобретение относится к способу получения 4,4'-дихлордифенилсульфона, являющегося мономером в синтезе термостойких полиариленсульфоновых полимеров. Способ осуществляют следующим образом. Проводят взаимодействие хлорсульфоновой кислоты с избытком хлорбензола при 20-60oС, добавляют к полученной смеси 4-хлорбензолсульфохлорид в мольном соотношении к исходному хлорбензолу 0,39-0,49 : 1 и выдерживают при 145-165oС до прекращения выделения хлористого водорода, превращают образующуюся. 4-хлорбензолсульфокислоту в 4-хлорбензолсульфохлорид действием хлорсульфоновой кислоты в мольном соотношении к исходному хлорбензолу 0,75-1,24 : 1 при 20-80oС с последующим выделением 4,4-дихлордифенилсульфона и плава 4-хлорбензолсульфохлорида, содержащего до 35 мас.% 4,4'-дихлордифенилсульфона. Плав 4-хлорбензолсульфохлорида без очистки может быть направлен на синтез 4,4'-дихлордифенилсульфона на следующую операцию. Способ позволяет уменьшить количество технологических стадий процесса и исключить образование неорганических солевых отходов. 4 з.п.ф-лы, 2 табл.
| Способ получения смеси 4,4 -дихлордифенилсульфона и -хлорбензолсульфохлорида | 1975 |
|
SU763332A1 |
| DE 1972805 А1, 07.01.1999 | |||
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
Авторы
Даты
2002-08-20—Публикация
2001-05-03—Подача