Изобретение относится к микробиологии и может быть использовано при контроле биологической активности препаратов для лечения и профилактики дисбактериозов (пробиотиков) медицинского и ветеринарного назначения.
Известно, что одним из показателей специфической активности пробиотиков (колибактерин, бификол, лактобактерин и др.) и производственных штаммов бактерий для их изготовления является наличие антагонистического действия в отношении патогенной и условно-патогенной микрофлоры. Антагонистическую активность пробиотиков и бактериальных штаммов определяют in vitro регламентированными способами, которые включают совместное культивирование с тест-культурами в жидкой или на плотной питательной среде. Наиболее распространен способ отсроченного антагонизма, когда подсев тест-штаммов на плотную питательную среду проводится через определенный период после посева испытуемой культуры. Подсев тест-штаммов, в качестве которых используют патогенные и условно-патогенные культуры шигелл, стафилококков, протея и др., проводят в виде перпендикулярных штрихов к выросшей испытуемой культуре. Антагонистическая активность последней количественно характеризуется величиной зоны подавления роста каждого тест-штамма, измеряемой в мм (ФС 42-3365-97 "Колибактерин сухой").
Недостатками данного способа определения антагонистической активности являются: использование патогенных и условно-патогенных бактериальных штаммов, работа с которыми трудоемка и требует специальных условий; затраты дорогостоящих питательных сред при проведении теста; значительная продолжительность теста (несколько суток).
Целью данного изобретения является разработка более простого способа определения антагонистической активности пробиотиков. Поставленная цель достигается благодаря тому, что в качестве тест-штамма используется культура светящихся бактерий.
Сущность изобретения заключается в следующем. Развитие in vitro бактериальной культуры, обладающей антагонистической активностью, сопровождается продукцией комплекса метаболитов, ингибирующих функциональную активность и развитие других популяций. Оценка антагонистической активности пробиотика может быть основана не только на учете подавления роста тест-культуры, но и с помощью определения угнетения отдельных функций, качественные и количественные изменения которых поддаются объективному контролю. Люминесцентные бактерии, интенсивность свечения которых обусловлена активностью фермента люциферазы, реагируют на интибирующее воздействие снижением интенсивности люминесценции (А. с. СССР 1335569, кл. С 12 Q 1/04; G 01 N 33/48, 1987 и А.с. СССР 1540439, кл. G 01 N 33/18, 1987). Для выявления данного эффекта не требуется совместное культивирование бактерий испытуемой и контрольной культур. Проявление данного эффекта поддается количественному учету при кратковременной совместной экспозиции препарата и тест-культуры (в течение 2 часов). Предлагаемый способ, исключая необходимость применения питательных сред, позволяет экспрессно оценить антагонистическую активность препаратов, содержащих бактериальные культуры или культуральные жидкости.
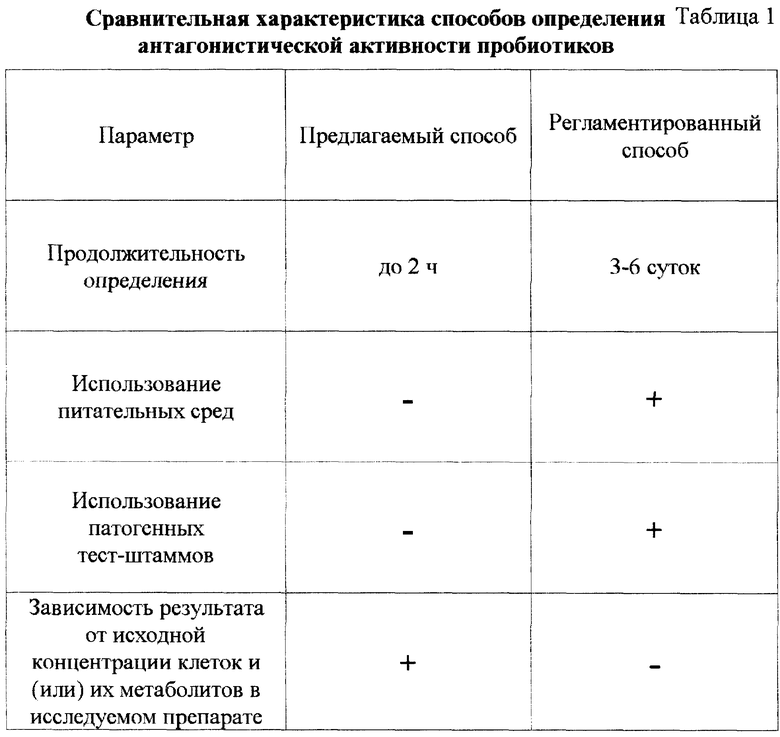
Достигаемый технический результат заключается в упрощении, снижении продолжительности и трудоемкости способа контроля пробиотиков (табл. 1).
Для осуществления предлагаемого способа могут быть использованы бактерии штаммов "Эколюм", "Escherichia coli lum+" и др., входящие в качестве биосенсоров в состав тест-систем для определения токсичности воды и водных экстрактов из объектов окружающей среды (ТУ 6-09-20-236-93, ТУ 846-001-0453805-00), и измерительные приборы - люминометры серии "Биотокс" (ТУ 446-У-028-00-ОТУ). Указанные тест-системы комплектуются биосенсорами в виде лиофилизированных культур.
Оценка антагонистической активности препарата основана на определении изменения интенсивности биолюминесценции бактерий и выражается количественно в виде индекса антагонистической активности - ИАА (безразмерная величина) по формуле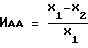
где X1 - интенсивность биолюминесценции контрольной (без препарата) пробы;
Х2 - интенсивность биолюминесценции опытной (с препаратом) пробы через определенное время совместной экспозиции исследуемого препарата и тест-штамма.
Уменьшение интенсивности биолюминесценции тест-штамма прямо пропорционально антагонистическому эффекту. Прибор "Биотокс" позволяет автоматически вычислять ИАА и производить обработку результатов измерений ИAA путем расчета среднеарифметического значения из трех параллельных измерений (контроль-опыт) в короткий промежуток времени.
Подготовка к проведению измерений включает регидратацию лиофилизированного тест-штамма 0,9%-ным раствором натрия хлорида, охлажденного до (4-8)oС в течение 30 мин. Регидратированную тест-культуру выдерживают не менее 30 мин до достижения температуры (15-20)oС. Необходимый для выполнения анализа (в трех повторностях) объем исследуемого препарата и тест-культуры составляет не более 1,5 мл. Для проведения измерения по 0,5 мл исследуемого препарата и тест-культуры помещают в три опытные кюветы объемом по 1,5 мл. В три контрольные кюветы добавляют по 0,5 мл 0,9%-ного раствора натрия хлорида и тест-культуры. Биотест проводится при темпераруре (15-20)oС и рН (6,5-8,0). Работа на приборе "Биотокс" производится согласно инструкции по эксплуатации прибора.
Пример 1. Контроль лактобактерина.
Ампулу с сухим лактобактерином вскрывают и регидратируют 0,9%-ным раствором натрия хлорида с температурой (15-20)oС из расчета 1 мл на одну дозу препарата. Продолжительность регидратации при интенсивном встряхивании составляет (2-5) мин. Из цельной суспензии с помощью 0,9%-ного раствора натрия хлорида готовят 5-ти и 10-кратное разведение препарата. По 0,5 мл цельного препарата и его разведении помещают в кюветы с 0,5 мл тест-штамма и выдерживают в течение 2 ч при температуре 20oС. Далее производят измерения ИАА на приборе "Биотокс". Величина ИАА зависит от концентрации препарата в пробе и составляет: для цельного лактобактерина - не менее 99; для разведения 5-кратного - не менее 10; для разведения 10-кратного - 0.
Пример 2. Контроль колибактерина.
Ампулу с сухим колибактерином вскрывают и регидратируют 0,9%-ным раствором натрия хлорида с температурой (15-20)oС из расчета 1 мл на одну дозу препарата. Продолжительность регидратации при интенсивном встряхивании составляет (2-5) мин. Из цельной суспензии с помощью 0,9%-ного раствора натрия хлорида готовят 5-ти и 10-кратное разведение препарата. По 0,5 мл цельного препарата и его разведений помещают в кюветы с 0,5 мл тест-штамма и выдерживают в течение 1 ч при температуре 20oС. Далее производят измерения ИАА на приборе "Биотокс". Величина ИАА зависит от концентрации препарата в пробе и составляет: для цельного колибактерина - не менее 96; для разведения 5-кратного - не менее 40; для разведения 10-кратного - менее 40.
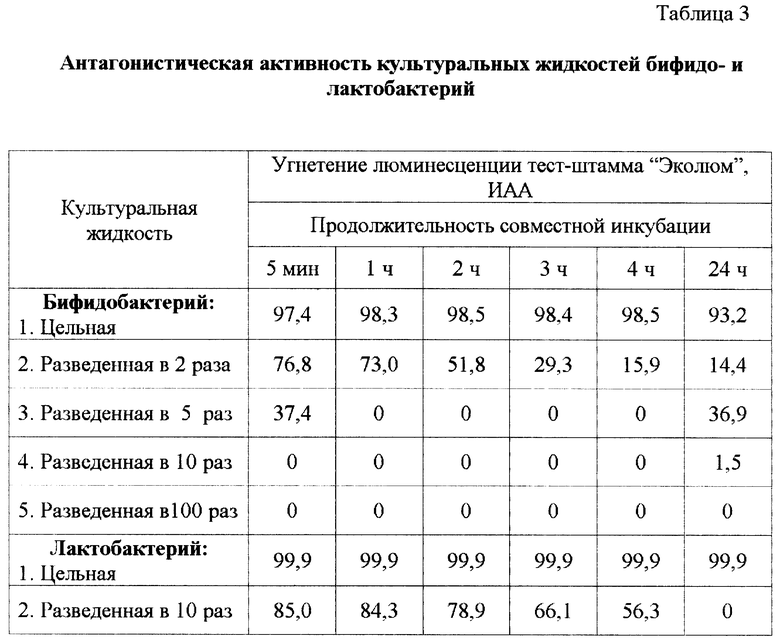
Пример 3. Контроль препарата на основе культуральной жидкости бифидобактерий штамма Bifidobacterium bifidum 1.
Из жидкого препарата с помощью 0,9%-ного раствора натрия хлорида готовят 2-х и 10-кратное разведение. По 0,5 мл цельного препарата и его разведении помещают в кюветы с 0,5 мл тест-штамма и выдерживают в течение 5 мин при температуре 20oС. Далее производят измерения ИАА на приборе "Биотокс". Величина ИАА зависит от концентрации препарата в пробе и составляет: для цельной культуральной жидкости - не менее 97; для разведения 2-кратного - не менее 70; для разведения 10-кратного - 0.
Применение предлагаемого способа контроля антагонистической активности пробиотиков предполагает определение параметров величины ИАА, продолжительности экспозиции и концентрации исследуемого материала для каждого препарата.
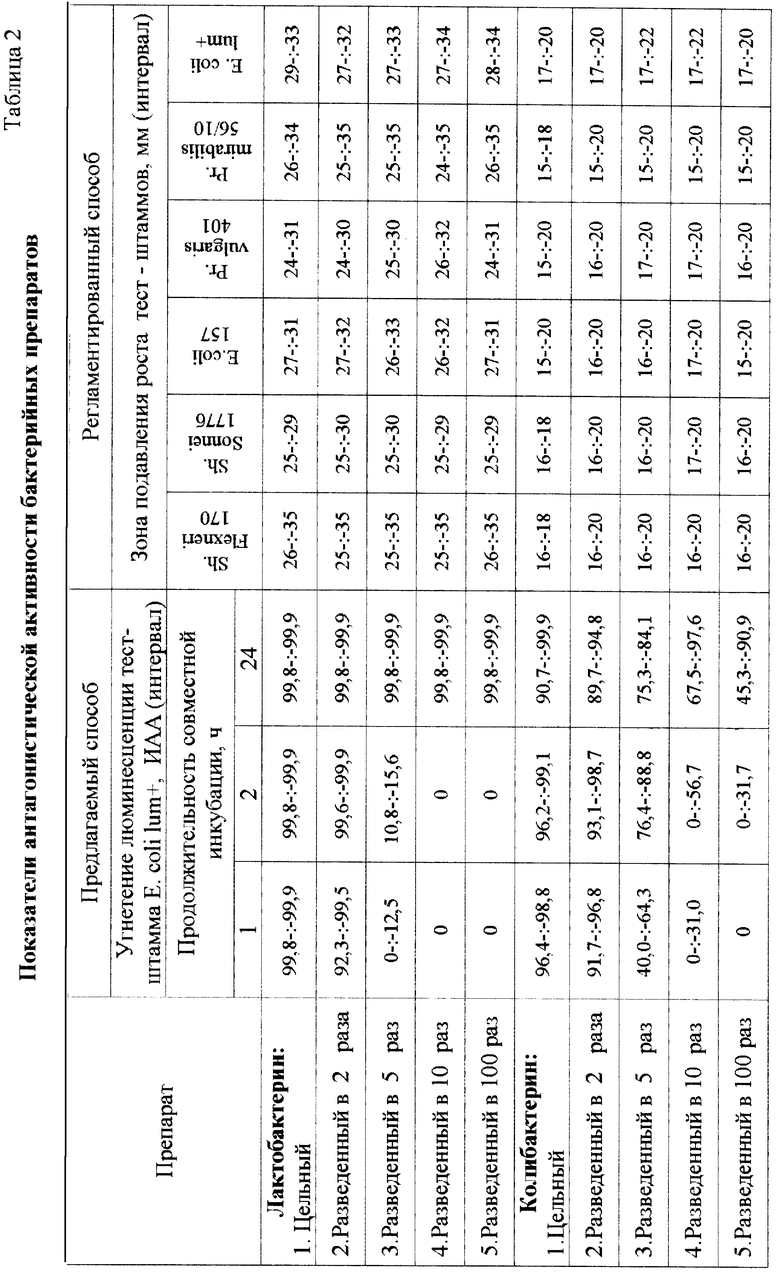
Сравнительные результаты антагонистической активности препаратов по отношению к различным тест-штаммам приведены в табл. 2 и 3.
Таким образом, разработанный способ контроля может быть использован в качестве основного или дополнительного теста при определении антагонистической активности пробиотиков на основе бактерий и (или) их метаболитов.
Изобретение относится к медицине, в частности к микробиологии. Способ контроля антагонистической активности препаратов in vitro основан на определении ингибирования биолюминесценции тест-штамма при кратковременной совместной экспозиции с испытуемым препаратом. Способ обеспечивает экспрессность, исключает расход питательных сред, прост в исполнении. 3 табл.
Способ определения антагонистической активности пробиотиков, включающий воздействие пробиотика на бактериальную тест-культуру, отличающийся тем, что в качестве тест-культуры используют люминисцентные бактерии, а антагонистическую активность пробиотика оценивают по изменению интенсивности биолюминесценции бактерий тест-культуры.
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| ШТАММ BACILLUS SUBTILIS ТРАХС, РЕЗИСТЕНТНЫЙ К ТЕТРАЦИКЛИНУ, РИФАМПИЦИНУ, АМПИЦИЛЛИНУ, ХЛОРАМФЕНИКОЛУ, СТРЕПТОМИЦИНУ, ОБЛАДАЮЩИЙ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ПАТОГЕННЫМ ВИДАМ МИКРООРГАНИЗМОВ | 1997 |
|
RU2118364C1 |
| ШТАММ БАКТЕРИЙ BACILLUS SUBTILIS, НЕСУЩИЙ СВОЙСТВО АНТИБИОТИКОРЕЗИСТЕНТНОСТИ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРЕПАРАТА "БАКТИСПОРИН" | 1995 |
|
RU2067616C1 |
| СПОСОБ ОЦЕНКИ РЕАКТОГЕННОСТИ И ИММУНОЛОГИЧЕСКОЙ БЕЗОПАСНОСТИ ВАКЦИНЫ | 1995 |
|
RU2086983C1 |
Авторы
Даты
2002-08-20—Публикация
2000-07-10—Подача