Изобретение относится к способу получения 2,5,8-тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинона (1) - полупродукта в синтезе 2,3,5,6,8-пентагидрокси-7-этил-1,4-нафтохинона (эхинохрома А), являющегося действующим началом кардиопротекторного и офтальмологического препаратов гистохром [1, 2].
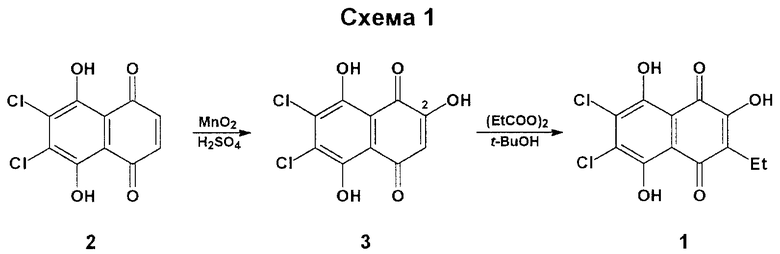
Известен способ получения целевого продукта 1, заключающийся в окислении 5,8-дигидрокси-2,3-дихлор-1,4-нафтохинона (2) диоксидом марганца (MnO2) в конц. H2SO4 и последующем свободнорадикальном С-этилировании полученного 2-гидрокси-6,7-дихлорнафтазарина (3) пропионилпероксидом (ЕtСОО)2 в кипящем трет-бутаноле (см. схему 1 в конце описания) [3].
Недостатком этого способа является использование пропионилпероксида, технологически неприемлемого из-за своей взрывоопасности.
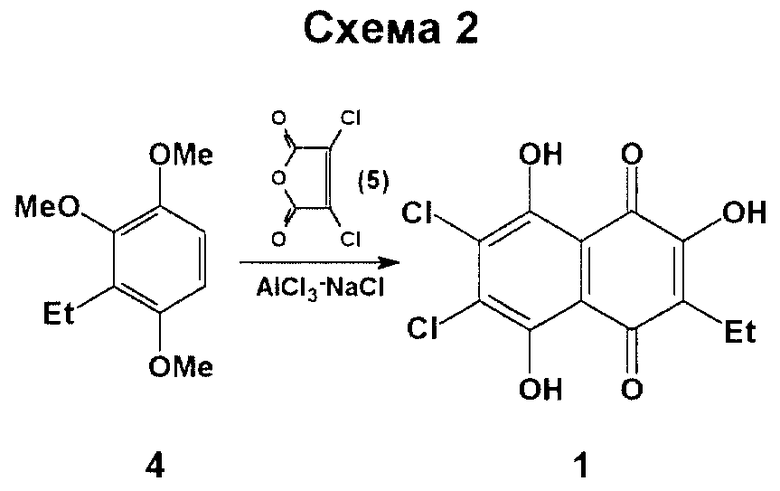
Наиболее близким к предлагаемому способу является способ получения 2,5,8-тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинона циклоацилированием 1,2,4-триметокси-3-этилбензола (4) дихлормалеиновым ангидридом (ДХМА, 5) в присутствии хлористого алюминия и хлорида натрия (см. схему 2 в конце описания) [3].
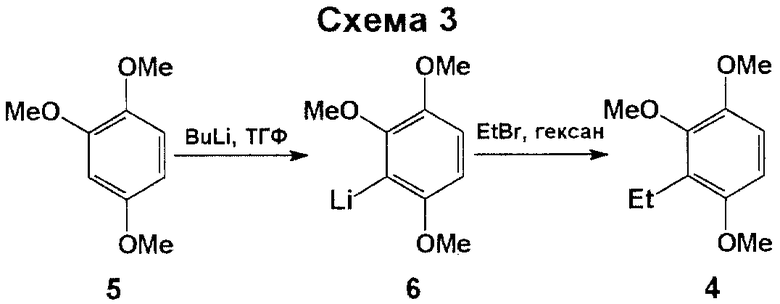
Недостатком этого способа является использование исходного субстрата 4, получаемого способом, в котором применяются пожароопасные реагенты. Последний заключается в литиировании 1,2,4-триметоксибензола (5) действием бутиллития (BuLi) в абс. тетрагидрофуране (ТГФ) и последующем этилировании полученного литиевого производного 6 этилбромидом в абс. гексане (см. схему 3 в конце описания) [4]. Растворы алкиллития в абсолютных органических растворителях являются пожароопасными реагентами и их приготовление сопряжено с известными трудностями [5].
Задача изобретения - разработка способа получения 2,5,8-тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинона (1), в котором используют исходное вещество, получаемое способом, не требующим применения пожароопасных реагентов.
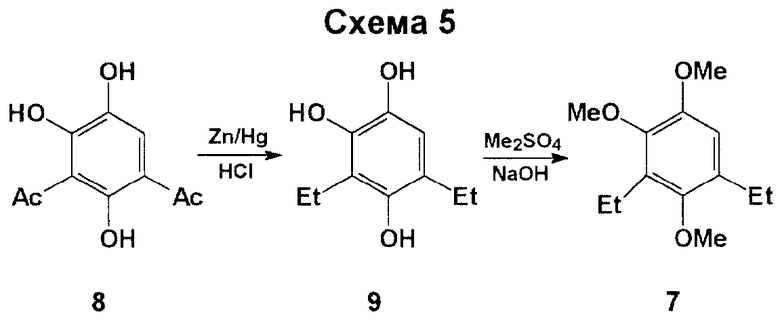
Задача решена тем, что в способе получения 2,5,8-тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинона циклоацилированием производного гидрохинона дихлормалеиновым ангидридом в присутствии хлористого алюминия и хлорида натрия в качестве производного гидрохинона используют 1,2,4-триметокси-3,5-диэтилбензол (7), получаемый путем восстановления 3,5-диацетил-1,2,4-тригидроксибензола (8) до 1,2,4-тригидрокси-3,5-диэтилбензола (9) с последующим его исчерпывающим метилированием.
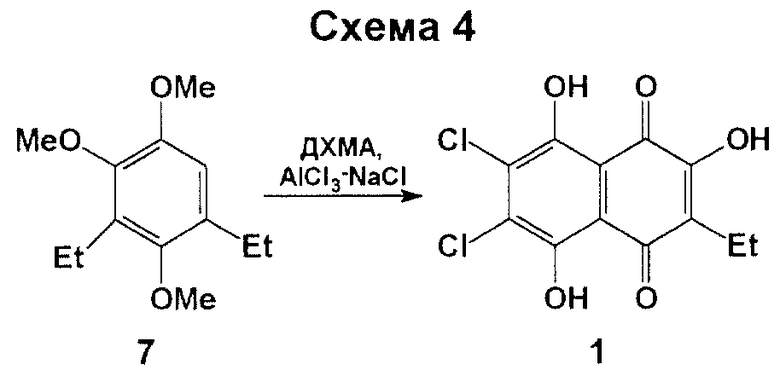
Предлагаемый способ получения целевого продукта 1 представлен на схеме 4, приведенной в конце описания.
В качестве исходного субстрата авторы используют соединение 7, а именно 1,2,4-триметокси-3,5-диэтилбензол, которое впервые получено путем восстановления 3,5-диацетил-1,2,4-тригидроксибензола (8) до 1,2,4-тригидрокси-3,5-диэтилбензола (9) с последующим его исчерпывающим метилированием (см. схему 5 в конце описания).
Конверсию 8-->9 осуществляют каким-либо восстанавливающим агентом, например, действием амальгамы цинка в водной кислоте, а конверсию 9-->7 - метилирующим агентом, например, действием диметилсульфата в водной щелочи. Соединение 7, используемое в предлагаемом способе в качестве исходного, получено способом, не требующим использования пожароопасных реагентов и абсолютных растворителей в отличие от его эквивалента - соединения 4, используемого в качестве исходного субстрата в способе-прототипе.
Сведения, подтверждающие возможность осуществления изобретения.
1,2,4-Тригидрокси-3,5-диэтилбензол (9). В трехлитровую колбу, снабженную механической мешалкой, не доходящей до дна, и обратным холодильником, помещают 600 г твердой амальгамы цинка [6], 31,5 г (0,15 моль) 3,5-диацетил-1,2,4-тригидроксибензола (8) [7] и 375 мл конц. HCl. Энергично перемешивая, реакционную смесь нагревают до кипения и спустя 30 мин порциями добавляют еще 31,5 г (0,15 моль) субстрата 8 и 375 мл конц. HCl. Смесь кипятят при перемешивании 3 ч, горячий раствор декантируют и оставляют на ночь. Образовавшийся на поверхности раствора при охлаждении верхний твердый слой и выпавший белый осадок отделяют фильтрованием и промывают небольшим (30 мл) количеством ледяной воды. Получают 58 г сырого продукта, который согласно данным ЯМР 1H спектроскопии содержит 80% (46,4 г) 1,2,4-тригидрокси-3,5-диэтилбензола (9). Спектр ЯМР 1H (СDСl3, δ, м.д.): 1,18 т (3Н, J 7,8, Me), 1,20 т (3Н, J 7,8, Me), 2,52 к (2Н, J 7,8, СН2), 2,68 к (2Н, J 7,8, CH2), 4,35 уш. с (1Н, ОН), 4,54 уш. с (1Н, ОН), 5,15 уш. с (1Н, ОН), 6,56 с (1Н, Наром.). Полученный сырой продукт 9 используют для получения 1,2,4-триметокси-3,5-диэтилбензола (7) без очистки.
1,2,4-Триметокси-3,5-диэтилбензол (7). Прибор состоит из четырехгорлой колбы, снабженной механической мешалкой, обратным холодильником, капельной воронкой и термометром. Сырой продукт (56,9 г), содержащий 45,5 г (0,25 моль) 1,2,4-тригидрокси-3,5-диэтилбензола (9) быстро в атмосфере азота обрабатывают щелочью, добавляя при энергичном перемешивании 400 г (360,7 мл) 10%-ного раствора едкого натра. Затем из капельной воронки добавляют 94,5 г (70,95 мл, 0,75 моль) диметилсульфата; реакционную смесь при этом хорошо перемешивают. Необходимо следить, чтобы температура не поднималась выше 40oС (охлаждение водой). После прибавления диметилсульфата реакционную смесь нагревают на кипящей водяной бане в течение 30 мин. После охлаждения реакционной смеси органический слой отделяют, а водный слой экстрагируют бензолом. Объединенные органические слои промывают разбавленным раствором едкого натра, а затем водой, сушат хлористым кальцием и растворитель удаляют в вакууме водоструйного насоса (20-30 мм рт. ст.). Остаток фракционируют в вакууме. Фракция с Ткип 133-139oС (7 мм рт. ст.) представляет собой 1,2,4-триметокси-3,5-диэтилбензол (7), выход 45,9 г (82%). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1,19 т (3Н, J 7,8, Me), 1,24 т (3Н, J 7,8, Me), 2,64 к (2Н, J 7,8, СН2), 2,66 к (2Н, J 7,8, CH2), 3,71 с (3Н, ОМе), 3,82 с (3Н, ОМе), 3,83 с (3Н, ОМе), 6,60 с (1Н, Наром.).
2,5,8-Тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинон (1). В расплав 410 г (3,07 моль) безв. АlСl3 и 80,8 г (1,38 моль) NaCl при 140oС при интенсивном перемешивании вносят смесь 44,8 г (0,2 моль) 1,2,4-триметокси-3,5-диэтилбензола (7) и 76,8 г (0,46 моль) дихлормалеинового ангидрида. Температуру смеси повышают до 195oС и расплав перемешивают 5 мин. Реакционную смесь охлаждают и гидролизуют раствором 300 мл конц. HCl в 4,0 л Н2О. Выделившийся за 12 ч осадок отделяют, промывают 2,0 л горячей Н2О и сушат. Горячей экстракцией хлороформом извлекают сырой продукт 1, который кристаллизуют из системы EtOH-H2O. Получают 2,5,8-тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинон (1), 36,0 г (59%), Тпл 156-158oС. Спектр ЯМР1Н (СDСl3, δ, м.д.): 1.18 т (3H, J 7,7, Me), 2,66 к (2Н, J 7,7, CH2), 7,42 (шир. сигн., 1 Н, β-ОН), 12,07 (уш. с, 1Н, α-ОН), 13,60 (с, 1Н, α-ОН). Масс-спектр [m/z (Iотн., %)]: 302/304/306 (М+, 100).
ЛИТЕРАТУРА
1. Патент РФ 2137472 // БИ 26, 1999.
2. Патент РФ 2134107 // БИ 22, 1999.
3. Anufriev V.Ph., Novikov V.L., Maximov О.В., Elyakov G.В., Levitsky D. О. , Lebedev A.V., Sadretdinov S.M., Shvilkin A.V., Afonskaya N.I., Ruda M. Ya, Cherpachenko N.M. // Bioorg. Med. Chem. Lett. 1998. Vol. 8, 6. P. 587-592.
4. Чижова А.Я., Кочергина Т.Ю., Ануфриев В.Ф., Денисенко В.А., Глазунов В.П. //Изв. АН, Сер. хим. 1999. 5. С. 947-952.
5. Уэйкфилд Б. Методы синтеза с использованием литийорганических соединений. M.: Мир. 1991. 183 с.
6. Карякин Ю. В. , Ангелов И.И. Чистые химические вещества. M.: Химия. 1974. С. 398.
7. Desai R.D., Mavani С.К. //J. Sci. Ind. Res. (India). 1953. Vol. 12 В. Р. 236-239.2
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5,8-ДИГИДРОКСИ-2,6-7-ТРИМЕТОКСИ-3-ЭТИЛ-1,4-НАФТОХИНОНА | 2005 |
|
RU2277083C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 2,3,5,8-ТЕТРАГИДРОКСИ-1,4-НАФТАХИНОНОВ | 1990 |
|
RU2022959C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5,8-ДИГИДРОКСИ-2,3,6-ТРИМЕТОКСИ-7-ЭТИЛ-1,4-НАФТОХИНОНА | 2001 |
|
RU2203265C2 |
| СПОСОБ ПОЛУЧЕНИЯ 6,7-ЗАМЕЩЕННЫХ 2,3,5,8-ТЕТРАГИДРОКСИ-1,4-НАФТОХИНОНОВ (СПИНАЗАРИНОВ) | 2012 |
|
RU2478607C1 |
| Способ получения 2,3,5,6,8-пентагидрокси-1,4-нафтохинона (спинохрома D) и промежуточные соединения, используемые в этом способе | 2016 |
|
RU2632668C2 |
| Способ получения спинохрома D | 2016 |
|
RU2612265C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИНОХРОМА Е | 2014 |
|
RU2561280C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЗАМЕЩЕННЫХ 3,3-ДИМЕТИЛ-3,4-ДИГИДРОИЗОХИНОЛИНОВ | 2001 |
|
RU2213735C2 |
| НОВЫЕ ОПТИЧЕСКИ АКТИВНЫЕ 4-ГИДРОКСИ-2-АЗА-9,10-АНТРАХИНОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2436775C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИТЕРПЕНОВОГО ГЛИКОЗИДА 3 - 0 - β - D-ГЛЮКОПИРАНОЗИЛ- (1 _→ 2) -α - Z- АРАБИНОПИРАНОЗИДА ХЕДЕРАГЕНИНА | 1994 |
|
RU2064934C1 |
Изобретение относится к усовершенствованному способу получения 2,5,8-тригидрокси-6,7-дихлор-1,4-нафтохинона циклоацилированием 1,2,4-триметокси-3,5-диэтилбензола дихлормалеиновым ангидридом в присутствии хлористого алюминия и хлорида натрия. 1,2,4-Триметокси-3,5-диэтилбензол получают восстановлением 3,5-диацетил-1,2,4-тригидроксибензола до 1,2,4-тригидрокси-3,5-диэтилбензола с последующим его исчерпывающим метилированием. Способ обеспечивает получение целевого продукта с выходом 59%, исключение использования пожаропасных реагентов при получении исходного соединения.
Способ получения 2,5,8-тригидрокси-6,7-дихлор-3-этил-1,4-нафтохинона циклоацилированием производного гидрохинона дихлормалеиновым ангидридом в присутствии хлористого алюминия и хлорида натрия, отличающийся тем, что в качестве производного гидрохинона используют 1,2,4-триметокси-3,5-диэтилбензол, получаемый путем восстановления 3,5-диацетил-1,2,4-тригидроксибензола до 1,2,4-тригидрокси-3,5-диэтилбензола, с последующим его исчерпывающим метилированием.
| Известия АН | |||
| Серия химическая, 1999, №5, с | |||
| Аэроплан | 1924 |
|
SU947A1 |
| Bioorg | |||
| Med | |||
| Chem | |||
| Lett | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| ПЕРЕНОСНОЙ КУХОННЫЙ ОЧАГ С КИПЯТИЛЬНИКОМ | 1920 |
|
SU587A1 |
| Synth | |||
| Commun | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Способ получения камфоры | 1921 |
|
SU119A1 |
| Synth | |||
| Commun | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Прибор для испытания исправности телефонных линий | 1923 |
|
SU2149A1 |
| Chem | |||
| Ber | |||
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| Зажим для концов велокамер, насаженных на дорн для вулканизации | 1924 |
|
SU2910A1 |
Авторы
Даты
2002-11-27—Публикация
2001-03-05—Подача