Изобретение относится к медицине, физиологии, патофизиологии, биологии и лабораторной диагностике. Диагностическое значение определения протеолитического фермента эластазы в различных отделах медицины, биологии и патофизиологии за последние годы резко возросло. Это связано с участием данного фермента в патогенезе многих заболеваний. Известно, что одной из причин нарушений регуляций многих функций организма, приводящих к патологии, является освобождение внутриклеточных протеолитических ферментов (Хендерсон Дж. Патофизиология органов пищеварения. С.-Петербург, 1997).
Особый интерес представляет сериновая протеиназа - лейкоцитарная эластаза, увеличение содержания которой наблюдается при острых и хронических воспалениях, некротических и других патологических процессах (Яровая Г.А., Доценко В. Л., Нешкова Е.А. Патогенетическая роль лейкоцитарной эластазы. Новый спектрофотометрический метод ее определения в плазме крови человека / Ассоциация медицинской лаборатории. Диагностика. Информационный бюллетень. 1, 1995, с. 16-18).
Являясь биохимическим маркером воспалительного процесса, эластаза может играть решающую роль в патогенезе тромбогеморрагических осложнений, нарушений дыхательной функции легких и множественной недостаточности органов как следствие обширных травм, перитонита и септицемий. В связи с вышеуказанными обстоятельствами определение уровня активности лейкоцитарной эластазы в плазме/сыворотке крови является важным показателем интенсивности степени развития воспалительной реакции, высокого риска развития тромбогеморрагических нарушений.
Прямое определение активности лейкоцитарной эластазы в крови и других биологических жидкостях связано с определенными трудностями, в основном, обусловленными быстрым взаимодействием фермента с L1-протеиназным ингибитором (L1-ПИ).
В связи с этим количество лейкоцитарной эластазы в плазме крови обычно оценивают иммунохимическими способами (радиоиммунологическими и иммуноферментными) - (Dunn et al., Anal. Biochem. 150:18-25,1985; Neuman et. al., Clin. Chem. Biochem. 22:693-697,1984; Jochum M., Frutz H./Selected Topics in clinical Enzymology/ Ed. D. M. Golberg, M.Werner. - Berlin, 1983.-Vol.2.-p. 13-18; Stein Т., et al. Immunoreactive elastase 1: Clinical evaluation of a new noninvasive test of pancreatic function // Clin.chem., - 1996.-Vol.42., 2.-р.222-226).
Вышеуказанные способы наряду с несомненными достоинствами (высокая чувствительность и специфичность) имеют ограничения в применении, наиболее важным из которых является невозможность оценки активности фермента. Измерительная процедура трудоемка, требует, например:
1) предварительной подготовки биологического материала,
2) многоэтапного проведения ИФА-анализа,
3) поэтапного внесения буферов,
4) многократной инкубации, измерения оптической плотности на ИФА-анализаторе,
5) построения эталонной кривой и вычисления концентрации эластазы.
Главные недостатки указанных аналогов:
- длительное время определения,
- высокая стоимость наборов.
Нами в качестве прототипа использован спектрометрический способ определения эластазы из комплекса с L1-ПИ и определение ее энзиматической активности непосредственно в плазме крови/сыворотке (В.Л. Доценко, Е.А. Нешкова, Г. А. Яровая. Выявление лейкоцитарной эластазы человека из комплекса с плазменным L1-протеиназным ингибитором по ее энзиматической активности с синтетическим субстратом // Вопросы медицинской химии, 1994, 3, с. 20-25).
Способ осуществляют следующим образом.
1. Активность эластазы определяют по скорости гидролиза N-третбутокси-карбонил-аланин-р-нитрофенилового эфира (BOC-Ala-ONp) и метокси-сукцинил-аланил-аланил-пропил-валин-р-нитроанилиду (MSAAPVpNA). Удельная активность препаратов эластазы по первому субстрату составляет 3-8 мкмоль/мин на 1 мг белка. Удельная амидазная активность эластазы, определяемая по MSAAPVpNA, составляет 4-7 мкмоль/мин на 1 мг белка. Кинетические свойства препаратов эластазы, определенные по вышеуказанным субстратам при 37oС, имеют следующие значения: для BOC-Ala-ONp рН 6,5 Км= 0,35 мМ, отношение Ккат/Км=11,7-103 М-1•с-1; для MSAAPVpNA рН 7,5 Км= 0,1 мМ, отношение Ккат/Км=117-103 М-1•с-1.
2. Молярную концентрацию фермента рассчитывают, используя величину концентрации белка в препарате эластазы. В экспериментах по подбору условий диссоциации комплекса эластаза - а1-ПИ используют коммерческий препарат ингибитора (фирма "Sigma") в концентрации 5 мг/мл в 0,1М трис-НСl-буферном растворе рН 8,0 или сыворотку крови доноров, разведенную в 15-50 раз физиологическим раствором NaCl. Лейкоцитарную эластазу в объеме 5-15 мкл с активностью 1,8-13,3 мЕ по MSAAPVpNA добавляют непосредственно в раствор ингибитора или в разведенную сыворотку крови (10-50 мкл), находящиеся в кювете спектрофотометра, и инкубируют 3 мин при комнатной температуре Контролем за полнотой ингибирования эластазы служит активность аналогичной смеси, определяемая по MSAAPVpNA в стандартных условиях.
3. Эластазоподобную активность плазмы крови определяют по скорости гидролиза BOC-Ala-ONp методом, примененным для определения этой активности в плазме крови Г.А. Парфенковой и соавт.
4. Влияние различных условий предварительной инкубации комплекса (рН 3,0, присутствие ацетона и ацетонитрила в инкубате) и условий определения активности фермента (состав буферного раствора, концентрация субстрата) исследуют по следующей схеме: после образования комплекса в кювету спектрофотометра добавляют 0,25-0,3 мл 0,1М NaH2PO4 с рH, доведенным ортофосфорной кислотой до 3,0, или физиологический раствор NaCl с тем же рН. Добавляемые в кювету растворы содержали определенную концентрацию ацетона или ацетонитрила. После инкубации в течение 3 мин и добавления соответствующего буферного раствора и субстрата определяют активность фермента.
5. Регистрацию скорости расщепления субстратов выявляемым ферментом производят на компьютеризированном двухлучевом спектрофотометре "Hitachi U-3200" при 30oС, используя и качестве оптического контроля кювету, содержащую все ингредиенты, кроме эластазы и сыворотки.
Недостатки способа:
1. Трудоемкость исполнения.
2. Неточность исследования в связи с нарушением нативности субстратов эластазы.
3. Дороговизна способа.
4. Использование токсических препаратов.
Задачи:
1. Упростить способ приготовления пробы.
2. Выделить микротипы кристаллов по картине специфической кристаллизации эластазы за счет повышения уровня ее содержания в сыворотке крови.
3. Выявить типовые кристаллограммы сыворотки крови при гинерэластаземии, обусловленной различными заболеваниями,
4. Сокращение стоимости определения эластазы.
5. Снижение трудоемкости, исключение использования токсичных ингредиентов.
6. Повышение точности.
Сущность изобретения заключается в том, что для определения гиперэластаземии сыворотку кропи наносят на кварцевую подложку, накрывают покровным стеклом, сушат при Т=+37-38oC, выдерживают на открытом воздухе 3,5-4 ч, затем исследуют в проходящем свете, и при наличии в препарате агрегации из прямоугольных и призматических кристаллов определяют гиперэластаземию.
Способ осуществляют следующим образом.
1. Для забора берут кровь из вены 3,0 мл, центрифугируют для получения сыворотки.
2. Сыворотку в виде капель объемом 0,01-0,02 мл каждая наносят на кварцевую подложку и накрывают покровным стеклом.
3. Высушивают в термостате при Т=+37-38oС на протяжении 1,5-2 ч.
4. Выдерживают на открытом воздухе 3,5-4 ч.
5. Под микроскопом в проходящем свете изучают картину кристаллизации, и при наличии в препарате агрегаций из мелких прямоугольных и призматических кристаллов определяют гиперэластаземию (перенасыщение сыворотки крови эластазой).
Нами предварительно были смоделированы эталонные кристаллограммы, для чего сыворотку крови здорового человека, помещенную в емкость, изготовленную из горного хрусталя, обогащали лейкоцитарной эластазой.
На фото 1(а-в) представлены эталонные кристаллограммы (КГ) сыворотки крови здорового человека, обогащенной эластазой.
КГ выполнены: агрегациями из прямоугольных кристаллов, фото 1а, концентрация эластазы - 220 нмоль/мин; агрегациями из прямоугольных и призматических кристаллов, фото 1б, концентрация эластазы - 270 нмоль/мин; агрегациями из прямоугольных и призматических кристаллов, фото 1в, концентрация эластазы - 430 нмоль/мин.
Нами проведено 1198 экспериментальных исследований.
Примеры.
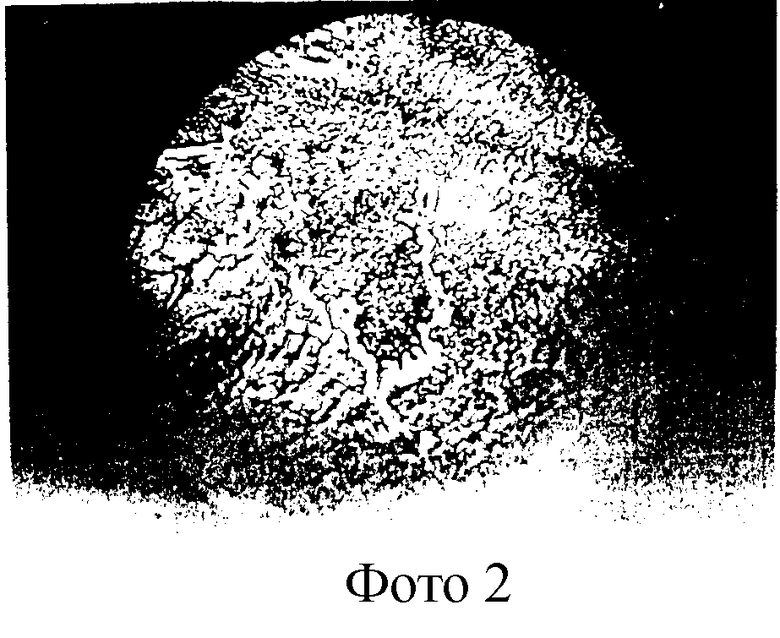
Пример 1, фото 2. Б-ная К., история болезни 238. Диагноз: Приступ острого панкреатита. На фото 2 приведена КГ сыворотки крови б-ной К., присутствуют агрегации из мелких прямоугольных и призматических кристаллов.
Технология: из вены б-ной К. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(5), объемом 0,01 мл каждая, нанесли на кварцевую подложку толщиной не менее 10 мм, каждую каплю накрыли покровным стеклом и высушили в термостате при Т=+37-38oС на протяжении 1,5 ч, затем выдержали на открытом воздухе 3,5 ч и изучили в проходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов, одновременно в СК определили уровень эластазы, который оказался повышенным и составил - 210 нмоль/мин при норме 190,1±3,40 нмоль/мин, предполагаемая гиперэластаземия подтвердилась.
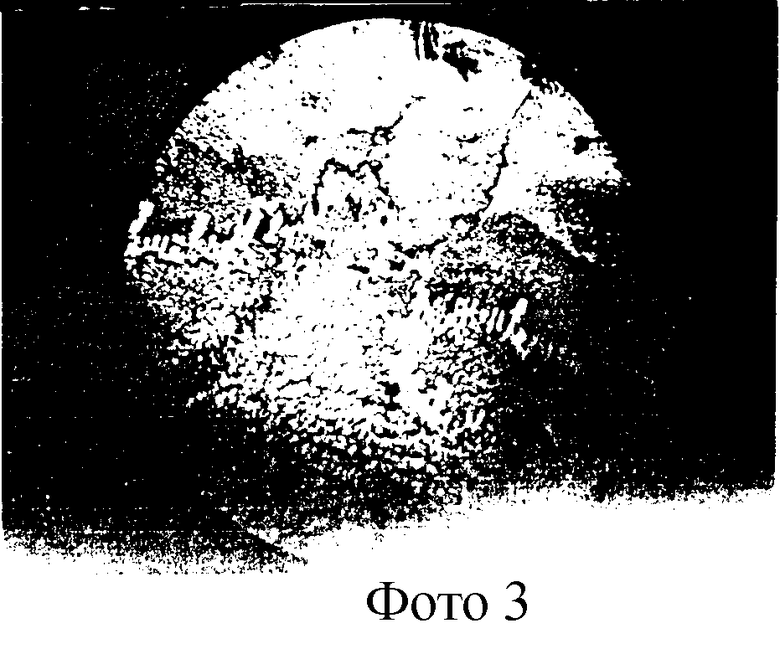
Пример 2, фото 3. Б-ной В., история болезни 1139. Диагноз: Проникающее ранение брюшной полости. Тромбоз мезентериальных артерий. На фото 3 приведена КГ сыворотки крови б-ного В., присутствуют агрегации из прямоугольных и призматических кристаллов.
Технология: из вены б-ного В. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(3), объемом 0,02 мл каждая, нанесли на кварцевую подложку толщиной около 10 мм, каждую каплю накрыли покровным стеклом и высушили в термостате при Т=+37-38oС на протяжении 2 ч, затем выдержали на открытом воздухе 4 ч и изучили в проходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов, одновременно в СК определили уровень эластазы, который оказался повышенным и составил - 236 нмоль/мин при норме 190,1±3,40 нмоль/мин, предполагаемая гиперэластаземия подтвердилась.
Пример 3, фото 4. Б-ная Ж., история болезни 1385. Диагноз: Послеродовый сепсис. На фото 4 приведена КГ сыворотки крови б-ной Ж., присутствуют агрегации из прямоугольных и призматических кристаллов.
Технология: из вены 6-ной Ж. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(5), объемом 0,02 мл каждая, нанесли на кварцевую подложку, каждую каплю накрыли покровным стеклом и высушили в термостате при Т=+37-38oС на протяжении 2 ч, затем выдержали на открытом воздухе 4 ч и изучили в проходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов. Одновременно в СК определили уровень эластазы (ЭЛ), который оказался повышенным и составил - 239 нмоль/мин, норма 190,1±3,40 нмоль/мин, предполагаемая гиперэластаземия подтвердилась.
Пример 4, фото 5. Б-ной Ф., история болезни 1390. Диагноз: Обострение хронического панкреатита. На фото 5 приведена КГ сыворотки крови б-ного Ф., присутствуют агрегации из прямоугольных и призматических кристаллов.
Технология: из вены б-ного Ф. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(4), объемом 0,02 мл каждая, нанесли на кварцевую подложку, каждую каплю накрыли покровным стеклом и высушили в термостате при Т=+38oС на протяжении 1,5 ч, затем выдержали на открытом воздухе 4 ч и изучили в проходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов, одновременно в СК определили уровень ЭЛ, который оказался повышенным и составил - 240 нмоль/мин при норме 190,1±3,40 нмоль/мин. Предлагаемая гиперэластаземия подтвердилась.
Пример 5, фото 6. Б-ная О., история болезни 1459. Диагноз: Хронический миелолейкоз, бластный криз. На фото 6 приведена КГ сыворотки крови б-ной О., присутствуют агрегации из прямоугольных и призматических кристаллов.
Технология: из вены б-ной О. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(5), объемом 0,01 мл каждая, нанесли на кварцевую подложку, каждую каплю накрыли покровным стеклом и высушили в термостате при Т=+37oС на протяжении 2 ча, затем выдержали на открытом воздухе 3,5 ч и изучили в проходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов, одновременно в СК определили уровень эластазы, который оказался повышенным и составил - 218 нмоль/мин, предполагаемая гиперэластаземия подтвердилась.
Пример 6, фото 7. Б-ной М., история болезни 498. Диагноз: Язвенная болезнь ДПК, период обострения, реактивный панкреатит. На фото 7 приведена КГ сыворотки крови б-ного М., присутствуют агрегации из прямоугольных и призматических кристаллов.
Технология: из вены б-ного М. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(4), объемом 0,02 мл каждая, наносили на кварцевую подложку, каждую каплю накрывали покровным стеклом и сушили в термостате при Т=+38oС на протяжении 2 ч, затем выдержали на открытом воздухе 4 ч и изучили в проходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов, одновременно в СК определили уровень эластазы, который оказался повышенным и составил 224 нмоль/мин. Предполагаемая гиперэластаземия подтвердилась.
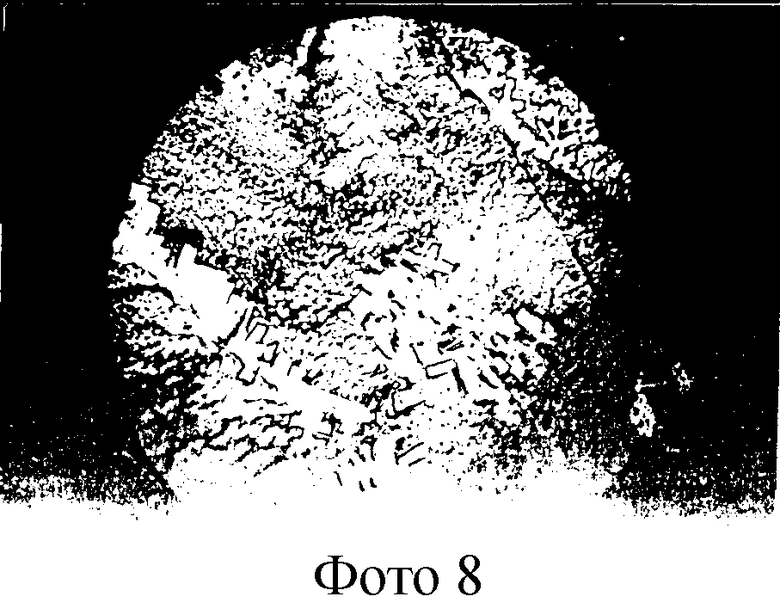
Пример 7, фото 8. Б-ной Ц., история болезни 1345. Диагноз: Сахарный диабет, диабетическая стопа, сепсис. На фото 8 приведена КГ сыворотки крови б-ного Ц., присутствуют агрегации из прямоугольных и призматических кристаллов.
Технология: из вены б-ного Ц. взято 3 мл крови, которая отцентрифугирована для получения сыворотки крови (СК). Капли СК(3), объемом 0,01 мл каждая, наносили на кварцевую подложку, каждую каплю накрывали покровным стеклом и сушили в термостате при Т=+38oС на протяжении 1,5 ч, затем выдержали на открытом воздухе 4 ч и изучили в приходящем свете под микроскопом. Найдены агрегации из прямоугольных и призматических кристаллов, одновременно в СК определили уровень эластазы, который оказался повышенным и составил - 250 нмоль/мин. Предполагаемая гиперэластаземия подтвердилась.
Преимущества предлагаемого способа
1. Упрощение способа определения гиперэластаземии.
2. Отсутствие сложных реактивов и приборов.
3. Экономическая выгода.
4. Возможность экспресс-диагностики гиперэластаземии.
5. Высокая информативность.
6. Достоверность.
7. Исключение использования токсичных компонентов.
Применение способа позволяет повысить достоверность получения результатов, значительно снизить трудозатраты, упростить способ определения гиперэластаземии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ГИПЕРФЕРМЕНТЕМИИ ПРИ НАРУШЕНИИ ВНЕШНЕСЕКРЕТОРНОЙ ФУНКЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2001 |
|
RU2216734C2 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРПРОЛАКТИНЕМИИ | 1999 |
|
RU2174682C2 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРКОРТИЗОЛЕМИИ | 2002 |
|
RU2216023C2 |
| СПОСОБ ЭКСПРЕСС-ДИАГНОСТИКИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ | 2004 |
|
RU2280865C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИПЕРДОФАНЕМИИ И ГИПЕРСЕРОТОНЕМИИ | 2000 |
|
RU2187110C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОБМЕННЫХ НАРУШЕНИЙ | 2000 |
|
RU2176790C1 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРГИСТАМИНЕМИИ | 2002 |
|
RU2223495C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИПЕР-БЕТА-ЭНДОРФИНЕМИИ | 1999 |
|
RU2150111C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИПЕРАЦЕТИЛХОЛИНЕМИИ | 2001 |
|
RU2212665C2 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРСЕКРЕЦИИ ФОЛЛИТРОПИНА И ЛЮТРОПИНА | 2000 |
|
RU2177620C2 |






Изобретение относится к медицине, физиологии, патофизиологии, биологии и лабораторной диагностике и может быть использовано для качественной экспресс-диагностики гиперэластаземии. Предложен способ определения гиперэластаземии, при котором сыворотку крови наносят на кварцевую подложку, накрывают покровным стеклом, сушат при 37-38oС, выдерживают на открытом воздухе 3,5-4 ч, затем исследуют в проходящем свете и при наличии в препарате агрегаций из прямоугольных и призматических кристаллов определяют гиперэластаземию. Технический результат: способ повышает достоверность контроля за гиперэластаземией, снижает трудозатраты. 8 ил.
Способ определения гиперэластаземии, отличающийся тем, что сыворотку крови наносят на кварцевую подложку, накрывают покровным стеклом, сушат при 37-38oС, выдерживают на открытом воздухе 3,5-4 ч, затем исследуют в проходящем свете и при наличии в препарате агрегаций из прямоугольных и призматических кристаллов определяют гиперэластаземию.
| ДОЦЕНКО В.Л | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - Вопросы медицинской химии, 1994, № 3, с | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ЛЕЙКОЦИТАРНОЙ ЭЛАСТАЗЫ В ПЛАЗМЕ КРОВИ | 1993 |
|
RU2039983C1 |
| US 5650275 A1, 22.07.1997 | |||
| WO 8808134 А1, 20.10.1988 | |||
| Устройство для автоматическогоупРАВлЕНия СЕпАРАТОРОМ НЕпРЕРыВНО-циКличЕСКОгО дЕйСТВия | 1978 |
|
SU810290A1 |
Авторы
Даты
2002-12-27—Публикация
2001-06-07—Подача