Изобретение относится к области органической химии, в частности к способу получения транс-3,4-диалкилтетрагидротиофенов общей формулы (1)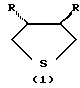
где R=н-C4H9, н-С5Н11, н-С7Н15.
Указанные соединения могут найти применение в качестве ускорителей вулканизации каучука, присадок к смазочным маслам и топливам.
Известен способ ([1] . Джемилев У.М., Ибрагимов А.Г., Ажгалиев М.Н., Муслухов P. P. Синтез и превращения металлоциклов. Сообщение 16. Синтез нового класса ациклических алюминийорганических соединений - трео-2,3-дизамещенных 1,4-диалюмабутанов - с использованием циркониевых катализаторов. Изв. АН. Сер. хим., 1995, 8, с. 1561-1567) получения транс-3,4-дизамещенных тетрагидротиофенов (1) взаимодействием трео-2,3-диалкилзамещенных 1,4-диалюмабутанов с трехкратным избытком элементной серы (S8) в кипящем бензоле (~ 80oС) в атмосфере аргона в течение 8 часов. Целевые продукты образуются с выходами 62-78% по схеме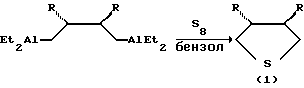
где R=alkyl.
Недостатком известного способа является повышенная пожароопасность процесса, т. к. реакция проходит в кипящем бензоле. Кроме того, бензол является токсичным растворителем, обладающим мутагенными свойствами.
Известен способ ([2]. Джемилев У.М., Ибрагимов А.Г., Ажгалиев М.Н., Муслухов P. P. Синтез и превращения металлоциклов. Сообщение 14. Стереоселективный синтез транс-3,4-дизамещенных диалкилтетрагидротиофенов Изв. АН. Серия хим. , 1994, 2, с.276-278) получения транс-3,4-дизамещенных диалкилтетрагидротиофенов (1) взаимодействием 1-этил-транс-3,4- диалкилалюмациклопентанов с трехкратным избытком элементной серы (S8) в растворе сухого бензола в атмосфере аргона при температуре ~80oС в течение 6-8 часов с выходами 65-80% по схеме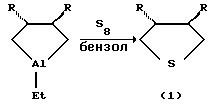
где R=alkyl.
Недостатки известного способа:
1. Повышенная пожароопасность процесса, т.к. реакция осуществляется в кипящем бензоле.
2. Проведение реакции с использованием токсичного бензола, который обладает мутагенными свойствами.
3. Повышенный расход одного из исходных реагентов (S8), который используется в трехкратном избытке по отношению к исходному 1-этил-транс-3,4-диалкилалюмациклопентану.
Предлагается новый способ получения транс-3,4-диалкилтетрагидротиофенов.
Сущность способа заключается во взаимодействии 1-этил-транс-3,4-диалкилалюмациклопентанов (АЦП) с тионилхлоридом (SOCl2), взятых в мольном соотношении АЦП:SOCl2=10:(10÷14), предпочтительно 10:12, в растворе гексана при температуре -40oС в течение 6-8 часов, предпочтительно 7 часов. Выход транс-3,4-диалкилтетрагидротиофенов составляет 73-82%. Реакция проходит по схеме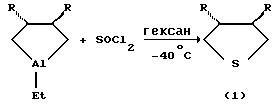
где R=н-C4H9, н-С5Н11, н-C7H15.
Проведение процесса при более высокой температуре (например, 0oС) снижает селективность реакции. Проведение процесса при более низкой температуре (например, -50oС) снижает скорость реакции. Изменение соотношения исходных реагентов в сторону увеличения содержания SOCl2 по отношению к АЦП не приводит к существенному повышению выхода целевых продуктов (1).
Существенные отличия предлагаемого способа.
Если в известном способе для сульфирования используется трехкратный избыток элементной серы (S8), реакция идет при повышенной температуре (~80oС) в кипящем бензоле. В предлагаемом способе в отличие от известного для сульфирования используется тионилхлорид (SOCl2), реакция идет при пониженной температуре (-40oС) в гексане.
Способ поясняется следующими примерами.
ПРИМЕР 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 10 ммолей 1-этил-транс-3,4-ди(н-бутил)алюмациклопентана в 10 мл гексана, при температуре -40oС добавляют 12 ммолей тионилхлорида (SOCl2) и перемешивают 7 часов при этой температуре. По окончании реакции реакционную массу обрабатывают 5%-ной НСl, выделяют транс-3,4-ди(н-бутил)тетрагидротиофен с выходом 78%.
Спектральные характеристики транс-3,4-ди(н-бутил)-тетрагидротиофена (1):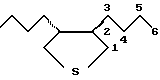
Спектр ЯМР 1Н (δ, м.д.): 0,92 (т, 6Н, СН3), 1,12-1,91 (м, 14Н, СН, СН2), 2,33-2,64, 2,86-3,06 (м, 4Н, СН2S).
Спектр ЯМР 13С (δ, м. д.): 36,51 т (С1), 48,77 д (С2), 32,73 т (С3), 30,21 т (С4), 22,94 т (С5), 14,06 к (С5). М+ 200.
Другие примеры, подтверждающие способ, приведены в таблице.
Добавление тионилхлорида и последующую реакцию сульфирования осуществляли при температуре -40oС в гексане.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 3-ТИА-ЭКЗО-ТРИЦИКЛО[5.2.1.0.]ДЕКАНА | 2002 |
|
RU2213742C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКИЛ-1,2-ДИЭТИЛЦИКЛОПРОПАНОВ | 2000 |
|
RU2183614C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛК-4Z-ЕНОВ | 2001 |
|
RU2203876C2 |
| СПОСОБ ПОЛУЧЕНИЯ 6-ТИАСПИРО[3,4]ОКТАНА | 2007 |
|
RU2368606C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 1,2-БИС(ДИАЛКИЛАЛЮМА)-1-АРИЛЭТАНОВ | 2000 |
|
RU2180267C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2-АРИЛ-3-МЕТИЛЕНАЛЮМАЦИКЛОПРОПАНОВ | 2000 |
|
RU2186067C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ E3,E8-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]ДЕКАНА И E3,E9-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]-ДЕКАНА | 2002 |
|
RU2221764C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2-АЗА-3-МЕТИЛ-4-АЛКИЛИДЕНАЛЮМАЦИКЛОГЕПТ-2-ЕНОВ | 2001 |
|
RU2203899C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ЭТИЛ-2-АЛКИЛИДЕНАЛЮМАЦИКЛОПЕНТАНОВ И 1-ЭТИЛ-2-МЕТИЛЕН-3-АЛКИЛАЛЮМАЦИКЛОПЕНТАНОВ | 2000 |
|
RU2183637C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2-БИС/(ДИАЛКОКСИ)АЛЮМА/-ЦИС-1,2-ДИФЕНИЛ(АЛКИЛ)ЭТИЛЕНОВ | 1996 |
|
RU2156766C2 |
Изобретение относится к способу получения транс-3,4-диалкилтетрагидротиофенов. Транс-3,4-диалкилтетрагидротиофены получают взаимодействием 1-этил-транс-3,4-диалкилалюмациклопентаны (АЦП) с тионилхлоридом (SOCl2) в мольном соотношении АЦП: SOCl2=10:(10÷14) в растворе гексана при температуре -40oС в течение 6-8 ч. Изобретение позволяет проводить реакцию при пониженной температуре, с использованием тионилхлорида вместо токсичного бензола. 1 табл.
Способ получения транс-3,4-диалкилтетрагидротиофенов общей формулы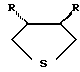
где R - н-С4Н9, н-С5Н11, н-С7-Н15,
отличающийся тем, что 1-этил-транс-3,4-диалкилалюмациклопентаны (АЦП) подвергают взаимодействию с тионилхлоридом (SOCl2) в мольном соотношении АЦП: SOCl2= 10: (10÷14) в растворе гексана при температуре -40oС в течение 6-8 ч.
| Джемилев У.М | |||
| и др | |||
| Синтез и превращение металлоциклов | |||
| Известия АН | |||
| Серия хим., 1994, № 2, с.276-278 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-3,4-ДИ(ЗАМЕЩЕННЫХ)-ТЕТРАГИДРОТИОФЕНОВ | 1993 |
|
RU2109740C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЮМОГЕНА КРАСНОГО 630-(639)- 5- | 0 |
|
SU175969A1 |
Авторы
Даты
2003-09-27—Публикация
2002-03-25—Подача