Изобретение относится к новым биологически активным веществам из класса алканкарбоновых кислот и может быть использовано в медицине и биологии в качестве основы для создания лекарственных препаратов.
В последнее время уделяют много внимания разработке и изучению специфических средств, стимулирующих или подавляющих иммунные реакции организма. Существующие в настоящее время препараты не обладают достаточной избирательностью действия и их применение может сопровождаться выраженными побочными явлениями. Они могут оказывать угнетающее влияние на кроветворение и вызывать лейкопению, тромбоцитопению, анемию, панцитопению, возможны активации вторичной инфекции, развитие септицемии. Это относится практически ко всем препаратам, проявляющим противоопухолевую активность (цитостатикам).
Есть препараты, которые применяются, например, как иммуностимуляторы, но при определенных условиях могут проявлять себя и как иммунодепрессанты.
Гетероциклический иммуномодулятор левамизол (М.Д.Машковский, Лекарственные средства, М., Медицина, 1986, т.2, стр. 169-170) может выполнять функции иммуномодулятора, способного усилить слабую реакцию клеточного иммунитета, ослабить сильную и не действовать на нормальную. Левамизол проявляет дозозависимое воздействие на иммунитет и применять его, например, в качестве иммуностимулятора нужно с осторожностью, так как при превышении доз возможно не иммуностимулирующее, а иммунодепрессивное действие, причем в некоторых случаях от малых доз левамизола. Применение левамизола может вызвать различные побочные явления. Клинические испытания показали, что у 30-40% больных, получающих левамизол, зарегистрированы разнообразные осложнения: головная боль, нарушение сна, аллергические реакции, агранулоцитоз, лейкопения.
Современные знания о патогенезе многих заболеваний, связанных с нарушением межклональных взаимоотношений за счет расстройства Th1/Th2 регуляторных влияний и баланса соответствующих цитокинов выдвигают требования к поиску новых иммуноактивных препаратов. В связи с этим представляют интерес препараты, проявляющие при первичном скрининге in vivo на интактных животных разнонаправленное влияние на интегральные показатели - антителообразование и ГЗТ, оказывающие влияние либо только на гуморальный, либо только на клеточный иммунитет и не оказывающие токсического воздействия на организм.
С целью расширения арсенала синтетических средств, обладающих иммуномодулирующими свойствами, предлагается использовать диметилэтаноламмониевую соль 4-хлорфенилтиоуксусной кислоты в качестве иммуномодулятора.
Диметилэтаноламмониевая соль 4-хлорфенилтиоуксусной кислоты обладает антиоксидантными свойствами ("Клиническая эффективность и безопасность цефалоспориновых антибиотиков производства ООО "АБОЛмед" сб. трудов НИИКИ, АГМУ и МКБ, Новосибирск, 2002, стр. 179).
Сущность изобретения заключается в том, что были исследованы иммуномодулирующие свойства диметилэтаноламмониевой соли 4-хлорфенилтиоуксусной кислоты по способности данного соединения влиять на количество ядросодержащих клеток крови у мышей (миелоактивные свойства), на количество антителообразующих клеток (IgM AOK) in vivo (первичный иммунный ответ), на спонтанную и митоген-стимулированную пролиферацию спленоцитов у мышей in vitro (антипролиферативные свойства), а также на пролиферацию клеток опухолевой линии (цитостатические свойства).
В работе использовали здоровых половозрелых животных мышей - гибридов (CBA•C57BL/6)F1 (CBF1) обоего пола, 8-10 недельного возраста, массой тела 18-20 г. Разброс в группах по исходной массе тела не превышал ±10%. Контрольные и опытные животные одного возраста и получены одновременно из одного питомника ("Рассвет", г. Томск). До и в период эксперимента контрольные и опытные животные содержались в виварии в одинаковых условиях: стандартных пластиковых клетках с мелкой древесной стружкой (не более 10 особей) на стандартном рационе. Все исследования проводились в одно и то же время суток (утром).
Данные обрабатывались по непараметрическому критерию U Вилкоксона-Манна-Уитни.
Пример 1. Определение миелоактивных свойств.
Опытной группе животных соединение вводили в дозе 1/10 LD50 внутрибрюшинно в объеме 0,5 мл ежедневно в течение 7 дней, через 24 часа после последнего введения определяли количество ядросодержащих клеток в периферической крови. Контрольным животным в таком же объеме и режиме вводили растворитель (воду). Критерием оценки миелоактивных свойств является изменение в лейкоцитарной формуле ±20%. Результаты выражали в количестве лейкоцитов в одном мл крови и в процентах к соответствующему контролю.
Как видно из данных табл.1, соединение достоверно обладает миелостимулирующими свойствами, т.е. существенно более, чем на 20% вызывает увеличение количества лейкоцитов (на 76%).
Пример 2. Определение количества IgM антителообразующих клеток in vivo.
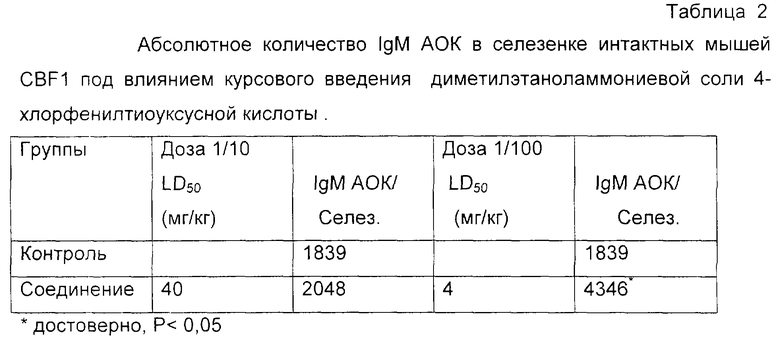
Соединение в дозе 1/10 LD50 в объеме 0,5 мл вводили внутрибрюшинно один раз в сутки ежедневно в течение 7 дней и в дозе 1/100 LD50 в объеме 0,5 мл вводили внутрибрюшинно один раз в сутки ежедневно в течение 5 дней.
Контрольным животным в таком же объеме и режиме вводили растворитель соединения (воду). В день последнего введения соединения животных иммунизировали внутривенно эритроцитами барана (ЭБ) в дозе 0,5•107/мышь. Количество IgM АОК в селезенке мышей оценивали на 4 сутки после иммунизации по количеству зон локального гемолиза в полужидкой среде модифицированным методом Cunningham (1968). Результаты выражали в абсолютном количестве IgM АОК в селезенке.
Как видно из данных табл. 2, диметилэтаноламмониевая соль 4-хлорфенилтиоуксусной кислоты достоверно стимулирует первичный гуморальный ответ.
Пример 3. Спонтанная, Con А- и PWM-индуцированная пролиферация клеток селезенки.
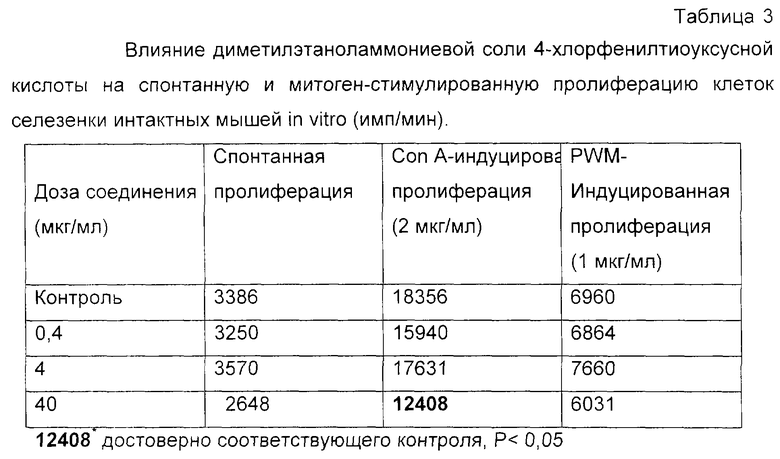
Клетки селезенки мышей культивировали в круглодонных планшетах для иммунологических реакций ("Linbro") при +37oС в атмосфере 5% СO2 и 95% воздуха. Абсолютное количество клеток, вносимых в лунку, составляло 200 000. Клетки стимулировали митогенами - конканавалином А (Con A, Sigma) или митогеном лаконоса (PWM, Sigma). Концентрации митогенов подбирались предварительным титрованием и использовались в оптимальной дозе, что составило для Con A 2 мкг/мл, а для PWM - 1 мкг/мл. Соединение в трех дозах вносили в лунки одновременно с митогенами. Пролиферативную активность клеток оценивали по включению Н3-тимидина в ДНК делящихся клеток. Метку вносили за 16 час до конца культивирования по 1 мкКи в каждую лунку планшета. Для этого основной раствор Н3-тимидина сначала растворяли в среде RPMI-1640 до концентрации 100 мкКи/мл, а затем по 10 мкл раствора добавляли в каждую лунку планшета. По окончании инкубации клетки собирали на стеклянно-волокнистые фильтры ("Flow Lab") с помощью аппарата Harvester ("Titertek"). Фильтры высушивали и помещали во флаконы для сцинтилляционного счета, и радиоактивность подсчитывали в толуольном сцинтилляторе (4 г дифенилоксазола, 0,1 г дифенил-оксазолилбензола на 1 л толуола) в жидкостном сцинтилляционном счетчике "Delta" (США). Результаты выражали в имп. /мин включенного тимидина на 2•105 клеток, представлены средние данные по триплету.
Как видно из данных табл.3, соединение способно проявлять при определенной дозе ингибирующие свойства на митоген-стимулированную пролиферацию интактных клеток селезенки мышей.
Пример 4. Оценка противоопухолевой активности проводилась in vitro на клетках мастоцитомы Р 815. Клетки засевали в концентрации 10•103/лунку, инкубировали с соединениями в течение 24 часов, за 6 часов до конца инкубации вносили 1 мкКи Н3-тимидина. По окончании инкубации клетки собирали на стеклянно-волокнистые фильтры ("Flow Lab") с помощью аппарата Harvester ("Titertek). Результаты выражали в имп./мин. Включенного тимидина на 10•103 клеток, представлены средние данные по триплету.
Как видно из данных табл.4, диметилэтаноламмониевая соль 4-хлорфенилтиоуксусной кислоты проявляет достоверный антипролиферативный эффект в дозе 200 м кг/мл.
Оценивая в целом результаты можно отметить, что по влиянию на миелоактивность и первичный гуморальный ответ диметилэтаноламмониевая соль 4-хлорфенилтиоуксусной кислоты может быть отнесена к иммуностимуляторам, а по влиянию на митогенстимулированную пролиферацию клеток селезенки интактных мышей и пролиферацию клеток опухолевой линии in vitro к иммунодепрессантам.
Приведенные примеры иллюстрируют наличие у диметиэтаноламмониевой соли 4-хлорфенилтиоуксусной кислоты иммуномодулирующих свойств, что позволит в будущем создавать на ее основе лекарственные средства для лечения различных иммунокомпрометированных состояний.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2245142C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2253444C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2224513C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2252757C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2240794C1 |
| ИММУНОДЕПРЕССАНТ | 2003 |
|
RU2253448C1 |
| ИММУНОДЕПРЕССАНТ | 2002 |
|
RU2228178C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2253447C1 |
| ИММУНОДЕПРЕССАНТ | 2016 |
|
RU2637643C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2253445C1 |


Предложено: применение диметилэтаноламмониевой соли 4-хлорфенилтиоуксусной кислоты, ранее известной как антигемолитическое и антиагрегационное средство, в качестве иммуномодулятора. Изобретение расширяет арсенал средств заявленного назначения. 4 табл.
Применение диметилэтаноламмониевой соли 4-хлорфенилтиоуксусной кислоты в качестве иммуномодулятора.
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА (ТРЕКРЕЗАНА) С ИММУНОТРОПНЫМ ДЕЙСТВИЕМ | 1996 |
|
RU2098088C1 |
| US 5456912, 10.10.1995 | |||
| Восстановитель для доменной плавки | 1971 |
|
SU506628A1 |
| Левковская Г.Г | |||
| и др | |||
| Двухядерные производные фенилтиоуксусной кислоты, их трис-[2-оксиэтил] аммониевые соли, влияние на функциональную активность тромбоцитов | |||
| Химико-фармацевтический журнал, 1984, т.18, №4, с.431-435. | |||
Авторы
Даты
2004-02-27—Публикация
2003-03-27—Подача