Область техники изобретения
Настоящее изобретение относится к агентам, представляющим собой трициклические соединения, которые обладают способностью ингибировать дифференцировку Th0-клеток в Тh2-клетки.
Предпосылки создания изобретения
СD4+-хелперные Т-клетки (называемые ниже в настоящем описании Th-клетками), участвующие в возникновении аллергических заболеваний или аутоиммунных заболеваний, в зависимости от продуцируемых ими цитокинов разделяют на два типа, а именно, на тип I хелперных Т-клеток (называемых ниже в настоящем описании как Тh1-клетки) и тип II хелперных Т-клеток (называемых ниже в настоящем описании как Тh2-клетки). Тh1-клетки продуцируют IL-2, IFN-γ, TNF-β и т.п., индуцируя тем самым клеточный иммунитет. С другой стороны, Тh2-клетки продуцируют IL-4, IL-5, IL-6, IL-10, IL-13 и т.п., индуцируя тем самым гуморальный иммунитет.
Th0-клетки, являющиеся общими предшественниками Th1-клеток и Th2-клеток, дифференцируются либо в Тh1-клетки, либо в Тh2-клетки в ответ на стимуляцию антигеном и затем созревают. Например, известно, что такая бактерия, как Bacillus tuberculosis, и такой вирус, как вирус гриппа, обладают способностью индуцировать дифференцировку с образованием Тh1-клеток, в то время как аллергены, такие как клещи и пыльца, индуцируют дифференцировку с образованием Тh2-клеток
В настоящее время опубликованы данные о том, что присутствие в организме Тh1-клеток и Тh2-клеток, имеющих различные функции, имеет существенное значение для предупреждения инфекции и возникновения аллергических заболеваний или аутоиммунных заболеваний, и имеется предположение о том, что ингибирование чрезмерной дифференцировки с образованием Тh2-клеток оказывает терапевтическое действие, направленное против аллергических заболеваний или аутоиммунных заболеваний, индуцируемых Тh2-клетками.
Соединения, имеющие каркас, аналогичный каркасу соединений по настоящему изобретению, и обладающие иммунносупрессорным действием или антиаллергическим действием, описаны, например, в WO 94/27980, WO 95/13067, WO 96/15123, WO 95/15318, WO 96/40659, WO 96/40143, WO 96/38412, WO 96/10012, WO 97/24356, WO 97/27181, WO 97/24324, WO 97/39999, WO 97/44333, WO 97/46524, WO 98/04508, WO 98/24766, WO 98/24782, WO 98/56785, FR 2301250, US 5593991, JP 47-7368 В, JP 51-91259 A, JP 8-3163 A, JP 9-124571 А, JP 9-71564 A, JP 9-124571 A, JP 11-79993 A, Bioorganic & Medicinal Chemistry Letters, том 5, №18, стр.2143-2146 (1995), J. Med. Chem., 1974, том 17 и №11, 1177-1181.
Описание изобретения
Задачей настоящего изобретения является создание высокоэффективных ингибиторов Тh2-дифференцировки.
Объектами настоящего изобретения являются:
[1] Фармацевтическая композиция, предназначенная для применения в качестве ингибитора Тh2-дифференцировки, включающая соединение, представленное формулой (I):
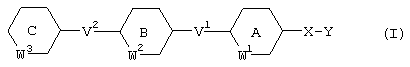
где кольцо А, кольцо В и кольцо С каждое независимо друг от друга представляет собой необязательно замещенное ароматическое карбоциклическое кольцо или необязательно замещенное 5- или 6-членное гетероциклическое кольцо, которое может быть сконденсировано с бензольным кольцом, и когда кольцо А, кольцо В и/или кольцо С представляет собой необязательно замещенное 5-членное гетероциклическое кольцо, W1, W2 и/или W3 обозначают связь,
Х обозначает простую связь, -О-, -СН2-, -NR1- (где R1 обозначает водород, необязательно замещенный (низш.)алкил, (низш.)алкенил или (низш.)алкилкарбонил) или -S(O)p-, где р обозначает целое число от 0 до 2;
Y обозначает водород, необязательно замещенный (низш.)алкил, необязательно замещенную (низш.)алкоксигруппу, необязательно замещенный (низш.)алкенил, необязательно замещенный (низш.)алкинил, необязательно замещенный ацил, необязательно замещенный циклоалкил, необязательно замещенный циклоалкенил, необязательно замещенный (низш.)алкоксикарбонил, необязательно замещенный сульфамоил, необязательно замещенную аминогруппу, необязательно замещенный арил или необязательно замещенный 5- или 6-членный гетероциклил;
R1 и Y вместе могут образовывать -(СН2)m-, -(СН2)2-Т-(СН2)2-, где Т обозначает О, S или NR’, -CR’=CH-CH=CR’-, -CH=N-CH=CH-, -N=CH-N=CH-, -C(=O)-O- (СН2)r-, -C(=O)-NR’-(CH2)r- или -C(=O)-NR’-N=CH-, где m равно 4 или 5, r равно 2 или 3 и R’ обозначает водород, (низш.)алкил или (низш.)алкенил;
Y может обозначает галоген, когда Х обозначает -СН2- или –NR’- и Y может представлять собой необязательно замещенный (низш.)алкилсульфонил
или необязательно замещенный арилсульфонил, когда Х обозначает -О- или –NR1-;
один из V1 и V2 обозначает простую связь, а другой обозначает -О-, -NH-, -ОСН2-, -СН2О-, -СН=СН-, -С≡С-, -CH(OR2)-, где R2 обозначает водород или (низш.)алкил, -СО-, -NHCHR3- или –CHR3NH-, где R3 обозначает водород или гидроксигруппу,
или его пролекарство, фармацевтически приемлемую соль или сольват.
[2] Фармацевтическая композиция, описанная в [1], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где Х обозначает -O- или –NR1-, где R1 обозначает водород, (низш.)алкил или (низш.)алкенил.
[3] Фармацевтическая композиция, описанная в [I], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где Y обозначает необязательно замещенный (низш.)алкил или необязательно замещенный (низш.)алкенил.
[4] Фармацевтическая композиция, описанная в [I], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где оба V1 и V2 обозначают простые связи.
[5] Фармацевтическая композиция, предназначенная для применения в качестве ингибитора Тh2-дифференцировки, включающая соединение, представленное формулой (Ia):
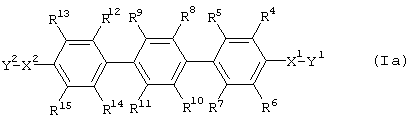
где R4, R5, R6, R7, R8, R9, R10, R11, R12, R13, R14 и R15 каждый независимо друг от друга обозначает водород, галоген, гидроксигруппу, необязательно замещенный (низш.)алкил, необязательно замещенную (низш.)алкокси-, карбоксигруппу или (низш.)алкоксикарбонил;
X1 и X2 каждый независимо друг от друга обозначает -О-, -СН2- или -NH-;
Y1 и Y2 каждый независимо друг от друга обозначает необязательно замещенный (низш.)алкил, необязательно замещенный арилалкил или необязательно замещенный (низш.)алкенил,
или его пролекарство, фармацевтически приемлемую соль или сольват.
[6] Фармацевтическая композиция, предназначенная для применения в качестве ингибитора Тh2-дифференцировки, включающая соединение, представленное формулой (Ib):
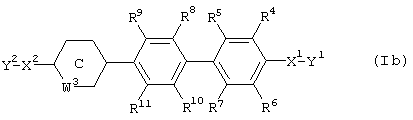
где кольцо С обозначает необязательно замещенное 5- или 6-членное гетероциклическое кольцо, включающее 1 или 2 гетероатома, и когда кольцо С представляет собой 5-членное гетероциклическое кольцо, W3 обозначает связь и другие символы имеют значения, указанные в [5],
или его пролекарство, фармацевтически приемлемую соль или сольват.
[7] Фармацевтическая композиция, предназначенная для применения в качестве ингибитора Тh2-дифференцировки, включающая соединение, представленное формулой (Iс):
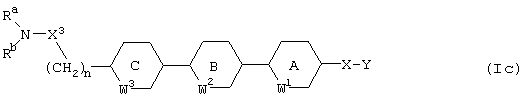
где кольцо А, кольцо В и кольцо С каждое независимо друг от друга обозначает необязательно замещенное бензольное кольцо или необязательно замещенное 5- или 6-членное гетероциклическое кольцо, содержащее 1 или 2 гетероатома, и
когда кольцо А, кольцо В и/или кольцо С представляет собой необязательно замещенное 5-членное гетероциклическое кольцо, W1, W2 и/или W3 обозначает связь;
X1 и Y1 имеют значения, указанные в [5];
X3 обозначает -О- или -NH-;
Ra и Rb каждый независимо друг от друга обозначает водород, необязательно замещенный (низш.)алкил, необязательно замещенный (низш.)алкенил, необязательно замещенный арил, необязательно замещенный циклоалкил, необязательно замещенный ацил, необязательно замещенный (низш.)алкоксикарбонил или необязательно замещенный (низш.)алкилсульфонил, или они вместе образуют
RcRdC= или -(CReRf)s-;
Rc и Rd каждый независимо друг от друга обозначает водород, необязательно замещенный (низш.)алкил, необязательно замещенный (низш.)алкенил, необязательно замещенный (низш.)алкинил, необязательно замещенную (низш.)алкокси-, необязательно замещенную (низш.)алкилтио-, необязательно замещенную (низш.)алкенилокси-, необязательно замещенную (низш.)алкинилоксигруппу, необязательно замещенный циклоалкил, необязательно замещенный арил или необязательно замещенный 5- или 6-членный гетероциклил или они вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенный циклоалкилиден;
Re каждый независимо друг от друга обозначает водород, (низш.)алкил, (низш.)алкокси- или аминогруппу, и Rf каждый независимо друг от друга обозначает водород, (низш.)алкил, (низш.)алкокси- или аминогруппу;
n обозначает целое число от 0 до 2 и s обозначает целое число от 2 до 6, или его пролекарство, фармацевтически приемлемую соль или сольват.
[8] Фармацевтическая композиция, описанная в [1], [2], [3], [4] или [7], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где кольцо А представляет собой необязательно замещенное бензольное кольцо.
[9] Фармацевтическая композиция, описанная в [1], [2], [3], [4] или [7], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где кольцо В представляет собой необязательно замещенное бензольное кольцо.
[10] Фармацевтическая композиция, описанная в [1], [2], [3], [4], [6] или [7], предназначенная для применения в качестве ингибитора Th2-дифференцировки, где кольцо С представляет собой необязательно замещенное бензольное кольцо, необязательно замещенное пиридиновое кольцо, необязательно замещенное пиримидиновое кольцо, необязательно замещенное пиридазиновое кольцо или необязательно замещенное пиразиновое кольцо.
[11] Фармацевтическая композиция, описанная в [5] или [6], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где один из R4 и R5 обозначает водород, гидроксигруппу или (низш.)алкил, а другой обозначает водород или галоген, и оба R6 и R7 обозначают атомы водорода.
[11-2] Фармацевтическая композиция, описанная в [5] или [6], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где один из R4 и R5 обозначает водород, а другой обозначает галоген, и оба R6 и R7 обозначают атомы водорода.
[12] Фармацевтическая композиция, описанная в [5] или [6], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где R8 и R11 каждый независимо друг от друга обозначает водород, гидроксигруппу, (низш.)алкил или (низш.)алкоксикарбонил, и R9 и R10 каждый независимо друг от друга обозначает гидроксигруппу, (низш.)алкил, (низш.)алкоксигруппу или (низш.)алкоксикарбонил.
[13] Фармацевтическая композиция, описанная в [5], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где R12, R13, R14 и R15 каждый независимо друг от друга обозначает водород или галоген.
[14] Фармацевтическая композиция, описанная в [5] или [6], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где один из X1 и X2 обозначает -О-, а другой обозначает -NH-.
[15] Фармацевтическая композиция, описанная в [5] или [6], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где Y1 и Y2 каждый независимо друг от друга обозначает замещенный галогеном (низш.)алкил или необязательно замещенный галогеном (низш.)алкенил.
[16] Фармацевтическая композиция, описанная в [5] или [6], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, где один из –X1-Y1 и –X2Y2 обозначает прениламиногруппу, а другой обозначает пренилоксигруппу.
[17] Фармацевтическая композиция, описанная в [6] или [7], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, которая представляет собой агент, обладающий терапевтическим и/или профилактическим действием в отношении аутоиммунного заболевания.
[18] Фармацевтическая композиция, описанная в любом из пунктов [1]-[16], предназначенная для применения в качестве ингибитора Тh2-дифференцировки, которая представляет собой агент, обладающий терапевтическим и/или профилактическим действием в отношении неспецифического язвенного колита, тяжелой псевдопаралитической миастении или люпус-нефрита.
[19] Способ лечения и/или предупреждения заболевания, вызываемого Th2-клетками или цитокинами, продуцируемыми Тh2-клетками, предусматривающий введение соединения, представленного формулой (I) согласно [1], или его пролекарства, фармацевтически приемлемой соли или сольвата.
[20] Способ ингибирования дифференцировки Th0-клеток в Тh2-клетки, предусматривающий введение соединения, представленного формулой (I) согласно [1], или его пролекарства, фармацевтически приемлемой соли или сольвата.
[21] Применение соединения, представленного формулой (I) согласно [1], или его пролекарства, фармацевтически приемлемой соли или сольвата для приготовления лекарственного средства, предназначенного для лечения и/или предупреждения заболевания, вызываемого Тh2-клетками или цитокинами, продуцируемыми Тh2-клетками.
[22] Применение соединения, представленного формулой (I) согласно [1], или его пролекарства, фармацевтически приемлемой соли или сольвата для приготовления лекарственного средства, предназначенного для ингибирования дифференцировки Th0-клеток в Тh2-клетки.
Наиболее предпочтительные варианты осуществления изобретения
В контексте описания понятие “галоген” обозначает фтор, хлор, бром и йод. Наиболее предпочтительными являются фтор и хлор.
Понятие “(низш.)алкил” обозначает алкил с прямой или разветвленной цепью, имеющий 1-10, предпочтительно 1-8, более предпочтительно 1-6 и наиболее предпочтительно 1-3 атома углерода, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, гексил, изогексил, н-гептил, изогептил, н-окстил, изооктил, н-нонил и н-децил.
Заместитель для “необязательно замещенного (низш.)алкила” может представлять собой, например, галоген; гидрокси-; (низш.)алкоксигруппу, которая может быть замещена (низш.)алкоксигруппой; ацил; ацилокси-; карбоксигруппу; (низш.)алкоксикарбонил; меркапто-; (низш.)алкилтио-; аминогруппу, которая может быть замещена гидроксигруппой, (низш.)алкилом или необязательно замещенным ацилом; иминогруппу, которая может быть замещена гидрокси-, (низш.)алкокси-, карбокси(низш.)алкокси-, арил(низш.)алкоксигруппой или 5- или 6-членным гетероциклилом; гидразоногруппу, которая может быть замещена карбамоилом или (низш.) алкоксикарбонилом; гидразиногруппу, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, необязательно замещенным (низш.)алкилиденом или циклоалкилиденом; аминооксигруппу, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, необязательно замещенным (низш.)алкилиденом или циклоалкилиденом; карбамоил, который может быть замещен (низш.)алкилом или аминогруппой; тиокарбамоил, который может быть замещен (низш.)алкилом; циклоалкил, который может быть замещен (низш.)алкилом или (низш.)алкоксигруппой; циклоалкенил, который может быть замещен (низш.)алкилом; цианогруппу; фенил, который может быть замещен одним или несколькими заместителями, выбранными из ряда, включающего гидроксигруппу, (низш.)алкил, карбоксигруппу, (низш.)алкоксикарбонил или (низш.)алкоксигруппу; 5- или 6-членный гетероциклил, который может быть замещен (низш.)алкилом и который может быть сконденсирован с бензольным кольцом. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений. Особенно предпочтительными заместителями являются галоген, гидрокси-; ацилоксигруппа; фенил, который может быть замещен (низш.)алкилом или (низш.)алкоксигруппой; или пиридил.
Алкильный фрагмент в понятиях "(низш.)алкоксигруппа", "(низш.)алкоксикарбонил", "(низш.)алкилсульфонил", "(низш.)алкилсульфонилокси-", "(низш.)алкилтио-", "(низш.)алкиламино-" и "(низш.)алкиленидиоксигруппа" имеет такое же значение, что и в описанном выше понятии "(низш.)алкил".
Заместитель для "необязательно замещенной (низш.) алкоксигруппы", "необязательно замещенного (низш.)алкоксикарбонила", "необязательно замещенного (низш.)алкилсульфонила" и "необязательно замещенной (низш.)алкилтиогруппы" может представлять собой, например, галоген; гидрокси-, (низш.)алкоксигруппу, которая может быть замещена ацилоксигруппой; ацил; ацилоксигруппу, которая может быть замещена гидрокси- или карбоксигруппой; карбоксигруппу; (низш.)алкоксикарбонил; (низш.)алкилтиогруппу; аминогруппу, которая может быть замещена (низш.)алкилом; фенил, который может быть замещен (низш.)алкилом или (низш.)алкоксигруппой; гетероциклил; гетероциклилкарбонилоксогруппу. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие "(низш.)алкилиден" обозначает двухвалентную углеводородную группу, имеющую 1-10, предпочтительно 1-6, более предпочтительно 1-3 атома углерода, типичными примерами которой являются метилиден, этилиден, пропилиден, изопропилиден, бутилиден, пентилиден, гексилиден, гептилиден, октилиден, нонилиден и децилиден.
Заместитель для "необязательно замещенного (низш.)алкилидена" может представлять собой, например, необязательно замещенный (низш.)алкенил, необязательно замещенную (низш.)алкокси-, необязательно замещенную (низш.)алкилтиогруппу, необязательно замещенный циклоалкил, необязательно замещенный арил или необязательно замещенный 5- или 6-членный гетероциклил. Предпочтительными заместителями являются (низш.)алкенил, (низш.)алкоксигруппа, циклоалкил, фенил или 5- или 6-членный гетероциклил. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие "(низш.)алкенил" обозначает алкенил с прямой или разветвленной цепью, имеющий одну или несколько двойных связей в любых положениях и 2-10, предпочтительно 2-8, более предпочтительно 3-6 атомов углерода. Типичными примерами могут служить винил, пропенил (2-пропенил, изопропенил и т.п.), бутенил, изобутенил, пренил, бутадиенил, пентенил, изопентенил, пентадиенил, гексенил, изогексенил, гексадиенил, гептенил, октенил, ноненил и деценил.
Заместители для "необязательно замещенного (низш.)алкенила" представляют собой такие же заместители, что и для описанной выше "необязательно замещенной (низш.)алкоксигруппы". (Низш.)алкенил может быть замещен этими заместителями в одном или нескольких из любых возможных положений. Предпочтительными группами являются группа, замещенная галогеном, или незамещенная группа.
(Низш.)алкенильный фрагмент в понятиях "(низш.)алкенилоксигруппа", "(низш.)алкенилоксикарбонил" и "(низш.)алкениламиногруппа" имеет такое же значение, что и для описанных выше понятий "(низш.)алкенил".
Заместитель для "необязательно замещенной (низш.)алкенилоксигруппы", "необязательно замещенного (низш.)алкенилоксикарбонила" и "необязательно замещенной (низш.)алкенилтиогруппы" имеет те же значения, что и заместитель для описанной выше "необязательно замещенной (низш.)алкоксигруппы". Эти заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие "(низш.)алкинил" обозначает алкинил с прямой или разветвленной цепью, имеющий 2-10, предпочтительно 2-8 и более предпочтительно 3-6 атомов углерода, типичными примерами которого являются этинил, пропинил (2-пропинил и т.п.), бутинил (2-бутинил и т.п.), пентенил, гексинил, гептинил, октинил, нонинил и децинил. Любая из этих групп имеет одну или несколько тройных связей в любых возможных положениях и необязательно содержит одну или несколько двойных связей.
Заместитель для "необязательно замещенного (низш.)алкинила" имеет такие же значения, что и заместитель для описанной выше "необязательно замещенной (низш.)алкоксигруппы". Эти заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие "ацил" обозначает алифатический ацил с прямой или разветвленной цепью, имеющий 1-20, предпочтительно 1-15, более предпочтительно 1-8, еще более предпочтительно 1-6 и наиболее предпочтительно 1-4 атома углерода, алициклический ацил, имеющий 4-9, предпочтительно 4-7 атомов углерода, и ароил. Типичными примерами являются формил, ацетил, пропионил, бутирил, изобутирил, валерил, пивалоил, гексаноил, акрилоил, пропиолоил, метакрилоил, кротоноил, циклопропилкарбонил, циклогексилкарбонил, циклооктилкарбонил и бензоил.
Понятие “ароил” обозначает ароматический карбоциклический карбонил и ароматический гетероциклилкарбонил.
Заместитель для "необязательно замещенного ацила" имеет такие же значения, что и заместитель для "необязательно замещенной (низш.)алкоксигруппы", при этом алициклический ацил и ароил могут, кроме того, содержать в качестве своих заместителей (низш.)алкил. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений. Особенно предпочтительным заместителем является галоген.
Ацильный фрагмент в “ацилоксигруппе” имеет такое же значение, что и для описанного выше “ацила”. Заместитель для “необязательно замещенной ацилоксигруппы” также имеет такое же значение, что и для описанного выше “необязательно замещенного ацила”, при этом указанные заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие “(низш.)алкилкарбонил” обозначает алифатический ацил, имеющий 2-4 атома углерода, такой как ацетил, пропионил, бутирил и изобутирил. Особенно предпочтительным является ацетил.
Понятие “циклоалкил” обозначает карбоциклическую группу, имеющую 3-6 атомов углерода, такую как циклопропил, циклобутил, циклопентил и циклогексил.
Заместителями для “необязательно замещенного циклоалкила” могут являться, например, (низш.)алкил, галоген, гидрокси-, карбоксигруппа, (низш.)алкоксикарбонил, (низш.)алкокси-, (низш.)алкилендиокси-, иминогруппа, которые могут быть замещены (низш,)алкоксигруппой, арилом или 5- или 6-членным гетероциклилом в одном или нескольких из любых возможных положений.
Понятие “циклоалкенил” обозначает группу, имеющую одну или несколько двойных связей в любом положении описанного выше циклоалкильного кольца, типичными примерами которой являются циклопропенил, циклобутенил, циклопентенил, циклогексенил и циклогексадиенил.
Заместители для “необязательно замещенного циклоалкенила” представляют собой такие же заместители, что и для описанного выше “циклоалкила”. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие “циклоалкилиден” обозначает двухвалентную карбоциклическую группу, имеющую 3-6 атомов углерода, такую как циклопропилиден, циклобутилиден, циклопентилиден и циклогексилиден.
Заместители для “необязательно замещенного циклоалкилидена” представляют собой такие же заместители, что и для описанного выше “циклоалкила”, при этом указанные заместители могут присутствовать в одном или нескольких из любых возможных положений. Предпочтительным является незамещенный циклоалкилиден.
Заместитель для “необязательно замещенной аминогруппы” может представлять собой, например, необязательно замещенный (низш.)алкил (заместителями для которого могут быть (низш.)алкоксигруппа, циклоалкил, необязательно замещенная аминогруппа (заместителем которой может быть ароил, который может быть замещен ацилокси(низш.)алкоксигруппой), необязательно замещенный арил (заместителями которого могут быть (низш.)алкил, (низш.)алкоксигруппа, (низш.)алкоксикарбонил), или гетероциклил); (низш.)алкенил; (низш.)алкинил; циклоалкил; арил, который может быть замещен (низш.)алкилом, карбоксигруппой, ацилом или (низш.)алкоксикарбонилом; сульфамоил, который может быть замещен (низш.)алкилом; необязательно замещенный (низш.)алкоксикарбонил (заместителями для которого могут быть галоген, ацилокси-, гидроксизамещенная ацилокси-, карбоксизамещенная ацилокси- или гетероциклилкарбонилоксигруппа); (низш.)алкилсульфонил и т.п. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений.
Понятие “необязательно замещенный карбамоил” обозначает карбамоил, который может быть замещен одной или несколькими группами, выбранными из ряда, включающего (низш.)алкил, (низш.)алкенил, (низш.)алкинил и т.п.
Понятие “необязательно замещенный сульфамоил” обозначает сульфамоил, который может быть замещен одной или несколькими группами, выбранными из ряда, включающего (низш.)алкил, (низш.)алкенил, (низш.)алкинил и т.п.
Понятие “ароматическое карбоциклическое кольцо” обозначает моноциклическое или полициклическое ароматическое карбоциклическое кольцо, такое как бензольное кольцо, нафталиновое кольцо, антраценовое кольцо и фенантреновое кольцо. Особенно предпочтительным является бензольное кольцо. “Ароматическое карбоциклическое кольцо” может быть также сконденсировано с одним или несколькими другими карбоциклическими кольцами и, таким образом, включает индановое кольцо, инденовое кольцо и дигидронафталиновое кольцо. Понятие “арил” обозначает группу, образованную путем удаления одного атома водорода из моноциклического или полициклического ароматического карбоциклического кольца, такого как фенил, нафтил, антрил и фенантрил. Особенно предпочтительным является фенил. “Арил” может быть сконденсирован с одним или несколькими другими карбоциклическими кольцами и может иметь в карбоциклическом кольце связь, с помощью которой осуществляется конденсация. Примерами являются инданил, инденил и дигидронафтил.
Заместитель для “необязательно замещенного ароматического карбоциклического кольца” и “необязательно замещенного арила” может представлять собой, например, галоген; гидроксигруппу; (низш.)алкил, который может быть замещен галогеном или карбоксигруппой; (низш.)алкоксигруппу, которая может быть замещена галогеном, арилом, гетероарилом или (низш.)алкоксигруппой; (низш.)алкенил; (низш.)алкинил; циклоалкил; (низш.)алкенилокси-; (низш.)алкинилокси-; циклоалкоксигруппу; ацил; ацилокси-; карбоксигруппу; (низш.)алкоксикарбонил; (низш.)алкенилоксикарбонил; (низш.)алкилтио-; (низш.)алкинилтио-; аминогруппу, которая может быть замещена (низш.)алкилом, циклоалкил(низш.)алкилом, арил(низш.)алкилом, гетероарил(низш.)алкилом, (низш.)алкенилом, циклоалкилом, ацилом, который необязательно замещен галогеном, (низш.)алкоксикарбонилом или (низш.)алкилсульфонилом; гидразиногруппу, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, необязательно замещенным (низш.)алкилиденом или циклоалкилиденом; аминооксигруппу, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, необязательно замещенным (низш.)алкилиденом или циклоалкилиденом; гуанидино-; нитрогруппу; (низш.)алкилсульфонил; дигидроксиборил; (низш.)алкилсульфонилоксигруппу, которая может быть замещена галогеном; арилсульфонил; арилсульфонилоксигруппу; арил; или 5- или 6-членную гетероциклическую группу. Эти заместители могут присутствовать в одном или нескольких из любых возможных положений. Примерами предпочтительных заместителей являются галоген; гидроксигруппа; (низш.)алкил, который может быть замещен галогеном; (низш.)алкоксигруппа, которая может быть замещена арилом или (низш.)алкоксигруппой, (низш.)алкенилокси-; ацилокси-; (низш.)алкилтио-; аминогруппа, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, ацилом, который необязательно замещен галогеном или (низш.)алкилсульфонилом; нитрогруппа, (низш.)алкилсульфонил; (низш ) алкилсульфонилоксигруппа, которая может быть замещена галогеном, или арилсульфонилоксигруппа.
Арильный фрагмент для “арилсульфонила” и “арилсульфонилоксигруппы” имеет такое же значение, что и для описанного выше “арила”, при этом особенно предпочтительным является фенил.
Заместитель для “необязательно замещенного арилсульфонила” имеет такие же значения, что и для описанного выше “необязательно замещенного арила”, и он может присутствовать в одном или нескольких из любых возможных положений. Особенно предпочтительной является незамещенная группа.
Понятие “5- или 6-членное гетероциклическое кольцо” обозначает 5- или 6-членное гетероциклическое кольцо, имеющее 1 или несколько гетероатомов, выбранных из О, S и N, и оно обычно может представлять собой ароматическое гетероциклическое кольцо, такое как пиррольное, имидазольное, пиразольное, пиридиновое, пиридазиновое, пиримидиновое, пиразиновое, триазольное, триазиновое, изоксазольное, оксазольное, оксадиазольное, изотиазольное, тиазольное, тиадиазольное, фурановое и тиофеновое кольцо, а также неароматическое гетероциклическое кольцо, такое тетрагидропирановое, дигидропиридиновое, дигидропиридазиновое, дигидропиразиновое, диоксановое, оксатиолановое, тиановое, пирролидиновое, пирролиновое, имидазолидиновое, имидазолиновое, пиразолидиновое, пиразолиновое, пиперидиновое, пиперазиновое и морфолиновое кольцо.
Предпочтительными “5- или 6-членными гетероциклическими кольцами”, представителями которых являются кольцо А, кольцо В или кольцо С, являются пиридиновое кольцо и пиримидиновое кольцо, каждое из которых содержит связь в положениях 2 и 5 соответственно.
Понятие “5- или 6-членное гетероциклическое кольцо, имеющее один или два гетероатома” включает в качестве “5- или 6-членного гетероциклического кольца” ароматическое гетероциклическое кольцо, такое как пиррольное, имидазольное, пиразольное, пиридиновое, пиридазиновое. Пиримидиновое, пиразиновое, изоксазольное, оксазольное, изотиазольное, тиазольное, фурановое и тиофеновое кольцо, а также неароматическое гетероциклическое кольцо, такое как диоксановое, оксатиолановое, тиановое, дигидропиридиновое, пирролидиновое, пирролиновое, имидазолидиновое, имидазолиновое, пиразолидиновое, пиразолиновое, пиперидиновое, пиперазиновое и морфолиновое кольцо. Особенно предпочтительным является ароматическое гетероциклическое кольцо.
“5- или 6-членная гетероциклическая группа”, которую обозначают Y и Y’, предпочтительно представляет собой 4-пиридил, 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 1,2-дигидропиридин-5-ил, 2,3-дигидропиридазин-6-ил, 1,2-дигидропиразин-5-ил и т.п.
“5- или 6-членное гетероциклическое кольцо, которое может быть сконденсировано с бензольным кольцом” может представлять собой, например, индольное, изоиндольное, бензимидазольное, индазольное, циннолиновое, фталазиновое, хиназолиновое, бензизоксазольное, бензоксазольное, бензоксадиазольное, бензотиазольное, бензизотиазольное, бензофурановое, бензотиофеновое, бензотриазольное, изобензофурановое, индолиновое, изоиндолиновое и хроменовое кольцо. Каждое из них может содержать связь в сконденсированном гетероциклическом кольце.
Заместитель в “необязательно замещенном 5- или 6-членном гетероциклическом кольце” и в “необязательно замещенном 5- или 6-членном гетероциклическом кольце, которое может быть сконденсировано с бензольным кольцом” может представлять собой, например, галоген; гидроксигруппу; (низш.)алкил, который может быть замещен гидрокси- или ацилоксигруппой; (низш.)алкоксигруппу, которая может быть замещена галогеном, арилом или 5- или 6-членной гетероциклической группой; (низш.)алкенил; (низш.)алкенилоксигруппу; (низш.)алкинил; (низш.)алкинилокси-; ацилокси-; карбоксигруппу; (низш.)алкоксикарбонил; меркапто-; (низш.)алкилтио-; (низш.)алкенилтио-; аминогруппу, которая может быть моно- или дизамещенной галогеном, необязательно замещенным (низш.)алкилом (заместителем которого является циклоалкил или 5- или 6-членная гетероциклическая группа), ацилом, который необязательно может быть замещен галогеном, (низш.)алкенилом, циклоалкилом или (низш.)алкилсульфонилом; иминогруппу, которая может быть замещена (низш.)алкилсульфонилом; гидразиногруппу, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, необязательно замещенным (низш.)алкилиденом или циклоалкилиденом; аминооксигруппу, которая может быть замещена (низш.)алкилом, (низш.)алкенилом, необязательно замещенным (низш.)алкилиденом или циклоалкилиденом; нитрогруппу; (низш )алкилсульфонил; арил; 5- или 6-членную гетероциклическую группу; оксогруппу; или оксид, при этом каждый из заместителей может присутствовать в одном или нескольких из любых возможных положений
Хотя заместитель для “необязательно замещенного 5- или 6-членного гетероциклического кольца, содержащего 1 или 2 гетероатома” имеет такие же значения, которые описаны выше, предпочтительным кольцом является кольцо, замещенное (низш.)алкилом, или незамещенное кольцо.
Выражение “когда кольцо А, кольцо В и/или кольцо С представляют собой необязательно замещенное 5-членное гетероциклическое кольцо, W1, W2 и/или W3 обозначает связь" означает, что когда кольцо А обозначает 5-членное гетероциклическое кольцо, W1 обозначает связь, указывающую положения, в которых V1 и Х присоединены к кольцу А, как это показано с помощью формулы:
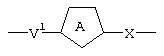
Аналогично этому, когда кольцо В или кольцо С представляет собой 5-членное гетероциклическое кольцо, W2 или W3 обозначает связь, указывающую положения, в которых присоединены V1 и V2, как это показано с помощью формулы:
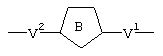 или
или 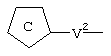
Каждый из X, V1 и V2 может быть непосредственно присоединен к гетероатому, входящему в состав кольца А, кольца В и кольца С соответственно.
Выражение "Ra и Rb вместе образуют -(CReRf)s-" обозначает, что Ra и Rb вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное насыщенное азотсодержащее гетероциклическое кольцо, представляющее собой, например, необязательно замещенный азиридин, необязательно замещенный азетидин, необязательно замещенный пирролидин, необязательно замещенный пиперидин и необязательно замещенный пергидроазепин (в данном случае заместитель представляет собой (низш.)алкил, (низш.)алкокси- или аминогруппу). Каждый из нескольких Re и Rf независимо друг от друга обозначает водород, (низш.)алкил, (низш.)алкокси- или аминогруппу, и они обычно включают -(СН2)2-, -(СН2)3-, -СН(Ме)(СН2)3-, -СН2СН(ОМе)(СН2)3-, -(СН2)3СН(NН2)(СН2)2- и т.п.
Ингибиторы Тh2-дифференцировки по изобретению могут включать фармацевтически приемлемую соль соединения формулы (I). Такая фармацевтически приемлемая соль может представлять собой, например, соль минеральной кислоты, такой как соляная кислота, серная кислота, азотная кислота, фосфорная кислота, фтористоводородная кислота и бромистоводородная кислота; соль органической кислоты, такой как муравьиная кислота, уксусная кислота, винная кислота, молочная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота и янтарная кислота; соль органического основания, такого как аммоний, триметиламмоний и триэтиламмоний; соль щелочного металла, такого как натрий и калий, а также соль щелочно-земельного металла, такого как кальций и магний.
Ингибиторы Тh2-дифференцировки по изобретению включают сольваты (предпочтительно гидраты) соединения формулы (I). Такой сольват может, например, представлять собой сольват с органическим растворителем или водой. Когда образуется гидрат, то может быть включено необходимое количество молекул воды.
Ингибиторы Тh2-дифференцировки по изобретению включают все стереоизомеры (например, атропический изомер и т.п.) соединения формулы (I).
Хотя ингибирующим действием в отношении Тh2-дифференцировки обладает любое соединение формулы (I), ниже перечислены наиболее предпочтительные соединения.
Соединения формулы (I), где:
1) кольцо А представляет собой необязательно замещенное ароматическое карбоциклическое кольцо или необязательно замещенное 5- или 6-членное гетероциклическое кольцо (ниже в настоящем описании обозначается как "кольцо А представляет собой А-1");
кольцо А представляет собой необязательно замещенное бензольное кольцо или необязательно замещенное 6-членное гетероциклическое кольцо (ниже в настоящем описании обозначается как "кольцо А представляет собой А-2");
кольцо А представляет собой необязательно замещенное бензольное кольцо (ниже в настоящем описании обозначается как "кольцо А представляет собой А-3");
кольцо А представляет собой бензольное кольцо, которое может иметь заместитель (галоген, гидроксигруппу, (низш.)алкил, (низш.)алкокси-, карбоксигруппу или (низш.)алкоксикарбонил) (ниже в настоящем описании обозначается как "кольцо А представляет собой А-4");
кольцо А представляет собой бензольное кольцо, которое может иметь заместитель (галоген, гидрокси- или (низш.)алкоксигруппу) (ниже в настоящем описании обозначается как "кольцо А представляет собой А-5");
кольцо А представляет собой бензольное кольцо, которое может быть замещено галогеном (ниже в настоящем описании обозначается как "кольцо А представляет собой А-6");
2) кольцо В представляет собой необязательно замещенное ароматическое карбоциклическое кольцо или необязательно замещенное 5- или 6-членное гетероциклическое кольцо (ниже в настоящем описании называется как "кольцо В представляет собой В-1");
кольцо В представляет собой необязательно замещенное бензольное кольцо или необязательно замещенное 6-членное гетероциклическое кольцо (ниже в настоящем описании называется как "кольцо В представляет собой В-2");
кольцо В представляет собой необязательно замещенное бензольное кольцо (ниже в настоящем описании называется как "кольцо В представляет собой В-3");
кольцо В представляет собой бензольное кольцо, которое может иметь заместитель (галоген, гидроксигруппу, необязательно замещенный (низш.)алкил, необязательно замещенную (низш.)алкоксигруппу или необязательно замещенный (низш.) алкоксикарбонил) (ниже в настоящем описании называется как "кольцо В представляет собой В-4");
кольцо В представляет собой бензольное кольцо, которое может иметь заместитель (гидроксигруппу, (низш.)алкил, (низш.)алкоксигруппу или (низш.) алкоксикарбонил) (ниже в настоящем описании называется как "кольцо В представляет собой В-5");
кольцо В представляет собой группу, выбранную из:
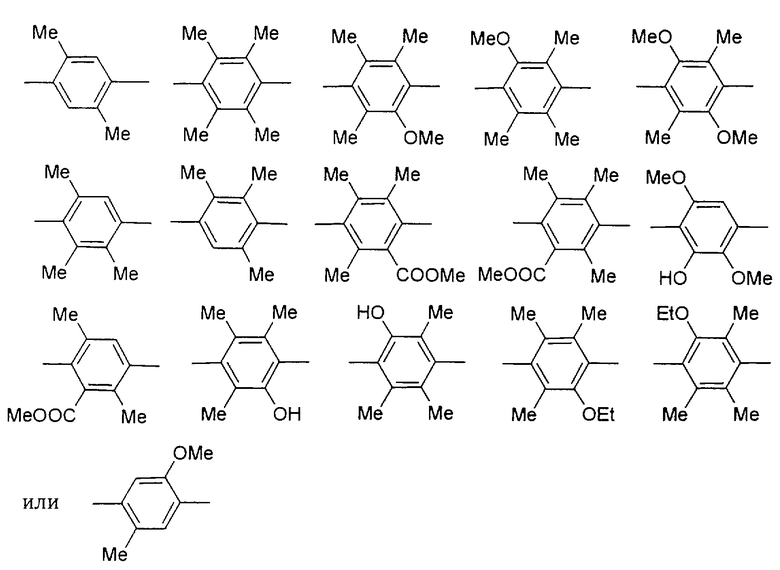
(ниже в настоящем описании называется как "В представляет собой В-6");
3) кольцо С представляет собой необязательно замещенное ароматическое карбоциклическое кольцо или необязательно замещенное 5- или 6-членное гетероциклическое кольцо (ниже в настоящем описании называется как "кольцо С представляет собой С-1");
кольцо С представляет собой необязательно замещенное бензольное кольцо или необязательно замещенное 6-членное гетероциклическое кольцо, содержащее 1 или 2 гетероатома (ниже в настоящем описании называется как "кольцо С представляет собой С-2");
кольцо С представляет собой необязательно замещенное бензольное кольцо, необязательно замещенное пиридиновое кольцо, необязательно замещенное пиримидиновое кольцо, необязательно замещенное пиридазиновое кольцо или необязательно замещенное пиразиновое кольцо (ниже в настоящем описании называется как "кольцо С представляет собой С-3");
кольцо С представляет собой бензольное кольцо, пиридиновое кольцо, пиримидиновое кольцо, пиридазиновое кольцо или пиразиновое кольцо (которое может быть замещено галогеном, (низш.)алкилом, (низш.)алкокси-, (низш.)алкенилокси- или (низш.)алкениламиногруппой) (ниже в настоящем описании называется как "кольцо С представляет собой С-4");
кольцо С представляет собой бензольное кольцо или пиридиновое кольцо (которое может быть замещено галогеном, (низш.)алкилом, (низш.)алкокси-, (низш.)алкенилокси- или (низш.)алкениламиногруппой) (ниже в настоящем описании называется как "кольцо С представляет собой С-5");
4) Х обозначает -О-, -СН2- или –NR1-, где R1 обозначает водород или необязательно замещенный (низш.)алкил (ниже в настоящем описании называется как "X представляет собой Х-1");
Х обозначает -О-, -СН2- или -NH- (ниже в настоящем описании называется как "X представляет собой Х-2");
Х обозначает -О- или -NH- (ниже в настоящем описании называется как "X представляет собой Х-3") или
Х обозначает -NH- (ниже в настоящем описании называется как "X представляет собой Х-4");
5) Y обозначает водород, необязательно замещенный (низш.)алкил, необязательно замещенный (низш.)алкенил или необязательно замещенный циклоалкил (ниже в настоящем описании называется как "Y представляет собой Y-1");
Y обозначает водород, (низш.)алкил, арилалкил, (низш.)алкенил или циклоалкил (ниже в настоящем описании называется как "Y представляет собой Y-2");
Y обозначает (низш.)алкил, бензил или (низш.)алкенил (ниже в настоящем описании называется как "Y представляет собой Y-3");
Y обозначает пренил (ниже в настоящем описании называется как "Y представляет собой Y-4");
6) оба V1 и V2 обозначают простые связи;
7) кольцо А, кольцо В, кольцо С, Х и Y присутствуют в любой из приведенных ниже комбинаций и оба V1 и V2 обозначают простые связи.
(А-3, В-3, С-2, Х-2, Y-1), (А-3, В-3, С-2, Х-2, Y-3), (А-3, В-3, С-2, Х-2, Y-4), (A-3, В-3, С-2, Х-3, Y-1), (А-3, В-3, С-2, Х-3, Y-3), (А-3, В-3, С-2, Х-3, Y-4), (А-3, В-3, С-4, Х-2, Y-1), (А-3, В-3, С-4, Х-2, Y-3), (А-3, В-3, С-4, Х-2, Y-4), (А-3, В-3, С-4, Х-3, Y-1), (А-3, В-3, С-4, Х-3, Y-3), (А-3, В-3, С-4, Х-3, Y-4), (А-3, В-3, С-5, Х-2, Y-1), (А-3, В-3, С-5, Х-2, Y-3), (А-3, В-3, С-5, Х-2, Y-4), (А-3, В-3, С-5, Х-3, Y-1), (А-3, В-3, С-5, Х-3, Y-3), (А-3, В-3, С-5, Х-3, Y-4), (А-3, В-4, С-2, Х-2, Y-1), (А-3, В-4, С-2, Х-2, Y-3), (А-3, В-4, С-2, Х-2, Y-4), (А-3, В-4, С-2, Х-3, Y-1), (A-3, B-4, C-2, X-3, Y-3), (А-3, В-4, С-2, Х-3, Y-4), (А-3, В-4, С-4, Х-2, Y-1), (А-3, В-4, С-4, Х-2, Y-3), (А-3, В-4, С-4, Х-2, Y-4), (А-3, В-4, С-4, Х-3, Y-1), (А-3, В-4, С-4, Х-3, Y-3), (А-3, В-4, С-4, Х-3, Y-4), (А-3, В-4, С-5, Х-2, Y-1), (А-3, В-4, С-5, Х-2, Y-3), (А-3, В-4, С-5, Х-2, Y-4), (А-3, В-4, С-5, Х-3, Y-1), (А-3, В-4, С-5, Х-3, Y-3), (А-3, В-4, С-5, Х-3, Y-4), (А-3, В-6, С-2, Х-2, Y-1), (А-3, В-6, С-2, Х-2, Y-3), (А-3, В-6, С-2, Х-2, Y-4), (А-3, В-6, С-2, Х-3, Y1), (А-3, В-6, С-2, Х-3, Y-3), (А-3, В-6, С-2, Х-3, Y-4), (А-3, В-6, С-4, Х-2, Y-1), (А-3, В-6, С-4, Х-2, Y-3), (А-3, В-6, С-4, Х-2, Y-4), (А-3, В-6, С-4, Х-3, Y-1), (А-3, В-6, С-4, Х-3, Y-3), (А-3, В-6, С-4, Х-3, Y-4), (А-3, В-6, С-5, Х-2, Y-1), (А-3, В-6, С-5, Х-2, Y-3), (А-3, В-6, С-5, Х-2, Y-4), (А-3, В-6, С-5, Х-3, Y-1), (А-3, В-6, С-5, Х-3, Y-3), (А-3, В-6, С-5, Х-3, Y-4), (А-4, В-3, С-2, Х-2, Y-1), (А-4, В-3, С-2, Х-2, Y-3), (А-4, В-3, С-2, Х-2, Y-4), (A-4, В-3, С-2, Х-3, Y-1), (А-4, В-3, С-2, Х-3, Y-3), (А-4, В-3, С-2, Х-3, Y-4), (А-4, В-3, С-4, Х-2, Y-1), (А-4, В-3, С-4, Х-2, Y-3), (А-4, В-3, С-4, Х-2, Y-4), (А-4, В-3, С-4, Х-3, Y-1), (А-4, В-3, С-4, Х-3, Y-3), (А-4, В-3, С-4, Х-3, Y-4), (А-4, В-3, С-5, Х-2, Y-1), (А-4, В-3, С-5, Х-2, Y-3), (А-4, В-3, С-5, Х-2, Y-4), (А-4, В-3, С-5, Х-3, Y-1), (А-4, В-3, С-5, Х-3, Y-3), (А-4, В-3, С-5, Х-3, Y-4), (А-4, В-4, С-2, Х-2, Y-1), (А-4, В-4, С-2, Х-2, Y-3), (А-4, В-4, С-2, Х-2, Y-4), (А-4, В-4, С-2, Х-3, Y-1), (А-4, В-4, С-2, Х-3, Y-3), (А-4, В-4, С-2, Х-3, Y-4), (А-4, В-4, С-4, Х-2, Y-1), (А-4, В-4, С-4, Х-2, Y-3), (А-4, В-4, С-4, Х-2, Y-4), (А-4, В-4, С-4, Х-3, Y-1), (А-4, В-4, С-4, Х-3, Y-3), (А-4, В-4, С-4, Х-3, Y-4), (А-4, В-4, С-5, Х-2, Y-1), (А-4, В-4, С-5, Х-2, Y-3), (А-4, В-4, С-5, Х-2, Y-4), (А-4, В-4, С-5, Х-3, Y-1), (А-4, В-4, С-5, Х-3, Y-3), (А-4, В-4, С-5, Х-3, Y-4), (А-4, В-6, С-2, Х-2, Y-1), (А-4, В-6, С-2, Х-2, Y-3), (А-4, В-6, С-2, Х-2, Y-4), (А-4, В-6, С-2, Х-3, Y-1), (А-4, В-6, С-2, Х-3, Y-3), (А-4, В-6, С-2, Х-3, Y-4), (А-4, В-6, С-4, Х-2, Y-1), (А-4, В-6, С-4, Х-2, Y-3), (А-4, В-6, С-4, Х-2, Y-4), (А-4, В-6, С-4, Х-3, Y-1), (А-4, В-6, С-4, Х-3, Y-3), (А-4, В-6, С-4, Х-3, Y-4), (А-4, В-6, С-5, Х-2, Y-1), (А-4, В-6, С-5, Х-2, Y-3), (А-4, В-6, С-5, Х-2, Y-4), (А-4, В-6, С-5, Х-3, Y-1), (А-4, В-6, С-5, Х-3, Y-3), (А-4, В-6, С-5, Х-3, Y-4), (А-6, В-3, С-2, Х-2, Y-1), (А-6, В-3, С-2, Х-2, Y-3), (А-6, В-3, С-2, Х-2, Y-4), (A-6, В-3, С-2, Х-3, Y-1), (А-6, В-3, С-2, Х-3, Y-3), (А-6, В-3, С-2, Х-3, Y-4), (А-6, В-3, С-4, Х-2, Y-1), (А-6, В-3, С-4, Х-2, Y-3), (А-6, В-3, С-4, Х-2, Y-4), (А-6, В-3, С-4, Х-3, Y-1), (А-6, В-3, С-4, Х-3, Y-3), (А-6, В-3, С-4, Х-3, Y-4), (А-6, В-3, С-5, Х-2, Y-1), (А-6, В-3, С-5, Х-2, Y-3), (А-6, В-3, С-5, Х-2, Y-4), (А-6, В-3, С-5, Х-3, Y-1), (А-6, В-3, С-5, Х-3, Y-3), (А-6, В-3, С-5, Х-3, Y-4), (А-6, В-4, С-2, Х-2, Y-1), (А-6, В-4, С-2, Х-2, Y-3), (А-6, В-4, С-2, Х-2, Y-4), (А-6, В-4, С-2, Х-3, Y-1), (А-6, В-4, C-2, X-3, Y-3), (А-6, В-4, С-2, Х-3, Y-4), (А-6, В-4, С-4, Х-2, Y-1), (А-6, В-4, С-4, Х-2, Y-3), (А-6, В-4, С-4, Х-2, Y-4), (А-6, В-4, С-4, Х-3, Y-1), (А-6, В-4, С-4, Х-3, Y-3), (А-6, В-4, С-4, Х-3, Y-4), (А-6, В-4, С-5, Х-2, Y-1), (А-6, В-4, С-5, Х-2, Y-3), (А-6, В-4, С-5, Х-2, Y-4), (А-6, В-4, С-5, Х-3, Y-1), (А-6, В-4, С-5, Х-3, Y-3), (А-6, В-4, С-5, Х-3, Y-4), (А-6, В-6, С-2, Х-2, Y-1), (А-6, В-6, С-2, Х-2, Y-3), (А-6, В-6, С-2, Х-2, Y-4), (А-6, В-6, С-2, Х-3, Y-1), (А-6, В-6, С-2, Х-3, Y-3), (А-6, В-6, С-2, Х-3, Y-4), (А-6, В-6, С-4, Х-2, Y-1), (А-6, В-6, С-4, Х-2, Y-3), (А-6, В-6, С-4, Х-2, Y-4), (А-6, В-6, С-4, Х-3, Y-1), (А-6, В-6, С-4, Х-3, Y-3), (А-6, В-6, С-4, Х-3, Y-4), (А-6, В-6, С-5, Х-2, Y-1), (А-6, В-6, С-5, Х-2. Y-3), (А-6, В-6, С-5, Х-2, Y-4), (А-6, В-6, С-5, Х-3, Y-1), (А-6, В-6, С-5, Х-3, Y-3), (А-6, В-6, С-5, Х-3, Y-4). Соединения формулы (Iа), представляющие собой:
1) соединение, где R4, R5, R6 и R7 каждый независимо друг от друга обозначает водород, галоген, гидроксигруппу, (низш.)алкил, (низш.)алкокси-, карбоксигруппу или (низш.)алкоксикарбонил (ниже в настоящем описании называется как "R4-R7 представляют собой R47-1");
соединение, где R4, R5, R6 и R7 каждый независимо друг от друга обозначает водород или галоген (ниже в настоящем описании называется как "R4-R7 представляют собой R47-2");
соединение, где один из R4 и R5 обозначает водород, а другой обозначает галоген, и оба R6 и R7 обозначают атомы водорода (ниже в настоящем описании называется как "R4-R7 представляют собой R47-3");
2) соединение, где R8, R9, R10 и R11 каждый независимо друг от друга обозначает водород, галоген, гидроксигруппу, необязательно замещенный (низш.)алкил, необязательно замещенную (низш.)алкокси-, карбоксигруппу или необязательно замещенный (низш.)алкоксикарбонил (ниже в настоящем описании называется как "R8-R11 представляют собой R811-1");
соединение, где R8, R9, R10 и R11 каждый независимо друг от друга обозначает водород, гидроксигруппу, (низш.)алкил, (низш.)алкоксигруппу или (низш.)алкоксикарбонил (ниже в настоящем описании называется как "R8–R11 представляют собой R811-2");
соединение, где R8 и R11 каждый независимо друг от друга обозначает водород, гидроксигруппу, (низш.)алкил или (низш.)алкоксикарбонил, и R9 и R10 каждый независимо друг от друга обозначает гидроксигруппу, (низш.)алкил,
(низш.)алкоксигруппу или (низш.)алкоксикарбонил (ниже в настоящем описании называется как "R8 – R11 представляют собой R81 1-3");
соединение, где R8 обозначает водород или (низш.)алкил, R9 обозначает гидроксигруппу, (низш.)алкил или (низш.)алкоксигруппу, R10 обозначает гидроксигруппу, (низш.)алкил, (ниэш.)алкоксигруппу или (низш.)алкоксикарбонил и R11 обозначает водород, гидроксигруппу, (низш.)алкил или (низш.)алкоксикарбонил (ниже в настоящем описании называется как "R8-R11 представляют собой R811-4");
соединение, где комбинация R8, R9, R10 и R11 имеет такие же значения, что и для указанного выше кольца В-6 (ниже в настоящем описании называется как "R8-R11 представляют собой R811-5");
3) соединение, где R12, R13, R14 и R15 каждый независимо друг от друга обозначает водород, галоген, гидроксигруппу, (низш.)алкил, (низш.)алкокси-, карбоксигруппу или (низш.)алкоксикарбонил (ниже в настоящем описании называется как "R12-R15 представляют собой R1215-1");
соединение, где R12, R13, R14 и R15 каждый независимо друг от друга обозначает водород или галоген (ниже в настоящем описании называется как "R12-R15 представляют собой R 1215-2");
соединение, где все R12, R13, R14 и R15 обозначают атомы водорода (ниже в настоящем описании называется как "R12 - R15 представляют собой R 1215-3");
4) соединение, где X1 и X2 каждый независимо друг от друга обозначает -O- или -NH- (ниже в настоящем описании называется как "Х1 и X2 представляют собой XI 2-1");
соединение, где один из X1 и X2 обозначает -О-, а другой обозначает -NH-, или оба обозначают -NH- (ниже в настоящем описании называется как "X1 и X2 представляют собой X1 2-2");
5) соединение, где Y1 и Y2 каждый независимо друг от друга обозначает водород, необязательно замещенный (низш.)алкил, необязательно замещенный (низш.)алкенил или необязательно замещенный циклоалкил (ниже в настоящем описании называется как "Y1 и Y2 представляют собой Y12-1");
соединение, где Y1 и Y2 каждый независимо друг от друга обозначает водород, необязательно замещенный галогеном (низш.)алкил, арилалкил, (низш.)алкенил или циклоалкил (ниже в настоящем описании называется как "Y1 и Y2 представляют собой Y12-2");
соединение, где Y1 и Y2 каждый независимо друг от друга обозначает необязательно замещенный галогеном (низш.)алкил или необязательно замещенный галогеном (низш.)алкенил (ниже в настоящем описании называется как "Y1 и Y2 представляют собой Y12-3");
соединение, где один из Y1 и Y2 обозначает пренил, а другой обозначает необязательно замещенный галогеном (низш.)алкил или необязательно замещенный галогеном (низш.)алкенил (ниже в настоящем описании называется как "Y1 и Y2 представляют собой Y12-4");
соединение, где оба Y1 и Y2 обозначают пренил (ниже в настоящем описании называется как "Y1 и Y2 представляют собой Y12-5");
6) соединение, где R4-R7, R8-R11, R12-R15, X1 и X2 и Y1 и Y2 имеют значения, соответствующие любой из приведенных ниже комбинаций:
(R47-1, R811-4, R1215-1, Х12-1, Y12-5), (R47-2, R811-4, R1215-2, Х12-1, Y12-3), (R47-2, R811-4, R1215-2, Х12-1, Y12-5), (R47-2, R811-4, R1215-2, Х12-2, Y12-3), (R47-2, R811-4, R1215-2, Х12-2, Y12-5), (R47-2, R811-4, R1215-3, Х12-1, Y12-3), (R47-2, R811-4, R1215-3, Х12-1, Y12-5), (R47-2, R811-4, R1215-3, Х12-2, Y12-3), (R47-2, R811-4, R1215-3, Х12-2, Y12-5), (R47-2, R811-5, R1215-2, Х12-1, Y12-3), (R47-2, R811-5, R1215-2, Х12-1, Y12-5), (R47-2, R811-5, R1215-2, X12-2, Y12-3), (R47-2, R811-5, R1215-2, Х12-2, Y12-5), (R47-2, R811-5, R1215-3, Х12-1, Y12-3), (R47-2, R811-5, R1215-3, Х12-1, Y12-5), (R47-2, R811-5, R1215-3, Х12-2, Y12-3), (R47-2, R811-5, R1215-3, Х12-2, Y12-5), (R47-3, R811-4, R1215-2, Х12-1, Y12-3), (R47-3, R811-4, R1215-2, Х12-1, Y12-5), (R47-3, R811-4, R1215-2, Х12-2, Y12-3), (R47-3, R811-4, R1215-2, Х12-2, Y12-5), (R47-3, R811-4, R1215-3, Х12-1, Y12-3), (R47-3, R811-4, R1215-3, Х12-1, Y12-5), (R47-3, R811-4, R1215-3, Х12-2, Y12-3), (R47-3, R811-4, R1215-3, Х12-2, Y12-5), (R47-3, R811-5, R1215-2, Х12-1, Y12-3), (R47-3, R811-5, R1215-2, Х12-1, Y12-5), (R47-3, R811-5, R1215-2, Х12-2, Y12-3), (R47-3, R811-5, R1215-2, Х12-2, Y12-5), (R47-3, R811-5, R1215-3, Х12-1, Y12-3), (R47-3, R811-5, R1215-3, Х12-1, Y12-5), (R47-3, R811-5, R1215-3, Х12-2, Y12-3), (R47-3, R811-5, R1215-3, Х12-2, Y12-5).
Соединения формулы (Ib), представляющие собой:
1) соединение, где R4, R5, R6 и R7 каждый представляет собой R47-1, соединение, где R4, R5, R6 и R7 каждый представляет собой R47-2, соединение, где R4, R5, R6 и R7 каждый представляет собой R47-3,
2) соединение, где R8, R9, R10 и R11 каждый представляет собой R811-1, соединение, где R8, R9, R10 и R11 каждый представляет собой R811-2, соединение, где R8, R9, R10 и R11 каждый представляет собой R811-3, соединение, где R8, R9, R10 и R11 каждый представляет собой R811-4, соединение, где R8, R9, R10 и R11 каждый представляет собой R811-5,
3) соединение, где кольцо С представляет собой С-1,
соединение, где кольцо С представляет собой С-2,
соединение, где кольцо С представляет собой С-3,
соединение, где кольцо С представляет собой бензол, пиридин, пиримидин, пиридазин или пиразин (который может быть замещен галогеном, (низш.)алкилом или (низш.)алкоксигруппой (ниже в настоящем описании называется как "кольцо С представляет собой С-4’"),
соединение, где кольцо С представляет собой бензол или пиридин (который может быть замещен галогеном, (низш.)алкилом или (низш.) алкоксигруппой) (ниже в настоящем описании называется как "кольцо С представляет собой С-5’"),
4) соединение, где X1 и Х2 представляют собой X12-1,
соединение, где X1 и Х2 представляют собой X12-2,
5) соединение, где Y1 и Y2 представляют собой Y12-1,
соединение, где Y1 и Y2 представляют собой Y12-2,
соединение, где Y1 и Y2 представляют собой Y12-3,
соединение, где Y1 и Y2 представляют собой Y12-4,
соединение, где Y1 и Y2 представляют собой Y12-5,
6) соединение, где R4-R7, R10-R11, кольцо С, X1 и X2 и Y1 и Y2 имеют значения, соответствующие любой из приведенных ниже комбинаций:
(R47-2, R811-4, С-2, Х12-1, Y12-3), (R47-2, R811-4, С-2, Х12-1, Y12-5), (R47-2, R811-4, С-2, Х12-2, Y12-3), (R47-2, R811-4, С-2, Х12-2, Y12-5), (R47-2, R811-4, С-4’, Х12-1, Y12-3), (R47-2, R811-4, С-4’, Х12-1, Y12-5), (R47-2, R811-4, С-4’, Х12-2, Y12-3), (R47-2, R811-4, С-4’, Х12-2, Y12-5), (R47-2, R811-4, С-5’, Х12-1, Y12-3), (R47-2, R811-4, С-5’, Х12-1, Y12-5), (R47-2, R811-4, С-5’, Х12-2, Y12-3), (R47-2, R811-4, С-5’, Х12-2, Y12-5), (R47-2, R811-5, С-2, Х12-1, Y12-3), (R47-2, R811-5, С-2, Х12-1, Y12-5), (R47-2, R811-5, С-2, Х12-2, Y12-3), (R47-2, R811-5, С-2, Х12-2, Y12-5), (R47-2, R811-5, С-4’, Х12-1, Y12-3), (R47-2, R811-5, С-4’, Х12-1, Y12-5), (R47-2, R811-5, С-4’, Х12-2, Y12-3), (R47-2, R811-5, С-4’, Х12-2, Y12-5), (R47-2, R811-5, С-5’, Х12-1, Y12-3), (R47-2, R811-5, C-5’, X12-1, Y12-5), (R47-2, R811-5, С-5’, Х12-2, Y12-3), (R47-2, R811-5, С-5’, Х12-2, Y12-5), (R47-3, R811-4, С-2, X12-1, Y12-3), (R47-3, R811-4, С-2, X12-1, Y12-5), (R47-3, R811-4, С-2, Х12-2, Y12-3), (R47-3, R811-4, С-2, Х12-2, Y12-5), (R47-3, R811-4, С-4’, X12-1, Y12-3), (R47-3, R811-4, С-4’, X12-1, Y12-5), (R47-3, R811-4, С-4’, Х12-2, Y12-3), (R47-3, R811-4, С-4’, Х12-2, Y12-5), (R47-3, R811-4, С-5’, X12-1, Y12-3), (R47-3, R811-4, С-5’, X12-1, Y12-5), (R47-3, R811-4, С-5’, Х12-2, Y12-3), (R47-3, R811-4, С-5’, Х12-2, Y12-5), (R47-3, R811-5, C-2, X12-1, Y12-3), (R47-3, R811-5, С-2, X12-1, Y12-5), (R47-3, R811-5, С-2, Х12-2, Y12-3), (R47-3, R811-5, С-2, Х12-2, Y12-5), (R47-3, R811-5, С-4’, X12-1, Y12-3), (R47-3, R811-5, С-4’, X12-1, Y12-5), (R47-3, R811-5, С-4’, Х12-2, Y12-3), (R47-3, R811-5, С-4’, Х12-2, Y12-5), (R47-3, R811-5, С-5’, X12-1, Y12-3), (R47-3, R811-5, С-5’, X12-1, Y12-5), (R47-3, R811-5, С-5’, Х12-2, Y12-3), (R47-3, R811-5, С-5’, Х12-2, Y12-5).
Соединения формулы (Iс), представляющие собой:
1) соединение, где кольцо А представляет собой А-1, соединение, где кольцо А представляет собой А-2, соединение, где кольцо А представляет собой А-3, соединение, где кольцо А представляет собой А-4, соединение, где кольцо А представляет собой А-5, соединение, где кольцо А представляет собой А-6,
2) соединение, где кольцо В представляет собой В-1, соединение, где кольцо В представляет собой В-2, соединение где кольцо В представляет собой В-3, соединение, где кольцо В представляет собой В-4, соединение, где кольцо В представляет собой В-5,
3) соединение, где кольцо С представляет собой С-1, соединение, где кольцо С представляет собой С-2, соединение, где кольцо С представляет собой С-3, соединение, где кольцо С представляет собой С-4, соединение, где кольцо С представляет собой С-5,
4) соединение, где Х1 обозначает -О- или -NH- (ниже в настоящем описании называется как "Х1 представляет собой Х-1″), соединение, где Х1 обозначает -NH- (ниже в настоящем описании называется как "X1 представляет собой Х-2"),
5) соединение, где Y1 представляет собой Y-1, соединение, где Y1 представляет собой Y-2, соединение, где Y1 представляет собой Y-3, соединение, где Y1 представляет собой Y-4,
6) соединение, где Ra и Rb каждый независимо друг от друга обозначает водород, (низш.)алкил, (низш.)алкенил, (низш.)алкоксикарбонил или (низш.)алкилсульфонил, или они вместе образуют RCRdC= или -(CReRf)s-, где Rc и Rd каждый независимо друг от друга обозначает водород, (низш.)алкил, (низш.)алкенил, (низш.)алкоксигруппу, арил или гетероциклическую группу или они вместе с атомом углерода, к которому они присоединены, образуют циклоалкилиден, Re каждый независимо друг от друга обозначает водород, (низш.)алкил, (низш )алкокси- или аминогруппу, и Rf каждый независимо друг от друга обозначает водород, (низш.)алкил, (низш.)алкокси- или аминогруппу, и s обозначает целое число от 2 до 6 (ниже в настоящем описании называется как "Ra и Rb представляют собой Rab-1″);
соединение, где Ra и Rb каждый независимо друг от друга обозначает водород, алкил, имеющий 1-6 атомов углерода, алкенил, имеющий 2-6 атомов углерода, алкоксикарбонил, имеющий 1-6 атомов углерода, или алкилсульфонил, имеющий 1-6 атомов углерода, или они вместе образуют RcRdC= или -(CReRf)s-, где Re и Rf каждый независимо друг от друга обозначает водород, алкил, имеющий 1-6 атомов углерода, алкенил, имеющий 2-6 атомов углерода, алкоксигруппу, имеющую 1-6 атомов углерода, фенил или 5- или 6-членную ароматическую гетероциклическую группу или они вместе с атомом углерода, к которому они присоединены, образуют циклоалкилиден, имеющий 5-6 атомов углерода, Re каждый независимо друг от друга обозначает водород, алкил, имеющий 1-6 атомов углерода, алкоксигруппу, имеющую 1-6 атомов углерода или аминогруппу, и Rf каждый независимо друг от друга обозначает водород, алкил, имеющий 1-6 атомов углерода, алкоксигруппу, имеющую 1-6 атомов углерода, или аминогруппу, и s обозначает целое число 4 или 5 (ниже в настоящем описании называется как "Ra и Rb представляют собой Rab-2");
соединение, где Ra и Rb каждый независимо друг от друга обозначает водород, алкил, имеющий 1-3 атома углерода, или алкоксикарбонил, имеющий 1-4 атома углерода, или они вместе образуют RcRdC= или -(CReRf)s-, где Rc и Rd каждый независимо друг от друга обозначает водород, алкил, имеющий 1-3 атома углерода, алкенил, имеющий 2-4 атома углерода, или алкоксигруппу, имеющую 1-3 атома углерода, Re каждый независимо друг от друга обозначает водород или алкил, имеющий 1-3 атома углерода, и Rf каждый независимо друг от друга обозначает водород или алкил, имеющий 1-3 атома углерода (ниже в настоящем описании называется как "Ra и Rb представляют собой Rab-3"),
соединение, где Ra и Rb каждый независимо друг от друга обозначает водород, алкил, имеющий 1-3 атома углерода, или алкоксикарбонил, имеющий 1-4 атома углерода, или они вместе образуют RcRdC=, один из Rc и Rd обозначает алкил, имеющий 1-3 атома углерода, а другой обозначает водород, алкил, имеющий 1-3 атома углерода или (низш.)алкоксигруппу, имеющую 1-3 атома углерода (ниже в настоящем описании называется как "Ra и Rb представляют собой Rab-4");
соединение, где Ra и Rb вместе образуют RcRdC= один из Rc и Rd обозначает алкил, имеющий 1-3 атома углерода, а другой обозначает алкил, имеющий 1-3 атома углерода или (низш.)алкоксигруппу, имеющую 1-3 атома углерода (ниже в настоящем описании называется как " Ra и Rb представляют собой Rab-5"),
7) соединение, где n равно 0 или 1 (ниже в настоящем описании называется как "n представляет собой n1");
соединение, где n равно 1 (ниже в настоящем описании называется как "n представляет собой n2"),
8) соединение, где кольцо А, кольцо В, кольцо С, X1, Y1 и Ra и Rb имеют значения, соответствующие любой из приведенных ниже комбинаций, и n равно 0 или 1.
(А-4, В-4, С-4, Х-1, Y-3, Rab-2), (А-4, В-4, С-4, Х-1, Y-3, Rab-3), (А-4, В-4, С-4, Х-1, Y-4, Rab-2), (А-4, В-4, С-4, Х-1, Y-4, Rab-3), (А-4, В-4, С-4, Х-2, Y-3, Rab-2), (А-4, В-4, С-4, Х-2, Y-3, Rab-3), (А-4, В-4, С-4, Х-2, Y-4, Rab-2), (А-4, В-4, С-4, Х-2, Y-4, Rab-3), (А-4, В-4, С-5, Х-1, Y-3, Rab-2), (А-4, В-4, С-5, Х-1, Y-3, Rab-3), (А-4, В-4, С-5, Х-1, Y-4, Rab-2), (А-4, В-4, С-5, Х-1, Y-4, Rab-3), (А-4, В-4, С-5, Х-2, Y-3, Rab-2), (А-4, В-4, С-5, Х-2, Y-3, Rab-3), (А-4, В-4, С-5, Х-2, Y-4, Rab-2), (А-4, В-4, С-5, Х-2, Y-4, Rab-3), (А-4, В-6, С-4, Х-1, Y-3, Rab-2), (А-4, В-6, С-4, Х-1, Y-3, Rab-3), (А-4, В-6, С-4, Х-1, Y-4, Rab-2), (А-4, В-6, С-4, Х-1, Y-4, Rab-3), (А-4, В-6, С-4, Х-2, Y-3, Rab-2), (А-4, В-6, С-4, Х-2, Y-3, Rab-3), (А-4, В-6, С-4, Х-2, Y-4, Rab-2), (А-4, В-6, С-4, Х-2, Y-4, Rab-3), (А-4, В-6, С-5, Х-1, Y-3, Rab-2), (А-4, В-6, С-5, Х-1, Y-3, Rab-3), (А-4, В-6, С-5, Х-1, Y-4, Rab-2), (А-4, В-6, С-5, Х-1, Y-4, Rab-3), (А-4, В-6, С-5, Х-2, Y-3, Rab-2), (А-4, В-6, С-5, Х-2, Y-3, Rab-3), (А-4, В-6, С-5, Х-2, Y-4, Rab-2), (А-4, В-6, С-5, Х-2, Y-4, Rab-3), (А-6, В-4, С-4, Х-1, Y-3, Rab-2), (А-6, В-4, С-4, Х-1, Y-3, Rab-3), (A-6, В-4, С-4, Х-1, Y-4, Rab-2), (А-6, В-4, С-4, Х-1, Y-4, Rab-3), (А-6, В-4, С-4, Х-2, Y-3, Rab-2), (А-6, В-4, С-4, Х-2, Y-3, Rab-3), (А-6, В-4, С-4, Х-2, Y-4, Rab-2), (А-6, В-4, С-4, Х-2, Y-4, Rab-3), (А-6, В-4, С-5, Х-1, Y-3, Rab-2), (А-6, В-4, С-5, Х-1, Y-3, Rab-3), (А-6, В-4, С-5, Х-1, Y-4, Rab-2), (А-6, В-4, С-5, Х-1, Y-4, Rab-3), (А-6, В-4, С-5, Х-2, Y-3, Rab-2), (А-6, В-4, С-5, Х-2, Y-3, Rab-3), (А-6, В-4, С-5, Х-2, Y-4, Rab-2), (А-6, В-4, С-5, Х-2, Y-4, Rab-3), (А-6, В-6, С-4, Х-1, Y-3, Rab-2), (А-6, В-6, С-4, Х-1, Y-3, Rab-3), (А-6, В-6, С-4, Х-1, Y-4, Rab-2), (А-6, В-6, С-4, Х-1, Y-4, Rab-3), (А-6, В-6, С-4, Х-2, Y-3, Rab-2), (А-6, В-6, С-4, Х-2, Y-3, Rab-3), (А-6, В-6, С-4, Х-2, Y-4, Rab-2), (А-6, В-6, С-4, Х-2, Y-4, Rab-3), (А-6, В-6, С-5, Х-1, Y-3, Rab-2), (А-6, В-6, С-5, Х-1, Y-3, Rab-3), (А-6, В-6, С-5, Х-1, Y-4, Rab-2), (А-6, В-6, С-5, Х-1, Y-4, Rab-3), (А-6, В-6, С-5, Х-2, Y-3, Rab-2), (А-6, В-6, С-5, Х-2, Y-3, Rab-3), (А-6, В-6, С-5, Х-2, Y-4, Rab-2), (А-6, В-6, С-5, Х-2, Y-4, Rab-3).
Более конкретно, предпочтительными являются соединения, описанные в WO 98/04508, или представленные ниже соединения (в таблицах 1-3 приведены структуры фрагментов, обозначенных символами A1, A2,..., B1, B2,..., C1, C2,..., которые используются в таблице 4 или в табл. 5-12. В таблицах сНех обозначает циклогексил, сРr обозначает циклопропил).
Ниже описан способ получения соединения формулы (I)
Способ получения соединения формулы (I’)
Соединение, представленное приведенной ниже формулой (I’) (ниже в настоящем описании называется как соединение (I’)), можно получать путем взаимодействия соединения, представленного формулой (IIа) (ниже в настоящем описании называется как соединение (IIа)), с бициклическим соединением, представленным формулой (IIIa) (ниже в настоящем описании называется как соединение (IIIa)), или путем взаимодействия соединения, представленного формулой (IIb) (ниже в настоящем описании называется как соединение (IIb)), с бициклическим соединением, представленным формулой (IIIb) (ниже в настоящем описании называется как соединение (IIIb)):
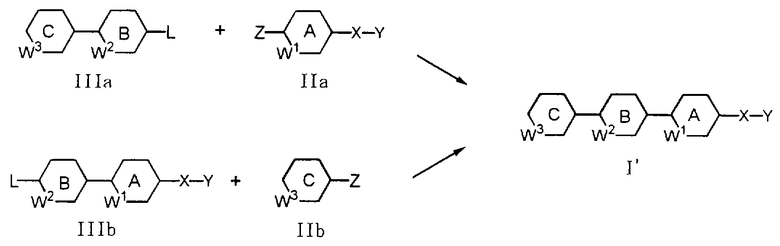
где один из заместителей L и Z обозначает дигидроксиборил, ди(низш.)алкилборил или ди(низш.)алкоксиборил, а другой обозначает галоген или –OSO2(CqF2+1) (q обозначает целое число от 0 до 4), и другие символы имеют указанные выше значения).
Соединение (IIа) и соединение (IIIa) или соединение (IIb) и соединение (IIIb) подвергают взаимодействию в смеси пригодного растворителя (например, бензола, толуола, N,N-диметилформамида, диметоксиэтана, тетрагидрофурана, диоксана, этанола или метанола) с водой или в безводной системе в присутствии палладиевого катализатора (например, Рd(РРh3)4, РdCl2(РРh3)2, PdCl2, Pd(OAc)2 или РdСl2(СН3СN)2, предпочтительно Рd(РРh3)4) в основных условиях (в присутствии такого основания, как К3РO4, NаНСО3, NaOEt, Nа2СО3, Еt3N, Ва(ОН)2, Сs2СО3, CsF, NaOH или Ag2CO3) при комнатной температуре или при нагревании в течение периода времени от нескольких десятков минут до нескольких десятков часов, получая соединение (I’).
Один из заместителей L и Z в соединениях, подвергаемых взаимодействию друг с другом, представляет собой любую борильную группу, которую можно использовать в реакции Сузуки (Chemical Communication 1979, 866, Journal of Organic Synthesis Society, 1993, том 51, № 11, стр.91-100), и предпочтительно она представляет собой дпгидроксиборил. Другой заместитель представляет собой любую уходящую группу, которую можно использовать в реакции Сузуки, такую как галоген или -OSO2(CqF2q+1), где q обозначает целое число от 0 до 4. Особенно предпочтительными являются галоген и трифторметансульфонилоксигруппа (ниже в настоящем описании сокращенно обозначается как OTf), при этом наиболее предпочтительными являются бром, йод и OTf.
Другие заместители в кольце А, кольце В и кольце С в соединениях (IIа), (IIIa), (IIb) и (IIIb) и -X-Y представляют собой любые группы, которые не оказывают неблагоприятного влияния на реакцию Сузуки, включая указанные группы за исключением галогена и -OS02(CqF2q+1), где q обозначает целое число от 0 до 4.
Например, Y может представлять собой необязательно замещенный (низш.)алкил, необязательно замещенный (низш.)алкенил, необязательно замещенный (низш.)алкинил, необязательно замещенный ацил, необязательно замещенный циклоалкил, необязательно замещенный циклоалкенил, необязательно замещенный арил или необязательно замещенное 5- или 6-членное гетероциклическое кольцо, которое может быть сконденсировано с бензольным кольцом, и когда Х обозначает -СН2-, Y может также обозначать необязательно замещенную (низш.)алкоксигруппу. Когда Х обозначает -О- или –NR’-, то Y может также обозначать необязательно замещенный (низш.)алкоксикарбонил, необязательно замещенный (низш.)алкилсульфонил или необязательно замещенный арилсульфонил.
Даже тогда, когда любой из заместителей в кольцах А, В и С представляет собой галоген, описанная выше реакция может протекать достаточно успешно, если способность к взаимодействию заместителей L и Z является относительно более высокой.
Описанная выше реакция также может быть осуществлена даже в том случае, когда любой из заместителей в кольцах А, В и С или -X-Y обозначает гидроксигруппу. Реакцию предпочтительно осуществляют после введения обычно используемой гидроксизащитной группы (такой как, например, метоксиметил, бензил, трет-бутилдиметилсилил, метансульфонил или паратолуолсульфонил), которую затем удаляют.
Хотя соединение (I’) наиболее эффективно и просто синтезируют с помощью описанной выше реакции Сузуки, в указанной выше схеме можно также вместо борильной группы использовать кремний, цинк или олово.
Например, когда один из заместителей L и Z обозначает –SiR
Когда один из заместителей L и Z обозначает -SnR
Требуемое соединение также может быть синтезировано путем подвергания взаимодействию соединения, где один из заместителей L и Z обозначает - Zn(Hal), где Hal обозначает галоген, а другой обозначает галоген (Асе. Chem. Res, 1982, 15, 340-348). Хотя можно использовать любой обычно применяемый палладиевый катализатор, предпочтительными примерами являются Pd(PPh3)4, PdCl2(dppf) (где dppf обозначает 1,1’-бис(дифенилфосфино)ферроцен), PdCl2(PPh3)2, PdCl2(PdCl2(орто-толил)3)2 и Pd(OAc)2.
Любую из этих реакций можно осуществлять в пригодном растворителе (например, N,N-диметилформамиде, тетрагидрофуране) при комнатной температуре или при нагревании в течение периода времени от нескольких десятков минут до нескольких десятков часов.
Соединения (IIIa) и (IIIb), используемые в приведенной выше схеме, могут представлять собой известные соединения или они могут быть получены из соединения, представленного формулой (Va) (ниже в настоящем описании называется как соединение (Va)), или соединения, представленного формулой (Vb) (ниже в настоящем описании называется как соединение (Vb)), которые можно синтезировать известным методом или методом, описанным ниже:
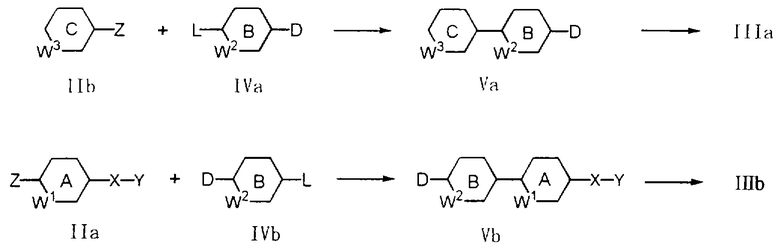
где D и L обозначают группы, которые не оказывают неблагоприятного влияния на взаимодействие с Z в условиях реакции Сузуки, и когда соединение, представленное формулой (IVa) или (IVb), представляет собой симметричное соединение, они могут представлять собой группы, аналогичные L, и где другие символы имеют указанные выше значения.
Сначала для взаимодействия соединения (IIb) с соединением (IVa) или соединения (IIа) с соединением (IVb) осуществляют стадию, аналогичную описанной выше стадии, получая соединение (Va) или (Vb). Если соединение (IVa) или (IVb) не является симметричным соединением, D предпочтительно представляет собой группу, которая не оказывает существенного неблагоприятного влияния на взаимодействие L и Z в условиях реакции Сузуки и которая может быть легко превращена в L. Например, можно использовать гидроксигруппу, водород, формил и нитрогруппу. L или Z можно подвергать взаимодействию с использованием кремния, цинка или олова вместо описанной выше борильной группы.
После этого D превращают в заместитель L, которая может использоваться в реакции Сузуки.
Например, когда D обозначает гидроксигруппу, взаимодействие с трифторметансульфонилирующим агентом (например, с трифторметансульфоновым ангидридом, трифторметансульфонилхлоридом или N-фенилтрифторметансульфонимидом) осуществляют в пригодном растворителе (например, в дихлорметане, хлороформе, тетрагидрофуране, бензоле или толуоле) в присутствии основания (гидрида натрия, пиридина, триэтиламина или карбоната калия) при -20°С или при нагревании в течение периода времени от нескольких минут до нескольких десятков часов, получая требуемое соединение, где L обозначает ОТf.
Когда D обозначает водород, взаимодействие с галогенирующим агентом (например, с хлором, бромом, йодом или N-бромсукцинимидом) осуществляют в пригодном растворителе (например, в уксусной кислоте, дихлорметане, хлороформе, четыреххлористом углероде, N,N-диметилформамиде или воде) при -20°С или при нагревании в течение периода времени от нескольких минут до нескольких десятков часов, получая требуемое соединение, где L обозначает галоген.
Когда D обозначает формил, его подвергают окислению с помощью стандартной реакции Байера-Виллигера, получая формилоксигруппу, которую затем гидролизуют, получая гидроксигруппу. После этого используют процедуру, аналогичную описанной выше, получая соединение, где L обозначает OTf.
Когда D обозначает нитрогруппу, ее восстанавливают до аминогруппы и подвергают реакции Зандмейера, получая соединение, где L обозначает галоген.
Способ получения соединения (I’’)
Соединение, представленное приведенной ниже формулой (I’’) (ниже в настоящем описании называется как соединение (I’’)), можно получать с помощью реакции Сузуки между соединением, представленным формулой (VI) (ниже в настоящем описании называется как соединение (VI)), и соединением, представленным формулой (IIа) (ниже в настоящем описании называется как соединение (IIа)), или путем реакции конденсации между соединением, представленным формулой (VII) (ниже в настоящем описании называется как соединение (VII)), и соединением, представленным формулой (VIII) (ниже в настоящем описании называется как соединение (VIII)):
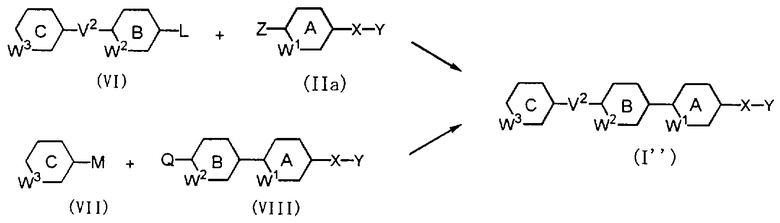
где один из М и Q обозначает гидрокси- или аминогруппу, а другой обозначает галоген, (низш.)алкилсульфонилокси-, арилсульфонилоксигруппу, (низш.)алкилсульфонил или арилсульфонил либо непосредственно, либо в качестве заместителя в метильной группе, или один обозначает литий или Mg(Hal), где Hal обозначает галоген, а другой обозначает карбоксигруппу, (низш.)алкоксикарбонил, карбамоил или формил, или один обозначает формил, а другой обозначает галогенированный метил, или один обозначает этинил, а другой обозначает галоген, и другие символы имеют указанные выше значения.
Условия, в которых подвергают взаимодействию соединение (VI) и соединение (IIа), являются аналогичными условиям, которые используются в способе получения соединения (I’).
При взаимодействии соединения (VII) и соединения (VIII), когда V2 в требуемом соединении обозначает -О-, -NH-, -ОСH2-, -СН2О- или -NHCH2-, один из заместителей М и Q обозначает гидрокси- или аминогруппу, а другой обозначает уходящую группу, такую как галоген, (низш.)алкилсульфонилокси-, арилсульфонилоксигруппа, (низш.)алкилсульфонил или арилсульфонил или метил, имеющий такую уходящую группу в качестве заместителя. Эти два соединения подвергают взаимодействию в пригодном растворителе (например, в бензоле, толуоле, ацетоне, ацетонитриле, N,N-диметилформамиде, диметилсульфоксиде, пиридине, метаноле или этаноле) в присутствии основания (например, гидрида натрия, пиридина, триэтиламина, карбоната калия, гидроксида натрия или гидроксида калия) необязательно в присутствии медного катализатора (порошка меди, CuCl или СuО) при 0°С или при нагревании в течение периода времени от нескольких минут до нескольких десятков часов, получая требуемое соединение.
При взаимодействии соединения (VII) и соединения (VIII), когда V2 в требуемом соединении обозначает -СО- или -СН(ОН)-, то один из заместителей М и Q обозначает литий или металлорганическое соединение, такое как Mg(Hal), где Hal обозначает галоген, а другой обозначает карбоксигруппу, (низш.)алкоксикарбонил, карбамоил или формил. Эти два соединения подвергают взаимодействию в пригодном растворителе (например, в диэтиловом эфире, тетрагидрофуране, диметоксиэтане или диоксане) при -78°С или при нагревании в течение периода времени от нескольких минут до нескольких часов, получая требуемое соединение.
Когда V2 в требуемом соединении обозначает -CH(ORg)-, где Rg обозначает (низш.)алкил, то получают соединение, где V2 обозначает -СН(ОН)-, и затем подвергают его алкилированию.
Требуемое соединение, где V2 обозначает -СО-, можно получать, подвергая взаимодействию соединение, где V2 обозначает -СН(ОН)-, с окислителем, таким как хромистый ангидрид или реактив Джонса, в пригодном для окислителя растворителе, таком как трет-бутиловый спирт или ацетон при 0°С или при нагревании в течение нескольких часов. Требуемое соединение, где V2 обозначает -СН(ОН)-, можно получать путем восстановления соединения, в котором V2 обозначает -СО-, в пригодном растворителе (например, в диэтиловом эфире, тетрагидрофуране, диметоксиэтане, диоксане, метаноле и этаноле) в присутствии борогидрида лития, алюмогидрида лития и т.п.
Когда V2 в требуемом соединении обозначает -СН=СН-, один из заместителей М и Q обозначает формил, а другой обозначает галогенированный метил (галоген может представлять собой, например, хлор, бром или йод). В этом случае требуемое соединение можно получать с помощью реакции Виттига (Organic Reaction, 1965, том 14, стр. 270).
Когда V2 в требуемом соединении обозначает -СН≡СН-, то один из заместителей М и Q обозначает этинил, а другой обозначает галоген (предпочтительно бром или йод), и синтез можно осуществлять с помощью реакции сочетания (см., например, в Synthesis, 1980, 627; Tetrahedron, 1982, 38, 631) с использованием обычно применяемого палладиевого катализатора.
Другие заместители в кольце А, кольце В и кольце С в соединениях (VI), (IIа), (VII) и (VIII) и -X-Y представляют собой любые группы, которые не оказывают неблагоприятного влияния на взаимодействие L и Z в условиях реакции Сузуки или на конденсацию М и Q. Даже тогда, когда любой из заместителей в соединениях (VI) и (IIа), участвующих в реакции, обозначает галоген, описанная выше реакция может протекать достаточно успешно, если способность к взаимодействию заместителей L и Z является относительно более высокой. Хотя осуществление описанной выше реакции оказывается возможным даже тогда, когда любой из заместителей обозначает гидроксигруппу, в этом случае предпочтительно осуществлять реакцию после введения защитной группы, которую затем удаляют обычным методом.
Соединение (VI) в описанной выше реакционной схеме может представлять собой известное соединение или его можно синтезировать из соединения, представленного формулой (X) (ниже в настоящем описании называется как соединение (X)), которое синтезируют способом, описанным ниже:
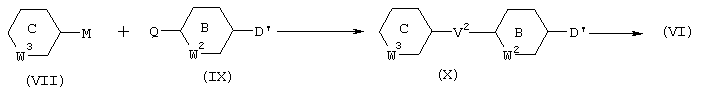
где D’ обозначает группу, которая не оказывает неблагоприятного влияния на конденсацию между М и Q, и если соединение, представленное формулой (IX), является симметричным соединением, то она может представлять собой группу, идентичную Q, а другие символы имеют указанные выше значения.
Если соединение (IX) не является симметричным соединением, то D' предпочтительно обозначает группу, которая не оказывает существенного неблагоприятного влияния на конденсацию между М и Q и которая может быть легко превращена в L. Например, можно использовать водород, формил или защищенную гидрокси- или нитрогруппу. Защитная группа для гидроксигруппы может, например, представлять собой бензил, трет-бутилдиметилсилил и метоксиметил. Метод превращения D’ в L аналогичен методу, описанному выше для превращения D в L. Остальные условия аналогичны условиям взаимодействия соединения (VII) и соединения (VIII).
Соединение (VIII) может представлять собой известное соединение или оно может быть получено известным методом или соединение синтезируют стандартным методом из описанного выше соединение (Vb).
Соединение, представленное формулой (I’’’):
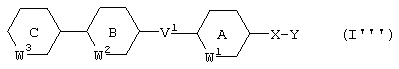
где каждый символ имеет указанные выше значения, также может быть синтезировано аналогично методу синтеза соединения (I’’).
Для получения соединений формулы (Iс) могут использоваться приведенные ниже в качестве примера методы.
(Метод А)
Например, соединение, представленное формулой (Iс’) (ниже в настоящем описании называется как соединение (Iс’)), где Ra и Rb каждый независимо друг от друга обозначает водород, необязательно замещенный (низш.)алкил, необязательно замещенный (низш.)алкенил, необязательно замещенный арил, необязательно замещенный циклоалкил, необязательно замещенный ацил или необязательно замещенный (низш.)алкоксикарбонил, или они вместе образуют -(CReRF)r-, может быть получено из соединения, представленного формулой (XI) (ниже в настоящем описании называется как соединение (XI)), и соединения представленного формулой (XII) (ниже в настоящем описании называется как соединение (XII)):
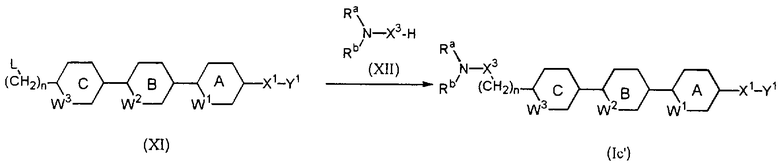
где заместитель L обозначает уходящую группу, такую как галоген, (низш.)алкилсульфонил, арилсульфонил, (низш.)алкилсульфонилокси- или арилсульфонилоксигруппа, и другие символы имеют указанные выше значения.
Соединения (XI) и (XII) подвергают взаимодействию в пригодном растворителе (например, в бензоле, толуоле, ацетоне, ацетонитриле, тетрагидрофуране, N,N-диметилформамиде, диметилсульфоксиде, пиридине, метаноле или этаноле) необязательно в присутствии основания (например, гидрида натрия, трет-бутоксида калия, пиридина, триэтиламина, карбоната калия, гидроксида натрия или гидроксида калия) при 0°С или при нагревании в течение периода времени от нескольких минут до нескольких десятков часов, получая соединение (Iс’).
Соединение (Iс’’), где Ra и Rb вместе образуют RcRdC=, получают из RcRdC=N-X3 и соединения (XI) согласно описанному выше методу или из соединения (Iс’), где Ra и Rb обозначают атомы водорода, полученного из соединения (XI), и соединения, представленного формулой (XIII) (ниже в настоящем описании называется как соединение (XIII)):
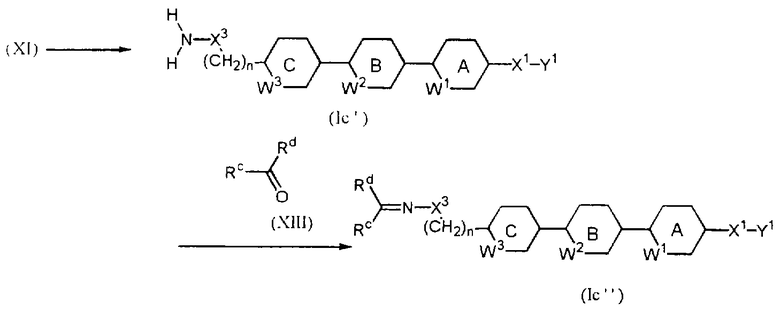
где каждый символ имеет указанные выше значения.
Сначала соединение (XI) подвергают взаимодействию с гидразином в пригодном растворителе (например, в толуоле, тетрагидрофуране, N,N-диметилформамиде, диметилсульфоксиде, пиридине, метаноле или этаноле) или без использования какого-либо растворителя, получая соединение (Ic’, X3=NH), или применяют метод с использованием N-гидроксифталимида, описанный в Journal of Chemical Society, 1926, 2348, или метод с использованием бензогидроксамовой кислоты, описанный в Journal of Chemical Society, 1927, 874, получая соединение (Iс’, Х3=O). Полученное таким образом соединение подвергают дегидратирующей конденсации с карбонильным производным (XIII), таким как кетон или альдегид, необязательно в присутствии кислотного катализатора (соляной кислоты, уксусной кислоты, трифторуксусной кислоты, (низш.)алкансульфоновой кислоты, арилсульфоновой кислоты и т.п.), получая требуемое соединение (Ic’’).
Когда один из Rc и Rd в соединении (Ic’’) обозначает (низш.)алкоксигруппу, осуществляют взаимодействие с карбонильным производным (RcC(=O)Rd) в пригодном растворителе (например, в толуоле, тетрагидрофуране, диоксане или дихлорметане) в присутствии кислоты (соляной кислоты, уксусной кислоты, перхлорной кислоты и т.п.), превращая тем самым продукт в требуемое соединение, имеющее другие Rc и Rd.
Соединение (Iс’), где Ra и Rb обозначают атомы водорода, можно также синтезировать из соединения, представленного формулой (ХI’) (ниже в настоящем описании называется как (XI’)):
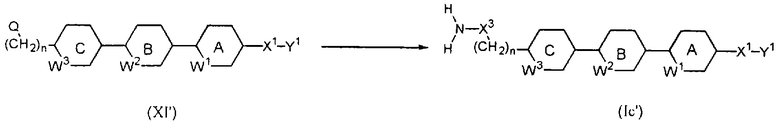
где Q обозначает NH2 или группу, которая не оказывает неблагоприятного влияния на реакцию Сузуки и которая может быть превращена в заместитель L обычным методом, а другие символы имеют указанные выше значения.
Например, соединение (ХI’, Q=OH) превращают в алкоксид или феноксид с использованием пригодного основания (например, гидрида натрия, трет-бутоксида калия, карбоната калия, гидроксида натрия и гидроксида калия) и затем подвергают взаимодействию с хлорамином или O-арилсульфонилгидроксиламином (Journal of Organic Chemistry, 1973 (38) 1239-1241) или соединение (ХI’, Q=NH2) подвергают взаимодействию с хлорамином или гидроксиламин-O-сульфоновой кислотой (Journal of Organic Chemistry, 1949 (14)813).
(Метод Б)
Соединение (Iс’) можно также получать путем взаимодействия соединения, представленного формулой (XIV) (ниже в настоящем описании называется как соединение (XIV)), с соединением, представленным формулой (XV) (ниже в настоящем описании называется как соединение (XV)):
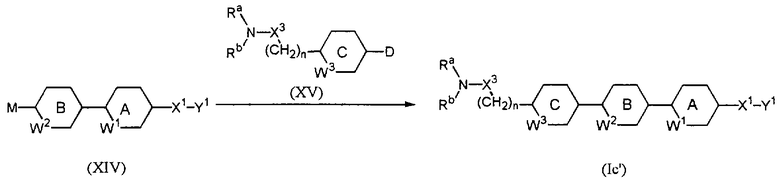
где один из М и D обозначает дигидроксиборил, ди(низш.)алкилборил или ди(низш.)алкоксиборил, а другой обозначает галоген или -OSO2(CqF2q+1), где q обозначает целое число от 0 до 4, а другие символы имеют указанные выше значения.
Соединение (XIV) и соединение (XV) подвергают взаимодействию в смеси пригодных растворителей (например, бензола, толуола, N,N-диметилформамида, диметоксиэтана, тетрагидрофурана, диоксана, этанола или метанола) с водой или в безводной системе в присутствии палладиевого катализатора (например, Рd(РРh3)4, PdCl2(PPh3)2, PdCl2, Pd(OAc)2 или PdCl2(CH3CN)2, предпочтительно Pd(PPh3)4) в основных условиях (в присутствии основания, такого как К3РO4, NaHCO3, NaOEt, Na2CO3, Et3N, Ba(OH)2, Сs2СО3, CsF, NaOH или Ag2CO3) при комнатной температуре или при нагревании в течение периода времени от нескольких десятков минут до нескольких десятков часов, получая соединение (Iс’).
Соединение (XV) может представлять собой известное соединение или его можно получать методом, описанным выше для получения соединений (Iс’) и (Iс’’).
Один из заместителей М и D представляет собой борильную группу, которая может применяться в реакции Сузуки, предпочтительно дигидроксиборил. Другой представляет собой уходящую группу, которая может применяться в реакции Сузуки, такую как галоген или - OSO2(CqF2q+1), где q обозначает целое число от 0 до 4. Особенно предпочтительными группами являются галоген и трифторметансульфонилоксигруппа (ниже в настоящем описании сокращенно называется как OTf), при этом наиболее предпочтительными являются бром, йод и ОТf.
Другие заместители в кольце А, кольце В и кольце С в соединениях (XIV) и (XV) и –X1-Y1 представляют собой любые группы, которые не оказывают неблагоприятного влияния на реакцию Сузуки, включая указанные выше группы, за исключением галогена и - OSO2(CqF2q+1), где q обозначает целое число от 0 до 4, при этом даже в том случае, когда любой из заместителей в кольцах А, В и С обозначает галоген, описанная выше реакция может протекать довольно успешно, если способность к взаимодействию заместителей М и D является относительно более высокими.
Соединения (XI) и (ХI’) в приведенной выше реакционной схеме могут представлять собой известные соединения или они могут быть синтезированы согласно известному методу или описанному ниже методу:
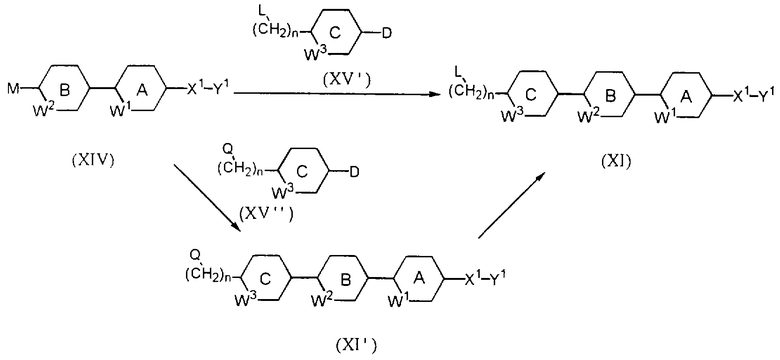
где заместитель Q обозначает NH2 или группу, которая не оказывает неблагоприятного влияния на реакцию Сузуки и которая может быть превращена обычным методом в заместитель L, а другие символы имеют указанные выше значения.
Используя соединение (XIV), которое является известным соединением или получают методом, описанным в WO 98/04508, и соединение (XV), которое является известным соединением или которое получают из известного соединения стандартным методом, получают соединение (XI) аналогично описанным выше стадиям реакции Сузуки. Если заместитель L оказывает неблагоприятное влияние на реакцию Сузуки, то сначала используют соединение (XV’’), получая соединение (XI’’), после чего заместитель Q превращают в заместитель L.
Например, когда заместитель Q обозначает гидроксигруппу, то его превращение в галоген может быть осуществлено в стандартных условиях, или требуемое соединение может быть получено с использованием пригодного сульфонилирующего агента (например, метансульфонилхлорида, паратолуолсульфонилхлорида или трифторметансульфонового ангидрида). В том случае, когда заместитель Q обозначает гидроксигруппу, которая была ранее защищена пригодной защитной группой, такой как бензил, трет-бутилдиметилсилил или метоксиметил, защитные группы удаляют стандартным методом с получением гидроксигруппы, и осуществляют последующую процедуру согласно описанному выше методу, получая требуемое соединение.
В том случае, когда заместитель Q обозначает (низш.)алкилтио- или необязательно замещенную арилтиогруппу, каждая из них также может быть превращена в соответствующую сульфоновую форму с помощью пригодного окислителя (например, перекиси водорода, перуксусной кислоты, мета-хлорпербензойной кислоты, оксона моноперсульфата).
Соединение (XIV), используемое в описанной выше реакции, может представлять собой известное соединение или оно может быть получено из известного соединения с помощью реакции Сузуки.
Хотя соединение (I) наиболее эффективно и просто синтезируют с помощью описанной выше реакции Сузуки, в приведенной выше схеме вместо борильной группы можно также использовать кремний, цинк или олово, как это описано в WO 98/04508.
В том случае, когда соединение имеет заместитель, который оказывает влияние на описанную выше реакцию, то такая группа может быть сначала защищена пригодной защитной группой, которую затем удаляют на соответствующей стадии стандартным методом. Например, если гидроксигруппа влияет на реакцию, то ее защищают, например, метоксиметильной, метансульфонильной, бензильной, трифторметансульфонильной или трет-бутилдиметилсилильной группой, которую удаляют на соответствующей стадии.
Например, когда гидроксигруппу защищают метансульфонильной группой, то осуществляют взаимодействие с метансульфонилхлоридом в растворителе, таком как дихлорметан, хлороформ или четыреххлористый углерод, в присутствии основания, такого как триэтиламин или пиридин, при охлаждении на льду или при комнатной температуре в течение нескольких часов. Удаление защитной группы можно осуществлять в растворителе, таком как диметилсульфоксид, N,N-диметилформамид, тетрагидрофуран, диоксан и диметоксиэтан, с помощью 1-4 н. гидроксида натрия, гидроксида калия, его водного раствора, метоксида натрия или бромида этилмагния при комнатной температуре или при нагревании в течение периода времени от нескольких десятков минут до нескольких часов.
Когда для защиты гидроксигруппы используют метоксиметил, то взаимодействие с метилхлорметиловым эфиром осуществляют в растворителе, таком как тетрагидрофуран, диоксан и диметоксиэтан, в присутствии гидрида натрия или диизопропилэтиламина, осуществляя при этом защиту гидроксигруппы. Удаление защитной группы можно осуществлять обычным методом в растворителе, таком как метанол, тетрагидрофуран и уксусная кислота, с использованием соляной кислоты или серной кислоты.
Когда в качестве защитной группы используют трет-бутилдиметилсилил, то осуществляют взаимодействие с трет-бутилдиметилсилилхлоридом или трет-бутилдиметилсилилтрифлатом в растворителе, таком как N,N-диметилформамид, ацетонитрил, тетрагидрофуран и дихлорметан, в присутствии имидазола, триэтиламина или 2,6-лутидина. Удаление защитной группы осуществляют путем взаимодействия с фторидом тетрабутиламмония в растворителе, таком как тетрагидрофуран.
Соединение, полученное согласно описанному выше методу, может быть затем превращено в пролекарство.
Понятие "пролекарство" обозначает любое соединение, которое может легко превращаться in vivo в активное соединение по изобретению, при этом пролекарство может быть получено стандартным методом. Метод отбора и получения пригодного производного в виде пролекарства описан, например, в Design of Prodrugs, Elsevier, Amsterdam, 1985. Согласно этому методу группу, обычно используемую для получения пролекарства, вводят в карбокси-, гидрокси- или аминогруппу, связанную с соединением по изобретению в любом положении.
Например, когда в качестве заместителя в кольце А или в кольце С присутствует гидроксигруппа, то можно, например, вводить такие группы, как –СОСН2СН2СООН, -СОСН=СНСООН, -СОСH2SО3Н, -РО3Н2, -СОСН3NМе и -СО-Ру (где Ру обозначает пиридил).
Когда в качестве заместителя в кольце А или в кольце С присутствует аминогруппа, то можно вводить такие группы, как –СООСRhRiОСОСН2Rj (где Rh и Ri каждый независимо друг от друга обозначает водород или (низш.)алкил, Rj обозначает Н, -ОН, -CONHRk, -OCONHRk, -(NHCOCR1Rm)uNHCOCH3, -(NHCOCR1Rm)uNHCOC2H5, -CSNH2, -(OCH2CH2)tOH, -ОСН3, -(ОСН2СН2)tОСН3, -СОСН3, -СОС2Н5, -ОСОСН3, -ОСОС2Н5, -NHOH, -NНСОNН2, NHCSNH2, -NНSО2СН3, -N(SO2CH3)2, -SO2NH2, -SOMe, -SO2СН3, -OCH2CONH2, -ОСН2СОN(СН3)2, -SO2N(СН3)2, -РО(ОСН3)2, -NHCSNHC2H5Et, -CH=NNHCONH2, -CH=NNHCSNH2, -СН=NNНSO2СН3, триазолил, тетразолил и т.п., Rk Rl и Rm каждый обозначает водород или (низш.)алкил, t равно 1 или 2, u обозначает целое число от 0 до 2), -СООСН(Ме)ОСОСМе3, -СООСН2OСО(СН2)14Ме, -СООСН2OСО-Pyr, -СН2NНСО-С6Н4-орто-ОСН2OАс и т.п., где Pyr обозначает пиридил, Ас обозначает ацетил.
Когда для получения пролекарства в аминогруппу, присутствующую в любом положении в соединении по изобретению, вводят указанный выше замещенный ацилоксикарбонил (-СООСRhRiОСОСН2Rj), то аминогруппу, присутствующую в любом положении соединения по изобретению, подвергают α-галоалкоксикарбонилированию и взаимодействию с пригодной карбоновой кислотой в соответствующих условиях, получая пролекарство.
Метод синтеза такого ацилоксиалкилкарбамата описан, например, в WO 96/18605.
Как правило содержащее аминогруппу соединение по изобретению и α-галоалкилхлорформиат подвергают взаимодействию в инертном растворителе (в диэтиловом эфире, тетрагидрофуране, 1,4-диоксане, этилацетате, толуоле и т.п.) в присутствии основания (пиридина, триэтиламина, N-метилморфолина и т.п.) при температуре от 0°С до комнатной температуры, получая галоалкоксикарбаматное производное. Затем полученное таким образом соединение подвергают взаимодействию в растворителе (в N,N-диметилформамиде, N,N-диметилацетамиде, диметилсульфоксиде, сульфолане и т.п.) с солью замещенной карбоновой кислоты (например, с солью щелочного металла, солью щелочноземельного металла, солью серебра, солью ртути и т.п.) при комнатной температуре или при нагревании в течение периода времени от нескольких часов до нескольких дней, получая пролекарство.
Заместитель, который может оказывать влияние на образование пролекарства, если он присутствует, предварительно может быть защищен с помощью соответствующей защитной группы, которую затем удаляют стандартным методом на соответствующей стадии.
В контексте настоящего описания понятие "ингибитор Th2-дифференцировки" относится к фармацевтической композиции, которая обладает способностью ингибировать дифференцировку Th0-клеток в Тh2-клетки, т.е. к фармацевтической композиции, предназначенной для лечения и/или предупреждения заболеваний, индуцируемых Тh2-клетками или цитокинами, продуцируемыми Тh2-клетками.
Ингибиторы Тh2-дифференцировки по изобретению вызывают уменьшение популяции Тh2-клеток, приводя к уменьшению уровня цитокинов, которые продуцируются Тh2-клетками, оказывая тем самым ингибирующее действие на активацию В-клеток и производство антител, которое заключается в следующем.
Существует мнение о том, что активация В-клеток, находящихся в покое, требует наличия контакта между Тh2-клетками и В-клетками, а также стимуляции цитокинами, продуцируемыми Тh2-клетками, и ингибиторы Th2-дифференцировки по изобретению оказывают ингибирующее воздействие также и на активацию B-клеток самими Тh2-клетками. Вследствие этого оказывается возможным осуществлять более эффективное лечение и предупреждение аллергических заболеваний и аутоиммунных заболеваний по сравнению с использованием обычных антиаллергических агентов.
Известно, что определенные аллергические заболевания, такие как астма и воспаление дыхательных путей, индуцируются самими Тh2-клетками, и ингибиторы Тh2-дифференцировки по изобретению также обладают эффективностью в отношении лечения заболеваний, для которых, например, ожидается, что применение только ингибиторов производства IgE не является эффективным.
Ингибиторы Тh2-дифференцировки по изобретению не ингибируют дифференцировку Th0-клеток в Тh1-клетки, обладая тем самым высокой избирательностью в отношении Тh2-клеток. Вследствие этого они не оказывают ингибирующего воздействия на защиту от инфекции, вызываемой вирусом или внутриклеточным паразитом, в которой, как считается, участвуют Тh1-клетки (например, в отношении туберкулеза, лепры, заболеваний, вызываемых микроорганизмами семейства Chlamydiaceae), однако эффективно ингибируют прогрессирование синдрома приобретенного иммунодефицита (СПИД), представляя собой таким образом эффективное лекарственное средство, обладающее слабыми побочными действиями.
Ингибиторы Тh2-дифференцировки по изобретению обладают эффективностью в отношении иммунных заболеваний, классифицируемых как Тh2-тип иммунных заболеваний. Например, их предпочтительно используют в качестве терапевтических и/или профилактических агентов в отношении иммунных заболеваний, связанных с трансплантацией (хроническое заболевание “трансплантат против хозяина” (РТПХ)), аутоиммунных заболеваний (в частности, неспецифических для органа аутоиммунных заболеваний) и аллергических заболеваний Тh2-типа. Типичными примерами заболеваний являются неспецифический язвенный колит, системная красная волчанка, тяжелая псевдопаралитическая миастения, системная прогрессирующая склеродерма, ревматоидный артрит, интерстициальный цистит, болезнь Хашимото, базедова болезнь, аутоиммунная гемолитическая анемия, идиопатическая тромбоцитопеническая пурпура, синдром Гудпасчера, атопический гастрит, пернициозная анемия, болезнь Аддисона, пузырьчатка, пемфигоид, лентрикулярный увеит, симпатическая офтальмия, первичный билиарный цирроз, активный хронический гепатит, синдром Шегрена, полимиозит, дерматомиозит, полиартериит нодозный, ревматическая лихорадка, гломерулонефрит (люпус-нефрит, IgA-нефропатия и т.п.), аллергический энцефалит, атопические аллергические заболевания (например, бронхиальная астма, аллергический ринит, аллергический дерматит, аллергический конъюнктивит, поллиноз, крапивница, аллергия на пищу и т.п.), синдром Омена, хронический двусторонний конъюнктивит и синдром гиперэозинофилии. Наибольшая эффективность достигается прежде всего в отношении неспецифических для органа аутоиммунных заболеваний, таких как иммунные заболевания, связанные с трансплантацией (хроническое заболевание РТПХ), неспецифический язвенный колит, системная красная волчанка, тяжелая псевдопаралитическая миастения, системная прогрессирующая склеродерма, ревматоидный артрит, люпус-нефрит, интерстициальный цистит и т.п.
Введение ингибиторов Тh2-дифференцировки можно осуществлять пероральным и парентеральным путем. Пероральное введение можно осуществлять стандартным образом с использованием обычно применяемой композиции, например, в виде таблетки, гранулы, порошка, капсулы, пилюли, раствора, сиропа, композиций для буккального или сублингвального применения. Когда введение осуществляют парентеральным путем, то предпочтительно применяют обычно используемую композицию, такую как внутримышечная или внутривенная инъецируемая композиция, суппозиторий, композиции для чрезкожного введения и композиции, предназначенные для ингаляции. Особенно предпочтительным является пероральное введение.
Для получения фармацевтической композиции эффективное количество соединения по изобретению при необходимости можно смешивать с различными фармацевтическими добавками, пригодными для приготовления конкретной дозируемой формы, такими как эксципиент, связующее вещество, замасливатель, разрыхлитель, разбавитель и т.п. Композицию для инъекций можно приготавливать с использованием носителя, пригодного для одновременной стерилизации.
Типичными примерами могут служить лактоза, сахар, глюкоза, крахмал, карбонат кальция или кристаллическая целлюлоза, которые применяют в качестве эксципиента, метилцеллюлоза, карбоксиметилцеллюлоза, гидроксипропилцеллюлоза, желатин или поливинилпирролидон, которые применяют в качестве связующего вещества, карбоксиметилцеллюлоза, карбоксиметилцеллюлоза натрия, крахмал, альгинат натрия, агаровый порошок или лаурилсульфат натрия, которые применяют в качестве разрыхлителя, тальк, стеарат магния или макрогол, которые применяют в качестве замасливателя. В качестве основы для суппозитория можно использовать, например, масло какао, макрогол или метилцеллюлозу. Предназначенную для инъекции жидкую композицию в виде эмульсии или суспензии можно приготавливать с использованием обычно применяемых солюбилизирующего агента, суспендирующего агента, эмульгатора, стабилизатора, консерванта, агента для придания изотоничности и других добавок, а композиция для перорального введения может содержать подслащивающие вещества и корригенты.
Ингибиторы Тh2-дифференцировки по изобретению могут вводиться индивидуально или при необходимости в сочетании с другими антиаллергическими агентами. Агент, применяемый в такой комбинации, может представлять собой, например, стероид, известный антиаллергический агент или бронхолитическое средство.
Хотя дозы ингибиторов Тh2-дифференцировки по изобретению предпочтительно регулируют с учетом возраста пациента, веса тела, типа и серьезности заболеваний, а также пути введения, обычно она составляет для взрослых людей от 0,05 до 100 мг/кг/день, предпочтительно от 0,1 до 10 мг/кг/день. Хотя дозы, вводимые парентерально, сильно варьируются в зависимости от пути введения, обычно доза составляет от 0,0001 до 10 мг/кг/день, предпочтительно от 0,001 до 1 мг/кг/день. Такую дозу можно разделять на несколько частей, которые вводят в течение дня.
Ниже изобретение проиллюстрировано на примерах, которые не направлены на ограничение его объема.
Примеры
Эталонный пример 1. Синтез соединения (1-6)
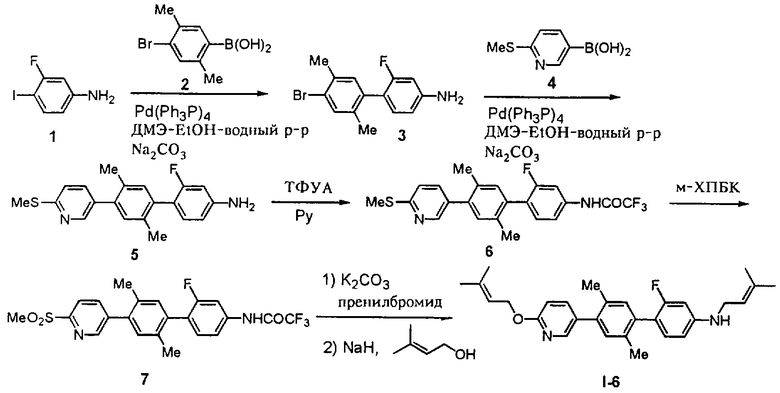
(Стадия 1)
К раствору соединения (1) (23,7 г, 0,1 моля) в смеси диметоксиэтан (300 мл) - этанол (150 мл) добавляли водный раствор (150 мл) бороновой кислоты (2) (22,88 г, 0,1 моля) и карбоната натрия (31,8 г, 0,3 моля) и реакционную смесь подвергали деаэрации. Добавляли тетракис(трифенилфосфин)палладий (3,47 г, 3 моля) и смесь выдерживали при температуре дефлегмации в атмосфере азота в течение 2 ч, после чего разбавляли водой и экстрагировали этилацетатом. Экстракт промывали насыщенным соляным раствором, сушили, концентрировали и образовавшийся остаток кристаллизовали из гексана, получая соединение (3) (24,92 г, выход: 84%).
(Стадия 2)
Аналогично методу, описанному для стадии 1, соединение (3) (20,0 г, 68,0 молей) и бороновую кислоту (4) (14,94 г, 88,3 моля) подвергали взаимодействию в течение 18 ч и полученный экстракцией остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат=2:1), получая соединение (19,24 г, выход: 84%).
(Стадия 3)
К раствору соединения (5) (21,15 г, 62,5 моля) в дихлорметане (200 мл) добавляли при охлаждении на льду пиридин (6,6 мл, 81,2 моля), а затем трифторуксусный ангидрид (10,6 мл, 75,0 молей) и смесь перемешивали при комнатной температуре в течение 1 ч Реакционную смесь разбавляли этилацетатом и затем промывали последовательно водой, 1н. соляной кислотой и 5%-ным водным раствором бикарбоната натрия, сушили и концентрировали, получая соединение (6) (22,80 г; выход: 84%).
(Стадия 4)
К раствору соединения (6) (14,0 г, 32,2 моля) в дихлорметане (300 мл) добавляли при охлаждении на льду мета-хлорпербензойную кислоту (14,46 г, 83,8 моля) и смесь перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь объединяли с водным раствором тиосульфата натрия, экстрагировали этилацетатом, промывали дважды насыщенным водным раствором бикарбоната натрия, сушили и концентрировали. Остаток промывали гексаном, получая соединение (7) (12,97 г; выход 86%).
(Стадия 5)
Рствор соединения (7) (15,0 г, 32,2 моля) в ДМФ (65 мл) объединяли с карбонатом калия (6,67 г, 48,2 моля), затем добавляли пренилбромид (4,81 мл, 41,8 моля), и после этого перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь разбавляли этилацетатом, промывали последовательно водой и насыщенным соляным раствором, сушили и концентрировали, получая остаток, который растворяли в тетрагидрофуране (150 мл). Добавляли при охлаждении на льду реакционную смесь, полученную путем добавления гидрида натрия (60%-ный в минеральном масле, 3,85 г, 96,5 моля) к раствору пренола (9,8 мл, 96,5 моля) в тетрагидрофуране (150 мл), и смесь перемешивали еще в течение 2 ч при этой же температуре. Реакционную смесь разбавляли этилацетатом, промывали последовательно водой и насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 7:1), получая соединение (1-6) (12,5 г; выход: 87%).
tпл 87-88°C;
1Н-ЯМР (СDСl3) δ Н 1,74 (s, 3Н), 1,78 (s, 3H), 1,79 (s, 3Н), 1,80 (s, 3H), 2,22 (s, 3Н), 2,26 (s, 3Н), 3,71 (d, J=6,9 Гц, 2Н), 4,87 (d, J=7,2 Гц, 2Н), 5,32-5,37 (m, 1H), 5,55-5,60 (m, 1H), 6,35-6,47 (m, 2H), 6,81 (dd, J=0,6, 8,4 Гц, 1Н), 7,02-7,13 (m, 3Н), 7,59 (dd, J=2,4, 8,4 Гц, 1H), 8,16 (dd, J=0,9, 5,7 Гц, 1H) част./млн. ИК (Nujol): 3330, 2923, 2853, 1627, 1606, 1564, 1527, 1481, 1471, 1395, 1376, 1357, 1337, 1284, 1240, 1178, 1116, 990 см-1.
Эталонный пример 2. Синтез соединения (1-134)
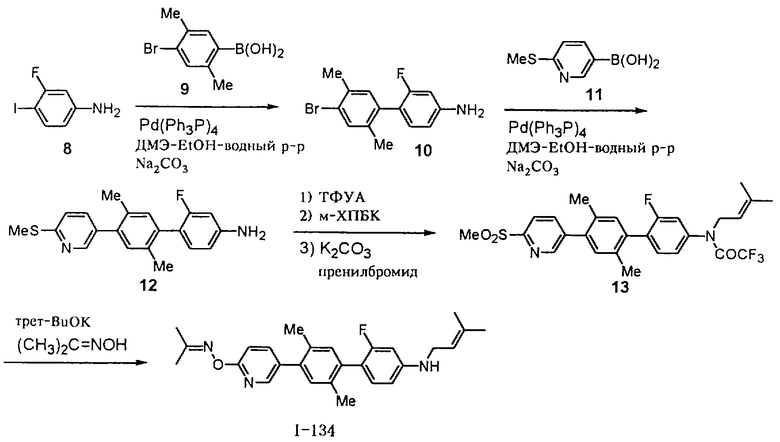
(Стадия 1)
К раствору соединения (8) (23,7 г, 0,1 моля, Journal of Organic Chemistry, 1961 (26), 3351-3356) в смеси диметоксиэтан (300 мл) - этанол (150 мл) добавляли бороновую кислоту (9) (22,88 г, 0,1 моля) и водный раствор (150 мл) карбоната натрия (31,8 г, 0,3 моля), после чего реакционную смесь подвергали деаэрации. Добавляли тетракис(трифенилфосфин)палладий (3,47 г, 3 моля) и смесь выдерживали при температуре дефлегмации в атмосфере азота в течение 2 ч, затем разбавляли водой и экстрагировали этилацетатом. Экстракт промывали насыщенным соляным раствором, сушили и концентрировали и образовавшийся остаток кристаллизовали из гексана, получая соединение (10) (24,92 г, выход: 84%).
(Стадия 2)
Аналогично методу, описанному для стадии 1, из соединения (10) (1,47 г, 5 молей) и бороновой кислоты (11) (1,01 г, 6 молей) получали соединение (12) (1,56 г; выход: 92%).
(Стадия 3)
К раствору соединения (12) (1,56 г, 4,62 моля) в дихлорметане (5 мл) добавляли при охлаждении на льду пиридин (0,56 мл, 6,92 моля), а затем трифторуксусный ангидрил (0,78 мл, 5,54 моля) и смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь разбавляли этилацетатом и затем промывали последовательно водой, 5%-ным водным раствором бикарбоната натрия и насыщенным соляным раствором, после чего сушили и концентрировали. Остаток, растворенный в дихлорметане (16 мл), обрабатывали при охлаждении на льду метахлорпербензойной кислотой (2,0 г, 11,6 моля) и перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь обрабатывали водным раствором тиосульфата натрия и экстрагировали хлороформом, промывали дважды 5%-ным водным раствором бикарбоната натрия, сушили и затем концентрировали. Остаток растворяли в N,N-диметилформамиде (8 мл), объединяли с карбонатом калия (720 мг, 5,21 моля), а затем с пренилбромидом (0,52 мл, 4,34 моля), и перемешивали при комнатной температуре в течение 14 ч. Реакционную смесь разбавляли этилацетатом, промывали последовательно водой и насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат =2:1), получая соединение (13) (1,71 г; выход: 69%).
(Стадия 4)
К раствору ацетоксима (137 мг, 1,87 моля) в N,N-диметилформамиде (3 мл) добавляли гидрид натрия (60%-ный в минеральном масле, 137 мг, 1,87 моля) и смесь перемешивали при комнатной температуре в течение 1 ч, после чего добавляли еще одну порцию соединения (13) (250 мг, 0,468 моля). Смесь перемешивали при комнатной температуре в течение 14 ч, разбавляли этилацетатом, промывали последовательно 5%-ным водным раствором лимонной кислоты и насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан: этилацетат = 7:3), получая соединение (1-134) (126 мг; выход: 62%).
tпл 135-137°C;
1Н-ЯМР (СDСl3) δ 1,74 (s, 3Н), 1,78 (s, 3H), 2,09 (s, 3H), 2,16 (s, 3Н), 2,22 (s, 3Н), 2,26 (s, 3Н), 3,72 (d, J=6,6 Гц, 2Н), 3,90 (br s, 1H), 5,35 (m, 1H), 6,39 (dd, J=2,4, 12,3 Гц, 1H), 6,46 (dd, J=2,4, 8,4 Гц, 1H), 7,06 (t, J=8,4 Гц, 1H), 7,12 (s, 1H), 7,13 (s, 1H), 7,23 (dd, J=0,6, 8,7 Гц, 1H), 7,70 (dd, J=2,4, 8,7 Гц, 1H), 8,28 (dd, J=0,6, 2,4 Гц, 1Н) част./млн.
Эталонный пример 3. Синтез соединения (9)
Суспензию 1,4-дибром-2,5-диметилбензола (154 г, 583 моля) в тетрагидрофуране (1,3 л) охлаждали до -78°С и затем по каплям в течение 30 мин добавляли 1,53 М раствор бутиллития в гексане (400 мл, 612 молей). После перемешивания реакционной смеси при этой же температуре в течение еще 1 ч добавляли в виде одной порции триизопропилборат (170 мл, 734 моля) и удаляли охлаждающую среду, давая смеси нагреться при перемешивании в течение 1 ч. После добавления воды (300 мл) и 1 н. соляной кислоты (650 мл) смесь экстрагировали этилацетатом и экстракт промывали водой и насыщенным соляным раствором, сушили и концентрировали. Кристаллический остаток промывали гексаном и фильтровали, получая соединение (9) (1 15 г; выход 86%).
Эталонный пример 4. Синтез соединения (11)
Раствор, содержащий 1,53М раствор бутиллития в гексане (500 мл, 765 молей) в тетрагидрофуране (1,28 л), охлаждали до -78°С и по каплям в течение 40 мин добавляли раствор 5-бром-2-метилтиопиридина (142 г, 695 молей) в тетрагидрофуране (400 мл). После перемешивания реакционной смеси при этой же температуре в течение еще 30 мин по каплям в течение 30 мин добавляли триизопропилборат (195 мл, 834 моля). Охлаждающую среду удаляли и смеси давали нагреться при перемешивании в течение 30 мин. После добавления воды (320 мл) смесь концентрировали при пониженном давлении и остаток еще раз разбавляли водой (710 мл) и изопропиловым эфиром (210 мл). Реакционную смесь перемешивали при комнатной температуре, добавляя по каплям 3 н. соляную кислоту (675 мл), осадившийся кристаллический продукт фильтровали, промывали водой и изопропиловым эфиром и сушили, получая соединение (11) (111 г; выход: 95%).
tпл 151-154°C.
Аналитически рассчитано для C6H8BNO2S: С, 42,64; Н, 4,77; N, 8,29; S, 18,97. Обнаружено: С, 42,56; Н, 4,88; N, 8,14; S, 18,79.
1H-NMR (ДМСО-d6) δ 2,51 (s, 3H), 7,25 (dd, J=0,9, 8,1 Гц, 1Н), 7,93 (dd, J=2,1, 8,1 Гц, 1 Н), 8,73 (dd, J=0,9, 2,1 Гц, 1 Н) част./млн.
Эталонный пример 5. Синтез соединения (I-179)
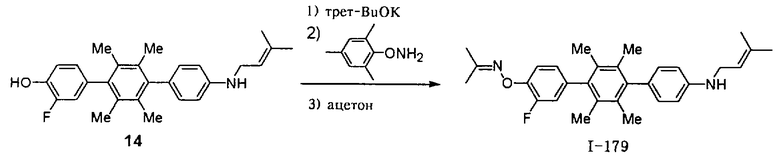
Раствор соединения (14) (261 мг, 0,65 моля), который получали согласно методу, описанному в WO 98/04508, в метаноле (4 мл) охлаждали до 0°С, обрабатывали третбутоксидом калия (75 мг, 0,65 моля) и перемешивали в течение 15 мин. После отгонки растворителя при пониженном даывлении и последующей сушки остаток растворяли в N,N-диметилформамиде (2,5 мл). Добавляли O-мезитиленсульфонилгидроксиламин (Journal of Organic Chemistry, 1973 (38) 1239-1241) (251 мг, 1,16 моля) и реакционную смесь перемешивали в течение 1 ч, сливали на воду и экстрагировали смесью этиловый эфир:этилацетат (1:1). Экстракт промывали водой и насыщенным соляным раствором, сушили, концентрировали, получая остаток, который растворяли в метаноле (3 мл), объединяли с ацетоном (0,48 мл, 6,5 моля) и перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь концентрировали и остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 10:1), получая соединение (I-179) (118 мг; выход: 40%).
tпл 129-130°C;
1Н-ЯМР (СDС13) δ 1,74 (s, 3H), 1,78 (s, 3H), 1,96 (s, 6H), 1,98 (s, 6H), 2,06 (s, 3H), 2,15 (s, 3H), 3,60 (br s, 1H), 3,74 (d, J=6,6 Гц, 2Н), 5,40 (m, 1H), 6,69 (d, J=8,7 Гц, 2H), 6,87-6,98 (m, 4H), 7,48 (t, J=8,4 Гц, 1H) част./млн.
Эталонный пример 6. Синтез соединения (I-235)
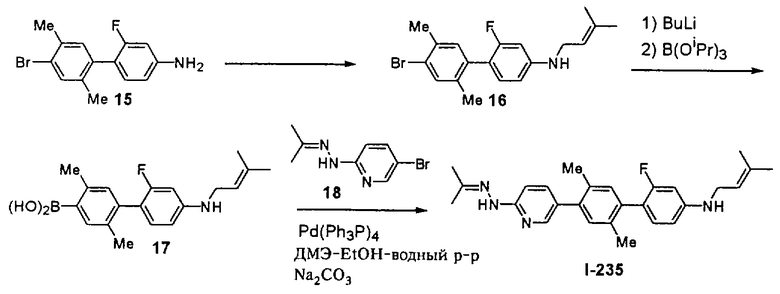
(Стадия 1) Синтез соединения (16)
К раствору соединения (15) (4,41 г, 15,0 молей) в дихлорметане (45 мл) последовательно добавляли З-метил-2-бутенал (1,74 мл, 18,0 молей), уксусную кислоту (1,8 г, 30,0 молей) и триацетоксиборогидрид натрия (6,36 г, 30,0 молей) и реакционную смесь перемешивали в течение 15 ч. Реакционную смесь сливали на воду, экстрагировали этилацетатом, экстракт промывали водным раствором бикарбоната натрия и насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 9:1), получая соединение (16) (4,09 г; выход: 75%).
(Стадия 2) Синтез соединения (17)
Раствор соединения (16) (2,4 г, 6,62 моля) в тетрагидрофуране (24 мл) охлаждали до -78°С и затем обрабатывали по каплям в течение 30 мин 1,53 М бутиллитием (10,4 мл, 15,9 моля). После перемешивания реакционной смеси еще в течение 2 ч добавляли триизопропилборат (5,5 мл, 23,8 моля), охлаждающую среду удаляли и смеси давали нагреться до комнатной температуры при перемешивании в течение 30 мин. Реакционную смесь сливали на воду, затем экстрагировали этилацетатом и экстракт промывали водным раствором хлорида аммония и насыщенным соляным раствором, сушили и концентрировали. Кристаллический остаток промывали гексаном и фильтровали, получая соединение (17) (1,82 г, выход: 87%).
1H-ЯМР (ДМСО-d6) δ 1,70 (s, 3Н), 1,72 (s, 3Н), 2,12 (s, 3H), 2,63 (s, 3Н), 3,63 (br t, 2H), 5,28 (br t, 1H), 6,01 (br t, 1H), 6,37 (dd, J=2,1, 13,2 Гц, 1Н), 6,46 (dd, J=2,1, 8,4 Гц, 1Н), 6,92 (s, 1 Н), 6,97 (t, J=8,4 Гц, 1 Н), 7,77 (s, 1 Н) част./млн.
(Стадия 3) Синтез соединения (1-235)
Аналогично методу, описанному для стадии 1 в примере для ссылки 2, получали соединение (1-235) (268 мг; выход: 83%) из соединения (18) (175 мг, 0,75 моля) и бороновой кислоты (17) (245 мг, 0,75 моля).
пена; 1Н-ЯМР (СDСl3) δ 1,74 (s, 3Н), 1,78 (s, 3Н), 1,93 (s, 3Н), 2,08 (s, 3Н), 2,22 (s, 3Н), 2,27 (s, 3Н), 3,72 (br d, J=5,4 Гц, 2H), 3,77 (br s, 1H), 5,35 (m, 1H), 6,38 (dd, J=2,4 Гц, 12,3, 1H), 6,45 (dd, J=2,4, 8,4 Гц, 1H), 7,06 (t, J=8,4 Гц, 1Н), 7,12 (s, 1H), 7,13 (s, 1H), 7,27 (d, J=8,4 Гц, 1H), 7,61 (dd, J=2,1, 8,4 Гц, 1Н), 7,68 br s, 1H), 8,13 (d, J=2,1 Гц, 1Н) част./млн.
Эталонный пример 7. Синтез соединения (18)
5-Бром-2-гидразинопиридин (Journal of Heterocyclic Chemistry, 1986 (23) 1071) (376 мг, 2,0 моля) выдерживали при температуре дефлегмации в течение 15 мин в ацетоне (1 мл) и этаноле (4 мл). Реакционную смесь концентрировали, получая соединение (18) в виде кристаллического остатка (456 мг, количественный выход).
Эталонный пример 8. Синтез соединения (1-189)
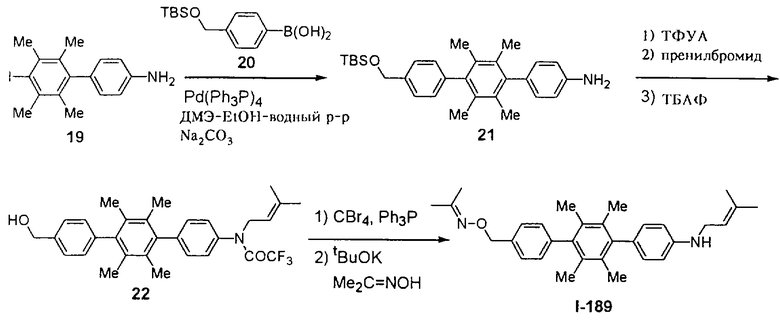
(Стадия 1) Синтез соединения (21)
К раствору соединения (19) (500 мг, 1,42 моля) в смеси диметоксиэтан (6 мл) - этанол (1,5 мл) добавляли бороновую кислоту (20) (624 мг, 1,57 моля) и 2М водный раствор карбоната натрия (3 мл) и смесь подвергали деаэрации. Добавляли тетракис(трифенилфосфин)палладий (49 мг, 0,04 моля) и смесь выдерживали при температуре дефлегмации в атмосфере азота в течение 18 ч, охлаждали, разбавляли водой и затем экстрагировали этилацетатом. Экстракт промывали насыщенным соляным раствором, сушили, концентрировали, получая остаток, который очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 4:1), получая соединение (21) (604 мг; выход: 95%).
(Стадия 2) Синтез соединения (22)
К раствору соединения (21) (604 мг, 1,36 моля) в тетрагидрофуране (6 мл) при охлаждении на льду добавляли триэтиламин (0,28 мл, 2,03 моля), а затем трифторуксусный ангидрид (0,23 мл, 1,63 моля) и смесь перемешивали в течение 15 мин. Реакционную смесь разбавляли этилацетатом и затем промывали последовательно водой и насыщенным соляным раствором, сушили и концентрировали.
Раствор неочищенного продукта в N,N-диметилформамиде (4 мл) объединяли с карбонатом калия (375 мг, 2,71 моля), а затем с пренилбромидом (0,31 мл, 2,71 моля) и перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь сливали на воду, экстрагировали смесью этилацетат - этиловый эфир (1:1) и экстракт промывали последовательно водой и концентрированным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 19:1) и растворяли в тетрагидрофуране (8 мл). Добавляли при охлаждении на льду 1М раствор тетрабутиламмонийфторида в тетрагидрофуране (0,15 мл, 1,5 моля) и смесь перемешивали в течение 1 ч. Реакционную смесь сливали на воду, экстрагировали этилацетатом и экстракт промывали насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 3:1), получая соединение (22) (543 мг, выход: 81%)
(Стадия 3) Синтез соединения (I-189)
Раствор соединения (22) (236 мг, 0,48 моля) в дихлорметане (4 мл) обрабатывали при охлаждении на льду трифенилфосфином (162 мг, 0,62 моля), а затем четырехбромистым углеродом (205 мг, 0,62 моля) и перемешивали в течение 30 мин. Реакционную смесь разбавляли этилацетатом, промывали последовательно водой и насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 9:1) и растворяли в N,N-диметилформамиде (3 мл).
К раствору ацетоксима (139 мг, 1,9 моля) в N.N-диметилформамиде (2 мл), добавляли трет-бутоксид калия (187 мг, 1,67 моля) и смесь перемешивали при комнатной температуре в течение 30 мин, после чего охлаждали до 0°С. Образовавшуюся реакционную смесь объединяли с раствором брома в N,N-диметилформамиде и перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь сливали на воду, экстрагировали смесью этиловый эфир:этилацетат (1:1) и экстракт промывали насыщенным соляным раствором, сушили и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (гексан:этилацетат = 10:1) и кристаллизовали из этилового эфира - гексана, получая соединение (I-189) (117 мг; выход: 54%).
tпл=127,5-128,5°С; 1Н-ЯМР (СDСl3) δ 1,73 (s, 3H), 1,78 (s, 3Н), 1,92 (s, 3H), 1,95 (s, 9H), 1,99 (s, 6H), 3,76 (d, J=6,6 Гц, 2Н), 5,15 (s, 2H), 5,41 (m, 1H), 6,74 (d, J=8,1 Гц, 2H), 7,00 (d, J=8,1 Гц, 2H), 7,16 (d, J=8,1 Гц, 2H), 7,41 (d, J=8,1 Гц, 2Н) 30 част./млн.
Эталонный пример 9. Синтез соединения (I-80)
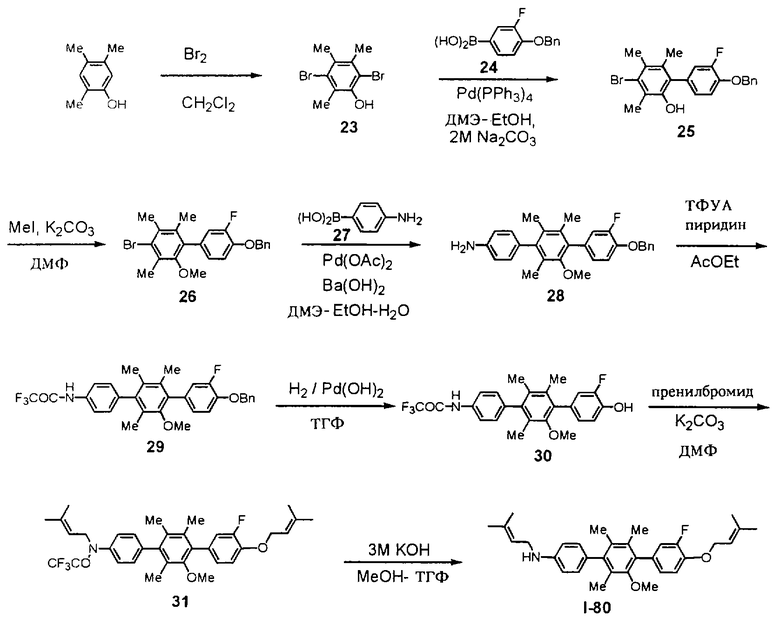
(Стадия 1)
К раствору 2,4,5-триметилфенола (68,0, 0,5 моля) в дихлорметане (450 мл) добавляли по каплям в течение 1 ч 23 мин при охлаждении на льду раствор брома (52,8 мл, 1,03 моля) в дихлорметане (150 мл). После завершения добавления по каплям смесь перемешивали еще в течение 2 ч 40 мин. К смеси, содержащей бикарбонат натрия (100 г), пентагидрат тиосульфата натрия (60 г) и воду (1 л), добавляли при интенсивоном перемешивании реакционную смесь. Реакционную смесь дважды экстрагировали дихлорметаном и экстракт сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток кристаллизовали из гексана, получая соединение (23) (117 г; выход: 80%). tпл=138-142°C.
(Стадия 2)
К раствору соединения (23) (88,2 г, 0,3 моля) в смеси диметоксиэтан (600 мл) - этанол (300 мл) добавляли водный раствор (600 мл) бороновой кислоты (24) (73,8 г, 0,3 моля) и карбоната натрия (127 г, 1,2 моля) и реакционную смесь подвергали деаэрации. Добавляли тетракис(трифенилфосфин)палладий (17,3 г, 15 молей) и смесь выдерживали при температуре дефлегмации в атмосфере азота в течение 3 ч. Реакционную смесь объединяли с 4 н. соляной кислотой (600 мл) и экстрагировали этилацетатом. Экстракт промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным соляным раствором, сушили и концентрировали, получая остаток, который кристаллизовали из метанола, получая соединение (25) (92,9 г; выход: 75%).
tпл 148-150°C
(Стадия 3)
К раствору соединения (25) (83,0 г, 0,2 моля) в N,N-диметилформамиде (500 мл) добавляли карбонат калия (30,4 г, 0,22 моля) и метилйодид (13,7 мл, 0,22 моля) и смесь перемешивали при комнатной температуре в течение 24 ч. Реакционную смесь объединяли с 1 н. соляной кислотой (220 мл) и водой (300 мл) и экстрагировали этилацетатом. Экстракт промывали водой и насыщенным соляным раствором, сушили и концентрировали, получая остаток, который кристаллизовали из метанола, получая соединение (26) (78,5 г; выход 92%).
tпл 112-114°С
(Стадия 4)
К раствору соединения (26) (73,0 г, 170 молей) в смеси диметоксиэтан (500 мл) - этанол (100 мл) добавляли бороновую кислоту (27) (27,4 г, 200 молей), октагидрат гидроксида бария (126 мг, 400 молей) и воду (100 мл) и реакционную смесь подвергали деаэрации. Добавляли ацетат палладия (0,4 г, 1,78 моля) и смесь выдерживали при температуре дефлегмации в атмосфере азота в течение 1 ч, затем добавляли еще одну порцию ацетата палладия (0,4 г, 1,78 моля) и смесь выдерживали при температуре дефлегмации еще в течение 7 ч. К реакционной смеси добавляли активированный уголь (10 г), смесь фильтровали через целит и концентрировали. Остаток растворяли в этилацетате (1 л), промывали водой, сушили и концентрировали. Остаток объединяли при охлаждении на льду с 4 н. раствором хлористого водорода в этилацетате (85 мл) и осадившийся гидрохлорид выделяли фильтрацией. Гидрохлорид объединяли с 1 н. раствором гидроксида натрия (170 мл) и экстрагировали этилацетатом. Экстракт промывали водой, насыщенным соляным раствором, насыщенным водным раствором бикарбоната натрия и насыщенным соляным раствором, сушили, концентрировали и кристаллизовали из метанола, получая соединение (28) (47,8 г; выход: 64%).
tпл 151-153°C
(Стадия 5)
К раствору соединения (28) (40,0 г, 90,6 моля) в этилацетате (300 мл) добавляли при охлаждении на льду пиридин (8,9 мл, 110 молей), а затем трифторуксусный ангидрид (14,1 мл, 100 молей) и смесь перемешивали в течение 20 мин. Реакционную смесь промывали последовательно водным раствором хлорида аммония, водой, водным раствором бикарбоната натрия и насыщенным соляным раствором, сушили, концентрировали и кристаллизовали из этилацетата-гексана, получая соединение (29) (47,5 г; выход: 98%). tпл 167-169°С
(Стадия 6)
К раствору соединения (29) (45,0 г, 83,7 моля) в тетрагидрофуране (300 мл) добавляли 20%-ный гидроксид палладия на угле (3,0 г) и смесь перемешивали при комнатной температуре в атмосфере водорода в течение 3 ч. Катализатор отфтльтровывали и реакционную смесь концентрировали и кристаллизовали из этилацетата - гексана, получая соединение (30) (37,1 г; выход: 99%), tпл 242-244°C.
(Стадия 7)
К раствору соединения (30) (36,0 г, 80,5 моля) в ДМФ (400 мл) добавляли по каплям в течение 5 мин при охлаждении на льду карбонат калия (25,0 г, 181 моль), а затем пренилбромид (19,9 мл, 173 моля). После перемешивания при комнатной температуре в течение 18 ч добавляли карбонат калия (5,5 г, 40 молей) и пренилбромид (4,6 мл, 40 молей) и смесь перемешивали еще в течение 1 ч. Реакционную смесь объединяли с 1 н. соляной кислотой (250 мл) и водой (250 мл) и экстрагировали этилацетатом. Экстракт промывали водой и насыщенным соляным раствором, сушили и концентрировали, получая неочищенный продукт, представляющий собой соединение (31) в виде масла. Этот продукт использовали на следующей стадии реакции без дополнительной очистки.
(Стадия 8)
Неочищенный продукт, представляющий собой соединение (31), полученный согласно описанному выше методу, растворяли в смеси тетрагидрофуран (100 мл) - метанол (500 мл), обрабатывали при охлаждени на льду 3 н. водным раствором гидроксида калия (80 мл) и перемешивали в течение 2 ч. Осадившийся кристаллический продукт выделяли фильтрацией и промывали водой и метанолом. Полученный кристаллический продукт очищали с помощью хроматографии на силикагеле (гексан: этилацетат = 10:1) и кристаллизовали из этанола (250 мл), получая соединение (I-80) (31,3 г; выход: 80%). tпл, 106-108°C (EtOH).
1Н-ЯМР (СDСl3) δ 1,74 (s, 3H), 1,77 (s, 3Н), 1,78 (s, 3H), 1,82 (s, 3H), 1,988 (s, 3Н), 1,992 (s, 3Н), 2,03 (s, 3Н), 3,34 (s, 3Н), 3,70 (brs, 1H), 3,74 (d, J=6,7 Гц, 2H), 4,64 (d, J=7,0 Гц, 2H), 5,36-5,42 (m, 1H), 5,54-5,60 (m, 1H), 6,69 (d, J=8,9 Гц, 2Н), 6,96 (d, J=8,5 Гц, 2H), 6,98-7,25 (m, 3H) част./млн. ИК (Nujol): 3438, 2927, 2854, 1612, 1518, 1466, 1292, 991, 816 см-1.
Аналитически рассчитано для C32H38FNO2: С, 78,82, Н, 7,85; N, 2,87, F, 3,90.
Обнаружено: С, 78,92; Н, 7,67; N, 2,96, F, 3,82.
Эталонный пример 10. Синтез других соединений (I)
Следующие соединения (I) синтезировали аналогично методу, описанному в эталонном примере 9.
(I-89)
tпл 93-94,5°C;
1Н-ЯМР (СDСl3, 300 МГц) δ 1,74 (s, 3Н), 1,77 (s, 6H), 1,82 (s, 3Н), 1,57 (s, 3Н), 1,96 (s, 3Н), 2,06 (s, 3Н), 3,32 (s, 3Н), 3,75 (d, J=6,9 Гц, 2H), 4,64 (d, J=6,9 Гц, 2H), 5,37-5,42 (m, 1H), 5,54-5,60 (m, 1H), 6,71 (d, J=7,8 Гц, 2H), 6,85 (dq, J=8,3, 1,1 Гц, 1H), 6,92 (dd, J=12,0, 1,8 Гц, 1H), 7,04 (t, J=8,6 Гц, 1H), 7,13 (d, J=8,7 Гц, 2H) част./млн;
ИК (Nujol) 3437, 1610, 1576, 1518, 1292, 1242, 1115, 991, 814 см-1.
Аналитически рассчитано для C32H38FNO2: C, 78,82 Н, 7,85; F, 3,90; N, 2,87.
Обнаружено: С, 78,90; Н, 7,92; F, 3,78; N, 3,11.
(I-102)
tпл 143-144°С; 1Н-ЯМР (СDСl3, 300 МГц) δ 1,75 (s, 3Н), 1,79 (s, 3Н), 2,06 (s, 3Н), 2,09 (s, 3Н), 3,35 (s. 3Н), 3,36 (s, 3Н), 3,78 (t, J=6,0 Гц, 2H), 3,83-3,94 (m, 3Н), 4,53 (br s, 1H), 5,34-5,44 (m, 2H), 6,48 (dd, J=8,4, 0,9 Гц, 1H), 6,73-6,79 (m, 1Н), 6,92-6,98 (m, 2H), 7,43 (dd, J=8,4, 2,4 Гц, 1Н), 8,05 (dd, J=2,4, 0,6 Гц, 1Н) част./млн.
(I-108)
tпл 96-97°C; 1Н-ЯМР (СDСl3) δ 1,74 (s, 3Н), 1,79 (s, 6Н), 1,82 (s, 3H), 2,05 (s, 6Н), 2,18 (s, 3Н), 3,74 (d, J=6,6 Гц, 2H), 4,87 (d, J=7,2 Гц, 2H), 5,39 (t, J=6,9 Гц, 1H), 5,58 (t, J=7,2 Гц, 1Н), 6,70 (d, J=8,4 Гц, 2H), 6,81 (d, J=8,4 Гц, 1H), 6,96-6,99 (m, 3Н), 7,57 (dd, J=0,9, 8,7 Гц, 1H), 8,16 (d, J=2,1 Гц, 1Н) част./млн.
ИК (КВг): 3345, 2972, 2913, 1613, 1560, 1522, 1490, 1466, 1281, 1240, 982, 827 см-1.
(I-55)
tпл 84-86°C; 1Н-ЯМР (СDСl3) δ 1,74 (s, 3Н), 1,77 (s, 3Н), 1,79 (s, 3Н), 2,23 (s, 3Н), 2,28 (s, 3Н), 3,71 (d, J=6,9 Гц, 2H), 4,93 (d, J=6,9 Гц, 2Н), 5,32-5,61 (m, 2H), 6,36-6,48 (m, 2H), 7,05 (t, J=8,4 Гц, 1H), 7,09 (s, 1H), 7,15 (s, 1H), 8,53 (s, 2H) част./млн.
ИК (КВг): 3224, 3315, 2970, 2923, 1628, 1592, 1534, 1474, 1438, 1377, 1341, 1317, 1249, 1173, 1110, 993 см-1.
(I-81)
1Н-ЯМР (СDСl3, 300 МГц) δ 1,74 (s, 3H), 1,78 (s, 3H), 1,80 (s, 3H), 1,83 (s, 3H), 1,98 (s, 3H), 2,07 (s, 3H), 3,33 (s, 3H), 3,75 (d, J=6,6 Гц, 2H), 4,88 (d, J=6,9 Гц, 2H), 5,36-5,43 (m, 1H), 5,55-5,62 (m, 1H), 6,71 (d, J=8,0 Гц, 2H), 6,84 (dd, J=2,4, 0,8 Гц, 1H), 7,30 (d, J=8,0 Гц, 2H), 7,40 (dd, J=8,6, 2,4 Гц, 1H), 7,98 (dd, J=2,4, 0,8 Гц, 1Н) част./млн.
(I-90)
tпл 111-112°С; 1Н-ЯМР (СDСl3) δ 1,75 (s, 3H), 1,78 (s, 3H), 2,00 (s, 6H), 2,05 (s, 3H), 3,32 (s, 3H), 3,75 (d, J=6,9 Гц, 2H), 4,82 (dq, J=1,4, 8,6 Гц, 2H), 5,39 (m, 1H), 6,70 (d, J=8,7 Гц, 2H), 6,93-6,97 (m, 3H), 7,64 (dd, J=2,4, 8,4 Гц, 1H), 8,10 (dd, J=0,3, 2,1 Гц, 1H) част./млн.
ИК (КВг): 3407, 2931, 2860, 1613, 1521, 1292, 1274, 1259, 1240, 1164, 1070, 823 см-1.
(I-114)
tпл 91-91°С; 1Н-ЯМР (СDСl3) δ 1,73 (s, 6H), 1,77 (s, 6H), 2,03 (s, 3Н), 2,05 (s, 6H), 2,7 (s, 3Н), 3,73 (d, J=6,6 Гц, 4Н), 5,39 (t, J=6,9 Гц, 2H), 6,52-6,57 (m, 4H), 6,95-7,01 (m, 4H) част./млн.
(I-120)
tпл 79-81°С; 1Н-ЯМР (СDСl3) δ 1,73 (s, 3H), 1,74 (s, 3Н), 1,77 (s, 6H), 2,06 (s, 3Н), 2,07 (s, 3Н), 2,27 (s, 3Н), 3,72 (d, J=6,9 Гц, 2Н), 3,89 (m, 2H), 4,47 (m, 1H), 5,37 (m, 2H), 6,43-6,53 (m, 3Н), 6,95 (d, J=8,1 Гц, 1Н), 7,01 (s, 1H), 7,07 (s, 1H), 7,48 (dd, J=2,1, 8,4 Гц, 1H), 8,14 (d, J=2,1 Гц, 1H) част./млн.
(I-121)
tпл 180-182°C, 1Н-ЯМР (СDСl3) δ 1,26 (d, J=6,3 Гц, 12Н), 1,99 (s, 12H), 3,47 (s, 2H), 3,68 (sept, J=6,3 Гц, 2H), 6,65 (d, J=8,6 Гц, 4Н), 6,97 (d, J = 8,6 Гц, 4Н) част./млн; ИК (КВг): 3392, 1612, 1520, 1313, 1290, 1182, 810 см-1.
(I-122)
tпл, 151-153°С; 1Н-ЯМР (СDСl3) δ 1,27 (d, J=6,0 Гц, 12H), 1,96 (s, 3H), 1,97 (s, 3Н), 2,01 (s, 3Н), 3,68 (m, 2H), 3,20-3,78 (bs, 2H), 4,90 (s, 1H), 6,67 (bd, J=6,9 Гц, 2H), 6,71 (d, J= 8,4 Гц, 2H), 6,97 (d, J=7,8 Гц, 2H), 7,11 (d, J-8,4 Гц, 2H) част./млн.
ИК (КВг): 3504, 3397, 2965, 2923, 2869, 1610, 1519, 1461, 1413, 1382, 1317, 1292, 1245, 1180, 1126, 1074, 815 см-1.
(I-123)
tпл 165-167°С; 1Н-ЯМР (СDСl3) δ 1,27 (d, J=6,0 Гц, 12H), 2,06 (s, 6H), 3,32 (s, 6H), 3,69 (sept, J=6,0 Гц, 2H), 6,75 (br s, 4H), 7,14 (br d, J=8,4 Гц, 4Н) част./млн.
(I-124)
tпл 192-194°С; 1Н-ЯМР (СDСl3) δ 1,26 (d, J=6,6 Гц, 12H), 1,99 (s, 6H), 2,06 (s, 3Н), 3,32 (s, 3Н), 3,48 (br s, 2H), 3,68 (sept, J=6,6 Гц, 2H), 6,66 (d, J=8,4 Гц, 4H), 6,96 (d, J=8,4 Гц, 2H), 7,12 (br d, J=8,4 Гц, 2Н) част./млн.
(I-125)
tпл 102-104°С; 1Н-ЯМР (СDСl3) δ 1,25 (d, J=6,3 Гц, 6H), 1,26 (d, J=6,0 Гц, 6H), 2,04 (s, 6H), 2,21 (s, 3H), 3,50 (brs, 2H), 3,63-3,72 (m, 2H), 6,62-6,67 (m, 4H), 6,96 (d, J=8,7 Гц, 2H), 7,01 (s, 1H), 7,17 (d, J=8,4 Гц, 2H) част./млн.
ИК (КВг): 3377, 2964, 2921, 1612, 1521, 1482, 1463, 1382, 1315, 1290, 1245, 1184, 825 см-1.
(I-126)
tпл 113-115°С; 1Н-ЯМР (СDСl3) δ 1,73 (s, 6H), 1,77 (s, 6H), 2,20 (s, 6H), 3,72 (d, 4H, J=6,6 Гц), 4,07 (br s, 2H), 5,36 (t, J=6,6 Гц, 2H), 6,40 (dd, J=12,3, 2,3 Гц, 2H), 6,46 (dd, J=8,1, 2,3 Гц, 2H), 7,05-7,10 (m, 4H) част./млн.
(I-132)
tпл 72-73°C; 1Н-ЯМР (СDСl3) δ 1,74 (s, 3Н), 1,77 (s, 3H), 1,80 (s, 6H), 2,05 (s, 3Н), 2,09 (s, 3Н), 2,26 (s, 3Н), 3,72 (d, J=6,6 Гц, 2Н), 4,94 (d, J=6,9 Гц, 2Н), 5,35-5,39 (m, 1H), 5,57-5,62 (m, 1H), 6,50-6,54 (m, 2H), 6,93 (d, J=7,8 Гц, 1Н), 7,05 (s, 1H), 7,07 (s, 1Н), 8,54 (s, 2H) част./млн.
(I-133)
tпл 111-112°C. 1Н-ЯМР (СDСl3) δ 1,07 (3H, s), 1,09 (3H, s), 1,73 (3H, s), 1,77 (3H, s), 1,97 (3H, s), 1,98 (3H, s), 2,06 (3H, s), 2,18 (1H, m), 3,32 (3H, s), 3,76 (2H, d, J=6,9 Гц), 3,87 (2H, d, J=6,9 Гц), 5,40 (1H, m), 5,69 (1H, brs), 6,63 (1H, dd, J=2,1, J=8,1 Гц), 6,73 (2H, d, J=8,1 Гц), 6,77 (1H, d, J=2,1 Гц), 6,90 (1H, d, J=8,4 Гц), 7,14 (2H, d, J=7,5 Гц) част./млн.
Эталонный пример 11. Синтез пролекарств соединений (I-6)
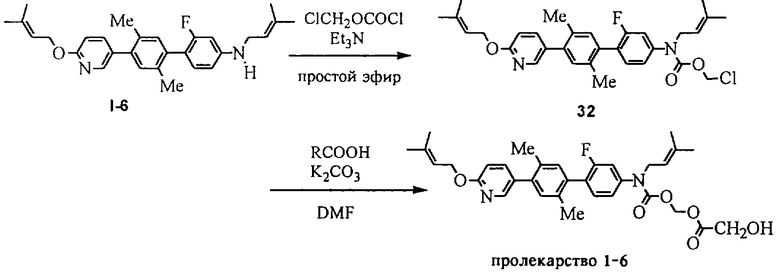
(Стадия 1) Синтез соединения (32)
Соединение (I-6), полученное согласно методу, описанному в эталонном примере 1 (444 мг, 1 моль), растворяли в безводном простом эфире (40 мл), охлаждали на льду, перемешивали в атмосфере азота, последовательно обрабатывая при этом хлорметилхлорформиатом (194 мг, 1 моль) и триэтиламином (210 мл, 1 ммоля), после чего ледяную баню удаляли и смесь перемешивали еще в течение 4 ч. Осадок, образовавшийся в реакционой смеси, отфильтровывали, смесь промывали водой и сушили над безводным сульфатом натрия и растворитель отгоняли при пониженном давлении, получая 540 мг соединения (32) в виде масла.
Аналитически рассчитано для C31H34N2O3FCl: С, 69,33; Н, 6,38; N, 5,22, F, 3,54; Cl, 6,60.
Обнаружено: С, 68,85; Н, 6,42; N, 5,21; F, 3,58; Cl, 7,06.
(Стадия 2) Синтез пролекарства соединений (I-6)
Смесь, содержащую гликолевую кислоту (38 мг, 0,5 моля), карбонат калия (35 мг, 0,25 моля) и N,N-диметилформамид (1 мл), перемешивали при пониженном давлении при комнатной температуре в течение 10 мин, после чего обрабатывали раствором соединения (32) (54 мг, 0,1 моля) в N,N-диметилформамиде (0,5 мл), а затем бромидом калия (12 мг, 0,1 моля) и после этого интенсивно перемешивали в атмосфере аргона в течение 20 ч. Реакционную смесь разбавляли простым эфиром (5 мл), твердый продукт отфильтровывали и смесь промывали водой и сушили над безводным сульфатом натрия, после чего растворитель отгоняли при пониженном давлении, получая неочищенный продукт, который очищали с помощью хроматографии на силикагеле (элюент: гексан:этилацетат = 2:1), получая 27 мг пролекарства соединения (I-6) в виде масла.
1Н-ЯМР (СDСl3) δ 1,58 (3Н, s), 1,73 (3Н, s), 1,80 (3Н, s), 1,82 (3Н, s), 2,20 (3Н, s), 2,28 (3Н, s), 2,33 (1Н, bs), 4,25 (2Н, bs), 4,30 (2Н, d, J=6,9 Гц), 4,88 (2Н, d, J=6,9 Гц), 5,30 (1Н, bt, J=6,9 Гц), 5,58 (2Н, bt, J=6,9 Гц), 5,90 (2Н, bs), 6,83 (1H, d, J=8,4 Гц), 6,95-7,30 (3Н), 7,13 (2Н, bs), 7,60 (1H, dd, J=8,4 Гц, 2,4 Гц), 8,18 (1 Н, d, J=2,4 Гц) част./млн.
Аналитически рассчитано для С33H37N2О6F: С, 68,73; Н, 6,47; N, 4,86; F, 3,29.
Обнаружено: С, 68,59; Н, 6,68; N, 4,98; F, 3,25.
Эксперимент 1. Ингибируюшее действие на индукцию дифференцировки Тh0-клеток в Тh2-клетки
1. Животные
В эксперименте для индукции дифференцировки Th0-клеток в Тh2-клетки использовали 9-11-недельных самок мышей линии BALB/cCrSlc, которых получали от фирмы Japan SLC, Inc., или линии BALB/cAnNCrj, которые получали от фирмы Charles River Japan, Inc.
В эксперименте для индукции диференцировки Th0-клеток в Тh1-клетки использовали 8-недельных самок мышей линии C57BL/6NCrj, которых получали от фирмы Charles River Japan, Inc.
2. Иммунизация и введение соединений по изобретению
В эксперименте для индукции дифференцировки Th0-клеток в Тh2-клетки в качестве антигена использовали DNP-As (динитрофенилированный протеин из Ascaris (экстракт протеина из аскаридов свиней)), 10 мкг которого и 250 мкг Alum (адъювант, представляющий собой гидроксид алюминия) в физиологическом растворе в конечном объеме 50 мкл инъецировали в подошвы обеих задних лап каждой мыши, осуществляя тем самым иммунизацию. В группе, служащей в качестве отрицательного контроля, аналогичным образом обрабатывали каждое животное, вводя путем инъекции 50 мкл физиологического раствора. Через 6 дней после инъекции из правого и левого колена удаляли два подколенных лимфатических узла, пропускали их через металлическую сетку (размер ячеек 200 меш) и вносили в сбалансированный солевой раствор Хенка (HBSS) для получения клеточной суспензии. В группе, обработанной физиологическим раствором, вследствие малого количества выделенных клеток объединяли и подвергали исследованию препараты, полученные от двух животных. Соединение по изобретению суспендировали в 0,5%-ной метилцеллюлозе (МЦ) и вводили перорально в дозе по 0,1 мл на 20 г веса тела мыши каждый день в течение периода времени со дня иммунизации по 5-й день. Контрольную группу, иммунизированную носителем, и группу, служившую в качестве отрицательного контроля, обрабатывали таким же объемом 0,5%-ной МЦ.
В другом варианте в эксперименте для того, чтобы индуцировать дифференцировку Th0-клеток в Тh1-клетки, нежизнеспособные бактерии Mycobacterium tuberculosis линии H37RA (фирма DIFCO) суспендировали в физиологическом растворе и осуществляли иммунизацию дозами по 125 мкг/50 мкл согласно описанному выше методу. В группе, обработанной физиологическим раствором, объединяли и подвергали анализу препараты, полученные от 4 животных.
3. Обнаружение внутриклеточных цитокинов с помощью FACS-метода (метод клеточного сортера с возбуждением флуоресценции)
Клетки, полученные из подколенных лимфатических узлов указанных выше мышей, суспендировали с плотностью 1-2×106 клеток/мл (в объеме 1-2 мл) в среде RPMI 1640 (содержащей 10% фетальной бычьей сыворотки (ФБС) и 50 мкМ 2-меркаптоэтанола) и дополняли ФМА (форбол-12-миристат-13-ацетат) в конечной концентрации 50 нг/мл и 250 нг/мл А23187 (Са-ионофор) и затем инкубировали при 37°С в присутствии 5% СО2. После инкубации в течение 4 ч добавляли брефелдин А до получения конечной концентрации 10 мкг/мл и смесь инкубировали еще в течение 2 ч. Клетки выделяли и промывали дважды буфером для окрашивания (ЗФР, содержащий 1% ФБС и 0,1% азида натрия) и суспендировали в 100 мкл буфера для окрашивания, содержащем 5 мкг/мл Fc Block (очищенное крысиное моноклональное антитело к мышиному CD16/CD32, фирма Pharmingen), и инкубировали на льду в течение 5 мин для того, чтобы блокировать неспецифическую адсорбцию меченого антитела, и затем объединяли с равным объемом меченного с помощью Cy-Chrome крысиного моноклонального антитела к мышиному CD4 (фирма Pharmingen), которое было разбавлено в 200 раз буфером для окрашивания и подвергнуто инкубации на льду в течение 30 мин. После трехкратной промывки буфером для окрашивания клетки суспендировали в ЗФР, объединяли с равным объемом фиксирующего раствора (4%-ный пара-формальдегид) и инкубировали при 4°С в течение ночи, осуществляя тем самым фиксацию. Полученные таким образом зафиксированные клетки дважды промывали буфером для окрашивания, суспендировали в буфере для увеличения проницаемости клеточных мембран (ЗФР, содержащий 1% ФБС, 0,5% сапонина и 0,1% азида натрия) и инкубировали на льду в течение 10 мин, после чего каждый образец клеток выделяли и делили на две одинаковые части. Каждую часть суспендировали в 100 мкл буфера для увеличения проницаемости клеточных мембран, содержащем 5 мкг/мл Fc Block, и инкубировали на льду в течение 5 мин для того, чтобы блокировать неспецифическую адсорбцию меченого антитела на клетках. Одну часть объединяли со 100 мкл каждого из меченного с помощью флуоресцинизотиоцианата (ФИТЦ) крысиного моноклонального антитела к мышиному IFNγ (фирма Pharmingen) и меченного с помощью РЕ (фосфатидилэтаноламин) крысиного моноклонального антитела к мышиному IL-4 (фирма Pharmingen), каждое из которых было разбавлено в 50 раз буфером для увеличения проницаемости клеточных мембран и подвергнуто инкубации на льду в течение 30 мин. Другую часть, служившую в качестве контроля для определения неспецифической адсорбции меченого антитела, объединяли каждый раз со 100 мкл каждого из контрольных антител, взятых в такой же концентрации, т.е. меченного с помощью ФИТЦ очищенного антитела к крысиному IgGlк (фирма Pharmingen) и меченного с помощью РЕ очищенного антитела к крысиному IgGlк (фирма Pharmingen), для осуществления такого же окрашивания. После трехкратной промывки буфером для увеличения проницаемости клеточных мембран и дважды буфером для окрашивания клетки суспендировали в 500 мкл буфера для окрашивания и переносили с помощью найлоновой сетки в пробирку для FACS-анализа.
Для определения процента IFNγ-позитивных клеток (Тh1) и процента IL-4-позитивных клеток (Th2) среди СD4-позитивных Т-клеток использовали устройство типа FACScan (фирма Nippon Becton Dickinson Company Ltd.), после чего из полученных результатов каждый раз вычитали процент клеток, позитивных в отношении неспецифического связывания, окрашенных с помощью контрольного антитела, получая % Тh1 и % Th2, при этом в эксперименте по изучению Th2-дифференцировки определяли отношение Тh2-клеток/Тh1 -клеток и затем на основе этих данных оценивали влияние соединения по изобретению на дифференцировку Th0-клеток в Тh1-клетки или Тh2-клетки. Достоверные различия анализировали с помощью критерия множественных сравнений Дуннета и t-критерия Стьюдента. Результаты представлены в таблицах 13 и 14.
Результаты
Как следует из результатов, приведенных в таблице 13, для CD4-позитивных Т-клеток в подколенном лимфатическом узле мышей линии BALB/c, иммунизированных с помощью DNP-As, характерно увеличение % Th2 и отношения Th2/Th1 по сравнению с неиммунизированной группой, которой вводили путем инъекции только физиологический раствор, что свидетельствует о доминантной индукции Тh2-дифференцировки. При такой индукции каждое из соединений I-55, I-80, I-90, I-102, I-132 и I-133 в дозе 40 мг/кг и I-89 в дозе 10 мг/кг, вводимое пероральным путем в течение 6 последовательных дней после иммунизации, вызывало существенное ингибирование увеличения % Th2 и отношения Th2/Th1, приводя к изменению доминантного Тh2-состояния. Соединение I-6 существенно ингибировало увеличение % Th2 и отношения Th2/Th1 в концентрации 10 мг/кг или выше, приводя к изменению доминантного Тh2-состояния.
С другой стороны, как следует из данных, приведенных в таблице 4, для СD4-позитивных Т-клеток в подколенном лимфатическом узле мышей линии C57BL/6, иммунизированных с помощью нежизнеспособных бактерий Mycobacterium tuberculosis, характерно избирательное увеличение % Th1 по сравнению с неиммунизированной группой, которой вводили путем инъекции только физиологический раствор, что свидетельствует о индукции доминантной Th1-дифференцировки. При такой индукции ни одно из соединений I-6, I-80, I-89 и I-102 не оказывало влияния на увеличение % Th1.
Таким образом, установлено, что соединения по изобретению обладают избирательным ингибирующим действием на дифференцировку Th0-клеток в Th2-клетки.
Пример 1. Таблетка
Соединение (I-6) 15 мг
Крахмал 15 мг
Лактоза 15 мг
Кристаллическая целлюлоза 19 мг
Поливиниловый спирт 3 мг
Дистиллированная вода 30 мл
Стеарат кальция 3 мг
Все компоненты кроме стеарата кальция смешивали до гомогенного состояния, измельчали в порошок и сушили, получая гранулы соответствующего размера После этого добавляли стеарат кальция и смесь прессовали, получая таблетку.
Пример 2. Гранула
Соединение (I-80) 30 г
Лактоза 265 г
Стеарат магния 5 г
Компоненты тщательно смешивали и прессовали, затем измельчали в порошок, распределяли по размерам и просеивали, получая гранулы соответствующего размера.
Пример 3. Капсула
Соединение (I-89) 10 г
Промышленный оксид магния 20 г
Лактоза 70 г
Перечисленные выше компоненты тщательно смешивали, получая отдельные частицы или тонкоизмельченный порошок, и заполняли капсулу.
Промышленная применимость
Как следует из результатов описанных выше экспериментов, любое из соединений по изобретению обладает ингибирующим действием на дифференцировку Th0-клеток в Тh2-клетки, и, таким образом, они могут очень эффективно применяться в качестве ингибиторов Тh2-дифференцировки клеток и в качестве терапевтических агентов при лечении аутоиммунных заболеваний.
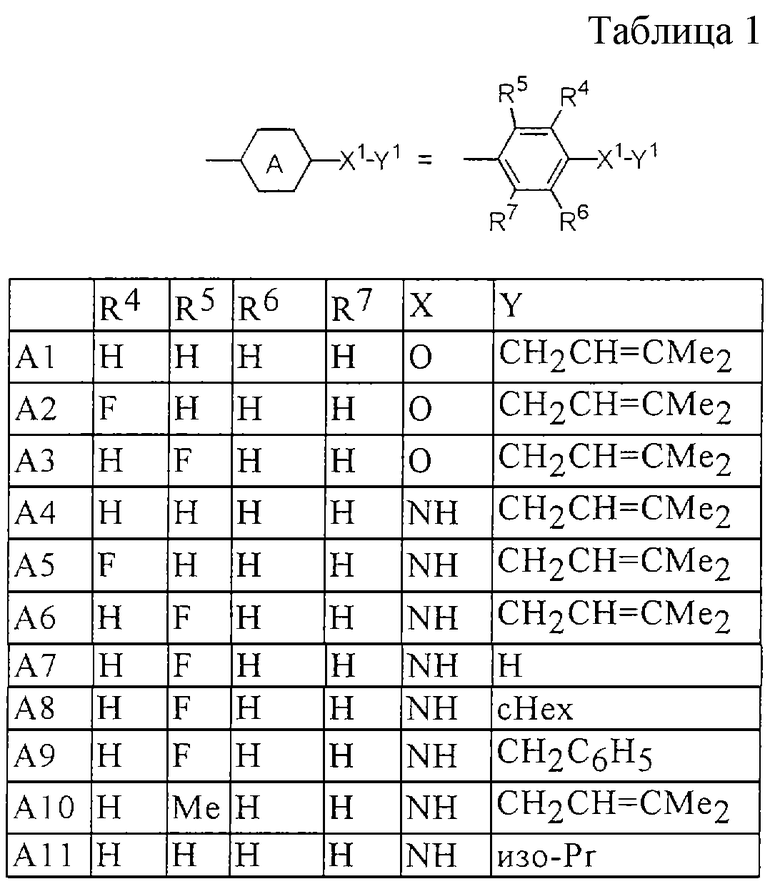
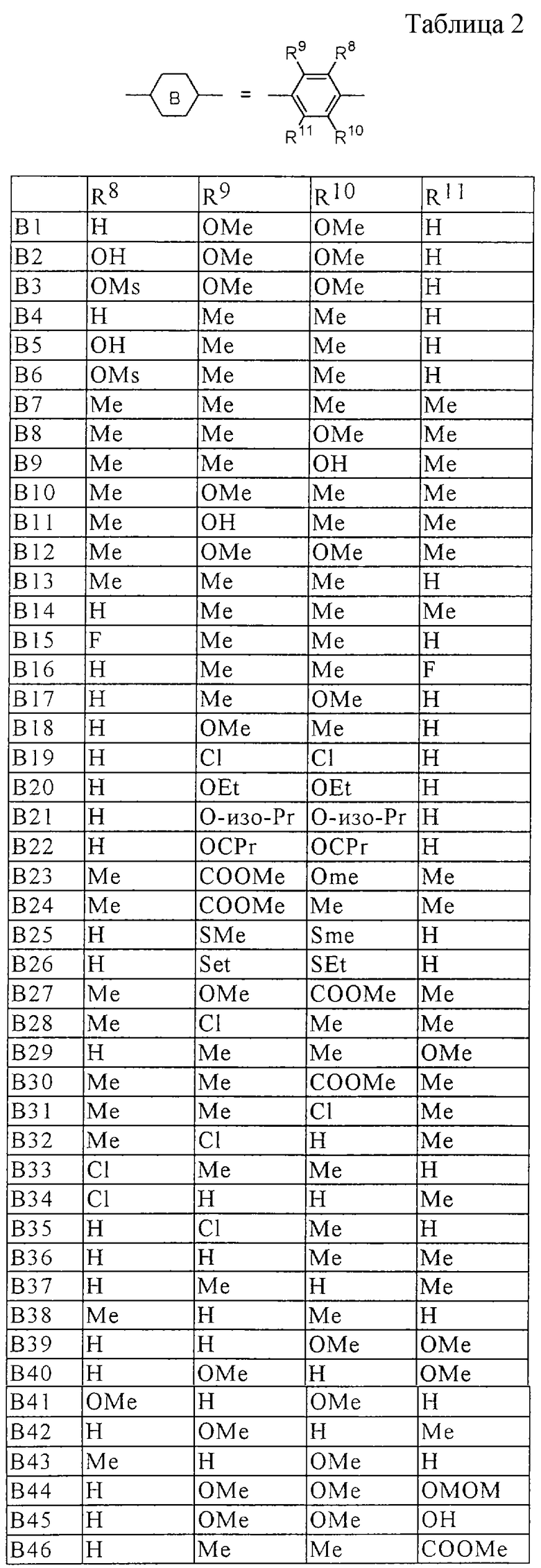
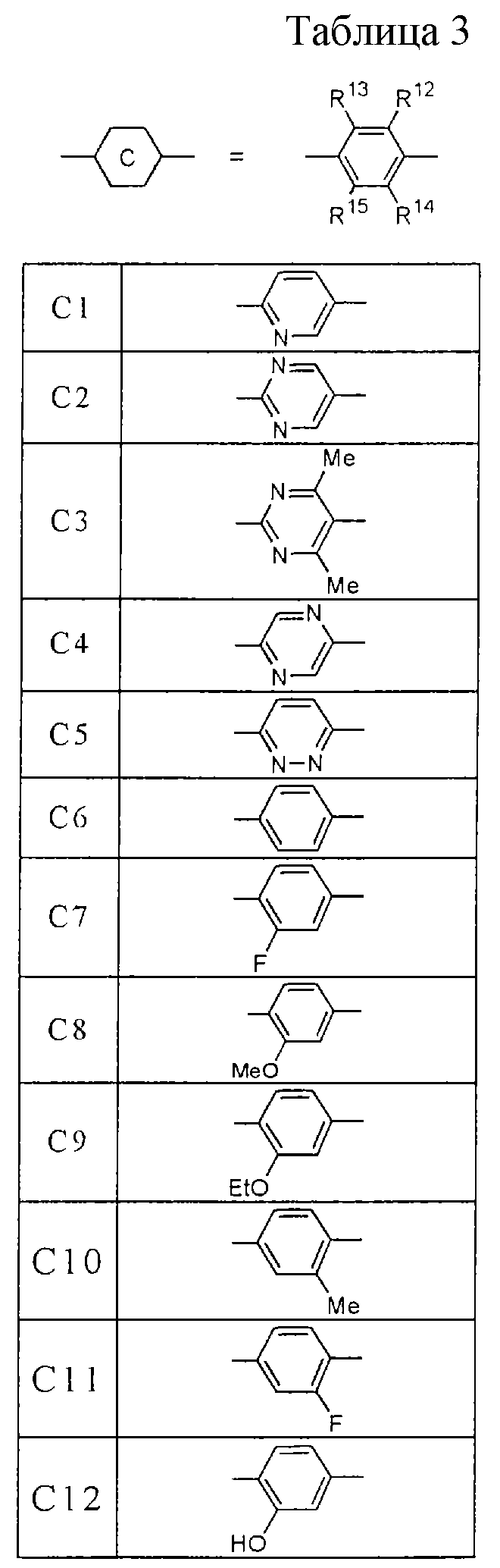
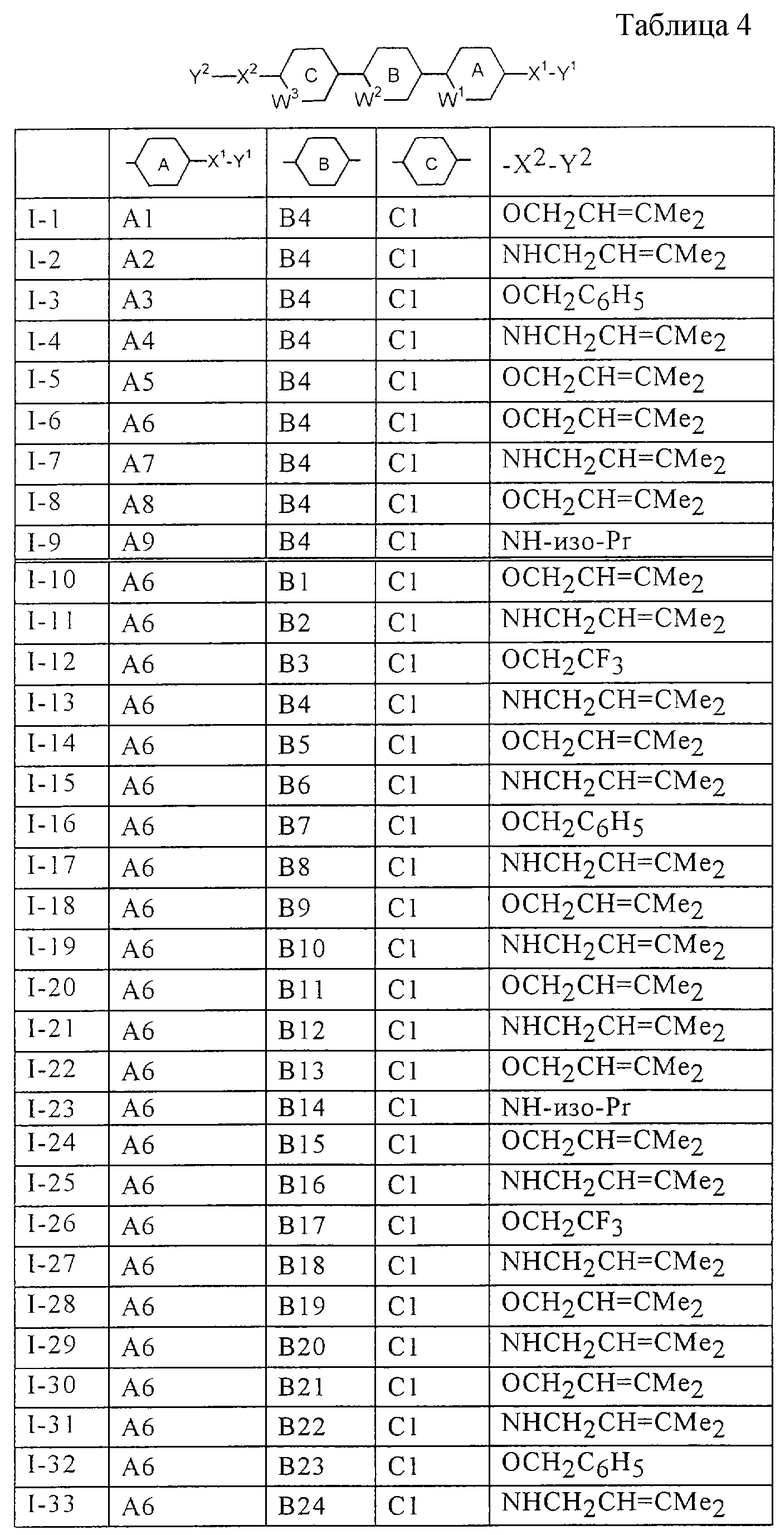
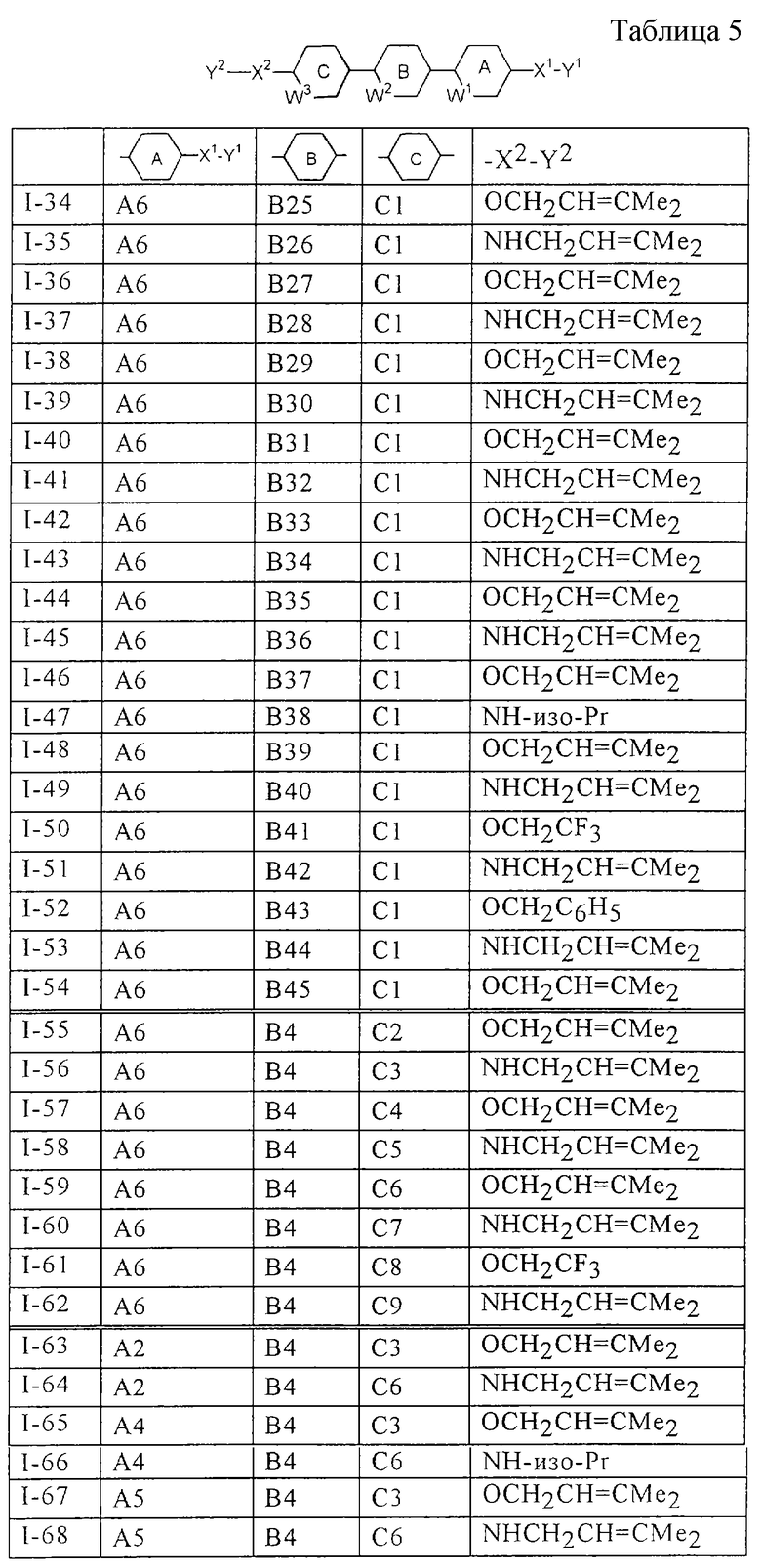
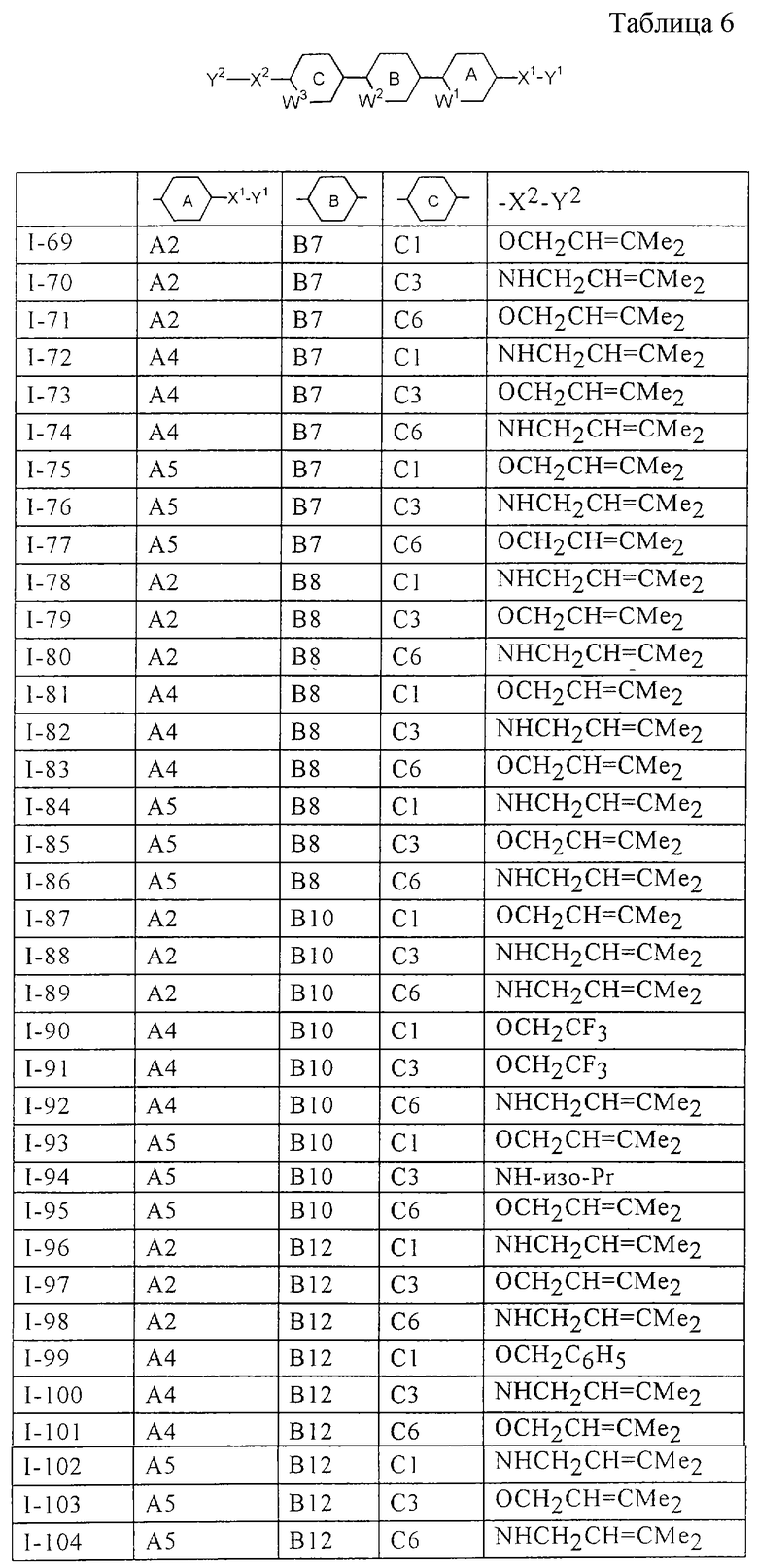
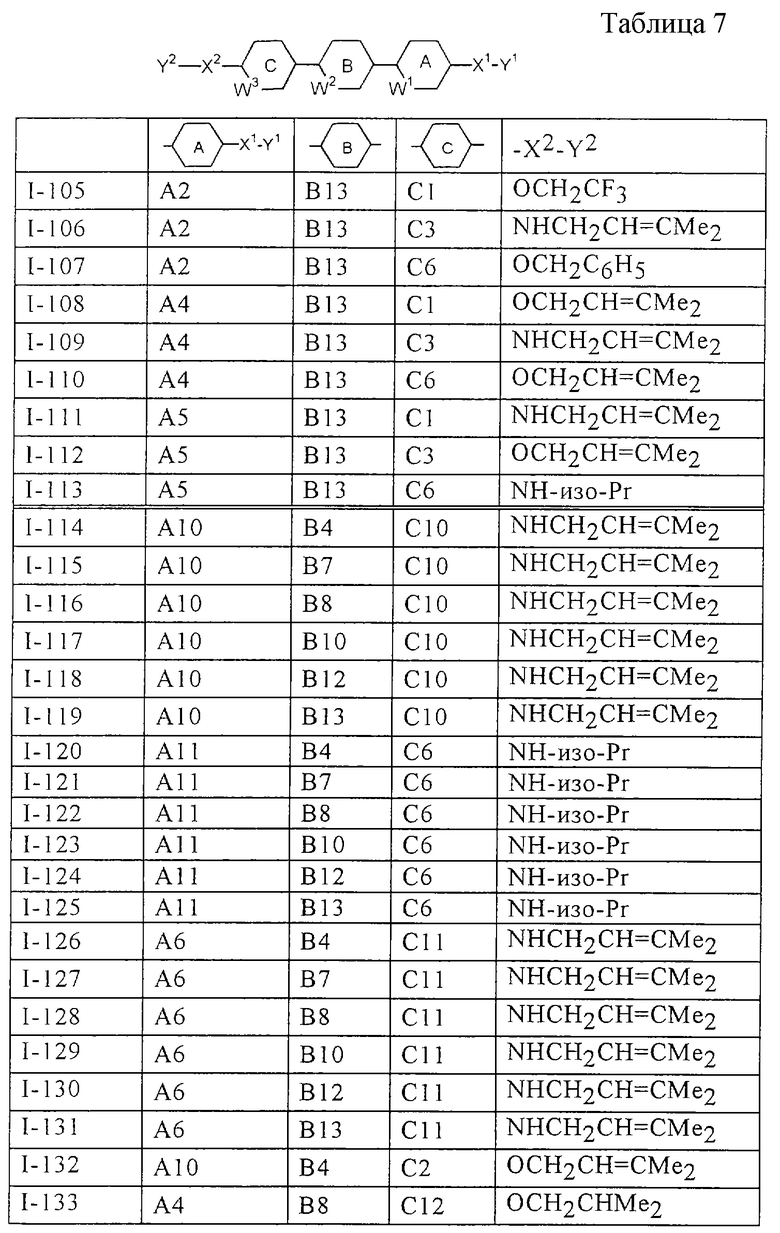
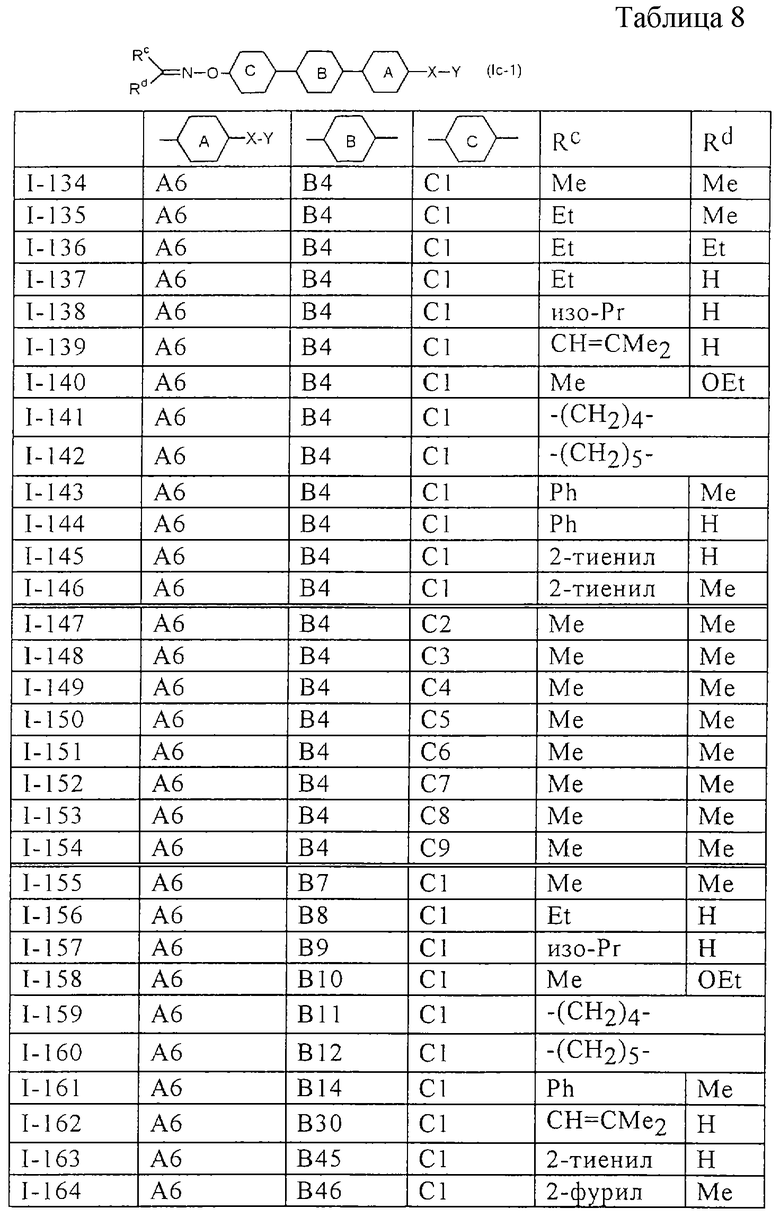
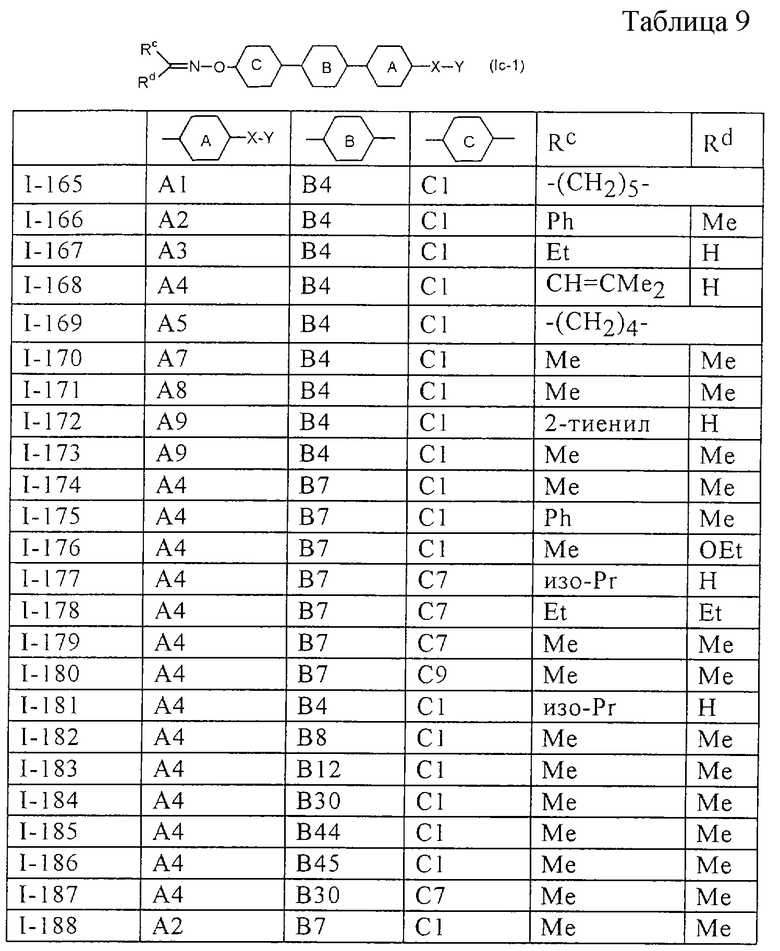
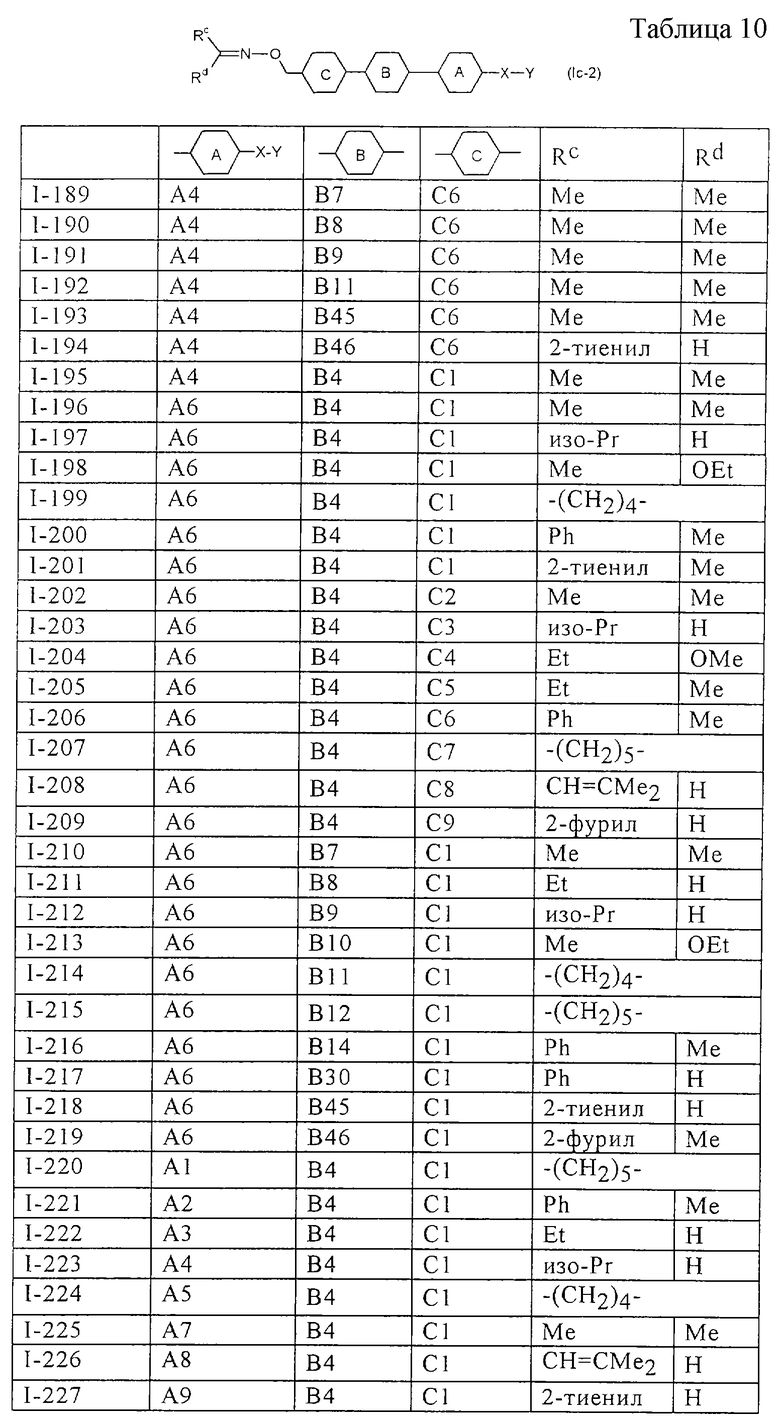
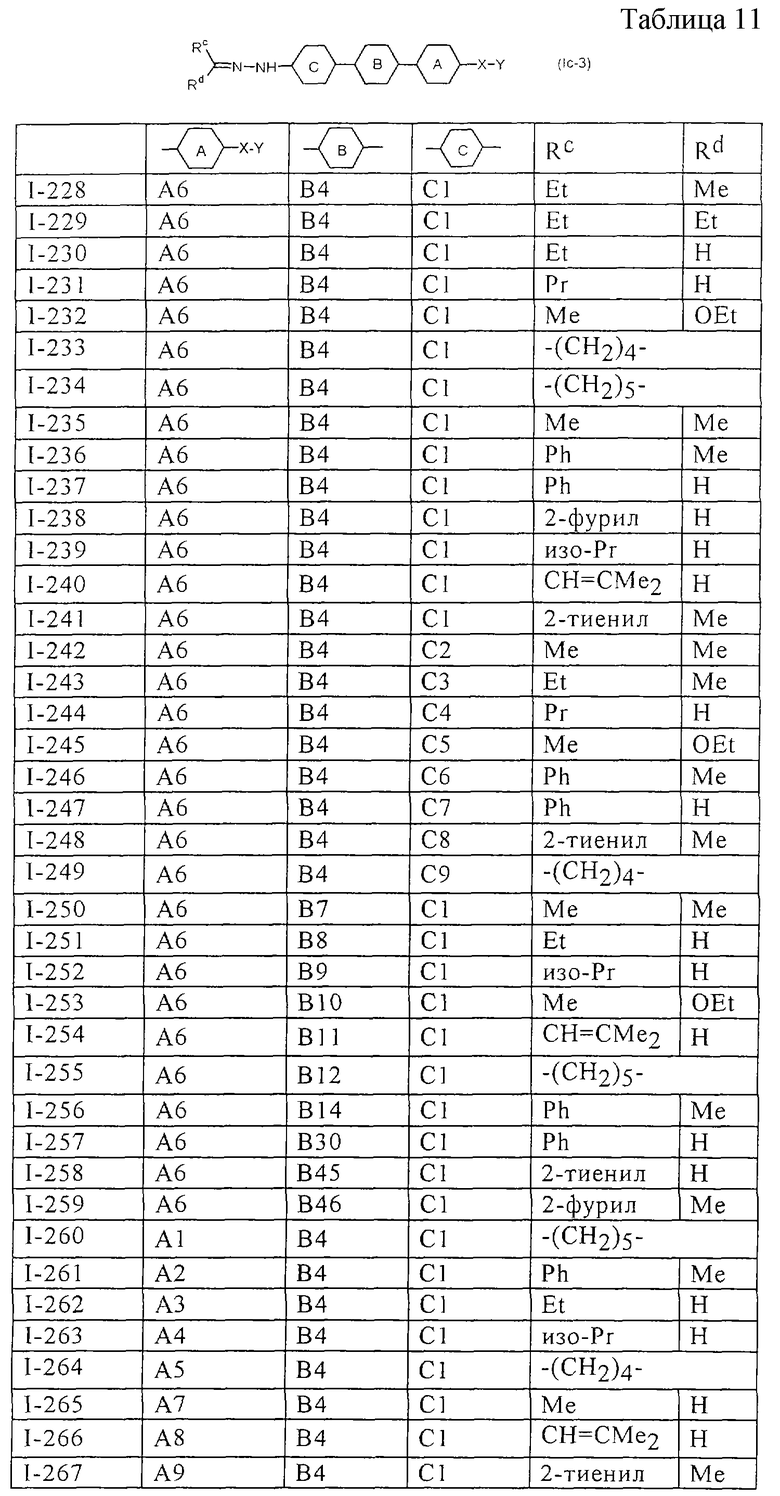
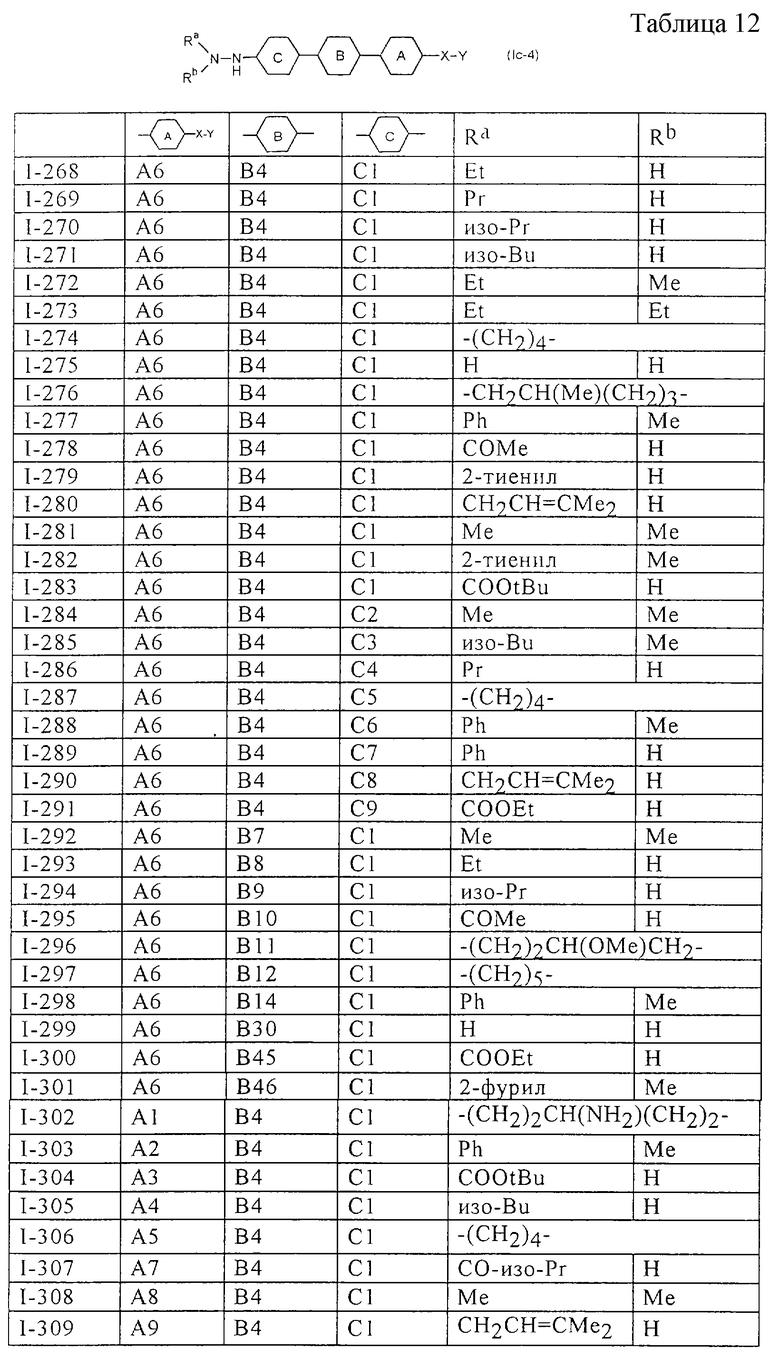
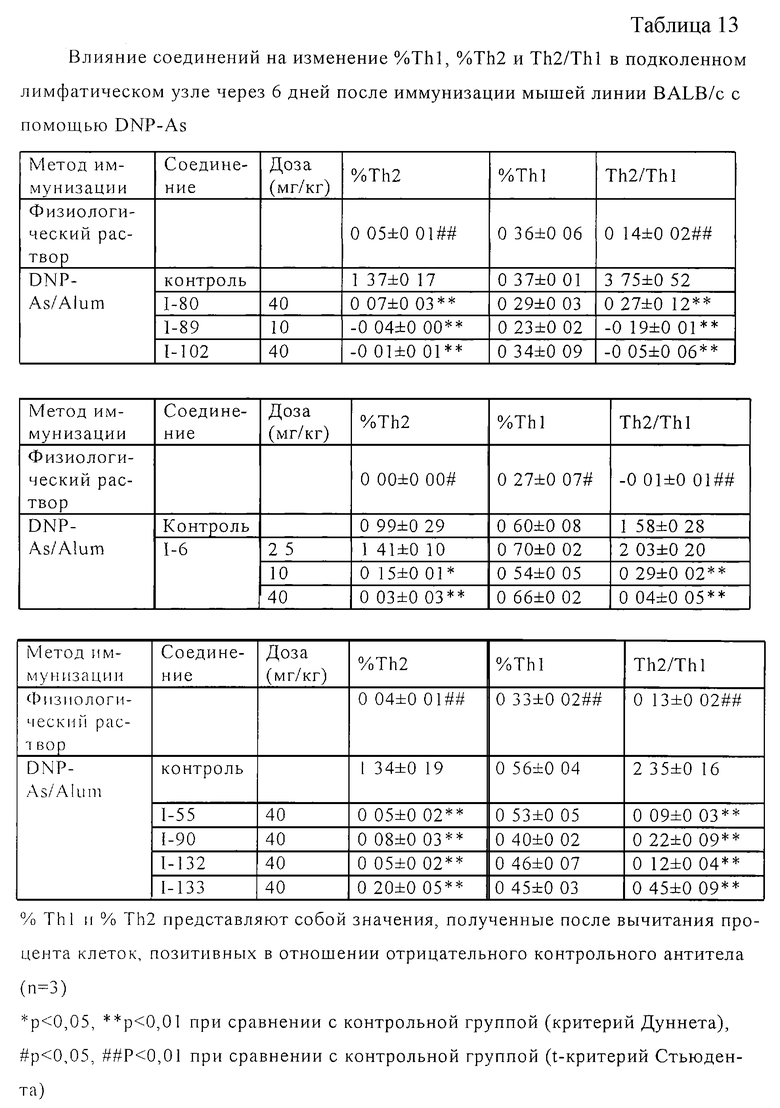
| название | год | авторы | номер документа |
|---|---|---|---|
| СУЛЬФИРОВАННЫЕ АМИНОКИСЛОТНЫЕ ПРОИЗВОДНЫЕ И СОДЕРЖАЩИЕ ИХ ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ | 1997 |
|
RU2198656C2 |
| АНТАГОНИСТ NPY Y5 | 2000 |
|
RU2264810C2 |
| Гетероциклические соединения в качестве ингибиторов киназы RET | 2017 |
|
RU2742115C2 |
| 5-ЧЛЕННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ЛЕКАРСТВЕННЫХ ЦЕЛЕЙ | 2008 |
|
RU2515968C2 |
| ПРОИЗВОДНЫЕ ДИБЕНЗООКСАЗЕПИНА ИЛИ ДИБЕНЗОДИОКСЕПИНА И ПРОТИВООПУХОЛЕВАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2167871C2 |
| 17-ДЕЗОКСИ-1,3,5(10)-ЭСТРАТРИЕН, СПОСОБЫ ЛЕЧЕНИЯ, СПОСОБ СИНТЕЗА 7АЛЬФА-МЕТИЛЭСТРОНА, СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2233288C2 |
| ПРОИЗВОДНЫЕ АМИНОМЕТИЛПИРРОЛИДИНА, ИМЕЮЩИЕ АРОМАТИЧЕСКИЕ ЗАМЕСТИТЕЛИ | 2000 |
|
RU2255938C2 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОИЗОХИНОЛИНА И ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2000 |
|
RU2256661C2 |
| ДИГИДРОБЕНЗОДИАЗЕПИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2000 |
|
RU2247115C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ АНТАГОНИЗИРОВАНИЯ АНГИОТЕНЗИНА II | 1992 |
|
RU2168510C2 |
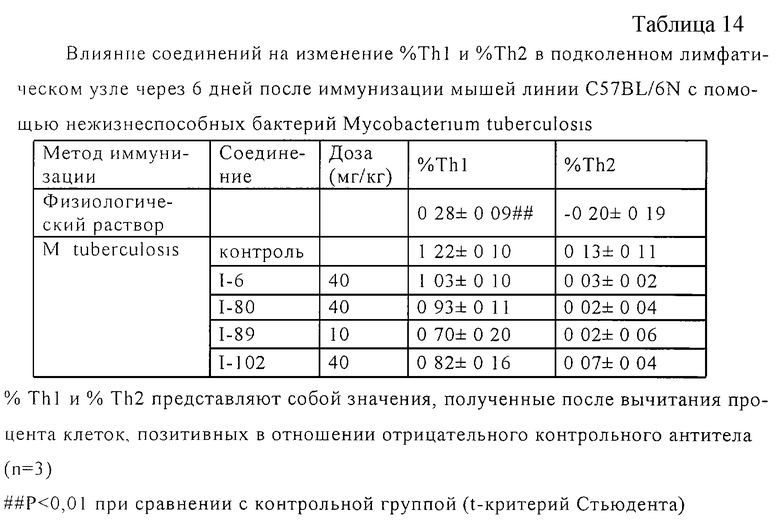
Изобретение относится к области медицины, может использоваться при лечении аллергических заболеваний и аутоиммунных заболеваний и касается фармацевтической композиции, предназначенной для применения в качестве ингибитора Th2-дифференцировки, включающей соединение формулы (I). Композиция обладает повышенной активностью. 3 с. и 11 з.п. ф-лы, 14 табл.
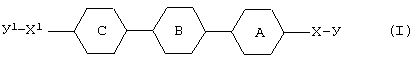
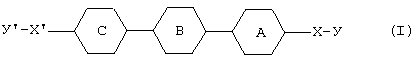
где каждое из колец А и В независимо необязательно замещенное бензольное кольцо, где заместителями являются галоген, гидроксигруппа, низший алкил, низший алкоксил, карбоксигруппа или низший алкоксикарбонил; кольцо С представляет собой необязательно замещенное бензольное кольцо, необязательно замещенное пиридиновое кольцо, необязательно змещенное пиримидиновое кольцо, необязательно замещенное пиридазиновое кольцо или необязательно замещенное пиразиновое кольцо, где заместителями являются низший алкил или гидроксигруппа;
каждый из Х и Х′ обозначает -О-, -СН2- или -NH-;
каждый из Y и Y′ обозначает необязательно замещенный (низш.)алкил или необязательно замещенный (низш.)алкенил, или его пролекарство, фармацевтически приемлемую соль или сольват.
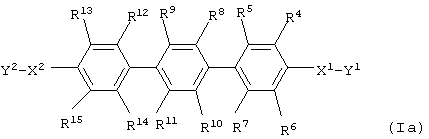
где R4, R5, R6, R7, R8, R9, R10, R11, R12, R13, R14 и R15 каждый независимо друг от друга обозначает водород, галоген, гидроксигруппу, (низш.)алкил, (низш.)алкоксил, карбоксигруппу или (низш.)алкоксикарбонил;
Х1 и Х2 каждый независимо друг от друга обозначает -О-, -СН2- или -NH-;
Y1 и Y2 каждый независимо друг от друга обозначает необязательно замещенный (низш.)алкил, необязательно замещенный арилалкил или необязательно замещенный (низш.)алкенил,
или его пролекарство, фармацевтически приемлемую соль или сольват.
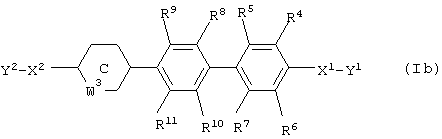
где кольцо С обозначает необязательно замещенное пиридиновое кольцо, необязательно замещенное пиримидиновое кольцо, необязательно замещенное пиридазиновое кольцо или необязательно замещенное пиразиновое кольцо, где заместителями являются гидроксил, низший алкил, или его пролекарство, фармацевтически приемлемую соль или сольват.
| ЛИНЕЙНЫЕ ИЛИ ЦИКЛИЧЕСКИЕ ПЕПТИДЫ, ИХ ПРИМЕНЕНИЕ, СПОСОБ ЛЕЧЕНИЯ | 1993 |
|
RU2130317C1 |
| Способ получения щелочных ксантогенатов низших и/или средних спиртов | 1977 |
|
SU895981A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| J | |||
| Autibiot, 1999, 52, 2, р.89-95. | |||
Авторы
Даты
2004-06-20—Публикация
2000-07-14—Подача