Изобретение относится к биотехнологии, конкретно к генетической инженерии, и представляет собой рекомбинантный аттенуированный штамм бактерий Salmonella enteriditis E-23/pGEX-2T-TBI, способный продуцировать искусственный белок TBI, состоящий из В- и Т-клеточных эпитопов ВИЧ-1. Предложенный рекомбинантный штамм микроорганизмов является кандидатом для конструирования живой вакцины против ВИЧ-1.
Сальмонеллы обладают естественной способностью проникать через эпителий слизистой преимущественно с помощью М-клеток и размножаться как в локальных интерстинальных лимфоидных образованиях, так и парентеральной лимфоидной ткани [1]. Поэтому ослабленные, но способные к инвазии штаммы сальмонелл являются привлекательным средством доставки гетерологичных антигенов к слизистой желудочно-кишечного тракта с последующим вовлечением в процесс иммунной системы [2, 3]. Данный подход может быть использован для создания вакцин против вирусов, проникающих в организм парентеральным путем и/или через слизистую генитального и ректального тракта.
Эффективность векторов на основе Salmonella проиллюстрирована многими экспериментами на животных, в которых использовались сальмонеллы, продуцирующие белки вирусов, бактерий и простейших [4, 5]. Антигены, продуцированные штаммами сальмонелл, стимулируют антиген-специфичные системные IgG, Т-хелперный ответ, CD8+ I-класса или CD4+ II-класса CTL ответ, а также наработку секреторных антител в слизистой оболочке [6]. Одним из ярких примеров является использование штаммов сальмонелл, экспрессирующих фрагмент гена С tetanus toxsoid [7] и обеспечивающих полную защиту мышей от парентерального заражения столбнячным токсином.
Рядом авторов описаны большие вариации иммунного ответа к различным антигенам, экспрессированным в сальмонеллах. Причиной этому могут служить различные факторы, в том числе уровень экспрессии, клеточная локализация антигена, путь введения и схема вакцинации [8].
В настоящее время создан ряд различных аттенуированных штаммов сальмонелл. Эти штаммы способны инвазировать лимфоидную ткань кишечного тракта, но обнаруживают пониженную патогенность даже при больших дозах [9, 10].
Известен штамм бактерий Salmonella typhimurium SL 7207, который экспрессирует белок gp120 ВИЧ-1 [11, прототип]. Штамм вводили мышам per os. В результате у мышей регистрировали выраженный иммунный ответ к вирусному белку gp120 вируса иммунодефицита человека. Наблюдался и пролиферативный ответ спленоцитов иммунизированных мышей, а также была показана цитотоксическая активность спленоцитов. Однако следует отметить, что в данном аналоге существенным недостатком является то, что данный штамм индуцирует иммунитет только к одному вирусному белку ВИЧ-1, а также не продемонстрировано формирование мукозального иммунитета после иммунизации указанным штаммом и вируснейтрализующая активность сывороток иммунизированных животных.
Технической задачей изобретения является создание на основе аттенуированного штамма Salmonella enteriditis E-23 рекомбинантного штамма Salmonella enteriditis E-23/pGEX-2T-TBI, обеспечивающего конститутивный синтез белка-иммуногена TBI, содержащего несколько эпитопов иммуногенных белков ВИЧ-1 и вызывающего индукцию специфических нейтрализующих ВИЧ-1 антител при введении животным, т.е. являющегося кандидатом в живую вакцину против ВИЧ-1.
Подходящим кандидатом в белки-иммуногены является белок TBI (Т and В cell epitopes contaning immunogen). Сконструированный четырех-α-спиральный белок обладает оптимальной композицией эпитопов и предсказанной третичной структурой [12, 13]. Аминокислотная последовательность белка TBI включает четыре Т-клеточных эпитопа и пять В-клеточных нейтрализующих эпитопов из белков env и gag ВИЧ-1. У мышей и обезьян Macaque rhesus, иммунизированных TBI, формировался как клеточный, так и гуморальный ответ к ВИЧ-1. Было показано, что анти-ТВI антитела обладали ВИЧ-1-нейтрализующей активностью. Полученные результаты свидетельствуют о перспективности данного подхода.
Известен аттенуированный штамм Salmonella enteriditis E-23, (cya, CRP), обладающий пониженной вирулентностью [14]. На мышах, телятах и обезьянах показано, что вирулентность этого штамма снижена примерно в 1000 раз по сравнению с родительским штаммом, при сохранении инвазивной активности. Этот штамм по ряду основных свойств может быть использован для решения поставленной задачи, т.е. для создания на его основе вакцины против ВИЧ-1.
Поставленная задача решается генетической трансформацией штамма Salmonella enteriditis E-23 (cya, CRP) плазмидой pGEX-2T-TBI [15], обеспечивающей конститутивный синтез белка TBI, и при введении штамма лабораторным животным, вызывающая индукцию специфических анти-ВИЧ антител и специфического клеточного ответа.
Сконструированный штамм получил обозначение S. enteriditis E-23/pGEX-2T-TBI и депонирован под номером В-884 в коллекции НИИ ККМ ГНЦ ВБ "Вектор".
Культурально-морфологические признаки:
Морфология: грамотрицательные палочки, средних размеров, расположены хаотично.
Культуральные свойства: растет на мясопептонном агаре, глюкозоминимальном агаре Девиса, средах Мак-Конки, Левина, Кауфмана, колонии в S-форме мелких размеров через 18 часов роста при 37°С. В мясопептонном бульоне, желчном бульоне, жидкой глюкозоминимальной среде А (Девиса) - диффузное помутнение через 18 часов роста. В цитратминимальной среде (Девиса) - отсутствие роста.
Резистентность к антибиотикам: на всех вышеперечисленных средах растет в присутствии ампициллина (100 мкг /мл)
Антигенная структура:
O9,12Hg,m
Биохимические свойства.
Не утилизирует цитрат на агаре Симмонса, не продуцирует индол, не расщепляет мочевину, не обладает фенилаланилтрансаминазной активностью, реакция Фогес-Проскауэра - отрицательная; продуцирует сероводород в течение 48 часов, обладает лизин- и орнитилкарбоксилазными активностями и аргининдегидролазной активностью; ферментирует глюкозу, не ферментирует лактозу, сахарозу, мальтозу, сорбит, инозит, дульцит, адонит; в течение 48 часов ферментирует рамнозу, манит, трегалозу. Желатину не разжижает.
Чувствительность к бактериофагам:
Чувствителен к бактериофагу Р22.
Плазмидный профиль:
Плазмида pGEX-2T-TBI с молекулярной массой 5382 kb. Данная плазмида получена авторами и обеспечивает синтез белка TBI в клетках сальмонелл [15].
Изобретение иллюстрируется следующими графическими материалами:
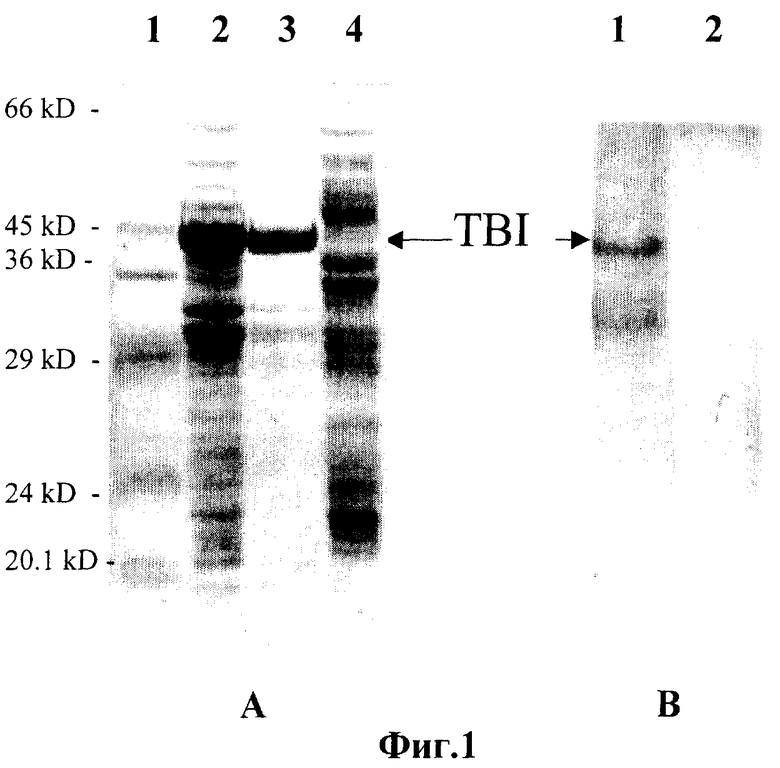
Фиг.1.
А. Синтез белка TBI клетками сальмонелл по данным электрофореза в 15% ПААГ.
1. Маркер молекулярных масс
2. Лизат клеток Salmonella enteriditis E-23/pGEX-2T-TBI.
3.Очищенный белок TBI
4. Лизат клеток Salmonella enteriditis E-23, не содержащих плазмиду.
В. Иммуноблотинг с использованием сывороток макак, иммунизированных ВИЧ-1.
1. Лизат клеток Salmonella enteriditis E-23/pGEX-2T-TBI.
2. Лизат клеток Salmonella enteriditis E-23, не содержащих плазмиду.
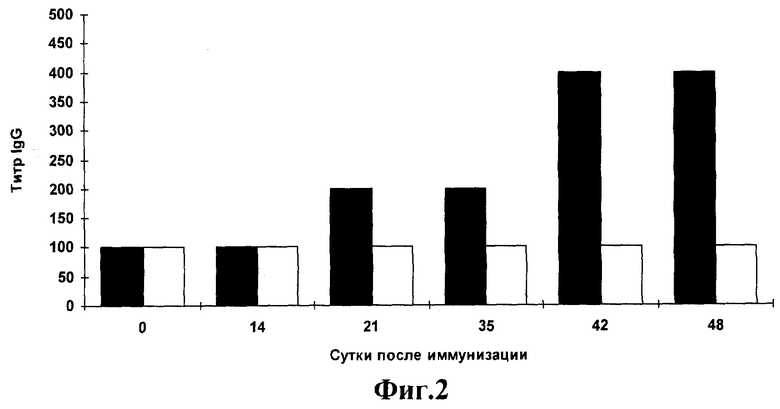
Фиг.2.
Анализ системного гуморального ответа к очищенному вирусу ВИЧ-1 сывороток мышей, иммунизированных штаммом Salmonella enteriditis E-23/pGEX-2T-TBI no данным ИФА.
 S. enteriditis E-23/pGEX-2T-TBI
S. enteriditis E-23/pGEX-2T-TBI
 S. enteriditis E-23
S. enteriditis E-23
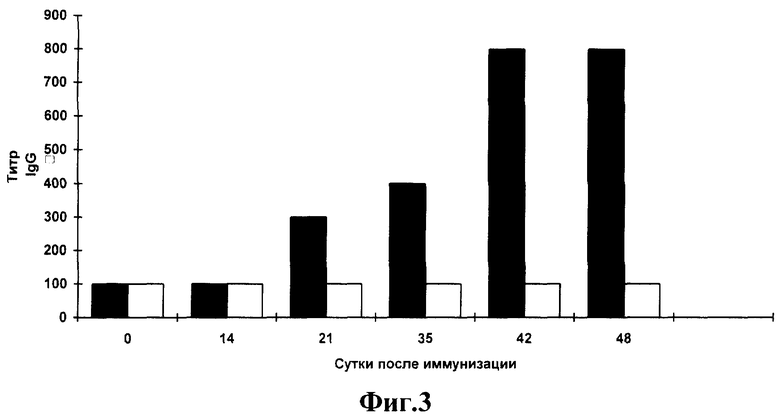
Фиг.3.
Анализ системного гуморального ответа к рекомбинантным белкам ВИЧ-1 сывороток мышей, иммунизированных штаммом Salmonella enteriditis E-23/pGEX-2T-TBI по данным ИФА.
 S. enteriditis E-23/pGEX-2T-TBI
S. enteriditis E-23/pGEX-2T-TBI
 S. enteriditis E-23
S. enteriditis E-23
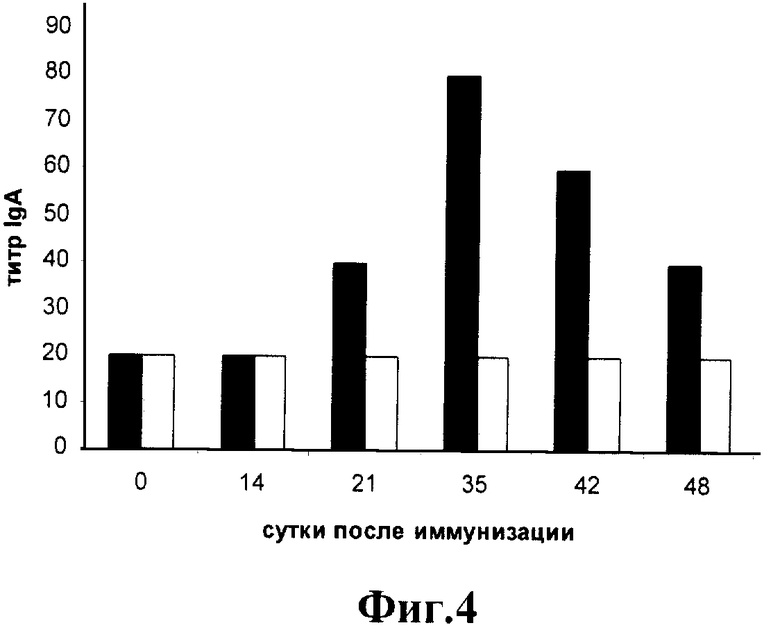
Фиг.4.
Оценка мукозального иммунного ответа к очищенному вирусу ВИЧ-1 сывороток мышей, иммунизированных штаммом Salmonella enteriditis E-23/pGEX-2T-TBI по данным ИФА.
 S. enteriditis E-23/pGEX-2T-TBI
S. enteriditis E-23/pGEX-2T-TBI
 S.enteriditis E-23
S.enteriditis E-23
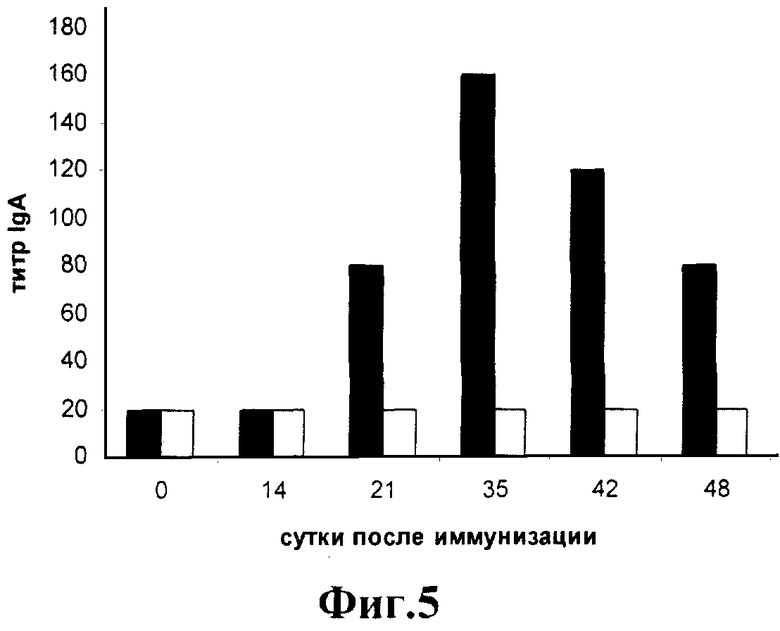
Фиг.5.
Оценка мукозального иммунного ответа к рекомбинантным белкам ВИЧ-1 сывороток мышей, иммунизированных штаммом Salmonella enteriditis E-23/pGEX-2T-TBI по данным ИФА.
 S. enteriditis E-23/pGEX-2T-TBI
S. enteriditis E-23/pGEX-2T-TBI
 S. enteriditis E-23
S. enteriditis E-23
Для лучшего понимания сущности изобретения ниже следуют примеры его осуществления.
Пример 1. Получение рекомбинантного штамма Salmonella enteriditis E-23/pGEX-2T-TBI
Трансформация.
Электропорация. Культуру клеток Salmonella enteriditis E-23 выращивают в среде YT до ОП=0,5, охлаждают, 1 мл культуральной жидкости центрифугируют 2 мин при 6000 об/ мин на центрифуге Eppendorf. Осадок клеток ресуспендируют в 800 мкл охлажденной, бидистилированной воды и осаждают центрифугированием 1 мин при 6000 об/мин. Процедуру промывки повторяют 5 раз. Затем осадок ресуспендируют в 200 мкл 10% глицерина, центрифугируют 1 мин при 6000 об/мин и ресуспендируют в 40 мкл 10% глицерина.
К суспензии клеток добавляют 0,5 мкг плазмидной ДНК. Образец помещают в кювету для электропорации, время импульса составляет 4 сек при напряжение 2,5 В. Для электропорации используют электропоратор фирмы BIORAD. Затем добавляют по 300 мкл YT среды и инкубируют 1 час при 37°С. Клетки рассевают на StI агар с ампициллином (100 мкг/мл). Выросшие на агаре с ампициллином колонии обозначают как Salmonella enteriditis E-23/pGEX-2T-TBI. Все манипуляции с плазмидной ДНК проводят согласно описанным методикам [16].
Культивирование
Клетки Salmonella в enteriditis E-23/pGEX-2T-TBI выращивают следующим образом: отдельную колонию сальмонеллы засевают в 50 мл среды YT, содержащей ампициллин (100 мкг/мл), и инкубируют 16 часов 37°С; клетки осаждают центрифугированием.
Белковый электрофорез и иммуноблотинг
Клетки Salmonella enteriditis E-23/pGEX-2T-TBI осаждают из 100 мкл культуры. Осадок растворяют в воде и добавляют 40 мкл литического буфера (1М трис-НСl рН 8,8, 5% ДСН, 20% глицерин, 10% меркаптоэтанол, 0,02% бромфеноловый синий) и выдерживают на кипящей водяной бане 5 мин. Электрофоретическое разделение белков проводят в 13%-ном полиакриламидном геле в присутствии 0,1% ДСН по Лэммли [17]. Перенос белков из геля на фильтр осуществляют по описанной методике [16] при напряжении электрического поля 10 В/см2 в течение 2 часов. Фильтры помещают в 3%-ный раствор БСА в 0,01 М трис-HCl, рН 7,5, 0,05% твин-20 на 1 час, после чего инкубируют 1 час с раствором антител макак, иммунизированных ВИЧ-1, разведенным в буфере 0,01М трис-HCl, рН 7,5, 0,15 М NaCl, 0,05% твин-20, 0,05% NaN3, 0,001M ФМСФ. Этот же раствор используют для последующей отмывки фильтров и для инкубации с конъюгатом антител с фосфатазой. Результаты представлены на фиг.1. В лизате клеток Salmonella enteriditis E-23/pGEX-2T-TBI присутствует белок с молекулярной массой, соответствующей 45 кДа, и выявляемый антителами к ВИЧ-1. Это свидетельствует о продукции белка TBI в клетках S. enteriditis E-23/pGEX-2T-TBI.
Пример 2. Исследование способности целевого штамма индуцировать гуморальный иммунный ответ.
Культивирование
Для иммунизации клетки Salmonella enteriditis E-23/pGEX-2T-TBI выращивают следующим образом: отдельную колонию сальмонеллы засевают в 50 мл среды YT, содержащей ампициллин (100 мкг/мл), и инкубируют 16 часов 37°С; клетки осаждают центрифугированием и ресуспендируют в 1 мл физ. раствора. Концентрацию клеток определяют титрованием.
Иммунизация. Для иммунизации были использованы мыши линии BALB/c, весом 12-15 грамм, полученные из вивария ГНЦ ВБ "Вектор". Животные содержались на стандартном рационе.
Иммунизацию животных полученным штаммом проводили однократно, перректально, введением 108 клеток Salmonella enteriditis E-23/pGEX-2T-TBI на мышь. Забор крови производили на 0, 14, 21, 35, 42 и 48 сутки после введения сальмонелл.
Иммуноферментный анализ. Специфичность образующихся антител в сыворотках мышей анализируют с помощью ИФА. Для выявления антител против ВИЧ-1 используют очищенный инактивированный вирус ВИЧ-1 и смесь рекомбинантных белков ВИЧ-1: gag, gp120, env1 и env2. В каждом эксперименте берут образцы от трех животных. Эти образцы смешивают, после чего определяют титр специфических антител. Титр определяют как превышение титра сывороток мышей, иммунизированных Salmonella enteriditis E-23/pGEX-2T-TBI над титром сывороток мышей, иммунизированных исходным штаммом Salmonella enteriditis E-23. На каждую точку делают два повтора. Результаты представлены на фиг.2, 3. Начиная с третьей недели после иммунизации мышей клетками Salmonella enteriditis E-23/pGEX-2T-TBI обнаруживается продукция IgG к ВИЧ-1, причем продукция антител остается на высоком уровне на протяжении всего срока наблюдения(48 суток).
Определение мукозального иммунного ответа. Оценку мукозального ответа проводят путем анализа титра IgA в слизистой кишечника иммунизированных животных. Выделение слизистой кишечника животных проводят согласно методу, описанному в работе [18]. Специфичность образующихся антител класса А определяют методом ИФА, используя в качестве антигенов очищенный вирус ВИЧ-1 и смесь рекомбинантных белков ВИЧ-1: gag, gp120, env1 и env2. Результаты представлены на фиг.4, 5. Продукция специфичных к ВИЧ-1 IgA обнаруживается, начиная с третьей недели после иммунизации, и достигает максимального значения на 35 сутки от начала иммунизации.
Пример 3. Исследование способности целевого штамма индуцировать клеточный иммунный ответ.
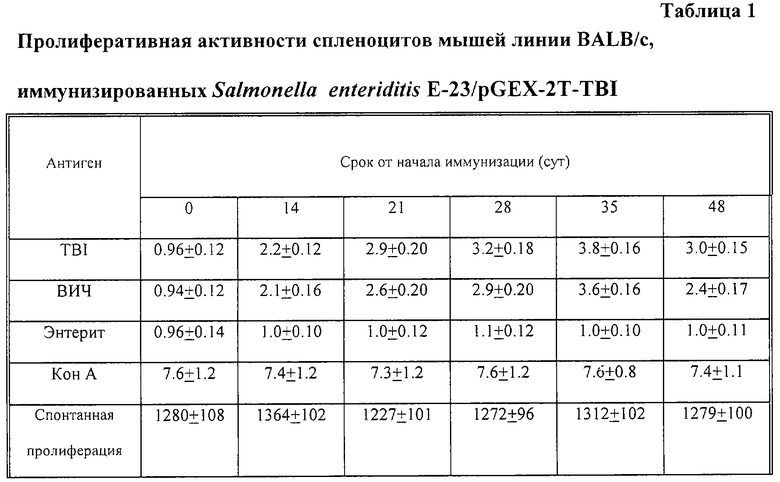
Реакция бласттрансформации. Реакцию бласттрансформации спленоцитов проводят на 0, 14, 21, 28, 35 и 48 сутки после введения сальмонелл по ранее описанной методике [19]. В качестве специфического антигена используют инактивированный ВИЧ-1, в качестве неспецифического антигена - вирус энтерита норки. В лунку планшета вносят по 100 мкл каждого компонента. Концентрация антигенов 2 мкг/мл. В качестве митогена используют конканавалин А (производства "Sigma", США) в концентрации 5 мкг/мл. Клетки, стимулированные антигенами, инкубируют в течение 78 ч. За 18 ч до окончания срока инкубации вносят 3H-тимидин (Санкт-Петербург) в дозе 2 мкКи на лунку. Клеточный ответ оценивают по показателю индекса стимуляции, который характеризует отношение пролиферации спленоцитов, индуцированных специфическими антигенами к спонтанной пролиферации спленоцитов (табл.1). Результаты, приведенные в табл. 1, свидетельствуют о том, что иммунизация клетками Salmonella enteriditis E-23/pGEX-2T-TBI вызывает формирование клона клеток памяти, поскольку индекс стимуляции клеток in vitro специфическими белками ВИЧ достоверно увеличивается (Р<0.01) на 14 сутки по сравнению с показателями на 0 сутки (день проведения иммунизации). Этот показатель сохраняется на высоком уровне на всем сроке наблюдения (48 суток).
Пример 4. Оценка вируснейтрализующей активности сывороток.
Вируснейтрализующую активность сывороток определяют методом учета ингибирования репродукции вируса ВИЧ-1 по снижению его инфекционного титра. Для этого используют перевиваемые лимфобластоидные клетки человека МТ-4. Клетки культивируют в концентрации 3.0-5.0×105 клеток в 1 мл среды RPMI 1640 с 10% сыворотки эмбрионов коров, 100 мкг/мл гентамицина. В реакции вируснейтрализации используют штамм ВИЧ-1899А (Х4), полученный из коллекции штаммов вирусов иммунодефицита человека НИИ вирусологии им. Д.И. Ивановского РАМН. Множественность заражения составляет 100 ТЦД50. Сыворотки инактивируют на водяной бане при температуре 56°С в течение 30 мин. В лунки пластиковой 96-луночной панели (“Costar”, США) вносят по 50 мкл следующих разведении сывороток: 1:10, 1:20, 1:40, 1:80, 1:160, 1:320, 1:640, 1:1280, т.д и добавляют 50 мкл суспензии вируса. Смесь инкубируют в течение 1 ч при 37°С. После инкубации вносят по 100 мкл взвеси чувствительных клеток МТ-4 в количестве 90-100×103 кл/лунку. Панель инкубируют при 37°С в атмосфере с 5% CO2 и 98% влажности в течение 5-7 суток до момента учета результатов. В качестве контролей используют: “контроль вируса” - вирус с добавлением среды без сыворотки, “контроль клеток” - клетки в питательной среде, “контроль цитотоксичности сывороток” - клетки + сыворотки. Учет результатов проводят на 5-7 день после начала эксперимента. Ингибирование репродукции вируса оценивают по снижению его инфекционного титра, который определяют по ТЦД50 (50% тканевая цитопатическая доза). Данные по определению нейтрализующих титров антител в сыворотках крови иммунных животных сведены в табл. 2.
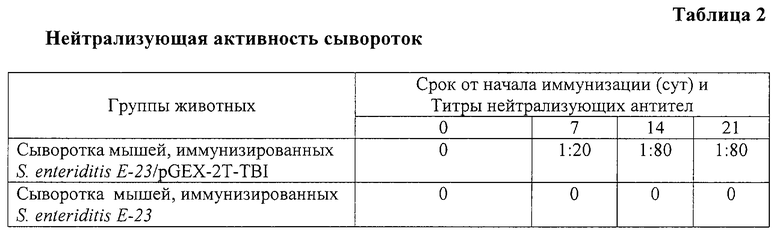
Данные, представленные в табл.2, свидетельствуют о том, что образующиеся после введения рекомбинантного штамма антитела обладают вируснейтрализующей активностью.
Таким образом, сконструированный штамм Salmonella enteriditis E-23/pGEX-2T-TBI продуцирует белок TBI и при введении животным индуцирует выраженный специфический гуморальный (как системный, так и местный) и клеточный иммунный ответ к ВИЧ-1. Предложенный рекомбинантный штамм может быть использован для конструирования живой вакцины против ВИЧ-1.
Источники информации
1. Siebers A., Finlay B.B.M. Cells and the pathogenesis of mucosal and systemic infections. Trends Microbiol. 1996, 4: 22-29.
2. Hopkins S., Kraehenbuhl J-P., Schodel F. et al. A recombinant Salmonella typhimurium vaccine induces local immunity by four different routes of immunization. Infect, and Immun. 1995, 63: 3279-3286.
3. Международная заявка № 98/48026, кл. МПК6: С 12 N 15/74, опубл. 29.10.98 и Бюллетень ИСМ, вып.46, № 10, 1999, стр.124.
4. Khan CM, Villarreal-Ramos В, Pierce RJ et al. Construction, expression, and immunogenicity of multiple tandem copies of the Schistosoma mansoni peptide 115-131 of the P28 glutathione S-transferase expressed as C-terminal fusions to tetanus toxin fragment С in a live aro-attenuated vaccine strain of Salmonella. J. Immunol. 1994, 12: 5634-5642.
5. Sadoff J.C., Ballou W.R., Baron L.S. et al. Oral Salmonella typhimurium vaccine expressing circumsporozoite protein protects against malaria. Science. 1988, 240: 336-338.
6. Hormaeche C.E. Live attenuated Salmonella vaccines and their potential as oral combined vaccines carrying heterologous antigens. J. Immunol. Meth. 1991, 142: 113-120.
7. Fairweather N.F., Chatfield S.N., Makoff A.J. et. al. Oral vaccination of mice against tetanus by use of a live attenuated Salmonella carrier. Infect. Immun. 1990, 58: 1323-1326.
8. Roberts M., Bacon A., Li J. et al. Prior immunity to homologous Salmonella serotypes suppresses local and systemic anti-fragment С antibody responses and protection from tetanus toxin in mice immunized with Salmonella strains expressing fragment C. Infect, and Immun. 1999, 67: 3810-3815.
9. Hormaeche C.E., Khan С.М., Mastroenii P. et al. Salmonella vaccines: mechanisms of immunity and their use as carriers of recombinant antigens. In: Ala Aldenen D.A., Hormaeche C.E. (ed.). Molecular and clinical aspects of bacterial vaccine development. England, Chichester, John Wiley & Sons Ltd., 1995, p.119-154.
10. Международная заявка № 14240, кл. МПК6: С 12 N 15/31, опубл. 16.03.00 и Бюллетень ИСМ, вып.46, № 3, 2001, стр.17.
11. Fouts T.R., Tuskan R.G., Chada S.et al. Construction and immunogenicity of Salmonella typhimurium vaccine vectors that express HIV-1 gp120. Vaccine. 1995, 13(17): 1697-1705.
12. Eroshkin A.M., Karginova E.A., Gileva I.P. et. al. Design of four-helix bundle protein as a candidate for HIV vaccine. Protein Eng. 1995, 8(2): 167-173.
13. Loktev V.B., Ilyichev A.A., Eroshkin A.M. et. al. Design of immunogens as components of a new generation of molecular vaccines. J. Biotechnol. 1996, 44(13): 129-137.
14. Бойченко М.Н., Воробьев А.А., Тымчук С.Н. Перспектива получения мутантов суа и crp сальмонелл для использования в качестве вакцинных штаммов. Вестн. РАМН. 1995, (10): 37-39.
15. Лебедев Л.Р., Карпенко Л.И., Порываева В.А. и др. Конструирование вирусоподобных частиц, экспонирующих эпитопы ВИЧ-1. Молекул. биол. 2000, (3): 280-285.
16. Маниатис Т., Фрич Э., Сэмбрук Дж. Молекулярное клонирование. М.: Мир, - 1984.
17. Laemmli Е. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature. 1970, 227: 680-685.
18. Jackson R.J., Fujihashi K., Xu A.J. et. al. Optimizing oral vaccines: induction of systemic and mucosal B-cell and antibody responses to tetanus toxoid by use of cholera toxin as an adjuvant. Infect. Immun. 1993, 61: 4272-4279.
19. Хоробрых В.В., Пронин А.В., Киркин А.Ф. и др. Методы постановки реакции бласт-трансформации в микромодификации. Иммунология. 1983, (3): 76-79.
| название | год | авторы | номер документа |
|---|---|---|---|
| СУППОЗИТОРИИ ДЛЯ ИММУНОПРОФИЛАКТИКИ ВИРУСНЫХ ИНФЕКЦИЙ | 2004 |
|
RU2296560C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PCDNA-TCI, ОБЕСПЕЧИВАЮЩАЯ ЭКСПРЕССИЮ ИСКУССТВЕННОГО ГЕНА TCI В КЛЕТКАХ ЭУКАРИОТ, И РЕКОМБИНАНТНЫЙ АТТЕНУИРОВАННЫЙ ШТАММ БАКТЕРИЙ SALMONELLA ENTERITIDIS E-23/PCDNA-TCI КАК КАНДИДАТ ДЛЯ КОНСТРУИРОВАНИЯ ЖИВОЙ ДНК-ВАКЦИНЫ ПРОТИВ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2003 |
|
RU2248396C2 |
| ШТАММ БАКТЕРИЙ SALMONELLA ENTERIDITIS E-23 BMC120 ДЛЯ ИММУНИЗАЦИИ ПРОТИВ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2001 |
|
RU2192277C1 |
| РЕКОМБИНАНТНЫЙ АТТЕНУИРОВАННЫЙ ШТАММ БАКТЕРИЙ SALMONELLA TYPHIMURIUM T10/PKHBC - ПРОДУЦЕНТ КОРОВОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В | 2002 |
|
RU2216590C1 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ПРОТИВ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА | 2006 |
|
RU2317107C2 |
| ШТАММ БАКТЕРИЙ SALMONELLA TYPHIMURIUM Т-10 ВМС160 ДЛЯ ИММУНИЗАЦИИ ПРОТИВ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2001 |
|
RU2192886C1 |
| ВАКЦИНА ПРОТИВ ВИРУСНЫХ ИНФЕКЦИЙ | 2000 |
|
RU2217162C2 |
| Рекомбинантный химерный полипептид-иммуноген nTBI, обладающий способностью индуцировать антитела, нейтрализующие вирус иммунодефицита человека 1 типа, и предназначенный для использования в качестве компонента вакцины против ВИЧ-1 | 2016 |
|
RU2642258C1 |
| Искусственный ген YkuJ-MPER, кодирующий химерный белок-иммуноген YkuJ-MPER, рекомбинантная плазмидная ДНК pET21a-YkuJ-MPER, обеспечивающая экспрессию искусственного гена YkuJ-MPER, и химерный белок-иммуноген YkuJ-MPER, являющийся носителем мембранно-проксимальной области ВИЧ-1 и направленный на индукцию в организме широконейтрализующих антител | 2017 |
|
RU2679076C1 |
| РЕКОМБИНАНТНАЯ ПРОТИВОГРИППОЗНАЯ ВАКЦИНА С ШИРОКИМ СПЕКТРОМ ЗАЩИТЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2017 |
|
RU2757013C2 |
Изобретение относится к биотехнологии, конкретно к генетической инженерии. Предложен рекомбинантный аттенуированный штамм бактерий Salmonella enteriditis E-23/pGEX-2T-TBI, продуцирующий искусственный белок TBI, состоящий из Т- и В-клеточных эпитопов ВИЧ-1. Штамм получен путем генетической трансформации штамма Salmonella enteriditis E-23 (суа, CRP) плазмидой pGEX-2T-TBI. При введении животным рекомбинантный штамм микроорганизмов индуцирует выраженный специфический гуморальный и клеточный иммунный ответ к ВИЧ-1. Рекомбинантный штамм может быть использован для конструирования живой вакцины против ВИЧ-1. 5 ил., 2 табл.
Рекомбинантный аттенуированный штамм бактерий Salmonella enteriditis E-23/pGEX-2T-TBI, депонированный в коллекции НИИ ККМ ГНЦ ВБ "Вектор" под номером В-884 - продуцент искусственного белка-иммуногена TBI, содержащего эпитопы нескольких белков ВИЧ-1.
| FOUTS T.R | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Vaccine | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| WO 9939735, 12.08.1999. | |||
Авторы
Даты
2004-09-27—Публикация
2002-10-31—Подача