Изобретение относится к химии производных лактамов, а именно к новому способу получения N-(2-хлоралкил)-и N-алкилароматических производных лактамов общей формулы:

где R=Н, Cl,
R'=(СН2)3, (СН2)5,
которые могут являться модификаторами непредельных карбоцепных каучуков и резиновых смесей на их основе.
Известен способ получения N-(2-хлор-2-метилбутил)-и N-(2-хлор-1-метилбутил)капролактамов присоединением N-хлоркапролактама по двойной связи 2-метилбутена-2 [Хардина И.А., Тужиков О.И., Харченко Н.И., Депон. В ВИНИТИ, №3812 -В97 от 29.12.97, Хардина И.А., Тужиков О.И., Корнеев А.В., Химия и технология элементорганических мономеров и полимерных материалов: Сб. науч. тр. ВолгГТУ, Волгоград, 1996, с.43-51]. Этот способ является наиболее близким к предлагаемому изобретению. Он осуществляется взаимодействием N-хлоркапролактама с 2-метилбутеном-2 в присутствии в качестве катализаторов кислот Льюиса - четыреххлористого титана и четыреххлористого олова - в среде толуола при температуре 20-22°С. Продукты присоединения образуются в условиях электрофильного присоединения по и против правила Марковникова. Данным способом получают N-замещенные лактамы иного строения.
Недостатками данного способа является использование катализаторов кислотного типа, вызывающих частичное разложение N-хлоркапролактама, низкий выход продуктов присоединения (24%) и большая продолжительность синтеза (7-7,5 часов).
Задачей предлагаемого изобретения является разработка технологически приемлемого малостадийного метода синтеза N-замещенных лактамов.
Техническим результатом является сокращение времени реакции в 20-30 раз, расширение ассортимента получаемых соединений, а также упрощение способа выделения целевых продуктов за счет отсутствия стадии щелочного разложения катализаторов и водной промывки реакционной массы.
Поставленный технический результат достигается в новом способе получения N -замещенных лактамов общей формулы:
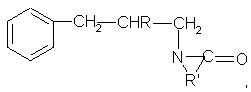
где R=Н, Cl,
R'=(СН2)3, (СН2)5,
заключающимся в присоединении N-хлорлактамов к аллилбензолу, причем в качестве N-хлорлактамов используют N-хлорбутиролактам или N-хлоркапролактам, и процесс проводят при мольном соотношении N-хлорлактама и аллилбензола, равном 1-1,15:1, в присутствии катализатора моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля, взятого в количестве 0,4-4,0% мас., в среде инертного растворителя, например хлорбензола, при температуре 100-125°С в течение 15-20 минут.
Сущностью метода является реакция присоединения N-хлорлактамов к аллилбензолу в условиях радикального инициирования:

где R'=(СН2)3, (СН2)5.
В качестве побочных продуктов образуются лактамы и продукт аллильного галогенирования исходного олефина -1-хлораллилбензол.
Преимуществом данного метода является получение продуктов присоединения с выходом 75-80%, а также возможность получения гомологов данного ряда, которые могут являться модификаторами непредельных неполярных каучуков и резиновых смесей на их основе.
В присутствии перекисного инициатора присоединение N-хлорлактамов по двойной связи протекает против правила Марковникова, при этом образуются два продукта -1,2 и 1,Н - присоединения (I, II).
Образование продуктов присоединения (I, II) можно объяснить природой используемого перекисного катализатора, не активного в побочной реакции дезактивации исходных N-хлорлактамов. В присутствии в качестве катализаторов кислот Льюиса (TiCl4, SnCl4) под действием остаточного хлористого водорода происходит частичное восстановление N-хлорлактамов до лактамов по реакции:
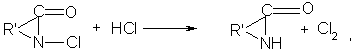
где R'=(СН2)3, (СН2)5,
что снижает выход целевых продуктов.
Образование продуктов присоединения протекает по радикально-цепному механизму. На первой стадии происходит термораспад перекисного инициатора:
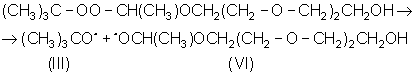
Продукты термораспада пероксиацеталей исследовались в работе [Алейникова Т.П. Дис. канд. хим. наук, Волгоград: Волгоград, политехн. ин-т, 1983.-140 с., Туровский А.А., Навроцкий В.А., Туровский Н.А., Алейникова Т.П., Кущ О.В., ЖОХ, 1985, т.55, вып.1, с.173-176].
Радикал (III) распадается на ацетон и метильный радикал, радикал (IV) фрагментирует с образованием метильного радикала, окиси углерода и триэтиленгликоля. Метальные радикалы взаимодействуют с N-хлорлактамом, генерируя амидильный радикал, присоединяющийся по двойной связи олефина по схеме:
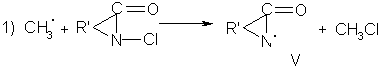
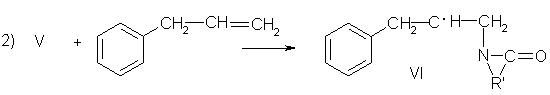





где R'=(СН2)3, (СН2)5.
Определено наиболее эффективное количество пероксида, необходимое для присоединения N-хлорлактамов к аллилбензолу. Так, в случае N-хлоркапролактама оптимальным условием проведения реакции является использование пероксида в количестве 0,4-0,6% мас. от веса N-хлоркапролактама, дальнейшее повышение содержания пероксида приводило к образованию побочных теломерных продуктов аллилбензола. В случае N-хлорбутиролактама оптимальным количеством пероксида является 3,8-4% мас. Оптимальными условиями проведения реакции является температурный интервал 100-125°C (область интенсивного генерирования свободных радикалов пероксидом) и время реакции 15-20 минут. Дальнейшее повышение температуры или увеличение продолжительности реакции нецелесообразно, так как это приводит к осмолению реакционной массы и загрязнению целевых продуктов, а уменьшение температуры приводит к неэффективному длительному протеканию процесса.
Данную реакцию рекомендуется проводить при мольном соотношении N-хлорлактама и аллилбензола 1-1,15:1, т.е. при небольшом избытке N-хлорлактама, что определяется содержанием основного вещества в N-хлорлактамах. Используемые N-хлорлактамы были получены хлорированием лактамов в среде хлороформа; в ходе их выделения при отгонке растворителя происходит частичная потеря активного хлора и восстановление в исходные лактамы, приводящее к образованию N-хлорлактамов с выходом 85-98%. Реакцию следует проводить в высококипящих растворителях, не образующих свободных радикалов и не содержащих подвижных атомов водорода, например хлорбензол, ксилолы и нитробензол. Не рекомендуется использовать в качестве растворителей амины, спирты и карбоновые кислоты, содержащие реакционноспособные по отношению к N-хлорлактамам группы.
Способ осуществляется следующим образом.
К раствору смеси N-хлорлактама и аллилбензола в хлорбензоле в токе аргона при перемешивании по каплям добавляют раствор пероксида в хлорбензоле. Реакционную смесь нагревают при перемешивании в токе инертного газа до температуры 100-125°C и выдерживают при этой температуре в течение 15-20 минут. Указанное время реакции соответствует полному исчерпанию N-хлорлактама в реакционной массе. После этого отгоняют под вакуумом растворитель, непрореагировавший аллилбензол и побочный продукт 1-хлораллилбензол. Осуществляя данный способ в промышленности, можно организовать рецикл аллилбензола и хлорбензола с использованием в последующем синтезе. Полученный маслянистый продукт реакции при необходимости направляется на разделение на целевые продукты и побочные с помощью колоночной хроматографии на силикагеле. Выход целевых продуктов составляет 75-80%.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Синтез N-(2-хлорпропилфенил)капролактама и N-пропилфенилкапролактама.
К продутому аргоном раствору смеси 4,5 г (0,0305 моль) N-хлоркапролактама и 3,6 г (0,0305 моль) аллилбензола (мольное соотношение N-хлоркапролактам: аллилбензол=1:1) в 10 мл хлорбензола при комнатной температуре по каплям добавили раствор 0,028 г (1,05·10-4 моль) моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля в 5 мл хлорбензола и нагревали реакционную массу при перемешивании в токе аргона до 100-125°С.
По достижении температуры в указанном интервале реакционную массу выдерживали при перемешивании в течение 15 минут. После этого отогнали под вакуумом растворитель, 1-хлораллилбензол и непрореагировавший аллилбензол, получили 7,1 г маслянистого продукта, из которого с помощью колоночной хроматографии на силикагеле (элюент - смесь хлороформа, гексана и изопропилового спирта при объемном соотношении 6:9:1) выделено 3,2 г (0,012 моль, 39,3%) N-(2-хлорпропилфенил) капролактама, 2,6 г (0,011 моль, 36,1%) N-пропилфенилкапролактама и 1,3 г капролактама.
N-(2-Хлорпропилфенил) капролактам (I),  =1,0399 г·см-3,
=1,0399 г·см-3, 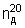 =1,5339. C15H20ClNO.
=1,5339. C15H20ClNO.
Найдено, %: С 67,95, Н 7,67, Cl 13,25, N 5,11.
Вычислено, %: С 67,80, Н 7,53, Cl 13,37, N 5,27.
N-Пропилфенилкапролактам (II),  =1,0254 г (см-3,
=1,0254 г (см-3, 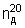 =1,5203. C15H21NO.
=1,5203. C15H21NO.
Найдено, %: С 78,06, Н 9,23, N 5,91.
Вычислено, %: С 77,92, Н 9,09, N 6,06.
ПМР - спектр (I), δ, м.д.: 2,6 д J 7 Гц (2Н, СН2), 3,3 д J 4 Гц (2Н, N-СН2), 4,1 с (1Н, CHCl), протоны фрагмента капролактама -1,67 с (6Н, (СН2)3), 2,7 уш. с (2Н, СО-СН2), 3,1 с (2Н, N-CH2), фенильные протоны -6,6 с (1Н), 6,95 с (2Н), 7,4 с (2Н).
ПМР - спектр (II), δ, м.д.: 1,33-1,5 м (2Н, С-СН2-С), 2,5 д J 7 Гц (2Н, СН2), 3,0 д J 6 Гц (2Н, N-СН2), протоны фрагмента капролактама -1,65 с (6Н, (СН2)3), 2,6 уш. с (2Н, СО-СН2), 3,1 с (2Н, N-СН2), фенильные протоны -6,5 с(1Н), 6,85 с (2Н),7,3 с (2Н).
ИК -спектр (I), ν, см-1: 1084, 1184, 1264 (C-N), 1708 (С=О).
ИК -спектр (II), ν, см-1: 1040, 1164, 1264 (C-N), 1692 (С=О).
Масс-спектр (I), м/е:188

153 (PhCH2CHClCH2 +, 21,6%), 139 (PhCH2C+HCl, 14,0%), 126

91 (PhCH2 + 100%), 77 (Ph+, 27,4%).
Масс-спектр (II), м/е: 154
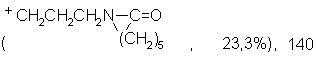

9,6%), 119 (PhCH2CH2CH2 + 19,2%), 105 (PhCH2CH2 +, 23,3%), 91 (PhCH2 +, 100%), 77 (Ph+, 27,0%).
ПМР -спектр капролактама, δ, м.д.: 1,64 с (6Н, (СН2)3), 2,26 д J 7 Гц (2Н, СО-СН2), 3,06 д J 4 Гц (2Н, N-CH2), 8,17 с (1Н, NH).
ИК-спектр капролактама, ν, см-1: 1090, 1120, 1200, 1240, 1260, 1290
(C-N), 1660 (С=O), 3210 (N-H).
Масс-спектр капролактама, м/е: 113 (М+, 100%), 85

Пример 2.
Синтез N-(2-хлорпропилфенил)капролактама и N-пропилфенилкапролактама.
К продутому аргоном раствору смеси 5,2 г (0,035 моль) N-хлоркапролактама и 3,6 г (0,0305 моль) аллилбензола (мольное соотношение N-хлоркапролактам: аллилбензол=1,15:1) в 12 мл хлорбензола при комнатной температуре по каплям добавили раствор 0,03 г (1,1·10-4 моль) моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля в 5 мл хлорбензола и нагревали реакционную массу при перемешивании в токе аргона до 100-125°С.
По достижении температуры в указанном интервале реакционную массу выдерживали при перемешивании в течение 15 минут. После этого отогнали под вакуумом растворитель, 1-хлораллилбензол и непрореагировавший аллилбензол, получили 7,7 г маслянистого продукта, из которого с помощью колоночной хроматографии на силикагеле (элюент - смесь хлороформа, гексана и изопропилового спирта при объемном соотношении 6:9:1) выделено 3,4 г (0,0128 моль, 42%) N-(2-хлорпропилфенил) капролактама, 2,5 г (0,0108 моль, 35,4%) N-пропилфенилкапролактама и 1,8 г капролактама.
Пример 3.
Синтез N-(2-хлорпропилфенил)бутиролактама и N-пропилфенилбутиролактама.
К раствору смеси 5,8 г (0,049 моль) N-хлорбутиролактама и 5,7 г (0,048 моль) аллилбензола (мольное соотношение N-хлорбутиролактам: аллилбензол=1:1) в 24 мл хлорбензола при комнатной температуре по каплям в токе аргона добавили раствор 0,224 г (8,4·10-4 моль) моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля в 8 мл хлорбензола и нагревали реакционную массу при перемешивании в токе аргона до 100-125°С.
По достижении температуры в указанном интервале реакционную массу выдерживали при перемешивании в течение 20 минут. Затем отогнали под вакуумом растворитель, 1-хлораллилбензол и непрореагировавший аллилбензол, получили 10 г маслянистого продукта, из которого с помощью колоночной хроматографии на силикагеле (элюент -смесь хлороформа, гексана и изопропилового спирта в соотношении 6:9:1) выделено 5 г (0,021 моль, 43,8%) N-(2-хлорпропилфенил)бутиролактама, 3,4 г (0,017 моль, 35,4%) N-пропилфенилбутиролактама и 1,6 г бутиролактама.
N-(2-Хлорпропилфенил)бутиролактам (III),  =1,0576 г·см-3,
=1,0576 г·см-3, 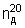 =1,5303. C13H16ClNO.
=1,5303. C13H16ClNO.
Найдено, %: С 65,82, Н 6,88, Cl 14,83, N 5,74.
Вычислено, %: С 65,68, Н 6,74, Cl 14,95, N 5,89.
N-Пропилфенилбутиролактам (IV),  =1,0289 г·см-3,
=1,0289 г·см-3, 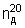 =1,5263. C13H17NO.
=1,5263. C13H17NO.
Найдено, %: С 77,0, Н 8,52, N 6,74.
Вычислено, %: С 76,85, Н 8,37, N 6,90.
ПМР - спектр (III), δ, м.д.: 2,8 д J 6 Гц (2Н, СН2), 3,4 д J 6 Гц (2Н, N-СН2), 4,1 с (1Н, CHCl), протоны фрагмента бутиролактама -1,75 с (2Н, СН2), 2,9 уш. с (2Н, СО-СН2), 3,3 с (2Н, N-CH2), фенильные протоны -6,8 с (1Н), 7,3 с (2Н), 7,8 с (2Н).
ПМР - спектр (IV), δ, м.д.: 1,45 уш. с (С-СН2-С), 2,7 д J 7 Гц (2Н, СН2), 3,2 т J 6 Гц (2Н, N-СН2), протоны фрагмента бутиролактама -1,72 с (2Н, СН2), 2,8 уш. с (2Н, СО-СН2), 3,3 с (2Н, N-СН2), фенильные протоны -6,7 с (1Н), 7,2 с (2Н), 7,6 с (2Н).
ИК - спектр (III), ν, см-1: 1076, 1284 (C-N), 1700 (С=O).
ИК - спектр (IV), ν, см-1: 1032, 1284 (C-N), 1688 (С=O).
Масс- спектр (III), м/е: 160
 153 (PhCH2CHClCH2 +, 21,6%), 139 (PhCH2C+HCl, 12,5%), 98
153 (PhCH2CHClCH2 +, 21,6%), 139 (PhCH2C+HCl, 12,5%), 98
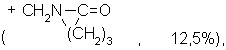 (PhCH2 +, 100%), 77 (Ph+, 28,6%).
(PhCH2 +, 100%), 77 (Ph+, 28,6%).
Масс-спектр (IV), м/е: 126
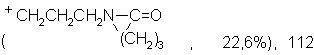

(PhCH2CH2CH2 +, 18,0%), 105 (PhCH2CH2 +, 21,8%), 91 (PhCH2 +, 100%), 77 (Ph+ 28,0%).
ПМР -спектр бутиролактама, δ, м.д.: 1,7 с (2Н, СН2), 2,5 д J 6 Гц (2Н, СО-СН2), 3,2 д J 4 Гц (2Н, N-CH2), 8,2 с (1Н, NH).
ИК -спектр бутиролактама, ν, см-1: 1068, 1168, 1276 (C-N), 1664 (С=О), 3200 (N-H).
Пример 4.
Синтез N-(2-хлорпропилфенил)бутиролактама и N-пропилфенилбутиролактама.
К раствору смеси 6,6 г (0,055 моль) N-хлорбутиролактама и 5,7 г (0,048 моль) аллилбензола (мольное соотношение N-хлорбутиролактам аллилбензол=1,15:1) в 26 мл хлорбензола при комнатной температуре по каплям в токе аргона добавили раствор 0,25 г (9,4·10-4 моль) моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля в 10 мл хлорбензола и нагревали реакционную массу при перемешивании в токе аргона до 100-125°С.
По достижении температуры в указанном интервале реакционную массу выдерживали при перемешивании в течение 20 минут. Затем отогнали под вакуумом растворитель, 1-хлораллилбензол и непрореагировавший аллилбензол, получили 10,5 г маслянистого продукта, из которого с помощью колоночной хроматографии на силикагеле (элюент - смесь хлороформа, гексана и изопропилового спирта в соотношении 6:9:1) выделено 5,2 г (0,022 моль, 45,8%) N-(2-хлорпропилфенил)бутиролактама, 3,3 г (0,0163 моль, 34%) N-пропилфенилбутиролактама и 2 г бутиролактама.
Таким образом, разработан технологически малостадийный метод синтеза N-замещенных лактамов, образующихся с выходом до 80%. Структура описанных соединений подтверждена ПМР-, ИК- и масс-спектрами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-АЛКОКСИДИАЛКИЛПЕРОКСИДОВ | 2005 |
|
RU2284321C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-5,6-ДИ (ЗАМЕЩЕННЫХ)-ГЕПТ-1-ЕНОВ | 1993 |
|
RU2100337C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ β-ДИКЕТОНОВ И КЕТОЭФИРОВ | 2000 |
|
RU2187493C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛ-2-(4-МЕТИЛФЕНИЛ)-ИМИДАЗОЛО[1,2-А]-ПИРИДИН-3-(N, N-ДИМЕТИЛАЦЕТАМИДА), ЭФИРЫ, КРИСТАЛЛИЧЕСКИЕ ЭФИРЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2254334C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ (2-ДИАЛКОКСИФОСФОРИЛ-4-ЦИАНО)БУТАНАМИДИНОВ | 2009 |
|
RU2385870C1 |
| Способ получения лактамоалюминатов натрия | 1976 |
|
SU739070A1 |
| Способ получения -ацетиленовых спиртов | 1977 |
|
SU745888A1 |
| Способ получения N-С @ -С @ -ацилированных лактамов | 1985 |
|
SU1311206A1 |
| Способ получения производных пергидротиазепина или их аддитивных солей с галоидводородными кислотами | 1986 |
|
SU1801110A3 |
| Способ получения 13-кето-13Н-6,11-дигидроизохино[3,2-в]хиназолина | 1987 |
|
SU1558914A1 |
Изобретение относится к химии производных лактамов, а именно к способу получения N-(2-хлоралкил)- и N-алкилароматических производных лактамов общей формулы:
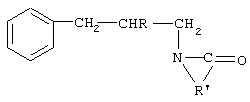
где R=Н, Cl,
R'=(СН2)3, (СН2)5,
которые могут являться модификаторами непредельных карбоцепных каучуков и резиновых смесей на их основе. Способ получения указанных N-замещенных лактамов заключается в присоединении N-хлорлактамов к аллилбензолу, причем в качестве N-хлорлактамов используют N-хлорбутиролактам или N-хлоркапролактам. Процесс проводят при мольном соотношении N-хлорлактама к аллилбензолу, равном 1-1,15:1, в присутствии катализатора моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля, взятого в количестве 0,4-4,0% мас., в среде инертного растворителя, например хлорбензола, при температуре 100-125°C в течение 15-20 минут. Технический результат - сокращение времени реакции в 20-30 раз, упрощение способа выделения целевых продуктов, а также расширение ассортимента получаемых соединений.
Способ получения N-замещенных лактамов общей формулы:
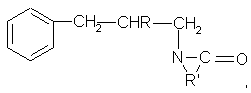
где R=Н, Cl;
R'=(СН2)3, (СН2)5,
заключающийся в присоединении N-хлорлактамов к аллилбензолу, причем в качестве N-хлорлактамов используют N-хлорбутиролактам или N-хлоркапролактам, процесс проводят при мольном соотношении N-хлорлактама и аллилбензола, равном 1-1,15:1, в присутствии катализатора моно-трет-бутилперокси-α-метилметоксиэтоксиэтилового эфира этиленгликоля, взятого в количестве 0,4-4,0 мас.%, в среде инертного растворителя, например хлорбензола, при температуре 100-125°C в течение 15-20 мин.
| ХАРДИНА И.А | |||
| и др | |||
| Химия и технология элементорганических мономеров и полимерных материалов | |||
| Сб | |||
| научн | |||
| тр | |||
| ВолгГТУ | |||
| Волгоград, 1996, с | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| N-( α -АЛКОКСИАЛКИЛ)КАПРОЛАКТАМЫ, ОБЛАДАЮЩИЕ ИНСЕКТО- И АКАРОРЕПЕЛЛЕНТНОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2017732C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(p, р-ДИХЛОРВИНИЛ)-ЛАКТАМОВ | 0 |
|
SU349687A1 |
Авторы
Даты
2005-02-20—Публикация
2003-08-27—Подача