Изобретение относится к области органической химии и может найти применение в аналитической химии, биоорганической химии, биохимии и прикладной медицине.
При изучении физиологически активных соединений необходимы их меченые аналоги.
Известен (S)-α-циано-3-феноксибензил-(1R)-(2',2'-дибромвинил)-2,2-диметилциклопропанкарбоксилат формулы
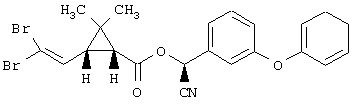
Данное соединение, получившее наименование “дельтаметрин”, является синтетическим пиретроидом, сильным ингибитором нервной проводимости и применяется как инсектицид (E.Enan et al. //Biochem.Parmacol. 1992. Vol.43. 1777. A.Enz, E.Pombo-Villar// Biochem.Parmacol. 1997. Vol.54. 321).
Однако его меченный тритием аналог не описан.
Техническим результатом, достигаемым настоящим изобретением, является расширение ассортимента меченых аналогов физиологически активных соединений.
Достигается указанный технический результат получением высокомеченного тритием [3H]-(S)-α-циано-3-феноксибензил-(1R)-(2',2'-дибромвинил)-2,2-диметилциклопропанкарбоксилата формулы

Ниже приведен пример реализации изобретения.
Известно, что замена атомов соединений на их меченые аналоги не приводит к изменению каких-либо свойств исходного соединения (Evans Е.А. - Tritium and its compounds London Butterworths, 1974, p.48).
Пример.
В первую камеру двухкамерной реакционной ампулы помещали 55 мг 5%PdO/BaSО4 и 55 мг PdO, во вторую - раствор 20 мг дельтаметрина в 250 мкл смеси диоксана с триэтиламином (10:1). Вторую камеру замораживали жидким азотом, ампулу вакуумировали до давления 0,1 Па и заполняли газообразным тритием до давления 400 гПа. Затем первую камеру нагревали до 70°С. При этом окись палладия восстанавливалась, а тритиевая вода перемораживалась во вторую камеру. Реакционную ампулу вакуумировали до давления 0,1 Па, продолжая нагревать первую камеру до 70°С, и заполняли аргоном. Затем содержимое второй камеры переносили в первую камеру, которую запаивали. Таким образом, реакционная смесь в первой камере состояла из восстановленного катализатора, 100% тритиевой воды, триэтиламина и раствора дельтаметрина в диоксане. Содержимое ампулы нагревали в течение 20 мин при 140°С. Затем ее вскрывали, реакционную смесь разбавляли 0,5 мл хлороформа, катализатор отделяли фильтрованием и промывали последовательно хлороформом (3×1 мл) и метанолом (3×1 мл) (общая радиоактивность реакционной смеси 12,5 Ки). Тритиевую воду, диоксан и триэтиламин отгоняли на роторе. Лабильный тритий удаляли, несколько раз растворяя вещество в метаноле (5х2 мл) и упаривая последний (общая радиоактивность реакционной смеси стала 0,6 Ки).
Очистку меченого препарата осуществляли методом ВЭЖХ в две стадии:
1) на колонке 4,6×150 мм Kromasil 100, 5 мкм, С18, v 1,0 мл/мин, в системе метанол-вода (90:10), время удерживания 4,86 мин.
2) на колонке 4,6×150 мм Kromasil 100, 5 мкм, C18, v 1,0 мл/мин, в системе метанол-вода (85:15), время удерживания 10,02 мин.
Выход меченого дельтаметрина 37% с молярной радиоактивностью 9,3 Ки/ммоль.
Таким образом, получено новое высокомеченное тритием физиологически активное соединение.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [H]-(E)-N-[(4-ГИДРОКСИ-3-МЕТОКСИФЕНИЛ)МЕТИЛ]-8-МЕТИЛ-6-НОНЕНАМИД | 2004 |
|
RU2268256C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [H]-РАПАМИЦИН | 2003 |
|
RU2233285C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [H]-АЦЕТОНИД 9АЛЬФА-ФТОРО-16АЛЬФА-ГИДРОКСИПРЕДНИЗОЛОНА | 2004 |
|
RU2278122C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [Н]-5-ХЛОРО-8-ГИДРОКСИХИНОЛИН | 2005 |
|
RU2284322C1 |
| МЕЧЕННЫЙ ТРИТИЕМ 2-АРАХИДОНОИЛ-[1,3-H]-ГЛИЦЕРИН | 2005 |
|
RU2280024C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ [Н]АМФОТЕРИЦИН В | 2006 |
|
RU2323224C1 |
| РАВНОМЕРНОМЕЧЕННАЯ ТРИТИЕМ [H]ТРАНС-3,7-ДИМЕТИЛ-9-(2,6,6-ТРИМЕТИЛ-3-ОКСО-1-ЦИКЛОГЕКСЕН-1-ИЛ)-2,4,6,8-НОНАТЕТРАЕНОВАЯ КИСЛОТА | 2006 |
|
RU2318806C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ [H]-14-ГИДРОКСИДАУНОМИЦИН АДРИАМИЦИНОНА | 2006 |
|
RU2305103C1 |
| ВЫСОКОМЕЧЕННАЯ ТРИТИЕМ 7-(4'-ДИМЕТИЛАМИНО-ФЕНИЛ)-7-ОКСО-2,4-ГЕПТАДИЕНГИДРОКСАМОВАЯ КИСЛОТА | 2001 |
|
RU2206562C1 |
| ВЫСОКОМЕЧЕННЫЕ ТРИТИЕМ МОНОФТОРХИНОЛОНЫ | 2001 |
|
RU2191187C1 |
Настоящее изобретение относится к области органической химии и может найти применение в аналитической химии, биоорганической химии, биохимии и прикладной медицине. Сущность изобретения заключается в том, что получен высокомеченный тритием аналог физиологически активного соединения - [3H](S)-α-циано-3-феноксибензил-(1R)-(2',2'-дибромвинил)-2,2-диметилциклопропанкарбоксилат формулы

Высокомеченный тритием [3H](S)-α-циано-3-феноксибензил-(1R)-(2',2'-дибромвинил)-2,2-диметилциклопропанкарбоксилат формулы

| RU 2058888 C1, 27.04.1996 | |||
| МАШИНА ДЛЯ НАНЕСЕНИЯ МЕРЕИ И ГЛАЖЕНИЯ КОЖИ | 1967 |
|
SU223989A1 |
| US 5242907 A, 07.09.1993 | |||
| ENZ A | |||
| ET AL., "Class II Pyrethroids: Noninhibitors Calcineurin", Biochemical Pharmacology, 1997, v.54, №1, p.321-323. | |||
Авторы
Даты
2005-03-27—Публикация
2003-12-19—Подача