Данное изобретение относится к способу выявления и количественного определения специфичной ДНК или РНК с использованием способа изометричного удлинения праймера (ИУП).
Традиционные способы выявления и количественного определения уникальных последовательностей нуклеиновых кислот, таких как ДНК и РНК, включают в себя наряду с другими способами Саузерн-блоттинг, Нозерн-анализ и анализ методом защиты от РНКазы и полимеразную цепную реакцию (ПЦР). Однако, если обсуждается выявление специфичного вида РНК в образце, то Нозерн-блоттинг и анализ методом защиты от РНКазы имеют ограничения, связанные с эффективностью, трудоемкостью, точностью, высокой стоимостью, чувствительностью, необходимостью в образце РНК большего размера, специализированным оборудованием и большим количеством биологически опасного материла и радиоизотопных отходов, которые при этом образуются. В частности, как Нозерн-блоттинг, так и анализ методом защиты от РНКазы требуют 2-3 дня для выполнения анализов. Кроме того, Нозерн-блоттинг требует разгонки РНК в геле, перенесения РНК на твердую подложку, подготовку пробы и выполнение реакции гибридизации. Требования по чувствительности составляют 5 мкг образца для адекватной чувствительности. Нозерн-блоттинг основан на принципе гибридизации между мишенью и нуклеиновой кислотой зонда. Кроме того, стоимость реакции довольно высока, так же как и количество биологически опасного материала и радиоизотопных отходов, которые при этом образуются.
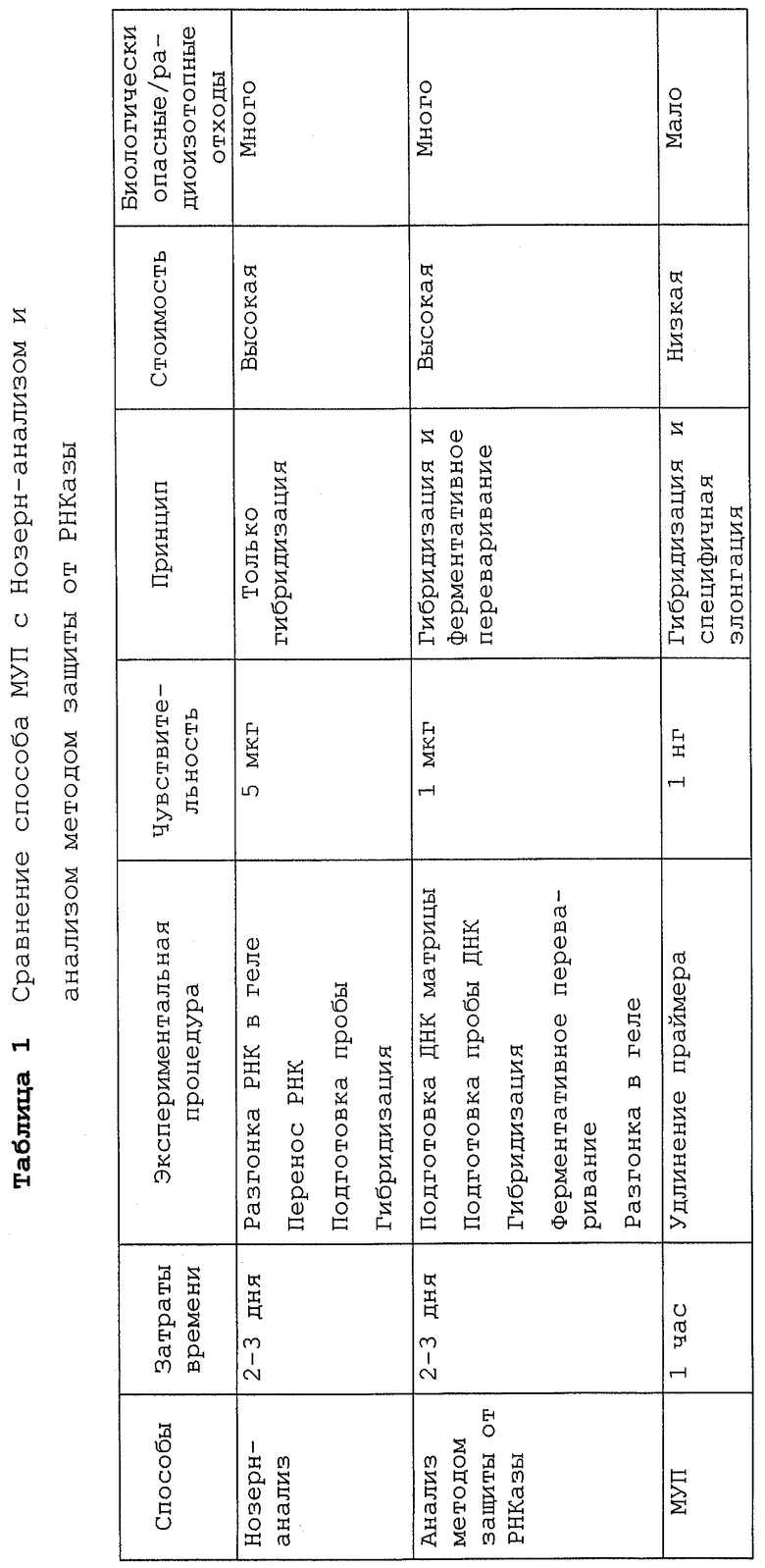
Сходным образом анализ методом защиты от РНКазы требует 2-3 дня для получения соответствующих результатов. Экспериментальная процедура требует приготовления матрицы ДНК, приготовления РНК-зонда, проведения реакции гибридизации, реакции ферментативного переваривания и разгонки в геле. Чтобы получить хорошие результаты, необходим 1 мкг образца РНК-мишени. Принцип анализа методом защиты от РНКазы состоит в комбинации реакций гибридизации и ферментативного переваривания. Как и в способе Нозерн-блоттинга, выполнение данной реакции является дорогостоящим. Кроме того, в больших количествах образуются биологически опасные и являющиеся радиоизотопными отходами продукты. Таблица сравнения различных факторов, связанных с Нозерн-блоттингом, анализом методом защиты от РНКазы и способом множественного удлинения праймера (МУП) согласно данному изобретению представлена в таблице 1.
В патенте США No 5846710 заявлено применение технологии удлинения праймера для скрининга различных молекул РНК. Однако в этом патенте не заявлено выявление ДНК- или РНК-мишени в образце.
В патенте США No 5994079 показано формирование РНК/ДНК гибрида посредством отжига ДНК-праймера со специфичной РНК и удлинение праймера с использованием обратной транскриптазы. Гибрид выявляют с помощью антитела, специфичного для гибрида РНК/ДНК. Однако в этом патенте не заявлено выявление ДНК- или РНК-мишени в образце, как в данном изобретении.
Общепризнано, что в данной области существует необходимость в способе выявления нуклеиновой кислоты, который прост, расходует меньше времени, чувствителен, рентабелен с точки зрения затрат и оказывает небольшое вредное влияние на окружающую среду. Данное изобретение, как описано ниже, отвечает всем этим требованиям.
Данное изобретение удовлетворяет указанным выше необходимостям.
Направлением данного изобретения является способ выявления или количественного определения в образце нуклеиновой кислоты, являющейся мишенью, который включает в себя:
(a) приготовление праймера или праймеров, специфично совпадающих с предварительно определяемым положением нуклеиновой кислоты-мишени;
(b) отжиг праймера или праймеров по пункту (а) с нуклеиновой кислотой-мишенью в условиях высокой жесткости для получения дуплекса праймер-нуклеиновая кислота в предварительно определяемом положении нуклеиновой кислоты-мишени;
(c) смешивание дуплекса праймер-нуклеиновая кислота по пункту (b) со смесью, содержащей
(1) один или два, или три типа свободных нетерминирующих нуклеотидов и по меньшей мере один тип нетерминирующего нуклеотида, который необязательно мечен регистрируемым маркером, и
(2) в присутствии или в отсутствие терминирующего нуклеотида такого типа, который отличается от одного или двух, или трех типов нетерминирующих нуклеотидов по пункту (1);
(d) выполнение удлинения праймера посредством ферментативной или химической реакции в соответствующем буфере; и либо
(e) выявление или количественное определение количества сигнала метки на нуклеотидах, удлиняющих праймер, либо
(f) выявление или количественное определение количества удлиненных праймеров с помощью масс-спектрометрии.
В указанном выше способе праймером может быть праймер нуклеиновой кислоты, олигодезоксирибонуклеотид, олигорибонуклетид или сополимер дезоксирибонуклеиновой кислоты и рибонуклеиновой кислоты. Представляющей интерес нуклеиновой кислотой может быть дезоксирибонуклеиновая кислота, рибонуклеиновая кислота или сополимер дезоксирибонуклеиновой кислоты и рибонуклеиновой кислоты.
В предпочтительном варианте способ может включать в себя применение смеси, содержащей следующую комбинацию нетерминирующих и терминирующих нуклеотидов:
(a) dATP, dCTP, dGTP, ddTTP или ddUTP,
(b) dATP, dCTP, dTTP или dUTP, ddGTP,
(c) dATP, dGTP, dTTP или dUTP, ddCTP,
(d) dCTP, dGTP, dTTP или dUTP, ddATP,
(e) dATP, dCTP, dGTP,
(f) dATP, dCTP, dTTP или dUTP,
(g) dATP, dGTP, dTTP или dUTP, или
(h) dCTP, dGTP, dTTP или dUTP.
В способе данного изобретения можно использовать по меньшей мере один нетерминирующий нуклеотид, который метят регистрируемым маркером. Регистрируемый маркер может содержать фрагмент фермента или белка, радиоактивный изотоп, флуоресцентный фрагмент или химическую группу, такую как биотин. Кроме того, этап способа выявления или количественного определения можно выполнить посредством масс-спектрометрии.
Некоторые ферменты, используемые в реакции удлинения праймера согласно изобретению, включают в себя зависимый от матрицы фермент, такой как ДНК-полимераза I E.coli или "фрагмент Кленова" этой полимеразы, ДНК-полимераза Т4, ДНК-полимераза Т7, ДНК полимераза T.aquaticus, обратная транскриптаза ретровирусов, или их комбинацию.
Приведенные и другие предметы изобретения будут более полно понятны из последующего описания изобретения, справочных чертежей, прилагаемых к нему, и прилагаемой к нему формулы изобретения.
Описание чертежей
Фигура 1 представляет собой схему реакции множественного удлинения праймера для выявления и количественного определения специфичной последовательности ДНК.
Фигура 2 представляет собой схему применения способа множественного удлинения праймера для выявления и количественного определения РНК.
Направлением данного изобретения является способ выявления и количественного определения специфичной нуклеотидной последовательности с использованием способа изометричного удлинения праймера (ИУП).
Резюмируя изобретение, ДНК- или РНК-мишень в образце гибридизуют с единственным или множественными олигонуклеотидными праймерами. Затем праймер(ы) удлиняют с помощью ДНК-полимеразы или обратной транскриптазы в присутствии одного, двух или трех типов предварительно меченых свободных нуклеотидов. По меньшей мере один из четырех типов нуклеотидов, необходимых для непрерывного удлинения, не включают в реакцию или заменяют соответствующим типом нуклеотида-терминатора, такого как дидезоксинуклеотиды. Затем специфичная нуклеиновая кислота-мишень может быть выявлена и количественно определена посредством измерения наличия или отсутствия сигнала, создаваемого меткой на удлиненном праймере(ах). Когда удлиненный праймер отделяют от свободных нуклеотидов, удлиненный праймер анализируют на включение метки.
Праймер, соответствующий положению на нуклеиновой кислоте-мишени, будет удлинен, и будет получена популяция нуклеиновых кислот удлиненного праймера одинаковой длины (изометричных), поскольку в зависимости от последовательности будет включено определенное количество нуклеотидов. Количественное определение указанных одинаково удлиненных праймеров будет точным измерением числа или количества нуклеиновой кислоты-мишени. Если в образце имеется много копий ДНК- или РНК-мишени, количество копий продукта удлинения праймера, включающего в себя меченый нуклеотид, будет соответственно возрастать, способствуя более интенсивному общему сигналу. Таким образом, путем сравнения интенсивности сигнала, наблюдаемого в неизвестном образце, со стандартизованным известным количеством ДНК или РНК можно выявить и/или количественно определить количество ДНК- или РНК-мишени в образце. В другом варианте специфичная нуклеиновая кислота-мишень может быть выявлена или количественно определена посредством измерения количества указанных видов нуклеиновых кислот удлиненного праймера равной длины с использованием метода масс-спектрометрии.
Отсутствие свободного нуклеотида в реакционном буфере вызывает терминацию удлинения праймера там, где был бы встроен пропущенный нуклеотид. Таким образом, получают дискретную длину продукта удлинения праймера.
В области данного изобретения возможны многие очевидные варианты. Например, в реакции удлинения праймера может отсутствовать не только один тип нуклеотида, а два или три типа нуклеотидов. Также можно использовать различные метки, которые не ограничены радиоактивными нуклеотидами, но могут быть флуоресцентными, а также ферментативными.
В используемом здесь смысле "нуклеиновой кислотой" или "нуклеотидом" может быть дезоксирибонуклеиновая кислота, рибонуклеиновая кислота или сополимер дезоксирибонуклеиновой кислоты и рибонуклеиновой кислоты. Образец нуклеиновых кислот может быть природным или синтетическим. Образцом нуклеиновой кислоты может быть нуклеиновая кислота природного происхождения, и она может быть получена из любого организма. Некоторые примеры организмов, к которым применим способ данного изобретения, включают в себя растения, микроорганизмы, вирусы, птиц, позвоночных, беспозвоночных, млекопитающих, организм человека, лошадей, собак, коров, кошек, свиней или овец. Нуклеиновая кислота-мишень может быть природного происхождения или может быть синтезирована ферментативным путем in vivo, синтезирована ферментативным путем in vitro или синтезирована неферментативным путем.
Образец, содержащий представляющую интерес нуклеиновую кислоту или кислоты, может включать в себя геномную ДНК организма, ее РНК-транскрипты или кДНК, полученную с ее РНК-транскриптов. Образец, содержащий представляющую интерес нуклеиновую кислоту или кислоты, также может включать в себя внегеномную ДНК из организма, ее РНК-транкрипты, или кДНК, полученную на ее РНК-транскриптах. Также представляющая интерес нуклеиновая кислота или кислоты могут быть синтезированы посредством полимеразной цепной реакции.
Представляющая интерес нуклеиновая кислота может включать в себя неприродные аналоги нуклеотидов, такие как дезоксиинозин или 7-деаза-2-дезоксигуанозин. Указанные аналоги дестабилизируют дуплексы ДНК и могут дать возможность для отжига праймера и реакции удлинения так, чтобы они происходили в двунитевом образце без полного разделения нитей.
Представляющая интерес нуклеиновая кислота может включать в себя один или большее количество фрагментов, которые позволяют аффинно отделять представляющую интерес нуклеиновую кислоту от не включенного реагента и/или праймера. Например, представляющая интерес нуклеиновая кислота может содержать биотин, который обеспечивает возможность аффинного отделения представляющей интерес нуклеиновой кислоты от невключенного реагента и/или праймера посредством связывания биотина с молекулами семейства авидина, которые связаны с твердым носителем. Последовательность представляющей интерес нуклеиновой кислоты может содержать последовательность ДНК или РНК, которая дает возможность для аффинного отделения интересующей нуклеиновой кислоты от невключенного реагента и/или праймера посредством образования пар оснований с комплементарной последовательностью, присутствующей в нуклеиновой кислоте, связанной с твердым носителем. Представляющая интерес нуклеиновая кислота может быть мечена регистрируемым маркером; указанный регистрируемый маркер может отличаться от любого регистрируемого маркера, присутствующего в реагенте или связанного с праймером.
В используемом здесь смысле термин "нормальный нуклеотид" или "нормальное основание" определяют как нуклеотидное основание дикого типа или ранее известное стандартное нуклеотидное основание, для которого стараются идентифицировать мутацию в сайте основания. Термином "стандартное нуклеотидное основание" обозначено понятие, которое включает в себя любое известное основание, которое может включать в себя основание дикого типа, или известное мутантное основание, при условии, что основание известно, и требуется узнать его вариант. Таким образом, в качестве примера нормальным основанием может быть известное основание дикого типа, для которого ищут мутации в данном положении. Наоборот, известным основанием может быть известный мутант, для которого ищут основание дикого типа в данном положении. В альтернативном случае известным нормальным основанием может быть известный мутант, для которого ищут другой мутантный вариант основания. Поэтому способ согласно изобретению можно применять к любой известной последовательности, которая может быть использована для определения присутствия любого другого варианта основания в данном сайте.
В используемом здесь смысле термин "праймер" или "олигонуклеотидный праймер" относится к олигонуклеотиду, который способен действовать как точка инициации синтеза в том случае, когда он помещен в условия, которые позволяют осуществлять синтез продукта удлинения праймера, который комплементарен нити нуклеиновой кислоты (матрице), в присутствии различных факторов, например таких, как нуклеотиды и ферменты, такие как ДНК-полимераза, и при соответствующей температуре и рН.
Альтернативным образом термин "праймер" определяют как любой фрагмент нуклеиновой кислоты, полученный из любого источника. Например, праймер может быть получен фрагментацией фрагментов нуклеиновой кислоты большего размера, таких как геномная ДНК, кДНК или ДНК, которая была получена посредством ПЦР. Другими словами, природа праймера не ограничена тем, как праймер получен - фрагментацией ли нуклеиновой кислоты природного или синтетического происхождения или синтезом нуклеиновой кислоты праймера. Кроме того, праймером может быть олигодезоксирибонуклеотид, сополимер олигодезоксирибонуклеотидов, олигорибонуклеотиды, сополимер рибонуклеотидов или сополимер дезоксирибонуклеотидов и рибонуклеотидов. Праймер может быть либо природным, либо синтетическим. Олигонуклеотидный праймер может быть синтезирован либо ферментативным путем in vivo, ферментативно in vitro либо неферментативным путем in vitro. Праймер можно метить регистрируемым маркером, этот регистрируемый маркер может отличаться от любого регистрируемого маркера, присутствующего в реагенте, или соединенного с интересующей нуклеиновой кислотой. Кроме того, праймер должен иметь последовательность, соответствующую фланкирующей последовательности в конкретном интересующем положении рядом и выше по течению идентифицируемого нуклеотидного основания.
Кроме того, праймер должен обладать способностью к гибридизации или отжигу с нуклеотидами, присутствующими в интересующей нуклеиновой кислоте. Одним из путей выполнения требуемой гибридизации является наличие зависимого от матрицы праймера, являющегося в значительной степени комплементарным или полностью комплементарным известной последовательности оснований.
Олигонуклеотидный праймер может содержать один или большее количество компонентов, которые связывают праймер с твердым носителем для аффинного отделения праймера от невключенного реагента и/или интересующей нуклеиновой кислоты. Такие аффинные компоненты включают в себя, не ограничиваясь этим, дигитонин, магнитные шарики и лиганды, такие как белковые лиганды, включая антитела. Предпочтительно компонентом является биотин. В случае использования биотина праймер, содержащий биотин, делает возможным аффинное отделение праймера от невключенного реагента и/или интересующей нуклеиновой кислоты посредством связывания биотина со стрептавидином, который связан с твердым носителем. Последовательность олигонуклеотидного праймера может включать в себя последовательность ДНК, которая делает возможным аффинное отделение праймера от невключенного реагента и/или интересующей нуклеиновой кислоты посредством спаривания оснований с комплементарной последовательностью, присутствующей в нуклеиновой кислоте, связанной с твердым носителем.
В используемом здесь смысле термин "реакция удлинения праймера" относится к условиям реакции, при которых проводят зависимую от матрицы реакцию синтеза нуклеиновой кислоты. Условия для осуществления зависимой от матрицы реакции удлинения праймера могут быть созданы, в частности, за счет присутствия подходящего зависимого от матрицы фермента. Некоторыми подходящими, зависимыми от матрицы ферментами, являются ДНК-полимеразы. ДНК-полимераза может быть нескольких типов. Однако ДНК-полимераза должна быть зависимой от праймера и матрицы. Например, в некоторых протоколах также могут быть использованы ДНК-полимераза I E.coli или ее "фрагмент Кленова", ДНК-полимераза Т4, ДНК-полимераза Т7 ("секвеназа"), ДНК-полимераза T.aquaticus или обратная транскриптаза ретровирусов. В некоторых протоколах также могут быть использованы РНК-полимеразы, такие как РНК-полимераза Т3 или Т7. В зависимости от полимеразы должны быть использованы различные условия, и для реакций гибридизации и удлинения праймера могут требоваться различные пределы температуры.
В используемом здесь смысле термин "нить удлинения праймера" включает в себя нить, которая образуется в дуплексе напротив матрицы после добавления праймера. Предпочтительно удлинение праймера прекращается в результате включения терминатора в нить удлинения праймера.
В используемом здесь смысле термин "матрица" означает нуклеиновую кислоту, включая двунитевую ДНК, однонитевую ДНК и РНК или их любые модификации, и может иметь любую длину или последовательность.
В используемом здесь смысле термин "терминатор" или "терминатор цепи" относится к основанию нуклеиновой кислоты, такому как A, G, С, Т или U, или аналогу, который эффективно терминирует реакцию удлинения праймера в том случае, когда он включен в нить удлинения праймера напротив нити матрицы. Предпочтительно терминатором является дидезоксинуклеотид. Также предпочтительно терминатор является либо немеченым, либо меченым так, чтобы он отличался от метки на нетерминирующем основании. Также в используемом здесь смысле, когда термин "терминатор" или "терминатор цепи" упоминается в единственном числе, это не означает, что используется молекула из одного нуклеотида. Точнее, единственная форма термина "терминатор" относится к типу нуклеотида, основания нуклеиновой кислоты или аналога нуклеиновой кислоты, который используется при анализе. Например, если терминатором является ddA, то все множество ddA упоминается в единственной форме, а не только единственная молекула ddA. В альтернативном случае "терминатор" может означать отсутствие конкретного типа нуклеотида, так что удлинение праймера останавливается из-за отсутствия специфичного нуклеотида в локусе. Например, если требуется, чтобы реакция удлинения праймера останавливалась напротив "С" на матричной нити, нетерминирующие основания А, Т и G должны быть включены в реакционную смесь удлинения праймера, а "G", который является комплементом "С", - не должен. Таким образом, отсутствие комплементарного основания будет вызывать терминацию реакции удлинения праймера с результатом, аналогичным, например, результату при добавлении терминирующего дидезоксинуклеотида.
В используемом здесь смысле термин "не-терминатор" или "не-терминатор цепи" включает в себя нуклеотидное основание, которое не терминирует реакцию удлинения праймера при его включении в нить удлинения праймера. Предпочтительно, чтобы по меньшей мере один не-терминатор в реакции удлинения праймера являлся меченым. Также в используемом здесь смысле, когда термин "не-терминатор" или "не-терминатор цепи" упоминается в единственном числе, это не означает, что используется молекула из одного нуклеотида. Точнее, единственная форма термина "не-терминатор" относится к типу нуклеотида, основания нуклеиновой кислоты или аналога нуклеиновой кислоты, который используется при анализе. Например, если терминатором является G, то все множество G упоминается в единственной форме, а не только единственная молекула G.
В используемом здесь смысле термин "мутант" или "мутация" означает любое основание в матричной нити, которое отличается от основания дикого типа или нормального основания. Мутация, которая может быть обнаружена с использованием способа настоящего изобретения, может представлять собой совершенно любой тип мутации, включая мутацию одного основания, инсерцию, делению или транслокацию гена, при условии, что затронуто основание на матрице прямо напротив основания сразу же с 3'-конца отожженного праймера.
В используемом здесь смысле термин "метка" относится к любой молекуле, которую связывают с терминирующим или нетерминирующим нуклеотидом для получения регистрируемого сигнала. Метка может быть радиоактивной, хемилюминесцентной, белковым лигандом, таким как антитело, или в случае использования флуоресцентной группы могут быть использованы различные флуоресцентные группы для каждого типа нетерминирующего нуклеотидного основания. Указанные флуоресцирующие метки должны обладать свойством наличия спектроскопически отличимых эмиссионных спектров.
В альтернативном случае способ регистрации метки включения нуклеотидного основания в продукт удлинения праймера может быть основан на измерении технологией масс-спектрометрии, как приведено в примерах в патенте США No.5885775, который включен здесь в виде ссылки в полном объеме.
В используемом здесь смысле фраза "условия гибридизации высокой жесткости" относится к условиям гибридизации нуклеиновых кислот, таким как условие промывки в 0,1XSSC при 42°С, но не ограничены этим. Условия гибридизации обычно можно найти в книгах, содержащих основные молекулярно-биологические протоколы, таких как Ausubel et al., Current Protocols in Molecular Biology Greene and Wiley, pub. (1994), которая включена здесь в виде ссылки в полном объеме.
Как здесь использовано, "тонкослойная хроматография (ТСХ)" может быть выполнена на бумажном носителе на основе продуктов целлюлозы, но может быть сделана в любом веществе, которое позволяет молекулам быть тонкодиспергированными и формировать единообразный слой. Указанные вещества включают в себя, но не ограничиваясь этим, неорганические вещества, такие силикагель, оксид алюминия, диатомовую землю или силикат магния. Органические вещества включают в себя, но не ограничиваясь этим, целлюлозу, полиамид или порошок полиэтилена. Способы тонкослойной хроматографии обычно описаны в книгах химических протоколов, таких как протоколы, изложенные в общих чертах в Freifelder, Physical Biochemistry - Applications to Biochemistry and Molecular Biology, second ed., опубликованной Freeman and Co. (1982), которая включена здесь в виде ссылки в полном объеме, особенно в главе 8, в которой обсуждаются технологии хроматографии, в частности тонкослойная хроматография на страницах 229-232.
Модификацией способа идентификации и/или количественного определения интересующей нуклеиновой кислоты является отделение нити удлинения праймера от интересующей нуклеиновой кислоты после реакции удлинения с использованием соответствующих денатурирующих условий. Денатурирующие условия могут включать в себя нагревание, обработку щелочью, формамидом, мочевиной, глиоксалем, ферментами и их комбинации. Денатурирующие условия также могут включать в себя обработку 2,0 н. NaOH.
Специалист в данной области может понять, что терминатор можно метить меткой, отличной от метки не-терминатора, что затем может быть использовано для того, чтобы дифференцировать включение терминатора или не-терминатора в нить удлинения праймера. В данной заявке терминатор в виде отсутствия конкретного типа нуклеотида приведен в качестве примера только в целях упрощения иллюстрации, но данная иллюстрация не должна быть истолкована как ограничение формулы изобретения каким-либо образом. Дифференциально меченый или немеченый терминатор также охватывается изобретением, при условии, что метка терминатора отличается от метки нетерминатора.
Специалист в данной области также может понять, что при том условии, что последовательность матрицы по меньшей мере частично известна, можно сконструировать праймер, который связывается с матричной нитью так, что может происходить связывание праймера на матричной нити. Специалист в данной области также может понять, что способ согласно изобретению на практике может применяться с использованием нескольких праймеров в одной или большем количестве пробирок для анализа.
Особенностью способа согласно изобретению является то, что можно создать мощный сигнал, если нетерминаторы одинаково мечены, поскольку достигается эффект суммирования сигнала при включении нескольких меченых нетерминаторов, включенных в нить удлинения праймера. Точность возрастает в том случае, когда наблюдаются сигналы при использования различных меток, специфичных для различных терминаторов или нетерминаторов.
Целью данного изобретения также является предоставление набора и реагентов для быстрого и точного количественного или неколичественного, по желанию, определения наличия или отсутствия нуклеиновой кислоты-мишени в образце. Каждый компонент набора(ов) может быть индивидуально упакован в собственный подходящий контейнер. Индивидуальные контейнеры также могут быть мечены таким образом, при котором идентифицировано содержимое. Кроме того, индивидуально упакованные компоненты могут быть помещены в больший по размеру контейнер, способный вместить все требуемые компоненты. Вместе с набором могут быть даны инструкции, которые объясняют, как использовать набор. Указанные инструкции могут быть написаны на наборе или приложены к нему.
Следующие примеры предлагаются в качестве иллюстрации данного изобретения, а не в качестве ограничения.
ПРИМЕР.
Суммарную РНК экстрагировали из мозга крыс способом RNAzol В (Tels-tel, ТХ). Концентрацию суммарной РНК измеряли по оптической плотности при OD 260 нм. Суммарную РНК разбавляли свободной от РНКазы водой, обработанной диэтилпирокарбонатом (ДЭПК, DEPC). В каждую пробирку отбирали аликвоты по 5 мкл разбавленного раствора РНК с различными количествами, как показано в таблице 2, и затем смешивали с 1 мкл синтетического олигонуклеотидного праймера 5'-GTGGGAACCGTGTCA-3' (SEQ ID NO:1), который представляет собой последовательность, совпадающую со специфичной кДНК мозга крыс (неопубликованные данные). Смесь РНК-праймер нагревали при 70°С в течение 3 минут и инкубировали на льду в течение 3 минут. После быстрого центрифугирования пробирки реакцию удлинения праймера начинали добавлением 14 мкл реакционной смеси, содержащей трис-HCl буфер (рН 7,5) при конечной концентрации 20 мМ, 15 единиц ингибитора РНКазы, 0,5 мМ dATP, dGTP, 1 мкл dCTPα32P и 100 единиц обратной транскриптазы MMVL. Реакцию выполняли при 37°С в течение 20 минут и останавливали нагреванием реакционной пробирки до 100°С в течение 2 минут. 1 мкл реакционной смеси использовали для тонкослойной хроматографии (TRIM USA, Maryland), чтобы отделить свободный dCTPα32P. Затем радиоактивность меченого праймера считали в сцинтилляционном счетчике (Beckman LS 5000). Результаты показаны в таблице 2.
Все указанные выше стадии включают в себя химические процессы, манипуляции и протоколы, которые были автоматизированы или поддаются автоматизации. В связи с этим введение предпочтительного способа практического применения данного изобретения в работу соответствующим образом запрограммированной роботизированной рабочей станции в результате приведет к значительному снижению себестоимости и увеличению продуктивности практически любой диагностической процедуры, которая зависит от выявления специфичных нуклеотидных последовательностей или отличий в последовательностях нуклеиновых кислот, полученных из биологических образцов.
Все цитированные здесь материалы включены в виде ссылки в полном объеме.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДЕТЕКЦИИ ВАРИАНТА ПОСЛЕДОВАТЕЛЬНОСТИ НУКЛЕИНОВОЙ КИСЛОТЫ С ПОМОЩЬЮ АНАЛИЗА ТЕРМИНАЦИИ СО СДВИГОМ | 2000 |
|
RU2200762C2 |
| СПОСОБ АМПЛИФИКАЦИИ МАТРИЧНОЙ НУКЛЕИНОВОЙ КИСЛОТЫ | 2001 |
|
RU2284357C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ХАРАКТЕРИСТИК ПОСЛЕДОВАТЕЛЬНОСТИ МОЛЕКУЛЫ НУКЛЕИНОВОЙ КИСЛОТЫ ПУТЕМ ОБНАРУЖЕНИЯ И ХАРАКТЕРИСТИКИ ВАРИАЦИЙ ЭТОЙ ПОСЛЕДОВАТЕЛЬНОСТИ | 1998 |
|
RU2264468C2 |
| БИБЛИОТЕКИ ДЛЯ СЕКВЕНИРОВАНИЯ НОВОГО ПОКОЛЕНИЯ | 2014 |
|
RU2698125C2 |
| ОБНАРУЖЕНИЕ ИЗМЕНЕНИЙ КОНФОРМАЦИИ ПОЛИМЕРАЗЫ НУКЛЕИНОВЫХ КИСЛОТ С ПОМОЩЬЮ НАНОТРУБКИ | 2015 |
|
RU2721965C2 |
| Способ определения субстратной эффективности производных трифосфатов дезоксиуридина для ДНК-полимераз методом реакции достраивания праймера | 2019 |
|
RU2731739C1 |
| СПОСОБ ПОВЫШЕНИЯ СПЕЦИФИЧНОСТИ ОБРАТНОЙ ТРАНСКРИПЦИИ | 2008 |
|
RU2459872C2 |
| Способ ферментативного получения модифицированных ДНК для создания реагентов, специфично связывающихся с гидрофобными участками высокомолекулярных органических соединений | 2017 |
|
RU2699522C2 |
| СПОСОБ ЗАЩИТЫ ОТ-ПЦР ОТ КОНТАМИНАЦИИ ПРОДУКТАМИ АМПЛИФИКАЦИИ НА ОСНОВЕ РАЗРУШАЮЩЕГО ДЕЙСТВИЯ УРАЦИЛ-ДНК-ГЛИКОЗИЛАЗЫ | 2005 |
|
RU2307167C2 |
| СПОСОБ УДАЛЕНИЯ ЗАГРЯЗНЯЮЩЕЙ НУКЛЕИНОВОЙ КИСЛОТЫ ИЗ РЕАКЦИЙ ОБРАТНОЙ ТРАНСКРИПЦИИ И АМПЛИФИКАЦИИ | 2010 |
|
RU2550277C2 |

Изобретение относится к биохимии и молекулярной биологии и может быть использовано в диагностических тестах и аналитических системах любого назначения, предполагающих обнаружение в образце специфических последовательностей нуклеиновой кислоты. Предложены варианты способа выявления последовательности - "мишени" ДНК или РНК, который основан на проведении реакции удлинения праймера в условиях, обеспечивающих определенное лимитирование размера продукта (изометричное удлинение праймера, ИУП). Указанные условия заключаются в применении на стадии наращивания праймера, предварительно гибридизованного с соответствующим участком последовательности - "мишени", реакционной смеси, в которой по крайней мере один из типов дНТФ либо отсутствует, либо заменен соответствующим терминирующим субстратом. При использовании предлагаемого способа существенно повышается чувствительность анализа и сокращается время его проведения. 3 с. и 41 з.п. ф-лы, 2 ил., 2 табл.
(a) приготовление по меньшей мере одного праймера, специфично связывающегося с предопределенным участком нуклеиновой кислоты-мишени;
(b) отжиг по меньшей мере одного праймера из пункта (а) с нуклеиновой кислотой-мишенью с образованием дуплекса праймер-нуклеиновая кислота в предопределенном участке нуклеиновой кислоты-мишени;
(c) смешивание дуплекса праймер-нуклеиновая кислота из пункта (b) со смесью нетерминирующих нуклеотидов, где по меньшей мере один из четырех необходимых типов нуклеотидов для непрерывного удлинения в процессе реакций удлинения праймера отсутствует в смеси нетерминирующих нуклеотидов и где по меньшей мере один нетерминирующий нуклеотид мечен детектируемым маркером;
(d) выполнение изометрического удлинения праймера посредством ферментативной или химической реакции в соответствующем буфере с получением продуктов изометрического удлинения праймера, где удлинение праймера терминируется у нуклеотида нуклеиновой кислоты-мишени, который комплементарен отсутствующему нетерминирующему нуклеотиду из пункта (с);
(е) выявление сигнала метки на продуктах изометрического удлинения праймера.
(a) dATP, dCTP, dGTP;
(b) dATP, dCTP, dTTP или dUTP;
(c) dATP, dGTP, dTTP или dUTP или
(d) dCTP, dGTP, dTTP или dUTP.
(a) приготовление по меньшей мере одного праймера, специфично связывающегося с предопределенным участком нуклеиновой кислоты-мишени;
(b) отжиг по меньшей мере одного праймера из пункта (а) с нуклеиновой кислотой-мишенью, с образованием дуплекса праймер-нуклеиновая кислота в предопределенном участке нуклеиновой кислоты-мишени;
(c) смешивание дуплекса праймер-нуклеиновая кислота из пункта (b) со смесью нетерминирующих нуклеотидов, где по меньшей мере один из четырех необходимых типов нуклеотидов для непрерывного удлинения в процессе реакций удлинения праймера отсутствует в смеси нетерминирующих нуклеотидов;
(d) выполнение изометрического удлинения праймера посредством ферментативной или химической реакции, где удлинение праймера терминируется у нуклеотида нуклеиновой кислоты-мишени, который комплементарен отсутствующему нетерминирующему нуклеотиду из пункта (с);
(e) выявление продуктов изометрического удлинения праймера.
(a) отжиг по меньшей мере одного праймера с нуклеиновой кислотой-мишенью, где праймер мечен детектируемым маркером;
(b) удлинение меченого праймера с образованием продуктов изометрического удлинения праймера путем пропуска по меньшей мере одного из четырех необходимых типов нуклеотидов для непрерывного удлинения в процессе реакции удлинения праймера;
(с) выявление меченых продуктов удлинения праймера.
Приоритет по пунктам
| US 4965188, 23.10.1990 | |||
| US 5710028, 20.01.1998 | |||
| US 5849542, 15.12.1998 | |||
| RU 97117182 A 20.08.1999. |
Авторы
Даты
2005-11-27—Публикация
2001-06-07—Подача