Изобретение относится к области биоорганической химии, а именно к способу получения фосфотиоатных аналогов олигодезоксирибонуклеотидов общей формулы I
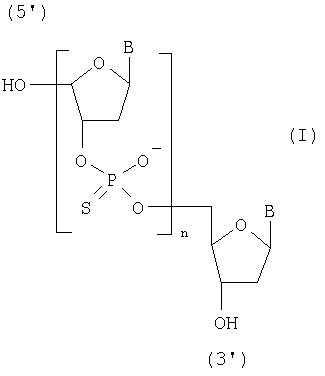
где В - остаток аденина, гуанина, тимина и цитозина и n=1-20, которые могут быть использованы в молекулярной биологии и медицине в качестве исходных соединений для получения фосфотиоатных аналогов олигодезоксирибонуклеотидных реагентов.
Известен способ получения фосфотиоатных аналогов олигодезоксирибонуклеотидов общей формулы I путем получения N,Р-защищенных фосфотиоатных аналогов олигодезоксирибонуклеотидов общей формулы II
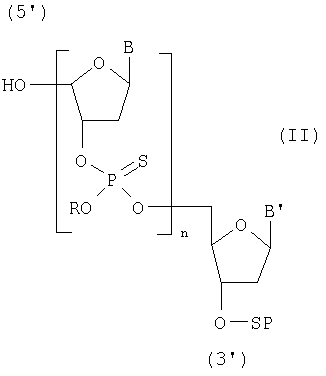
где R - β-цианоэтил, SP-твердофазный носитель, В' - остаток N6-бензоиладенина, N2-изобутирилгуанина, N4-бензоилцитозина и тимина и n=6-20,
твердофазным фосфоамидитным методом и обработки полученных соединений водным аммиаком для удаления N,P-защитных групп и носителя [Xu Q., Musier-Forsyth К., Hammer R.P., Barany G., 1996, Nucleic Acids Research, v.24, N9, pp.1602-1607].
Недостатками данного способа являются высокая концентрация мономеров (0,1 М) и активирующего реагента, необходимость проведения стадий копирования и сульфуризации в каждом цикле и большое время наращивания одного цикла цепи (больше пяти минут).
Наиболее ближайшим к заявляемому способу - прототипом, является способ получения фосфотиоатных аналогов олигодезоксирибонуклеотидов общей формулы I путем получения N-защищенных олигодезоксирибонуклеозид Н-фосфонатов общей формулы III
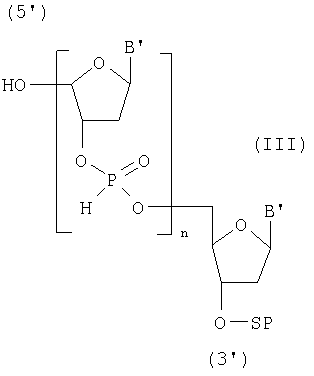
где SP-твердофазный носитель, В' - остаток N6-бензоиладенина, N2-изобутирилгуанина, N4-бензоилцитозина и тимина и n=1-20,
твердофазным H-фосфонатным методом и последовательной обработки полученных соединений раствором элементарной серы и водным аммиаком [Froehler B.C., Tetrahedron Letters, 1986, v.27, N 46, рр.5575-5578].
Получение фосфотиоатных аналогов N-защищенных олигодезоксирибонуклеозидов на твердой фазе (0,1 микромолярный масштаб) при комнатной температуре в синтезаторе состоит из следующих стадий:
1) промывка реактора с твердофазным носителем безводным ацетонитрилом (45 секунд);
2) удаление 5'-защитной группы с нуклеозида (или олигодезоксирибонуклеозид Н-фосфоната), присоединенного к твердофазному носителю 2,5%ным раствором дихлоруксусной кислоты в дихлорметане (60 секунд);
3) промывка реактора с носителем смесью безводных пиридина и ацетонитрила (45 секунд);
4) смешивание раствора мономера (0,01 М N,5'-защищенный дезоксирибонуклеозид 3'-Н-фосфонат) и раствора активирующего реагента (0,05 М пивалоил хлорид), подача смеси в реактор и конденсация с 5'-гидроксильной группой концевого нуклеозида, связанного с носителем (90 секунд), при этом расход мономера на присоединение одного звена составляет 2,5 мг;
5) повторение операций 1-4 до получения защищенного олигодезоксирибонуклеозид Н-фосфоната с необходимым числом мономерных звеньев (время цикла присоединения одного мономерного звена составляет 240 секунд);
6) удаление 5'-защитной группы с олигодезоксирибонуклеозид Н-фосфоната 2,5%ным раствором дихлоруксусной кислоты в дихлорметане (60 секунд);
7) превращение Н-фосфонатных групп в фосфотиоатные обработкой 0,1 М раствором элементарной серы в смеси триэтиламина и дисульфида углерода (5 минут).
Полученные соединения обрабатывают водным аммиаком для удаления N-защитных групп и носителя.
Недостатками прототипа являются большое время наращивания одного цикла цепи (240 секунд) и повышенный расход исходных мономеров (2,5 мг на присоединение одного звена).
Технической задачей настоящего изобретения является повышение производительности способа получения целевого продукта за счет сокращения времени получения промежуточного продукта (защищенных олигодезоксирибонуклеозид Н-фосфонатов общей формулы III) и экономии используемых реагентов.
Поставленная техническая задача достигается предлагаемым способом, включающим промывку растворителем твердофазного носителя с закрепленным на нем нуклеозидом, содержащим 5'-O-защитную группу, удаление 5'-O-защитной группы нуклеозида, связанного с носителем, повторную промывку растворителем твердофазного носителя с закрепленным на нем нуклеозидом, содержащим 5'-гидроксильную группу, удаление 5'-O-защитной группы, промывку твердофазного носителя растворителем, смешивание раствора N,5'-защищенного дезоксирибонуклеозид 3'-Н-фосфоната и раствора активирующего реагента и подачу смеси в реактор за время 0,4-0,5 секунды, конденсацию с 5'-гидроксильной группой концевого нуклеозида, связанного с носителем, за 2-3 секунды, причем операции смешивания, подачи и конденсации повторяют 14-20 раз, повторение всех вышеперечисленных операций до получения N-защищенного олигодезоксирибонуклеозид Н-фосфоната с необходимым числом мономерных звеньев, обработку полученного соединения раствором серы с последующей промывкой реактора при температуре реагентов на всех стадиях синтеза, равной 30-35°С, отщепление носителя и удаление N-защитных групп водным аммиаком. Расход исходного мономера на присоединение одного звена составляет 0,4-0,6 мг.
Определяющим отличием заявляемого способа от прототипа является экспериментально подобранный оптимальный режим проведения синтеза, а именно смешивание N,5'-защищенных дезоксирибонуклеозид 3'-Н-фосфонатов с активирующим реагентом и подача их в реактор с носителем за время 0,4-0,5 секунды, конденсация с 5'-гидроксильной группой концевого нуклеозида, связанного с носителем, за 2-3 секунды, причем эти операции повторяют 14-20 раз при температуре реагентов на всех стадиях синтеза, равной 30-35°С, что позволяет повысить производительность способа, и это было не очевидно на основании известных закономерностей протекания химических реакций, однако стало возможным за счет предварительно установленной зависимости эффективности присоединения N,5'-защищенных дезоксирибонуклеозид 3'-Н-фосфонатов к наращиваемой цепи от времени, прошедшего после их смешивания с раствором активирующего реагента. Сокращение времени смешивания и подачи смеси мономеров и конденсирующего агента приводит к более эффективному образованию межнуклеотидной связи на твердофазном носителе, что позволяет сократить время одного цикла наращивания цепи в 6 раз (с 240 до 36 сек) и снизить расход используемых дефицитных реактивов в 4-6 раз.
Изобретение иллюстрируется следующими примерами конкретного выполнения.
Пример 1. Получение фосфотиоатного аналога декадезоксирибонуклеотида d(CpsCpsGpsApsTpsTpsGpsApsCpsG).
Синтез проводили по специальной программе на синтезаторе АСМ-10У фирмы «БИОССЕТ» (Россия), управляемом персональным компьютером. В качестве твердофазного носителя использовали CPG-500 (фирма «Serva», Германия) с емкостью по нуклеозиду - 21 микромоль/грамм.
Объем реактора - 0,012 мл (5 мг носителя), масштаб синтеза - 0,1 микромолярный, температура термостата синтезатора - 30°С.
Для получения целевого продукта осуществили:
1) промывку реактора с твердофазным носителем безводным ацетонитрилом (0,3 мл, 6 секунд),
2) удалили 5'-O-защитную группу (монометокситритил) обработкой 3%-ным раствором трифторуксусной кислоты в дихлорметане (0,2 мл, 8 секунд),
3) промыли реактор безводным ацетонитрилом (0,3 мл, 6 секунд),
4) провели смешивание 2 мкл раствора мономера (15 мг N,5'-защищенного дезоксирибонуклеозид 3'-Н-фосфоната в 1 мл смеси (1:1) безводных пиридина и ацетонитрила) и 2 мкл раствора активирующего реагента (0,10-0,15 мл пивалоил хлорида в 9 мл смеси (1:1) безводных пиридина и ацетонитрила) и подачу смеси в реактор за время 0,4 секунды, конденсацию с 5'-гидроксильной группой концевого нуклеозида, связанного с носителем, за 3 секунды, причем операции смешивания, подачи и конденсации повторяли 20 раз в течение 16 секунд,
5) повторили все вышеперечисленные операции 8 раз до получения N-защищенного олигодезоксирибонуклеозид Н-фосфоната длиной 10 звеньев (время цикла присоединения одного мономерного звена составляет 36 секунд),
6) обработали реактор с олигодезоксирибонуклеозид H-фосфонатом 0,1 М раствором элементарной серы в смеси (1:9) триэтиламина и дисульфида углерода (0,3 мл, 5 минут),
7) промыли реактор смесью (1:9) триэтиламина и дисульфида углерода (0,3 мл, 30 секунд) для удаления раствора серы.
По завершению синтеза носитель переносили из реактора в полиэтиленовую пробирку и обрабатывали 25%-ным водным аммиаком (0,5 мл) для отщепления носителя и удаления N-защитных групп при температуре 57°С в течение 18 часов и выделяли продукт методом электрофореза в полиакриламидном геле.
Расход мономера в одном цикле - 0,6 мг.
Время одного цикла наращивания цепи - 36 секунд.
Выход продукта - 2,7 о.е. (при длине волны 260 нм).
Пример 2. Получение фосфотиоатного аналога эйкозадезоксирибонуклеотида
d(CpsCpsGpsApsTpsTpsGpsApsCpsGpsGpsTpsCpsApsApsCpsGpsApsApsT).
Продукт получали как в примере 1, но
1) температура термостата равнялась 35°С;
2) концентрация мономеров составляла 10 мг/мл смеси;
3) объем дозы реагентов - 0,003 мл раствора;
4) время смешивания растворов - 0,5 секунды;
5) время конденсации - 2 секунды;
6) операции смешивания, подачи и конденсации повторяли 14 раз;
7) повторение операций - 18 раз. Расход мономера в одном цикле - 0,4 мг.
Время одного цикла наращивания цепи - 36 секунд.
Выход целевого продукта - 2,4 о.е. (при длине волны 260 нм).
Способ позволяет с высокой производительностью получать целевой продукт, затрачивая при этом меньшее количество дефицитных реактивов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5`-АМИНОАЛКИЛФОСФАТ ОЛИГОДЕЗОКСИРИБОНУКЛЕОТИДОВ | 2005 |
|
RU2292350C1 |
| Способ синтеза олиго/поли/ нуклеотидов и устройство для его осуществления | 1990 |
|
SU1773916A1 |
| МОДИФИЦИРОВАННЫЕ ОЛИГОНУКЛЕОТИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2708237C2 |
| МОДИФИЦИРОВАННЫЕ ОЛИГОНУКЛЕОТИДЫ, АКТИВИРУЮЩИЕ РНКазу Н | 2017 |
|
RU2740501C2 |
| СПОСОБ СИНТЕЗА МОДИФИЦИРОВАННЫХ ПО АТОМУ ФОСФОРА НУКЛЕИНОВЫХ КИСЛОТ | 2009 |
|
RU2572826C2 |
| СПОСОБ СИНТЕЗА В РАСТВОРЕ МАКРОМОЛЕКУЛ ИЗ ЗВЕНЬЕВ ПРОИЗВОДНЫХ УГЛЕВОДОВ | 2021 |
|
RU2819631C1 |
| СПОСОБ СИНТЕЗА МОРФОЛИНОВЫХ ОЛИГОМЕРОВ | 2008 |
|
RU2606627C2 |
| СИНТЕЗ ФОСФИТИЛИРОВАННЫХ СОЕДИНЕНИЙ С ИСПОЛЬЗОВАНИЕМ ЧЕТВЕРТИЧНОГО ГЕТЕРОЦИКЛИЧЕСКОГО АКТИВАТОРА | 2005 |
|
RU2440364C2 |
| ГИБРИДНЫЙ ОЛИГОНУКЛЕОТИД, СОДЕРЖАЩИЙ ФОСФОРОТИОАТНУЮ И/ИЛИ ФОСФОРОДИТИОАТНУЮ СВЯЗИ, ТЕРАПЕВТИЧЕСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ ГЕННОЙ ЭКСПРЕССИИ | 1993 |
|
RU2115658C1 |
| СИНТЕЗ ОЛИГОНУКЛЕОТИДОВ | 2006 |
|
RU2465280C2 |
Изобретение относится к способу получения фосфотиоатных аналогов олигодезоксирибонуклеотидов общей формулы (I), где В - остаток тимина, цитозина, аденина или гуанина, n=1-20, на твердофазном носителе, которые могут быть использованы в молекулярной биологии и медицине в качестве исходных соединений для получения фосфотиоатных аналогов олигодезоксирибонуклеотидных реагентов. Способ включает промывку растворителем носителя с закрепленным на нем нуклеозидом, содержащим 5'-O-защитную группу, удаление 5'-O-защитной группы нуклеозида, связанного с носителем, повторную промывку растворителем твердофазного носителя с закрепленным на нем нуклеозидом, содержащим 5'-гидроксильную группу, смешивание N,5'-защищенных дезоксирибонуклеозид-3'-Н-фосфонатов с активирующим реагентом, подачу смеси в реактор, конденсацию с 5'-гидроксильной группой концевого нуклеозида, связанного с носителем, повторение этих операций до получения защищенного олигодезоксирибонуклеозид Н-фосфоната с необходимым числом мономерных звеньев, обработку полученного соединения раствором серы, а затем водным аммиаком для отщепления носителя и удаления N-защитных групп. При этом смешивание N,5'-защищенных дезоксирибонуклеозид-3'-Н-фосфонатов с активирующим реагентом и подачу смеси в реактор проводят за 0,4-0,5 секунды, а конденсацию с 5'-гидроксильной группой концевого нуклеозида за 2-3 секунды, причем эти операции повторяют 14-20 раз при температуре реагентов на всех стадиях синтеза, равной 30-35°С. Изобретение позволяет повысить производительность способа за счет сокращения времени получения промежуточного продукта и экономии используемых реагентов.
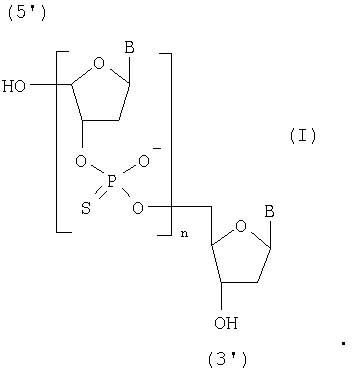
Способ получения фосфотиоатных аналогов олигодезоксирибонуклеотидов общей формулы I
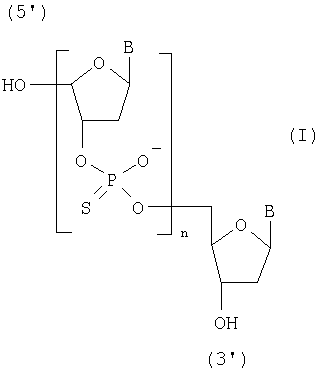
где В - остаток тимина, цитозина, аденина или гуанина;
n=1-20,
на твердофазном носителе, включающий промывку растворителем носителя, с закрепленным на нем нуклеозидом, содержащим 5'-O-защитную группу, удаление 5'-O-защитной группы нуклеозида, связанного с носителем, повторную промывку растворителем твердофазного носителя, с закрепленным на нем нуклеозидом, содержащим 5'-гидроксильную группу, смешивание N,5'-защищенных дезоксирибонуклеозид-3'-Н-фосфонатов с активирующим реагентом, подачу смеси в реактор, конденсацию с 5'-гидроксильной группой концевого нуклеозида, связанного с носителем, повторение этих операций до получения защищенного олигодезоксирибонуклеозид Н-фосфоната с необходимым числом мономерных звеньев, обработку полученного соединения раствором серы, а затем водным аммиаком для отщепления носителя и удаления N-защитных групп, отличающийся тем, что смешивание N,5'-защищенных дезоксирибонуклеозид-3'-Н-фосфонатов с активирующим реагентом и подачу смеси в реактор проводят за 0,4-0,5 с, а конденсацию с 5'-гидроксильной группой концевого нуклеозида за 2-3 с, причем эти операции повторяют 14-20 раз при температуре реагентов на всех стадиях синтеза, равной 30-35°С.
| B.C.FROEHLER | |||
| Deoxynucleoside H-phosphonate Diester Intermediates in the Synthesis of Intemucleotide Phosphate Analouges | |||
| Tetrahedron Letters | |||
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
| Способ синтеза олиго/поли/ нуклеотидов и устройство для его осуществления | 1990 |
|
SU1773916A1 |
| СПОСОБ ПОЛУЧЕНИЯ 3'-ФОСФАТ,N,P-НЕЗАЩИЩЕННЫХ ФОСФОТИОАТНЫХ АНАЛОГОВ ОЛИГОДЕЗОКСИРИБОНУКЛЕОТИДОВ | 1997 |
|
RU2131881C1 |
| Способ получения олигодезокситионуклеотидов | 1981 |
|
SU979361A1 |
| US 5278302 A, 11.01.1994. | |||
Авторы
Даты
2007-01-27—Публикация
2005-09-28—Подача