Изобретение относится к соединениям, обладающим агонистической активностью в отношении гликопротеинового гормона, в частности к соединениям, обладающим агонистической активностью в отношении лютеинизирующего гормона (LH) и фолликулостимулирующего гормона (FSH). Изобретение также относится к фармацевтическим композициям, содержащим такие соединения, и к использованию этих соединений в лекарственной терапии, в частности для контроля оплодотворения.
Гонадотропины играют важную роль в различных функциях организма, включая метаболизм, регулирование температуры и репродуктивный процесс. Гипофизные гонадотропины FSH и LH, например, играют существенно важную роль в стимулировании развития и созревания фолликул, в то время как LH включены в индуцирование процессов овуляции (Sharp, R.M. Clin. Endocrinol 33:787-807, 1990; Dorrington and Armstrong, Recent Prog. Horm. Res 35: 301-342, 1979; Levy et al, Human Reproduction 15:2258-2265, 2000).
В настоящее время LH применят в клинических условиях, в комбинации с FSH, для стимулирования яичников, т.е. гиперстимулирования яичников для оплодотворения in vitro (IVF) и индуцирования овуляции у бесплодных, не способных к овуляции женщин (Insler, V., Int. J. Fertility 33:85-97, 1988, Navot and Rosenwaks, J. Vitro Fert. Embryo Transfer 5:3-13, 1988), а также для мужского гипогонадизма и мужского бесплодия.
Гонадотропины действуют на специфические типы клеток, относящиеся к половой железе, для инициации яичниковой и тестикулярной дифференциации и стероидогенеза. Действия таких гипофизарных и плацентарных гормонов опосредованы специфическими рецепторами мембраны плазмы, которые являются членами большого семейства спаренных рецепторов G-протеинов. Они состоят из простого полипептида с семью трансмембранными доменами и являются способными к взаимодействию с G-протеинами, приводящему к активации аденилциклазы.
Гонадотропины, предназначенные для терапевтических целей, могут быть выделены из мочи человека и имеют низкую чистоту (Morse et al, Amer. J. Reproduct. Immunol. and Microbiology 17:143, 1988). Альтернативно, их можно получить в виде рекомбинантных гонадотропинов. В дополнение к этим белкам рецепторы гонадотропина можно активировать или дезактивировать при помощи низкомолекулярных соединений, полученных синтетическим путем. В WO 00/61586 описаны бициклические гетероароматические соединения. Эксперименты in vitro и in vivo показали, что они являются полезными в качестве LH агонистов.
У нормальных женщин высвобождение гипофизарных LH и FSH характеризуется большим всплеском в середине цикла, который предшествует овуляции. Овуляция характеризуется тремя отличительными физиологическими особенностями, а именно созреванием ооцитов, фолликулярным разрывом и лютеинизацией. В то время как роль большого всплеска LH в индуцировании этих явлений in vivo не обсуждается, роль всплеска FSH менее ясна. Однако недавно было показано, что FSH индуцирует созревание ооцитов in vitro путем индуцирования скопления клеток с продуцированием фактора, положительно преодолевающего индуцированную гипоксантином остановку мейоза (Lu et al, Mol. Cell. Endocrinol. 164:191-196, 2000). Полагают, что этот фактор представляет собой активирующий мейоз стерол (MAS).
Данное изобретение относится к низкомолекулярным соединениям, которые обладают LH активность. В дополнение к LH активности они проявляют также FSH активность, что явилось неожиданным. В основном, такие соединения представляют собой тиено[2,3-d]пиримидины, которые являются замещенными в положении 4 пиримидинового кольца фенильной группой, которая, в свою очередь, замещена в мета-положении. Такой заместитель включает трехатомную спейсерную группу (NH-C(O)-CH2), которая, кроме того, функционализирована замещенной аминогруппой. Соединения, главным образом, обладают различной степенью FSH агонистической активности, но, как правило, меньшей, чем LH агонистическая активность.
Настоящее изобретение относится к глицин-замещенным производным тиено[2,3-d]пиримидина общей формулы I

или их фармацевтически приемлемой соли, где
Х представляет собой О или Н,Н;
А представляет собой S, NH, N(R6), O или связь;
R1 представляет собой (1-4С)алкил, (2-4С)алкенил, фенил или (2-5С)гетероарил, где фенильное или гетероарильное кольцо необязательно замещено одним или несколькими заместителями группы: гидрокси, галоген, нитро, трифторметил, циано, амино или (1-4С)(ди)алкиламино;
R2 представляет собой Н, (1-4С)алкил, (1-4С)алкокси(2-4С)алкил или гидрокси(2-4С)алкил;
R3 и R4 независимо выбирают из Н, (1-4С)алкила и гидрокси(1-4С)алкила;
R5 представляет собой Н или (1-4С)алкил, и
R6 может быть выбран из тех же самых групп, как описано для R1.
Термин (1-4С)алкил, как используется в определении формулы (I), означает разветвленную или неразветвленную алкильную группу, содержащую 1-4 атома углерода, например метил, этил, н-попил, изопропил, н-бутил, втор-бутил или трет-бутил.
Термин (1-4С)алкенил, как используется в определении формулы (I), означает разветвленную или неразветвленную алкенильную группу, содержащую 2-4 атома углерода, например винил, 1-пропенил, 2-пропенил, 1-метилвинил, 1-бутенил, 2-бутенил, 3-бутенил, 2-метил-1-пропенил, 2-метил-2-пропенил, 1-метил-1-пропенил, 1-этилвинил.
Термин (1-4С)алкокси(1-4С)алкил означает алкильную группу, содержащую 1-4 атома углерода, связанную через атом кислорода с другой алкильной группой, содержащей 1-4 атома углерода, при этом алкильные группы имеют те же значения, как определены выше.
Термин (1-4С)алкокси(2-4С)алкил означает алкильную группу, содержащую 1-4 атома углерода, связанную через атом кислорода с другой алкильной группой, содержащей 2-4 атома углерода, при этом алкильные группы имеют те же значения, как определены выше.
Термин гидрокси(1-4С)алкил означает гидроксильную группу, присоединенную к алкильной группе, содержащей 1-4 атома углерода, при этом алкильные группы имеют те же значения, как определены выше.
Термин гидрокси(2-4С)алкил означает гидроксильную группу, присоединенную к алкильной группе, содержащей 2-4 атома углерода, при этом алкильные группы имеют те же значения, как определены выше.
Термин (1-4С)(ди)алкиламино означает одну или две алкильные группы, содержащие 1-4 атома углерода, как определено выше, присоединенные к атому азота.
Термин (2-5С)гетероарил означает необязательно замещенную ароматическую группу, содержащую 2-5 атомов углерода, включающую по меньшей мере один гетероатом, выбранный из N, O и/или S, например имидазолил, тиенил, фурил или пиридил.
Термин галоген означает фтор, хлор, бром или йод.
Было обнаружено, что соединения приведенной выше формулы I демонстрируют агонистическую LH и FSH активность. В биоанализе in vitro, в котором использовали клетки СНО, стабильно транфицированные рецептором LH или FSH человека, соответственно, было определено значение ЕС50 в отношении LH рецептора менее 5·10-8 М, в то время как в отношении FSH рецептора значение ЕС50 составило менее 10-5 М. Обычно FSH активность составляет от около 1% от стимуляции агониста LH до около 10% от стимуляции агониста LH.
Настоящее изобретение также относится к фармацевтической композиции, включающей производное тиено[2,3-d]пиримидина, или его соли общей формулы I.
Таким образом, соединения по настоящему изобретению могут применяться в терапии. Следующий аспект настоящего изобретения относится к применению тиено[2,3-d]пиримидина общей формулы I для получения лекарственного средства для контроля оплодотворения, более предпочтительно индуцирования овуляции. Соединения по настоящему изобретению используют для активации как LH, так и FSH рецепторов. В связи с этим соединения по настоящему изобретению можно использовать в способе для лечения женщин с проблемами, связанными с оплодотворением.
Соединения тиено[2,3-d]пиримидина по настоящему изобретению могут содержать один или более хиральных атомов углерода. В связи с этим соединения можно получать в виде хирально чистых соединений или в виде смеси диастереомеров и/или энантиомеров. Способы получения хирально чистых соединений хорошо известны из уровня техники, например кристаллизация или хроматография.
Для применения в терапии соли соединений формулы I представляют собой соли, в которых противоион является фармацевтически приемлемым. Однако кислотно-аддитивные соли оснований формулы I также могут найти применение, например, в получении или очистке фармацевтически приемлемого соединения. Все соли, являются они фармацевтически приемлемыми или нет, включены в объем данного изобретения.
Примеры кислотно-аддитивных солей включают соли, полученные из минеральных кислот, таких как хлористоводородная кислота, фосфорная кислота, серная кислота, предпочтительно хлористоводородная кислота, и органических кислот, например лимонной кислоты, винной кислоты, уксусной кислоты, молочной кислоты, малеиновой кислоты, малоновой кислоты, фумаровой кислоты, гликолевой кислоты, янтарной кислоты и т.п.
Подходящие пути введения соединений формулы I или их фармацевтически приемлемых солей, также обозначенных в данном описании как активный ингредиент, включают внутримышечные инъекции, подкожные инъекции, внутривенные инъекции или внутрибрюшинные инъекции, пероральное и интраназальное введение. Предпочтительно соединения могут вводиться перорально. Точная доза и режим введения активного ингредиента, или его фармацевтической композиции, будут зависеть, главным образом, от ожидаемого терапевтического эффекта (лечение бесплодия; контрацепция) и могут изменяться в зависимости от конкретного соединения, пути введения и возраста и состояния конкретного субъекта, которому вводится лекарственный препарат.
Главным образом, парентеральное введение требует более низких доз, чем остальные способы введения, которые более зависят от адсорбции. Однако доза для людей предпочтительно содержит 0,0001-25 мг на кг веса тела. Желаемая доза может быть представлена в виде одной дозы или в виде нескольких субдоз, вводимых через подходящие интервалы в течение дня. В случае, если реципиентом является женщина, дозы могут вводиться через подходящие дневные интервалы в течение менструального цикла для фолликулярной поддержки или в виде единичной дозы для индуцирования овуляции. Дозы, так же как и режим введения, могут различаться для реципиентов женского и мужского пола.
В случае применений in vitro или ex vivo, например в IVF применении, соединения по настоящему изобретению используют в инкубационной среде в концентрации приблизительно 0,01-5 мкг/мл.
Настоящее изобретение, таким образом, также относится к фармацевтическим композициям, включающим соединение тиено[2,3-d]пиримидина формулы I, в смеси с фармацевтически приемлемыми вспомогательными веществами и, необязательно, другими терапевтическими агентами. Вспомогательные вещества могут быть «приемлемыми» в смысле их совместимости с другими ингредиентами композиции и безвредности для реципиентов.
Фармацевтические композиции включают композиции, подходящие для перорального, ректального, назального, местного (включая чрескожное, буккальное и сублингвальное), вагинального или парентерального (включая подкожное, внутримышечное, внутривенное и внутрикожное) введения. Композиции можно получать любым способом, хорошо известным в области фармации, например, используя способы, описанные в Gennaro et al., Remington,s Pharmaceutical Sciences (18th ed., Mack Publishing company, 1990, см., в частности, часть 8: Pharmaceutical Preparations and Their Manufacture).
Такие способы включают стадию связывания активного ингредиента с любым вспомогательным агентом. Вспомогательный(е) агент(агенты), называемые также добавочными ингредиентами, включают агенты, традиционно используемые в данной области (Gennaro, supra), такие как наполнители, связывающие вещества, разбавители, разрыхлители, смазывающие вещества, красители, отдушки и увлажняющие агенты.
Фармацевтические композиции, подходящие для перорального введения, представлены в виде отдельных дозированных единиц, таких как пилюли, таблетки или капсулы, или в виде порошка или гранул, или в виде раствора или суспензии. Активный ингредиент также может быть представлен в виде болюса или пасты. Композиции можно также получать в форме суппозиториев или клизм для ректального введения.
Для парентерального введения подходящие композиции включают водные и неводные стерильные инъекции. Композиции могут быть представлены в контейнерах, включающих одну или несколько доз, например запаянные пузырьки и ампулы, и могут храниться в условиях сушки замораживанием (в лиофилизированной форме), когда требуется только добавление стерильного водного носителя, например воды, перед применением.
Композиции, или составы, подходящие для введения путем назальной ингаляции, включают тонко измельченные порошки или пылевидные частицы, генерируемые отмеренными дозами герметизированными аэрозольными устройствами, распылителями или инсуффляторами.
Соединения тиено[2,3-d]пиримидина по настоящему изобретению также могут вводиться в форме имплантируемых фармацевтических устройств, состоящих из ядра активного вещества, заключенного в мембрану, регулирующую скорость его высвобождения. Такие имплантанты применяют подкожно или местно, и высвобождение активного ингредиента происходит с приблизительно постоянной скоростью в течение относительно длительных промежутков времени, например от недель до нескольких лет. Способы получения имплантируемых фармацевтических устройств, как таковых, известны в данной области техники, например, как описано в европейском патенте 0303306 (AKZO N.V.).
Таким образом, соединения, согласно данному изобретению, могут применяться для тех же самых клинических целей, что и природный LH, с тем преимуществом, что они обладают FSH активностью, проявляют улучшенные свойства стабильности и могут вводиться различным образом.
Соединения по настоящему изобретению, представленные общей формулой (I), получают, главным образом, путем нуклеофильного замещения соединений общей формулы (II), где Q=Cl или Br, аминами общей формулы (III) в подходящем растворителе, таком как N,N-диметилформамид или ТГФ, при комнатной температуре в присутствии третичного основания, такого как N,N-дизопропилэтиламин. Большинство аминов общей формулы (III) являются коммерчески доступными.

Производные формулы (II), где Q=Cl или Br, можно получить региоселективным ацилированием мета-производных анилина формулы (V-a) хлорангидридами карбоновой кислоты типа (IV), где Q=Cl или Br, в присутствии третичного основания, такого как N,N-дизопропилэтиламин, в подходящем растворителе, таком как дихлорметан или ТГФ.

Соединения формулы (V) можно получить при помощи хорошо известного в данной области восстановления функциональной нитрогруппы в производных формулы (VI), используя подходящий восстановитель, такой как водород, в присутствии металлического катализатора (Pd/Pt). Соответствующие способы восстановления описаны в: P.M. Carabateas, P.R. Brundage, K.O. Gellote, M.D. Gruett, R.R. Lorenz, J. Heterocycl. Chem. 21, 1849 (1984). Альтернативно, восстановление можно проводить хлоридом олова (II) в протонном растворителе, таком как этанол, в присутствии хлористоводородной кислоты, при повышенной температуре (J. Heilbron, J. Chem. Soc, 1279 (1940)).

Тиенопиримидины общей формулы (VI) можно получить конденсацией карбоновых кислот (VII) с трет-бутиламином под воздействием агента связывания, такого как тетрафторборат О-(бензотриазол-1-ил)-N,N,N,,N,-тетраметилурония (TBTU) или гексафторфосфат бромтрипирролидинофосфония (PyBrOP), и третичного основания, например N,N-диизопропилэтиламина.

Омыление соответствующих сложных этиловых эфиров (VIII) до карбоновых кислот (VII) происходит в присутствии основания, такого как гидроксид лития, гидроксид калия или гидроксид натрия, в водном диоксане при повышенной температуре (от 80°С до температуры кипения).

Бициклические системы общей формулы (VIII) получают замещением хлоридов формулы (X) этилмеркаптоацетатом действием N,N-диизопропилэтиламина с последующей катализируемой основанием циклизацией промежуточных тиоэфиров (IX). Этот способ образования кольца тиено[2,3-d]пиримидина описан в: S.A. Abdel-Hady, M.A. Badawy, Y.A. Ibrahim, Sulfur Lett. 9, 101 (1989) и S. Tumkevicius, Liebigs Ann., 1703 (1995).

Подходящими условиями для реакции циклизации являются этоксид натрия в этаноле или N,N-диизопропилэтиламин в толуоле/этаноле (1/1, об/об), при температуре кипения.
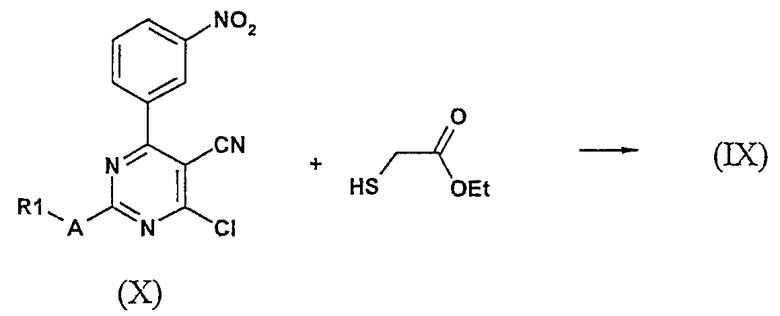
Соединения формулы (Х) можно синтезировать следующими способами, описанными в литературе, как, например, описано A.A. Santilli, D.H. Kim and S.V. Wanser, J. Heterocycl. Chem. 8, 445, 1971. В типичных условиях эксперимента амид, имеющий общую структуру (XI), обрабатывали POCl3 при повышенной температуре (от 80°С до температуры кипения). Добавление соответствующего растворителя, например диоксана, и/или добавление либо PCl5, либо N,N-диметиланилина к реакционной смеси может в результате сократить время реакции и обеспечить более высокие выходы хлоридов (Х).
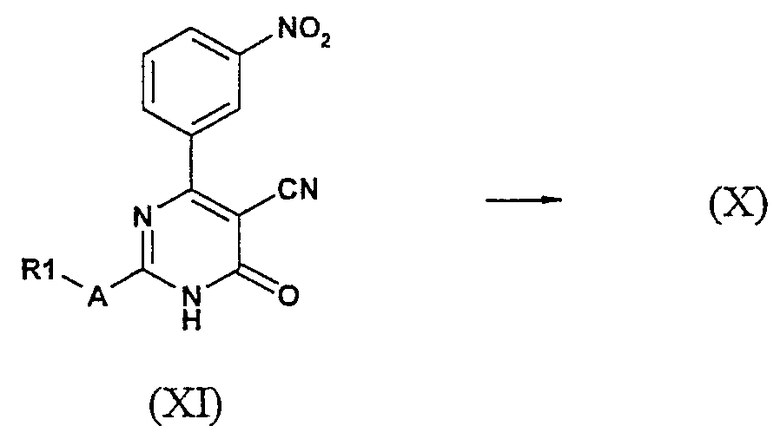
Основной путь, приводящий к получению лактамов формулы (XI), включает конденсацию этилцианоацетата с 3-нитробензальдегидом и соединениями (XII), которые могут представлять собой изотиомочевину (XII-a), изомочевину (XII-b), монозамещенные гуанидины (XII-c), дизамещенные гуанидины (XII-d) или амидины (XII-e).

В обычном эксперименте этилцианоацетат, 3-нитробензальдегид и производное (XII) суспендируют в подходящем растворителе, например этаноле, метаноле, N,N-диметилформамиде, N-метилпирролидиноне, тетрагидрофуране или пиридине, и добавляют основание, такое как карбонат калия, ацетат натрия, метоксид натрия или этоксид натрия. Реакция проходит при повышенной температуре (от 70°С до температуры кипения). После фильтрации остатки переносят в воду и подкисляют (рН 2), после чего происходит осаждение продуктов (XI) (S. Kambe, K. Saito and H. Kishi, Synthesis, 287 (1979); A.M. Abd-Elfattah, S.M. Hussain and A.M. El-Reedy, Tetrahedron 39, 3197 (1983); S.M. Hussain, A.A. El-Barbary and S.A. Mansour, J. Heterocycl. Chem. 22, 169 (1985)).

Альтернативно, соединения данного изобретения, в которых А=N, представленные формулой (I-a), можно получить из производных сульфоксида общей формулы (XIII) путем нуклеофильного замещения нуклеофилами амина общей структуры (XIV). Реакцию обычно проводят при повышенной температуре в присутствии третичного основания, такого как N,N-дизопропилэтиламин, в подходящем растворителе, таком как 1,4-диоксан.

Подобным образом, соединения данного изобретения, в которых А=О, представленные формулой (I-b), можно получить из производных сульфоксида общей формулы (XIII) путем нуклеофильного замещения нуклеофилами алкоксида общей структуры (XV). Реакцию проводят в присутствии трет-бутоксида калия с избытком спирта R1-OH.
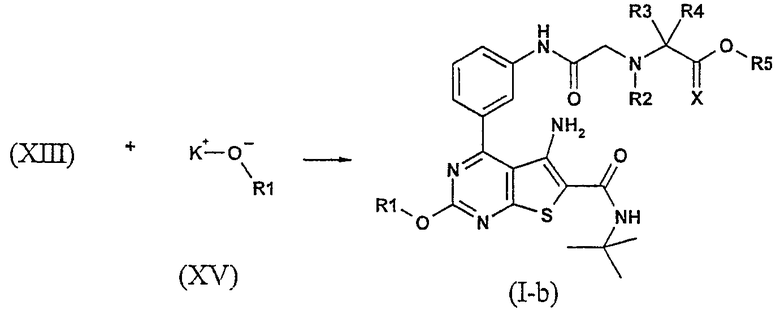
Производные сульфоксида общей формулы (XIII) можно получить окислением соединений общей формулы (I), где R1=Ме и А=S, представленных формулой (I-c). Окисление осуществляют при помощи 3-хлорпербензойной кислоты в трифторуксусной кислоте. Кислотная природа растворителя предотвращает окисление 5-амино группы в соответствующее 5-нитрозопроизводное.

Хорошо известны способы определения связывания рецептора, так же как анализы in vitro и in vivo для определения биологической активности гонадотропинов. Как правило, экспрессированный рецептор контактирует с тестируемым соединением, и измеряют связывание или стимуляцию или ингибирование функционального ответа.
Для того чтобы измерить функциональный ответ, выделенную ДНК, кодирующую ген рецептора LH или FSH, предпочтительно рецептора человека, экспрессировали в подходящих клетках хозяина. Такой клеткой может быть клетка яичника китайского хомячка, но также подходящими являются и другие клетки. Предпочтительными клетками являются клетки, происходящие от млекопитающих (Jia et al, Mol.Endocrin., 5:759-776, 1991).
Способы конструирования клеточных линий, экспрессирующих рекомбинантный LH или FSH, хорошо известны в данной области (Sambrook et al., Molecular Cloning: a Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, latest edition). Экспрессия рецептора достигается путем экспрессии ДНК, кодирующей желаемый белок. В настоящее время в данной области техники хорошо известны методы сайт-направленного мутагенеза, лигирования добавленных последовательностей, ПЦР и конструирования подходящих систем экспрессии. Части или полную конструкцию ДНК, кодирующую желаемый белок, можно получить синтетическим путем, используя стандартные методы твердофазного синтеза, предпочтительно, для включения рестрикционных сайтов для облегчения лигирования. Для кодирующих последовательностей ДНК могут быть обеспечены подходящие элементы контроля для транскрипции и трансляции включенной кодирующей последовательности. Как хорошо известно, в настоящее время существуют системы экспрессии, которые совместимы с широким диапазоном хозяев, включая прокариотических хозяев, таких как бактерии, и эукариотических хозяев, таких как дрожжи, клетки растений, клетки насекомых, клетки млекопитающих, клетки птиц и т.п.
Клетки, экспрессирующие рецептор, затем контактируют с тестируемым соединением для наблюдения за связыванием, или стимуляцией, или ингибированием функционального ответа.
Альтернативно, для того чтобы измерить связывание соединения, можно использовать выделенные клеточные мембраны, содержащие экспрессированный рецептор.
Для измерения связывания можно использовать радиоактивно или флуоресцентно меченные соединения. В качестве контрольного соединения можно использовать человеческий рекомбинантный LH или FSH. В качестве альтернативы также проводят анализы конкурентного связывания.
Другой анализ включает скрининг соединений для определения свойств агониста LH или FSH рецептора путем определения стимулирования рецептора, опосредованного сАМР аккумуляцией. Таким образом, этот способ включает экспрессию рецептора на клеточной поверхности клетки хозяина и воздействие на клетку тестируемого соединения. Затем измеряют количество сАМР. Уровень сАМР должен быть пониженным или повышенным, в зависимости от ингибирующего или стимулирующего действия тестируемого соединения при его связывании с рецептором.
Помимо непосредственного измерения, например, уровней сАМР в подвергнутой воздействию соединения клетке, можно использовать клетки, которые помимо трансфекции кодирующей рецептор ДНК, также являются трансфицированными второй ДНК, кодирующей репортерный ген, экспрессия которого отвечает уровню сАМР. Такие репортерные гены могут быть индуцируемыми сАМР или могут быть сконструированы таким образом, чтобы они были связаны с новыми, реагирующими на сАМР элементами. Главным образом, экспрессия репортерного гена может контролироваться любым чувствительным элементом, реагирующим на изменения уровней сАМР. Подходящими репортерными генами являются, например, LacZ, щелочная фосфатаза, люцифераза светлячка и зеленый флуоресцентный белок. Принципы таких анализов трансактивации хорошо известны в данной области и описаны, например, в Stratowa, Ch, Himmler, A and Czernilofsky, A.P. (1995) Curr.Opin.Biotechnol.6:574.
Для отбора соединений, проявляющих активность в отношении LH или FSH рецептора, тестирование при концентрации 10-5 М должно показывать активность, составляющую более 20% от максимальной активности, когда LH или FSH используют в качестве контроля для сравнения. Другим критерием может быть величина ЕС50, которая должна составлять <10-5 М, предпочтительно <10-7 М.
Специалисту в данной области должно быть понятно, что желаемые величины ЕС50 зависят от тестируемого соединения. Например, соединение, величина ЕС50 которого менее чем 10-5 М, как правило, считается кандидатом для выбора лекарственного средства. Предпочтительно эта величина является менее чем 10-7 М. Однако соединение, имеющее более высокое значение ЕС50, но являющееся селективным в отношении конкретного рецептора, может быть даже более лучшим кандидатом.
Для скрининга соединений, являющихся агонистами LH рецептора, можно также использовать биоанализ клеток Лейдига мыши (Van Damme, M., Robersen, D. and Diczfalusy, E. (1974). Acta Endocrinol. 77: 655-671 Mannaerts, B., Kloosterboer, H. and Schuurs, A. (1987). Neuroendocrinology of reproduction. R. Rolland et al. Eds., Elsevier Science Publishers B.V., 49-58). В этом анализе стимуляцию LH рецептора, опосредованную продуцированием тестостерона, можно измерить в клетках Лейдига, выделенных у мужских особей мыши.
FSH агонистическую активность соединений можно определить также на модели ex vivo, используя культивированные мышиные фолликулы, в соответствии с Nayudu, P. and Osborn, S. (1992, J. Reproduction and Fertility 95:349-362). Для этого мышиные яичниковые фолликулы выделяли и культивировали в присутствии соединений, являющихся агонистами FSH, для индукции роста фолликулов. Измерения диаметра фолликул и эстрадиола в культуральной среде являлись показателями роста фолликул.
Для измерения in vivo активности соединений в отношении LH исследовали индукцию овуляции у незрелой женской особи мыши. В этом анализе незрелую самку мыши примировали выделенным из мочи FSH и приблизительно через 48 часов обрабатывали соединением-агонистом LH. После обработки агонистом LH животных умерщвляли и с помощью микроскопического анализа оценивали число женских зародышевых клеток в маточной трубе.
Для измерения in vivo активности соединений в отношении FSH незрелых самок крыс во время 0, 8, 24 и 32 часа обрабатывали соединением, являющимся агонистом FSH, для индукции роста фолликул. Через 52 часа после начала эксперимента животным вводили hCG путем инъекции, чтобы индуцировать овуляцию. Животных умерщвляли через 72 часа после начала эксперимента и с помощью микроскопического анализа оценивали число женских зародышевых клеток в маточной трубе. Помимо этого, определяли вес яичника.
Соединения данного изобретения могут применяться в клинических условиях, в том же режиме, как в настоящее время применяют LH или hCG. Такое применение включает LH замещение у субъектов с пониженной функцией половых желез, и мужского и женского пола, введение в середине цикла для индуцирования овуляции (индукции овуляции (OI) или контролируемой гиперстимуляции (COH) или стимуляции corpus luteum).
Приведенные ниже примеры являются иллюстрацией изобретения и никоим образом не должны интерпретироваться как ограничивающие объем изобретения.
ПРИМЕРЫ
Пример 1
трет-Бутил 5-амино-2-метилтио-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) 5-Циано-4-(3-нитрофенил)-2-метилтио-6-гидроксипиримидин
Смесь сульфата S-метилизотиомочевины (69,0 г), 3-нтробензальдегида (75,0 г), этилцианоацетата (56,0 мл) и карбоната калия (72,5 г) в абсолютном EtOH (1500 мл) перемешивали при 60°С в течение 16 часов. Реакционную смесь охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали, промывали абсолютным EtOH и растворяли в горячей воде (100°С). Раствор охлаждали до комнатной температуры, подкисляли 2 н. HCl до рН 2 и охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали и промывали ледяной водой. Оставшуюся в осадке воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 54,0 г.
MS-ESI: [M+H]+=289,0.
ТСХ: Rf=0,3, силикагель, DCM/MeOH=9/1 (об/об).
(b) 6-Хлор-5-циано-4-(3-нитрофенил)-2-метилтиопиримидин
К перемешиваемому раствору 5-циано-4-(3-нитрофенил)-2-метилтио-6-гидроксипиримидина (пример 1(а), 25,0 г) в сухом 1,4-диоксане (300 мл) добавляли POCl3 (100 мл). Через 3 часа при 90°С смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении. Остаток растворяли в 1,4-диоксане (100 мл) и полученный раствор охлаждали до 0°С. Осторожно добавляли ледяную воду. Полученный осадок отфильтровывали и промывали водой. Оставшуюся в осадке воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 26,0 г.
MS-ESI: [M+H]+=307,0.
ТСХ: Rf=0,5, силикагель, гептан/EtOAc=3/2 (об/об).
(с) Этил 5-циано-4-(3-нитрофенил)-2-метилтио-6-(этоксикарбонилметилтио)пиримидин
К перемешиваемому раствору этил 2-меркаптоацетата (9,3 мл) и 6-хлор-5-циано-4-(3-нитрофенил)-2-метилтиопиримидина (пример 1(b), 26,0 г) в смеси EtOH (250 мл) и DCM (250 мл) добавляли DIPEA (15,7 мл). Через 1 час при комнатной температуре к смеси добавляли 0,1 н. водный HCl (500 мл) и затем экстрагировали DCM (3x500 мл), сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 28,0 г.
MS-ESI: [M+H]+=391,4.
ТСХ: Rf=0,5, силикагель, гептан/EtOAc=3/2 (об/об).
(d) Этил 5-амино-4-(3-нитрофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат
Смесь этил 5-циано-4-(3-нитрофенил)-2-метилтио-6-(этоксикарбонилметилтио)пиримидина (пример 1(с), 28,0 г) и DIPEA (30 мл) в смеси толуола (150 мл) и EtOH (150 мл) перемешивали при температуре кипения с обратным холодильником (100°С) в течение 16 часов. Затем смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении. Оставшийся DIPEA удаляли совместным выпариванием с толуолом.
Выход: 28,0 г.
MS-ESI: [M+H]+=391,4.
ТСХ: Rf=0,6, силикагель, гептан/EtOAc=3/2 (об/об).
(е) Этил 5-амино-4-(3-нитрофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилат
К смеси этил 5-амино-4-(3-нитрофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилата (пример 1(d), 28,0 г), концентрированной водной HCl (15 мл) и хлорида олова (II) (41,0 г) в 1,4-диоксане (400 мл) добавляли EtOH (400 мл). Смесь перемешивали при 90°С в течение 16 часов. Затем смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении. Остаток суспендировали в EtOAc (1000 мл). Для достижения уровня рН 10-11 добавляли 4 н. водной NaOH. Смесь тщательно перемешивали и органический слой отделяли, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 21,0 г.
MS-ESI: [M+H]+=361,0.
ТСХ: Rf=0,6, силикагель, гептан/EtOAc=3/2 (об/об).
(f) 5-Амино-4-(3-аминофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоновая кислота
К раствору этил 5-амино-4-(3-нитрофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксилата (пример 1(е), 21,0 г) в смеси 1,4-диоксана (300 мл) и воды (100 мл) добавляли гидроксид калия (32,4 г). Через 16 часов при 90°С смесь охлаждали до 10°С и при тщательном перемешивании добавляли 2 н. водный раствор лимонной кислоты (300 мл). Полученный осадок отфильтровывали, промывали водой (180 мл) и сушили в вакууме.
Выход: 14,0 г.
MS-ESI: [M+H]+=333,0.
ТСХ: Rf=0,5, силикагель, DCM/MeOH=9/1 (об/об).
(g) трет-Бутил 5-амино-4-(3-аминофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксамид
К раствору 5-амино-4-(3-аминофенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоновой кислоты (пример 1(f), 14,0 г), DIPEA (17,4 мл) и трет-бутиламина (7,3 г) в DCM/DMF (1/1, об/об, 250 мл) добавляли TBTU (16,1 г). Через 3 часа при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (3x100 мл), 0,1 н. водным раствором HCl (100 мл) и водой (100 мл). Органический слой концентрировали при пониженном давлении. Неочищенный продукт очищали кристаллизацией из теплого абсолютного EtOH (300 мл).
Выход: 10,5 г.
MS-ESI: [M+H]+=388,2.
ВЭЖХ: Rf=30,72 мин, Luna C-18(2), 5 мкм, 250х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: вода/ACN/MeOH=от 90/9,5/0,5 до 0/95/5, время цикла=50 мин.
(h) трет-Бутил 5-амино-2-метилтио-4-(3-(2-бромацетамидо)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-2-метилтио 4-(3-аминофенил)- тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(g), 1,08 г) и DIPEA (2,43 мл) в сухом DCM (20 мл) добавляли бромацетилхлорид (615 мг). Через 3 часа при комнатной температуре смесь разбавляли DCM, промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали колоночной хроматографией на силикагеле, используя в качестве элюента гептан/EtOAc=3/2 (об/об).
Выход: 910 мг.
MS-ESI: [M+H]+=510,2.
ТСХ: Rf=0,5, силикагель, гептан/EtOAc=3/2 (об/об).
(i) трет-Бутил 5-амино-2-метилтио-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-метилтиотиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) в DCM (5 мл) добавляли N-метил-2-аминоэтанол (250 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водного ТФУК и воды.
Выход: 112 мг (соль ТФУК).
MS-ESI: [M+H]+=503,2.
ВЭЖХ: Rt=11,45 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 2
трет-Бутил 5-амино-2-метилтио-4-(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) в DCM (5 мл) добавляли 2-амино-2-метилпропанол (250 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 67 мг (соль ТФУК).
MS-ESI: [M+H]+=517,2.
ВЭЖХ: Rt=12,67 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 3
трет-Бутил 5-амино-2-метилтио-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) и N,N-диизопропилэтиламина (0,20 мл) в DCM (5 мл) добавляли гидрохлорид глицинметилового эфира (200 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 133 мг (соль ТФУК).
MS-ESI: [M+H]+=517,2.
ВЭЖХ: Rt=11,87 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 4
трет-Бутил 5-амино-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-2-метилтио-4-(3-(2-бромацетамидо)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 200 мг) в DCM (5 мл) добавляли N-(2-метоксиэтил)этиламин (266 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 84 мг (соль ТФУК).
MS-ESI: [M+H]+=531,2.
ВЭЖХ: Rt=12,62 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 5
трет-Бутил 5-амино-4-(3-((N-(R-1-метоксикарбонил-2-метилпроп-1-ил)глицинил)амино)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-2-метилтио-4-(3-(2-бромацетамидо)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) и N,N-диизопропилэтиламина (0,20 мл) в DCM (5 мл) добавляли гидрохлорид метилового эфира D-валина (250 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 77 мг (соль ТФУК).
MS-ESI: [M+H]+=559,2.
ВЭЖХ: Rt=13,22 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 6
трет-Бутил 5-амино-4-(3-((N,N-бис-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-2-метилтио-4-(3-(2-бромацетамидо)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) в DCM (5 мл) добавляли N,N-бис-(2-метоксиэтил)амин (400 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 166 мг (соль ТФУК).
MS-ESI: [M+H]+=561,3.
ВЭЖХ: Rt=13,62 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 7
трет-Бутил 5-амино-2-метилтио-4-(3-((2,3-дигидроксипроп-1-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) в DCM (5 мл) добавляли 3-амино-2-гидроксипропанол (250 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 164 мг (соль ТФУК).
MS-ESI: [M+H]+=519,2.
ВЭЖХ: Rt=12,62 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 8
трет-Бутил 5-амино-2-метилтио-4-(3-((1,3-дигидроксипроп-2-ил)глицинил)амино)фенил-тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-метилтио-тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(h), 250 мг) в DCM (5 мл) добавляли 2-амино-3-гидроксипропанол (250 мг). Через 16 часов при комнатной температуре смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 117 мг (соль ТФУК).
MS-ESI: [M+H]+=519,2.
ВЭЖХ: Rt=12,62 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 9
трет-Бутил 5-амино-2-фенил-4-(3-((N-этил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) 5-Циано-4-(3-нитрофенил)-2-фенил-6-гидроксипиримидин
Смесь бензамидингидрохлорида (16,4 г), 3-нитробензальдегида (15,1 г), этилцианоацетата (11,2 мл) и карбоната калия (16,6 мг) в абсолютном EtOH (250 мл) перемешивали при 60°С в течение 8 часов. Реакционную смесь охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали, промывали абсолютным EtOH и нагревали в воде (100°С) до тех пор, пока не получили прозрачный раствор. Раствор охлаждали до 50°С, подкисляли до рН 2, добавляя 2 н. водный раствор HCl и охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали и промывали водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 15,0 г.
MS-ESI: [M+H]+=319,2.
ТСХ: Rf=0,3, силикагель, DCM/MeOH=9/1 (об/об).
(b) 6-Хлор-5-циано-4-(3-нитрофенил)-2-фенилпиримидин
К перемешиваемому раствору 5-циано-4-(3-нитрофенил)-2-фенил-6-гидроксипиримидина (пример 9(а), 15,0 г) и диметиланилина (0,5 мл) в сухом 1,4-диоксане р.а. (200 мл) добавляли POCl3 (50 мл). Через 3 часа при 90°С теплую смесь отфильтровывали и фильтрат концентрировали при пониженном давлении. Остаток растворяли в 1,4-диоксане и добавляли ледяную воду. Полученный осадок отфильтровывали и промывали водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 15,8 г.
MS-ESI: [M+H]+=337,4.
ТСХ: Rf=0,8, силикагель, гептан/EtOAc=3/2 (об/об).
(с) Этил 5-циано-4-(3-нитрофенил)-2-фенил-6-(этоксикарбонилметилтио)-пиримидин
К перемешиваемому раствору этил 2-меркаптоацетата (5,15 мл) и 6-хлор-5-циано-4-(3-нитрофенил)-2-фенилпиримидина (пример 9(b), 15,8 г) в смеси EtOH (125 мл) и DCM (125 мл) в атмосфере азота добавляли DIPEA (8,71 мл). Через 2 часа при комнатной температуре смесь разбавляли DCM до полного растворения, промывали 0,5 н. водным раствором HCl, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 19,7 г.
MS-ESI: [M+H]+=421,2.
ТСХ: Rf=0,7, силикагель, гептан/EtOAc=3/2 (об/об).
(d) Этил 5-амино-4-(3-нитрофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксилат
К перемешиваемому раствору 5-циано-4-(3-нитрофенил)-2-фенил-6-(этоксикарбонилметилтио)пиримидина (пример 9(с), 19,7 г) в смеси абсолютного EtOH (100 мл) и толуола р.а. (100 мл) добавляли DIPEA (20,0 мл). Через 48 часов при 100°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, промывали холодным EtOH и сушили в вакууме при 40°С.
Выход: 17,0 г.
MS-ESI: [M+H]+=421,2.
ТСХ: Rf=0,5, силикагель, гептан/EtOAc=3/2 (об/об).
(е) Этил 5-амино-4-(3-аминофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксилат
К раствору этил 5-амино-4-(3-нитрофенил)-2-фенил-тиено[2,3-d]пиримидин-6-карбоксилата (пример 9(d), 16,6 г) в 1,4-диоксане р.а. (250 мл) добавляли хлорид олова (II) (23,0 г) в абсолютном EtOH. Добавляли 37% водный раствор HCl (6,9 мл) и смесь кипятили с обратным холодильником в течение 16 часов. Смесь оставляли охлаждаться до комнатной температуры и концентрировали при пониженном давлении. Остаток суспендировали в EtOAc (500 мл). Для достижения уровня рН 10-11 добавляли 4 н. водный NaOH. Смесь разбавляли добавлением насыщенного водного раствора NaCl. Органический слой отделяли, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 17,0 г.
MS-ESI: [M+H]+=421,2.
ТСХ: Rf=0,5, силикагель, гептан/EtOAc=3/2 (об/об).
(f) 5-Амино-4-(3-аминофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоновая кислота
К раствору этил 5-амино-4-(3-аминофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксилата (пример 9(е), 17,0 г) в смеси 1,4-диоксана (210 мл) и воды (80 мл) добавляли гидроксид калия (20,0 г). Через 16 часов при 90°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, суспендировали в воде (300 мл) и охлаждали до 0°С. Смесь подкисляли до рН 3, добавляя 2 н. водный раствор лимонной кислоты и перемешивали при 0°С до достижения комнатной температуры в течение 2 часов. Полученный осадок отфильтровывали, промывали водой и сушили в вакууме при 40°С.
Выход: 13,3 г.
MS-ESI: [M+H]+=363,0.
ТСХ: Rf=0,2, силикагель, DCM/MeOH=95/5 (об/об).
(g) трет-Бутил 5-амино-4-(3-аминофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксамид
К смеси 5-амино-4-(3-аминофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоновой кислоты (пример 9(f), 13,3 г) в смеси DCM (250 мл) и DMF (250 мл), в атмосфере азота, добавляли DIPEA (15,3 мл), трет-бутиламин (9,3 мл) и TBTU (14,1 г). Через 3 часа при комнатной температуре смесь разбавляли DCM и промывали насыщенным водным раствором NaHCO3, 0,1 н. водным раствором HCl и насыщенным водным раствором NaCl. Органический слой сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали при помощи хроматографии на силикагеле, используя в качестве элюента гептан/EtOAc=от 3/7 до 1/1 (об/об).
Выход: 14,7 г.
MS-ESI: [M+H]+=418,4.
ТСХ: Rf=0,4, силикагель, гептан/EtOAc=3/2 (об/об).
(h) трет-Бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-аминофенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксамида (пример 9(g), 5,8 г) и DIPEA (12,2 мл) в DCM (50 мл) по каплям добавляли бромацетилхлорид (2,80 мл). Через 3 часа при комнатной температуре смесь разбавляли DCM, промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали хроматографией на силикагеле, используя в качестве элюента гептан/EtOAc=3/2 (об/об). Получали смесь 1:1 (моль/моль) трет-бутил 5-амино-4-(3-(2-бромацетамидо)-фенил)-2-фенил-тиено[2,3-d]пиримидин-6-карбоксамида и трет-бутил 5-амино-4-(3-(2-хлорацетамидо)-фенил)-2-фенил-тиено[2,3-d]пиримидин-6-карбоксамида.
Выход: 2,6 г.
MS-ESI: [M+H]+=540,2, [M,+H]+=494,2.
ТСХ: Rf=0,3, силикагель, гептан/EtOAc=3/2 (об/об).
(i) трет-Бутил 5-амино-2-фенил-4-(3-((N-этил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксамида (пример 9(h), 500 мг) в DCM (5 мл) добавляли N-этил-2-аминоэтанол (500 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (100 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х50 мл), сушили (MgSO4) и концентрировали в вакууме. Неочищенный продукт очищали ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 271 мг (соль ТФУК).
MS-ESI: [M+H]+=547,2.
ВЭЖХ: Rt=11,88 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 10
трет-Бутил 5-амино-2-фенил-4-(3-(N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-фенилтиено[2,3-d]пиримидин-6-карбоксамида (пример 9(h), 500 мг) и N,N-диизопропилэтиламина (DIPEA, 1 мл) в DCM (5 мл) добавляли гидрохлорид метилового эфира глицина (700 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (100 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х50 мл), сушили (MgSO4) и концентрировали в вакууме. Неочищенный продукт очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водного раствора ТФУК и воды.
Выход: 321 мг (соль ТФУК).
MS-ESI: [M+H]+=547,2.
ВЭЖХ: Rt=12,54 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 11
трет-Бутил 5-амино-2-(2-фурил)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) 2-амидинофуран
В охлажденный (баня со льдом, 0°С) реакционный сосуд, содержащий 2-фуронитрил (13 мл), добавляли охлажденный (0°С) и насыщенный этанольный раствор HCl (40 мл). Полученный раствор оставляли до достижения комнатной температуры и перемешивали в атмосфере азота в течение 48 часов. После концентрирования реакционной смеси в вакууме остаток, содержащий соответствующий 2-фурилэтилимидат, повторно растворяли в этаноле (20 мл) и перемешивали при 0°С в атмосфере азота. Затем добавляли насыщенный этанольный раствор аммиака (40 мл) и реакционную смесь перемешивали в запаянном реакционном сосуде в течение 48 часов. После фильтрации реакционной смеси фильтрат концентрировали при пониженном давлении. Неочищенное соединение использовали на следующей стадии без дополнительной очистки.
Выход: 15,0 г.
(b) 5-Циано-4-(3-нитрофенил)-2-(2-фурил)-6-гидроксипиримидин
Смесь 2-амидинофурана (пример 11(а), 15 г), 3-нитробензальдегида (24 г), этилцианоацетата (17 мл) и карбоната калия (25 г) в абсолютном EtOH (300 мл) перемешивали при 60°С в течение 16 часов. Реакционную смесь охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали, промывали абсолютным EtOH и нагревали в воде (100°С) до получения суспензии молочного цвета. Суспензию охлаждали до 50°С, подкисляли до рН 2, добавляя 2 н. водный раствор HCl, и охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали и промывали ледяной водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 16,0 г.
MS-ESI: [M+H]+=309,2.
ТСХ: Rf=0,3, силикагель, DCM/MeOH=9/1 (об/об).
(с) 6-Хлор-5-циано-4-(3-нитрофенил)-2-(2-фурил)пиримидин
К перемешиваемому раствору 5-циано-4-(3-нитрофенил)-2-(2-фурил)-6-гидроксипиримидина (пример 11(b), 16,0 г) и диметиланилина (0,5 мл) в сухом 1,4-диоксане р.а. (250 мл) добавляли POCl3 (50 мл). Через 2 часа при 90°С теплую смесь отфильтровывали и фильтрат концентрировали при пониженном давлении. Остаток растворяли в 1,4-диоксане и добавляли в ледяную воду. Полученный осадок отфильтровывали и промывали водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 16,0 г.
MS-ESI: [M+H]+=327,2.
ТСХ: Rf=0,75, силикагель, гептан/EtOAc=3/2 (об/об).
(d) Этил 5-циано-4-(3-нитрофенил)-2-(2-фурил)-6-(этоксикарбонилметилтио)пиримидин
К перемешиваемому раствору этил 2-меркаптоацетата (5,4 мл) и 6-хлор-5-циано-4-(3-нитрофенил)-2-(2-фурил)пиримидина (пример 11(с), 16,0 г) в смеси EtOH (125 мл) и DCM (125 мл) в атмосфере азота добавляли DIPEA (9,1 мл). Через 2 часа при комнатной температуре смесь разбавляли DCM до полного растворения, промывали 0,5 н. водным раствором HCl, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 20,0 г.
MS-ESI: [M+H]+=411,2.
ТСХ: Rf=0,7, силикагель, гептан/EtOAc=3/2 (об/об).
(е) Этил 5-амино-4-(3-нитрофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксилат
К перемешиваемому раствору этил 5-циано-4-(3-нитрофенил)-2-(2-фурил)-6-(этоксикарбонилметилтио)пиримидина (пример 11(d), 20 г) в смеси абсолютного EtOH (100 мл) и толуола р.а. (100 мл) добавляли DIPEA (20,0 мл). Через 48 часов при 100°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, промывали холодным EtOH и сушили в вакууме при 40°С.
Выход: 20 г.
MS-ESI: [M+H]+=411,2.
ТСХ: Rf=0,6, силикагель, гептан/EtOAc=3/2 (об/об).
(f) Этил 5-амино-4-(3-аминофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксилат
К раствору этил 5-амино-4-(3-нитрофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксилата (пример 11(е), 20 г) в 1,4-диоксане р.а. (250 мл) добавляли раствор хлорида олова (II) (28,0 г) в абсолютном EtOH (250 мл). Добавляли 37% водный раствор HCl (8,5 мл) и смесь кипятили с обратным холодильником (90°С) в течение 16 часов. Смесь оставляли охлаждаться до комнатной температуры и концентрировали при пониженном давлении. Остаток суспендировали в EtOAc (500 мл). Для достижения уровня рН 10-11 добавляли 4 н. водный раствор NaOH. Смесь разбавляли добавлением насыщенного водного раствора NaCl. Органический слой отделяли, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 17,5 г.
MS-ESI: [M+H]+=381,2.
ТСХ: Rf=0,4, силикагель, гептан/EtOAc=3/2 (об/об).
(g) 5-Амино-4-(3-нитрофенил)-2-(2-фурил)тиено[2,3-d] пиримидин-6-карбоновая кислота
К раствору этил 5-амино-4-(3-аминофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксилата (пример 11(f), 17,5 г) в смеси 1,4-диоксана (210 мл) и воды (80 мл) добавляли гидроксид калия (23,0 г). Через 8 часов при 90°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, суспендировали в воде (300 мл) и охлаждали до 0°С. Смесь подкисляли до рН 3, добавляя 2 н. водный раствор лимонной кислоты, и перемешивали при 0°С до комнатной температуры в течение 2 часов. Полученный осадок отфильтровывали, промывали водой и сушили в вакууме при 40°С.
Выход: 16,9 г.
MS-ESI: [M+H]+=353,2.
ТСХ: Rf=0,2, силикагель, DCM/MeOH=95/5 (об/об).
(h) трет-Бутил 5-амино-4-(3-аминофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору 5-амино-4-(3-аминофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоновой кислоты (пример 11(g), 16,9 г) в смеси DCM (250 мл) и DMF (50 мл) в атмосфере азота добавляли DIPEA (19,2 мл), трет-бутиламин (11,6 мл) и TBTU (17,7 г). Через 3 часа при комнатной температуре образовывалось существенное количество желтого осадка, который отфильтровывали. Остаток промывали диэтиловым эфиром и сушили в вакууме при 40°С.
Выход: 18,0 г.
MS-ESI: [M+H]+=408,2.
ТСХ: Rf=0,4, силикагель, гептан/EtOAc=3/2 (об/об).
(i) трет-Бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-аминофенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 11(h), 250 мг) и DIPEA (0,5 мл) в DCM (5 мл) добавляли бромацетилхлорид (100 л). Через 3 часа при комнатной температуре смесь разбавляли DCM, промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали хроматографией на силикагеле, используя в качестве элюента гептан/EtOAc=3/2 (об/об). Получали смесь 1:1 (моль/моль) трет-бутил 5-амино-4-(3-(2-бромацетамидо)-фенил)-2-(2-тиенил)-тиено[2,3-d]пиримидин-6-карбоксамида и трет-бутил 5-амино-4-(3-(2-хлорацетамидо)-фенил)-2-(2-тиенил)-тиено[2,3-d]пиримидин-6-карбоксамида.
Выход: 124 мг.
MS-ESI: [M+H]+=540,2, [M,+H]+=494,2.
ТСХ: Rf=0,3, силикагель, гептан/EtOAc=3/2 (об/об).
(j) трет-Бутил 5-амино-2-(2-фурил)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)-фенил)-2-(2-фурил)-тиено[2,3-d]пиримидин-6-карбоксамида (пример 11(i), 130 мг) в DCM (5 мл) добавляли N-метил-2-аминоэтанол (200 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х10 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 81 мг (соль ТФУК)
MS-ESI: [M+H]+=523,2
ВЭЖХ: Rt=11,01 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 12
трет-Бутил 5-амино-2-(2-фурил)-4-(3-(N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 11(i), 130 мг) в DCM (5 мл) добавляли 2-амино-2-метилпропанол (260 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х50 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 54 мг (соль ТФУК).
MS-ESI: [M+H]+=537,2.
ВЭЖХ: Rt=11,15 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 13
трет-Бутил 5-амино-2-(2-фурил)-4-(3-(N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-фурил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 11(i), 130 мг) и DIPEA (0,5 мл) в DCM (5 мл) добавляли гидрохлорид метилового эфира глицина (324 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х10 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 74 мг (соль ТФУК).
MS-ESI: [M+H]+=537,2.
ВЭЖХ: Rt=12,09 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 14
трет-Бутил 5-амино-2-(2-тиенил)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) 5-Циано-4-(3-нитрофенил)-2-(2-тиенил)-6-гидроксипиримидин
Смесь 2-амидинотиофенгидрохлорида (10,0 г), 3-нитробензальдегида (9,7 г), этилцианоацетата (6,81 мл) и карбоната калия (10,1 г) в абсолютном EtOH (200 мл) перемешивали при 60°С в течение 8 часов. Реакционную смесь охлаждали до 0°С в бане со льдом, фильтровали, промывали абсолютным EtOH и остаток растворяли в воде (100°С). Раствор охлаждали до 50°С, подкисляли 2 н. водным раствором HCl до рН 2 и охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали и промывали ледяной водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 10,0 г.
MS-ESI: [M+H]+=325,0.
ТСХ: Rf=0,3, силикагель, DCM/MeOH=9/1 (об/об).
(b) 6-Хлор-5-циано-4-(3-нитрофенил)-2-(2-тиенил)пиримидин
К перемешиваемому раствору 5-циано-4-(3-нитрофенил)-2-(2-тиенил)-6-гидроксипиримидина (пример 14(а), 10,0 г) и диметиланилина (несколько капель) в сухом 1,4-диоксане (150 мл) добавляли POCl3 (30 мл). Через 3 часа при 90°С смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении. Остаток растворяли в 1,4-диоксане и осторожно добавляли ледяную воду. Полученный осадок отфильтровывали и промывали водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном и сушили в вакууме при 40°С.
Выход: 9,8 г.
MS-ESI: [M+H]+=343,4.
ТСХ: Rf=0,8, силикагель, гептан/EtOAc=3/2 (об/об).
(с) Этил 5-циано-4-(3-нитрофенил)-2-(2-тиенил)-6-(этоксикарбонилметилтио)пиримидин
К перемешиваемому раствору этил 2-меркаптоацетата (3,28 мл) и 6-хлор-5-циано-4-(3-нитрофенил)-2-(2-тиенил)пиримидина (пример 14(b), 9,8 г) в смеси EtOH (80 мл) и DCM (80 мл) в атмосфере азота добавляли DIPEA (5,57 мл). Через 2 часа при комнатной температуре смесь разбавляли DCM до полного растворения, промывали 0,5 н. водным раствором HCl, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 12,9 г.
MS-ESI: [M+H]+=427,2.
ТСХ: Rf=0,7, силикагель, гептан/EtOAc=3/2 (об/об).
(d) Этил 5-амино-4-(3-нитрофенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксилат
К перемешиваемому раствору этил 5-циано-4-(3-нитрофенил)-2-(2-тиенил)-6-(этоксикарбонилметилтио)пиримидина (пример 14(с), 12,9 г) в смеси абсолютного EtOH (75 мл) и толуола р.а. (75 мл) добавляли DIPEA (13,0 мл). Через 48 часов при 100°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, промывали холодным EtOH и сушили в вакууме при 40°С.
Выход: 11,0 г.
MS-ESI: [M+H]+=427,2.
ТСХ: Rf=0,6, силикагель, гептан/EtOAc=3/2 (об/об).
(е) Этил 5-амино-4-(3-аминофенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксилат
К раствору этил 5-амино-4-(3-нитрофенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксилата (пример 14(d), 10,86 г) в 1,4-диоксане (150 мл) добавляли раствор хлорида олова (II) (15 г) в абсолютном EtOH (150 мл). Добавляли 37% водный раствор HCl (4,5 мл) и смесь кипятили с обратным холодильником в течение 16 часов. Смесь оставляли охлаждаться до комнатной температуры и концентрировали при пониженном давлении. Остаток суспендировали в EtOAc (400 мл) и добавляли ТГФ до полного растворения. Для достижения уровня рН 10-11 добавляли 4 н. водный раствор NaOH. Смесь разбавляли добавлением насыщенного водного раствора NaCl. Органический слой отделяли, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 12,0 г.
MS-ESI: [M+H]+=397,2.
ТСХ: Rf=0,4, силикагель, гептан/EtOAc=3/2 (об/об).
(f) 5-Амино-4-(3-нитрофенил)-2-(2-тиенил)тиено[2,3-d] пиримидин-6-карбоновая кислота
К раствору этил 5-амино-4-(3-аминофенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксилата (пример 14(е), 10,1 г) в смеси 1,4-диоксана (150 мл) и воды (50 мл) добавляли гидроксид калия (13 г). Через 16 часов при 90°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, суспендировали в воде (180 мл) и охлаждали до 0°С. Смесь подкисляли до рН 3, добавляя 2 н. водный раствор лимонной кислоты, и перемешивали при 0°С в течение 2 часов. Полученный осадок отфильтровывали, промывали водой и сушили в вакууме при 40°С.
Выход: 6,3 г.
MS-ESI: [M+H]+=369,2.
ТСХ: Rf=0,2, силикагель, DCM/MeOH=95/5 (об/об).
(g) трет-Бутил 5-амино-4-(3-нитрофенил)-2-(2-тиенил)тиено[2,3-d] пиримидин-6-карбоксамид
К смеси 5-амино-4-(3-нитрофенил)-2-(2-тиенил)-тиено[2,3-d] пиримидин-6-карбоновой кислоты (пример 14(f), 6,3 г) в смеси DCM (125 мл) и ДМФА (N,N-диметилформамид) (25 мл) в атмосфере азота добавляли DIPEA (7,1 мл), трет-бутиламин (4,3 мл) и TBTU (6,6 г). Через 3 часа при комнатной температуре смесь разбавляли DCM и промывали насыщенным водным раствором NaHCO3, 0,1 н. водным раствором HCl и насыщенным водным раствором NaCl. Органический слой сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали хроматографией на силикагеле, используя в качестве элюента гептан/EtOAc=3/7 до 1/1 (об/об).
Выход: 6,45 г.
MS-ESI: [M+H]+=424,2.
ТСХ: Rf=0,3, силикагель, гептан/EtOAc=3/2 (об/об).
(h) трет-Бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-нитрофенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 14(g), 5,0 г) и DIPEA (10,5 мл) в DCM (50 мл) добавляли бромацетилхлорид (2,40 мл). Через 3 часа при комнатной температуре смесь разбавляли DCM, промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали хроматографией на силикагеле, используя в качестве элюента гептан/EtOAc=3/2 (об/об). Получали смесь трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-тиенил)-тиено[2,3-d]пиримидин-6-карбоксамида и трет-бутил 5-амино-4-(3-(2-хлорацетамидо)фенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксамида.
Выход: 3,0 г.
MS-ESI: [M+H]+=546,2, [M,+H]+=500,2.
ТСХ: Rf=0,2, силикагель, толуол/EtOAc=7/1 (об/об).
(i) трет-Бутил 5-амино-2-(2-тиенил)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)-фенил)-2-(2-тиенил)-тиено[2,3-d]пиримидин-6-карбоксамида (пример 14(h), 100 мг) в DCM (5 мл) добавляли N-метил-2-аминоэтанол (140 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х10 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 59 мг (соль ТФУК).
MS-ESI: [M+H]+=539,2.
ВЭЖХ: Rt=11,01 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 15
трет-Бутил 5-амино-2-(2-тиенил)-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 14(h), 100 мг) и DIPEA (0,5 мл) в DCM (5 мл) добавляли гидрохлорид метилового эфира глицина (250 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х10 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 74 мг (соль ТФУК)
MS-ESI: [M+H]+=553,0
ВЭЖХ: Rt=12,57 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 16
трет-Бутил 5-амино-2-(2-тиенил)-4-(3-((N,N-ди-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(2-тиенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 14(h), 100 мг) в DCM (5 мл) добавляли N,N-д-(2-метоксиэтил)-амин (200 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (50 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х10 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 59 мг (соль ТФУК).
MS-ESI: [M+H]+=597,4.
ВЭЖХ: Rt=13,84 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 17
трет-Бутил 5-амино-2-этиламино-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) трет-Бутил 5-амино-2-метансульфинил-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метилтио-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 4, 1,0 г) в трифторуксусной кислоте (ТФУК, 25 мл) добавляли 3-хлорпербензойную кислоту (m-CPBA, 1,0 г). Через 17 часов реакционную смесь концентрировали при пониженном давлении при температуре окружающей среды (20°С), повторно растворяли в DCM (100 мл), осторожно промывали насыщенным водным раствором NaHCO3 (2х50 мл) и водой (50 мл), сушили (MgSO4) и концентрировали в вакууме. Неочищенный остаток использовали на следующей стадии без дополнительной очистки.
Выход: 820 мг.
MS-ESI: [M+H]+=547,3.
ТСХ: Rf=0,2, силикагель, DCM/MeOH=9/1 (об/об).
(b) трет-Бутил 5-амино-2-этиламино-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)-тиено[2,3-d]пиримидин-6-карбоксамида (пример 17(а), 100 мг) и DIPEA (0,5 мл) в 1,4-диоксане (5 мл) добавляли гидрохлорид этиламина (150 мг) и реакционную смесь нагревали до 60°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 36 мг (соль ТФУК).
MS-ESI: [M+H]+=528,4.
ВЭЖХ: Rt=10,21 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 18
трет-Бутил 5-амино-2-(N,N-диметиламино)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) трет-Бутил 5-амино-2-метансульфинил-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метилтио-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 1(i), 1,0 г) в трифторуксусной кислоте (ТФУК, 25 мл) добавляли 3-хорпербензойную кислоту (m-CPBA, 1,0 г). Через 17 часов реакционную смесь концентрировали при пониженном давлении при температуре окружающей среды (20°С), повторно растворяли в DCM (100 мл), осторожно промывали насыщенным водным раствором NaHCO3 (2х50 мл) и водой (50 мл), сушили (MgSO4) и концентрировали в вакууме. Неочищенный остаток использовали на следующей стадии без дополнительной очистки.
Выход: 910 мг.
MS-ESI: [M+H]+=519,6.
ТСХ: Rf=0,15, силикагель, DCM/MeOH=9/1 (об/об).
(b) трет-Бутил 5-амино-2-(N,N-диметиламино)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 18(а), 100 мг) и DIPEA (0,5 мл) в 1,4-диоксане (5 мл) добавляли гидрохлорид диметиламина (150 мг) и реакционную смесь нагревали до 60°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 36 мг (соль ТФУК).
MS-ESI: [M+H]+=500,2.
ВЭЖХ: Rt=10,03 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 19
трет-Бутил 5-амино-2-этиламино-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) трет-Бутил 5-амино-2-метансульфинил-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метилтио-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 3, 1,0 г) в трифторуксусной кислоте (ТФУК, 25 мл) добавляли 3-хлорпербензойную кислоту (m-CPBA, 1,0 г). Через 17 часов реакционную смесь концентрировали при пониженном давлении при температуре окружающей среды (20°С), повторно растворяли в DCM (100 мл), осторожно промывали насыщенным водным раствором NaHCO3 (2х50 мл) и водой (50 мл), сушили (MgSO4) и концентрировали в вакууме. Неочищенный остаток использовали на следующей стадии без дополнительной очистки.
Выход: 680 мг.
MS-ESI: [M+H]+=533,6.
ТСХ: Rf=0,17, силикагель, DCM/MeOH=9/1 (об/об).
(b) трет-Бутил 5-амино-2-этиламино-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 19(а), 100 мг) и DIPEA (0,5 мл) в 1,4-диоксане (5 мл) добавляли гидрохлорид этиламина (150 мг) и реакционную смесь нагревали до 60°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 57 мг (соль ТФУК).
MS-ESI: [M+H]+=514,2.
ВЭЖХ: Rt=12,56 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 20
трет-Бутил 5-амино-2-изопропиламино-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)-тиено[2,3-d]пиримидин-6-карбоксамида (пример 17(а), 100 мг) и DIPEA (0,5 мл) в 1,4-диоксане (5 мл) добавляли изопропиламин (150 мг) и реакционную смесь нагревали до 60°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 57 мг (соль ТФУК).
MS-ESI: [M+H]+=542,4.
ВЭЖХ: Rt=11,01 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 21
трет-Бутил 5-амино-2-аллиламино-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 19(а), 100 мг) и DIPEA (0,5 мл) в 1,4-диоксане (5 мл) добавляли аллиламин (200 мг) и реакционную смесь нагревали до 60°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 65 мг (соль ТФУК).
MS-ESI: [M+H]+=526,4.
ВЭЖХ: Rt=13,18 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 22
трет-Бутил 5-амино-2-метокси-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 17(а), 200 мг) в метаноле (5 мл) добавляли трет-бутоксид калия (100 мг) и реакционную смесь нагревали до 50°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали водным раствором хлорида аммония (1М, 25 мл), насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 92 мг (соль ТФУК).
MS-ESI: [M+H]+=515,4.
ВЭЖХ: Rt=12,21 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 23
трет-Бутил 5-амино-2-аллилокси-4-(3-((N-этил-N-(2-метоксиэтил)-глицинил)-амино)-фенил)-тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-этил-N-(2-метоксиэтил)-глицинил)-амино)-фенил)-тиено[2,3-d]пиримидин-6-карбоксамида (пример 17(а), 200 мг) в аллиловом спирте (5 мл) добавляли трет-бутоксид калия (100 мг) и реакционную смесь нагревали до 50°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали водным раствором хлорида аммония (1М, 25 мл), насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 63 мг (соль ТФУК).
MS-ESI: [M+H]+=541,4.
ВЭЖХ: Rt=12,71 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 24
трет-Бутил 5-амино-2-изопропокси-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-2-метансульфинил-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 17(а), 200 мг) в изопропаноле (5 мл) добавляли трет-бутоксид калия (100 мг) и реакционную смесь нагревали до 50°С в течение 3 часов. После концентрирования реакционной смеси при пониженном давлении остаток переносили в DCM (50 мл) и промывали водным раствором хлорида аммония (1М, 25 мл), насыщенным солевым раствором (1 М, 25 мл) и водой (25 мл). Затем органический слой сушили (MgSO4) и концентрировали в вакууме. Полученный таким образом остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 32 мг (соль ТФУК).
MS-ESI: [M+H]+=543,4.
ВЭЖХ: Rt=12,93 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 25
трет-Бутил 5-амино-2-(4-пиридил)-4-(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
(а) 5-Циано-4-(3-нитрофенил)-2-(4-пиридил)-6-гидроксипиримидин
Смесь гидрохлорида 4-амидинопиридина (16,5 г), 3 нитробензальдегида (15,1 г), этилцианоацетата (11,2 мл) и карбоната калия (16,6 г) в абсолютном EtOH (250 мл) перемешивали при 60°С в течение 16 часов. Реакционную смесь охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали, промывали абсолютным EtOH и нагревали в воде (100°С) до получения прозрачного раствора. Раствор охлаждали до 50°С, подкисляли до рН 2, добавляя 2 н. водный раствор HCl, и охлаждали до 0°С в бане со льдом. Полученный осадок отфильтровывали и промывали ледяной водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном.
Выход: 18,3 г.
MS-ESI: [M+H]+=320,2.
ТСХ: Rf=0,2, силикагель, DCM/MeOH=9/1 (об/об).
(b) 6-Хлор-5-циано-4-(3-нитрофенил)-2-(4-пиридил)пиримидин
К перемешиваемому раствору 5-циано-4-(3-нитрофенил)-2-(4-пиридил)-6-гидроксипиримидина (пример 25(а), 18,3 г) и диметиланилина (0,5 мл) в сухом 1,4-диоксане р.а. (200 мл) добавляли POCl3 (50 мл). Через 3 часа при 90°С смесь отфильтровывали и фильтрат концентрировали при пониженном давлении. Остаток растворяли в 1,4-диоксане и добавляли ледяную воду. Полученный осадок отфильтровывали и промывали водой. Оставшуюся воду удаляли совместным выпариванием с 1,4-диоксаном. Выход: 17,2 г.
MS-ESI: [M+H]+=338,4.
ТСХ: Rf=0,7, силикагель, гептан/EtOAc=3/2 (об/об).
(с) Этил 5-циано-4-(3-нитрофенил)-2-(4-пиридил)-6-(этоксикарбонилметилтио)пиримидин
К перемешиваемому раствору 6-хлор-5-циано-4-(3-нитрофенил)-2-(4-пиридил)пиримидина (пример 25(b), 17,2 г) в смеси EtOH (125 мл) и DCM (125 мл) в атмосфере азота добавляли DIPEA (9,8 мл). Через 2 часа при комнатной температуре смесь разбавляли DCM до полного растворения, промывали 0,5 н. водным раствором HCl, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 20,5 г.
MS-ESI: [M+H]+=422,0.
ТСХ: Rf=0,6, силикагель, гептан/EtOAc=3/2 (об/об).
(d) Этил 5-амино-4-(3-нитрофенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксилат
К перемешиваемому раствору этил 5-циано-4-(3-нитрофенил)-2-(4-пиридил)-6-(этоксикарбонилметилтио)пиримидина (пример 25(с), 20,5 г) в смеси абсолютного EtOH (100 мл) и толуола р.а. (100 мл) добавляли DIPEA (20,0 мл). Через 48 часов при 100°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, промывали холодным EtOH и сушили в вакууме при 40°С.
Выход: 15,7 г.
MS-ESI: [M+H]+=422,2.
ТСХ: Rf=0,5, силикагель, гептан/EtOAc=3/2 (об/об).
(е) Этил 5-амино-4-(3-аминофенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксилат
К раствору этил 5-амино-4-(3-нитрофенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксилата (пример 25(d), 15,7 г) в 1,4-диоксане р.а. (250 мл) добавляли раствор хлорида олова (II) (21,0 г) в абсолютном EtOH (250 мл). Добавляли 37% водный раствор HCl (6,9 мл) и смесь кипятили с обратным холодильником (90°С) в течение 16 часов. Смесь оставляли охлаждаться до комнатной температуры и концентрировали при пониженном давлении. Остаток суспендировали в EtOAc (500 мл). Для достижения уровня рН 10-11 добавляли 4 н. водный раствор NaOH. Смесь разбавляли добавлением насыщенного водного раствора NaCl. Органический слой отделяли, сушили (MgSO4) и концентрировали при пониженном давлении.
Выход: 12,0 г.
MS-ESI: [M+H]+=392,2.
ТСХ: Rf=0,3, силикагель, гептан/EtOAc=3/2 (об/об).
(f) 5-Амино-4-(3-нитрофенил)-2-(4-пиридил)тиено[2,3-d] пиримидин-6-карбоновая кислота
К раствору этил 5-амино-4-(3-аминофенил)-2-(4-пиридил)-тиено[2,3-d]пиримидин-6-карбоксилата (пример 25(е), 12,0 г) в смеси 1,4-диоксана (210 мл) и воды (80 мл) добавляли гидроксид калия (15,7 г). Через 16 часов при 90°С смесь охлаждали до 0°С. Полученный осадок отфильтровывали, суспендировали в воде (300 мл) и охлаждали до 0°С. Смесь подкисляли до рН 3, добавляя 2 н. водный раствор лимонной кислоты, и перемешивали при 0°С до комнатной температуры в течение 2 часов. Полученный осадок отфильтровывали, промывали водой и сушили в вакууме при 40°С.
Выход: 12,0 г.
MS-ESI: [M+H]+=364,2.
ТСХ: Rf=0,1, силикагель, DCM/MeOH=95/5 (об/об).
(g) трет-Бутил 5-амино-4-(3-аминофенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксамид
К смеси 5-амино-4-(3-аминофенил)-2-(4-пиридил)тиено[2,3-d] пиримидин-6-карбоновой кислоты (пример 25(f), 12,0 г) в смеси DCM (250 мл) и ДМФА (50 мл) в атмосфере азота добавляли DIPEA (12,9 мл), трет-бутиламин (7,8 мл) и TBTU (11,9 г). Через 2 часа при комнатной температуре смесь разбавляли DCM и промывали насыщенным водным раствором NaHCO3, 0,1 н. водным раствором HCl и насыщенным водным раствором NaCl. Органический слой сушили (MgSO4) и концентрировали при пониженном давлении. Неочищенный продукт очищали хроматографией на силикагеле, используя в качестве элюента дихлорметан/метанол=1/0 до 95/5 (об/об).
Выход: 12,2 г.
MS-ESI: [M+H]+=419,4.
ТСХ: Rf=0,3, силикагель, гептан/EtOAc=3/2 (об/об).
(h) трет-Бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксамид
К раствору трет-бутил 5-амино-4-(3-нитрофенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 25(g), 2,0 г) и N,N-диметиланилина (3,0 мл) в ТГФ (50 мл) добавляли по каплям раствор бромацетилбромида (0,59 мл) в ТГФ (25 мл). Через 30 мин при комнатной температуре смесь концентрировали при пониженном давлении, затем растворяли в DCM (100 мл), промывали насыщенным водным раствором NaHCO3, сушили (MgSO4) и концентрировали в вакууме. Остаток использовали на следующей стадии без дополнительной очистки.
Выход: 2,3 г.
MS-ESI: [M+H]+=539,2.
ТСХ: Rf=0,3, силикагель, гептан/EtOAc=3/2 (об/об).
(i) трет-Бутил 5-амино-2-(4-пиридил)-4-(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)-фенил)-2-(4-пиридил)-тиено[2,3-d]пиримидин-6-карбоксамида (пример 25(h), 200 мг) в DCM (5 мл) добавляли 2-амино-2-метилпропанол (300 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (100 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х50 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 73 мг (соль ТФУК).
MS-ESI: [M+H]+=548,2.
ВЭЖХ: Rt=9,65 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 26
трет-Бутил 5-амино-2-(4-пиридил)-4-(3-((N,N-бис-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
К перемешиваемому раствору трет-бутил 5-амино-4-(3-(2-бромацетамидо)фенил)-2-(4-пиридил)тиено[2,3-d]пиримидин-6-карбоксамида (пример 25(h), 200 мг) в DCM (5 мл) добавляли бис-(2-метоксиэтил)амин (300 мг). После перемешивания в течение 17 часов при комнатной температуре реакционную смесь разбавляли DCM (100 мл), промывали насыщенным водным раствором NaHCO3 (1 М, 2х50 мл), сушили (MgSO4) и концентрировали в вакууме. Остаток очищали при помощи ВЭЖХ, используя колонку Luna C-18 со следующим градиентом: 0,1% водный ТФУК + 10% водный ACN/ACN=от 90/10 до 10/90 (об/об) за 30 мин. Указанное в заголовке соединение затем лиофилизовали из смеси 1,4-диоксана, 0,1% водный ТФУК и воды.
Выход: 170 мг (соль ТФУК).
MS-ESI: [M+H]+=592,2.
ВЭЖХ: Rt=12,02 мин, колонка Luna C-18(2), 3 мкм, 100х2,0 мм, УФ детекция=210 нм, температура печи=40°С, поток=0,25 мл/мин, элюент: фосфатный буфер 50 мМ рН 2,1/вода/ACN=от 10/80/10 до 10/10/80 (об/об/об), время цикла=20 мин.
Пример 27
CHO-LH и CHO-FSH биоактивность in vitro
Активность соединений в качестве агонистов LH испытывали на клетках яичника китайского хомячка (Chinese Hamster Ovary (CHO)), стабильно транфицированных рецептором LH человека и котранфицированных элементом (CRE), являющимся чувствительным к cAMP/промотором, направляющим экспрессию репортерного гена люциферазы светлячка. Связывание лиганда с Gs-соединенным рецептором LH приводит в результате к повышению сАМР, что, в свою очередь, индуцирует повышенную трансактивацию люциферазной репортерной конструкции. Количественное определение сигнала люциферазы осуществляли с использованием счетчика люминесценции. Для испытываемых соединений вычисляли значения ЕС50 (концентрация тестируемого соединения, вызывающая полумаксимальную (50%) стимуляцию). Для этой цели использовали программу GraphPad PRISM, версия 3.0 (GraphPad software Inc., San Diego).
Аналогичным способом активность соединений в качестве агонистов FSH испытывали на клетках СНО, транфицированных репортерным геном люциферазы и рецептором FSH человека. Результаты представлены в таблице 1.
Биоактивность in vivo
Для измерения in vivo активности соединений, являющихся агонистами рецептора LH/FSH, исследовали индукцию овуляции у незрелых мышей. В этом анализе незрелую самку мыши примировали выделенным из мочи FSH (Humegon 12,5 IU/животное). Приблизительно через 48 часов животных обрабатывали соединениями-агонистами LH/FSH, получение которых описано в примерах 1, 4, 9 и 17, с дозой 50 мг/кг. Животных умерщвляли спустя 24 часа после обработки LH/FSH агонистом и под микроскопом подсчитывали число зародышевых клеток в маточной трубе. В среднем было исследовано 10-15 животных. Среднее число подсчитанных зародышевых клеток составляло 8, за исключением соединения примера 17 (где это количество составило 0,4).
мер
(3-((N-метил-N-(2-гидроксиэтил)-
глицинил)амино)фенил)тиено[2,3-d]-
пиримидин-6-карбоксамид
(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N-этил-N-(2-метоксиэтил)-
глицинил)амино)фенил)тиено[2,3-d]-
пиримидин-6-карбоксамид
(3-((N-(R-1-метоксикарбонил-2-
метилпроп-1-ил)глицинил)амино)-
фенил)тиено[2,3-d]пиримидин-6-
карбоксамид
(3-((N,N-бис-(2-метоксиэтил)глицинил)-
амино)фенил)тиено[2,3-d]-
пиримидин-6-карбоксамид
(3-((2,3-дигидроксипроп-1-ил)глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
(3-((1,3-дигидроксипроп-2-ил)глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
(3-((N-этил-N-(2-гидроксиэтил)-
глицинил)амино)фенил)тиено[2,3-d]-
пиримидин-6-карбоксамид
(3-(N-(метоксикарбонилметил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
-4-(3-((N-метил-N-(2-гидроксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-(N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-(N-(метоксикарбонилметил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N-метил-N-(2-гидроксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N-(метоксикарбонилметил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N,N-ди-(2-метоксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N-этил-N-(2-метоксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
диметиламино)-4-(3-((N-метил-
N-(2-гидроксиэтил)глицинил)-
амино)фенил)тиено[2,3-d]-
пиримидин-6-карбоксамид
-4-(3-((N-(метоксикарбонилметил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
N-(2-метоксиэтил)глицинил)-
амино)фенил)тиено[2,3-d]-
пиримидин-6-карбоксамид
4-(3-((N-(метоксикарбонилметил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N-этил-N-(2-метоксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
4-(3-((N-этил-N-(2-метоксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
-4-(3-((N-этил-N-(2-метоксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
-4-(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)-
тиено[2,3-d]пиримидин-6-карбоксамид
-4-(3-((N,N-бис-(2-метоксиэтил)-
глицинил)амино)фенил)тиено-
[2,3-d]пиримидин-6-карбоксамид
| название | год | авторы | номер документа |
|---|---|---|---|
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОАРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРИМЕНЕНИЕ | 2001 |
|
RU2271360C2 |
| ПРОИЗВОДНЫЕ ТИЕНО[2,3-D]ПИРИМИДИНА И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ ФЕРТИЛЬНОСТИ | 2002 |
|
RU2298011C2 |
| ЗАМЕЩЕННЫЕ ПИРРОЛЫ, АКТИВНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2013 |
|
RU2666538C2 |
| НОВЫЕ МОДУЛЯТОРЫ РЕЦЕПТОРА GLP-1 | 2012 |
|
RU2634896C2 |
| ИНГИБИТОРЫ FGFR4 | 2014 |
|
RU2715708C2 |
| ПЕРВИЧНЫЕ КАРБОКСАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ BТK | 2014 |
|
RU2708395C2 |
| ЗАМЕЩЕННЫЕ НИКОТИНИМИДНЫЕ ИНГИБИТОРЫ ВТК, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В ТЕРАПИИ РАКОВЫХ, ВОСПАЛИТЕЛЬНЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2677884C2 |
| ИНГИБИРУЮЩИЕ JAK СОЕДИНЕНИЯ НА ОСНОВЕ ПИРАЗОЛОПИРИМИДИНА И СПОСОБЫ | 2010 |
|
RU2675857C2 |
| НОВЫЕ ЗАМЕЩЕННЫЕ БИАРИЛОВЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ИНДОЛАМИН-2,3-ДИОКСИГЕНАЗЫ (IDO) | 2018 |
|
RU2786586C2 |
| НЕКОТОРЫЕ ИНГИБИТОРЫ ПРОТЕИНКИНАЗЫ | 2015 |
|
RU2671494C2 |
Описываются глицин-замещенные тиено [2,3-D]пиримидины формулы I:

где Х представляет собой О или Н,Н; А представляет собой S, NH, N(R6), О или связь; R1 представляет собой (1-4С)алкил, (2-4С)алкенил, незамещенный фенил или незамещенный фурил, тиенил, пиридил; R2 представляет собой Н, (1-4С)алкил, (1-4С)алкокси(2-4С)алкил или гидрокси(2-4С)алкил; R3 и R4 независимо выбирают из Н, (1-4С)алкила и гидрокси(1-4С)алкила; R5 представляет собой Н или (1-4С)алкил, и R6 представляет собой (1-4С)алкил. Соединения обладают агонистической активностью в отношении гликопротеинового гормона, в частности обладают агонистической активностью в отношении лютеинизирующего гормона (LH) и фолликулостимулирующего гормона (FSH). Изобретение также описывает фармацевтические композиции, содержащие такие соединения, и использование этих соединений в лекарственной терапии, в частности для контроля оплодотворения. 5 н. и 6 з.п. ф-лы, 1 табл.

или его фармацевтически приемлемая соль,
где Х представляет собой О или Н,Н;
А представляет собой S, NH, N(R6), О или связь;
R1 представляет собой (1-4С)алкил, (2-4С)алкенил, незамещенный фенил или незамещенный фурил, тиенил, пиридил;
R2 представляет собой Н, (1-4С)алкил, (1-4С)алкокси(2-4С)алкил или гидрокси(2-4С)алкил;
R3 и R4 независимо выбирают из Н, (1-4С)алкила и гидрокси(1-4С)алкила;
R5 представляет собой Н или (1-4С)алкил и
R6 представляет собой (1-4С)алкил.
трет-бутил 5-амино-2-метилтио-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил}тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((N-(R-1-метоксикарбонил-2-метилпроп-1-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((N,N-бис-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((2,3-дигидроксипроп-1-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метилтио-4-(3-((1,3-дигидроксипроп-2-ил)глицинил)амино)фенил-тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-фенил-4-(3-((N-этил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-фенил-4-(3-(N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(2-фурил)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(2-фурил)-4-(3-(N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(2-фурил)-4-(3-(N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(2-тиенил)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(2-тиенил)-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(2-тиенил)-4-(3-((N,N-ди-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-этиламино-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(N,N-диметиламино)-4-(3-((N-метил-N-(2-гидроксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-этиламино-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-изопропиламино-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-аллиламино-4-(3-((N-(метоксикарбонилметил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-метокси-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-аллилокси-4-(3-((N-этил-N-(2-метоксиэтил)-глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-изопропокси-4-(3-((N-этил-N-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(4-пиридил)-4-(3-((N-(1-гидрокси-2-метилпроп-2-ил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид;
трет-бутил 5-амино-2-(4-пиридил)-4-(3-((N,N-бис-(2-метоксиэтил)глицинил)амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид,
или его фармацевтически приемлемые соли.
| Устройство для смазки шатунных подшипников | 1941 |
|
SU61586A1 |
| RU 99104796 A, 20.01.2001. | |||
Авторы
Даты
2007-02-27—Публикация
2002-08-29—Подача