Изобретение относится к поиску новых штаммов - продуцентов биологически активных веществ, перспективных для микробиологической промышленности и генной инженерии, и касается получения нового штамма, продуцирующего сайт-специфическую эндонуклеазу, способную узнавать и расщеплять последовательность нуклеотидов 5'- ATGCA^T-3'.
Сайт-специфические эндонуклеазы являются важнейшим инструментом работы в генной инженерии. В связи с этим поиск новых ферментов продолжает быть актуальным и в настоящее время. Интерес представляет поиск продуцентов, обладающих более высокой продукцией фермента, а также ферментов со свойствами, выгодно отличающими их от используемых в настоящее время аналогов.
Известен штамм Anabaena variabilis, продуцирующий фермент эндонуклеазу рестрикции AvaIII, являющийся изошизомером заявляемой, был впервые выделен в 1979 г. [1], однако в настоящее время коммерческим препаратом не является из-за низкой активности.
Известны штамм Bacteroides fragilisBE3, продуцирующий фермент BfrBI [2]; штамм Moraxella phenylpyruvica RFL1103, продуцирующий фермент Mph1103I, штамм Neisseria sicca, продуцирующий фермент NsiI, штамм Phormidium inundatum, продуцирующий фермент PinBI [3], штамм Staphylococcus species D5, продуцирующий фермент SspD5II [4]. Zooglea species2, продуцирующий эндонуклеазу рестрикции Zsp2I [5].
Все штаммы продуцируют эндонуклеазы, аналогичные по сайту узнавания и расщепления заявляемой. Данные по активности для большинства из них не представлены в литературе.
Штаммы рода Staphylococcus или Neisseria относятся к патогенным микроорганизмам и могут представлять опасность при работе с ними. Наиболее близким к заявляемому штамму является штамм Staphylococcus species D5, продуцирующий фермент SspD5II [4]. Staphylococcus species D5 (прототип) содержит две эндонуклеазы, а наличие нескольких эндонуклеаз рестрикции всегда затрудняет процесс выделения чистого препарата фермента и дает очень низкий выход (SspD5II получают 8000 единиц фермента с 1 г биомассы).
Технической задачей изобретения является получение непатогенного штамма, способного расти на простых питательных средах, продуцирующего эндонуклеазу рестрикции, узнающую и расщепляющую нуклеотидную последовательность 5'-ATGCAT-3', с высоким выходом фермента, стабильного при хранении и способного проявлять активность при низкотемпературных условиях реакции.
Поставленная техническая задача решается выявлением и использованием штамма-продуцента сайт-специфической эндонуклеазы рестрикции Asi372I.
Штамм Arthrobacter species 372, выделенный в процессе анализа образцов почвы, является продуцентом эндонуклеазы рестрикции, названной Asi372I, согласно общепринятой номенклатуре [6]. Штамм культивируется при температуре 20-30°С и является продуцентом эндонуклеазы, обладающей высокой активностью при температуре 20-30°С. Согласно классификации Бердже этот род был описан еще в 1947 г. [7], однако по сравнению с представителями других родов, эндонуклеаз рестрикции II типа для этого рода обнаружено очень мало [6].
Штамм хорошо растет на простых питательных средах и не относится к патогенным штаммам.
В штаммах рода Arthrobacter эндонуклеаза рестрикции с такой специфичностью выделена впервые.
Данный штамм содержит только одну рестриктазу, что является его преимуществом. Выход биомассы составляет 5,5±0,5 г/л L-бульона. А содержание фермента - 40000 единиц активности Е/1 г биомассы.
Эндонуклеаза рестрикции данной специфичности используется для исследования в молекулярной биологии, физического картирования различных геномов.
Идентификацию штамма проводят общепринятыми методами [7-9].
Штамм обладает следующими свойствами:
Морфология клеток: грамположительные палочки (коккобациллы) одиночные и пары, подвижные, 0,9-1,3×1,5-2,5 цитоплазма зернистая, спор нет. Ферментируют глюкозу, лактозу и сахарозу.
Морфология колоний: округлые, гладкие, плоские с точкой роста, полупрозрачные, желтоватые, с ровным краем, однородные.
Культуральные свойства: Штамм аэроб, желатин гидролизует. Кислота из углеводов в результате их окисления не образуется, газ не выделяет, каталазоположителен.
Растет на среде РПА с 1%-ной глюкозой и дрожжевым экстрактом и МПА с 1,5-ным дрожжевым экстрактом.
Оптимальная температура - 20-3 0°С. Оптимальная рН для роста: 6,0-8,0. Штамм растет от 5 до 40°С. Слабый рост наблюдается при рН 5,5 и 8,5. На средах: МПА с 1,5М Nad, МПА с Brein Heart 1% (Difco, США), Плоскирева и Левина роста нет.
Основываясь на полученных данных, выделенный нами штамм относится к роду Arthrobacter и назван как Arthrobacter species Mn 372.
Штамм Arthrobacter sp.Mn372 депонирован в НИИ ККМ ФГУП (НИИ культур клеток федерального унитарного предприятия) Государственного Научного Центра вирусологии и биотехнологии "Вектор" под регистрационным номером В-1058, а продуцируемая им эндонуклеаза рестрикции названа Asi372I.
Штамм хранится в питательной среде с глицерином.
Для культивирования Arthrobacter sp.Mn372 применяют среду следующего состава (г/л): пептон - 10.0, дрожжевой экстракт - 5.0, NaCl-5.0, рН 7.0-7.2. Штамм растет также на минимальной среде, содержащей дрожжевой экстракт.
Для получения препарата фермента штамм выращивают в пол-литровых колбах в качалке при 200 об/мин и температуре 6-27°С в течение 24-48 час (в зависимости от температуры). Клетки осаждают центрифугированием при 5000 об/мин и температуре 4-5°С. Выделение проводят путем хроматографической очистки на фосфоцеллюлозе Р-11("Whatman", Англия). Все операции по выделению Asi372I. проводят при температуре 4-5°С. Клетки суспендируют в буфере А (10 мМ калий фосфатный буфер рН 7.5, 7 мМ β-меркаптоэтанол, 0.1 мМ ЭДТА) из расчета 4 мл на 1 г биомассы и разрушают ультразвуком на дезинтеграторе ("MSE", Англия), затем осветляют центрифугированием на центрифуге J-21B ("Bekman", США) со скоростью 18000 об/мин в течение 30 мин. Экстракт наносят на колонку (1.6×14 см) фосфоцеллюлозы Р-11 ("Whatman", Англия), промывают буфером А и смывают фермент в градиенте концентрации NaCI (0.1 -0.8 М). Фракции, содержащие эндонуклеазу рестрикции диализуют против буфера В (10 мМ трис-HCI рН 7,5, 1 мМ β-меркаптоэтанол, 0.1 мМ ЭДТА. Фракции с ферментом диализуют против 50%-ного раствора глицерина в буфере А.
Для электрофореза используют агарозу фирмы ("Sigma", США). Рестрикционный анализ проводят в 20 мкл реакционной смеси, содержащей 10 мМ трис рН 7.5, 10 мМ MgCI2, 10 мМ NaCI, 1 мМ дитиотреитол (ДТТ) и 1 мкг ДНК λсI857 при температуре 25-30°С.
Выход фермента из 1 г клеток составляет 40000 ед. акт (Е). За единицу активности принимают минимальное количество фермента, которое в течение 1 ч при температуре 30°С в оптимальных условиях полностью гидролизует 1 мкг ДНК фага λсI857.
Штамм является уникальным не только по наличию данной эндонуклеазы рестрикции, но и имеет дополнительные свойства. Клетки штамма способны расти при диапазоне температуры 6-37°С, а фермент гидролизует ДНК фага лямбда и Т7 с наибольшей активностью при температуре 20-37°С. Фермент также гидролизует ДНК при более низких температурах (6-20°С). Инактивация фермента происходит уже через 2 мин прогревания при температуре 50°С.
Определяющим отличием предлагаемого штамма от штамма-прототипа является:
штамм относится к роду Arthrobacter;
широкий температурный оптимум роста штамма;
рост на простых питательных средах с добавлением дрожжевого экстракта;
наличие эндонуклеазы рестрикции Asi372I;
активность фермента 40000 Е/г сырой биомассы.
Для определения узнаваемой последовательности нуклеотидов эндонуклеазой рестрикции Asi372I проводят сравнение экспериментально полученных путем электрофореза в 1%-ном агарозном геле фрагментов, образующихся при гидролизе ДНК фага λcI857dam-dcm- с контрольными. Результаты сравнительного анализа позволяют сделать вывод, что данная эндонуклеаза узнает последовательность нуклеотидов (5'-ATGCAT-3').
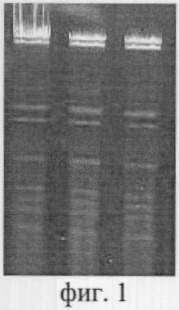
На фиг.1 представлена электрофореграмма продуктов гидролиза ДНК фага λcI857dam-dcm- ферментом Asi372I, Asi372I и Zsp2I, Zsp2I (сайт узнавания 5'-ATGCAT-3'). Как видно из представленной фигуры, идентичность полос расщепления при параллельном и совместном гидролизе подтверждает их изошизомерию. Фермент гидролизует не только dam-ДНК, но и dam+ДНК.
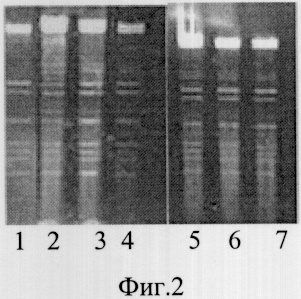
На фигуре 2 представлена картина гидролиза ДНК фага λdam+ и dam- эндонуклеазой рестрикции Asi372I и контрольные фрагменты, полученные после добавления в реакционную смесь с ДНК фермента Zsp2I.
Таким образом, метилирование ДНК метилазой dam не влияет.на работу полученного фермента.
Интерпретация полученных экспериментальных данных позволяет утверждать, что исследуемая эндонуклеаза рестрикции является изошизомером рестриктазы Zsp2I.
Таким образом, впервые выделена высокоактивная эндонуклеаза рестрикции, узнающая и расщепляющая последовательность нуклеотидов 5'-ATGCAT-3', из штамма, относящегося к роду Arthrobacter, имеющая оптимальную температуру рестрикции 20-30°С, работа которой не зависит от dam метилирования.
Поскольку предлагаемый штамм получен впервые и никогда не использовался, можно сделать вывод о соответствии предлагаемого штамма критериям изобретения "новизна" и "изобретательский уровень".
Описание фигур
Фиг.1. Электрофореграмма продуктов гидролиза ДНК фага λcI857dam- ферментом Аsi3721(дор.1), Asi372I и Zsp2I (дор.2), Zsp2I (дор.3), (сайт узнавания 5'- ATGCAT-3')
Фиг.2. Картина гидролиза ДНК фага λdam+ (дорожки 2-4) и dam-(дорожки 5-7) эндонуклеазой рестрикции Asi372I и контрольные фрагменты (1), полученные после добавления в реакционную смесь с ДНК фермента Zsp2I.
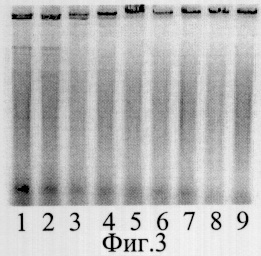
Фиг.3. Электрофореграмма продуктов гидролиза Asi372I+λCI857 после прогревания фермента.
Изобретение иллюстрируется следующими примерами конкретного выполнения.
Пример 1. Культивирование штамма. Клетки штамма-продуцента пересевают бактериологической петлей на агаризованную среду с дрожжевым экстрактом. Косяки помещают в термостат при температуре 27±2°С. После 18 ч инкубации подросшие клетки пересевают в колбы со свежей питательной средой.
Культивирование проводят на качалке при 22±2°С с аэрацией, при перемешивании - 200 об/мин 24 ч. Клетки собирают центрифугированием на центрифуге J-21 при 5000 об/мин и температуре 4-5°С. Урожай биомассы составляет 5 г/л среды.
Дезинтеграцию, выделение и очистку проводят по описанной выше методике. Содержание фермента в биомассе составляет 40000Е/г.
Пример 3. Определение специфичности и активности фермента.
Специфичность фермента определяют по картине параллельного и совместного гидролиза ДНК фага лямбда (фиг.1). Идентичность картин гидролиза на 1-3 дорожках говорит о том, что эти ферменты узнают и расщепляют одинаковую последовательность нуклеотидов 5'-ATGCAT-3'.
Пример 4. Определение термочувствительности фермента. Фермент прогревают при температуре 50°С: 0, 2, 4, 6, 8, 10, 12, 15, 30 мин. Результаты представлены на фиг.3.
Инактивация фермента происходит уже через 2 мин после начала прогревания. Следовательно фермент чувствителен к высокой температуре.
СПИСОК ЛИТЕРАТУРЫ
1. Roizes G., Nardeux P.C., Monier R. A new specific endonuclease from Anabaena variabilis], FEBS Lett. 104: 39-44 (1979).
2. Azeddoug, H., Reysset, G., Sebald, M. Characterization of restriction endonuclease BfrBI from Bacteroides fragilis strains ВЕЗ and AIP 10006. FEMS Microbiol. Lett. 95: 133-136 (1992).
3. Piechula S., Valeron K., SwiatecW., Biedrzycka I., Podhajska A.J. Mesophilic cyanobacteria producing thermophilic restriction endonucleases., BfrCI Bacteroides fragilis AIPI0006 FEMS Microbiol. Lett. 198: 135-140 (2001).
4. Shiryaev S.A., Zheleznyakova E.N., Matvienko N.N., Zheleznaya L.A., Matvienko N.I. Two new site-specific endonucleases from Staphylococcus species strain D5.Biokhimiia 65: 553-561 (2000).
5. Catalog. New England BioLabs., 2003. NEB Inc. USA. (Каталог Сибэнзим. Продукты для молекулярно-биологических исследований. 2004).
6. Roberts R.J., Belfort M., Bestor Т., Bhagwat A.S., Bickle T.A., Bitinaite J.,// Nucleic Acids Res. - 2003. - V.31. - P.1805-1812.
7. Определитель бактерий Берджи. В 2-х т. Т. 1: Пер. с англ./ Под ред. Дж.Хоулта, Н.Крига, П.Снита, Дж.Стейли, С.Уилльямса - М.: Мир, 1997. - 432 с.
8. Методы общей бактериологии: Пер. с англ./ Под ред. Ф.Герхардта и др. - М.: Мир, 1984. - 264 с.
9. А.С.Лабинская Микробиология с техникой микробиологических исследований - М.: Медицина, 1972. - 479 с.
Изобретение относится к области микробиологии и может быть использовано в микробиологической промышленности и в генной инженерии. Штамм Arthrobacter species Mn372 является продуцентом эндонуклеазы рестрикции Asi372I, являющейся изошизомером эндонуклеазы рестрикции Ava III. Применение изобретения позволяет по упрощенной технологии получить эндонуклеазу рестрикции, узнающую и расщепляющую последовательность нуклеотидов между 5'-ATGCA' и Т-3' концами. 3 ил.
Штамм бактерии Arthrobacter sp.Mn372, депонированный в НИИ коллекции культур микроорганизмов Федерального государственного унитарного предприятия ГНЦ ВБ «Вектор» под №В-1058, - продуцент эндонуклеазы рестрикции Asi372I, узнающей и расщепляющей последовательность нуклеотидов между 5'-ATGCA' и Т-3' концами и являющейся изошизомером эндонуклеазы рестрикции Ava III.
| SHIRYAEV SA, ZHELEZNYAKOVA EN, MATVIENKO NN, ZHELEZNAYA LA, MATVIENKO NI, Two new site-specific endonucleases from Staphylococcus species strain D5, Biochemistry (Mosc) | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2007-07-10—Публикация
2005-09-22—Подача