Изобретение относится к синтезу новых биологически активных химических соединений, конкретно к β-гидроксиникотиноилгидразону 2-метил-3-гидрокси-4-формил-5-оксиметилпиридина дигидрохлорида общей формулы I:
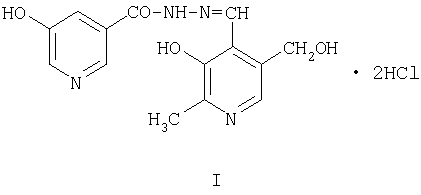
который обладает антиоксидантным, гепатопротекторным и иммуномодулирующим действием и может найти применение в медицине.
Прототипом по действию и соединением родственным по химической структуре, является широко применяемый в медицине антиоксидант - мексидол.
Задачей изобретения является создание более эффективного антиоксиданта, проявляющего дополнительно иммуномодулирующую и гепатопротекторную активность.
Поставленная задача достигается новой химической структурой формулы I, получаемой при взаимодействии гидразида 5-гидроксиникотиновой кислоты с 2-метил-3-гидрокси-4-формил-5-оксиметилпиридином гидрохлоридом в присутствии растворителя и соляной кислоты при нагревании. Выход целевого продукта составил 93,3% от теоретического. Соединение I - светло-желтое кристаллическое вещество, растворимое в воде, мало растворимое в ДМСО и других органических растворителях.
Т. пл. (с разложением) 216-217°С. Найдено, %: С 45,00; Н 4,26; N 14,65; Cl 18,75: C14H16N4O4Cl2. Вычислено, %: С 44,80; Н 4,26; N 14,91; Cl 18,92; ИК-спектр, см-1: 3370, 3310, 1680, 1610, 1550, 1310, 1150, 1050, 830. УФ-спектр, нм: 300,338 (в этаноле). Пример. β-Гидроксиникотиноилгидразон 2-метил-3-гидрокси-4-формил-5-оксиметилпиридина дигидрохлорид (I).
К раствору 3,06 г (0,02 моль) гидразида 5-гидроксиникотиновой кислоты в 450 мл воды при 35-40°С добавляют 3,3 мл соляной кислоты, раствор 4,07 г (0,02 моль) 2-метил-3-гидрокси-4-формил-5-оксиметилпиридина гидрохлорида в 19 мл воды и перемешивают при 55-60°С в течение 1 часа. Реакционную массу упаривают в вакууме при 75-80°С и Рост.=20 мм рт.ст., досушивают при 100°С, получают 7,0 г соединения I (93,3%).
Острую токсичность исследуемого соединения I и препарата сравнения - мексидола изучали в опытах на мышах массой 18-22 г с определением ЛД50 по методу Литчфилда и Уилкоксона. Соединения вводили внутрибрюшинно. ЛД50 соединения I составляет 700 мг/кг, мексидола - 800 мг/кг.
Было изучено влияние соединения I и мексидола на антиоксидантную, гепатопротекторную и иммунологическую реактивность крыс, индуцированную эритроцитами барана (ЭБ), в норме, а также в условиях повышенной и пониженной иммунной реактивности. Проведены следующие серии экспериментов:
1 серия экспериментов - на здоровых животных;
2 серия экспериментов - в условиях острого токсического поражения печени;
3 серия экспериментов - в условиях экспериментального острого панкреатита.
Исследования проведены на крысах Вистар массой 120-180 г. В первой серии экспериментов соединение I и мексидол вводили пятикратно (интервал 24 ч), внутрибрюшинно. Развитие гуморального иммунного ответа (ГИО) и гиперчувствительности замедленного типа (ГЗТ) индуцировали внутрибрюшинным введением ЭБ (однократно в дозе 108 кл/кг). Для оценки выраженности ГИО в селезенке определяли количество антителообразующих клеток (АОК) (Мальберг К., Зигль Э., 1987) и число иммунных розеткообразующих клеток (РОК) (Зауэр X., 1987) через 5 суток после внутрибрюшинной иммунизации (2×109 ЭБ). При оценке выраженности ГЗТ, через 4 суток после внутрибрюшинной сенсибилизации ЭБ (10 клеток), в подушечку задней конечности вводили разрешающую дозу антигена (106 ЭБ). Спустя 24 ч определяли разницу массы (РМЛ) и количества кариоцитов (РКЛ) в регионарном и контралатеральном лимфатических узлах (Федосеева В.Н. и соавт., 1993).
Во второй серии экспериментов воспроизводили модель острого токсического гепатита путем внутримышечного введения 50% раствора четыреххлористого углерода (CCl4) на оливковом масле (3 мл/кг) и внутрибрюшинного введения соединения I и мексидола в течение 5 дней с интервалом 24 ч. Развитие ГИО и ГЗТ индуцировали так же, как и в первой серии экспериментов.
В третьей серии экспериментов моделировали острый панкреатит по Шалимову С.А. и соавт. (1989) в модификации Чуевой Т.В.(2002). Экспериментальным крысам проводили лапаротомию, затем при помощи жидкого азота производили криогенное воздействие на головку поджелудочной железы, через 3 часа развивался острый отечный панкреатит, подтвержденный морфологически. Соединение I и мексидол вводили внутрибрюшинно в течение 7 дней после операции с интервалом 24 ч. Экспериментально установлено, что максимальная иммуносупрессия при моделировании острого панкреатита отмечается на 5-7 сутки. В связи с этим исследование количества АОК, РОК и показателей ГЗТ проводили на 7 сутки после лапаротомии по той же схеме, что и в первой серии экспериментов.
Соединение I и мексидол вводили во всех исследованиях в экспериментально подобранных дозах 35 мг/кг и 30 мг/кг соответственно. Животных выводили из опыта декапитацией под эфирным наркозом.
Интенсивность перекисного окисления липидов оценивали по содержанию в сыворотке крови ацилгидроперекисей (В.И.Бенисевич, Л.И.Идельсон, 1973) и малонового диальдегида (Н.Д.Стальная, Т.Г.Гаришвилли, 1977). Антиоксидантный статус оценивали по методике вычисления каталазного числа. Величины всех перечисленных показателей определяли унифицированными методами. Математический анализ полученных данных проводили с помощью программы «Statistica 6.0 StatSoft, USA».
Установлено, что пятикратное внутрибрюшинное введение соединения I вызывает достоверное иммуностимулирующее действие, увеличивает количество АОК в 2,1 раза и РОК в 1,9 раза по сравнению с контролем. Внутрибрюшинное введение мексидола не оказывает влияния на иммунный ответ животных (табл.1).
Острая токсичность и влияние соединения I и мексидола на формирование ГИО и ГЗТ, индуцированных ЭБ
мг
×106
Как следует из данных, приведенных в табл.1, соединение I стимулирует развитие реакции гиперчувствительности замедленного типа на эритроциты барана. Разница масс регионального и контралатерального лимфатических узлов (РМЛ) и количество в них ядросодержащих клеток (РКЛ) при введении соединения I увеличиваются в 2,7 раза. Препарат сравнения - мексидол обладает аналогичной активностью.
При исследовании биохимических показателей сыворотки крови здоровых животных, характеризующих антиоксидантную активность, установлено, что введение соединения I и мексидола не влияет на данные показатели и, следовательно, на процессы ПОЛ (табл.2).
Влияние соединения I и мексидола на процессы перекисного окисления липидов у крыс
гр.
усл.ед.
мкмоль/л
Во второй серии экспериментов была изучена иммуномодулирующая активность соединения I и мексидола в условиях повышенной иммунной реактивности. В качестве экспериментальной модели патологии была использована модель токсического поражения печени, которая моделировалась путем внутримышечного введения четыреххлористого углерода (CCl4) (табл.3).
Влияние соединения I и мексидола на формирование ГИО и ГЗТ в условиях острого токсического поражения печени
гр.
тыс./орган
млн./орган
Мг
×106
Установлено, что внутримышечное введение крысам в течение 5 дней оливкового масла не влияет на формирование ГИО, индуцированного ЭБ. Введение CCl4 повышает иммунологическую реактивность на ЭБ, что проявляется увеличением в селезенке отравленных крыс числа иммунных АОК в 3,2 раза, РОК в 1,8 раза по сравнению с контрольной группой животных (табл.3).
При внутрибрюшинном введении соединения I, в течение 5 суток в дозе 35 мг/кг, показатели количества АОК и РОК оставались на уровне контрольных данных, несмотря на введение CCl4. Иммуномодулирующая активность соединения I превосходит таковую у мексидола.
Исследование развития ГЗТ выявило аналогичную с ГИО динамику изменения показателей. Установлено, что максимальным корригирующим влиянием на показатели РМЛ и РКЛ, при токсическом поражении печени, обладает соединение I. Внутрибрюшинное введение соединения I в дозе 35 мг/кг оказывает выраженное гепатопротекторное действие, в серии экспериментов с данным соединением не наблюдалось достоверного увеличения показателей РМЛ и РКЛ по сравнению с контрольными данными (табл.3).
Введение CCl4 статистически достоверно приводит к выраженному повышению содержания продуктов ПОЛ в экспериментальной группе животных. Кроме того, отмечается достоверное, в 2,1 раза, снижение активности каталазы, по сравнению с контрольной группой животных (табл.4). Все это дает возможность говорить об усилении процессов ПОЛ у животных в условиях острой токсической гепатопатии.
Влияние соединения I и мексидола на процессы перекисного окисления липидов в условиях острого токсического поражения печени
гр.
усл. ед.
мкмоль/л
Соединение I проявляет выраженные антиоксидантные и мембранно-стабилизирующие свойства в условиях токсической гепатопатии. Его внутрибрюшинное введение полностью защищает мембраны гепатоцитов от повреждающего действия CCl4, показатели интенсивности ПОЛ остаются на уровне контрольных данных. Внутрибрюшинное введение мексидола уменьшает выраженность процессов ПОЛ, но уступает по активности соединению I. Так, введение мексидола в дозе 30 мг/кг, уменьшает концентрацию АГП и МДА в 1,3 раза, увеличивает концентрацию каталазы в 1,2 раза по сравнению с данными, полученными у животных с токсической гепатопатией (табл.4).
В третьей серии экспериментов изучалась коррекция нарушений иммунной реактивности соединением I и мексидолом в условиях вторичного иммунодефицита на модели острого отечного панкреатита. Результаты экспериментов по изучению ГИО и ГЗТ на ЭБ при экспериментальном остром отечном панкреатите представлены в табл.5. Выявлено, что на 7-е сутки количество иммунных АОК и РОК в селезенке крыс с острым панкреатитом уменьшилось по сравнению с контролем в 2,6 и 2,3 раза соответственно. Показатели РМЛ и РКЛ уменьшились в 1,7 и 1,9 раза соответственно. Данные показатели в группе животных с ложной лапаротомией не отличаются от контрольных данных.
Влияние соединения I и мексидола на формирование ГИО и ГЗТ в условиях острого отечного панкреатита
гр.
тыс./орган
млн./орган
мг
×l06
Введение препарата сравнения - мексидола достоверно увеличивает количество антитело - и розеткообразующих клеток. Однако данные показатели не достигают уровня контрольных значений. Введение соединения I, как и в серии экспериментов с моделированием токсического поражения печени, оказывает максимальное воздействие на иммунную реактивность крыс, индуцированную ЭБ, в условиях острого панкреатита. Показатели АОК и РОК в данной серии экспериментов остаются на уровне контрольных данных, т.е. наблюдается иммунокоррегирующий эффект, наиболее выраженный в условиях вторичного иммунодефицита.
Соединение I стимулирует развитие реакции ГЗТ в условиях острого панкреатита. Показатели РМЛ и РКЛ в серии экспериментов с введением данного соединения достигают уровня контрольных значений. Данная тенденция наблюдается и в сериях экспериментов с введением мексидола. Однако показатель РМЛ в экспериментах с применением мексидола не достигает уровня контрольных значений (табл.5).
Экспериментальная модель острого отечного панкреатита характеризуется развитием цитолитического поражения тканей и увеличением концентрации продуктов ПОЛ. Концентрация АГП и МДА возрастает в 3,2 и 2 раза, соответственно, по сравнению с контрольной группой животных. Активность каталазы снижается с 25,3±3,9 в контроле, до 8,4±1,1 в группе животных с острым панкреатитом (табл.6).
Влияние соединения I и мексидола на процессы перекисного окисления липидов в условиях острого отечного панкреатита.
гр.
усл.ед
мкмоль/л
Следует отметить, что в группе «ложнооперированных» животных не наблюдается отклонения показателей уровня продуктов ПОЛ и активности каталазы от контрольных данных. Введение соединения I в условиях острого отечного панкреатита сохраняет исследуемые показатели на уровне контрольных данных. По антиоксидантному и мембранопротекторному действию данное соединение превосходит мексидол (табл.6).
Таким образом, заявляемое соединение I в дозе 35 мг/кг вызывает выраженную стимуляцию гуморального иммунного ответа у крыс. Мексидол в дозе 30 мг/кг данной активностью не обладает.
Соединение I и мексидол не влияют на процессы перекисного окисления липидов в физиологических условиях.
По влиянию на реакцию гиперчувствительности замедленного типа соединение I проявляет равную с мексидолом активность.
Соединение I отменяет иммуносупрессирующий эффект, возникающий при экспериментальном остром панкреатите, и иммуностимуляцию, индуцированную введением CCl4, и на данных моделях превосходит по иммуномодулирующему, антиоксидантному и гепатопротекторному действию препарат сравнения - мексидол.
Данное соединение может быть использовано при создании препаратов с антиоксидантным, иммуномодулирующим и гепатопротекторным действием.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОДГОТОВКИ ЭРИТРОЦИТОВ ДЛЯ СТИМУЛЯЦИИ ИММУНОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ У ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2000 |
|
RU2157702C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АДАПТОГЕННОЙ И ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2013 |
|
RU2516886C1 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2253447C1 |
| СПОСОБ УМЕНЬШЕНИЯ ТОКСИЧЕСКОГО ПОВРЕЖДЕНИЯ ПЕЧЕНИ | 2007 |
|
RU2342132C2 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2253444C1 |
| Способ получения средства, обладающего нейропротективной, иммуномодулирующей активностью | 2022 |
|
RU2784435C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2021 |
|
RU2797119C2 |
| ИММУНОМОДУЛЯТОР | 2003 |
|
RU2245142C1 |
| СПОСОБ ПОДГОТОВКИ ЭРИТРОЦИТОВ ДЛЯ СТИМУЛЯЦИИ ИММУНОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ У ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 1996 |
|
RU2114433C1 |
| СПОСОБ СТИМУЛЯЦИИ ИММУНОЛОГИЧЕСКОЙ РЕАКТИВНОСТИ У ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 1995 |
|
RU2084896C1 |
Изобретение относится к области новых биологически активных химических соединений, а именно к β-гидроксиникотиноилгидразону 2-метил-3-гидрокси-4-формил-5-оксиметилперидина дигидрохлорида общей формулы I, который обладает антиоксидантным, гепатопротекторным и иммуномодулирующим действием. Соединение формулы I получают взаимодействием гидразида 5-гидроксиникотиновой кислоты с 2-метил-3-гидрокси-4-формил-5-оксиметилпиридином гидрохлоридом в присутствии растворителя и соляной кислоты при нагревании. Соединение формулы I вызывает выраженную стимуляцию гуморального иммунного ответа у крыс. Известный антиоксидант - мексидол данной активностью не обладает. По влиянию на реакцию гиперчувствительности замедленного типа соединение I проявляет равную с мексидолом активность. Соединение формулы I отменяет иммуносупрессирующий эффект, возникающий при экспериментальном остром панкреатите, и иммуностимуляцию, индуцированную введением CCl4, и на данных моделях превосходит по иммуномодулирующему, антиоксидантному и гепатопротекторному действию мексидол. 6 табл.
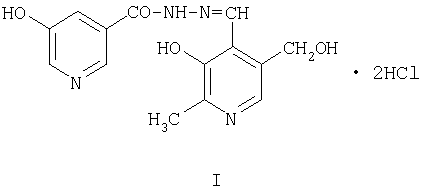
β-Гидроксиникотиноилгидразон 2-метил-3-гидрокси-4-формил-5-оксиметилпиридина дигидрохлорид формулы
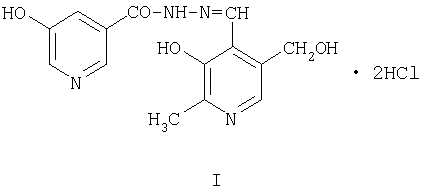
проявляющий антиоксидантную, гепатопротекторную и иммуномодулирующую активность.
| RU 2002115704 А, 10.12.2003 | |||
| 3,28-ДИ-О-НИКОТИНАТ БЕТУЛИНА, ПРОЯВЛЯЮЩИЙ ГЕПАТОПРОТЕКТОРНУЮ И АНТИ-ВИЧ АКТИВНОСТЬ | 1999 |
|
RU2174982C2 |
| ИММУНОМОДУЛЯТОР С АНТИМИКОБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ "ИЗОФОН", СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 1997 |
|
RU2141322C1 |
| DE 4207401 А1, 16.09.1993 | |||
| SAREL, S | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2007-08-10—Публикация
2006-02-17—Подача