Изобретение относится к органической химии, точнее к получению кремнийорганических соединений, а именно 1-триметилсилилпропаргилового спирта, формулы 1
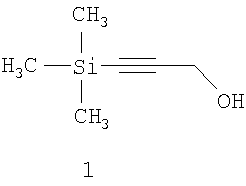
нашедшего широкое применение в технологии тонкого органического синтеза, в качестве исходного вещества.
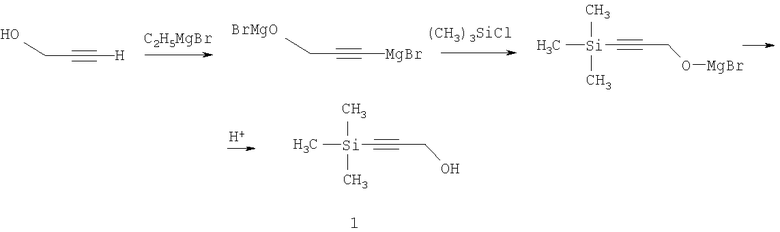
Известен способ получения 1-триметилсилилпропаргилового спирта с выходом 43,5%, основанный на взаимодействии пропаргилового спирта с избытком этилмагнийбромида и последующей обработке триметилхлорсиланом. [Комаров Н.В., Шостаковский М.Ф. Синтез первичных γ-кремнеорганических ацетиленовых спиртов. Изв. АН СССР. Сер. химическая, 1960, с.1300-1302; Миронов В.Ф., Максимова Н.Г. Синтез непредельных кремнеорганических соединений на основе пропаргилового спирта. Изв. АН СССР. Сер. химическая, 1960, с.2059-2060.]
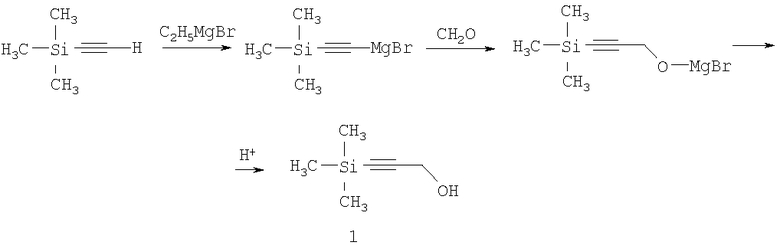
Известен способ получения 1-триметилсилилпропаргилового спирта с выходом 69,7% взаимодействием триметилсилилэтинилмагний бромида с формальдегидом. Однако труднодоступность и дороговизна триметилсилилэтинилмагний бромида делает ограниченным использование этого способа [Шостаковский М.Ф., Комаров Н.В., Ярош О.Г. Синтез триалкилэтинилсиланов и кремнеацетиленовых спиртов. Изв. АН СССР. Сер. химическая, 1966, с.101-104].
Наиболее близким аналогом к заявляемому является способ получения 1-триметилсилилпропаргилового спирта взаимодействием 1-триметилсилокси-2-пропинола-1 с этилмагний бромидом и последующим гидролизом разбавленным раствором соляной кислоты по схеме:
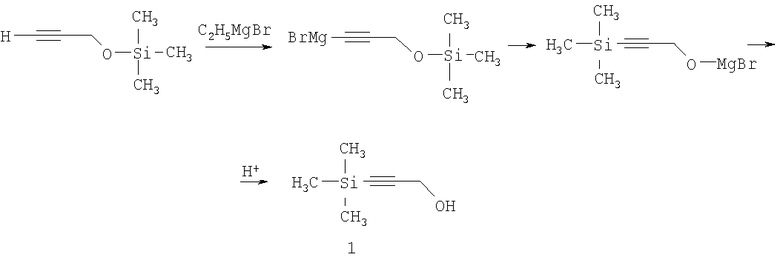
В данном способе требуется кипячение реакционной массы в течение 9 часов [Medvedeva A.S., Novokshonov V.V., Demina М.М., Voronkov M.G. An unusual rearrangement of 1-trimethylsiloxy-3-bromomagnesium-2-propyne. J. Organomet. Chem. 553 (1998), 481-482].
Описанные способы требуют использования металлоорганических реагентов - реактивов Гриньяра, которые получают с использованием металлического магния и алкилбромида в среде эфирного растворителя, что сопряжено с более жесткими требованиями безопасности и длительны в исполнении.
Технической задачей заявляемого способа является разработка безопасного простого способа получения 1-триметилсилилпропаргилового спирта из пропаргилового спирта, исключающего применение металлоорганического синтеза и дорогостоящих защитных групп, при одновременном снижении себестоимости получаемого продукта, путем использования более дешевых и доступных реагентов.
Поставленная техническая задача решается путем использования дипропаргилового эфира щавелевой кислоты, который получают при азеотропной этерификации щавелевой кислоты пропаргиловым спиртом по схеме:
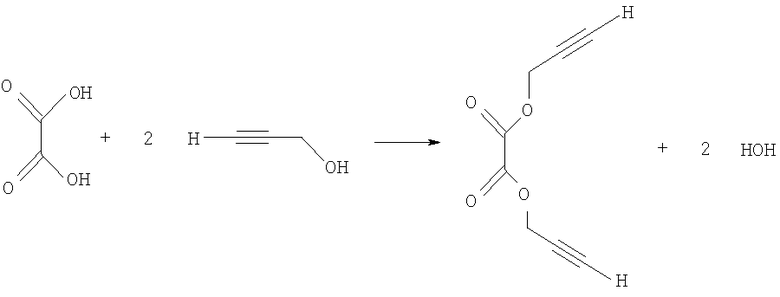
Выход дипропаргилового эфира щавелевой кислоты достигает 78%.
Из уровня техники не известно соединение дипропаргиловый эфир щавелевой кислоты, используемое нами для получении 1-триметилсилилпропаргилового спирта.
Силилирование пропаргилового эфира щавелевой кислоты под действием N-триметилсилилдиэтиламина и хлорида цинка в среде органического растворителя при температуре кипения, с последующим гидролизом реакционной массы водным раствором соляной кислоты протекает в соответствии со схемой:
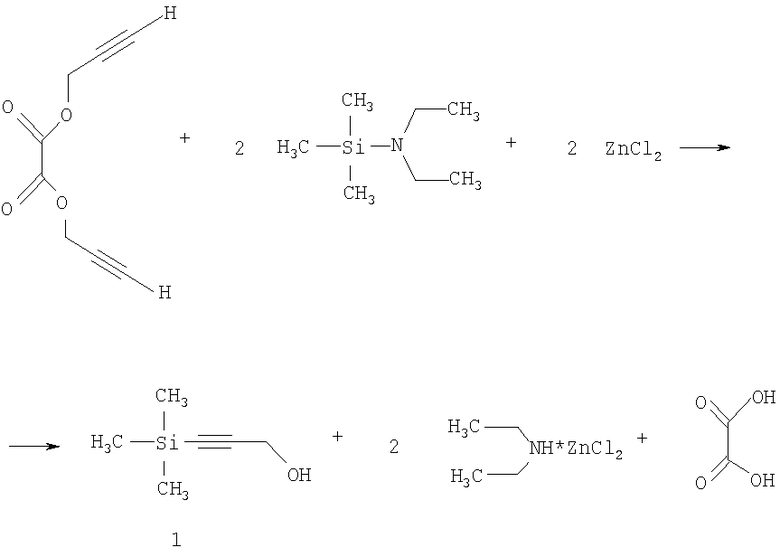
Оптимальные условия силилирования ацетиленовых соединений определяли тем, что органическим растворителем может быть 1,4-диоксан, либо толуол, либо дихлорметан, но лучшим растворителем является 1,4-диоксан. [Direct electrophilic silylation of terminal alkynes / A.Andreev, V.Konshin, N.Komarov, M.Rubin, C.Brouwer, V.Gevorgyan // Org.Lett. - 2004. - Vol.6. - №3. - p.421-424.]
Пример получения дипропаргилового эфира щавелевой кислоты
В прибор, состоящий из колбы, снабженной насадкой Дина-Старка с обратным холодильником, помещают 500 мл бензола, 1 моль (90 г) щавелевой кислоты и 3 моль (168,18 г) пропаргилового спирта. Нагревают при интенсивном кипении растворителя до прекращения отделения воды.
После охлаждения реакционной массы продукт закристаллизовывается, его отфильтровывают, промывают бензолом и сушат. Выход 78%.
Тпл 103-104°С
ЯМР 1Н (CDCl3, δ м.д., J/Гц):2.59 (т, 2Н); 4,90 (д., 4Н).
Масс-спектр (ЭУ, 70эВ), m/z(Ioтн(%)): 137 [М+-29] (0,5), 39 (100).
Пример получения 1-триметилсилилпропаргилового спирта
В прибор для синтеза, состоящий из колбы, снабженной мешалкой и обратным холодильником, помещают 300 мл абсолютного 1,4-диоксана, 1,08 моль (146 г) безводного хлорида цинка и 0,9 моль (130 г) N-триметилсилилдиэтиламина, нагревают при перемешивании до 50°С и прибавляют раствор 0,3 моль (49,8 г) дипропаргилового эфира щавелевой кислоты, растворенный в 150 мл 1,4-диоксана. Реакционную массу нагревают, поддерживая равномерное кипение растворителя в течение 2 часов. После охлаждения реакционную массу выливают в делительную воронку, содержащую 1000 мл 15%-ного раствора соляной кислоты, встряхивают, органическую фазу отделяют, водную фазу экстрагируют хлороформом. Органические фазы объединяют, растворитель отгоняют, остаток перегоняют в вакууме. Получают 58,5 г вещества с Ткип 49°С/3 мм рт.ст. Выход 76%.
ИК-спектр (KBr), ν/cm-1: 3344 (ОН), 2177(С≡С).
ЯМР 1Н (CDCl3, δ, м.д., J/Гц):0,18 (с., 9Н), 1,84 (с., 1Н), 4,27 (с., 2Н).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выделения аминокислот из белковых гидролизатов | 1972 |
|
SU447033A1 |
| Способ получения дипропаргиловых эфиров непредельных дикарбоновых кислот | 1980 |
|
SU883009A1 |
| Способ получения производных 4 -пиперидин /морфолин/ - бутин-2-карбоновых кислот | 1967 |
|
SU248687A1 |
| СПОСОБ СИНТЕЗА МАНДИПРОПАМИДА И ЕГО ПРОИЗВОДНЫХ | 2006 |
|
RU2470914C9 |
| Способ получения этиленненасыщенных гидроксиацеталей | 1979 |
|
SU1011047A3 |
| СПОСОБ ПОЛУЧЕНИЯ 6-АМИНОКАПРОНОВОЙ КИСЛОТЫ | 2021 |
|
RU2786162C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИГИДРОПИРИДИНА | 1972 |
|
SU357726A1 |
| Способ получения метиловых эфиров трикарбоновых кислот | 1978 |
|
SU719996A1 |
| Способ получения 5-меркапто-1,2,3-триазолов | 1979 |
|
SU961559A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАФТОРБУТАДИЕНА | 2002 |
|
RU2247104C2 |
Изобретение относится к получению 1-триметилсилилпропаргилового спирта, широко применяемого в качестве исходного компонента в технологии тонкого органического синтеза. Техническая задача - разработка простого, безопасного способа получения 1-триметилсилилпропаргилового спирта, исключающего применение металлоорганического синтеза и дорогостоящих защитных групп, при одновременном снижении себестоимости получаемого продукта путем использования более дешевых и доступных реагентов. Предложено получение 1-триметилсилилпропаргилового спирта силилированием дипропаргилового эфира щавелевой кислоты под действием N-триметилсилилдиэтиламина и хлорида цинка в среде растворителя при температуре его кипения с последующим гидролизом соляной кислотой, экстрагированием и перегонкой в вакууме. Дипропаргиловый эфир щавелевой кислоты предложено получать взаимодействием щавелевой кислоты с пропаргиловым спиртом в среде бензола при температуре его кипения и постоянном водоотделении. 2 н.п. ф-лы.
1. Способ получения 1-триметилсилилпропаргилового спирта, включающий получение из пропаргилового спирта его производного с последующим силилированием и гидролизом соляной кислотой, экстрагированием и перегонкой в вакууме, отличающийся тем, что в качестве производного пропаргилового спирта используют дипропаргиловый эфир щавелевой кислоты и силилирование проводят под действием N-триметилсилилдиэтиламина и хлорида цинка в среде растворителя при температуре его кипения.
2. Способ получения дипропаргилового эфира щавелевой кислоты путем взаимодействия щавелевой кислоты с пропаргиловым спиртом в среде бензола при температуре его кипения и постоянном водоотделении.
| Medvedeva A.S | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| - Journal of Organometallic Chemistry, 1998, 553, p.481-482 | |||
| Aleksey A | |||
| Andreev et al | |||
| Direct electrophilic silylation of terminal alkynes | |||
| - Organic Letters, 2004, vol.6, № 3, p.421-424 | |||
| Способ получения триметилсилилпропаргилового спирта | 1991 |
|
SU1766923A1 |
| Шостаковский М.Ф., Комаров Н.В., | |||
Авторы
Даты
2009-11-20—Публикация
2008-10-29—Подача