Данное изобретение относится к иммортализованным клеточным линиям птиц и к применению этих клеток для продуцирования вирусов. Клетки в соответствии с изобретением, в частности, полезны для продуцирования рекомбинантных вирусных векторов, которые можно применять для получения терапевтических и/или профилактических композиций для лечения животных и более конкретно людей.
Эукариотические клеточные линии являются основополагающими для промышленного получения вирусных вакцин и многих продуктов биотехнологии. Биологические препараты, продуцируемые в клеточных культурах, включают ферменты, гормоны, иммунобиологические препараты (моноклональные антитела, интерлейкины, лимфокины) и противораковые агенты. Хотя многие более простые белки можно продуцировать, используя бактериальные клетки, более сложные белки, которые являются гликозилированными, в настоящее время должны быть получены в эукариотических клетках.
Клетки птиц много лет используют для продуцирования вирусных векторов. Например, вирус осповакцины, применяемый для получения профилактической композиции для лечения оспы, культивировали на эмбриональных фибробластах цыпленка (CEF). Клетки птиц особенно полезны, поскольку многие вирусы, применяемые в фармацевтической композиции, способны реплицироваться на них. Более примечательно, что различные вирусы способны расти только на клетках птиц. Это имеет место, например, в случае вируса млекопитающих Анкара (MVA), который неспособен расти на клетках млекопитающих. Этот поксвирус, который имеет происхождение от вируса осповакцины, путем более чем 500 пассажей на CEF использовали в ранние семидесятые годы для вакцинации людей с иммунодефицитом против оспы. Теперь MVA, в основном, применяют в качестве вектора для целей генотерапии. Например, MVA применяют в качестве вектора для гена MUC1 для вакцинации пациентов против опухоли, экспрессирующей этот антиген (Scholl et al., 2003, J Biomed Biotechnol., 2003, 3, 194-201). MVA, несущий ген, кодирующий антигены HPV, также применяют в качестве вектора для терапевтического лечения карциномы яичника. Недавно MVA стал вектором первого выбора для получения профилактического лечения против вновь возникших заболеваний или вероятного биологического оружия, как, например, вирус Западного Нила и сибирская язва.
В связи с этим существует возрастающая потребность в продуцировании вирусов. К настоящему времени чаще всего используемый способ продуцирования MVA включает стадию репликации вируса на CEF. Однако использование CEF связано с различными трудностями. Во-первых, получение CEF включает много стадий, которые приходится осуществлять вручную.
Кроме того, данный способ продуцирования вируса зависит от доступности яиц, которые могут быть полностью разрушены в случае заражения производителей. Эта проблема является все более релевантной в связи с распространением птичьего гриппа.
Кроме того, многие CEF обладают обратнотранскриптазной активностью (ОТ). ОТ представляет собой фермент, необходимый для воспроизведения ретровирусов. Ретровирусы обнаружены во многих различных видах. ОТ не является инфекционной у людей или животных, и не было показано, что она вызывает какие-либо вредные эффекты для здоровья у людей. С использованием анализа на основе высокочувствительной полимеразной цепной реакции (ПЦР) активность ОТ обнаружена в ничтожно малых количествах в вакцинах, полученных с эмбриональными фибробластами цыпленка. Источником фермента, вероятно, является частичный вирусный геном, кодирующий ОТ, который, по-видимому, интегрировал в клетки цыпленка сотни или тысячи лет назад. Неизвестно, чтобы ретровирусы птиц, которые продуцируют эту ОТ, поражали людей. Хотя вирус иммунодефицита человека (ВИЧ, вирус, который приводит к СПИДу), представляет собой ретровирус, активность ОТ, обнаруженная в вакцинах, определенно не имеет происхождения от ВИЧ. Кроме того, присутствие ОТ не подтверждает присутствия ретровируса. Тем не менее, клеточная линия без эндогенной активности ОТ представляла бы интерес.
С целью освобождения способа продуцирования вируса от использования CEF существует возрастающая потребность в клеточной линии птиц, которая дала бы возможность репликации и продуцирования вируса. Иммортализованные клеточные линии можно поддерживать или замораживать от партии к партии на месте продуцирования, и они всегда доступны для нового процесса продуцирования. Кроме того, поскольку они ограничены промышленным предприятием, они меньше подвергаются заражению экзогенным загрязнителем. Их применение дает возможность резкого уменьшения ручных манипуляций, необходимых для способа продуцирования. Все эти свойства приводят к снижению стоимости и продолжительности процесса продуцирования, а также к сведению к минимуму потенциального заражения.
Наконец, клеточные линии могут быть полностью охарактеризованы и, таким образом, полностью согласуются со стандартами добросовестной лабораторной практики и требованиями различных медицинских учреждений.
Различные клеточные линии птиц уже описаны. Например, DF1 (US 5879924) представляет собой спонтанно иммортализованную линию клеток цыпленка, имеющую происхождение от яиц 10-суточного возраста линии East Lansing Line (ELL-0). Эти клетки полезны в качестве субстратов для размножения вирусов, экспрессии рекомбинантных белков и продуцирования рекомбинантных вирусов. Однако эта клеточная линия чувствительна к различным вирусам, таким как вирус герпеса Meleagrid 1 (вирус герпеса индюков), вирус оспы птиц, реовирус, вирус саркомы и лейкемии птиц и вирус саркомы Рауса.
Иммортализованные клетки птиц могут быть также получены из эмбриональных стволовых клеток путем прогрессирующего отделения от факторов роста и фидерного слоя, сохраняя, таким образом, признаки роста и бесконечную продолжительность жизни, характерные для недифференцированных стволовых клеток. Единственной доступной клеточной линией птиц, полученной данным способом, является клеточная линия кур Ebx (WO 2005007840), которая находилась в контакте с фидерными слоями мышиного происхождения, что вызывало дополнительные вопросы регулирующих органов, такие как заражение мышиными вирусами и присутствие эндогенных ретровирусных последовательностей в куриных клетках. Кроме того, эти клеточные линии описаны при некоторых условиях как нестабильные и склонные к дифференциации.
Также основана постоянная клеточная линия эмбрионов утки, свободная от эндогенных ретровирусов птиц. Клеточная линия, обозначенная как DEC 99 (Ivanov et al. Experimental Pathology and Parasitology, 4/2000 Bulgarian Academy of Sciences), прокультивирована в течение 140 последовательных пассажей и не является канцерогенной для птиц. Клеточная линия DEC 99 представляет собой стандартную систему клеточной культуры, которая использована для исследования и может быть применена для нужд биотехнологии. Эта клеточная линия является подходящей моделью для исследований в области клеточной биологии, вирусологии, иммунологии, токсикологии и для получения диагностик и вакцин. Исследована чувствительность постоянной клеточной линии эмбриона утки (CL) DEC 99 к инфекции вакцинными штаммами поксвируса птиц (APV), адаптированными к эмбрионам (Ivanov et al. Experimental Pathology and Parasitology, 4/6 2001 Bulgarian Academy of Sciences). Использованы вакцинные штаммы FK и Dessau происхождения от домашней птицы и голубей соответственно. Проводили последовательные пассажи штаммов вирусов (13 пассажей) на первичных клеточных культурах эмбрионов утки (СС). Проводили дальнейшие пассажи адаптированных вирусных штаммов (12 пассажей) в СС клеточной линии DEC 99, где наблюдали типичный цитопатический эффект (ЦПЭ). Продуцирование инфекционных вирионов проверяли путем заражения 11-суточных эмбрионов белых леггорнов, где образовывались типичные разрастания оспы на хориоаллантоисных мембранах (ХАМ). В клетках DEC 99 штамм FK вызывал ранний ЦПЭ по сравнению со штаммом Dessau и достигал титра 10625 CCID50/мл. Вирусные штаммы, адаптированные к DEC 99, индуцировали типичные кожные положительные реакции после вакцинации двухмесячных цыплят. Таким образом, DEC 99 в качестве стандартной СС системы оказалась пригодной для получения вакцин против оспы птиц. Тем не менее, данная конкретная клеточная линия является медленно растущей после пассажа 40 и неспособна расти в суспензии.
Нуклеиново-кислотные последовательности из ранней области аденовируса 5 человека уже использованы для трансформации некоторых специфичных человеческих клеток in vitro (клеточные линии 293 и PER.C6; Fallaux, F.J. et al., Hum. Gene Ther. 9: 1909-17 (1998); Graham, F.L. et al., J. Gen. Virol. 36: 59-74 (1977)).
В целом аденовирусный геном состоит из двунитевой линейной молекулы ДНК длиной примерно 36 кб, которая содержит последовательности, кодирующие более 30 белков. На каждом из ее концов присутствует короткая инвертированная последовательность из 100-150 нуклеотидов в зависимости от серотипов, обозначенная ИКП (инвертированный концевой повтор). ИКП вовлечены в репликацию аденовирусного генома. Область капсидации примерно из 300 нуклеотидов локализована на 5' конце генома сразу после 5' ИКП.
Ранние гены распределены на 4 области, которые дисперсно распределены в аденовирусном геноме, обозначенные Е1-Е4 (Е обозначает "early, ранний"). Ранние области включают по меньшей мере шесть транскрипционных единиц, которые обладают собственными промоторами. Экспрессия ранних генов является самостоятельно регулируемой, причем некоторые гены экспрессируются раньше других. Три области, Е1, Е2 и Е4, соответственно, являются существенными для репликации вируса. Таким образом, если аденовирус является дефектным по одной из этих функций, то есть если он не может продуцировать по меньшей мере один белок, кодируемый одной из этих областей, этот белок должен быть предоставлен ему в транс-положении.
Ранняя область Е1 локализована на 5' конце аденовирусного генома и содержит 2 вирусные транскрипционные единицы, Е1А и Е1В, соответственно. Эта область кодирует белки, которые очень рано участвуют в вирусном цикле и существенны для экспрессии почти всех других генов аденовируса. В частности, транскрипционная единица Е1А кодирует белок, который транс-активирует транскрипцию других вирусных генов, включая транскрипцию с промоторов областей Е1В, Е2А, Е2В и Е4.
Guilhot et al. (Guilhot, C. et al., Oncogene 8: 619-24(1993)) было показано, что ретровирусная трансдукция белка 12S Е1А из Ad5 может привести к иммортализации клеток перепела. Однако в WO 2005042728 раскрыто, что невозможно иммортализировать клетки птиц, когда ген Е1А вводят путем трансфекции депротеинизированной ДНК вместо ретровирусной инфекции. В WO 2005042728, кроме того, указано: "что крайне эффективная и стабильная трансдукция посредством ретровирусной инфекции создает клеточный пул, достаточно большой, чтобы содержать индивидуальные клетки со спонтанными геномными изменениями, которые обладают блокированным апоптозом, который обычно индуцируется при инактивации ретинобластомы" (с.10).
Присутствие ретровирусных последовательностей в клетках, полученных Guilhot et al., затрудняет использование таких клеток для получения биологического препарата и более конкретно для терапевтических соединений.
Авторы изобретения неожиданно обнаружили, что клетки птиц и, более конкретно, клетки Cairina moschata могут быть эффективно иммортализованы путем трансфекции Е1А невирусным вектором.
С целью решения различных проблем, связанных с использованием CEF и/или с использованием ранее доступных клеточных линий, в настоящем изобретении предложена иммортализованная клетка птиц, содержащая нуклеиново-кислотную последовательность Е1А, характеризующаяся тем, что клетку получают способом, включающим стадию трансфекции клетки невирусным вектором, включающим нуклеиново-кислотную последовательность Е1А, и где клетка не содержит нуклеиново-кислотную последовательность Е1В.
Настоящее изобретение также относится к способу иммортализации клетки птиц, включающему стадию трансфекции клетки невирусным вектором, включающим нуклеиново-кислотную последовательность Е1А, и где указанный способ не включает стадию трансфекции клетки включающим нуклеиново-кислотной последовательностью Е1В.
Иммортализованная клетка, как используют здесь, относится к клетке, способной расти в культуре в течение более чем 35 пассажей.
Термин "число пассажей" относится к числу раз, сколько раз клеточная популяция извлечена из культурального сосуда и претерпела процесс субкультивирования (пассажа), с целью поддержания клеток при достаточно низкой плотности для стимуляции дальнейшего роста.
Как используют на протяжении всей заявки, термины в единственном числе используют в том смысле, что они означают "по меньшей мере один", "по меньшей мере первый", "один или более чем один" или "множество" компонентов или стадий, на которые ссылаются, если контекст не требует иного. Например, термин "клетка" включает множество клеток, включающее их смеси.
Термин "и/или" при использовании здесь включает значение "и", "или" и "все или любая другая комбинация элементов, связанных указанным термином".
Как используют здесь, термин "содержащий" предназначен для обозначения, что продукты, композиции и способы включают компоненты или стадии, на которые ссылаются, но не исключают другие. "Состоящий по существу из" при использовании для определения продуктов, композиций и способов должен подразумевать исключение других компонентов или стадий какой-либо существенной значимости. Таким образом, композиция, состоящая по существу из перечисленных компонентов, не должна исключать следовые примеси и фармацевтически приемлемые носители. "Состоящий из" должен подразумевать исключение более чем следовых элементов других компонентов или стадий.
Как используют здесь, термин "нукпеиново-кислотная последовательность Е1А" относится к нуклеиново-кислотной последовательности продуктов всех генов области Е1А аденовируса, включая нуклеиново-кислотную последовательность, кодирующую две основные РНК: 13S и 12S.
Предпочтительно термин "нуклеиново-кислотная последовательность Е1А" относится к нуклеиново-кислотной последовательности, включающей нуклеиново-кислотную последовательность, которая имеет по меньшей мере 60% идентичности нуклеиново-кислотной последовательности с SEQ ID №:1. В более предпочтительной форме осуществления изобретения Е1А относится к нуклеиново-кислотной последовательности, включающей нуклеиново-кислотную последовательность, которая имеет по меньшей мере 70%, предпочтительно по меньшей мере 80% и даже более предпочтительно по меньшей мере 90% идентичности нуклеиново-кислотной последовательности с SEQ ID №:1. В более предпочтительной форме осуществления Е1А относится к нуклеиново-кислотной последовательности, приведенной в SEQ ID №:1.
Как используют здесь, термин "нуклеиново-кислотная последовательность Е1В" относится ко всей нуклеиново-кислотной последовательности области Е1В аденовируса, включающей нуклеиново-кислотную последовательность, кодирующую 3 основных полипептида 19 кДа и 55 кДа.
Как используют здесь, термин "по существу такая же нуклеиново-кислотная последовательность" относится к молекуле нуклеиновой кислоты, обладающей достаточной идентичностью со сравнительным полинуклеотидом, чтобы гибридизоваться со сравнительным полинуклеотидом в умеренно жестких условиях гибридизации. В одной форме осуществления молекула нуклеиновой кислоты имеет по существу такую же нуклеотидную последовательность, как сравнительная нуклеотидная последовательность, представленная в SEQ ID №:1.
Гибридизация относится к связыванию комплементарных нитей нуклеиновой кислоты (то есть смысловой и антисмысловой нитей или зонда и ДНК-мишени) друг с другом посредством водородных связей, подобных связям, которые имеют место в природе в хромосомной ДНК. Уровни жесткости, используемые для гибридизации данного зонда с ДНК-мишенью, может легко варьировать специалист в данной области техники.
Выражение "жесткая гибридизация" используют здесь как относящееся к условиям, при которых гибриды полинуклеиновой кислоты стабильны. Как известно специалистам в данной области техники, стабильность гибридов отражена в температуре плавления (Tm) гибридов. Как правило, стабильность гибрида является функцией концентрации иона натрия и температуры. Типично реакцию гибридизации проводят в условиях более низкой жесткости с последующими отмывками варьирующей, но более высокой жесткости. Ссылка на жесткость гибридизации относится к таким условиям отмывки.
Как используют здесь, выражение "умеренно жесткая гибридизация" относится к условиям, которые позволяют ДНК-мишени связываться с комплементарной нуклеиновой кислотой, которая обладает примерно 60% идентичностью, предпочтительно примерно 75% идентичностью, более предпочтительно примерно 85% идентичностью с ДНК-мишенью; где более чем примерно 90% идентичность с ДНК-мишенью особенно предпочтительна. Предпочтительно умеренно жесткие условия представляют собой условия, эквивалентные гибридизации в 50% формамиде, 5× растворе Денхардта, 5× SSPE, 0,2% ДСН при 42°C с последующей отмывкой в 0,2× SSPE, 0,2% ДСН при 65°C.
Как используют здесь, выражение "невирусный вектор" особенно относится к вектору плазмидного происхождения, и, может быть, такой вектор комбинируют с одним или более чем одним веществом, улучшающим эффективность трансфекции, и/или стабильность вектора и/или защиту вектора in vivo от иммунной системы организма-хозяина. Эти вещества широко документированы в литературе, которая доступна специалистам в данной области техники (см., например, Felgner et al., 1987, Proc. West. Pharmacol. Soc. 32, 115-121; Hodgson and Solaiman, 1996, Nature Biotechnology 14, 339-342; Remy et at., 1994, Bioconjugate Chemistry 5, 647-654). Для иллюстрации, но без ограничения, они могут представлять собой полимеры, липиды, в частности катионные липиды, липосомы, ядерные белки или нейтральные липиды. Эти вещества можно использовать отдельно или в комбинации. Примеры таких соединений, в частности, приведены в патентных заявках WO 98/08489, WO 98/17693, WO 98/34910, WO 98/37916, WO 98/53853, EP 890362 или WO 99/05183. Комбинацией, которая может быть рассмотрена, является плазмидный рекомбинантный вектор, объединенный с катионными липидами (DOGS, DC-CHOL, спермин-холином, спермидин-холином и подобными) и нейтральными липидами (DOPE).
Выбор плазмид, которые можно использовать в контексте настоящего изобретения, широк. Они могут представлять собой клонирующие и/или экспрессионные векторы. В целом они известны специалистам в данной области техники, и ряд их имеется в продаже, но также возможно сконструировать или модифицировать их с помощью методов генной инженерии. Можно упомянуть в качестве примеров плазмиды, имеющие происхождение от pBR322 (Gibco BRL), pUC (Gibco BRL), pBluescript (Stratagene), pREP4, pCEP4 (Invitrogene) или p Poly (Lathe et al., 1987, Gene 57, 193-201). Предпочтительно плазмида, используемая в контексте настоящего изобретения, содержит точку начала репликации, обеспечивающая инициацию репликации в продуцирующей клетке и/или в клетке-хозяине (например, точка начала репликации Со1Е1 может быть выбрана для плазмиды, предназначенной для продуцирования в Е. coli, а система oriP/EBNA1 может быть выбрана, если желательно, чтобы она автономно реплицировалась в клетке-хозяине млекопитающего (Lupton and Levine, 1985, Mol. Cell. Biol. 5, 2533-2542; Yates et al., Nature 313, 812-815). Она может содержать дополнительные элементы, улучшающие ее поддержание и/или стабильность в данной клетке (последовательность cer, которая стимулирует поддержание плазмиды в мономерном состоянии (Summers and Sherrat, 1984, Cell 36, 1097-1103, Sequences for integration into the cell genome).
Термин "невирусный вектор" исключает вирусные векторы, такие как, например, вектор, имеющий происхождение от поксвируса (вирус осповакцины, в частности, MVA, вирус оспы канареек и тому подобное), от аденовируса, от ретровируса, от вируса герпеса, от альфавируса, от пенистого вируса или от аденоассоциированного вируса.
Настоящее изобретение также относится к клеткам, имеющим происхождение от клетки согласно изобретению. Как используют здесь, термин "имеющий происхождение" относится к клеткам, которые развиваются или дифференцируют из клетки согласно изобретению или имеют ее в качестве предка.
Термин "число пассажей" относится к числу раз, сколько раз клеточная популяция извлечена из культурального сосуда и претерпела процесс субкультивирования (пассажа), с целью поддержания клеток при достаточно низкой плотности для стимуляции дальнейшего роста.
Как используют здесь, термин "трансфицированный" относится к стабильной трансфекции или транзитной трансфекции клетки по изобретению.
Термин "стабильная трансфекция" или "стабильно трансфицированный" относится к введению и интеграции чужеродной нуклеиново-кислотной последовательности в геном трансфицированной клетки. Термин "стабильный трансфектант" относится к клетке, в геномную ДНК которой стабильно интегрирована чужеродная ДНК.
Согласно предпочтительной форме осуществления изобретения клетка птиц по изобретению имеет происхождение от клетки семейства Anatidae или семейства Phasianidae. Среди Anatidae клетки, принадлежащие к родам Cairina или Anas особенно предпочтительны. Даже более предпочтительно клетки согласно изобретению принадлежат к виду Cairina moschata или Anas platyrhynchos.
Предпочтительно клетка согласно изобретению получена из эмбрионального организма. Способы, дающие возможность выделения клеток из живого организма, хорошо известны специалистам в данной области техники. Например, можно использовать способы, раскрытые в примере 2. Согласно предпочтительной форме осуществления изобретения первичную клетку выделяют из эмбриона, принадлежащего к семейству Anatidae, возраст которого составляет между 0 и 20 сутками, более предпочтительно между 5 и 15 сутками и даже более предпочтительно между 11 и 14 сутками.
Согласно предпочтительной форме осуществления изобретения нуклеиново-кислотную последовательность Е1А встраивают в последовательность ДНК-мишени клетки согласно изобретению.
Как используют здесь, "последовательность ДНК-мишени" представляет собой предопределенную область в пределах генома клетки, которая является мишенью для модификации путем гомологичной рекомбинации с вектором. Последовательности ДНК-мишеней включают структурные гены (то есть последовательности ДНК, кодирующие полипептиды, включающие в случае эукариот интроны и экзоны), регуляторные последовательности, такие как энхансерные последовательности, промоторы и тому подобное, а также другие области в пределах интересующего генома. Последовательность ДНК-мишени может также представлять собой последовательность, которая, когда она является мишенью вектора, не обладает эффектом на функцию генома-хозяина.
Как используют здесь, "встроенный в последовательность ДНК-мишени" в широком смысле означает, что процесс гомологичной рекомбинации, который приводит к инсерции иммортализующего гена, вводит делецию или прерывание в последовательность ДНК, являющуюся мишенью.
Для получения иммортализованной клетки птиц, где нуклеиново-кислотная последовательность Е1А встроена в последовательность ДНК-мишени, вектор, используемый в способе согласно изобретению, может дополнительно содержать две гомологичные последовательности, способные к гомологичной рекомбинации с областью последовательности ДНК-мишени, нативной для генома указанной клетки.
Присутствие этих гомологичных последовательностей дает возможность сайт-специфической инсерции молекулы нуклеиновой кислоты по изобретению в последовательность ДНК-мишени посредством гомологичной рекомбинации.
Термин "гомологичная рекомбинация" относится к обмену фрагментов ДНК между двумя молекулами ДНК в сайте по существу идентичных нуклеотидных последовательностей. Согласно данной конкретной форме осуществления изобретения внутри вектора находятся последовательности, которые гомологичны с участками последовательности, содержащейся внутри последовательности ДНК-мишени. В предпочтительной форме осуществления изобретения гомологичные последовательности в векторе переноса на сто процентов гомологичны области последовательности-мишени. Однако можно использовать более низкую гомологию последовательности. Таким образом, можно использовать столь низкую гомологию последовательности, как примерно 80%.
Гомологичные последовательности в векторе переноса содержат по меньшей мере 25 п.о. Предпочтительны более длинные участки, по меньшей мере 500 п.о., и более предпочтительно по меньшей мере 5000 п.о.
Согласно более предпочтительной форме осуществления изобретения молекула нуклеиновой кислоты окружена гомологичными последовательностями в векторе.
Как используют здесь, "окружены" означают, что одна из гомологичных последовательностей локализована выше молекулы нуклеиновой кислоты по изобретению, и что одна из гомологичных последовательностей локализована ниже молекулы нуклеиновой кислоты по изобретению. Как используют здесь, "окружены" не обязательно означает, что две гомологичные последовательности непосредственно сшиты с 3' или с 5' концом иммортализующего гена, и иммортализующий ген и гомологичные последовательности могут быть разделены неограниченным числом нуклеотидов.
Специалист в данной области техники способен выбрать подходящие гомологичные последовательности для направления на конкретную последовательность ДНК в геноме клетки, подлежащей иммортализации. Например, одна гомологичная последовательность может быть гомологична участку последовательности-мишени, где другая гомологичная последовательность гомологична последовательности ДНК, локализованной выше или ниже последовательности-мишени. Согласно другому примеру, одна из гомологичных последовательностей может быть гомологична последовательности ДНК, локализованной выше последовательности ДНК-мишени, где другая гомологичная последовательность гомологична последовательности ДНК, локализованной ниже последовательности ДНК-мишени. В другом примере обе гомологичные последовательности гомологичны последовательностям, локализованным внутри последовательности ДНК-мишени.
Согласно предпочтительной форме осуществления изобретения последовательность ДНК-мишени представляет собой ген HPRT (гипоксантингуанинфосфорибозилтрансферазы).
Геномная последовательность, включающая промотор HPRT и ген HPRT Cairina moschata, приведена в SEQ ID №:2. Последовательность, кодирующая HPRT, начинается в кодоне ATG в положении 8695 нуклеиново-кислотной последовательности, приведенной в SEQ ID №:2, где последовательность выше этого ATG кодона представляет собой промоторную последовательность HPRT.
Специалист в данной области техники способен выбрать гомологичные последовательности, необходимые для интеграции нуклеиново-кислотной последовательности Е1А в ген HPRT. Поскольку между различными членами семейства геномные последовательности, кодирующие HPRT, высоко гомологичны, специалист в данной области техники также способен сконструировать гомологичные последовательности, необходимые для направления в ген HPRT клеток каждой птицы.
Согласно более предпочтительной форме осуществления изобретения гомологичные последовательности приспособлены для встраивания нуклеиново-кислотной последовательности Е1А ниже промотора HPRT клетки. В данной конкретной форме осуществления молекула нуклеиновой кислоты по изобретению оперативно сцеплена с эндогенным промотором HPRT клетки. Под "оперативно сцепленной" подразумевают, что нуклеиново-кислотная последовательность Е1А сцеплена с промотором таким образом, что дает возможность ее экспрессии в клетке.
Согласно данной конкретной форме осуществления гомологичная последовательность слева от молекулы нуклеиновой кислоты по изобретению предпочтительно имеет нуклеиново-кислотную последовательность, которая гомологична по меньшей мере 500 непрерывных п.о. и более предпочтительно по меньшей мере 5000 непрерывных п.о. нуклеиново-кислотной последовательности, начинающейся с нуклеотида в положении 1 и заканчивающейся нуклеотидом в положении 8694 нуклеиново-кислотной последовательности, приведенной в SEQ ID №:2, при условии, что эта гомологичная последовательность не гомологична нуклеиново-кислотной последовательности, начинающейся с нуклеотида в положении 8695 и заканчивающейся нуклеотидом в положении 26916 нуклеиново-кислотной последовательности, приведенной в SEQ ID №:2. Кроме того, эта левая гомологичная последовательность предпочтительно непосредственно сшита со стартовым кодоном нуклеиново-кислотной последовательности Е1А. Согласно еще более предпочтительной форме осуществления изобретения гомологичная последовательность слева от молекулы нуклеиновой кислоты по изобретению состоит из нуклеиново-кислотной последовательности, начинающейся с нуклеотида в положении 1 и заканчивающейся нуклеотидом в положении 8694 нуклеиново-кислотной последовательности, приведенной в SEQ ID №:2. Гомологичная последовательность справа от нуклеиново-кислотной последовательности Е1А предпочтительно имеет нуклеиново-кислотную последовательность, которая гомологична по меньшей мере 500 непрерывных п.о. и более предпочтительно по меньшей мере 5000 непрерывных п.о. нуклеиново-кислотной последовательности, начинающейся с нуклеотида в положении 10580 и заканчивающейся нуклеотидом в положении 18009 нуклеиново-кислотной последовательности, приведенной в SEQ ID №:2. И более предпочтительно гомологичная последовательность справа от нуклеиново-кислотной последовательности Е1А состоит из нуклеиново-кислотной последовательности, начинающейся с нуклеотида в положении 10580 и заканчивающейся нуклеотидом в положении 18009 нуклеиново-кислотной последовательности, приведенной в SEQ ID №:2.
Соответственно, настоящее изобретение также относится к клетке птиц, содержащей нуклеиново-кислотную последовательность Е1А, характеризующейся тем, что эта клетка получена способом, включающим стадию трансфекции клетки невирусным вектором, включающим нуклеиново-кислотную последовательность Е1А, где клетка не содержит нуклеиново-кислотную последовательность Е1 В, и где нуклеиново-кислотная последовательность Е1А оперативно сцеплена с эндогенным промотором HPRT клетки.
Согласно предпочтительной форме осуществления вектор, используемый в способе согласно изобретению, включает первый селективный маркер, где этот первый селективный маркер представляет собой положительный селективный маркер, и где первый селективный маркер окружен гомологичными последовательностями, содержащимися в векторе. В этом отношении процесс гомологичной рекомбинации, который происходит между вектором и геномом клетки, приводит к интеграции нуклеиново-кислотной последовательности Е1А и первого селективного маркера. Когда вектор переноса является кольцевым, "окружен" означает, что первый селективный маркер и нуклеиново-кислотная последовательность Е1А расположены в одном и том же участке вектора, где этот участок ограничен гомологичными последовательностями.
Как используют здесь, термин положительный селективный маркер исключительно относится к гену, кодирующему продукт, который дает возможность только клеткам, которые несут этот ген, выживать и/или расти в определенных условиях. Типичные селективные маркеры кодируют белки, которые придают устойчивость к антибиотикам или другим токсинам, например, к ампициллину, неомицину, метотрексату или тетрациклину, восполняют ауксотрофные недостаточности или обеспечивают критические нутриенты, недоступные из комплексной среды. В предпочтительной форме осуществления согласно изобретению первый селективный маркер кодирует белок, который придает устойчивость к антибиотикам.
Интеграция первого селективного маркера дает возможность селекции клеток, в которые встроена нуклеиново-кислотная последовательность Е1А. Соответственно, способ согласно изобретению может дополнительно включать стадию, где указанные клетки культивируют в среде, которая дает возможность роста только клеток, в которые встроен первый селективный маркер, например, в среде, которая содержит антибиотик.
Согласно более предпочтительной форме осуществления изобретения первый селективный маркер в векторе окружен последовательностями, дающими возможность его супрессии. Эти последовательности, дающие возможность супрессии первого селективного маркера, не окружают нуклеиново-кислотную последовательность Е1А. Когда вектор является кольцевым, последовательности, дающие возможность супрессии первого селективного маркера, первый селективный маркер и нуклеиново-кислотная последовательность Е1А расположены в одном и том же участке вектора переноса, где этот участок ограничен гомологичными последовательностями.
Последовательности, дающие возможность супрессии фрагмента нуклеиновой кислоты, хорошо известны специалистам в данной области техники (Nunes-Duby, S. et al. (1998) Nucleic Acids Res. 26:391-406). Эти последовательности могут распознаваться одним или более чем одним специфичным ферментом, который индуцирует супрессию нуклеиновой кислоты, содержащейся между указанными последовательностями, где эти ферменты называют "рекомбиназой". Например, эти хорошо известные рекомбиназы, дающие возможность супрессии фрагмента нуклеиновой кислоты, представляют собой рекомбиназы FLP, ISCE1 и Cre.
Типичной сайт-специфической рекомбиназой является рекомбиназа Cre. Cre представляет собой 38-кДа продукт гена cre (рекомбинация циклизации) бактериофага Р1 и представляет собой сайт-специфическую ДНК рекомбиназу семейства Int, Sternberg, N. et al. (1986) J. Mol. Biol. 187: 197-212. Cre распознает 34-п.о. сайт генома Р1, называемый loxP (локус кроссинговера Р1) и эффективно катализирует реципрокную консервативную рекомбинацию ДНК между парами сайтов loxP. Сайт loxP состоит из двух 13-п.о. инвертированных повторов, фланкирующих 8-п.о. не палиндромную сердцевинную область. Cre-опосредованная рекомбинация между двумя прямо повторяющимися сайтами loxP приводит в результате к эксцизии ДНК между ними в виде ковалентно замкнутого кольца. Cre-опосредованная рекомбинация между парами сайтов loxP в инвертированной ориентации приведет к инверсии находящейся между ними ДНК вероятнее, чем к эксцизии. Разрыв и воссоединение ДНК ограничены дискретными положениями внутри сердцевинного участка и протекает на нитях одновременно путем транзитной связи фосфотирозин-ДНК-белок с ферментом.
Другой сайт-специфической рекомбиназой является I-Scel. Другую эндонуклеазу хоминга интронов, например, I-Tlil, I-Ceul, I-Crel, I-Ppol и PI-Pspl, можно также заменять I-Scel в способе согласно изобретению. Многие перечислены Belfort and Roberts ((1997) Nucleic Acids Research 25:3379-3388). Многие из этих эндонуклеаз имеют происхождение из геномов органелл, в которых паттерн использования кодонов отличается от стандартного ядерного паттерна использования кодонов. Чтобы использовать такие гены для ядерной экспрессии их эндонуклеаз, может быть необходимо изменение кодирующей последовательности для совпадения с последовательностью ядерных генов. I-Scel является двунитевой эндонуклеазой, которая расщепляет ДНК внутри ее сайта распознавания. I-Scel генерирует 4 п.о. зигзагообразный разрыв с выступающими 3'ОН группами.
Фермент I-Scel имеет известный сайт распознавания. Сайт распознавания I-Scel представляет собой несимметричную последовательность, которая продолжается более 18 п.о.
5' TAGGGATAACAGGGTAAT3'
3' ATCCCTATTGTCCCATTA5'
Другой сайт-специфической рекомбиназой является FLP рекомбиназа. Flp рекомбиназа распознает определенный сайт минимум 34 п.о., который выдерживает только ограниченную вырожденность его последовательности распознавания (Jayaram, 1985; Senecoffet al., 1988). Исследовано взаимодействие между рекомбиназой Flp и последовательностью FRT (Panigrahi et al., 1992). Примеры вариантов последовательности FRT приведены Jayaram (1985) и Senecoff et al. (1988), и анализ на Flp-опосредованную рекомбинацию на различных субстратах описан Snaith et al. (1996).
Соответственно, способ согласно изобретению может дополнительно включать стадию, состоящую в супрессии первого селективного маркера из генома указанной первичной клетки. В целях супрессии первого селективного маркера клетку трансфицируют геном, кодирующим рекомбиназу, специфичную для последовательностей, дающих возможность супрессии первого селективного маркера. Способы и векторы, способные трансфицировать указанный ген в клетку, хорошо известны специалистам в данной области техники, например, можно использовать способ, раскрытый в примере 4 настоящей заявки. Можно также использовать векторы, описанные ранее.
Согласно предпочтительной форме осуществления вектор, используемый в способе согласно изобретению, включает второй селективный маркер, который не окружен указанными гомологичными последовательностями, где второй селективный маркер представляет собой отрицательный селективный маркер. Этот второй селективный маркер, в частности, полезен, когда вектор, используемый в способе согласно изобретению, является кольцевым, присутствие этого второго селективного маркера дает возможность разрушения клеток, в которых процесс гомологичной рекомбинации привел к встраиванию участка вектора переноса, который не содержит нуклеиново-кислотную последовательность Е1А. Когда вектор является кольцевым, тот факт, что второй селективный маркер не окружен гомологичными последовательностями, означает, что второй селективный маркер и нуклеиново-кислотная последовательность Е1А не расположены в одном и том же участке вектора переноса, где этот участок ограничен гомологичными последовательностями.
Соответственно, способ согласно изобретению может дополнительно включать стадию, где клетки культивируют в среде, которая дает возможность роста только клеток, в которые не встроен второй селективный маркер. Эту стадию можно осуществлять одновременно со стадией, где указанные первичные клетки культивируют в среде, которая дает возможность роста только клеток, в которые встроен первый селективный маркер, или отдельно от этой стадии.
Согласно предпочтительной форме осуществления изобретения вектор включает третий селективный маркер, где этот третий селективный маркер представляет собой отрицательный селективный маркер, и где этот третий селективный маркер локализован между последовательностями, дающими возможность супрессии первого селективного маркера. Это означает, что стадия, состоящая в супрессии первого селективного маркера, также приведет к супрессии третьего селективного маркера. Присутствие третьего селективного маркера дает возможность разрушения клеток, в которых присутствует первый селективный маркер. Когда вектор является кольцевым, тот факт, что третий селективный маркер локализован между последовательностями, дающими возможность супрессии первого селективного маркера, означает, что третий селективный маркер и первый селективный маркер расположены в одном и том же участке вектора переноса, где указанный участок ограничен последовательностями, дающими возможность супрессии первого селективного маркера.
Как используют здесь, термин отрицательный селективный маркер исключительно относится к гену, кодирующему продукт, который уничтожает клетки, которые несут этот ген, в определенных условиях. Эти гены в особенности включают "суицидный ген". Продукты, кодируемые этими генами, способны к преобразованию пролекарства в цитотоксическое соединение. Многочисленные пары суицидный ген/пролекарство в настоящее время доступны. Более конкретно можно упомянуть пары:
- тимидинкиназа вируса простого герпеса типа I (HSV-1 ТК) и ацикловир или ганцикловир (GCV) (Caruso et al., 1993, Proc. Natl. Acad. Sci. USA 90, 7024-7028; Culver et al., 1992, Science 256, 1550-1552; Ram et al., 1997, Nat. Med.3, 1354-1361);
- цитохром р450 и циклофосфамид (Wei et al., 1994, Human Gene Therapy 5, 969-978);
- пуриннуклеозидфосфорилаза из Escherichia coli (E.coli) и 6-метилпуриндезоксирибонуклеозид (Sorscher et al., 1994, Gene Therapy 1, 233-238);
- гуанинфосфорибозилтрансфераза из E.coli и 6-тиоксантин (Mzoz and Moolten, 1993, Human Gene Therapy 4, 589-595) и
- цитозиндеаминаза (CDаза) и 5-фторцитозин (5FC);
- FCU1 и 5-фторцитозин (5FC) (WO 9954481);
- FCU1-8 и 5-фторцитозин (5FC) (WO 2005007857).
Указанный третий селективный маркер дает возможность селекции клеток, в которых произошла супрессия первого селективного маркера. Соответственно, способ согласно изобретению может дополнительно включать стадию, на которой клетку культивируют в среде, которая не дает возможности роста клетки, содержащей третий селективный маркер. Например, среда, которая не дает возможности роста клеток, содержащих FCU1 в качестве третьего селективного маркера, содержит 5-фторфитозин.
Первый, второй и третий селективный маркер можно использовать по отдельности. Например, вектор, используемый в способе согласно изобретению, может включать первый и третий селективные маркеры, но не второй, или второй и третий селективные маркеры, но не первый.
Согласно предпочтительной форме осуществления изобретения нуклеиново-кислотная последовательность Е1А, первый, второй и/или третий селективный маркер помещают под контролем элементов, необходимых для их экспрессии в клетке, подлежащей иммортализации.
Элементы, необходимые для экспрессии, состоят из группы элементов, дающих возможность транскрипции нуклеотидной последовательности на РНК и трансляции РНК на полипептид, в частности, промоторных последовательностей и/или регуляторных последовательностей, которые эффективны в указанной клетке, и, может быть, последовательностей, требующихся для возможности экскреции или экспрессии на поверхности клеток-мишеней для указанного полипептида. Эти элементы могут быть регулируемыми или конститутивными. Конечно, промотор адаптирован к выбранному вектору и к клетке-хозяину. Можно упомянуть, например, эукариотические промоторы генов PGK (фосфоглицераткиназы), МТ (металлотионеина; Mclvor et al., 1987, Mol. Cell Biol. 7, 838-848), α-1 антитрипсина, CFTR, промоторы гена, кодирующего мышечную креатинкиназу, актинового легочного сурфактанта, иммуноглобулина или β-актина (Tabin et al., 1982, Mol. Cell Biol. 2, 416-436), SRα (Takebe et al., 1988, Mol. Cell. 8, 466-472), ранний промотор вируса SV40 (вируса обезьян), ДКП RSV (вируса саркомы Рауса), промотор MPSV, промотор TK-HSV-1, ранний промотор вируса CMV (цитомегаловируса). Ранний промотор цитомегаловируса (CMV) является наиболее особенно предпочтительным.
Настоящее изобретение более конкретно относится, но не ограничено им, к способу иммортализации клетки, включающему стадии:
- переноса в клетку птиц вектора, включающего:
- нуклеиново-кислотную последовательность Е1А, окруженную гомологичными последовательностями;
- первый селективный маркер, где первый селективный маркер представляет собой положительный селективный маркер и где первый селективный маркер окружен указанными гомологичными последовательностями;
- последовательности, дающие возможность супрессии первого селективного маркера;
- второй селективный маркер, который не окружен гомологичными последовательностями, где второй селективный маркер представляет собой отрицательный селективный маркер;
- третий селективный маркер, где третий селективный маркер представляет собой отрицательный селективный маркер и где третий селективный маркер локализован между последовательностями, дающими возможность супрессии первого селективного маркера.
- культивирования клеток в среде, которая дает возможность роста клеток, в которые встроен первый селективный маркер;
- культивирования клеток в среде, которая не дает возможности роста клеток, в которые встроен второй селективный маркер;
- исключения первого селективного маркера из генома указанной клетки;
- культивирования указанной клетки в среде, которая не дает возможности роста клеток, содержащих третий селективный маркер.
Клетка согласно изобретению может дополнительно содержать одну или более чем одну нуклеиново-кислотную последовательность, дающую возможность размножения дефектного вируса. "Дефектный вирус" относится к вирусу, в котором один или более чем один вирусный ген, необходимый для его репликации, делетирован или сделан нефункциональным. Термин "нуклеиново-кислотная последовательность, дающая возможность размножения дефектного вируса", относится к нуклеиново-кислотной последовательности, обеспечивающей в трансположении функцию(и), которая дает возможность размножения дефектного вируса. Иными словами, указанная нуклеиново-кислотная последовательность(и) кодирует белок (белки), необходимый для репликации и капсидации дефектного вируса.
Клетка согласно изобретению может также содержать нуклеиново-кислотную последовательность, кодирующую целевое вещество. Как используют здесь, целевое вещество может включать, но не ограничено ими, фармацевтически активный белок, например, факторы роста, регуляторы роста, антитела, антигены, их производные, полезные для иммунизации или вакцинации, или тому подобное, интерлейкины, инсулин, G-CSF, GM-CSF, hPG-CSF, M-CSF или их комбинации, интерфероны, например, интерферон-α, интерферон-β, интерферон-γ, факторы свертывания крови, например, фактор VIII, фактор IX или tPA или их комбинации. "Целевое вещество", также относится к промышленным ферментам, например, для применения в целлюлозно-бумажной промышленности, текстильной модификации или производстве этанола. Наконец, "целевое вещество" также относится к белковой добавке или продукту, повышающему ценность, для кормов животных.
Согласно предпочтительной форме осуществления изобретения клетка согласно изобретению также содержит нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы и более предпочтительно рекомбинантную обратную транскриптазу теломеразы, описанную в ЕР 06360047.2. В предпочтительной форме осуществления изобретения, описанной в ЕР 06360047.2, нуклеиново-кислотная последовательность, кодирующая рекомбинантную обратную транскриптазу теломеразы, имеет по меньшей мере 70%, более предпочтительно по меньшей мере 90% и более предпочтительно по меньшей мере 95% идентичности нуклеиново-кислотной последовательности с нуклеиново-кислотной последовательностью, приведенной в SEQ ID №:2 ЕР 06360047.2. Предпочтительная нуклеиново-кислотная последовательность, кодирующая рекомбинантную обратную транскриптазу теломеразы, описанная в ЕР 06360047.2, является такой, как приведено в SEQ ID №:2 ЕР 06360047.2. Нуклеиново-кислотная последовательность обратной транскриптазы теломеразы SEQ ID №:2, описанная в ЕР 06360047.2, соответствует нуклеиново-кислотной последовательности обратной транскриптазы теломеразы SEQ ID №:3 в настоящем изобретении. Как следствие, согласно предпочтительной форме осуществления изобретения клетка согласно изобретению также содержит нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы, и более предпочтительно нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы, имеющую по меньшей мере 70%, более предпочтительно по меньшей мере 90% и более предпочтительно по меньшей мере 95% идентичности нуклеиново-кислотной последовательности SEQ ID №:3. Более предпочтительно нуклеиново-кислотная последовательность, кодирующая рекомбинантную обратную транскриптазу теломеразы, приведена в SEQ ID №:3 (dTERT).
Клетки, полученные способом согласно изобретению, клетка по изобретению и клетки, имеющие происхождение от нее, особенно полезны для репликации вируса. Вирусы могут быть живыми, аттенуированными, рекомбинантными или нет. Более предпочтительно эти клетки особенно полезны для репликации поксвируса (вируса осповакцины, в частности, MVA, вируса оспы канареек и т.д.), аденовируса, ретровируса, вируса герпеса, альфавируса, пенистого вируса или аденоассоциированного вируса.
Ретровирусы обладают свойством инфицирования делящихся клеток, и в большинстве случаев интеграции в них, и в этом отношении особенно пригодны для применения в связи с раком. Рекомбинантный ретровирус, как правило, содержит последовательности ДКП, область капсидации и нуклеотидную последовательность согласно изобретению, которая помещена под контролем ретровирусного ДКП или внутреннего промотора, такого как описано ниже. Ретровирусный вектор может содержать модификации, в частности, в ДКП (замещение промоторной области эукариотическим промотором) или в области капсидации (замещение гетерологичной областью капсидации, например, типа VL30) (см. французские заявки 94 08300 и 97 05203).
В аденовирусном векторе может полностью или частично отсутствовать по меньшей мере одна область, которая существенна для репликации и которая выбрана из областей Е1, Е2, Е4 и L1-L5. Предпочтительна делеция области Е1. Однако ее можно комбинировать с другой модификацией(ями)/делецией(ями), охватывающей, в частности, полностью или частично области Е2, Е4 и/или L1-L5. В качестве иллюстрации делеция основной части области Е1 и транскрипционной единицы Е4 обладает совершенно особым преимуществом. В целях повышения клонирующих емкостей в аденовирусном векторе может полностью или частично отсутствовать несущественная область ЕЗ. Согласно другой альтернативе, возможно использование минимального аденовирусного вектора, сохраняющего последовательности, которые существенны для капсидации, а именно 5' и 3' ИКП (инвертированный концевой повтор) и область капсидации. Различные аденовирусные векторы и методики их получения известны (см., например, Graham and Prevect, 1991, in Methods in Molecular Biology, Vol 7, p 109-128; Ed: E.J.Murey, The Human Press Inc).
Семейство поксвирусов включает вирусы подсемейств Chondropoxvirinae (поксвирусы позвоночных) и Entomopoxvirinae (поксвирусы насекомых). Среди них поксвирус согласно изобретению предпочтительно выбран из группы, включающей ортопоксвирусы, парапоксвирусы, авипоксвирусы, каприпоксвирусы, лепорипоксвирусы, Suipoxviruses (вирусы оспы свиней), Molluskipoxviruses (вирусы контагиозного моллюска), Yatapoxviruses (вирусы, вызывающие образование опухолей у человека и обезьян). Согласно более предпочтительной форме осуществления поксвирус по изобретению представляет собой ортопоксвирус.
Ортопоксвирус предпочтительно представляет собой вирус осповакцины и более предпочтительно модифицированный вирус осповакцины Анкара (MVA), в частности, MVA 575 (ЕСАСС V00120707) и MVA-BN (ECACC V00083008).
Термин "рекомбинантный вирус" относится к вирусу, содержащему экзогенную последовательность, встроенную в его геном. Как используют здесь, экзогенная последовательность относится к нуклеиновой кислоте, которая в природе не присутствует в исходном вирусе.
В одной форме осуществления экзогенная последовательность кодирует молекулу, обладающую прямо или косвенно цитотоксической функцией. Под "прямо или косвенно" цитотоксическим авторы изобретения подразумевают, что молекула, кодируемая экзогенной последовательностью, может сама по себе быть токсичной (например, рицин, фактор некроза опухоли, интерлейкин-2, интерферон-гамма, рибонуклеаза, дезоксирибонуклеаза, псевдомонадный экзотоксин А) или может претерпевать метаболизм с образованием токсичного продукта, либо она может действовать на что-либо другое с образованием токсичного продукта. Последовательность кДНК рицина раскрыта в статье Lamb et al. (Eur. J. Biochem., 1985, 148, 265-270), включенной здесь путем ссылки.
В предпочтительной форме осуществления изобретения экзогенная последовательность представляет собой суицидный ген. Суицидный ген кодирует белок, способный преобразовывать относительно нетоксичное пролекарство в токсичное лекарство. Например, фермент цитозиндеаминаза преобразует 5-фторцитозин (5FC) в 5-фторурацил (5FU) (Mullen et al. (1922) PNAS 89, 33); фермент тимидинкиназа вируса простого герпеса сенсибилизирует клетки к обработке антивирусным агентом ганцикловиром (GCV) или ацикловиром (Moolten (1986) Cancer Res. 46, 5276; Ezzedine et al. (1991) New Biol 3, 608). Можно использовать цитозиндеаминазу любого организма, например E. coli или Saccharomyces cerevisiae.
Таким образом, в более предпочтительной форме осуществления изобретения ген кодирует белок, обладающий активностью цитозиндеаминазы, и даже более предпочтительно белок, который описан в патентных заявках WO 2005007857 и WO 9954481.
В следующей форме осуществления экзогенный ген кодирует рибозим, способный к расщеплению РНК- или ДНК-мишени. РНК- или ДНК-мишени, которые нужно расщеплять, могут представлять собой РНК или ДНК, которые существенны для функции клетки, и их расщепление приводит в результате к клеточной гибели, РНК или ДНК, которые нужно расщеплять, могут представлять собой РНК или ДНК, которые кодируют нежелательный белок, например онкогенный продукт, и расщепление этой РНК или ДНК может предотвратить превращение клетки в канцерогенную.
Еще в одной следующей форме осуществления экзогенный ген кодирует антисмысловую РНК.
Под "антисмысловой РНК" авторы изобретения подразумевают молекулу РНК, которая гибридизуется с молекулой мРНК, кодирующей белок, или с другой молекулой РНК внутри клетки, такой как пре-мРНК или тРНК или рРНК, и препятствует ее экспрессии, либо гибридизуется с геном и препятствует его экспрессии.
В другой форме осуществления изобретения экзогенная последовательность замещает функцию дефектного гена в клетке-мишени. Существует несколько тысяч наследственных генетических заболеваний млекопитающих, включая людей, которые вызваны дефектными генами. Примеры таких генетических заболеваний включают муковисцидоз, где известно, что он представляет собой мутацию в гене CFTR; мышечную дистрофию Дюшенна, где известно, что он представляет собой мутацию в гене дистрофина; серповидно-клеточную анемию, где известно, что она представляет собой мутацию в гене НbА. Многие типы рака вызваны дефектными генами, в частности протоонкогенами и генами опухолевых супрессоров, которые претерпели мутацию.
Примерами протоонкогенов являются ras, src, bcl и т.д.; примерами генов опухолевых супрессоров являются р53 и Rb.
В следующей форме осуществления изобретения экзогенная последовательность кодирует опухолеассоциированный антиген (ТАА, Tumor Associated Antigen). ТАА относится к молекуле, которая обнаружена с более высокой частотой или плотностью в опухолевых клетках, чем в не опухолевых клетках такого же типа ткани. Примеры ТАА включают, но не ограничены ими, СЕА, MART-1, MAGE-1, MAGE-3, GP-100, MUC-1, MUC-2, точечно-мутированный онкоген ras, нормальный или точечно-мутированный р53, гиперэкспрессируемый р53, СА-125, PSA, C-erb/B2, BRCA I, BRCA II, PSMA, тирозиназу, TRP-1, TRP-2, NY-ESO-1, TAG72, KSA, HER-2/neu, bcr-abl, рах3-fkhr, ews-fli-1, сурвивин и LRP. Согласно более предпочтительной форме осуществления ТАА представляет собой MUC1.
Рекомбинантный вирус может включать более чем одну экзогенную последовательность, и каждая экзогенная последовательность может кодировать более чем одну молекулу. Например, может быть полезным сочетать в одном и том же рекомбинантном поксвирусе экзогенную последовательность, кодирующую ТАА, с экзогенной последовательностью, кодирующей цитокин.
В другой форме осуществления изобретения экзогенный ген кодирует антиген. Как используют здесь, "антиген" относится к лиганду, который может связываться антителом; сам антиген необязательно должен быть иммуногенным.
Предпочтительно антиген имеет происхождение от вируса, такого как, например, ВИЧ-1 (такой как gp 120 или gp 160), любой из вирусов иммунодефицита кошачьих, вирусы герпеса человека или животного, такие как gD или его производные, или немедленно-ранний белок, такой как ICP27, из HSV1 или HSV2, цитомегаловирус (такой как gB или его производные), вирус опоясывающего лишая (такой как gpI, II или III), либо от вируса гепатита, такого как вирус гепатита В, например, поверхностный антиген вируса гепатита В или его производное, вирус гепатита А, вирус гепатита С (преимущественно неструктурный белок из генотипа 1b штамма ja) и вирус гепатита Е, либо от других вирусных патогенов, таких как респираторно-синцитиальный вирус, папилломавирус человека (преимущественно белок Е6 и Е7 из штамма HPV16) или вирус гриппа, либо имеет происхождение от бактериальных патогенов, таких как Salmonella, Neisseria, Borrelia (например, OspA или OspB или их производные), либо Chlamydia, либо Bordetella, например, Р.69, РТ и FHA, либо имеет происхождение от паразитов, таких как плазмодий или токсоплазма.
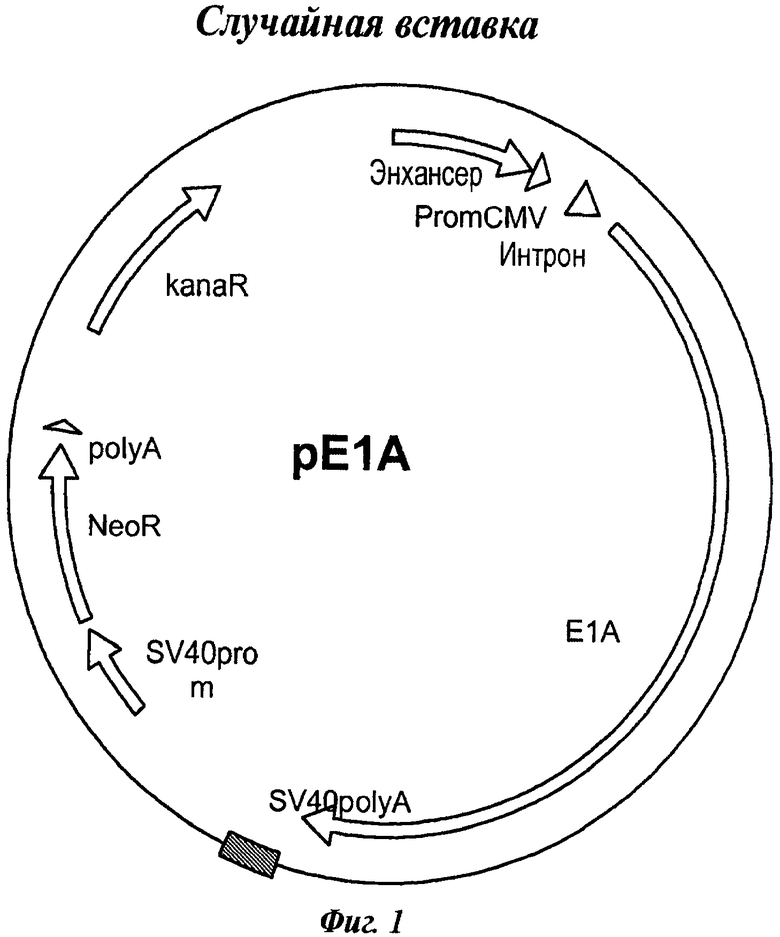
Фиг.1. Вектор, включающий ген, кодирующий нуклеиново-кислотную последовательность Е1А.
Фиг.2. Схематическое представление сайт-специфической инсерции нуклеиново-кислотной последовательности Е1А в ген HPRT.
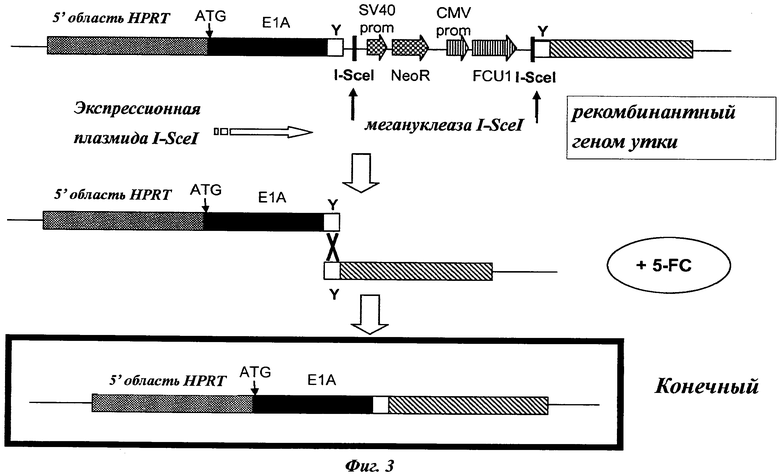
Фиг.3. Схематическое представление элиминации первого и третьего селективного маркера из генома иммортализованной клетки, полученной способом по изобретению.
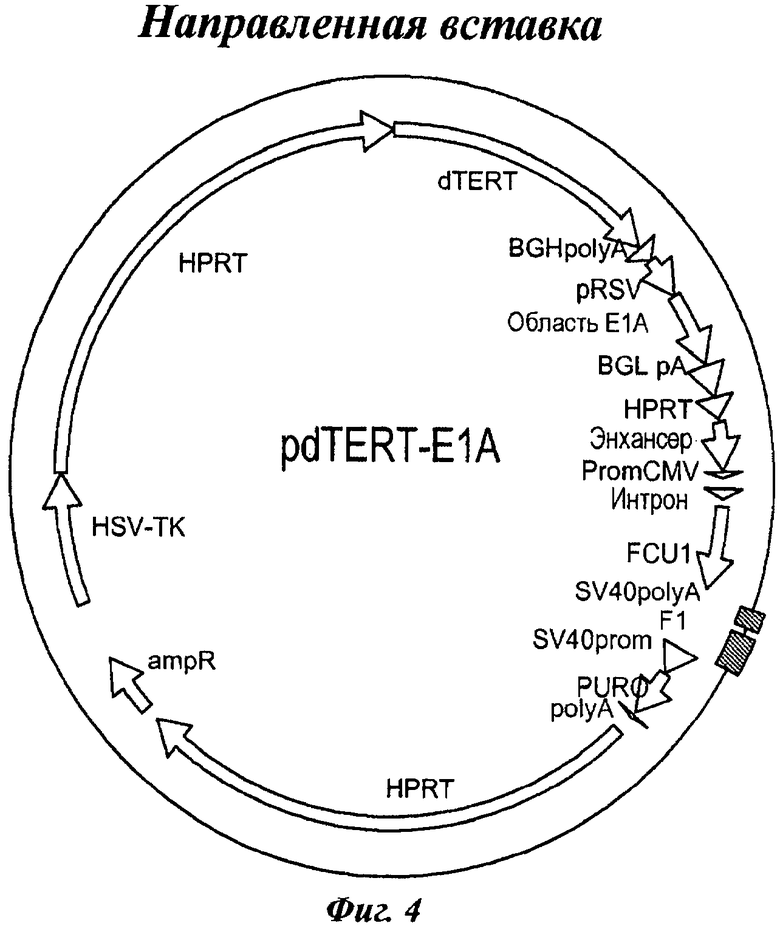
Фиг.4. Вектор, включающий ген, кодирующий обратную транскриптазу теломеразы Cairina moschata и нуклеиново-кислотную последовательность Е1А.
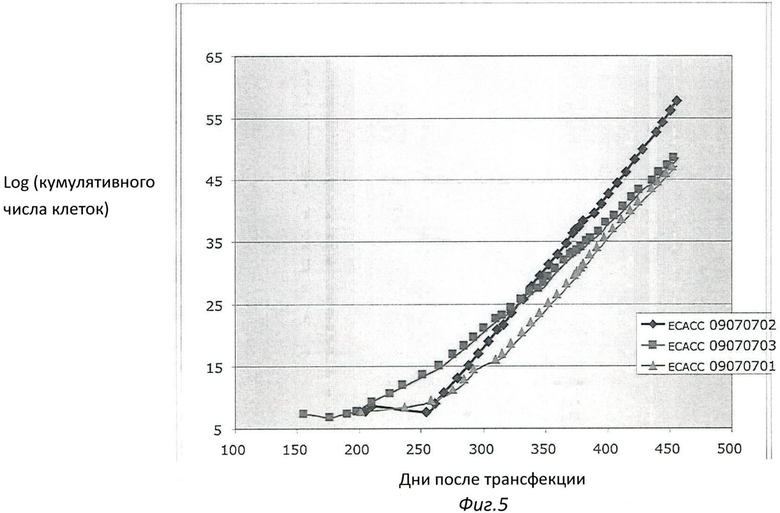
Фиг.5. Кривая роста иммортализованной клеточной линии Cairina moschata ЕСАСС 09070701, ЕСАСС 09070702 и ЕСАСС 09070703.
Фиг.6. Визуализация иммортализованной клеточной линии Cairina moschata ЕСАСС 09070701 световой микроскопией (пассаж 21).
Фиг.7. Визуализация иммортализованной клеточной линии Cairina moschata ЕСАСС 09070702 световой микроскопией (пассаж 24).
Фиг.8. Визуализация иммортализованной клеточной линии Cairina moschata ЕСАСС 09070703 световой микроскопией (пассаж 28).
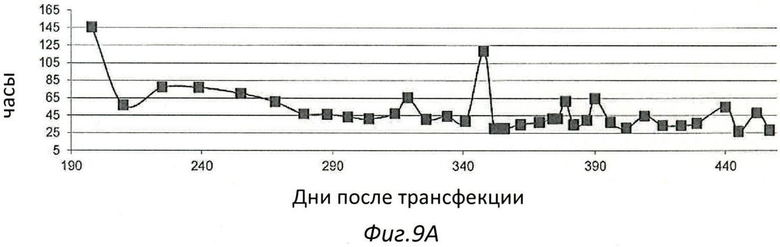
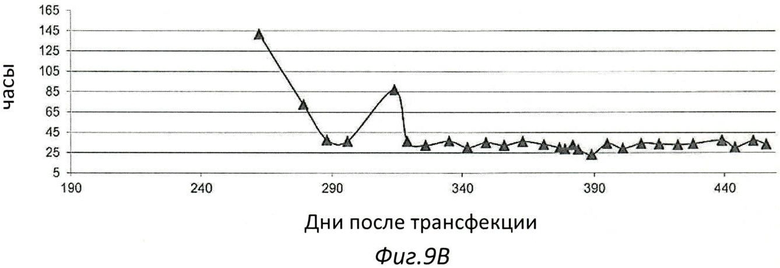
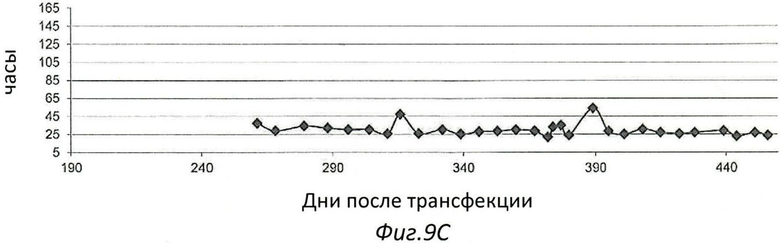
Фиг.9. Развитие времени удвоения популяции иммортализованной клеточной линии Cairina moschata ЕСАСС 09070703 (Фиг.9А), ЕСАСС 09070701 (Фиг.9В) и ЕСАСС 09070702 (Фиг.9С).
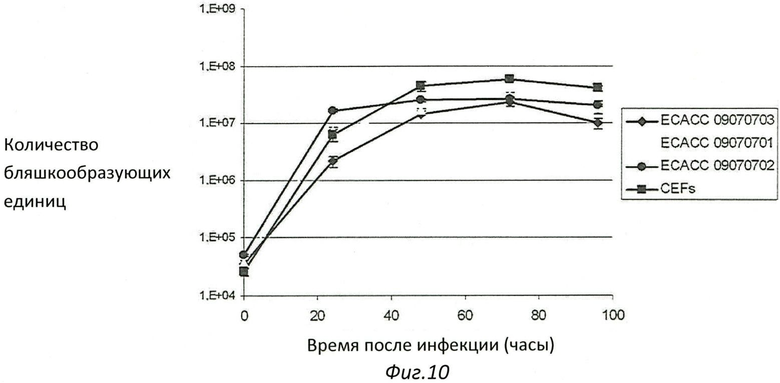
Фиг.10. Продуцирование модифицированного вируса вакцинии Анкара (MVA) в иммортализованной клеточной линии Cairina moschata ЕСАСС 09070701, ЕСАСС 09070702 и ЕСАСС 09070703 (MOI 0,05).
Примеры
Пример 1. Основание иммортализованной клеточной линии птиц, содержащей нуклеиново-кислотную последовательность Е1А
А. Плазмидные конструкции
А-1. Плазмидные конструкции для случайной вставки
С этой целью использовали плазмиду, не имеющую специфичной общей последовательности гомологии с геномом Cairina moschata (плазмиду Е1А) (фиг.1).
А-2. Плазмидные конструкции для направленной вставки
Сконструирована плазмида, содержащая 5 кб фрагменты, гомологичные гену HPRT Cairina moschata, окружающие нуклеиново-кислотную последовательность Е1А (SEQ ID №:1), и два селективных маркера. Ген HPRT, кодирующий гипоксантингуанинфосфорибозилтрансферазу, выбран в качестве адекватного сайта для конститутивной экспрессии нуклеиново-кислотной последовательности Е1А.
Эти два селективных маркера представляют собой ген FCU1 (Erbs et al. Cancer Res. 2000, 15, 60:3813-22) под контролем промотора CMV (Thomsen et al. PNAS 1984, 81, 3:659-63) и ген устойчивости к неомицину (или пуромицину), помещенный под контролем промотора SV40. Экспрессионные кассеты устойчивости к неомицину (или пуромицину) и FCU-1 окружены сайтами расщепления Sce1, которые дают возможность элиминации селективных кассет из конечной клеточной линии. Снаружи от плеч гена HPRT встроен селективный маркер, кодирующий HSVTK, направляемый промотором RSV (фиг.2).
Б. Получение партии СЕС из яиц Cairina moschata и описание субпопуляций
Б.1 Получение партии СЕС из 12-суточный яиц Cairina moschata и описание субпопуляций
25 оплодотворенных яиц SPF инкубируют при 37,5°C. Яйца вскрывают после12 суток инкубации, следуя доступному протоколу.
23 эмбрионов измельчают, промывают один раз фосфатно-солевым буферным раствором Дульбекко (ФСБ) и диссоциируют в TrypLE Select (Invitrogen) 5 часов при комнатной температуре.
После низкоскоростного центрифугирования клетки ресуспендируют в базовой среде Игла (БСИ) с добавлением 10% фетальной сыворотки теленка (ФСТ), гентамицина 0,04 г/л, высевают в 500 см2 тройные флаконы и инкубируют при 37°C 5% CO2.
После 24 ч конфлюентные клетки извлекали из флаконов, используя TrypLE Select (5 мл/тройной флакон), часть клеток повторно высевали в 175 см2 флаконы для второго пассажа. Остальные клетки концентрировали при 107 клеток/мл в соответствующей среде (60% БСИ, 30% ФСТ и 10% ДМСО) и замораживали в контейнере, регулируемом изопропиловым спиртом (контейнер для замораживания NALGENE® "Mr. Frosty" 1°C) при -80°C, после чего переносили в жидкий азот для длительного хранения, составляя банк исходных клеток (50×1,5×107 клеток/флакон, 44×1×107 клеток/флакон).
Проводят пассаж клеток, оставшихся в культуре, классически вплоть до 18 пассажей, в течение 3 первых пассажей неприкрепленные клетки собирают низкоскоростным центрифугированием кондиционированной среды, повторно высевают и проводят следующий пассаж таким же путем, как исходную культуру.
Субпопуляции, проявляющие характерные отличительные морфологические признаки, воспроизводимо выделили в течение продолжительности жизни культуры.
Б.2. Получение партии СЕС из 19-суточных яиц Cairina moschata и описание субпопуляций
29 оплодотворенных яиц SPF Cairina moschata, полученных из AFFSSA Ploufragan, инкубируют при 37,5°C во влажной атмосфере.
Яйца вскрывают после 19 суток, и эмбрионы стерильно экстрагируют. 20 эмбрионов обезглавливают, конечности удаляют, а печень используют для получения других клеток. Туловища эмбрионов измельчают, промывают один раз в ФСБ Дульбекко (Sigma, кат. №D8537, партия 46K2428) и диссоциируют в 500 мл TrypLE Select (Gibco, кат. №12563, партия 1319986 и 1339844) 2 часа при 37°C.
После 5 минут центрифугирования при 2000 об/мин клетки ресуспендируют в БСИ (базовой среде Игла, Gibco, кат. №41010, партия 8270) с добавлением 10% фетальной сыворотки теленка (JRH, кат. №12003-1000М, партия 5А0102, код TG P4001Q), гентамицина 0,04 г/л и L-глутамина 4 мМ. Конечный объем 1,5 л (1,9×106 клеток/мл) суспензии высевают в 10 тройных флаконов (500 см2) и инкубируют при 37°C 5% CO2.
После 24 ч конфлюентные клетки промывают ФСБ и извлекают из флаконов, используя TrypLE Select. Клетки считают и центрифугируют 4-5 минут при 2000 об/мин. Осадок концентрируют при 5×106 или 107 клеток/мл в подходящей среде (60% БСИ, 30% ФСТ и 10% ДМСО). Суспензию заполняют в криофлаконы (Nunc) и замораживают при -80°C с промежуточной 2 ч стадией при -20°C, после чего переносят в жидкий азот для длительного хранения, составляя банк первичных клеток (110 криофлаконов, 107 клеток/флакон) СЕТС19р1 (эмбриональные клетки туловища утки, 19-суточные эмбрионы, пассаж 1).
В предпочтительной форме осуществления настоящего изобретения получение партии СЕС из яиц Cairina moschata проводят в соответствии с альтернативой Б.2. (из 19-суточных яиц Cairina moschata).
В. Способы трансфекции
В данной области техники известно большое число способов трансфекции для введения вектора, способного направлять экспрессию интересующей нуклеотидной последовательности. Неограничивающий перечень этих способов перечислен здесь ниже: преципитация CaPO4, электропорация, липофектиновый способ трансфекции. Данный пример основан на методике преципитации CaPO4.
Конфлюентность клеток должна составлять примерно 80-50%. Среду заменяют за два часа до добавления CaPO4/ДНК. 30 мкг ДНК ресуспендируют в 31 мкл 2 М CaCl2 - 161,3 мМ Трис pH 7,6. H2O добавляют до конечного объема 0,5 мл.
Затем 2 альтернативы:
а) Для трансфекции 0,5 мл 2× HEBS распределяют в 15 мл стерильной пробирке Falcon и добавляют по каплям раствор ДНК при мягком перемешивании на вортексе или барботирования раствора ДНК. Раствор должен приобрести молочный цвет. Смесь оставляют стоять при комнатной температуре на 10-30 мин. Затем стерильной пипеткой раствор пипетируют один раз внутрь и наружу в боксе для тканевых культур, чтобы разбить хлопья, и наносят по каплям на клетки. Затем клетки инкубируют между 6 часами и ночью при 37°C. Мелкий осадок должен покрывать поверхность клеток. С целью завершения процедуры трансфекции нагревают до 37°C концентрированный раствор глицерина. Среду отсасывают, добавляют 5 мл БСИ для промывания слоя клеток, затем среду отсасывают и добавляют 1 мл концентрированного раствора глицерина на 2 мин или менее. Затем осторожно добавляют 10 мл БСИ для разбавления глицерина и БСИ-глицерин полностью удаляют. Затем добавляют 10 мл желаемой среды, и чашки инкубируют при подходящей температуре.
или
б) Для трансфекции 0,5 мл 2× HEBS распределяют в 15 мл стерильной пробирке Falcon и добавляют по каплям раствор ДНК при мягком перемешивании на вортексе или барботирования раствора ДНК. Раствор должен приобрести молочный цвет. Смесь оставляют стоять при комнатной температуре на 10-30 мин. Затем стерильной пипеткой раствор пипетируют один раз внутрь и наружу в боксе для тканевых культур, чтобы разбить хлопья, и наносят по каплям на клетки. Затем клетки инкубируют между 6 часами и ночью при 37°C.
В предпочтительной форме осуществления настоящего изобретения трансфекцию (преципитацию CaPO4) проводят согласно альтернативе б).
Г. Способы отбора
Г-1. Способ отбора на случайную вставку
Давление отбора применяют от 48 до 72 часов спустя после трансфекции: клетки диссоциируют TrypLE Select, центрифугируют при низкой скорости и повторно высевают в БСИ с ФСТ 10% и G418 800 мкг/мл, предпочтительно 500 мкг/мл (и необязательно с ганцикловиром 25 мкг/мл, предпочтительно 10 мкг/мл).
Проводят серийные пассажи клеток до возможности выделения индивидуально растущих клонов.
Г-2. Способ отбора на направленную вставку
Давление отбора применяют от 48 до 72 часов спустя после трансфекции: клетки диссоциируют TrypLE Select, центрифугируют при низкой скорости и повторно высевают в БСИ с ФСТ 10%; ганцикловиром 25 мкг/мл, предпочтительно 10 мкг/мл; и G418 800 мкг/мл, предпочтительно 500 мкг/мл (или пуромицином 0,5 мкг/мл).
Проводят серийные пассажи клеток до возможности выделения индивидуально растущих клонов.
Затем клетки трансфицируют экспрессионной плазмидой мегануклеазы I-Scel, следуя способу, описанному ниже.
Для отбора элиминации селективных маркеров 5-фторцитозин (5-FC) наносят через 48 часов после трансфекции: клетки диссоциируют TrypLE Select, центрифугируют при низкой скорости и повторно высевают в среду с 5-FC в интервале концентрации от 10-3 до 10-7 М и поддерживают селекцию G418 (или пуромицином)/ганцикловиром (БСИ с ФСТ 10%; 5-FC; ганцикловиром 25 мкг/мл, предпочтительно 10 мкг/мл; и G418 800 мкг/мл, предпочтительно 500 мкг/мл (или пуромицином 0,5 мкг/мл) (фиг.3).
Пример 2. Основание иммортализованной клеточной линии птиц, содержащей нуклеиново-кислотную последовательность Е1А и нуклеиново-кислотную последовательность рекомбинантной обратной транскриптазы теломеразы
А. Плазмидные конструкции
А-1. Плазмидные конструкции для случайной вставки
С этой целью использовали плазмиду, не имеющую специфичной общей последовательности гомологии с геномом Cairina moschata.
А-2. Плазмидные конструкции для направленной вставки
Сконструирована плазмида (плазмида dTERT-E1A), включающая 5 кб фрагменты, гомологичные гену HPRT Cairina moschata, окружающие ген обратной транскриптазы теломеразы Cairina moschata (SEQ ID №:3), нуклеиново-кислотную последовательность Е1А (SEQ ID №:1) и два селективных маркера. Ген HPRT, кодирующий гипоксантингуанинфосфорибозилтрансферазу, выбран в качестве адекватного сайта для конститутивной экспрессии нуклеиново-кислотной последовательности Е1А.
Эта два селективных маркера представляют собой ген FCU1 (Erbs et al. Cancer Res. 2000, 15, 60:3813-22) под контролем промотора CMV (Thomsen et al. PNAS, 1984, 81, 3:659-63) и ген устойчивости к пуромицину, помещенный под контролем промотора SV40. Экспрессионные кассеты устойчивости к пуромицину и FCU-1 окружены сайтами расщепления Sce1, который дает возможность элиминации селективных кассет из конечной клеточной линии. Снаружи от плеч гена HPRT встроен селективный маркер, кодирующий HSVTK, направляемый промотором RSV (фиг.4).
Б. Получение партии СЕС из 19-суточных яиц Cairina moschata и описание субпопуляций
29 оплодотворенных яиц SPF Cairina moschata, полученных из AFFSSA Ploufragan, инкубируют при 37,5°C во влажной атмосфере.
Яйца вскрывают после 19 суток, и эмбрионы стерильно экстрагируют. 20 эмбрионов обезглавливают, конечности удаляют, а печень используют для получения других клеток. Туловища эмбрионов измельчают, промывают один раз в ФСБ Дульбекко (Sigma, кат. № D8537, партия 46K2428) и диссоциируют в 500 мл TrypLE Select (Gibco, кат. №12563, партия 1319986 и 1339844) 2 часа при 37°C.
После 5 минут центрифугирования при 2000 об/мин клетки ресуспендируют в БСИ (базовой среде Игла, Gibco, кат. №41010, партия 8270) с добавлением 10% фетальной сыворотки теленка (JRH, кат. №12003-1000М, партия 5А0102, код TG P4001Q), гентамицина 0,04 г/л и L-глутамина 4 мМ. Конечный объем 1,5 л (1,9×106 клеток/мл) суспензии высевают в 10 тройных флаконов (500 см2) и инкубируют при 37°C 5% CO2.
После 24 ч конфлюентные клетки промывают ФСБ и извлекают из флаконов, используя TrypLE Select. Клетки считают и центрифугируют 4-5 минут при 2000 об/мин. Осадок концентрируют при 5×106 или 107 клеток/мл в подходящей среде (60% БСИ, 30% ФСТ и 10% ДМСО). Суспензию заполняют в криофлаконы (Nunc) и замораживают при -80°C с промежуточной 2 ч стадией при -20°C, после чего переносят в жидкий азот для длительного хранения, составляя банк первичных клеток (110 криофлаконов, 107 клеток/флакон) СЕТС19р1 (эмбриональные клетки туловища утки, 19-суточные эмбрионы, пассаж 1).
В. Способы трансфекции
В данной области техники известно большое число способов трансфекции для введения вектора, способного направлять экспрессию интересующей нуклеотидной последовательности. Не ограничивающий перечень этих способов перечислен здесь ниже: преципитация CaPO4, электропорация, липофектиновый способ трансфекции. Данный пример основан на электропорации.
Трансфекцию проводят, используя устройство Amaxa's Nucleofector и набор Basic Fibroblast (Amaxa, кат. № VPI-1002). Клетки центрифугируют в течение 10 мин при 700 об/мин (100 г) и ресуспендируют в растворе Basic Nucleofector Solution (100 мкл на 106 клеток); 100 мкл суспензии смешивают с 3-6 мкг ДНК и переносят в кювету, помещенную в Nucleofector (программа U-12). После электропорации образец переносят в 6 см культуральную чашку, заполненную 5 мл культуральной среды, предварительно уравновешенной в инкубаторе при 37°C/5% CO2. После инкубации в течение ночи 37°C 5% CO2 культуральную среду обновляют, и продолжают инкубацию.
Г. Способы отбора
Г-1. Способ отбора на случайную вставку
Давление отбора применяют от 48 до 72 часов спустя после трансфекции: клетки диссоциируют TrypLE Select, центрифугируют при низкой скорости и повторно высевают в БСИ с ФСТ 10% и G418800 мкг/мл, предпочтительно 500 мкг/мл (и необязательно с ганцикловиром 25 мкг/мл, предпочтительно 10 мкг/мл).
Проводят серийные пассажи клеток до возможности выделения индивидуально растущих клонов.
Г-2. Способ отбора на направленную вставку
Давление отбора применяют от 48 до 72 часов спустя после трансфекции: клетки диссоциируют TrypLE Select, центрифугируют при низкой скорости и повторно высевают в БСИ с ФСТ 10%; ганцикловиром 25 мкг/мл, предпочтительно 10 мкг/мл; и пуромицином 0,5 мкг/мл.
Проводят серийные пассажи клеток до возможности выделения индивидуально растущих клонов.
Затем клетки трансфицируют экспрессионной плазмидой мегануклеазы I-Scel, следуя способу, описанному ниже.
Для отбора элиминации селективных маркеров 5-фторцитозин (5-FC) наносят через 48 часов после трансфекции: клетки диссоциируют TrypLE Select, центрифугируют при низкой скорости и повторно высевают в среду с 5-FC в интервале концентрации от 10-3 до 10-7 М и поддерживают пуромицином/ганцикловиром (БСИ с ФСТ 10%; 5-FC; ганцикловиром 25 мкг/мл, предпочтительно 10 мкг/мл; и пуромицином 0,5 мкг/мл).
Пример 3: Иммортализованные клеточные линии Cairina moschata ECACC 09070701, ECACC 09070702 и ECACC 09070703.
Клеточные линии Cairina moschata ECACC 09070701 (T17-17703В), ECACC 09070702 (T17-17703B2) и ECACC 09070703 (T17-17703A) были получены из первичных эмбриональных клеток Cairina moschata, как описано в Примере 2, путем направленной вставки (электропорацией) с помощью плазмиды dTERT-E1A.
Клеточные линии выращивали от 210 до 260 дней после трансфекции, после фазы старения/кризиса в виде субпопуляций ECACC 09070701, ECACC 09070702 и ECACC 09070703 была начата новая непрерывная экспоненциальная фаза роста. Соответствующие кривые роста (Фиг.1) показывают эволюцию популяции до 456-го дня после трансфекции. Число удвоений популяции (PDL), рассчитанное за этот период (ECACC 09070703: 138 PDL; ECACC 09070701: 131 PDL; ECACC 09070702: 166 PDL), далеко превосходило предел Хайфлика (Hayflick). На основании этого клеточные линии Cairina moschata ECACC 09070701 (T17-17703В), ECACC 09070702 (T17-17703B2) и ECACC 09070703 (T17-17703A) определили как иммортализованные клеточные линии. Клетки этих трех линий являются мелкими клетками, растущими в стабильном статическом монослое (см. Фиг.6, 7 и 8).
Эти три линии Cairina moschata также демонстрируют разное время генерации. Среднее время удвоения популяции (PDT) составляет 30 часов для ECACC 09070702, 35 часов для ECACC 09070701 и 47 часов для ECACC 09070703 (Фиг.9).
- Уровень удвоения популяции (PDL) - это число клеточных генераций (2-кратное увеличение биомассы). Расчет PDL с: PDL = Ln(конечное/начальное число клеток)/Ln(2);
- Время удвоения популяции (PDT), также называемое временем генерации, - это время, необходимое для удвоения одной популяции. Расчет PDT: PDT=Δt*Ln(2)/Ln(конечное/начальное число клеток).
Пример 4. Получение модифицированного вируса вакцинии Ankara (MVA) с использованием иммортализованных клеточных линий Cairina moschata ECACC 09070701, ECACC 09070702 и ECACC 09070703.
Амплификационные возможности для MVA иммортализованных клеточных линий Cairina moschata ECACC 09070701, ECACC 09070702 и ECACC 09070703 оценивали далее и сравнивали с первичными куриными эмбриональными фибробластами (CEFs), которые обычно используют как субстрат для продуцирования MVA. Чтобы облегчить завершение размножения вирусов и титрование был выбран MVA (депонированный в CNCM под номером №602 1-721), экспрессирующий GFP. Иммортализованные клеточные линии Cairina moschata ECACC 09070701, ECACC 09070702, ECACC 09070703 и CEFs высевали на 2·106 клеток в Т-колбы на 25 см2 и культивировали в течение 24 ч во влажной атмосфере при 37°C, 5% CO2. Затем удаляли культуральную среду (Basal Medium Eagle (BME), дополненную 10% фетальной телячьей сыворотки (FCS) и 4 мМ L-глутамина), и клетки инфицировали при MOI 0.05 с помощью 500 мкл вируса MVA, разведенного в PBS 1% катионов, 1% FCS. После 30 минут стадии адсорбции оставшуюся суспензию вирусов удаляли, клетки промывали однократно PBS и затем добавляли 5 мл BME 10% FCS в каждую колбу. Затем добавляли свежую культуральную среду и клетки помещали в инкубатор. Вирус выделяли замораживанием-оттаиванием из клеток и супернатанта через 0, 24, 48, 72 и 96 часов инфекции при 37°C, 5% CO2. Выделенную вирусную суспензию обрабатывали ультразвуком перед титрованием, чтобы разбить агрегаты. Титрование осуществляли в трех повторах на CEF, засеянных в 6 см культуральных чашках, инфицированных логарифмическими разведениями вируса и покрытых агаром. Бляшкообразующие единицы MVA, экспрессиирующие GFP, визуализировали с помощью флуоресцентного бинокуляра и подсчитывали через 72 часа.
Как показано на Фиг.10, иммортализованные клеточные линии Cairina moschata ECACC 09070701, ЕСАСС 09070702 и ЕСАСС 09070703 были пермиссивными к MVA и обеспечивали амплификацию MVA, сравнимую с той, которая имеет место на классическом субстрате CEF. Для всех протестированных клеточных линий максимальный выход вируса был достигнут через 72 часа после инфекции и составлял от 2,3·107 до 5,7·107 бляшкообразующих единиц всего. Соответственно, во всех клетках наблюдался ясный цитопатический эффект (данные не представлены).


































Изобретения относятся к области генетической инженерии, в частности к иммортализованным эмбриональным клеткам птиц. Иммортализованная эмбриональная клетка птиц или клетки, имеющие происхождение от нее, содержит нуклеиново-кислотную последовательность Е1А для репликации вируса или для продуцирования целевого вещества или вируса. Иммортализованную эмбриональную клетку получают способом, включающим стадию трансфекции этой клетки невирусным вектором, содержащим указанную нуклеиново-кислотную последовательность Е1А и нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы. Причем клетки, имеющие происхождение от указанной клетки, представляют собой клетки, которые развиваются или дифференцируются из нее или имеют ее в качестве предка. Клетки согласно изобретению, в частности, полезны для продуцирования рекомбинантных вирусных векторов. 7 н. и 30 з.п. ф-лы, 10 ил., 4 пр.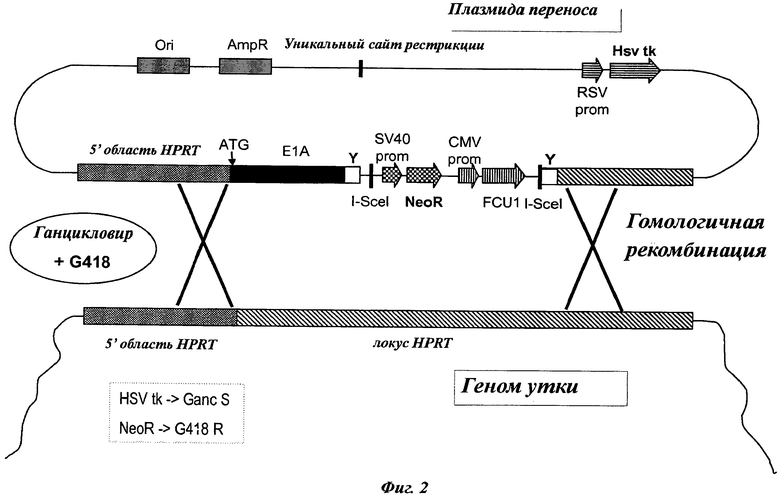
1. Иммортализованная эмбриональная клетка птиц или клетки, имеющие происхождение от нее, содержащая нуклеиново-кислотную последовательность Е1А, для репликации вируса или для продуцирования целевого вещества или вируса, характеризующаяся тем, что указанная клетка получена способом, включающим стадию трансфекции этой клетки невирусным вектором, содержащим указанную нуклеиново-кислотную последовательность Е1А и нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы, причем клетки, имеющие происхождение от указанной клетки, представляют собой клетки, которые развиваются или дифференцируются из нее или имеют ее в качестве предка.
2. Иммортализованная клетка по п.1, где указанная нуклеиново-кислотная последовательность Е1А встроена в эндогенный ген HPRT указанной клетки птиц.
3. Иммортализованная клетка по п.2, где нуклеиново-кислотная последовательность Е1А оперативно сцеплена с эндогенным промотором HPRT указанной клетки.
4. Иммортализованная клетка по п.1, где указанная нуклеиново-кислотная последовательность Е1А включает последовательность, кодирующую две основных РНК 13S и 12S.
5. Иммортализованная клетка по п.1, где указанная клетка имеет происхождение от животного, принадлежащего к семейству Anatidae.
6. Иммортализованная клетка по п.5, где указанное животное принадлежит к виду Cairina moschata.
7. Иммортализованная клетка по п.5, где указанное животное принадлежит к виду Anas platyrhynchos.
8. Иммортализованная клетка по п.1, где указанная нуклеиново-кислотная последовательность Е1А является такой, как приведено в SEQ ID №:1.
9. Иммортализованная клетка по п.1, где указанная нуклеиново-кислотная последовательность, кодирующая рекомбинантную обратную транскриптазу теломеразы, имеет по меньшей мере 95% идентичности нуклеиново-кислотной последовательности с SEQ ID №:3.
10. Иммортализованная клетка по п.1, где указанная нуклеиново-кислотная последовательность, кодирующая рекомбинантную обратную транскриптазу теломеразы, является такой, как приведено в SEQ ID №:3.
11. Иммортализованная эмбриональная клетка птиц или клетки, имеющие происхождение от нее, содержащая нуклеиново-кислотную последовательность Е1А, для репликации вируса или для продуцирования целевого вещества или вируса, характеризующаяся тем, что указанная клетка получена способом, включающим стадию трансфекции этой клетки невирусным вектором, содержащим указанную нуклеиново-кислотную последовательность Е1А и нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы, причем указанная клетка также содержит нуклеиново-кислотную последовательность, кодирующую целевое вещество, причем клетки, имеющие происхождение от указанной клетки, представляют собой клетки, которые развиваются или дифференцируются из нее или имеют ее в качестве предка.
12. Иммортализованная клетка по п.11, где указанное целевое вещество представляет собой фармацевтически активный белок.
13. Иммортализованная эмбриональная клетка птиц или клетки, имеющие происхождение от нее, содержащая нуклеиново-кислотную последовательность Е1А, для репликации вируса или для продуцирования целевого вещества или вируса, характеризующаяся тем, что указанная клетка получена способом, включающим стадию трансфекции этой клетки невирусным вектором, содержащим указанную нуклеиново-кислотную последовательность Е1А и нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы, причем указанная клетка также содержит кассету комплементации, дающую возможность размножения дефектного вируса, причем клетки, имеющие происхождение от указанной клетки, представляют собой клетки, которые развиваются или дифференцируются из нее или имеют ее в качестве предка.
14. Применение иммортализованной клетки по любому из пп.1-13 для репликации вируса.
15. Применение по п.14, где указанный вирус выбран из группы, состоящей из вируса коровьей оспы, вируса эктромелии (оспы мышей), вируса оспы обезьян, вируса осповакцины, вируса оспы и MVA.
16. Применение иммортализованной клетки по любому из пп.1-13 для продуцирования целевого вещества.
17. Применение иммортализованной клетки по любому из пп.1-13 для продуцирования вируса.
18. Применение по п.17, где вирус представляет собой поксвирус.
19. Применение по п.18, где вирус представляет собой вирус осповакцины.
20. Применение по п.19, где вирус осповакцины представляет собой MVA.
21. Применение по п.17, где указанный вирус представляет собой рекомбинантный вирус.
22. Способ иммортализации эмбриональной клетки птиц, включающий стадию трансфекции клетки невирусным вектором, включающим нуклеиново-кислотную последовательность Е1А и нуклеиново-кислотную последовательность, кодирующую рекомбинантную обратную транскриптазу теломеразы.
23. Способ по п.22, где вектор включает две последовательности, гомологичные последовательностям, присутствующим в геноме указанной клетки.
24. Способ по п.23, где нуклеиново-кислотная последовательность Е1А окружена указанными гомологичными последовательностями.
25. Способ по п.23, где указанный вектор дополнительно включает первый селективный маркер, где первый селективный маркер представляет собой положительный селективный маркер, и где первый селективный маркер окружен указанными гомологичными последовательностями.
26. Способ по п.25, где первый селективный маркер окружен последовательностями, дающими возможность его супрессии.
27. Способ по п.25, где указанный вектор включает второй селективный маркер, который не окружен указанными гомологичными последовательностями, где указанный селективный маркер представляет собой отрицательный селективный маркер.
28. Способ по п.27, где указанный вектор включает третий селективный маркер, где указанный третий селективный маркер представляет собой отрицательный селективный маркер, и где указанный третий селективный маркер локализован между последовательностями, дающими возможность супрессии первого селективного маркера.
29. Способ по п.25, характеризующийся тем, что он дополнительно включает стадию, на которой указанные клетки культивируют в среде, которая дает возможность роста только клеток, в которые встроен первый селективный маркер.
30. Способ по п.27, характеризующийся тем, что он дополнительно включает стадию, на которой указанные клетки культивируют в среде, которая не дает возможности роста клеток, в которые встроен второй селективный маркер.
31. Способ по п.28, где указанный способ дополнительно включает стадию, состоящую в исключении первого селективного маркера из генома клетки.
32. Способ по п.31, где клетки, полученные после стадии, состоящей в исключении первого селективного маркера из генома указанных клеток, культивируют в среде, которая не дает возможности роста клеток, содержащих третий селективный маркер.
33. Способ по п.22, где указанная клетка взята от организма, принадлежащего к семейству Anatidae.
34. Способ по п.33, где указанный организм принадлежит к виду Cairina moschata.
35. Способ по п.33, где указанный организм принадлежит к виду Anas platyrhynchos.
36. Способ по п.22, где указанная нуклеиново-кислотная последовательность Е1А встроена в последовательность ДНК-мишени указанной клетки.
37. Способ по п.36, где указанная последовательность ДНК-мишени представляет собой ген HPRT.
| ОКУЛЯР | 1926 |
|
SU6136A1 |
| WO 2005042728, 12.05.2005 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
Авторы
Даты
2013-02-20—Публикация
2008-07-02—Подача