Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса пиридо[2′,3′:3,4]пиразоло[1,5-a] пиримидина и к способу их получения, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем.
Известны структурные аналоги заявленных соединений - 2,4-дизамещенные пиридо[2′,3′:3,4]пиразоло[1,5-a]пиримидины, получаемые кипячением
3-аминопиразоло [3,4-b] пиридина с 1,3-дикетонами (ацетилцетоном, бензоилацетоном, дибензоилметаном и 1,1,1-трифторпентан-2,4-дионом) в этаноле (Poreba К., Opolski A., Wietrzyk J., Kowalska М. // Arch. Pharm. Pharm. Med. Chem. 2001, 334(7), 219-223):

К недостаткам данного способа относится невозможность получения этил N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-a]пиримидин-4-карбоксамидов.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-a]пиримидин-4-карбоксамидов.
Поставленная задача осуществляется путем взаимодействия 1-арил-4,5-диароил-1H-пиррол-2,3-дионов (Ia-з) с 3-амино-4,6-диметил-2H-пиразоло[3,4-b]пиридином (II) в среде инертного апротонного растворителя по следующей схеме:
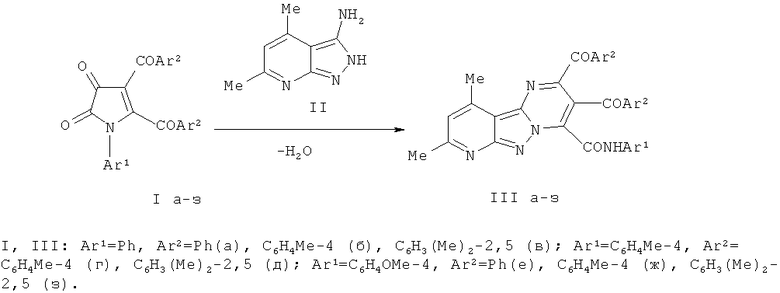
Процесс ведут при температуре 108-110°C, а в качестве растворителя используют абсолютный толуол.
Из патентной и технической литературы не были выявлены способы получения N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-a]пиримидин-4-карбоксамидов, имеющие сходные признаки с заявляемым способом, а именно не использовались исходные продукты, растворитель, в котором проходит реакция, и интервал температур, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 8,10-Диметил-N(4-толил)-2,3-ди(4-толуоил)пиридо[2′,3′:3,4]пиразоло[1,5-a]пиримидин-4-карбоксамид (IIIг).
Раствор 1.0 ммоль 1-(4-толил)-4,5-ди(4-толуоил)-1H-пиррол-2,3-диона (I г) и 1.0 ммоль 3-амино-4,6-диметил-2H-пиразоло[3,4-b]пиридина (II) в 20 мл абсолютного толуола кипятили при Т-108°C в течение 3-х ч, охлаждали, образовавшийся осадок отфильтровывали. Выход 83%, т.пл. 267-268°C (из этилацетата). Соединение (IIIг) C35H29N5O3.
Найдено, %: C 74.00; H 5.11; N 12.30.
Вычислено, %: C 74.06; H 5.15; N 12.34.
Соединение (IIIг) - ярко-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в обычных органических растворителях, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIг), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний группы NH при 3176 см-1, амидной и двух кетонных карбонильных групп при 1684, 1664 и 1649 см-1.
В спектре ЯМР 1H соединения (IIIг), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствуют синглеты пяти метильных групп в области 2.28-2.81 м.д., и синглет группы NH при 11.36 м.д.
Пример 2. 2,3-Бис(2,5-диметилбензоил)-8,10-диметил-N-(4-толил)пиридо[2′,3′:3,4]пиразоло[1,5-a]пиримидин-4-карбоксамид (IIIд).
Раствор 1.0 ммоль 1-(4-толил)-4,5-бис(2,5-диметилбензоил)-1H-пиррол-2,3-диона (Iд) и 1.0 ммоль 3-амино-4,6-диметил-2H-пиразоло[3,4-b]пиридина (II) в 20 мл абсолютного толуола кипятили при Т-110°C в течение 4-х ч, охлаждали, образовавшийся осадок отфильтровывали. Выход 79%, т.пл. 215-216°C (из толуола). Соединение (IIIд) C37H33N5O3.
Найдено, %: C 74.64; H 5.54; N 11.78.
Вычислено, %: C 74.60; H 5.58; N 11.76.
Соединение (IIIд) - ярко-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в обычных органических растворителях, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIд), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний группы NH при 3188 см-1, амидной и двух кетонных карбонильных групп при 1689, 1673 и 1665 см-1.
В спектре ЯМР 1Н соединения (IIIг), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствуют синглеты семи метальных групп в области 2.12-2.70 м.д., и синглет группы NH при 11.20 м.д.
Соединения (IIIа-в, е-з) синтезировали аналогично.
Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить неописанные в литературе N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-а]пиримидин-4-карбоксамиды (IIIа-з) с хорошими выходами, которые могут найти применение в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств.
Пример 3. Фармакологическое исследование соединений (IIIа, г, д, ж) на наличие анальгетической активности.
Оценку анальгетических свойств соединений (IIIа, г, д, ж) изучали на беспородных мышах массой 18-22 грамм методом термического раздражения «горячая пластинка» по Эдди и Леймбах (Eddy N.B., Leimbarh D.J.-Pharmacol and Exper. Gher., 1953, 385-393). В качестве препарата сравнения использовали анальгин (М.Д. Машковский, «Лекарственные средства», т.1, стр.184, М., Медицина, 1978).
Проведенные исследования показали (см. табл.), что соединения (IIIа, г, д, ж) обладают анальгетической активностью.
Изобретение относится к новым N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-а]пиримидин-4-карбоксамидам формулы I, обладающим анальгетической активностью, и к способу их получения. В формуле I
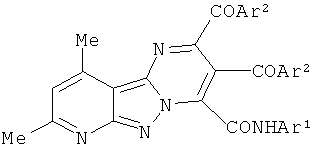
Ar1=Ph, C6H4Me-4, C6H4OMe-4; Ar2=Ph, C6H4Me-4, С6Н3(Ме)2-2,5. Способ получения указанных соединений заключается во взаимодействии 1-арил-4,5-диароил-1Н-пиррол-2,3-дионов с 3-амино-4,6-диметил-2Н-пиразоло[3,4-b]пиридином при температуре 108-110°С в среде абсолютного толуола. 2 н. и 2 з.п. ф-лы, 1 схема, 1 табл., 3 пр.
1. N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-а]пиримидин-4-карбоксамиды формулы
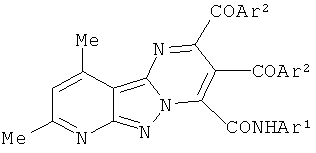
где Ar1 - Ph, C6H4Me-4, C6H4OMe-4; Ar2 - Ph, C6H4Me-4, С6Н3(Ме)2-2,5.
2. Способ получения N-арил-2,3-диароил-8,10-диметилпиридо[2′,3′:3,4]пиразоло[1,5-а]пиримидин-4-карбоксамидов общей формулы
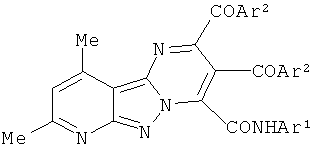
где Ar1 - Ph, C6H4Me-4, C6H4OMe-4; Ar2 - Ph, C6H4Me-4, С6Н3(Ме)2-2,5,
отличающийся тем, что 1-арил-4,5-диароил-1Н-пиррол-2,3-дионы подвергают взаимодействию с 3-амино-4,6-диметил-2Н-пиразоло[3,4-b]пиридином.
3. Способ по п.2, отличающийся тем, что процесс ведут при температуре 108-110°С.
4. Способ по п.2, отличающийся тем, что в качестве растворителя используют абсолютный толуол.
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛ 7-АРИЛКАРБАМОИЛ-6-БЕНЗОИЛ-2-МЕТИЛ-3-ФЕНИЛПИРАЗОЛО[1,5-a]ПИРИМИДИН-5-КАРБОКСИЛАТОВ | 2009 |
|
RU2421455C2 |
| ЕР 1505068 А1, 09.02.2005 | |||
| ЕР 1921079 А1, 14.05.2008 | |||
| G.H.ELGEMEIE et al, Studies on aminoazoles: synthesis of pyrazolo[1,5-a]pyrimidines and their aza derivatives, J | |||
| PRAKT | |||
| CHEM., 1989, 331(3), 466-474. | |||
Авторы
Даты
2013-04-10—Публикация
2012-02-07—Подача