ТЕХНИЧЕСКАЯ ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к сфере лекарственных препаратов, в частности к кристаллическим формам эсзопиклона и их составу, процессу приготовления и медицинскому применению.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Зопиклон, лекарственный препарат, используемый для лечения нарушения сна, был разработан компанией RHONE-PONLENC RORER PHARMACEUTICAL COMPANY LTD, ФРАНЦИЯ, в середине 80-х гг. прошлого столетия и запущен в серийное производство в более 80 странах, как, например, в странах Европы, под торговым названием ИМОВАН (IMOVANE®). Объем продаж данного лекарства достиг 160 миллионов долларов США в 1999 г., препарат использовался в Китае около 10 лет. В настоящее время существует множество производителей данного препарата, включая компании Shanghai Huashi Pharmaceutical Co., Ltd, Qilu Pharmaceutical Co., Ltd, и Guangdong Shunfeng Pharmaceutical Co., Ltd. Формула зопиклона представлена ниже:
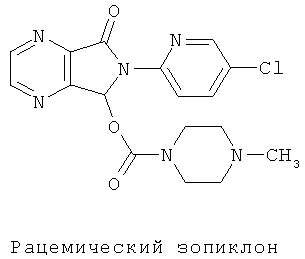
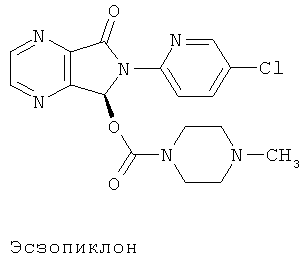
S-зопиклон (эсзопиклон) - один хиральный правовращающий мономер зопиклона с химическим названием: (+)-(3)-(4-метилпиперазин-1-карбоксилат)(6-(5-хлоропиридинил-2-ил)-7-карбонил-6,7-дигидро-5-Н-пирроло[3,4-b]пиразин-5-ил эфир). С 1998 г. препарат разрабатывался компанией Sepracor Inc., а в октябре 2004 г. был одобрен Управлением по контролю за качеством пищевых продуктов и лекарственных средств для продажи на рынке. Однако у рацемического зопиклона существует ряд тяжелых побочных эффектов, включая горький привкус во рту, вызванный выделением препарата в слюне, сухость во рту, сонливость, утренняя усталость, головная боль, головокружение и нарушение нейромоторных функций. По сравнению с рацемическим зопиклоном S-изомер имеет ряд преимуществ и меньшее количество побочных эффектов. Как показали фармакодинамические исследования, правовращающий энантиомер зопиклона значительно способствует его краткосрочному гипнотическому эффекту, таким образом оказывая лучшее влияние, чем рацемический зопиклон. Тем временем, было доказано, что S-зопиклон обладает значительно более низкой токсичностью, чем рацемический зопиклон, как показало сравнительное исследование острой токсичности. В отличие от рацемического зопиклона S-изомер может иметь антитревожный эффект без влияния на спортивную координацию. Было отмечено, что зопилкон является стереоселективным по отношению к рецептору бензодиазепина, при этом S-изомер обладает способностью связывания с рецептором бензодиазепина приблизительно в 50 раз выше, чем R-изомер.
Известно, что такое соединение, как, например, лекарственный препарат, может существовать в различных кристаллических формах, что называется полиморфизмом. В общем, различные кристаллические формы одного и того же препарата могут иметь различные физические свойства и химическую стойкость. Очень важно при производстве фармацевтических препаратов использовать лекарство в качестве биоактивного компонента именно той кристаллической формы, которая не только проявляет его терапевтический эффект, но также эффективно снижает его токсичность и побочные эффекты. До сегодняшнего дня среди данных об опубликованных препаративных методах и применениях состава S-зопиклона не было представлено описаний его определенной кристаллической формы.
СУТЬ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является предоставление стойкой кристаллической формы S-зопиклона.
Другой целью настоящего изобретения является предоставление метода приготовления кристаллической формы S-зопиклона.
Еще одной целью настоящего изобретения является предоставление состава, которое является кристаллической формой S-зопиклона.
Еще одной целью настоящего изобретения является предоставление медицинского применения кристаллической формы S-зопиклона.
Согласно одному аспекту настоящего изобретения, представлена кристаллическая форма S-зопиклона, выявленная спектром порошковой рентгеновской дифракции, дифференциальной сканирующей калориметрией (ДСК) и инфракрасным спектром поглощения (ИК), четко изображенная на соответствующих чертежах. Соответствующие данные представлены следующим образом:
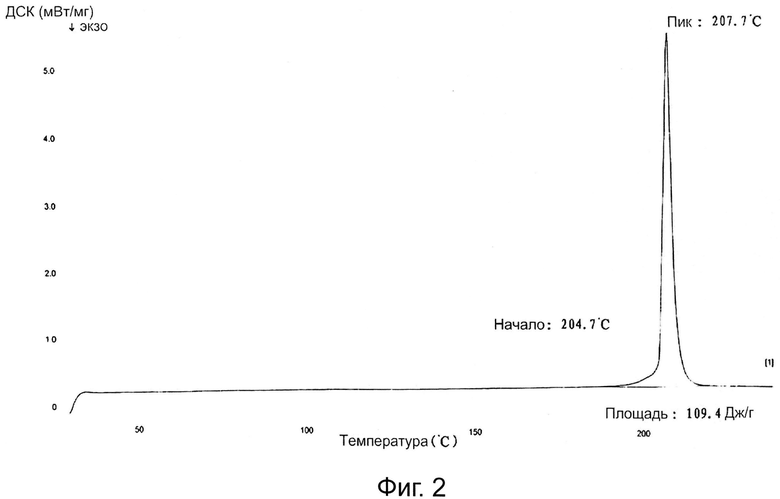
Пик ДСК термограммы проявляется приблизительно при 207,7°С.
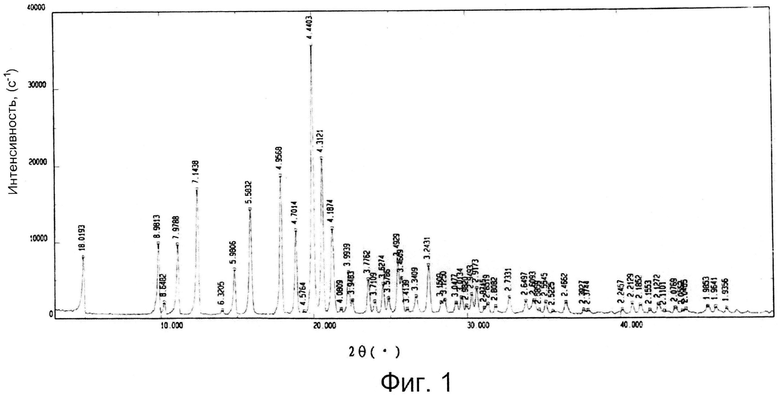
Спектр порошковой рентгеновской дифракции препарата имел характерные пики, выраженные в условиях 2θ при средних значениях (θозначает угол отражения) приблизительно 11,08°, приблизительно 12,38°, приблизительно 15,86°, приблизительно 17,88°, приблизительно 19,98° и приблизительно 20,58°.
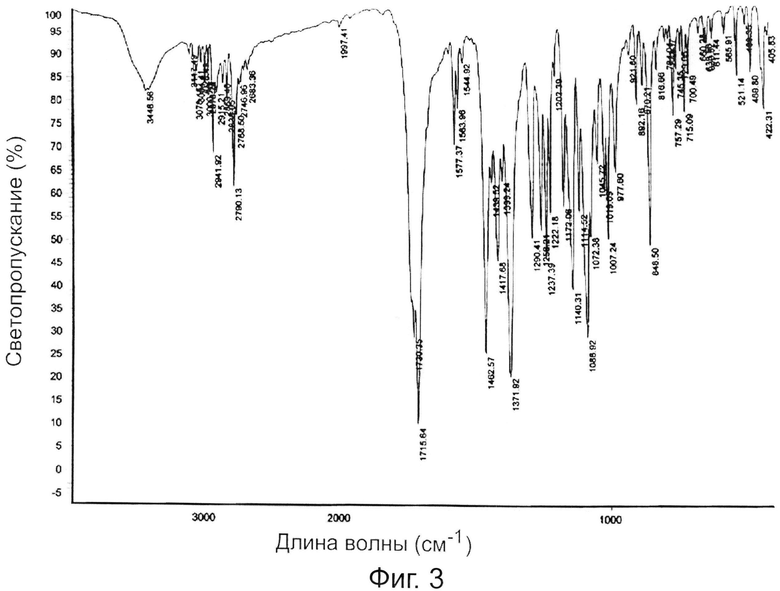
Его инфракрасный спектр поглощения (ИК) имел характерные пики приблизительно при 3078 см-1, приблизительно 2942-2838 см-1, приблизительно 2790 см-1, приблизительно 1716 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1, и приблизительно 757 см-1, предпочтительно при приблизительно 3078 см-1, приблизительно 2942-2838 см-1, приблизительно 2790 см-1, приблизительно 1716 см-1, приблизительно 1577-1545 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1, приблизительно 1007 см-1, приблизительно 849 см-1 и приблизительно 757 см-1.
Кристаллическая форма S-зопиклона по настоящему изобретению характеризуется общепризнанными методами спектра рентгеновской дифракции, дифференциальной сканирующей калориметрией (ДСК) и инфракрасным спектром поглощения (ИК).
В общем, спектр порошковой рентгеновской дифракции, полученный из кристаллического соединения, является характерным для данной кристаллической формы, выраженной в условиях 2θ, с использованием Cu-Ka излучения.
ДСК известна специалистам данной области, используется для измерения температуры термоперехода при поглощении и отдаче теплоты в связи с изменением кристаллической структуры и плавлением кристаллического тела. Постоянный анализ показала, что разница между температурой термоперехода и температурой плавления обычно находится в пределах приблизительно ±2°С, обычно в пределах приблизительно ±1°С. Поэтому состав со специфическим пиком ДСК или температурой плавления означает, что разница между пиком ДСК и температурой плавления находится в пределах ±2°С, что считается альтернативным методом определения различных кристаллических форм S-зопиклона. Таким образом, предварительное определение различных кристаллических форм соединения может быть проведено, основываясь на (по крайней мере, частично) характерно различной температуре перехода.
Инфракрасный спектр поглощения (ИК) используется для измерения поглощения инфракрасного света, вызванное специфическими химическими связями, которые относятся к инфракрасно-колебательным спектрам в молекулах.
И ДСК, и ИК могут предоставить нам информацию о физико-химических свойствах кристаллической формы S-зопиклона.
приготовления S-зопиклона, который используется в качестве сырья для изготовления кристаллической формы S-зопиклона согласно настоящему изобретению, представляет собой следующее:
Соединить рацемический зопиклон и D-(+)-яблочную кислоту со смесью метанола и ацетона для растворения перемешиванием при температуре 20-30°С, остудить до 0-10°С поддерживать данную температуру на протяжении приблизительно 6-48 часов, продолжая перемешивать, отфильтровать, промыть метанолом и высушить для получения D-(+)-яблочной кислоты S-зопиклона. Далее, прежде полученную D-(+)-яблочную кислоту S-зопиклон растворяют водой. Значение рН устанавливается на уровне 6-9, затем раствор экстрагируют этилацетатом, высушивают, концентрируют и фильтруют для получения фильтрационного кека. Фильтрационный кек промывают и высушивают для получения S-зопиклона в качестве сырья.
Специалистам данной области трудно предугадать, получится ли кристаллическая форма данного соединения, что тесно связано с условиями его приготовления. Для процесса очищения S-зопиклона использование этилацетата в качестве растворителя имеет ряд преимуществ: более низкая токсичность, более простое обращение, сниженные затраты и лучший результат. Поэтому изобретатели в достаточной мере исследовали различные условия кристаллизации с использованием этилацетата в качестве растворителя.
В соответствии с одним аспектом настоящего изобретения, представлен метод кристаллизации S-зопиклона, который состоит из следующих этапов:
(a). Растворить S-зопиклона этилацетатом температурой от 60°С до температуры рефлюкса. Используется 10-80 мл этилацетата из расчета на 1 г S-зопиклона, предпочтительно 25-50 мл этилацетата на 1 г S-зопиклона;
(b). Дать раствору остыть при комнатной температуре до 30-50°С, предпочтительно 35-45°С; поддерживать температуру на протяжении 10 мин - 12 часов, предпочтительно 1-6 часов;
(c). Постоянно охлаждать до температуры 10 - -10°С, предпочтительно 5 - -5°С; поддерживать температуру на протяжении 10 мин - 12 часов, предварительно 1-6 часов; и
(d). Отделить кристаллическую структуру.
При этом данный метод кристаллизации может выполняться с помощью устройства для перемешивания или без него, предпочтительно при помощи устройства для перемешивания.
В соответствии с другим аспектом настоящего изобретения, получен лекарственный препарат с терапевтически эффективным количеством кристаллической формы S-зопиклона по данному изобретению и фармацевтически приемлемым носителем. Дополнительно, данный препарат формирует комплексные средства вместе с другими активными ингредиентами.
В соответствии с еще одним аспектом настоящего изобретения, медицинский препарат по данному изобретению формируется в фармацевтический препарат одноразовой дозы. Также фармацевтический препарат одноразовой дозы означает форму дозировки, например каждую таблетку при таблеточной форме, каждую капсулу при капсульной форме, каждый флакон при жидкостях для перорального применения и каждый мешочек при гранулах, и т.д.
В соответствии с еще одним аспектом настоящего изобретения, медицинский препарат может содержать 0,1-99,9 весового % кристаллической формы S-зопиклона по настоящему изобретению наряду с фармацевтически приемлемым носителем. Предпочтительно, весовой процент кристаллической формы S-зопилкона по настоящему изобретению в препарате составляет 0,1-20 весовой %, наиболее предпочтительно - 1-10 весовой %.
В общем, кристаллическая форма S-зопиклона по настоящему изобретению и фармацевтически приемлемый носитель могут использоваться для формирования медицинского препарата согласно данному изобретению по стандартным фармацевтическим технологиям, например, при помощи процессов традиционного смешивания, гранулирования и таблетирования. Специалистам в данной области хорошо известно, что типы и характеристики фармацевтически приемлемого носителя зависят от количества активного ингредиента, смешиваемого с носителем, выбранного способа введения и других известных факторов. Указанный фармацевтически приемлемый носитель согласно настоящему изобретению включает в себя различные типы органических и неорганических носителей, которые могут вводиться в сочетании с препаратом, например, носители, используемые для твердых препаратов, таких как вспомогательные вещества, смазочные вещества, связывающие компоненты, разрыхрытели и покрывающие вещества, также могут применяться фармацевтически приемлемые добавки, такие как окрашивающие вещества и подсластители. В соответствии с одним аспектом настоящего изобретения, фармацевтически приемлемые носители выбираются из группы, состоящей из сахаров, таких как мальтоза, глюкоза, фруктоза, декстран, сахароза, лактоза, циклодекстрины (напрмер, β-циклодекстрин), крахмал, целлюлоза и их производные; сахарных спиртов, таких как маннитол, сорбитол и ксилитол; неорганических кислот, таких как хлористоводородная кислота, серная кислота и фосфорная кислота; неорганических солей, таки как хлорид натрия, хлорид калия, пиросульфит натрия, гидросульфит натрия, тиосульфат натрия, карбонат кальция, биокарбонат кальция, карбонаты и фосфаты щелочных металлов и их водяные растворы; аминокислот, таких как глицин, метионин и гидрохлорид цистеина; органических солей, таких как двунатрий ЭДТД, ЭДТА кальция-натрия, лактат натрия, стеарат (такой как кальция стеарат и магния стеарат) и альгинат; и также другие фармацевтически приемлемые носители, такие как меркаптоуксусная кислота, уксусная кислота, витамин С, производные силикона, желатин, поливинилпирролидон, глицерин, твин-80, агар, поверхностно-активные вещества, полиэтиленгликоль, фосфолипиды, каолин и тальковая пудра, и т.д.
В соответствии с еще одним аспектом настоящего изобретения, фармацевтически приемлемый препарат, содержащий кристаллическую форму S-зопиклон по данному изобретению, может быть изготовлен в виде любой фармацевтически приемлемой дозировке, к которой относятся таблетки, такие как таблетки в сахарной облатке, таблетки в пленочной оболочке и таблетки с энтеросолюбильным покрытием; капсулы, такие как твердые капсулы и мягкие капсулы; жидкости для перорального применения, таблетки для растворения в щечном кармане, гранулы, растворимые гранулы, пилюли, порошок, пасты, пеллеты, суспензии, присыпки, растворы, инъекции, суппозитории, мази, пластыри, крема, спрэи, капли и повязки. При этом препарат по настоящему изобретению предпочтительно представлен в пероральной форме, например, капсулы, таблетки, жидкости для перорального применения, гранулы, пилюли, порошок и пеллеты, и т.д.; и инъекции, например, порошковые инъекции, растворы для инъекций и растворы для внутривенного вливания, наиболее предпочтительная форма - таблетки.
В соответствии с еще одним аспектом настоящего изобретения, пероральный препарат стабильной кристаллической формы S-зопиклона может содержать традиционные вспомогательные вещества, связывающие компоненты, объемообразующие агенты, разбавители, таблетирующие агенты, смазочные агенты, разрыхлители, красители, подсластители и увлажняющие компоненты и, дополнительно, на таблетки можно наносить покрытие.
Предпочтительно, вспомогательные вещества могут быть представлены лактозой, D-маннитолом, D-сорбитолом, крахмалом (например, α-крахмал, амилопектин и декстрин), целлюлозами и их производными (например, кристаллическая целлюлоза, гидроксипропилцеллюлоза с низкой степенью замещения и карбоксиметилцеллюлоза натрия), гуммиарабиком, легкой безводной кремниевой кислотой, синтетическим силикатом алюминия и алюмосиликатом магния, и т.д.
Предпочтительно, смазывающие вещества могут быть представлены стеаратом магния, стеаратом кальция, тальковой пудрой и силикатным гелем, и т.д.
Предпочтительно, соединяющие компоненты могут быть представлены крахмалом (например, α-крахмалом, декстрином и амилопектином), сахарозой, трегалозой, желатином, гуммиарабиком, целюлозами и их производными (например, метилцеллюлоза, карбоксиметилцеллюлоза, карбоксиметилцеллюлоза натрия, кристаллическая целлюлоза, гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза), D-маннитолом и пирролидоном, и т.д.
Предпочтительно, разрыхрытелия могут быть представлены лактозой, крахмалом, натрия карбоксиметилкрахмалом, целюллозами и их производными (например, карбоксиметилцеллюлоза, карбоксиметилцеллюлоза кальция и гидроксипропилцеллюлоза с низкой степенью замещения) и легкой безводной кремниевой кислотой, и т.д.
Предпочтительно, покрывающие агенты могут быть представлены гидроксипропилметилцеллюлозой, гидроксипропилцеллюлозой, этилцеллюлозой, карбоксиметилцеллюлозой и поливиниловым спиртом, и т.д.
Предпочтительно, красители могут быть представлены водорастворимым пищевым тартазином желтым красителем (пищевые красители, например, пищевой красный №2 и №3, пищевой №4 и №5, пищевой синий №1 и №2), водонерастворимым осажденным красителем (например, алюминиевая соль водорастворимого пищевого тартазина желтого красителя), природными красителями (например, β-каротин, хлорофилл и колкотар) и т.д.
Предпочтительно, подсластители могут быть представлены сахарином натрия, дикалия глицирризатом, аспартамом и стевией, и т.д.
В соответствии с одним аспектом настоящего изобретения, медицинский препарат может вводиться традиционным способом субъекту любым путем, например, перорально, локально, парентерально или ингаляционно, предпочтительно - перорально.
В соответствии с одним аспектом настоящего изобретения, при использовании для лечения нарушения сна, одна доза медицинского препарата содержит 1-15 мг кристаллической формы S-зопиклона, предпочтительно содержит 3-12 мг кристаллической формы S-зопиклона.
В соответствии с еще одним аспектом настоящего изобретения, применение и дозировка медицинского препарата определяется в зависимости от состояния пациента, принимающего препарат согласно данному изобретению, его можно принимать один раз в день ежедневно по 1-10 одноразовых доз за раз, например, перед сном, по 1-10 мешочков, или 1-10 пилюль или 1-10 таблеток.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 представляет спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению.
Фиг.2 представляет график ДСК кристаллической формы S-зопиклона по настоящему изобретению.
Фиг.3 представляет инфракрасный спектр поглощения кристаллической формы S-зопиклона по данному изобретению.
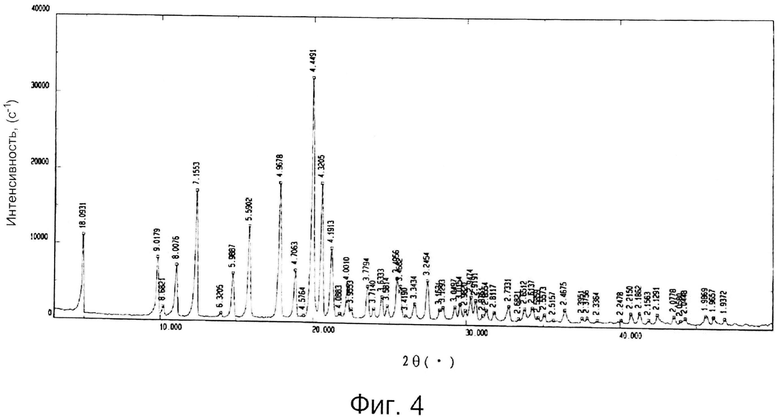
Фиг.4 представляет спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению, подверженному действию высокой температуры (60°С) в течение 10 дней.
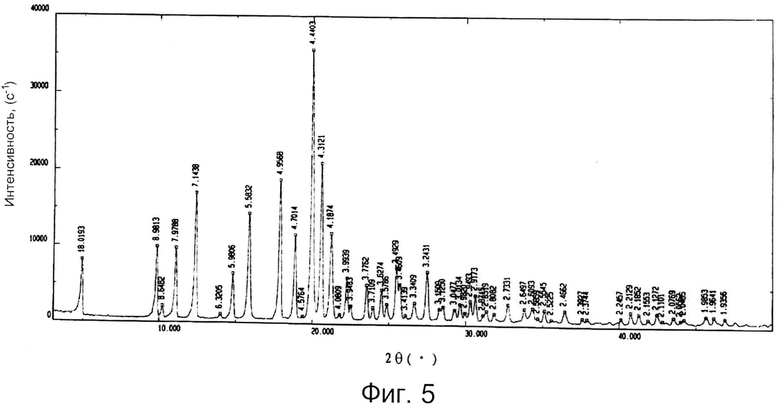
Фиг.5 представляет спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению, подверженному действию высокой влажности (25°С, относительная влажность 92,5%) в течение 10 дней.
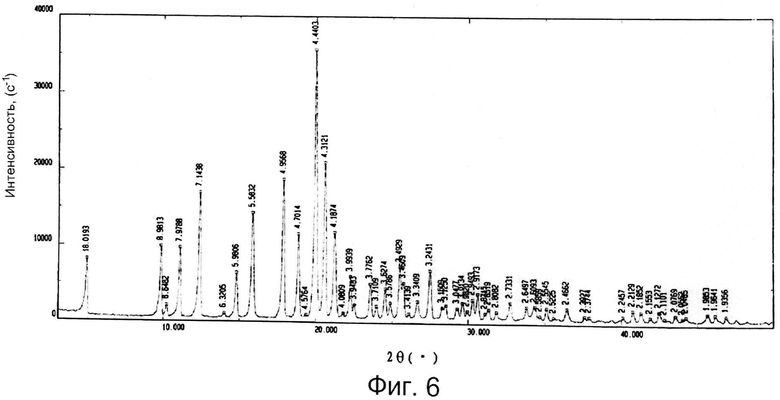
Фиг.6 представляет спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению, подверженному действию интенсивного света (4500±500Lx) в течение 10 дней.
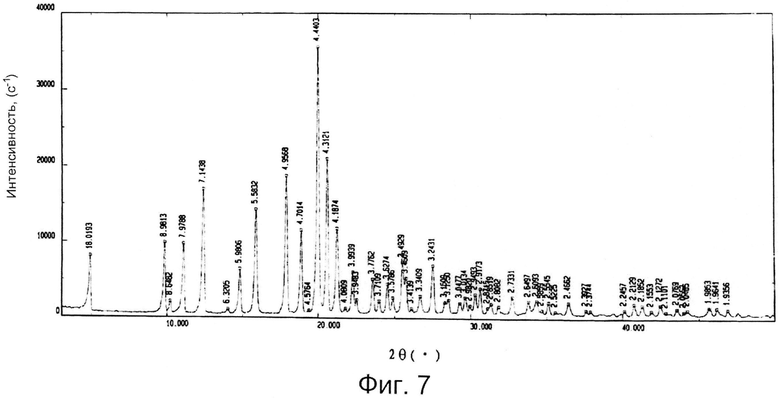
Фиг.7 представляет спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению при температуре 40±2°С и относительной влажности 75±5% в течение 6 месяцев.
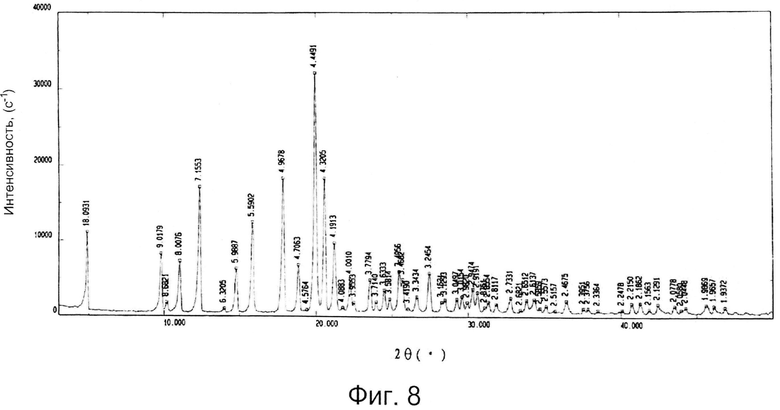
Фиг.8 представляет спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению, подверженному действию комнатной температуры в течение 36 месяцев.
В соответствии с одним аспектом настоящего изобретения, представлено применение кристаллической формы S-зопиклона по данному изобретению в приготовлении медикамента для лечения нарушения сна. Ниже приведены результаты фармакодинамики.
Исследование 1. Результаты фармакодинамики кристаллической формы S-зопиклона по данному изобретению
В отличие от структуры препарата бензодиазепин, S-зопиклон действует на другом сайте связывания рецептора бензодиазепина в комплексе ГАМКА-рецептор/Cl канал.
Кристаллическая форма S-зопиклона по данному изобретению в качестве тестируемого препарата была приготовлена в соответствии с Примером 1 настоящего изобретения.
1. Фармакодинамическое исследование кристаллической формы S-зопиклона в лабораторных условиях
Значение IC50 связывания S-зопиклона с рецептором бензодиазепина составляет 21±3 (нмоль/л), где IC50 означает половину максимальной подавляющей концентрации, обратно пропорциональной способности связывания с рецептором. Таким образом, она указывает на то, что S-зопиклон обладает сильной способностью связывания с рецептором. Как показали исследования, хотя химическая структура S-зопиклона и отличается от структуры препарата бензодиазепина, оба препарата обладают сходными механизмами действия связывания рецептора бензодиазепина, но имеют различные сайты связывания.
2. Фармакодинамическое исследования кристаллической формы S-зопиклона в естественных условиях
Мужские особи крыс Лонг-Эванс (весом 250-275 г) были отобраны и разделены на 3 группы, их кормили на протяжении 12-часового цикла дня и ночи. После недели кормления был проведен эксперимент.
2.1 Анализ спонтанной активности
С целью измерения общей спонтанной активности, наблюдалась горизонтальная активность крыс при открытых обстоятельствах. Соответственно, все животные были помещены в 8 черных комнат, защищенных от света, их спонтанная активность наблюдалась при помощи инфракрасных датчиков, вмонтированных в стены с равными интервалами записи каждые 10 мин на протяжении 120 минут.
Животным вводилась кристаллическая форма S-зопиклона в дозировке 10 мг/кг массы тела. Через 30-60 минут после введения препарата поглощающий эффект на двигательную способность достиг пика и исчез через 2 часа.
2.2 Лабиринтный тест
Введение кристаллической формы S-зопиклона при 10 мг/кг массы тела имело значительный эффект на всех выходах, открытых и закрытых выходах. При дозировке 5 мг/кг массы тела и 10 мг/кг массы тела наблюдалось, что кристаллическая форма S-зопиклона может значительно увеличивать время пребывания в открытых проходах.
Как показали вышеуказанные результаты, кристаллическая форма S-зопиклона имела существенный эффект не только для лечения нарушения сна, но также и лечения тревожного состояния, не влияя на способность к спортивной координации.
Исследование 2. Изучение свойств и стойкости кристаллической формы S-зопиклона
Продукт был представлен белым или сероватым/желтоватым кристаллом или кристаллическим порошком.
1. Растворимость
Тест на растворимость был проведен при помощи обычных растворителей в соответствии с методом ОБЩЕГО УВЕДОМЛЕНИЯ в Chinese Pharmacopoeia (редакция 2000).
Кристаллическая форма S-зопиклона по данному изобретению в качестве испытуемого препарата была приготовлена в соответствии с Примером 1 настоящего изобретения.
Метод исследования: необходимое количество мелкого порошка кристаллической формы S-зопиклона было точно измерено, в него было добавлено определенное количество растворит€;ля с точностью ±2%. При температуре 25±2°С, раствор интенсивно встряхивали на протяжении 30 секунд, эта процедура повторялась через 5-минутные интервалы. В течение 30 минут наблюдалось поведение растворимости. Результаты представлены в Таблице 1.
Выводы
Кристаллическая форма S-зопиклона по данному изобретению легко растворяется в хлороформе, растворяется в соляной кислоте (0,1 моль/л), слабо растворяется в ацетоне, этилацетате или метаноле, очень слабо растворяется в этаноле и эфире и практически не растворяется в воде.
2. Стойкость
Кристаллическая форма S-зопиклона по данному изобретению в качестве испытуемого препарата была приготовлена в соответствии с Примером 1 настоящего изобретения.
2.1 Испытание при высоких температурах (60°С)
Кристаллическая форма S-зопиклона по данному изобретению была введена партиями в открытый и бесцветный прозрачный бюкс и помещена в терморегулирующий контейнер (60°С) на 10 дней. Образцы были отобраны на 5-й и 10-й дни соответственно для измерения их стойкости в соответствии с ключевыми понятиями, относящимися к стойкости. Результаты представлены в Таблице 3.
Как показали результаты, кристаллическая форма S-зопиклона остается стойкой после 10 дней воздействия высокой температуры (60°С), и ее параметры практически полностью соответствовали параметрам 0-го дня, включая характер, температуру таяния и содержание примесей, таких как левозопиклон. Спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению, подверженного воздействию высокой температуры на протяжении 10 дней, представлен на Фиг.4.
2.2 Испытание при высокой влажности (25°С, относительная влажность: 92,5%)
Кристаллическая форма S-зопиклона по данному изобретению была партиями введена в открытый и бесцветный прозрачный бюкс и помещена в закрытый сосуд (KNO3 насыщенный раствор, относительная влажность: 92,5%) на 10 дней. Образцы были отобраны на 5-й и 10-й день соответственно для измерения их стойкости в соответствии с ключевыми понятиями, относящимися к стойкости. Тем временем, вес тестируемого препарата перед и после исследования был тщательно измерен. Результаты представлены в Таблице 2 и Таблице 3.
Как показали результаты после 10 дней воздействия высокой влажности наблюдалось небольшое увеличение массы кристаллической формы S-зопиклона, практически при полном соответствии с 0-м днем. Результаты представлены в Таблице 2. Спектр рентгеновской дифракции кристаллической формы S-зопиклона, подверженного воздействию высокой влажности на протяжении 10 дней, представлен на Фиг.5.
2.3 Испытание при воздействии интенсивного света
Кристаллическая форма S-зопиклона по данному изобретению была введена в открытый и бесцветный прозрачный бюкс и подвержена прямому воздействию интенсивного света (4500±500 люкс) на протяжении 10 дней. Образцы были отобраны на 5-й и 10-й день соответственно для измерения их стойкости в соответствии с ключевыми понятиями, относящимися к стойкости. Результаты представлены в Таблице 3.
Как показали результаты, кристаллическая форма S-зопиклона оставалась стойкой после 10 дней воздействия интенсивного света (4500±500 люкс), а ее параметры практически полностью соответствовали параметрам 0-го дня, включая характер, температуру таяния и содержание примесей, таких как левозопиклон. Спектр рентгеновской дифракции кристаллической формы S-зопиклона, подвергаемого воздействию интенсивного света (4500±500 люкс) на протяжении 10 дней, представлен на Фиг.6.
2.4 Ускоренное испытание
Кристаллическая форма S-зопиклона была расфасована в упаковки, подобные коммерческим, и помещена в терморегулирующий контейнер (температура: 40±2°С, относительная влажность: 75±5%) на 6 месяцев. Образцы были отобраны на 1-й, 2-й, 3-й и 6-й месяц соответственно для измерения их стойкости в соответствии с ключевыми понятиями, относящимися к стойкости. Результаты представлены в Таблице 4.
Как показали результаты, кристаллическая форма S-зопиклона оставалась стойкой после 6 месяцев ускоренного испытания. Ее параметры почти полностью соответствовали параметрам 0-го дня, включая характер, температуру таяния и содержание примесей, таких как левозопиклона. Спектр рентгеновской дифракции кристаллической формы S-зопиклона в условиях температуры 40±2°С и относительной влажности 75±5% на протяжении 6 месяцев представлен на Фиг.7.
2.5 Испытание при длительном хранении образца
Кристаллическая форма S-зопиклона была расфасована в упаковки, подобные коммерческим, и хранилась при комнатной температуре. Образцы были отобраны на 3-й, 6-й, 9-й, 12-й, 18-й, 24-й и 36-й месяцы соответственно для измерения их стойкости в соответствии с ключевыми понятиями, относящимися к стойкости. Данные в сравнении с 0-м днем представлены в Таблице 5.
Как показали результаты испытания при длительном хранении образца кристаллическая форма S-зопиклона оставалась стойкой, а ее параметры практически полностью соответствовали параметра 0-го дня, включая характер, температуру таяния и содержание примесей, таких как левозопиклон. Спектр рентгеновской дифракции кристаллической формы S-зопиклона по данному изобретению при комнатной температуре на протяжении 36 месяцев представлены на Фиг.8.
Выводы:
В заключение кристаллическая форма S-зопиклона по данному изобретению была введена в открытый и бесцветный прозрачный бюкс и помещена в различные среды на 10 дней, включая высокую температуру (60°С), относительную влажность (92,5%) и воздействие интенсивного света (4500±500 люкс). К тому же после 6 месяцев ускоренного исследования кристаллической формы S-зопиклона, расфасованного в упаковки, подобные коммерческим, (температура: 40±2°С, относительная влажность: 75±5%), по сравнению с результатами 0-го дня, не было обнаружено значительных изменений во многих параметрах, включая характер, температуру таяния и содержание примесей, таких как левозопиклон. Результаты влияющих факторов показали, что кристаллическая форма S-зопиклона по данному изобретению должна храниться в герметичном и сухом месте.
После 36 месяцев испытания при длительном хранении образца кристаллическая форма S-зопиклона, расфасованного в упаковки, подобные коммерческим, при комнатной температуре, по сравнению с результатами 0-го дня, не наблюдалось значительных изменений в параметрах, включая характер, температуру таяния и содержание примесей, таких как леовозопиклон.
При условиях вышеуказанного испытания не наблюдалось явления трансформации кристаллов. Было основательно подтверждено, что кристаллическая форма S-зопиклона по настоящему изобретению обладает стойкой структурой.
Исследование 3. Фармакокинетическое изучение одноразового введения кристаллической формы S-зопиклона здоровым добровольцам
1. Цель
Одноразовое введение различных дозировок препарата здоровым волонтерам изучалось с точки зрения оценки его фармакокинетического профиля, а также правила распределения, метаболизма и выведения в естественных условиях. Поскольку кристаллическая форма S-зопиклона была разработана для введения субъекту перорально, также изучалось влияние потребления пищи на поглощение, распределение, метаболизм и выведение препарата.
2. Метод.
Оценка фармакокинетики: согласно результатам фазы I клинического теста на переносимость и предварительно разработанной дозе фазы II клинического теста, все добровольные участники теста могут переносить высокую дозу 11,25 мг/кг МТ (массы тела), три различные группы в соответствии с дозировкой были разбиты следующим образом: группа низкой дозировки, группа умеренной дозировки и группа высокой дозировки составляли 3, 6 и 12 мг/кг МТ соответственно. Использовалась тройная перекрестная модель латинских квадратов. Все субъекты были вразброс разделены на три тестовые группы, при проведении каждого теста субъектам вводился тестируемый препарат в различных дозировках. Таким образом, после 3 тестов каждому субъекту был введен тестируемый препарат в высокой, умеренной и низкой дозировке в соответствии с моделью латинских квадратов. Интервал между двумя тестами составлял 2 недели.
К тому же изучалось влияние потребления пищи на метаболизм препарата в естественных условиях. 8 субъектов были выборочно разделены на 2 группы. В 2 тестах, субъекты каждой группы получили препарат в одной и той же дозировке (6 мг) натощак и через 5 мин после стандартного приема пища. Интервал между двумя тестами составлял 2 недели.
После одноразового введения тестируемого препарата, были собраны образцы венозной крови с 6 мл антикоагулянта гепарина на 0-й (непосредственно до введения препарата), 15-й мин, 30-й мин, 45-й мин, 60-й мин, 1,5-й час, 2-й час, 3-й час, 4-й час, 6-й час, 8-й час, 12-й час, 16-й час и 24-й час соответственно для определения концентрации S-зопиклона. Для получения кривой соотношения концентрации-времени концентрация препарата в плазме каждого субъекта определялась ВЭЖХ в различное время. Были посчитаны основные фармакокинетические параметры субъектов, в том числе, средняя концентрация мочи (СКМ), Cmax (концентрация), Tmax (время), CKM 0~∝, CKM0-t И t1/2, и т.д.
3. Отбор субъектов
Численность: (предварительно определенная численность и анализированная численность) 10 человек в группе.
Критерии включения и исключения: возраст 19-45 лет и индекс массы тела (ИМТ) 19-29 кг/м2.
При отборе физическое здоровье субъектов подтверждалось в соответствии с их историей болезни, медицинским осмотром, ЭКГ и лабораторными анализами. Более того, перед исследованием должна быть подписано форма информированного согласия (ФИС).
4. Характеристика, применение и дозировка тестируемого препарата
Кристаллическая форма S-зопиклона была приготовлена в таблетках с оболочкой (3 мг S-зопиклон/таблетка) в соответствии с Примером 1 и Примером 9, была один раз введена перорально.
5. Продолжительность лечения
После одноразового перорального введения было проведено наблюдение в течение двадцати четырех часов.
6. Критерии оценки
Фармакокинетические индексы: для получения кривой соотношения концентрации-времени концентрация препарата была определена сразу перед введением и в различные промежутки времени после введения препарата. Были посчитаны основные фармакокинетические параметры, в том числе Cmax, Tmax, СКМ0~∝, CKM0-t И t1/2, и т.д.
Индексы безопасности: при отборе и через 24 часа после введения препарата был измерен ряд показателей, включая жизненные показатели, проведен медицинский осмотр, ЭКГ и клинические анализы. Во время исследования нежелательные явления своевременно записывались.
7. Статистический метод
Фармакокинетика: для расчета основных фармакокинетических параметров использовалось программное обеспечение для статистического анализа 3Р97.
Безопасность: значимые клинические показатели безопасности представлены в таблице в соответствии с их типом и частотой.
8. Результаты и выводы
Субъекты строго следовали протоколу исследования, не отклоняясь от него и не нарушая его, не совмещая препараты. По немедицинским причина один из субъектов не сдал последний 3-й образец крови через 8 часов после введения препарата в дозировке 12 мг/кг МТ.
Фармакокинетические результаты.
Фармакокинетические параметры субъектов после одноразового введения кристаллической формы S-зопиклона показаны в Таблице 6.
Результаты безопасности:
В качестве нежелательной реакции был зафиксирован, горький привкус во рту и большинства субъектов (25%-40%), другой нежелательной реакцией было головокружение и головная боль. Как показали результаты, по сравнению с группами низкой и умеренной дозировки, больше видов и более частые случаи нежелательных реакций проявлялись в группе с высокой дозировкой (12 мг/кг МТ). Два субъекта в группе дозировки 12 мг/кг МТ впали в состояние делирия, включая говорливость, гиперактивность и бессознательное состояние. Но эти нежелательные реакции были неострыми и непродолжительными. В течение 12 часов после введения препарата, все нежелательные реакции исчезли без специального лечения.
Выводы:
Таблетки кристаллической формы S-зопиклона могут быстро поглощаться после перорального введения препарата. Дозировка и концентрация препарата в плазме в рамках 3-12 мг имели хорошее линейное соотношение. Общие нежелательные реакции включали горький привкус во рту и головокружение, указывая на то, что кристаллическая форма S-зопиклона по данному изобретению имеет хорошие показатели безопасности для клинического использования.
Кристаллическая форма относится к типу твердых веществ с атомами (или ионами и молекулами), организованными стерически-периодически. В общем, кристаллические формы органического препарата относятся к молекулярной решетке, которая может образовывать различные кристаллические формы в зависимости от различных условий процесса. Более того, различные кристаллические формы одного и того же препарат часто могут приводить к значительным различиям во многих физико-химических свойствах (например, внешний вид, растворимость, температура плавления и плотность), растворении и биологической доступности препарата, таким образом влияя на стойкость и биологическую доступность препарата. К настоящему времени исследователи полиформизма препаратов стали неотъемлемым и важным аспектом для исследования и разработки, изучения и утверждения препарата, производства, контроля качества и исследования перед составлением формулы с целью выбора формы и дозировки для нового препарата.
Кристаллическая форма S-зопиклона по данному изобретению имеет следующие преимущества:
1. Она может иметь лучший терапевтический эффект для лечения нарушения сна, способствовать снятию тревожного состояния не влияя на спортивную координацию.
2. Она может поглощаться сразу после перорального введения. В рамках эффективной дозировки, концентрация препарата в крови и дозировка обладают хорошим линейным соотношением, что делает препарат более безопасным для клинического применения.
3. В условиях вышеуказанного исследования не исследовался феномен кристаллической трансформации. Есть подтверждения тому, что кристаллическая форма S-зопиклона по данному исследованию обладала стойкой структурой.
4. Она обладает хорошей текучестью и сжимаемостью (т.е. она легко прессуется в таблетку). Полное соответствие фармакодинамическим и фармакокинетическим требованиям для клинического применения в большой степени способствует практическому производству.
ПРИМЕРЫ
Следующие примеры иллюстрируют настоящее изобретение, но не ограничивают изобретение никоим образом.
Пример подготовительного процесса - приготовление S-зопиклона в качестве сырья
В 3-литровую реакционную склянку добавили рацемический зопиклон (100 г), D-(+)-яблочную кислоту (34 г), метанол (100 мл) и ацетон (1500 мл) для растворения, помешивая в течение 2 часов при комнатной температуре. Полученному раствору дали остыть до 6°С. По прошествии 24 часов при температуре 6°С, раствор помешивали в течение 1 часа, дважды профильтровали метанолом (общий объем - 100 мл) и высушили для получения D-(+)-яблочной кислоты S-зопиклона (52,5 г).
Вышеуказанную D-(+)-яблочную кислоту S-зопиклон (52,5 г) растворили водой (1000 мл), далее добавили бикарбонат калия (8%) для установления уровня рН 8; в осадок выпало твердое вещество. Затем раствор 4 раза экстрагировали этилацетатом (общий объем - 1000 мл). Затем слой этилацетата высушивали безводным сульфатом натрия (в качестве десиканта) в течение 5 часов, отфильтровали и удалили десикант. Раствор концентрировали дистилляцией, затем отфильтровали, 3 раза промыли этилацетатом (общий объем - 1000 мл) и высушили для получения S-зопиклона (33,2 г) в качестве сырья.
Пример 1 - приготовление кристаллической формы S-зопиклона
В 500-милилитровый сосуд добавили S-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (350 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжение 10 минут и дали остыть при комнатной температуре до приблизительно 40°С. После 2 часов помешивания при приблизительно 40°С раствор остудили до приблизительно 0°С, помешивали на протяжении 1 часа при температуре приблизительно 0°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (8,9 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°С, приблизительно 12,38°С, приблизительно 15,86°С, приблизительно 17,88°С, приблизительно 19,98°С и приблизительно 20,58°С.
Пик на ДСК термограмме был приблизительно при 207,7°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3078 см-1, приблизительно 2942-2838 см-1, приблизительно 2790 см-1, приблизительно 1715 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1 и приблизительно 757 см-1.
Пример 2 - приготовление кристаллической формы S-зопиклона
В 500-милилитровый сосуд добавили 3-зопиклон (10.0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (250 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 45°С. После 10 минут помешивания при приблизительно 45°С раствор остудили до приблизительно 1°С, помешивали на протяжении 2 часов при температуре приблизительно 1°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (9.0 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 29 приблизительно при 11,15°, приблизительно 12,38°, приблизительно 15,92°, приблизительно 17,79°, приблизительно 19,93° и приблизительно 20,52°.
Пик на ДСК термограмме был приблизительно при 208,4°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3081 см-1, приблизительно 2941-2838 см-1, приблизительно 2791 см-1, приблизительно 1716 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1 и приблизительно 758 см-1.
Пример 3 - приготовление кристаллической формы S-зопиклона
В 1000-милилитровый сосуд добавили 3-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (500 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 35°С. После 7 часов помешивания при приблизительно 35°С раствор остудили до приблизительно 3°С, помешивали на протяжении 5 часов при температуре приблизительно 3°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (8,7 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°, приблизительно 12,42°, приблизительно 15,87°, приблизительно 17,81°, приблизительно 19,90° и приблизительно 20,55°.
Пик на ДСК термограмме был приблизительно при 207,3°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3077 см-1, приблизительно 2942-2839 см-1, приблизительно 2791 см-1, приблизительно 1714 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1 и приблизительно 757 см-1.
Пример 4 - приготовление кристаллической формы S-зопиклона
В 250-милилитровый сосуд добавили S-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (100 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 50°С. После 4 часов помешивания при приблизительно 50°С раствор остудили до приблизительно 8°С, помешивали на протяжении 7 часов при температуре приблизительно 8°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (9,2 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°, приблизительно 12,38°, приблизительно 15,86°, приблизительно 17,85°, приблизительно 19,90° и приблизительно 20,58°.
Пик на ДСК термограмме был приблизительно при 207,2°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3077 см-1, приблизительно 2941-2837 см-1, приблизительно 2792 см-1, приблизительно 1715 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1 и приблизительно 758 см-1.
Пример 5 - приготовление кристаллической формы S-зопиклона
В 1000-милилитровый сосуд добавили 3-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (800 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 30°С. После 10 часов помешивания при приблизительно 30°С раствор остудили до приблизительно -5°С, помешивали на протяжении 50 минут при температуре приблизительно -5°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (8,4 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°, приблизительно 12,35°, приблизительно 15,86°, приблизительно 17,88°, приблизительно 19,94° и приблизительно 20,58°.
Пик на ДСК термограмме был приблизительно при 208,1°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3077 см-1, приблизительно 2943-2839 см-1, приблизительно 2791 см-1, приблизительно 1715 см-1, приблизительно 1463 см-1, приблизительно 1371 см-1 и приблизительно 757 см-1.
Пример 6 - приготовление кристаллической формы S-зопиклона
В 1000-милилитровый сосуд добавили S-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (750 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 45°С. После 10 часов помешивания при приблизительно 45°С раствор остудили до приблизительно 0°С, помешивали на протяжении 2 часов при температуре приблизительно 0°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (8,8 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°, приблизительно 12,38°, приблизительно 15,86°, приблизительно 17,86°, приблизительно 19,98° и приблизительно 20,58°.
Пик на ДСК термограмме был приблизительно при 207,5°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3078 см-1, приблизительно 2942-2838 см-1, приблизительно 2790 см-1, приблизительно 1717 см-1, приблизительно 1463 см-1, приблизительно 1371 см-1 и приблизительно 759 см-1.
Пример 7 - приготовление кристаллической формы S-зопиклона
В 500-милилитровый сосуд добавили S-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (400 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 35°С. После 12 часов помешивания при приблизительно 35°С раствор остудили до приблизительно -10°С, помешивали на протяжении 10 минут при температуре приблизительно -10°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (8.3 г).
Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°, приблизительно 12,34°, приблизительно 15,92°, приблизительно 17,88°, приблизительно 19,98° и приблизительно 20,58°.
Пик на ДСК термограмме был приблизительно при 207,7°С.
Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3078 см-1, приблизительно 2941-2837 см-1, приблизительно 2790 см-1, приблизительно 1715 см-1, приблизительно 1464 см-1, приблизительно 1372 см-1 и приблизительно 757 см-1.
Пример 8 - приготовление кристаллической формы S-зопиклона
В 1000-милилитровый сосуд добавили 3-зопиклон (10,0 г). Для постепенного растворения твердого вещества добавили, перемешали и подогрели этилацетат (700 мл). Полученный раствор нагревали в сосуде с обратным холодильником на протяжении 10 минут и дали остыть при комнатной температуре до приблизительно 38°С. После 12 часов помешивания при приблизительно 38°С раствор остудили до приблизительно 10°С, помешивали на протяжении 12 часов при температуре приблизительно 10°С, отфильтровали всасыванием и высушили в вакууме до получения кристаллической формы S-зопиклона (8,9 г). Определено по следующим данным:
Спектр порошковой рентгеновской дифракции показал характерные пики, которые проявились в условиях 2θ приблизительно при 11,08°, приблизительно 12,41°, приблизительно 15,86°, приблизительно 17,81°, приблизительно 19,98° и приблизительно 20,58°.
Пик на ДСК термограмме был приблизительно при 207,6°С. Инфракрасный спектр поглощения (ИК) показал характерные пики приблизительно при 3081 см-1, приблизительно 2943-2838 см-1, приблизительно 2790 см-1, приблизительно 1715 см-1, приблизительно 1466 см-1, приблизительно 1372 см-1 и приблизительно 757 см-1.
Пример 9 - приготовление таблеток кристаллической формы S-зопиклона
Формула
Было изготовлено десять тысяч таблеток, каждая таблетка содержит 3 мг кристаллической формы S-зопиклона по данному изобретению.
Особые этапы процесса представляют собой следующее:
кристаллическую форму S-зопиклона, лактозу, кукурузный крахмал, предварительно клейстеризованный крахмал, повидон К30, натрия карбоксиметилкрахмал и микропорошок силикатного геля пропустили через сито 100 меш соответственно для дальнейшего использования. Кристаллическую форму S-зопиклона взвесили согласно количеству, указанному в формуле, и равномерно перемешали с другими вспомогательными средствами, в прогрессии увеличивая в равных количествах. Смесь 3 раза пропустили через сито 100 меш. Необходимое количество повидона К30 водного раствора (8%) добавили в полученный порошок для получения мягкого материала. Мягкий материал гранулировали, пропустив его через сито 20 меш. Смоченные гранулы высушили при 50-60°С и пропустили через сито 20 меш до получения одинаковых гранул. Добавили микропорошок силикатного геля и хорошо перемешали. Затем добавили стеарат магния и хорошо перемешали. Угол покоя был измерен в значении менее 30°. Состав препарата был проверен, был определен вес таблеток, затем таблетки был изготовлены при помощи 6-миллиметрового плоского штамповального пресса для дальнейшего покрытия.
Полученные простые таблетки были покрыты веществом Opadry® II. В соответствии с обычной формулой Opadry® II (растворимый в желудке), был приготовлен раствор для нанесения оболочки с использованием воды в качестве растворителя. Твердое содержание раствора для оболочки составляло 18%. Температура входящего воздуха: 80°С, температура движущегося слоя: 38-40°С, давление распыления: 3.5 бар, скорость вращения сосуда для нанесения оболочки: 23 оборота в минуту, скорость подачи материала: 2-3 г/мин. Сформированная мембрана оболочки обладала большой прочностью, большой силой сцепления, полным покрытием и однородным цветом.
Таблетки давали пациентам приблизительно за 1 час до сна, одноразовое пероральное введение при дозировке 1-4 таблетки.
Пример 10 - приготовление капсул кристаллической формы S-зопиклона
Формула
Было изготовлено десять тысяч капсул, каждая капсула содержит 3 мг кристаллической формы S-зопиклона по данному изобретению.
Особые этапы процесса представляют собой следующее:
кристаллическую форму S-зопиклона, лактозу, кукурузный крахмал, предварительно клейстеризованный крахмал, повидон К30, натрия карбоксиметилкрахмал и микропорошок силикатного геля пропустили через сито 100 меш соответственно для дальнейшего использования. Кристаллическую форму S-зопиклона взвесили согласно количеству, указанному в формуле, и равномерно перемешали с другими вспомогательными средствами, в прогрессии увеличивая в равных количествах. Смесь 3 раза пропустили через сито 100 меш. Необходимое количество повидона К30 водного раствора (8%) добавили в полученный порошок для получения мягкого материала. Мягкий материал гранулировали, пропустив его через сито 20 меш. Смоченные гранулы высушили при 50-60°С и пропустили через сито 20 меш до получения одинаковых гранул. Добавили микропорошок силикатного геля и хорошо перемешали. Затем добавили стеарат магния и хорошо перемешали. Угол покоя был измерен в значении менее 30°. После проверки состава препарата была определена его вместимость.
Капсулы были изготовлены помещением в капсулы №3.
Капсулы давали пациенту за 1 час до сна, одноразовое пероральное введение при дозировке 1-4 капсулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМОРФНЫЕ И АМОРФНАЯ ФОРМЫ ФОСФАТНОЙ СОЛИ 8-ФТОР-2-{4-[(МЕТИЛАМИНО)МЕТИЛ]ФЕНИЛ}-1,3,4,5-ТЕТРАГИДРО-6Н-АЗЕПИНО[5.4.3-CD]ИНДОЛ-6-ОНА | 2005 |
|
RU2355691C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 1-(5'-(5-(3,5-ДИХЛОРО-4-ФТОРФЕНИЛ)-5-(ТРИФТОРМЕТИЛ)-4,5-ДИГИДРОИЗОКСАЗОЛ-3-ИЛ)-3'Н-СПИРО[АЗЕТИДИН-3,1'-ИЗОБЕНЗОФУРАН]-1-ИЛ)-2-(МЕТИЛСУЛЬФОНИЛ)ЭТАНОНА | 2013 |
|
RU2614978C2 |
| НОВЫЕ КРИСТАЛЛЫ УРАЦИЛЬНОГО СОЕДИНЕНИЯ | 2016 |
|
RU2686722C1 |
| КРИСТАЛЛ ПРОИЗВОДНОГО 1,3,5-ТРИАЗИНА ИЛИ ЕГО СОЛЬВАТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2837449C1 |
| Способ получения полиморфа гидрохлорида 2-[4-(метиламинометил)фенил]-5-фтор-бензофуран-7-карбоксамида | 2018 |
|
RU2783418C1 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРА ЯНУС-КИНАЗЫ | 2017 |
|
RU2838992C2 |
| КРИСТАЛЛИЧЕСКОЕ ВЕЩЕСТВО | 2018 |
|
RU2834293C2 |
| НОВАЯ КРИСТАЛЛИЧЕСКАЯ ФОРМА МЕТАНСУЛЬФОНАТ 5-ХЛОР-N-({ (5S)-2-ОКСО-3-[4-(5,6-ДИГИДРО-4H-[1,2,4]ТРИАЗИН-1-ИЛ)ФЕНИЛ]-1,3-ОКСАЗОЛИДИН-5-ИЛ} МЕТИЛ)ТИОФЕН-2-КАРБОКСАМИДА И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2663617C1 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА ПИРИДО[3,4-D]ПИРИМИДИНОВОГО ПРОИЗВОДНОГО | 2017 |
|
RU2793759C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 6-(1Н-ИМИДАЗОЛ-1-ИЛ)-2-ФЕНИЛХИНАЗОЛИНА И ЕГО СОЛЕЙ | 2010 |
|
RU2557547C2 |
Изобретение раскрывает кристаллическую форму S-зопиклона со спектром порошковой рентгеновской дифракции с использованием Cu-Ка-излучения, с характерными пиками, выраженными в условиях 2θ приблизительно при 11,08°, приблизительно 12,38°, приблизительно 15,86°, приблизительно 17,88°, приблизительно 19,98°С и приблизительно 20,58°; ДСК-термограммой, на которой пик проявляется приблизительно при 207,7°С, и инфракрасным спектром поглощения (ИК) с характерными пиками приблизительно при 3078 см-1, приблизительно 2942-2838 см-1, приблизительно 2790 см-1, приблизительно 1716 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1 и приблизительно 757 см-1. Также представлен способ приготовления кристаллической формы эсзопиклона, фармацевтический препарат и ее применение в изготовлении медикамента для лечения нарушения сна. 5 н. и 3 з.п. ф-лы, 8 ил., 10 пр., 6 табл.
1. Кристаллическая форма S-зопиклона со спектром порошковой рентгеновской дифракции с использованием Cu-Ка излучения с характерными пиками, выраженными в условиях 2θ приблизительно при 11,08°, приблизительно 12,38°, приблизительно 15,86°, приблизительно 17,88°, приблизительно 19,98° и приблизительно 20,58°; ДСК томограммой, на которой пик находится приблизительно при 207,7°С, и инфракрасным спектром поглощения (ИК) с характерными пиками приблизительно при 3078 см-1, приблизительно 2942-2838 см-1, приблизительно 2790 см-1, приблизительно 1716 см-1, приблизительно 1463 см-1, приблизительно 1372 см-1 и приблизительно 757 см-1.
2. Способ приготовления кристаллической формы S-зопиклона согласно п.1, отличающийся тем, что состоит из следующих этапов:
(a) растворение S-зопиклона в этилацетате температурой от 60°С до температуры рефлюкса, причем используют 10-80 мл этилацетата из расчета на 1 г S-зопиклона;
(b) охлаждение раствора при комнатной температуре до 30-50°С, выдержка при этой температуре в течение от 10 мин до 12 ч;
(c) охлаждение до температуры от 10 до -10°С, выдержка при этой температуре в течение от 10 мин до 12 ч; и
(d) отделение кристаллической формы.
3. Способ по п.2, отличающийся тем, что на этапе (а) используется 25-50 мл этилацетата из расчета на 1 г S-зопиклона; на этапе (b) охлаждение происходит при комнатной температуре до 35-45°С, и выдержка при этой температуре длится в течение 1-6 ч; на этапе (с) происходит охлаждение до температуры от 5 до -5°С, и выдержка при этой температуре длится в течение 1-6 ч.
4. Фармацевтический препарат для лечения нарушения сна, содержащий кристаллическую форму S-зопиклона по п.1 и фармацевтически приемлемый носитель.
5. Фармацевтический препарат по п.4, отличающийся тем, что одна доза фармацевтического препарата содержит 1-15 мг кристаллической формы S-зопиклона.
6. Фармацевтический препарат по п.5, отличающийся тем, что одна доза фармацевтического препарата содержит 3-12 мг кристаллической формы S-зопиклона.
7. Применение кристаллической формы S-зопиклона по п.1 в изготовлении медикамента для лечения нарушения сна.
8. Применение фармацевтического препарата по любому из пп.4-6 в изготовлении медикамента для лечения нарушения сна.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| CN 1854137 A, 01.11.2006 | |||
| TERBLANCHE R.J | |||
| ET AL, "Characterization of Zopiclone Crystal Forms Found Among Generic Raw", Drug development and industrial pharmacy, no.26(5), 2000, p.p.531-537 | |||
| ПРАВОВРАЩАЮЩИЙ ИЗОМЕР 6-(5-ХЛОР-2-ПИРИДИЛ)-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)-5-КАРБОНИЛОКСИ-7-ОКСО-6,7-ДИГИДРО-5Н-ПИРРОЛО-(3,4-B)ПИРАЗИНА И ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ КИСЛОТНО-АДДИТИВНАЯ СОЛЬ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2110519C1 |
Авторы
Даты
2013-09-10—Публикация
2009-04-17—Подача