Изобретение относится к области очистки серебра гидрометаллургическим методом из вторичных материалов, какими являются лом и отходы некоторых видов микроэлектроники. Способ касается очистки серебра от сопутствующих благородных металлов, в частности платины и палладия.
В большинстве известных технологий извлечения серебра из различных видов первичного и вторичного сырья широко представлены способы его первичной обработки в голове процесса окисляющими кислотами (серной, азотной) или их смесями (царской водкой) для его последующего осаждения в виде простого хлорида серебра (AgCl), проводимого введением в растворы хлорсодержащих реагентов в виде хлористого натрия (NaCl) или соляной кислоты (HCl). Такое широкое распространение этот осадительный прием получил из-за крайне малой растворимости AgCl в воде, составляющей величину 1,86×10-4 г/100 мл (И.П. Алимарин, Н.Н. Ушакова. Справочные таблицы по аналитической химии. Изд-во МГУ, 1960 г., с.22-24). Вместе с тем, в производственной практике часто возникает необходимость проведения операций разделения, когда в продуктивном растворе от переработки электронного скрапа после выщелачивания присутствует не только серебро, но и платиноиды. И получение затем целевого осадка хлорида серебра из этих растворов всегда сопряжено с его загрязнением солями платиновых металлов. Эта ситуация типична, поскольку при выделении AgCl происходит соосаждение с ним платины или палладия в форме труднорастворимых хлорокомплексов типа Ag2[MeCl4], где Me=Pt, Pd.
Именно эти обстоятельства требуют проведения довольно трудоемких и длительных стадий для последующей очистки серебра (М.А. Меретуков, А.М. Орлов. Металлургия благородных металлов. // М.: Металлургия, 1991. С.361-362). В результате полученный черновой осадок хлорида серебра затем направляется на выделение металла либо восстановлением пульпы 20%-ным раствором гидразина, либо спеканием с кальцинированной содой (Na2CO3) при высокой температуре. При их исполнении оба эти способа выделения серебра в металлическом состоянии не лишены недостатков. В первом при восстановлении пульпы соединениями гидразина происходит поверхностная металлизация частиц AgCl и прекращение доступа восстановителя в глубь зерна оставшейся соли. Поэтому процесс долго ведут при нагреве и непрерывном перемешивании в довольно концентрированных растворах ядовитого гидрата гидразина (N2H5OH). Во втором требуется плавка под флюсами в дуговых или индукционных печах в течение 1,5-2-х часов при температуре 1150°C.
Главный недостаток данных способов заключается в низком качестве получаемого металлического серебра, содержащего суммарное количество металлов-примесей не менее 2,4-3,0 мас.%.
Известный в металлургии цветных металлов процесс нитрования, который направлен на очистку благородных металлов от основной массы цветных, подробно описан в специальной литературе (И.К. Масленицкий, Л.В. Чугаев., В. Борбат. Металлургия благородных металлов. Изд.2. Металлургия. 1987, с.411-412). Однако использование данного приема для разделения и очистки самих драгоценных металлов в патентной литературе практически не представлено.
Единственным и наиболее близким к предлагаемому способу является выбранный в качестве прототипа способ очистки серебра от сопутствующих благородных металлов и золота (патент RU №2034063 Способ очистки серебра, Мамонов С.Н.; Голубова Е.А.; Золотов А.Ф. // от 30.04.1995). В данном способе-прототипе очистку серебра от примесей платиновых металлов проводят введением в азотнокислый раствор серебра (AgNO3) при нагревании и перемешивании соли нитрита натрия (NaNO2) до pH 3,0-3,5. Осадок нитрита серебра (AgNO2) отделяют, промывают и обрабатывают раствором NaOH до pH пульпы 11,5-12,5. Выделившийся оксид серебра (Ag2O) высушивают и прокаливают с получением металлического серебра. Маточный раствор от осаждения оксида серебра еще один раз используют для повторного осаждения нитрита серебра.
Основным недостатком прототипа является то, что качество очистки и выход целевого продукта, как указывают сами авторы, по данным этого способа сильно зависит от экспериментального задания pH реакционной среды. Это задание величины pH дважды за весь процесс должно осуществляться с высокой точностью. Его точное поддержание требуется сначала для проведения максимально возможного осаждения нитрита серебра. При изменении pH с 3,0 до 2,0 выход падает с 85-92% до 31,5%, а его увеличение сверх 3,5 ухудшает чистоту впоследствии выделяющегося серебра. Строгое соблюдение уровня pH в диапазоне 11,5-12,5 единиц служит целям более полного перевода AgNO2 в Ag2O при возможно меньшем избытке щелочи NaOH. Кроме этого, соль нитрита серебра, через которую проходит предлагаемая в прототипе очистка, является довольно хорошо растворимой и требует последующей рекуперации маточного раствора для более полного его извлечения. Подобный рецикл (возможный по данным авторов только один раз) требует дополнительных трудозатрат и создает временную технологическую задолженность по металлу.
Задачей настоящего изобретения является повышение уровня чистоты серебра при существенном упрощении стадий процесса в целом, при сохранении высокой степени выделения серебра от примеси платины и палладия.
Задача решается тем, что в предлагаемом способе очистки серебросодержащего материала, преимущественно от примесей благородных и цветных металлов, сначала осуществляют растворение серебросодержащего материала в азотной кислоте. Проводят введение нитрита натрия, фильтрование с выделением осадка и последующую переработку с получением металлического серебра. При этом перед выделением карбоната серебра в азотнокислый раствор при перемешивании вводят нитрит натрия и раствор выдерживают в течение 1 часа, затем вводят карбонат или бикарбонат натрия до pH пульпы в интервале 8-10, выделившуюся соль серебра отделяют от раствора фильтрованием при этом нитрит натрия и карбонат или бикарбонат натрия вводят в сухом виде, а нитрит натрия берут с 25%-ным избытком от стехиометрии. Главным отличительным признаком от аналогов и прототипа является использование для выделения и очистки серебра другого его более труднорастворимого соединения, а именно карбоната (Ag2CO3). Это приводит к получению технического результата, при котором осаждение серебра из реакционной смеси проводят однократной обработкой раствора сухим карбонатом натрия (Na2CO3) или бикарбонатом натрия NaHCO3. При достижении значения кислотности раствора в диапазоне pH 8-10 происходит образование лишь соли серебра состава Ag2CO3 - осадка белого цвета. При этом и нитрит натрия, и карбонат натрия или бикарбонат натрия вводят в сухом виде с целью более рационального использования объемов химических реакторов растворения и осаждения. Избыток нитрита натрия обеспечивает полноту разложения исходной азотной кислоты, который может присутствовать из-за непредставительного анализа исходного сырья. Соблюдение данных условий исключает канал его загрязнения путем гидролитического соосаждения платины и палладия из их крайне устойчивых нитритных комплексов (С.И. Гинзбург, Н.А. Езерская и др. Аналитическая химия платиновых металлов. М.: «Наука», 1972, с.61).
Химическое обоснование предлагаемого нами способа, которое помогает решить поставленную цель глубокой очистки серебра от платиновых и некоторых цветных металлов, состоит в большой разнице величин произведения растворимости Пр AgNO2=6.0×10-4 и Пр Ag2CO3=1,2×10-12 (Ю.Ю. Лурье. Справочник по аналитической химии. М., 1979, с.92-101). Кроме этого, очистка от основных примесей цветных металлов, а именно: токоподводящих медных проводов, олова и свинца, как основных компонентов припоя осуществляется на всех стадиях общего передела. Так, при растворении сырья в азотной кислоте олово и свинец переходят в нерастворимый остаток: первое в виде гидратированного диоксида (SnO2×H2O), а второй в виде гидролизованной формы (PbOHNO3). Медь выпадает в твердую фазу, очищая раствор при обработке раствора нитритом натрия, давая осадок комплексного нитрита Na3[Cu(NO2)5].
Поэтому сущность представленного изобретения заключается в последовательном проведении технологических операций для проведения разделения серебра путем осаждения его карбоната. Для этого после растворения серебра и палладия, которое проводят в растворе разведенной азотной кислоты, и последующей ее денитрации осуществляют стадию нитрования по условиям прототипа. Для этого в раствор вносят сухой нитрит натрия, который доводит pH среды до значения 3-4, при котором палладий быстро и количественно переходит в устойчивый к гидролизу нитритный комплекс вида Na2[Pd(NO2)4]. Платина, оставшаяся в нерастворимом остатке, впоследствии обрабатывается более сильными окислительными смесями и выделяется известными способами. В полученную от выщелачивания серебра и палладия реакционную среду вносят при перемешивании навеску сухого карбоната или бикарбоната натрия (Na2CO3, NaHCO3) для образования Ag2CO3 после достижения раствором начального значения pH 8. Перед переработкой отобранные вручную керамические конденсаторы различных модификаций от серии КМ-4,5 до КМ-6Б, имеющие в своем составе драгоценные металлы в количестве (г/1000 штук): серебро 2,48-7,61; платина 12,78-28,35; палладий 13,8-47,65, проходят подготовительную обработку, например, так, как это можно сделать и другими способами. В нашем случае она состоит из трех операций: снятия припоя, отжига и помола. Первая осуществляется, например, путем отгонки припоя в специальной обогреваемой при температуре 280-300°C центрифуге. Вторая, например, на поддонах в электрической печи накаливания при температуре 500-600°C в течение 2-3 часов. После проведения отжига полученный огарок охлаждается, взвешивается и размалывается в шаровой мельнице до крупности частиц 1-2 мм. После этого сырье поступает на отделение и очистку серебра от примесей металлов.
Пример 1
В титановый аппарат объемом 16 л, снабженный водяной рубашкой обогрева от внешнего термостата и якорной мешалкой заливают 3,2 л разведенной (1:1) 57%-ной азотной кислоты, включают нагрев и доводят температуру раствора до 50-60°C. Затем включают перемешивание и производят порционное (по 100-150 г) введение подготовленного сырья общей массы 5200 г, контролируя при этом процесс пенообразования. Перерабатываемый материал по данным усредненного по разным партиям химико-спектрального анализа содержит, мас.%: Ag 1,23; Pt 4,11; Pd 5,25. Аналитически определенное количество основных металлов, входящих в состав контролируемых примесей по ГОСТ 6836-80 «Серебро и серебряные сплавы», составляет: Cu 0,04; Pb 0,06; Sn 0,08.
Завершение растворения серебра и палладия определяют визуально по окончании выделения окислов азота. Нагрев реакционной массы прекращают, а отстоявшийся и охлажденный раствор фильтруют на нутч-фильтре. Отфильтрованный раствор сливают во второй стеклянный реактор, подают горячую воду в змеевик и после достижения температуры 70°C аккуратно проводят денитрацию азотной кислоты этиловым спиртом, протекающую с выделением большого количества газов, как следует из уравнения (1):
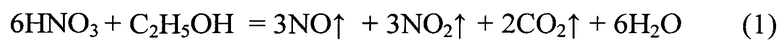
В полученный таким образом охлажденный до комнатной температуры азотнокислый раствор серебра и палладия при перемешивании вводят сухую навеску нитрита натрия (Na(NO)2,) массой 140 г (стехиометрическое количество с 25%-ным избытком) и оставляют на 1 час. Появление окраски светло-желтого цвета указывает на образование в растворе комплекса тетранитропалладоата натрия - Na2[Pd(NO2)4]. В случае незначительной кристаллизации призматических кристаллов в реакционный раствор добавляют дистиллированную воду до их полного растворения. Затем вводят навеску сухого карбоната натрия (Na2CO3), поддерживая pH раствора в интервале 8,0-10, при котором серебро образует кристаллы Ag2CO3 белого цвета по реакции (2):
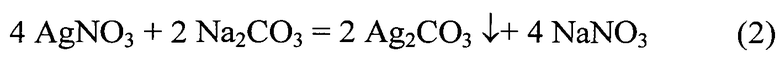
Выпавший осадок Ag2CO3 отделяют, промывают 1%-ным раствором Na2CO3 и сушат на вакуум-фильтре. Выделение металлического серебра из полученного осадка и палладия из маточного раствора проводят известными способами.
Серебряный порошок, полученный таким способом, удовлетворяет требованиям марки Ср 999.
Нерастворимый платиносодержащий остаток от выщелачивания направляют на извлечение и очистку платины.
Пример 2
В химический реактор из титана, описанный в примере 1, загружают подготовленный электронный скрап КМ - массой 7,8 кг и из напорной емкости постепенно, не давая бурно протекать реакции, вливают 6,5 л раствора разведенной в два раза азотной кислоты. По окончании протекания процесса растворения проводят фильтрацию, реакции разложения избытка азотной кислоты и последующее нитрование палладия по условиям примера 1. Синтез карбоната серебра проводят в соответствии с уравнением (3) постепенным введением в раствор необходимой навески бикарбоната натрия (NaHCO3), контролируя вспенивание раствора из-за выделения углекислого газа:
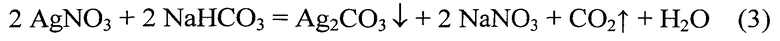
Последующие операции с выделением серебра из осадка Ag2CO3, палладия из этого продуктивного раствора, а платины из содержащего ее осадка проводят известными способами.
Таким образом, материалы данного изобретения представляются небольшим набором стандартных химических операций с соблюдением условий изобретения, не требующих для своего проведения специального оборудования, дефицитных реагентов и квалифицированных кадров. Поэтому данный способ очистки серебра может быть легко и быстро внедрен на любом аффинажном предприятии страны.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АФФИНИРОВАННОГО СЕРЕБРА ИЗ ПРОМПРОДУКТОВ | 1993 |
|
RU2049131C1 |
| СПОСОБ ОЧИСТКИ СЕРЕБРА | 1992 |
|
RU2034063C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ПЛАТИНОВЫХ МЕТАЛЛОВ | 2002 |
|
RU2238244C2 |
| ГИДРОМЕТАЛЛУРГИЧЕСКИЙ СПОСОБ ОТДЕЛЕНИЯ ЗОЛОТА, СЕРЕБРА, ПЛАТИНЫ И ПАЛЛАДИЯ ИЗ СОДЕРЖАЩЕГО ИХ МАТЕРИАЛА С ОДНОВРЕМЕННЫМ ИХ ОБОГАЩЕНИЕМ, ПРЕИМУЩЕСТВЕННО ИЗ СПЛАВА "ДОРЕ" | 1996 |
|
RU2096505C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ СЕРЕБРА ИЗ АЗОТНОКИСЛЫХ АКТИНОИД-СОДЕРЖАЩИХ РАСТВОРОВ (ВАРИАНТЫ) | 2016 |
|
RU2618874C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОДИСПЕРСНОГО УГЛЕКИСЛОГО СЕРЕБРА | 2015 |
|
RU2597377C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЛАГОРОДНЫХ МЕТАЛЛОВ ИЗ ПРОДУКТОВ, СОДЕРЖАЩИХ ХЛОРИД СЕРЕБРА, МЕТАЛЛЫ ПЛАТИНОВОЙ ГРУППЫ И ЗОЛОТО | 1999 |
|
RU2164255C2 |
| СПОСОБ ПЕРЕРАБОТКИ СВИНЕЦ- И СУЛЬФИДСОДЕРЖАЩИХ ШЛИХОВ ЗОЛОТА (ВАРИАНТЫ) | 2000 |
|
RU2196839C2 |
| СПОСОБ ПОЛУЧЕНИЯ СЕРЕБРА И МЕТАЛЛОВ ПЛАТИНОВОЙ ГРУППЫ | 2018 |
|
RU2680552C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ПЛАТИНОВЫХ МЕТАЛЛОВ | 1997 |
|
RU2111272C1 |
Изобретение относится к области очистки серебросодержащих материалов гидрометаллургическим методом, например вторичных материалов, какими являются лом и отходы некоторых видов микроэлектроники. Способ включает растворение серебросодержащего материала в азотной кислоте, введение при перемешивании в азотнокислый раствор нитрита натрия, выделение осадка соли серебра и последующую его переработку с получением металлического серебра. При этом после введения нитрита натрия реакционную смесь выдерживают в течение 1 часа, затем вводят карбонат или бикарбонат натрия до рН пульпы в интервале 8-10. Выделившийся осадок соли серебра в виде карбоната серебра отделяют от раствора фильтрованием. Нитрит натрия и карбонат или бикарбонат натрия вводят в сухом виде, при этом нитрит натрия берут с 25%-ным избытком от стехиометрии. Техническим результатом является повышение чистоты и степени выделения серебра из раствора при существенном упрощении процесса. 1 з.п. ф-лы, 2 пр.
1. Способ очистки серебросодержащего материала от примесей благородных и цветных металлов, включающий растворение серебросодержащего материала в азотной кислоте, введение при перемешивании в азотнокислый раствор нитрита натрия, выделение осадка соли серебра и последующую его переработку с получением металлического серебра, отличающийся тем, что после введения нитрита натрия реакционную смесь выдерживают в течение 1 часа, затем вводят карбонат или бикарбонат натрия до рН пульпы в интервале 8-10, выделившийся осадок соли серебра в виде карбоната серебра отделяют от раствора фильтрованием.
2. Способ по п.1, отличающийся тем, что нитрит натрия и карбонат или бикарбонат натрия вводят в сухом виде, при этом нитрит натрия берут с 25%-ным избытком от стехиометрии.
| СПОСОБ ОЧИСТКИ СЕРЕБРА | 1992 |
|
RU2034063C1 |
| СПОСОБ ПОЛУЧЕНИЯ АФФИНИРОВАННОГО СЕРЕБРА | 2004 |
|
RU2280086C2 |
| RU 2008109262 А, 20.09.2009 | |||
| МОЩНЫЙ CO*002-ЛАЗЕР НА СМЕСИ АТМОСФЕРНОГО ВОЗДУХА С УГЛЕКИСЛЫМ ГАЗОМ | 1995 |
|
RU2086064C1 |
| Способ получения цианурхлорида | 1972 |
|
SU465401A1 |
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
| Способ получения алюминиевых квасцов | 1933 |
|
SU38137A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИМЕЛЛИТОВОГО АНГИДР110 '^^^^«^о- | 0 |
|
SU253048A1 |
Авторы
Даты
2014-04-27—Публикация
2012-05-11—Подача