Уровень техники
Селективное каталитическое восстановление (SCR) оксидов азота, образующихся во время процессов горения, с использованием таких восстановителей, как NH3, было успешной промышленной технологией в течение более 30 лет. Первоначально ее внедряли для регулирования выбросов NOx в отходящих газах из стационарных электростанций и других промышленных предприятий. Недавно интерес к этой технологии возрос в результате ее применимости для обработки выбросов из мобильных источников энергии, таких как морские суда, автомобили, грузовики и машинное оборудование. Этот повышенный интерес в значительной мере стимулирован законодательными постановлениями, которые определяют выбросы из мобильных источников. Например, нормативные документы US ЕРА (Федерального агентства по охране окружающей среды США), которые будут действовать в 2010 году для мобильных дизельных двигателей, устанавливают такие уровни выбросов для NOx, что становится существенной эффективная дополнительная обработка выхлопов, и SCR представляет собой главенствующий технологический вариант.
В стационарных вариантах применения требования к катализатору не очень высоки. Например, стационарные двигатели обычно работают в режиме, близком к стабильному, в условиях постоянной температуры и с относительно низкой объемной скоростью газа. Кроме того, не являются слишком строгими требования к катализатору в отношении его объема. Однако в вариантах применения для дорожных мобильных установок требования к катализаторам являются гораздо более жесткими. В этом случае двигатели не работают в стационарном режиме или при постоянной температуре, но, напротив, их нагрузка (и тем самым температура) варьирует в широких пределах. В одной возможной конфигурации системы SCR-катализатор размещают ниже по потоку относительно дизельного сажевого фильтра (DPF), и регенерация забитого сажей DPF может вызывать прохождение высокотемпературного импульса горячего газа через расположенный ниже по потоку SCR-катализатор. Кроме того, мобильные варианты применения обычно предусматривают гораздо более высокие объемные скорости течения газа, и требования к катализатору в отношении его объема являются жесткими. Например, в ранних вариантах применения в области SCR для высоконагруженных дизельных двигателей объем катализатора был в несколько раз больше, чем рабочий объем двигателя! По этим причинам стала настоятельно необходимой разработка усовершенствованных катализаторов, которые имеют более высокую термостойкость и повышенную объемную активность, чтобы можно было найти экономичные технологические решения для соответствия все ужесточающимся нормативным предписаниям.
Технология, которую использовали в течение многих лет в стационарных вариантах применения, включает катализаторы на основе оксидов металлов, и в особенности таких, которые основаны на TiO2 в качестве носителя катализатора, и с активной каталитической функциональностью на основе оксида ванадия, V2O5. Таким образом, применяли смеси TiO2 (80-95%), WO3 (3-10%) и, необязательно, с остальным количеством, приходящимся на SiO2 (такие как DT-52™ и DT-58™), в качестве носителя катализатора, и активный компонент оксида ванадия обычно присутствует в количестве от 0,1 до 3% по весу. В этих катализаторах диоксид титана первоначально присутствует с относительно высокой площадью поверхности в анатазной форме. Применение и ограничения катализаторов на основе оксида ванадия для мобильных SCR-систем с использованием мочевины описаны в обзоре ″Studies in Surface Science and Catalysis″ (″Исследования в области свойств поверхностей и катализа»), под редакцией Granger, Р. и Parvulescu, V.I., том 171, Глава 9. Есть два соображения относительно высокой стабильности катализатора на основе оксида ванадия. Во-первых, катализаторы могут быть использованы в мобильных установках с компоновкой, где дизельный сажевый фильтр (DPF) размещают выше по потоку относительно SCR-катализатора на основе оксида ванадия. В этой компоновке ванадийоксидный катализатор может подвергаться воздействию экстремальных скачков температуры, связанных с экзотермической регенерацией дизельного сажевого фильтра (DPF). Второе соображение состоит в том, что желательно, чтобы катализатор на основе оксида ванадия сохранял свою каталитическую активность при высоких температурах (например, >550°C), чтобы лучше конкурировать с металлообменными цеолитными катализаторами на основе неблагородных металлов, которые проявляют высокую степень стабильности и активности при высоких температурах. Материал DT-58™ содержит 10% по весу SiO2, 9% по весу WO3 и 81% TiO2, и имеет удельную площадь поверхности около 90 м2/грамм. Однако хорошо известно, что катализаторы на основе диоксида титана и оксида ванадия не являются особенно стабильными термически. Есть несколько мнений относительно этого отсутствия термической стабильности. Во-первых, диоксид титана сам по себе склонен к спеканию при повышенной температуре, что связано с потерей площади поверхности. Во-вторых, диоксид титана при высоких температурах также подвергается преобразованию в рутильную кристаллическую форму, и эта форма в основном представляется менее активным носителем, чем анатазная форма. В-третьих, оксид ванадия без носителя имеет температуру плавления около 675°C, и тем самым, даже будучи нанесенным на носитель из диоксида титана, при повышенных температурах склонен до некоторой степени перемещаться и в конечном счете агрегироваться с образованием кристаллов оксида ванадия с малой площадью поверхности (и меньшей активностью).
По этим причинам настоятельно необходимым является повышение термической стабильности конечного катализатора, и в то же время с сохранением или повышением каталитической активности для селективного каталитического восстановления оксидов азота (SCR-DeNOx) из мобильных двигателей, работающих на обедненных смесях. Одновременное достижение обеих целей является весьма сложной задачей, поскольку часто один фактор может быть улучшен в ущерб другому. Например, описано введение диоксида кремния и/или редкоземельных металлов в диоксид титана для повышения стабильности, но требуется дальнейший прогресс в отношении, как стабильности, так и активности.
Стабилизированный аморфным диоксидом кремния ультратонкий анатазный диоксид титана ранее использовали в качестве катализаторов. Известно, что аморфный диоксид кремния улучшает стабильность анатазной фазы и сохранение удельной площади поверхности ультратонкого анатазного диоксида титана, и поэтому аморфный диоксид кремния представляет собой добавку в промышленные продукты типа DT-58™ и DT-S10™, и эти материалы могут быть использованы в промышленном масштабе в катализе для селективного каталитического регулирования дизельных выбросов, в особенности для DeNOx-вариантов применения.
Ранний патент описывает применение «кремниевой кислоты» для стабилизации анатазного диоксида титана для DeNOx (патент США 4,725,572). Однако при тщательном прочтении этого патента оказывается, что источником диоксида кремния на самом деле является коллоидальный дисперсный кремнезем. Более недавний патент США (U.S. 6956006 В1) также описывает применение коллоидального диоксида кремния для придания анатазному диоксиду титана повышенной термической и гидротермической стабильности. Недавно опубликованная патентная заявка США (U.S. 2007/0129241 А1) обсуждает DeNOx-катализаторы на основе оксида ванадия/диоксида титана с повышенной стабильностью. Использованный в ней источник диоксида кремния также представляет собой коллоидальный кремнезем. Однако эти титаноксидные катализаторы на основе коллоидального кремнезема, как отмечено, не имеют достаточной стабильности и приемлемой активности после воздействия экстремально высокой температуры. Катализаторы на основе диоксида титана, которые сводят к минимуму эти недостатки, нашли бы широкое применение, и были бы преимущественными.
В то время, как вышеупомянутый материал DT-58™ носителя представляет собой прототипный материал носителя для катализаторов дизельных выбросов, улучшенный носитель на основе диоксида титана должен был бы, в общем, быть (1) более термически стабильным, тем самым позволяя разместить его в более тесной близости к двигателю, и (2) более каталитически активным, тем самым обеспечивая возможность применения фильтра с корпусом меньшей величины (скажем, 10 л против 12 л) для содержания катализатора, тем самым оптимизируя (сокращая) размер системы регулирования выбросов.
Настоящее изобретение направлено на получение таких улучшенных титаноксидных носителей, модифицированных диоксидом кремния, и изготовленных из них катализаторов.
Сущность изобретения
Настоящее изобретение описывает композиции и способы получения стабильного ультратонкого анатазного диоксида титана для применения, например, в качестве материала носителя для ванадийоксидных катализаторов, предпочтительно для использования в системе каталитического регулирования выбросов. Стабилизация включает обработку диоксида титана растворимой формой диоксида кремния с низкой молекулярной массой и/или формой из мелких наночастиц (<5 нм), такой как, в предпочтительном варианте исполнения, силикат тетра(алкил)аммония, такой как силикат тетраметиламмония, или кремниевая кислота, которая служит для эффективного сохранения анатазной фазы предотвращения спекания (роста кристаллов) в жестких термических и гидротермических условиях, даже в присутствии оксида ванадия. Новые стабилизированные диоксидом кремния диоксиды титана, объединенные с оксидом ванадия, имеют равную или улучшенную каталитическую активность для селективного каталитического восстановления NOx по сравнению с доступными в настоящее время ванадийоксидными катализаторами на основе диоксида кремния-диоксида титана.
В одном из своих аспектов изобретение предлагает материал носителя катализатора, который включает частицы анатазного диоксида титана, включающие ≥85 весовых процентов в сухом весе TiO2 и ≤10 весовых процентов в сухом весе SiO2, причем SiO2 находится главным образом в форме с низкой молекулярной массой и/или в виде мелких наночастиц. Материал носителя катализатора дополнительно может включать, например, от 3% до 10% WO3, и может иметь удельную площадь поверхности по BET (Брунауэру-Эммету-Теллеру) по меньшей мере 80 м2/грамм. Материал носителя катализатора может включать, например, ≥85% по сухому весу TiO2, 3%-9% SiO2, и 3%-9% по сухому весу WO3. SiO2 может присутствовать со значением парциального монослоя менее 1,0 до того, как материал носителя катализатора подвергают спеканию. SiO2 в форме мелких наночастиц может иметь диаметр <5 нм. Форма SiO2 с низкой молекулярной массой может иметь MW <100000. SiO2 может включать атомы кремния, которые главным образом (то есть, >50%) находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения. SiO2 может включать фрагментарные участки, которые имеют глубину в основном ≤5 нм после перераспределения, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии. Используемый TiO2(необязательно, может быть получен не в присутствии мочевины.
В еще одном аспекте изобретение может представлять собой катализатор на основе оксида ванадия, включающий стабилизированный диоксидом кремния титаноксидный материал носителя катализатора, как он описан здесь, который включает распределенный на нем V2O5. Катализатор на основе оксида ванадия может включать, например, от 0,5% до 5% по сухому весу V2O5 (или, более предпочтительно, от 1,0 до 3%). V2O5 может присутствовать со значением парциального монослоя менее 1,0 перед спеканием. Катализатор на основе оксида ванадия может быть подвергнут спеканию, например, при температуре ≥650°C. В еще одном аспекте изобретение может представлять собой каталитическое устройство для нейтрализации дизельного выхлопа, включающее ванадийоксидный катализатор, как он здесь описан. В еще одном аспекте изобретение может представлять собой систему регулирования дизельного выхлопа, которая включает вышеописанное каталитическое устройство для нейтрализации дизельного выхлопа и дизельный сажевый фильтр, и в которой каталитическое устройство для нейтрализации дизельного выхлопа размещают выше по потоку или ниже по потоку относительно дизельного сажевого фильтра.
В еще одном из своих аспектов изобретение представляет собой способ, которым катализируют превращение оксидов азота в газообразный N2, включающий стадию, в которой выхлопы двигателя, включающие NOx, подвергают воздействию ванадийоксидного катализатора, описываемого здесь, с добавленным восстановителем для образования N2 и H2O. Восстановитель может представлять собой, например, NH3 и/или мочевину. В этом способе катализатор на основе оксида ванадия может включать, например, 0,5%-5% (или, более предпочтительно, от 1,0% до 3%) по сухому весу V2O5. Выхлопы двигателя могут быть пропущены через дизельный сажевый фильтр до или после обработки катализатором на основе оксида ванадия.
В еще одном из своих аспектов изобретение представляет собой способ получения материала носителя катализатора, включающий стадии, в которых получают суспензию, включающую TiO2, объединяют TiO2-суспензию с (1) раствором прекурсора диоксида кремния, включающим SiO2 главным образом в форме с низкой молекулярной массой и/или SiO2, включающий мелкие наночастицы, и с (2) WO3 с образованием смеси TiO2-WO3-SiO2, причем раствор прекурсора диоксида кремния объединяют с TiO2-суспензией до, после или в то время, когда WO3 объединяют с TiO2-суспензией, и затем смесь TiO2-WO3-SiO2 промывают, и подвергают спеканию с образованием стабилизированного диоксидом кремния титаноксидного материала носителя катализатора. В этом способе стабилизированный диоксидом кремния титаноксидный материал носителя катализатора может включать, например, 86%-94% по сухому весу TiO2, 3%-9% по сухому весу SiO2, и 3%-7% по сухому весу WO3, и титаноксидный материал носителя перед спеканием может иметь удельную площадь поверхности главным образом по меньшей мере 80 м2/грамм. TiO2 в суспензии может включать, например, частицы предварительно образованного гидроксида титана, оксигидроксида титана или диоксида титана. Необязательно, TiO2 в суспензии не получают в присутствии мочевины. Мелкие наночастицы, сформированные из SiO2, в растворе прекурсора диоксида кремния главным образом могут иметь диаметр <5 нм. Форма SiO2 с низкой молекулярной массой в растворе прекурсора диоксида кремния главным образом может иметь MW <100000. SiO2 в растворе прекурсора диоксида кремния может включать атомы кремния, которые главным образом (то есть, >50%) находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения. Раствор прекурсора диоксида кремния может включать раствор силиката тетра(алкил)аммония или кремниевую кислоту. SiO2 главным образом может включать фрагментарные участки, которые имеют глубину ≤5 нм после перераспределения, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии. Способ дополнительно может включать стадию, в которой смесь TiO2-WO3-SiO2 объединяют с V2O5 с образованием ванадийоксидного катализатора. Сформированный таким образом ванадийоксидный катализатор может включать, например, от 0,5% до 3% до 5% по сухому весу V2O5. V2O5 на нем может присутствовать со значением фрагментарного монослоя менее 1,0 до спекания. Ванадийоксидный катализатор может быть подвергнут спеканию, например, при температуре ≥650°C.
В еще одном аспекте изобретение обеспечивает способ получения стабилизированного диоксидом кремния титаноксидного материала носителя катализатора, включающий стадии, на которых получают TiO2-суспензию, включающую частицы TiO2, получают источник дисперсного диоксида кремния, объединяют TiO2-суспензию с источником дисперсного диоксида кремния с образованием смеси TiO2-SiO2, и доводят величину pH смеси TiO2-SiO2 до уровня <8,5 и температуру до <80°C, причем источник дисперсного диоксида кремния растворяют и переосаждают на частицах TiO2 с образованием стабилизированного диоксидом кремния титаноксидного материала носителя катализатора. Способ дополнительно может включать стадию, на которой объединяют стабилизированный диоксидом кремния титаноксидный материал носителя катализатора с WO3 с образованием стабилизированного диоксидом кремния титаноксид-вольфрамового материала носителя катализатора. Способ дополнительно может включать стадию, на которой стабилизированный диоксидом кремния титаноксид-вольфрамовый материал носителя катализатора промывают, и подвергают спеканию. Стабилизированный диоксидом кремния титаноксид-вольфрамовый материал носителя катализатора может включать, например, 86%-94% по сухому весу TiO2, 3%-9% по сухому весу SiO2, и 3%-7% по сухому весу WO3, и титаноксидный материал носителя перед спеканием может иметь удельную площадь поверхности главным образом по меньшей мере 80 м2/грамм. Частицы TiO2 в TiO2-суспензии могут включать, например, частицы предварительно образованного гидроксида титана, оксигидроксида титана или диоксида титана. Частицы TiO2 в TiO2-суспензии необязательно получают не в присутствии мочевины. SiO2 в смеси TiO2-SiO2 после растворения может включать атомы кремния, которые главным образом (то есть, >50%) находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения. Согласно способу, SiO2 на частицах TiO2 главным образом включает фрагментарные участки, которые имеют глубину ≤5 нм после перераспределения SiO2, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии. Способ дополнительно может включать стадию, в которой смесь TiO2-WO3-SiO2 объединяют с V2O5 с образованием ванадийоксидного катализатора. В этом способе ванадийоксидный катализатор может включать, например, от 0,5%-3% по сухому весу V2O5. V2O5 в ванадийоксидном катализаторе может присутствовать со значением фрагментарного монослоя менее 1,0 до спекания, и ванадийоксидный катализатор может быть подвергнут спеканию, например, при температуре ≥650°C.
Настоящий документ раскрывает по меньшей мере следующие объекты.
Объект 1. Материал носителя катализатора, включающий:
частицы анатазного диоксида титана, включающие ≥85% по сухому весу TiO2 и ≤10% по сухому весу SiO2, причем SiO2 находится главным образом в форме с низкой молекулярной массой и/или в форме мелких наночастиц.
Объект 2. Материал носителя катализатора в соответствии с Объектом 1, дополнительно включающий от 3% до 10% WO3.
Объект 3. Материал носителя катализатора в соответствии с Объектом 2, в котором удельная площадь поверхности по БЭТ составляет по меньшей мере 80 м2/грамм.
Объект 4. Материал носителя катализатора в соответствии с Объектом 1, включающий ≥85% по сухому весу TiO2, 3%-9% SiO2 и 3%-9% по сухому весу WO3.
Объект 5. Материал носителя катализатора в соответствии с объектом 1, в котором SiO2 присутствует со значением парциального монослоя менее 1,0 до спекания материала носителя катализатора.
Объект 6. Материал носителя катализатора в соответствии с Объектом 1, в котором SiO2 в форме мелких наночастиц имеет диаметр <5 нм.
Объект 7. Материал носителя катализатора в соответствии с Объектом 1, в котором SiO2 в форме с низкой молекулярной массой имеет молекулярную массу <100000.
Объект 8. Материал носителя катализатора в соответствии с Объектом 1, в котором SiO2 включает атомы кремния, которые главным образом находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения.
Объект 9. Материал носителя катализатора в соответствии с Объектом 1, в котором SiO2 включает фрагментарные участки, которые имеют глубину по существу ≤5 нм после перераспределения, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии.
Объект 10. Материал носителя катализатора в соответствии с Объектом 1, в котором TiO2 не был получен в присутствии мочевины.
Объект 11. Катализатор на основе оксида ванадия, включающий:
материал носителя катализатора в соответствии с Объектом 2, имеющий распределенный на нем V2O5.
Объект 12. Катализатор на основе оксида ванадия в соответствии с Объектом 11, включающий от 0,5% до 5% по сухому весу V2O5.
Объект 13. Катализатор на основе оксида ванадия в соответствии с Объектом 11, в котором V2O5 присутствует на нем со значением парциального монослоя менее 1,0 перед спеканием.
Объект 14. Катализатор на основе оксида ванадия в соответствии с Объектом 11, который был подвергнут спеканию при температуре ≥650°C.
Объект 15. Каталитическое устройство для нейтрализации дизельного выхлопа, включающее катализатор на основе оксида ванадия в соответствии с Объектом 11.
Объект 16. Система регулирования дизельного выхлопа, включающая:
каталитическое устройство для нейтрализации дизельного выхлопа в соответствии с Объектом 15; и
дизельный сажевый фильтр, и при этом каталитическое устройство для нейтрализации дизельного выхлопа размещают выше по потоку или ниже по потоку относительно дизельного сажевого фильтра.
Объект 17. Способ, в котором катализируют конверсию оксидов азота в газообразный N2, включающий:
воздействие на дизельные выхлопы, включающие NOx, катализатором на основе оксида ванадия в соответствии с Объектом 11, с добавленным восстановителем для образования N2 и H2O.
Объект 18. Способ в соответствии с Объектом 17, в котором восстановитель представляет собой NH3 и/или мочевину.
Объект 19. Способ в соответствии с Объектом 17, в котором катализатор на основе оксида ванадия включает 0,5%-3% по сухому весу V2O5.
Объект 20. Способ в соответствии с Объектом 17, в котором дизельные выхлопы пропускают через дизельный сажевый фильтр до или после воздействия катализатора на основе оксида ванадия.
Объект 21. Способ получения материала носителя катализатора, включающий стадии, на которых:
готовят суспензию, содержащую TiO2;
объединяют TiO2-суспензию с (1) раствором прекурсора диоксида кремния, содержащим SiO2 главным образом в форме с низкой молекулярной массой и/или SiO2, включающий мелкие наночастицы, и с (2) WO3 с образованием смеси TiO2-WO3-SiO2; причем раствор прекурсора диоксида кремния объединяют с TiO2-суспензией до, после или в то время, когда WO3 объединяют с TiO2-суспензией, и
промывают и подвергают спеканию смесь TiO2-WO3-SiO2 с образованием стабилизированного диоксидом кремния титаноксидного материала носителя.
Объект 22. Способ в соответствии с Объектом 21, в котором стабилизированный диоксидом кремния титаноксидный материал носителя включает
86%-94% по сухому весу TiO2, 3%-9% по сухому весу SiO2, и 3%-7% по сухому весу WO3; и в котором титаноксидный материал носителя первоначально имеет удельную площадь поверхности по меньшей мере 80 м2/грамм перед спеканием.
Объект 23. Способ в соответствии с Объектом 21, в котором TiO2 в суспензии включает предварительно сформированные частицы гидроксида титана, оксигидроксида титана или диоксида титана.
Объект 24. Способ в соответствии с Объектом 21, в котором TiO2 в суспензии получен не в присутствии мочевины.
Объект 25. Способ в соответствии с Объектом 21, в котором SiO2 в форме мелких наночастиц в растворе прекурсора диоксида кремния главным образом имеет диаметр <5 нм.
Объект 26. Способ в соответствии с Объектом 21, в котором SiO2 в форме с низкой молекулярной массой в растворе прекурсора диоксида кремния главным образом имеет MW <100000.
Объект 27. Способ в соответствии с Объектом 21, в котором SiO2 в растворе прекурсора диоксида кремния включает атомы кремния, которые главным образом находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения.
Объект 28. Способ в соответствии с Объектом 21, в котором раствор прекурсора диоксида кремния включает раствор силиката тетра(алкил)аммония или кремниевую кислоту.
Объект 29. Способ в соответствии с Объектом 21, в котором SiO2 главным образом включает фрагментарные участки, которые имеют глубину ≤5 нм после перераспределения, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии.
Объект 30. Способ в соответствии с Объектом 21, включающий стадию, в которой объединяют смесь TiO2-WO3-SiO2 с V2O5 с образованием катализатора на основе оксида ванадия.
Объект 31. Способ в соответствии с Объектом 30, в котором катализатор на основе оксида ванадия включает 0,5%-3% по сухому весу V2O5.
Объект 32. Способ в соответствии с Объектом 30, в котором V2O5 в катализаторе на основе оксида ванадия присутствует со значением парциального монослоя менее 1,0 перед спеканием.
Объект 33. Способ в соответствии с Объектом 30, включающий дополнительную стадию, на которой катализатор на основе оксида ванадия подвергают спеканию при температуре ≥650°C.
Объект 34. Способ получения стабилизированного диоксидом кремния титаноксидного материала носителя катализатора, включающий стадии, на которых:
готовят TiO2-суспензию, содержащую частицы TiO2;
готовят источник дисперсного диоксида кремния;
объединяют TiO2-суспензию с источником дисперсного диоксида кремния с образованием TiO2-SiO2-смеси; и
доводят значение pH TiO2-SiO2-смеси до <8,5 и температуру до <80°C, причем источник дисперсного диоксида кремния растворяют и переосаждают на частицах TiO2 с образованием стабилизированного диоксидом кремния титаноксидного материала носителя катализатора.
Объект 35. Способ в соответствии с Объектом 34, дополнительно включающий стадию, на которой объединяют стабилизированный диоксидом кремния титаноксидный материал носителя катализатора с WO3 для получения стабилизированного диоксидом кремния титаноксид-вольфрамового материала носителя катализатора.
Объект 36. Способ в соответствии с Объектом 35, дополнительно включающий стадии, на которых стабилизированный диоксидом кремния титаноксид-вольфрамовый материал носителя катализатора промывают и подвергают спеканию.
Объект 37. Способ в соответствии с Объектом 35, в котором стабилизированный диоксидом кремния титаноксид-вольфрамовый материал носителя катализатора включает:
86%-94% по сухому весу TiO2, 3%-9% по сухому весу SiO2, и 3%-7% по сухому весу WO3; и в котором титаноксидный материал носителя первоначально имеет удельную площадь поверхности по меньшей мере 80 м2/грамм перед спеканием.
Объект 38. Способ в соответствии Объектом 34, в котором частицы TiO2 в TiO2-суспензии включают предварительно сформированные частицы гидроксида титана, оксигидроксида титана или диоксида титана.
Объект 39. Способ в соответствии с Объектом 34, в котором частицы TiO2 в TiO2-суспензии получены не в присутствии мочевины.
Объект 40. Способ в соответствии с Объектом 34, в котором SiO2 в TiO2-SiO2-смеси, после растворения, включает атомы кремния, которые находятся главным образом в состояниях Q3, Q2, Q1 и Q0 координационного окружения.
Объект 41. Способ в соответствии с Объектом 34, в котором SiO2 на частицах TiO2 главным образом включает фрагментарные участки, которые имеют глубину ≤5 нм после перераспределения SiO2, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии.
Объект 42. Способ в соответствии с Объектом 35, включающий стадию, на которой объединяют смесь TiO2-WO3-SiO2 с V2O5 с образованием катализатора на основе оксида ванадия.
Объект 43. Способ в соответствии с Объектом 42, в котором катализатор на основе оксида ванадия включает 0,5%-3% по сухому весу V2O5.
Объект 44. Способ в соответствии с Объектом 42, в котором V2O5 катализатора на основе оксида ванадия присутствует со значением парциального монослоя менее 1,0 перед спеканием.
Объект 45. Способ в соответствии с Объектом 42, включающий дополнительную стадию, на которой катализатор на основе оксида ванадия подвергают спеканию при температуре ≥650°C.
Другие аспекты изобретения станут очевидными после рассмотрения нижеприведенного описания.
Краткое описание чертежей
Фигура 1 представляет график, показывающий влияние температуры кальцинирования на удельную площадь поверхности ванадийоксидного катализатора.
Фигура 2 представляет график, показывающий влияние температуры кальцинирования на процентное содержание анатазной фазы диоксида титана в ванадийоксидных катализаторах.
Фигура 3 представляет график, показывающий влияние температуры кальцинирования на DeNox-активность 1%-ных ванадийоксидных катализаторов.
Фигура 4 представляет график, показывающий влияние температуры кальцинирования на DeNox-конверсию 3%-ных ванадийоксидных катализаторов.
Фигура 5 представляет график, показывающий влияние температуры на DeNox-активность разнообразных ванадийоксидных катализаторов.
Фигура 6 представляет график, показывающий влияние температуры на удельную площадь поверхности носителя катализатора согласно настоящему изобретению сравнительно с традиционным носителем катализатора.
Фигура 7 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию кремнийоксид-вольфрамоксид-титаноксидного катализатора из Примера 6, показывающую двумерные фрагментарные участки диоксида кремния <2 нм глубиной на поверхности диоксида титана.
Фигура 8 представляет полученную с помощью сканирующей электронной микроскопии микрофотографию ванадийоксид-титаноксидного катализатора из Примера 10, показывающую распределенные на нем частицы коллоидального диоксида кремния с величиной ~20 нм.
Фигура 9 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию катализатора, показывающую частицы коллоидального диоксида кремния с величиной ~20 нм на наружной поверхности ванадийоксид-титаноксидного катализатора из Примера 10.
Фигура 10 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию частиц катализатора из Примера 11, показывающую кристаллы анатаза с фрагментарным двумерным слоем из диоксида кремния на наружной поверхности кристаллов. В этом изображении частицы диоксида кремния не наблюдаются.
Фигура 11 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию частиц катализатора из Примера 11, показывающую кристаллы анатаза с фрагментарным двумерным слоем из диоксида кремния на наружной поверхности кристаллов. В этом изображении можно видеть одну оставшуюся частицу диоксида кремния, которая имеет диаметр <5 нм.
Фигура 12 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию частиц катализатора из Примера 12, показывающую мелкие двумерные фрагментарные участки из диоксида кремния на анатазных кристаллитах.
Фигура 13 представляет полученную с помощью трансмиссионной электронной микроскопии микрофотографию кремнийоксидных фрагментарных участков, присутствующих на поверхности частиц катализатора из анатазного диоксида титана согласно Примеру 13.
Фигура 14 представляет полученную с помощью трансмиссионной электронной микроскопии микрофотографию кремнийоксидных фрагментарных участков, присутствующих на поверхности частиц катализатора из анатазного диоксида титана согласно Примеру 13.
Фигура 15 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию носителя катализатора перед добавлением оксида ванадия и спеканием. Изображение показывает края кристаллической решетки, связанные с анатазным диоксидом титана; диоксид кремния присутствует в виде фрагментарных участков с величиной 1-3 нм на поверхности диоксида титана (Пример 14).
Фигура 16 представляет полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию ванадийоксидного катализатора, которая показывает крупные (>20 нм) трехмерные включения диоксида кремния (смотри стрелки), которые плохо диспергированы на поверхности диоксида титана (например, Пример 15).
Фигура 17 представляет еще одну полученную с помощью трансмиссионной электронной микроскопии (ТЕМ) микрофотографию ванадийоксидного катализатора, которая показывает крупные (>20 нм), трехмерные включения диоксида кремния (смотри стрелки), которые плохо диспергированы на поверхности диоксида титана (например, Пример 15).
Фигура 18 представляет график, показывающий влияние разнообразных температур кальцинирования (активации) на deNox-каталитические активности форм ванадиевых катализаторов на носителе из диоксида титана.
Подробное описание изобретения
Первоочередной целью настоящего изобретения является получение стабильного, имеющего высокую удельную площадь поверхности титаноксидного материала носителя в анатазной кристаллической форме, главным образом для использования в качестве носителя для оксида ванадия (V2O5) в вариантах применения как катализатора для регулирования дизельного выхлопа. Стабилизация включает обработку диоксида титана диоксидом кремния в форме с низкой молекулярной массой и/или в форме мелких наночастиц, таким как растворимый прекурсорный силикат тетра(алкил)аммония (то есть, силикат тетраметиламмония) или тетраэтилортосиликат (TEOS). Другие примеры прекурсоров диоксида кремния с низкой молекулярной массой, которые могут быть использованы в настоящем изобретении, включают, но не ограничиваются таковыми, водные растворы галогенидов кремния (то есть, безводные SiX4, где X=F, Cl, Br или I), алкоксиды кремния (то есть, Si(OR)4, где R=метил, этил, изопропил, пропил, бутил, изобутил, втор-бутил, трет-бутил, пентилы, гексилы, октилы, нонилы, децилы, ундецилы и додецилы, например), прочие кремнийорганические соединения, такие как гексаметилдисилазан, соли фторкремниевой кислоты, такие как гексафторсиликат аммония [(NH4)2SiF6], растворы четвертичных силикатов аммония (например, (NR4)n, (SiO2), где R=H, или алкилы, такие как перечислено выше, и где n=0,1-2, например), водные растворы силиката натрия и калия (Na2SiO3, K2SiO3, и MSiO3, в которых М представляет Na или К в разнообразных количествах относительно Si), кремниевую кислоту (Si(OH)4), образованную ионным обменом любой из катионных форм оксида кремния, перечисленных здесь, с использованием кислотной ионообменной смолы (например, ионный обмен растворов силикатов щелочных металлов или растворов четвертичного силиката аммония).
Термин «форма с низкой молекулярной массой» диоксида кремния имеет отношение к частицам диоксида кремния, имеющим молекулярную массу (MW) менее чем около 100000. Термин «форма мелких наночастиц» имеет отношение к частицам диоксида кремния, имеющим диаметр <5 нм.
Акцент на улучшение термической/гидротермической стабильности для катализаторов на основе оксида ванадия является относительно новым, поскольку этот сегмент рынка мобильных устройств для регулирования выбросов пока только развивается. И только после того, как авторы настоящего изобретения провели обширное обследование традиционных катализаторов, выяснилось, что оптимизация катализаторов на основе оксида ванадия ставит условием, что (1) необходимо свести к минимуму общий уровень содержания диоксида кремния, и что (2) такие формы диоксида кремния, как растворимая форма с низкой молекулярной массой и/или форма мелких наночастиц, были наиболее эффективными в плане обеспечения требуемой стабильности и активности.
Материалы носителей катализаторов согласно настоящему изобретению проявляют необыкновенное сохранение анатазной фазы диоксида титана и удельной площади поверхности после жестких термических и/или гидротермических обработок, даже в присутствии оксида ванадия. В составах и способах получения согласно изобретению используют формы с низкой молекулярной массой и/или мелкие наночастицы диоксида кремния для получения исключительно ультратонкой анатазной фазы диоксида титана и стабильности удельной площади поверхности, тогда как конечный ванадийоксидный катализатор демонстрирует равную или повышенную каталитическую активность в отношении основанного на оксиде ванадия селективного каталитического восстановления NOx после ускоренного старения. Такие составы и способы ранее не были известны в технологии.
Два ключевых аспекта настоящего изобретения, которые отличают его от прототипа, включают природу аморфного диоксида кремния и способ, каковым его вводят в диоксид титана.
Что касается природы аморфного диоксида кремния, сначала необходимо провести различие между дисперсными формами аморфного диксида кремния и растворенными или газофазными формами, которые составлены аморфными силикатными мономерами или кластерами с очень низкой молекулярной массой, которые не рассматриваются как дисперсная форма, или включают очень мелкие наночастицы. Формы диоксида кремния, пригодные для настоящего изобретения, описаны здесь и называются «диоксид кремния с низкой молекулярной массой и/или из мелких (<5 нм) наночастиц». Два литературных источника, которые описывают типы аморфного диоксида кремния, представляют собой ″Ullmann′s Encyclopedia of Industrial Chemistry″ («Энциклопедия промышленной химии Ульмана»), пятое издание, том А23, стр.583-660, (1993), и ″The Chemistry of Silica″ («Химия кремнезема») автора R.К. Iler, 1979. Например, одной формой дисперсного аморфного диоксида кремния является коллоидальный кремнезем, или силиказоль. Этот тип диоксида кремния состоит из суспензий плотных, дискретных аморфных частиц диоксида кремния, которые имеют диаметры в диапазоне размеров между около 5 нм и 100 нм. В этом размерном диапазоне частицы обычно рассеивают видимый свет и, таким образом, образуют суспензии от мутных до непрозрачных. Обычно эти частицы также можно проанализировать методами рассеяния видимого света с использованием общедоступных на рынке приборов. Как будет видно из приведенных ниже примеров, без дополнительной модификации коллоидальный диоксид кремния в дисперсной форме (>5 нм) не является формой диоксида кремния, пригодной для настоящего изобретения. Одна причина того, что эта форма диоксида кремния является нежелательной (без последующего модифицирования) согласно настоящему изобретению, состоит в том, что большая часть массы диоксида кремния находится внутри частицы, и недоступна на поверхности для взаимодействия с титаноксидным субстратом. Так, согласно автору Iler (уже цитированная работа, стр.8), частицы аморфного диоксида кремния с диаметром 5 нм имеют 1500 силикатных атомов, и 37% из этих силикатных атомов находятся на поверхности частицы, тогда как в частице с размером 1 нм почти все силикатные атомы находятся на поверхности. Таким образом, для целей настоящего изобретения желательно использовать источники диоксида кремния, которые главным образом включают частицы, которые имеют диаметры <5 нм, и/или которые имеют низкие молекулярные массы, например, у которых MW составляет <100000, и тем самым являются доступными для взаимодействия с диоксидом титана. Исключением, как будет описано ниже, является последующее модифицирование дисперсного диоксида кремния с использованием условий pH и температуры, при котором дисперсный диоксид кремния растворяли, и переосаждали на поверхность диоксида титана.
Подразумевается, что термин «главным образом», где он используется в данной заявке, означает, что более 50% обсуждаемого процесса или материала имеют конкретную характеристику или состояние, на которые делается ссылка.
Например, как отмечено выше, в предпочтительном варианте осуществления настоящего изобретения материал носителя катализатора включает диоксид кремния, который главным образом находится в форме с низкой молекулярной массой и/или в форме мелких наночастиц. Этим подразумевается, что свыше 50% диоксида кремния находится либо в форме с низкой молекулярной массой (MW <100000), либо в форме мелких наночастиц (диаметр <5 нм), или представляет собой комбинацию обеих форм. В более предпочтительном варианте диоксид кремния включает >60% форм с низкой молекулярной массой и/или форм мелких наночастиц. В еще более предпочтительном варианте диоксид кремния включает >70% форм с низкой молекулярной массой и/или форм мелких наночастиц. В еще более предпочтительном варианте диоксид кремния включает >80%, и дополнительно еще более предпочтительно >90% форм с низкой молекулярной массой и/или форм мелких наночастиц диоксида кремния.
Кроме того, формы с низкой молекулярной массой или мелких наночастиц согласно настоящему изобретению предпочтительно имеют величины удельной геометрической площади поверхности >450 м2/г.
Дисперсные формы диоксида кремния (то есть, в которых диаметр составляет >5 нм) включают силикагель, осажденный кремнезем и пирогенный кремнезем. В то время как первичные частицы плотного, аморфного диоксида кремния в этих дисперсных формах могут быть очень мелкими (например, 2,5 нм), первичные частицы необратимо агломерируются друг с другом с образованием гораздо более крупных вторичных частиц, размеры которых могут варьировать от сотен нанометров до многих микрометров в диаметре. Очевидно, что большая часть силикатных атомов в этих вторичных частицах не является приближенной к поверхности и доступной для взаимодействия с диоксидом титана. Конечно, эти вторичные частицы легко проанализировать с использованием методов рассеяния видимого света, и, находясь в суспензии, частицы делают ее довольно непрозрачной. Дисперсный диоксид кремния в любой из этих форм, без последующего модифицирования, также непригоден для настоящего изобретения.
Один класс прекурсора диоксида кремния, который пригоден для настоящего изобретения, представляет собой высокощелочные растворы, называемые «водорастворимые силикаты». Они описаны автором Iler (приведенная выше ссылка, Глава 2). Эти растворы обычно прозрачны, поскольку частицы диоксида кремния, если присутствуют, в основном слишком малы, чтобы рассеивать видимый свет. Однако, в зависимости от концентрации диоксида кремния или щелочности, в этих растворах могут формироваться мелкие частицы диоксида кремния. Автор Iler (вышеприведенная ссылка, стр.133) приводит оценку, что для молярного отношения «SiO2:Na2O» на уровне 3,1 среднее число фрагментов SiO2 на частицу в разбавленных растворах составляет около 900, что является меньшим, чем 1500 силикатных фрагментов в вышеописанной частице с размером 5 нм. Такой силикатный прекурсор, даже если он может содержать некоторые наночастицы крупнее примерно 5 нм, пригоден для настоящего изобретения, поскольку большинство массы диоксида кремния находится в форме более мелких частиц с низкой молекулярной массой. Однако силикаты щелочных металлов не являются наиболее предпочтительной формой для настоящего изобретения, поскольку остаточные ионы щелочных металлов, такие как Na, являются исключительно эффективными каталитическими ядами для SCR-катализаторов на основе оксида ванадия.
Недавно природа наночастиц аморфного диоксида кремния в щелочных растворах более подробно была исследована авторами Fedeyko и др., (″Langmuir″, 2005, том 21, стр.5197-5206). Эти авторы использовали многочисленные способы, включая малоугловое рентгеновское рассеяние (SAXS) и малоугловое рассеяние нейтронов (SANS). Эти методы способны регистрировать присутствие наночастиц вплоть до размеров от около 2 до 3 нм. Авторы показали, что в разбавленном растворе, когда отношение [OH]/[SiO2] составляет менее чем около 1, диоксид кремния образует мелкие наночастицы, тогда как при [OH]/[SiO2] свыше 1 диоксид кремния присутствует в виде мономеров и олигомеров, которые слишком малы для обнаружения в экспериментах по рассеянию излучения. Этот последний тип частиц аморфного диоксида кремния, в основном слишком мелок для легкого детектирования методами рассеяния видимого света и рентгеновского излучения, который в настоящем изобретении называется «аморфный диоксид кремния с низкой молекулярной массой и/или из мелких наночастиц», и они являются предпочтительными формами диоксида кремния для настоящего изобретения.
Одним полезным средством для охарактеризования мономеров и олигомеров диоксида кремния в растворе является 29Si-ядерный магнитный резонанс (например, смотри Главу 3 в книге ″High Resolution Solid-State NMR of Silicates and Zeolites″ («Твердофазный ЯМР высокого разрешения силикатов и цеолитов») авторов G. Engelhardt и D. Michel, 1987). Метод может дать информацию об обычном тетраэдрическом координационном окружении атома Si, содержит ли Si или нет один или более смежных ближайших Si-соседей (связанных мостиковыми атомами кислорода). Обозначение, которое обычно используют для описания этой координации, является следующим: Q0 имеет отношение к центральному атому Si, не имеющему смежных ближайших Si-соседей, то есть, Si(ОН)4; Q1 относится к центральному атому Si с одним смежным ближайшим Si-соседом, то есть, Si(ОН)3(OSi)1; Q2 означает центральный атом Si с двумя смежными ближайшими Si-соседями, то есть, Si(ОН)2(OSi)2; Q3 имеет отношение к центральному Si-атому с тремя смежными ближайшими Si-соседями, то есть, Si(ОН)1(OSi)3; и Q4 относится к центральному Si-атому с четырьмя смежными ближайшими Si-соседями, то есть, Si(OSi)4.
Без намерения вдаваться в теорию, представляется, что для непосредственного использования (без дополнительной обработки для изменения формы диоксида кремния) желательным является применение растворов силикатов, которые состоят главным образом из олигомеров от Q0 до Q3. С другой стороны, растворы силикатных олигомеров, которые почти полностью состоят из Q4-частиц, нежелательны для настоящего изобретения. В принципе, это обосновывается тем, что для последних типов силикатных олигомеров основная часть диоксида кремния полностью окружена другими силикатными частицами, и тем самым недоступна для реакции с поверхностью диоксида титана, где она наиболее нужна для стабилизации анатаза.
Одна форма диоксида кремния, которая пригодна для применения в настоящем изобретении, представляет собой имеющийся в продаже на рынке щелочный раствор силиката тетраметиламмония. Понимание природы этого раствора может быть основано на более раннем исследовании. Авторы Engelhardt и Michel (вышеуказанная ссылка, стр.92) описывают исследование методом 29Si-ядерного магнитного резонанса 1М раствора SiO2 (приблизительно 6% по весу) с соотношением TMA/Si=1,0, что примерно эквивалентно концентрации ТМАОН (гидроксида тетраметиламмония) на уровне 9% по весу. В этом растворе диоксид кремния находится главным образом в форме кубического октамера, который содержит 8 атомов кремния, и они имеют Q3-координацию. Эти мелкие частицы составляют около 90% массы диоксида кремния. Реальный раствор силиката ТМА (тетраметиламмония), используемый в примерах настоящего изобретения, имеет несколько более высокую концентрацию диоксида кремния (9% по весу) и меньшую концентрацию ТМАОН (7% по весу), и тем самым распределение силикатных частиц несколько отличается от вышеуказанного литературного сообщения, как показано ниже в Таблице 6.
Еще одна форма диоксида кремния, которая пригодна для настоящего изобретения, представляет собой «кремниевую кислоту». Этот тип диоксида кремния описан в работе автора Iler (вышеуказанная ссылка, Глава 3). Более подробное охарактеризование кремниевой кислоты проведено с использованием метода 29Si-ядерного магнитного резонанса, как описано авторами G. Engelhardt и D. Michel (вышеуказанная ссылка, стр.100). Эта форма диоксида кремния может быть получена подкислением щелочных растворов силикатов, например, путем ионного обмена с использованием кислотных ионообменных смол.
Концепция парциального монослоя.
Представляет интерес демонстрация того, что составы и способы настоящего изобретения отличаются от прототипных примеров, и одно средство сделать это включает идею парциального монослойного покрытия поверхности субстрата добавленным оксидом. В приведенных ниже определениях подстрочный индекс «х» обозначает обсуждаемый добавленный оксид, например, диоксид кремния.
Сх=количество добавленного оксида в расчете на площадь поверхности для цельного монослойного покрытия, г/м2;
SA=площадь поверхности смешанного оксида;
Мх=количество добавленного оксида в расчете на массу для цельного монослойного покрытия; г/г смешанного оксида;
Lx=реальное количество добавленного оксида, нанесенного на смешанный оксид, г/г;
FMx=парциальный монослой добавленного оксида на состаренном смешанном оксиде;
TFM=парциальный монослой в целом на состаренном смешанном оксиде.
Mx=Cx×SA Уравнение 1).
FMx=Lx/Mx (Уравнение 2)
TFM=Sum(FMx) (Уравнение 3)
Во-первых, необходимо наилучшим образом оценить степень, Сх, монослойного покрытия идеально диспергированных добавленных оксидов на субстрате из оксида титана или подобных оксидов. Для оксида ванадия литературное значение для монослойного покрытия несущего оксида составляет 7-8 V-атомов/нм2, что соответствует 1100 микрограммов V2O5/м2. (Смотри работу авторов I.Е. Wachs и др., 2003). Для оксида вольфрама использовали литературное значение 4,5 W-атома/нм2 (I.E. Wachs, 2006), которое соответствует 1700 микрограммов WO3/м2. Для диоксида кремния было получено литературное значение 600 микрограммов SiO2/м2 (Iler, стр.36, вышеуказанная ссылка). Таким образом, в качестве примера, смешанный оксид, состоящий из 10% по весу SiO2 (0,10 г/г), 9% по весу WO3 (0,09 г/г) и 2% по весу V2O5 (0,02 г/г) с остальным количеством из TiO2, имеет измеренную по поглощению N2 удельную площадь поверхности по BET 250 м2/г. Значение TFM для этого материала составляет TFM=(1/250)×((0,10/600Е-6)+(0,09/1700Е-6)+(0,02/1100Е-6))=0,95. Это число показывает, что если бы добавленные оксиды SiO2, WO3 и V2O5 были идеально равномерно диспергированы на поверхности диоксида титана, смешанный оксид образовал бы 0,95 толщины монослоев из добавленных оксидов. Что касается отдельно диоксида кремния, то его парциальное монослойное покрытие составило бы 0,67, или две трети поверхности были бы покрыты идеально диспергированным покрытием из диоксида кремния. Составы согласно настоящему изобретению, будучи свежеприготовленными (то есть, после добавления добавленных оксидов, но до старения или спекания), обычно имеют величины удельной площади поверхности больше, чем около 100 м2/г, и общее количество добавленных оксидов на уровне 15% по весу или менее, и тем самым парциальное монослойное покрытие конкретно для диоксида кремния составляет около 0,80 или меньше.
Способы введения диоксида кремния для настоящего изобретения.
Нанесение покрытий на поверхность диоксида титана с использованием силикатов щелочных металлов или кремниевой кислоты, таких, как описано выше, в течение многих лет применяли в производственной практике промышленности по производству красок и покрытий. Например, см. главы 52 и 53 обзорной публикации ″Colloidal Silica, Fundamentals and Applications″ («Коллоидальный кремнезем, основы и применение»), в Surfactant Science Series, том 131, под редакцией Н.Е. Bergna, W.О. Roberts (2006). Как описано в Главе 52 работы Bergna и Roberts, один подход к нанесению на поверхность диоксида титана покрытий из диоксида кремния включает воздействие на несущие частицы диоксида титана диоксидом кремния в щелочных условиях, с концентрацией диоксида кремния, величина которой составляет менее предела растворимости для аморфного диоксида кремния. Как описано в Главе 53 работы Bergna и Roberts, еще один способ включает воздействие на поверхность титаноксидного носителя монокремниевой кислотой при низком значении pH, при концентрации диоксида кремния, которая опять же является очень низкой и ниже предела растворимости. Хотя способы введения диоксида кремния в вышеуказанных литературных ссылках представляют собой средства для введения диоксида кремния, пригодные согласно настоящему изобретению, есть несколько важных отличий. Одно отличие состоит в том, что для прототипа фазой диоксида титана, которую используют в качестве субстрата, является рутил (благодаря его более высокой способности рассеивать свет, чем анатаз), и отсутствует указание относительно того, как добавлением диоксида кремния с помощью этих способов можно предотвратить преобразование анатазной фазы в рутил. Второе важное отличие заключается в том, что частицы титаноксидного субстрата в составе прототипных красок и покрытий, независимо от того, являются ли они анатазом или рутилом, представляют собой субстраты с относительно малой удельной площадью поверхности, причем определенные по поглощению N2 величины удельной площади поверхности по BET обычно составляют менее чем около 15 м2/г. В-третьих, ключевое отличие состоит в степени покрытия поверхности добавленным оксидом, таким как диоксид кремния. Согласно вышеуказанному определению парциального монослойного покрытия, композиции соответственно настоящему изобретению, если они были приготовлены на субстрате с низкой удельной площадью поверхности (15 м2/г), имели бы значение общего парциального монослоя около 5 или больше, и парциальное монослойное покрытие конкретно для диоксида кремния составляло бы около ≥3. Таким образом, в прототипе кремнийоксидное покрытие присутствует поверх всей частицы диоксида титана, и с толщиной, которая превосходит толщину монослоя. Действительно, кремнийоксидное покрытие присутствует так, что полностью инактивирует фотокаталитическую активность поверхности диоксида титана. Наконец, в предпочтительном варианте осуществления настоящего изобретения, диоксид титана покрывают диоксидом кремния в условиях, где добавленный диоксид кремния далеко превышает предел растворимости в несколько сотен ч/млн. Как будет видно ниже, в настоящем изобретении диоксид кремния, будучи первоначально осажденным, не полностью покрывает поверхность диоксида титана, так что желательная каталитическая функциональность поверхности диоксида титана для SCR-реакции по-прежнему не утрачена. Поэтому тем самым может быть достигнута цель настоящего изобретения, состоящая в максимизации каталитической активности поверхности, с сохранением в то же время стабильности носителя.
Существует еще одно обоснование того, почему дисперсные кремнеземы не являются предпочтительными формами диоксида кремния для настоящего изобретения, в том числе формы дисперсного диоксида кремния с внутренней пористостью и, тем самым, высоким поровым объемом. Из литературы (например, Wachs и др., J. Cat., том 161, стр.211-221 (1996)) хорошо известно, что сам по себе диоксид кремния не является хорошим носителем для SCR-катализаторов на основе оксида ванадия, тогда как диоксид титана и легированный оксидом вольфрама диоксид титана представляют собой хорошие носители. Поэтому для настоящего изобретения желательно свести к минимуму величину удельной площади поверхности диоксида кремния, которая наличествует для неблагоприятного взаимодействия с оксидом ванадия, в то же время с доведением до максимума величины площади поверхности TiO2-WO3, чтобы сделать катализатор наиболее активным. Таким образом, используют количество диоксида кремния, достаточное только для стабилизации диоксида титана, и его применяют в форме (с молекулярным диспергированием на поверхности диоксида титана), которая оказывает минимальное неблагоприятное влияние на ванадийоксидный катализатор.
Наконец, теперь описан еще один подход к получению материалов согласно настоящему изобретению, в котором могут быть использованы вышеописанные дисперсные формы диоксида кремния. Хорошо известно, что дисперсный аморфный диоксид кремния является растворимым до такой степени, которая зависит от величины pH раствора и температуры, например, смотри работу автора Iler (вышеуказанная ссылка, стр.42). При значении pH выше примерно 9 и при температурах выше температуры окружающей среды аморфный диоксид кремния будет иметь заметную растворимость. Затем этот растворенный диоксид кремния может быть опять выведен в осадок, например, на поверхность диоксида титана, последующим снижением температуры и/или величины рН до уровня, который снижает растворимость диоксида кремния. Этим путем дисперсные кремнеземы, которые тщательно смешаны с анатазным диоксидом титана, могут быть растворены, и перераспределены с эффективным диспергированием на поверхности диоксида титана с помощью гидротермической обработки. Однако такая дополнительная обработка не является предпочтительным способом получения композиций согласно настоящему изобретению, поскольку эта стадия увеличивает продолжительность обработки и стоимость во время приготовления смешанного оксида. Наиболее предпочтительным является применение пригодного прекурсора диоксида кремния и непосредственная обработка диоксида титана.
Примеры
Исходный материал для оксида титана
В одном варианте осуществления настоящего изобретения использовали суспензию сульфатированного диоксида титана (смотри Таблицу 1). Такая суспензия сульфатированного диоксида титана может быть получена как промежуточный продукт в производственном процессе приготовления диоксида титана с использованием сернокислотного способа, например, как получают на производственном предприятии фирмы MIC в Танне, Франция. Такая суспензия включает около 27% имеющего высокую удельную площадь поверхности водного анатазного диоксида титана, TiO2. TiO2 имеет главным образом кристаллитные частицы, имеющие размеры менее 5 нанометров, и соответствующие удельные площади поверхности, определенные по BET поглощением N2, превышающие 250 м2/г. Суспензия имеет вязкость 0,5-3 пуаз, плотность 1275 кг/м3 и низкое значение pH примерно 1,5-2,0, что обусловливается тем фактом, что суспензия содержит около 6,6% по весу SO3. Однако настоящее изобретение не ограничивается применением этой суспензии. Здесь могла бы быть использована любая композиция, включающая водный анатазный диоксид титана. В самом деле, нет необходимости в применении сульфатированной суспензии диоксида титана в качестве исходного материала. Вместо этого мог бы быть использован высушенный прекурсор анатазного диоксида титана с низким содержанием сульфата.
Однако предпочтительным является приготовление используемой здесь суспензии диоксида титана из диоксида титана, который был получен не в присутствии мочевины.
В одном варианте осуществления изобретения TiO2-компонент применяемого здесь материала носителя катализатора главным образом имеет удельную площадь поверхности <400 м2/г и поровый объем <0,40 см3/г.
Экспериментальные методы: структуру и стабильность катализаторов на основе диоксида титана, и изменения, которые происходят во время воздействия повышенных температур, исследовали разнообразными путями. Использованные методы включают рентгеновский дифракционный анализ (РСА), трансмиссионную электронную микроскопию (ТЕМ), SEM (сканирующую электронную микроскопию), спектроскопию твердофазного ядерного магнитного резонанса высокого разрешения (NMR), азотную порометрию (N2 BET/BJH) и оценку каталитической активности в реакции NO с NH3 (DeNOx)
РСА: образцы оценивали по составу кристаллической фазы и размеру кристаллитов следующим образом. Образцы готовили для РСА вдавливанием в сферические держатели РСА PW1812/00 и затем анализировали с использованием дифрактометра Panalytical X′Pert Pro™, оснащенного закрытой (Cu) рентгеновской трубкой и датчиком положения X-Celerator. Эксплуатационные условия прибора были настроены на 45 кВ, 40 мА, 0,008°2θ/шаг и 50 секунд продолжительности выдержки. Идентификацию фаз проводили в режиме «поиск-совпадение» экспериментальных картинок с обеими базами данных ICCD и ICSD. Для Количественного Анализа Фазового состава методом рентгеновской дифракции использовали метод Ритвельда. Размер кристаллитов измеряли по одиночным пикам согласно формуле Шеррера, которую использовали в пакете программ Panalytical High Score. Формула Шеррера основывается на том факте, что размер кристаллитов является обратно пропорциональным полной ширине на половине (FWHM) индивидуального пика - чем более узкими являются пики, тем крупнее размер кристаллитов. Значение аппаратурного уширения, использованное для расчетов, заимствовали из LaB6-стандарта (стандартный референсный материал NIST (Национального института стандартов и технологии)). В дополнение, для расчета размера зерен также дополнительно применяли полнопрофильный метод, такой как Rietveld Analysis, из пакета программ X′Pert High-Score Plus™.
ТЕМ: образцы готовили для ТЕМ-анализа погружением медных (Cu) сеток для ТЕМ, полностью покрытых углеродом, непосредственно в приготовленный порошок. Затем сетки обследовали в трансмиссионном электронном микроскопе (ТЕМ) при увеличениях, варьирующих от 50- до 400000-кратных. Анализ проводили с использованием ТЕМ-прибора JEOL 2000FX II, работающего при напряжении 200 кВ. Во время процесса получения изображений особое внимание уделяли охарактеризованию размера и распределения фаз. Изображения были сняты с помощью цифровой CCD-камеры Gatan MultiScan™, и переведены в jpeg-формат.
SEM: образцы готовили для SEM-анализа диспергированием подготовленного порошка на алюминиевые SEM-подложки, покрытые коллоидальным графитовым углеродом. SEM-анализ проводили с использованием прибора JEOL 7401 при напряжении 2 кВ без электропроводного покрытия.
Охарактеризование образцов с помощью 29Si-ЯМР спектроскопии. Полезным подходом для охарактеризования состояния координации диоксида кремния в твердых образцах, содержащих диоксид кремния (например, смотри работу авторов Engelhardt и Michel, 1987 (вышеуказанная ссылка)), как описано выше, является спектроскопия 29Si-ядерного магнитного резонанса с вращением под магическим углом (29SIMASNMR). Однако проблема с 29Si-MASNMR состоит в том, что ядра 29Si присутствуют с низким природным относительным содержанием (4,7%), и поэтому метод является не очень чувствительным. Общеупотребительным методом повышения чувствительности является подход с кросс-поляризацией (например, смотри ″Colloid Chemistry of Silica″ (″Коллоидная химия кремнезема»), под редакцией Н. Bergna, ACS Series, том 234, стр.270 (1994)). В этом способе спиновую поляризацию от более распространенного спина, который имеет большой ядерный магнитный момент (в этом случае, 1Н), путем двойного резонанса переносят на менее распространенный спин (29Si). Этот метод обеспечивает резкое повышение чувствительности для 29Si-ЯМР сигнала, когда Si имеет связанную с ним группу (ОН). Хорошо известно, что в силикатах кремний имеет тетраэдрическую координацию, и окружен четырьмя ближайшими соседними кислородными атомами, ближайшими соседними атомами которых являются либо Н, либо Si. Можно было бы ожидать, что изолированный силикатный тетраэдр, который посажен на поверхность оксида титана, имел бы по меньшей мере один ближайший соседний атом Н, Si-ОН, и этот протон мог бы повышать чувствительность метода для ядра кремния. Измерения с помощью 29Si-HMP спектроскопии также могут быть проведены на жидких образцах, которые содержат растворимые силикаты с низкой молекулярной массой, как также описано авторами Engelhardt и Michel (вышеуказанная ссылка).
Азотная порометрия: образцы оценивали для азотной порометрии с использованием анализаторов Micromeretics TriStar™. Образцы подвергали дегазированию в течение ночи при температуре 150°C в потоке азота. Затем их охлаждали до комнатной температуры для измерения адсорбционной способности. Кривые адсорбции/десорбции измеряли при температуре жидкого азота. Удельную площадь поверхности определяли с использованием метода BET, и поровые объемы измеряли с использованием метода BJH (Баррета-Джойнера-Галенда) по адсорбционной ветви.
Оксид ванадия добавляли путем пропитки либо щелочным раствором (например, моноэтаноламина), либо из кислотного раствора (например, щавелевой кислоты). Затем импрегнированные материалы подвергали старению при высокой температуре в условиях гидротермической обработки (750°C в течение 16 часов в 10% H2O) (или при температуре 600°C-900°C в течение 6 часов в воздушной атмосфере), чтобы обеспечить ускоренное старение. Желательно иметь 100% анатаза с высокой удельной площадью поверхности (связанной с очень мелкими кристаллитами), и без кристаллического оксида вольфрама после обработки старением.
Примеры 1-3: эталонное тестирование промышленных материалов
В нижеследующих трех примерах авторы настоящего изобретения стремились провести сравнительное тестирование эффективности нескольких промышленных прототипных материалов, которые используются в SCR-устройствах, а именно DT-52™ (Пример 1), DT-58™ (Пример 2) и DT-S10™ (Пример 3). Свойства этих трех материалов перечислены в Таблице 2. Можно видеть, что DT-52™ содержит добавленный оксид вольфрама (но не диоксид кремния), DT-S10™ содержит добавленный диоксид кремния (но не оксид вольфрама), и DT-58™ содержит оба добавленные оксид вольфрама и диоксид кремния.
Для каждого из Примеров 1-3 базовые материалы были использованы в том состоянии, как были приобретены, и оксид ванадия размещали на них следующим путем. Готовили раствор моноэтаноламина (МЕА) в деминерализованной воде, который имел концентрацию 0,4 М (24,4 г/л МЕА). К этому раствору добавляли 10,9 г/л V2O5, (0,06 М). Для получения катализатора с конечным содержанием оксида ванадия на уровне 1% по весу приблизительно 13,7 г вышеуказанного раствора смешивали с 15,8 г титаноксидного носителя (потеря при прокаливании=5% по весу), и смесь нагревали в роторном испарителе в вакууме при температуре 75°C до полного высушивания. Затем полученный продукт прокаливали в статической муфельной печи при температуре 600°C, 700°C или 800°C. Подобным образом, катализаторы были получены с конечным содержанием оксида ванадия в 3% по весу при использовании 41,2 г раствора «МЕА/оксид ванадия» и 15,8 г оксида титана.
Затем проводили оценку пористости по N2, фазового состава и размера кристаллов методом РСА, и активности DeNOx полученных выше материалов (результаты приведены в Таблице 3). В отношении DeNOx-активности, 0,1 г образца из каждого примера катализатора с нанесенным оксидом ванадия гранулировали, и сортировали до размера -20/+40 меш, и помещали в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 1000 ч/млн NH3, 1000 ч/млн NO и 3% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час.
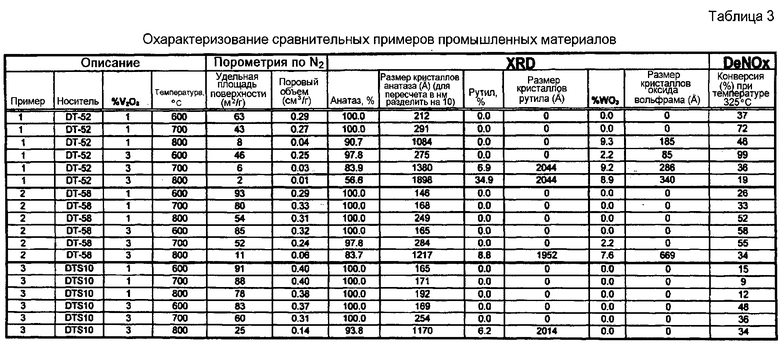
Визуальный обзор Таблицы 3 подтверждает тенденции, описанные в литературе, и что эти более высокие уровни содержания оксида ванадия и более высокие температуры связаны с потерей удельной площади поверхности, преобразованием анатазной фазы в рутильную, кристаллизацией оксида вольфрама и увеличением размера кристаллов (спекание). Однако поведение индивидуальных материалов отличает их друг от друга. В качестве примеров, данные для образцов с 3% по весу оксида ванадия нанесены на график на Фигурах 1 (удельная площадь поверхности по БЭТ) и Фигуре 2 (% анатазной фазы), которые являются показателями термической стабильности катализаторов.
Из этих Таблиц 1 и 2 и Фигур 1 и 2 можно ясно видеть, что материал DT-S10™ (с диоксидом кремния) имеет наивысшую термическую стабильность, после которого следует DT-58™ (с диоксидом кремния и оксидом вольфрама), и далее следует DT-52™ (только с оксидом вольфрама). Если бы единственным требованием для хорошего носителя ванадийоксидного катализатора была термическая стабильность, то явное преимущество было бы за DT-S10™.
На следующих двух фигурах (Фигуры 3 и 4) показаны степени конверсии DeNOx при температуре 325°C для материалов с содержанием 1% и 3% оксида ванадия, соответственно. Можно ясно видеть, что образец только с диоксидом кремния (DT-S10™) имеет наименьшую степень конверсии для большинства температур старения; есть только образец с 3% оксида ванадия, подвергнутый старению при температуре 800°C, который имеет активность, равную активности материала DT-58™.
Таким образом, на основании характеристик этих промышленных образцов, существует очевидная потребность в разработке катализатора, как с улучшенной стабильностью, так и с повышенной активностью.
Примеры 4-5. Нижеследующие примеры показывают характеристики двух дополнительных промышленных прототипных материалов (MIC DT-60™ и Тауса Corporation ITAC 115GS™) сравнительно с DT-58™. Образцы этих материалов были проанализированы для определения состава с использованием рентгеновского флуоресцентного анализа, с результатами, показанными в Таблице 4.
Результаты показывают, что образцы DT-60™ и Тауса™ содержат номинально около 10% по весу SiO2 и около 5% по весу WO3. Все три типа материалов содержали 0,9% по весу V2O5, нанесенного осаждением из МЕА-раствора, как в Примерах 1-3. Затем продукты были подвергнуты старению при температуре 800°C в течение 6 часов на воздухе в статической муфельной печи, и продукты были проанализированы с использованием N2-ВЕТ-метода. Для определения DeNOx-активности, (микрореактор), образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия, гранулировали, и сортировали до размера -20/+40 меш, и помещали в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 1000 ч/млн NH3, 1000 ч/млн NO и 3% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час.
В Таблице 5 ниже приведено сравнение стабильности удельной площади поверхности образцов.
Данные показывают, что образцы с более низким уровнем содержания оксида вольфрама имеют слегка повышенную стабильность, чем у DT-58™. Однако DeNOx-активности катализаторов, как представлено в Фигуре 5, показывают, что активность для образцов DT-60™ и Тауса™ является более низкой, чем активность для образца DT-58™. Таким образом, как для примеров 1-3, Примеры 4 и 5 демонстрируют необходимость более высокой стабильности и активности для новых материалов согласно настоящему изобретению.
Пример 6: стабилизация поверхности диоксидом кремния
Как отмечено здесь в разных местах, настоящее изобретение направлено на создание очень стабильного ультратонкого диоксида титана с использованием минимального количества добавки диоксида кремния. Как отмечено выше, дисперсные кремнеземы (например, коллоидальный, пирогенный и осажденный) не являются идеальными источниками диоксида кремния для применения в ванадиевых катализаторах на титаноксидном носителе, поскольку большая часть диоксид кремния недоступна для взаимодействия с поверхностью диоксида титана. Цель настоящего изобретения состояла в нахождении еще одной формы диоксида кремния, которая могла бы быть использована для более эффективной стабилизации поверхности диоксида титана, но которая оказывала бы минимальное неблагоприятное влияние на каталитическую активность оксида ванадия, нанесенного на поверхность носителя из диоксида титана.
Рассматривали применение диоксида кремния скорее в форме с низкой молекулярной массой и/или в виде мелких наночастиц, нежели в дисперсной форме, которая присутствует в вышеописанных традиционных аморфных кремнеземах. Формой диоксида кремния с наименьшей молекулярной массой в водном растворе является кремниевая кислота, Si(OH)4. Однако это химическое вещество имеет очень низкую растворимость в воде, и поэтому ограниченную концентрацию на уровне нескольких сотен частей на миллион (ч/млн). (Обсуждения химических аспектов водного диоксида кремния в воде можно найти, например, в работе автора Iler (вышеуказанная ссылка) и Brinker, С.J. и Scherer, G.W., 1990, глава 3).
Ввиду низкой растворимости Si(OH)4, авторы настоящего изобретения провели эксперименты с растворами силикатов тетра(алкил)аммония (включающих, но не ограничивающихся таковыми, тетраметиламмоний, ТМА). Эти реагенты содержат диоксид кремния в формах с низкой молекулярной массой (смотри работу авторов Engelhardt и Michel, вышеуказанная ссылка). Кроме того, диоксид кремния в этих растворах присутствует при явно высоких концентрациях (например, 9% по весу SiO2). Таким образом, авторы настоящего изобретения исследовали, могут ли или не могут молекулярные частицы в этих растворах быть достаточно мелкими, чтобы селективно реагировать с поверхностью диоксида титана, в то же время не создавая отдельной зоны для связывания с оксидом ванадия, что могло бы снизить каталитическую активность.
29Si-ЯМР спектроскопия жидкого образца растворимого силиката.
Для определения природы силикатных частиц в имеющемся в продаже на рынке растворе силиката в ТМА, коммерческий источник ТМА-силиката, использованный в этих примерах (раствор силиката в ТМА от фирмы Alfa, 9% SiO2), оценивали с использованием 29Si-HMP спектроскопии с помощью прибора с рабочей частотой 400 МГц по базам данных Spectral Data Services, Inc. В Таблице 6 показаны результаты.
Можно видеть, что ТМА-силикатный раствор содержит главным образом частицы диоксида кремния с порядком связывания Q3 или ниже. Однако есть некоторое количество диоксида кремния с порядком связывания Q4, так что не весь диоксид кремния содержится в растворе в идеальной форме (с порядком связывания Q3 или ниже). Однако, как будет здесь показано, авторы настоящего изобретения вновь обнаружили, что источники растворимого диоксида кремния, такие как силикаты тетра(алкил)аммония, могут быть применены для получения исключительно стабильных (анатазная фаза, высокая удельная площадь поверхности) катализаторов на основе оксида ванадия, которые проявляют превосходную каталитическую активность для селективного каталитического восстановления в реакциях с NOx.
Повышение стабильности путем новой обработки диоксидом кремния
Приведенные выше Примеры 1-5 выявляют характеристики стабильности и каталитической активности промышленных материалов, содержащих оксид ванадия и подвергнутых обработке в условиях ускоренного старения. Пример 6 демонстрирует улучшение термической стабильности, которое может быть достигнуто с использованием нового способа обработки диоксидом кремния согласно настоящему изобретению. Суспензию производимого в промышленности сульфатированного гидрогеля диоксида титана разбавили до содержания TiO2 21,6% по весу. 112,5 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. К этой суспензии добавили 33,3 г силиката тетраметиламмония (продукт TMA-SiO2 фирмы Alfa-Aesar, 9% SiO2, отношение TMA/SiO2=0,5). Эту смесь оставили для реагирования в течение 20 минут. Затем доводили значение pH до 6,0 добавлением концентрированного раствора NH4OH (29%-ного). Затем добавили 3,07 г паравольфрамата аммония (APT), и конечное значение pH доводили до 6,5 добавлением еще одной порции концентрированного раствора NH4OH. Эту смесь оставили реагировать в течение дополнительных 30 минут, и затем профильтровали, промыли осадок деминерализованной (DI) водой и высушили. Конечный номинальный состав этого продукта, в расчете на оксиды, был 81% по весу TiO2, 10% по весу SiO2 и 9% по весу WO3. Затем его разделили на порции, которые были подвергнуты кальцинированию в пределах температурного диапазона от 600°C до 900°C в течение 6 часов на воздухе с использованием статической муфельной печи. Промышленный образец DT-58™ с таким же составом также подвергали старению в идентичных условиях. Оба образца оценивали на предмет сохранения удельной площади поверхности с использованием метода БЭТ, с данными, показанными на Фигуре 6.
Данные на Фигуре 6 ясно показывают что, в то время, как составы двух продуктов номинально являются одинаковыми, образец, приготовленный с использованием новой формы диоксида кремния с низкой молекулярной массой и/или мелких наночастиц согласно настоящему изобретению, имеет гораздо более высокую термическую стабильность (в большей степени сохраняет удельную площадь поверхности), чем прототипный материал (DT-58™).
Охарактеризование твердых образцов методом 29Si MASNMR спектроскопии. Нижеследующий анализ ТМА-SiO2-материала согласно изобретению и традиционного материала (DT-58™) показывает, что диоксид кремния, присутствующий в материалах согласно настоящему изобретению, имеет весьма отличающиеся морфологические характеристики. Два образца, в своем «свежем» состоянии (перед добавлением оксида ванадия, но после кальцинирования при температуре 500°C), были подробно проанализированы с помощью Spectral Data Services, Inc., с использованием 29Si MASNMR спектроскопии на приборе с рабочей частотой 270 МГц. Была предпринята попытка провести эксперимент на DT-58™ с кросс-поляризацией, но спустя 1 час сигнал не был получен, и в этих условиях был бы виден интенсивный сигнал, если бы рядом с ядром Si присутствовали любые (ОН)-группы, как следовало бы ожидать для диоксида кремния, равномерно диспергированного на поверхности диоксида титана. Поэтому этот образец испытывали в течение 4 часов с использованием только MASNMR-метода. Был получен слабый сигнал с химическим сдвигом -111 м.д. относительно тетраметилсилана. Этот сигнал согласуется с Si в Q4-координационном окружении, или Si(OSi)4. Поэтому оба наблюдения (отсутствие сигнала кросс-поляризации и присутствие Q4-сигнала) в ЯМР-эксперименте согласуются с дисперсным диоксидом кремния, где большая часть Si находится внутри частицы диоксида кремния, и на поверхности диоксида кремния нет многочисленных Si(ОН)-групп.
Образец нового носителя катализатора испытывали при номинально таких же ЯМР-условиях, и этот образец также содержал 10% по весу SiO2, однако источником диоксида кремния был ТМА-SiO2, который содержит диоксид кремния в формах с низкой молекулярной массой и/или мелких наночастиц. В этом случае наблюдали интенсивный сигнал в эксперименте с 1H-29Si-Kpocc-поляризацией, который демонстрирует, что существуют гидроксильные группы, связанные с Si. Это поддерживает ту идею, что это тот диоксид кремния, который эффективно диспергирован на поверхности диоксида титана согласно настоящему изобретению. Кроме того, спектр был развернут на четыре пика, со следующими положениями и относительными интенсивностями: -110 м.д., 30%; -100 м.д., 50%; -90 м.д., 16%; и -82 м.д. (4%), и эти пики были отнесены к состояниям координации Q4, Q3, Q2 и Q1, соответственно, как показано в Таблице 6. Кроме того, можно видеть, что около 70% диоксида кремния находятся в таком координационном окружении (Q3, Q2 и Q1), что гидроксильные группы являются ближайшими соседними группами, и это дополнительно подкрепляет мнение, что диоксид кремния эффективно диспергирован на поверхности диоксида титана. Таким образом, авторы настоящего изобретения делают вывод, что применение прекурсора диоксида кремния с низкой молекулярной массой и/или в виде мелких наночастиц, такого как TMA-SiO2 или другие композиции, описываемые здесь, приводит к диоксиду кремния, который эффективно диспергируется на поверхности диоксида титана. В частности, предпочтительным координационным окружением атомов кремния на титаноксидном носителе согласно настоящему изобретению являются главным образом (по меньшей мере на 50%) состояния Q3, Q2, Q1 и Q0 координации, как определяется с помощью 29Si CP-MASNMR. Ключевое проявление этого отличия в природе диоксида кремния состоит в том, что хорошо диспергированный диоксид кремния является гораздо более эффективным, в расчете на массу, в отношении стабилизации диоксида титана. Поэтому для стабилизации диоксида титана требуется меньшее количество диоксида кремния, когда диоксид кремния хорошо диспергирован на поверхности диоксида титана.
Для дополнительной оценки природы кремнийоксидного покрытия на новом образце его подвергли ТЕМ-анализу, как показано в Фигуре 7, которая демонстрирует, что диоксид кремния присутствует в виде изолированных фрагментарных участков на поверхности анатазного диоксида титана. Фрагментарные участки проявляют двумерный характер в том плане, что их длина обычно составляет менее 5 нм, тогда как глубина (расстояние, отсчитываемое от поверхности диоксида титана) в типичном случае составляет менее 2 нм.
Пример 7: Преимущество состава TiO2:SiO2:WO3 с соотношением 90:4:6 в плане стабильности и активности.
Нижеследующий пример согласно изобретению демонстрирует благоприятные стабильность и активность материалов, полученных способами согласно настоящему изобретению. Суспензию производимого в промышленности гидрогеля сульфатированного диоксида титана разбавили до содержания TiO2 21,6% по весу. 208,3 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. (В одном варианте осуществления изобретения используемые здесь суспензию оксида титана и кремнийоксидный компонент смешивали при температуре <80°C и при величине pH <8,5. В альтернативном варианте, применяемые здесь суспензию диоксида титана и кремнийоксидный компонент смешивали при температуре <70°C и при величине pH <7,0). Затем добавили 3,4 г паравольфрамата аммония (APT, 88% WO3) и оставили реагировать в течение 30 минут. К этой смеси добавили 22,2 г силиката тетраметиламмония из Примера 6, и смесь оставили реагировать в течение 10 минут. Затем скорректировали значение pH до 6,5 добавлением концентрированного раствора NH4OH (29%-ного). Эту смесь оставили реагировать в течение дополнительных 20 минут, и затем профильтровали, осадок промыли деминерализованной (DI) водой и высушили при температуре 105°C, и потом кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3. На этот порошок осадили оксид ванадия из МЕА-раствора, как в вышеуказанных Примерах 1-3, чтобы конечное содержание составляло 2% по весу V2O5, в расчете на общий оксид. Затем часть высушенного порошка нагревали до температуры 750°C, и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O.
Пример 8: Преимущество состава TiO2:SiO2:WO3 с соотношением 90:5:5 в плане стабильности и активности. Этот пример дополнительно демонстрирует благоприятные стабильность и активность материалов, полученных способами согласно настоящему изобретению. Суспензию производимого в промышленности гидрогеля сульфатированного диоксида титана разбавили до содержания TiO2 21,6% по весу. 208,3 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. Затем добавили 2,8 г паравольфрамата аммония (APT, 88% WO3) и оставили реагировать в течение 30 минут. К этой смеси добавили 27,8 г силиката тетраметиламмония (TMA-SiO2, 9% SiO2), и смесь оставили реагировать в течение 10 минут. Затем скорректировали значение pH до 6,5 добавлением концентрированного раствора NH4OH (29%-ного). Эту смесь оставили реагировать в течение дополнительных 20 минут, и затем профильтровали, промыли осадок деминерализованной (DI) водой и высушили при температуре 105°C, и потом кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 5% по весу SiO2 и 5% по весу WO3. На этот порошок осадили оксид ванадия из МЕА-раствора, как в вышеуказанных Примерах 1-3, чтобы конечное содержание составляло 2% по весу V2O5 в расчете на общий оксид. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O.
Для формирования базового набора для сравнения, на 4 различных образца из DT-58™ осадили оксид ванадия до 2%-ного по весу содержания, как указано выше, и подвергли гидротермическому старению в таких же условиях. Результаты для этих четырех образцов затем усреднили.
Материалы из Примеров 7 и 8, наряду с эталонными DT-58™ - материалами, проанализировали методами РСА, азотной порометрии и на DeNOx-активность, с результатами, показанными ниже в Таблице 7. Чтобы оценить материалы для DeNOx-применения, 0,1 г образца из каждого примера катализатора с нанесенным оксидом ванадия и подвергнутого старению гранулировали и сортировали до размера 20/+40 меш, и помещали в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3/ 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Для каждого из материалов Примеров 7 и 8 проводили по два испытания DeNOx. На четырех эталонных 0Т-58™ - материалах провели в целом 10 испытаний. Результаты описаны двумя путями. Во-первых, описана степень конверсии NO. Второй метод включает расчет «скорости» реакции. Как известно специалистам с обычной квалификацией, SCR-реакция в основном представляется имеющей первый порядок по NO и нулевой порядок по NH3, и в этих условиях скорость реакции пропорциональна величине -ln(1-x), где «х» представляет долю конверсии (% конверсии/100). Скорость реакции представляет собой лучший метод сравнения образцов при высоких степенях конверсии. Из данных были рассчитаны базовые статистические параметры, и анализ отклонений продемонстрировал, что материалы согласно настоящему изобретению давали значительно отличающуюся (значение «Р» для нулевой гипотезы <0,05) и более высокую активность, чем эталонные образцы.
Таблица 7 ясно показывает, что образцы, полученные согласно настоящему изобретению (Примеры 7 и 8), сохраняют большую часть анатазной фазы, препятствуют кристаллизации оксида вольфрама и препятствуют росту кристаллов (то есть, демонстрируют меньшее спекание), чем базовые материалы. Кроме того, материалы согласно настоящему изобретению сохраняют более высокие удельную площадь поверхности и объем пор, чем это проявляют эталонные материалы. Наконец, материалы, полученные согласно настоящему изобретению, демонстрируют более высокую каталитическую активность в отношении SCR-реакции.
В нижеследующих двух примерах (9 и 10) продемонстрировано резкое различие в стабильности и активности между катализаторами, полученными с дисперсным (коллоидальным) диоксидом кремния, сравнительно с соответствующими изобретению материалами.
Пример 9. Новый материал согласно настоящему изобретению приготовили следующим путем: суспензию производимого в промышленности гидрогеля сульфатированного диоксида титана (включающую 27% TiO2, 7% сульфата и H2O) разбавили водой до получения дисперсии с содержанием TiO2 21,7% по весу. 207,7 г этой дисперсии нагревали при перемешивании в течение 20 минут до температуры 60°C, и затем добавили 2,3 г паравольфрамата аммония (APT, 88% WO3) при низком значении pH. APT оставили реагировать в течение 20 минут. Затем добавили 44,4 г растворимой формы диоксида кремния с низкой молекулярной массой в виде силиката тетраметиламмония (ТМА) (фирмы Alfa-Aesar, 9% по весу SiO2) и оставили реагировать в течение дополнительных 20 минут. Затем скорректировали значение pH до около 6,5 добавлением концентрированного раствора NH4OH (эта стадия могла бы быть проведена до добавления WO3). Затем суспензию профильтровали, промыли осадок для удаления сульфата аммония и затем высушили и кальцинировали при температуре 500°C в течение 6 часов на воздухе. Номинальный состав этого базового материала был 8% по весу SiO2, 4% по весу WO3 и 88% TiO2 (TiO2:SiO2:WO3=88:8:4).
Пример 10. Сравнительный образец получали с использованием традиционного дисперсного коллоидального кремнезема следующим путем: суспензию производимого в промышленности сульфатированного гидрогеля диоксида титана (27% TiO2) разбавили водой до получения дисперсии с содержанием TiO2 21,6% по весу. 203,7 г этой дисперсии нагревали при перемешивании до температуры 60°C, и затем добавили 2,3 г паравольфрамата аммония (APT - 88% WO3). APT оставили реагировать в течение 20 минут. Затем добавили 13,3 г дисперсного коллоидального кремнезема AS-30 (W.R. Grace - 30% по весу SiO2), и оставили реагировать в течение дополнительных 20 минут. Как будет понятно специалисту с обычной квалификацией в этой области технологии, эта форма коллоидального диоксида кремния стабилизирована ионами NH4 +, а не ионами Na+, поскольку последние являются каталитическим ядом для SCR-реакции. Затем скорректировали значение pH смеси до 6,5 добавлением концентрированного раствора NH4OH. Затем суспензию профильтровали, осадок промыли и высушили, и кальцинировали при температуре 500°C в течение 6 часов на воздухе. Номинальный состав этого базового материала был 8% по весу SiO2, 4% по весу WO3 и 88% TiO2. Таким образом, материалы обоих Примера 9 и Примера 10 номинально имеют одинаковый общий состав (88:8:4-TiO2:SiO2:WO3), в расчете на оксиды.
К этим двум базовым материалам, включающим диоксид титана, диоксид кремния и вольфрам, добавили оксид ванадия до целевого содержания 2% по весу V2O5. Оксид ванадия добавляли путем пропитки щелочным МЕА-раствором. Затем импрегнированные материалы подвергли старению при высокой температуре в условиях гидротермической обработки (750°C в течение 16 часов в 10% H2O), чтобы обеспечить ускоренное старение. Подвергнутые старению образцы оценивали с использованием рентгеноструктурного анализа, и наблюдаемые дифракционные картины анализировали с помощью анализа Ритвельда. Чтобы оценить материалы Примера 9 и Примера 10 для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и поместили в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Данные о степени и скорости конверсии NO приведены, как описано выше.
Результаты в Таблице 8 опять демонстрируют выраженное преимущество в отношении стабильности анатазной фазы (и устойчивости к спеканию), обеспечиваемой материалами согласно настоящему изобретению, преимущество в отношении сохранения удельной площади поверхности, связанной с соответствующими изобретению материалами, и преимущество в плане активности, связанной с настоящим изобретением (Пример 9), относительно образца, полученного с использованием коллоидального диоксида кремния (Пример 10).
Катализатор с нанесенным оксидом ванадия и подвергнутый старению из Примера 10 оценили с использованием SEM- (Фиг. 8) и ТЕМ-микроскопии (Фиг. 9). Изображения четко показывают присутствие частиц дисперсного коллоидального диоксида кремния, имеющих диаметры около 20 нм, покрывающих нижележащие частицы из оксида ванадия-анатазного диоксида титана с диаметром ~100-200 нм.
Пример 11. Этот пример демонстрирует еще один вариант осуществления настоящего изобретения, и он включает растворение дисперсного диоксида кремния с последующим переосаждением поверхностного покрытия из диоксида кремния на диоксид титана путем гидротермической обработки при повышенном значении pH. Суспензию производимого в промышленности гидрогеля сульфатированного диоксида титана разбавили до содержания TiO2 21,6% по весу. 833,3 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. Затем добавили 13,6 г паравольфрамата аммония (APT, 88% WO3), и оставили реагировать в течение 20 минут. Затем скорректировали значение pH до 6,0 добавлением концентрированного раствора NH4OH (29%-ного). К этой смеси добавили 80 г дисперсии пирогенного кремнезема (Cabot M-S, 10% SiO2 в деминерализованной воде), и смесь оставили реагировать в течение 20 минут. Затем скорректировали значение pH до 9,0 добавлением концентрированного раствора NH4OH (29%-ного), и эту суспензию нагревали с обратным холодильником в течение 6 часов. Затем ее медленно охладили для выпадения в осадок растворимого диоксида кремния, профильтровали, осадок промыли деминерализованной водой и высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3 (90:4:6). В этих условиях парциальное монослойное покрытие диоксида кремния на диоксиде титана было значительно ниже 1,0. На этот порошок осадили оксид ванадия из МЕА-раствора, как в вышеуказанных Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O.
Материал катализатора из Примера 11 проанализировали методами РСА, азотной порометрии и на DeNOx-активность, и ТЕМ. Чтобы оценить материал для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и помещали в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Результаты показаны в Таблице 9.
ТЕМ-анализы, как показано в Фигурах 10 и 11, показывают, что, в то время как присутствуют немногие остаточные сферические частицы диоксида кремния, которые были не полностью растворены и переосаждены, они типично имеют размер менее 5 нм. По большей части пирогенный кремнезем был в значительной мере растворен и переосажден на поверхность анатаза в виде крупнозернистого покрытия, где это является наиболее эффективным для модифицирования поверхностных характеристик нижележащего диоксида титана.
Эти результаты демонстрируют выраженное преимущество в отношении стабильности анатазной фазы (и устойчивости к спеканию), обеспечиваемой материалами согласно настоящему-изобретению, преимущество в отношении сохранения удельной площади поверхности, связанной с соответствующими изобретению материалами, и преимущество в плане активности, связанной с настоящим изобретением, когда диоксид кремния, первоначально в дисперсной форме, растворяют и перераспределяют в форме наночастиц для создания равномерного покрытия на поверхности диоксида титана.
Пример 12. Этот пример представляет еще одну демонстрацию преимущественного эффекта от перераспределения диоксида кремния в ходе гидротермической обработки, только в этом случае исходным источником является коллоидальный кремнезем. Суспензию производимого в промышленности сульфатированного гидрогеля диоксида титана разбавили до содержания TiO2 21,6% по весу. 208,3 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. К этой смеси добавили 6,7 г дисперсии коллоидального кремнезема AS-30 (W.R. Grace - 30% по весу SiO2), и смесь оставили реагировать в течение 30 минут. Затем добавили 3,4 г паравольфрамата аммония (APT, 88% WO3) и оставили реагировать в течение 10 минут. Затем скорректировали значение pH до 6,5 добавлением концентрированного раствора NH4OH (29%-ного). Затем значение pH скорректировали до 9,0 добавлением концентрированного раствора NH4OH (29%-ного), и эту суспензию нагревали с обратным холодильником в течение 6 часов. Затем ее профильтровали, осадок промыли деминерализованной водой и высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3 (90:4:6). В этих условиях фрагментарное монослойное покрытие диоксида кремния на диоксиде титана было значительно ниже 1,0. На этот порошок осадили оксид ванадия из МЕА-раствора, как в вышеуказанных Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O.
Материал катализатора из Примера 12 проанализировали методами РСА, азотной порометрии и на DeNOx-активность, и ТЕМ. Чтобы оценить материал для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера 20/+40 меш, и помещали в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час.
Результаты, показанные ниже в Таблице 10, сравнивали с получением из коллоидального кремнезема (но без гидротермической обработки, Пример 10). Анализы методами РСА и N2-BET показали, что материал Примера 12 имеет улучшенную стабильность анатазной фазы и устойчивость к спеканию, тогда как результаты относительно каталитической активности показывают, что материал Примера 12 также имеет повышенную каталитическую активность как напрямую связанную с гидротермическим перераспределением диоксида кремния.
ТЕМ-изображение материала из Примера 12 показано ниже в Фигуре 12. Анализ показывает, что, в то время как присутствуют немногие остаточные сферические частицы диоксида кремния, которые были не полностью растворены и переосаждены (с размером приблизительно 10 нм или менее), по большей части коллоидальный кремнезем был в значительной мере растворен и переосажден на поверхность анатаза в виде крупнозернистого, фрагментарного покрытия, где это является наиболее эффективным для модифицирования поверхностных характеристик диоксида титана.
Пример 13: кремниевая кислота. Этот пример представляет еще один вариант осуществления настоящего изобретения, в котором диоксид кремния с низкой молекулярной массой представляет собой кремниевую кислоту, образованную ионным обменом с силикатом натрия. Во-первых, разбавленный раствор (3% по весу SiO2) силиката натрия приготовили добавлением 569 г деминерализованной (DI) воды к 71 г силиката натрия Philadelphia Quartz ″N″, 28,7% по весу SiO2. Отвесили 650,7 г порции (взятой непосредственно из поставки) сильнокислой ионообменной смолы (Dowex 650С в Н-форме). Отдельно суспензию производимого в промышленности гидрогеля сульфатированного диоксида титана разбавили до содержания TiO2 21,6% по весу. 1666,7 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. Затем к разбавленному раствору силиката натрия при интенсивном перемешивании добавили ионообменную смолу, и отслеживали значение pH. Как только контроль величины pH показал, что ионообменная реакция подошла к концу (pH<3,0), смолу отфильтровали, и к суспензии диоксида титана добавили 533 г кремниевой кислоты. Эту смесь оставили реагировать в течение 20 минут. Затем добавили 27,3 г паравольфрамата аммония (APT, 88% WO3) и оставили реагировать в течение 20 минут. Затем скорректировали значение pH до 6,5 добавлением концентрированного раствора NH4OH (29%-ного). Затем смесь профильтровали, осадок промыли деминерализованной водой и высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3 (90:4:6). На этот порошок осадили оксид ванадия из МЕА-раствора, как в вышеуказанных Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O. Чтобы оценить материалы Примера 13 для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и поместили в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн N0 и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Подвергнутые старению образцы затем были оценены методами РСА, азотной порометрии и на DeNOx-активность, и сравнены с DT-58™, как показано в Таблице 11.
Можно ясно видеть, материал, полученный согласно настоящему изобретению, имеет более высокую стабильность анатазной фазы, лучшее сохранение удельной площади поверхности (устойчивость к спеканию) и более высокую DeNOx-активность, по сравнению с DT-58™. Провели ТЕМ-анализ материала из Примера 13, и результаты, обрисованные в Фигурах 13 и 14, показывают, что диоксид кремния присутствует в виде двумерных фрагментарных участков, хорошо распределенных на поверхности диоксида титана. Есть немного редких трехмерных частиц, идентифицируемых как диоксид кремния, присутствующих на некоторых из изображений, но они, по большей части, имеют размер менее, чем около 5 нм.
Пример 14. Этот пример представляет еще один вариант осуществления настоящего изобретения, в котором диоксид кремния с низкой молекулярной массой находится в форме кремниевой кислоты, образованной ионным обменом с силикатом натрия. Во-первых, разбавленный раствор (3% по весу SiO2) силиката натрия приготовили добавлением 59,7 г деминерализованной (DI) воды к 7,0 г силиката натрия Philadelphia Quartz ″N″, 28,7% по весу SiO2. Отвесили 13,5 г порции (взятой непосредственно из поставки) сильнокислой ионообменной смолы (Dowex 650С в Н-форме) и внесли в проточную колонку. Отдельно суспензию производимого в промышленности гидрогеля сульфатированного диоксида титана разбавили до содержания TiO2 21,6% по весу. 208,3 г этой суспензии поместили в круглодонную колбу, которая была оснащена мешалкой с механическим приводом. Эту суспензию нагревали до температуры 60°C с помощью нагревательной рубашки с регулированием температуры, и выдерживали при этой температуре в течение всего цикла приготовления. Затем 66,7 г разбавленного раствора силиката натрия пропустили через колонку для удаления натрия. Эту смесь оставили реагировать в течение 20 минут. Затем добавили 3,4 г паравольфрамата аммония (APT, 88% WO3) и оставили реагировать в течение 20 минут. Затем скорректировали значение pH до 6,5 добавлением концентрированного раствора NH4OH (29%-ного). Затем смесь профильтровали, осадок промыли деминерализованной водой и высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3 (90:4:6). Эта композиция, до добавления оксида ванадия, имела удельную площадь поверхности по методу N2-BET 221 м2/г, и таким образом диоксид кремния присутствует с величиной парциального монослойного покрытия 0,30, значительно ниже 1 монослоя. Этот образец оценили с использованием ТЕМ. Приготовили идентичный образец, с тем исключением, что оксид вольфрама добавили до диоксида кремния, и этот образец анализировали с помощью 29Si СР-MASNMR спектроскопии. Результаты ЯМР-исследования, показанные в Таблице 6, демонстрируют, что большая часть диоксида кремния, присутствующего в образце, имеет состояние координации Q3 или менее, как можно было бы ожидать для диоксида кремния, распределенного в двумерных фрагментарных участках на поверхности оксида титана. ТЕМ-изображение, представленное в Фигуре 15, показывает, что диоксид кремния присутствует как фрагментарное покрытие с величиной 1-3 нм на поверхности кристаллита анатазного диоксида титана, и нельзя было увидеть различимых трехмерных частиц диоксида кремния крупнее 5 нм в диаметре.
На этот порошок осадили оксид ванадия из МЕА-раствора, как в вышеуказанных Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O. Чтобы оценить материалы Примера 14 для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и поместили в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Подвергнутые старению образцы затем были оценены методами РСА, азотной порометрии и на DeNOx-активность, и сравнены с DT-58, как показано в Таблице 12.
Можно ясно видеть, что материал, полученный согласно настоящему изобретению, имеет более высокую стабильность анатазной фазы, лучшее сохранение удельной площади поверхности (устойчивость к спеканию) и более высокую DeNOx-активность, по сравнению с DT-58™.
Пример 15. Этот пример призван показать, что разнообразные материалы прототипа отличаются от материалов согласно настоящему изобретению. В частности, приведена ссылка на Патент США 4221768, колонки 3, 4 (строка 3), Пример 1, и патентный документ US 2007/0129241 (абзац 0026). В этом примере дисперсный коллоидальный диоксид кремния вводят в диоксид титана во время осаждения диоксида титана. Вначале, 1169 г воды налили в стеклянный стакан емкостью 4 л, и его поместили в ледяную баню для охлаждения. Затем к охлажденной воде медленно при перемешивании добавили 330 г раствора TiOCl2 (25,9% TiO2) так, чтобы температура раствора не возрастала выше 30°C, для получения 5,7%-ного раствора TiO2. Затем 544,6 г этого раствора внесли в стеклянный стакан емкостью 1 л, и энергично перемешивали. К этой смеси медленно добавили 4,33 г коллоидального кремнезема Ludox AS-30 (W.R. Grace - 30% SiO2). Затем к этой суспензии добавляли концентрированный раствор NH4OH (29%-ный), пока значение pH не достигло 7. Суспензию с выпавшим осадком подвергали старению в течение 2 часов. Затем ее профильтровали, осадок промыли деминерализованной водой, и затем высушили при температуре 105°C. Номинальный состав этого порошка, в расчете на оксиды, был 4% по весу SiO2, и 96% по весу TiO2. Затем 27 граммов высушенного порошка (84,5% твердых веществ) суспендировали в 100 г деминерализованной (DI) воды, нагрели до температуры 60°C, и затем добавили 1,7 г APT, и оставили реагировать в течение 20 минут. Затем значение pH довели до 7,0, и конечную смесь профильтровали, и осадок высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3. На этот порошок осадили оксид ванадия из МЕА-раствора, как в Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O. Чтобы оценить материалы Примера 15 для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и поместили в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Подвергнутые старению образцы затем были оценены методами РСА, азотной порометрии и на DeNOx-активность, и ТЕМ, и сравнены с DT-58™, как показано в Таблице 13 и Фигуре 16.
Результаты ясно показывают, что сравнительный материал Примера 15 (не сформированный из диоксида кремния с низкой молекулярной массой и/или из мелких наночастиц) явственно имеет более низкую стабильность и активность, чем даже эталонные образцы DT-58™. Кроме того, ТЕМ-анализ (Фиг. 16) показывает, что диоксид кремния присутствует в виде крупных трехмерных включений (например, с размером >20 нм и вплоть до 50 нм или больше).
Пример 16. Этот вариант исполнения подобен прототипным вариантам исполнения, где диоксид кремния вводят в растворенной форме в ходе осаждения (например, смотри патентный документ 4221768, колонка 3, строка 36), с тем исключением, что в этом примере используют ТМА-силикат согласно настоящему изобретению, как в Примерах 7, 8 и 9. В этом примере получают материал, в котором диоксид кремния опять же вводят во время осаждения диоксида титана. Однако в этом случае ТМА-силикат используют как источник диоксида кремния, и раствор титанилсульфата применяют как источник диоксида титана. Во-первых, в стакан емкостью 1 л внесли 990 г раствора титанилсульфата (10,1% TiO2, ~29% H2SO4). В отдельном стакане 26,5 г ТМА-силиката (9% по весу SiO2, фирма Alfa Aesar) разбавили 350 мл деминерализованной воды. В третий сосуд с носиком для непрерывного удаления суспензии с выпавшим осадком добавили 150 г нагретой воды, и содержимое этого сосуда перемешивали. Раствор титанилсульфата нагнетали в сосуд №3 с величиной расхода 20 мл/мин, и раствор ТМА-силиката также нагнетали в сосуд №3 с величиной расхода 10 мл/мин. Кроме того, в сосуд №3 также нагнетали концентрированный раствор NH4OH (29%-ный) для поддержания величины pH при осаждении оксидов на уровне 6,0. Сток декантата из сосуда №3 собирали в еще один стакан. Специалистам с обычной квалификацией в этой области технологии будет понятно, что сосуд №3 представляет собой проточный реактор с перемешиванием непрерывного действия. Как только осаждение оксидов завершилось, тогда осадок отфильтровали, промыли деминерализованной водой и затем высушили при температуре 105°C. Номинальный состав этого порошка, в расчете на оксиды, был 2,5% по весу SiO2, 97,5% по весу TiO2.
Затем 51,2 г высушенного порошка (73% твердых веществ) суспендировали в 122 г деминерализованной воды, нагрели до температуры 60°C, и затем добавили 1,8 г APT, и оставили реагировать в течение 20 минут. Затем значение pH довели до 6,5, и оставили реагировать в течение 20 минут. Полученную смесь профильтровали, и осадок высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 93,5% по весу TiO2, 2,5% по весу SiO2 и 4% по весу WO3 (93,5:2,5:4). На этот порошок осадили оксид ванадия из МЕА-раствора, как в Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O. Чтобы оценить материалы Примера 16 для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и поместили в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Подвергнутые старению образцы затем были оценены методами РСА, азотной порометрии и на DeNOx-активность, и сравнены с DT-58™, как показано в Таблице 14.
Результаты ясно показывают, что материал, полученный в условиях, в которых диоксид кремния с низкой молекулярной массой и/или в форме мелких наночастиц вводят во время осаждения диоксида титана, имеет меньшую стабильность анатазной фазы, меньшую устойчивость к спеканию и меньшую DeNOx-активность, чем базовые материалы. В Фиг. 17 показана полученная в трансмиссионном электронном микроскопе (ТЕМ) микрофотография ванадийоксидного катализатора, которая показывает крупные (>20 нм) трехмерные включения диоксида кремния, которые плохо диспергированы на поверхности диоксида титана.
Пример 17. Этот вариант исполнения подобен Примеру 16, только конечный состав перед добавлением оксида ванадия представляет собой 90:4:6 весовых процентов TiO2, SiO2, WO3. В этом примере получают материал, в котором диоксид кремния опять же вводили во время осаждения диоксида титана. Вначале, в стакан емкостью 1 л внесли 891 г раствора титанилсульфата (10,1% TiO2, ~29% H2SO4). В отдельном стакане 44,4 г ТМА-силиката (9% по весу SiO2, фирма Alfa Aesar) разбавили 400 мл деминерализованной воды. В третий сосуд с носиком для непрерывного удаления суспензии с выпавшим осадком добавили 150 г нагретой воды, и содержимое этого сосуда перемешивали. Раствор титанилсульфата нагнетали в сосуд №3 с величиной расхода 20 мл/мин, и раствор ТМА-силиката также нагнетали в сосуд №3 с величиной расхода 10 мл/мин. Кроме того, в сосуд №3 также нагнетали концентрированный раствор NH4OH (29%-ный) для поддержания величины pH при осаждении оксидов на уровне 6,0. Сток декантата из сосуда №3 собирали в еще один стакан. Специалистам с обычной квалификацией в этой области технологии будет известно, что сосуд №3 представляет собой проточный реактор с перемешиванием непрерывного действия. Как только осаждение оксидов завершилось, тогда осадок отфильтровали, промыли деминерализованной водой, и затем высушили при температуре 105°C. Номинальный состав этого порошка, в расчете на оксиды, был 4,3% по весу SiO2, 96,7% по весу TiO2.
Затем весь высушенный порошок суспендировали в ~150 г деминерализованной воды, нагрели до температуры 60°C, и затем добавили 6,8 г APT, и оставили реагировать в течение 20 минут. Затем значение pH довели до 6,5, и оставили реагировать в течение 20 минут. Полученную смесь профильтровали, и осадок высушили при температуре 105°C, и затем кальцинировали при температуре 500°C в течение 6 часов. Конечный номинальный состав этого продукта, в расчете на оксиды, был 90% по весу TiO2, 4% по весу SiO2 и 6% по весу WO3. На этот порошок осадили оксид ванадия из МЕА-раствора, как в Примерах 1-3, чтобы конечное содержание было 2% по весу V2O5, в расчете на общие оксиды. Затем часть высушенного порошка нагревали до температуры 750°C и выдерживали при этой температуре в течение 16 часов в воздушной атмосфере, которая содержала 10% по весу H2O. Чтобы оценить материалы Примера 17 для DeNOx-применения, образец весом 0,1 г каждого образца катализатора, содержащего оксид ванадия и подвергнутого старению, гранулировали, и сортировали до размера -20/+40 меш, и поместили в реактор для определения конверсии NO в присутствии NH3. Текущий поток, который содержал 5% O2, 500 ч/млн NH3, 500 ч/млн NO и 10% H2O, пропускали над катализатором с объемной скоростью 650 л/г катализатора в час. Подвергнутые старению образцы затем были оценены методами РСА, азотной порометрии и на DeNOx-активность, и сравнены с DT-58™, как показано в Таблице 15.
Результаты ясно показывают, что материал, полученный, когда растворимый диоксид кремния вводят во время осаждения диоксида титана, имеет меньшую стабильность анатазной фазы, меньшую устойчивость к спеканию и меньшую DeNOx-активность, чем базовые материалы.
Пример 18. Этот вариант исполнения демонстрирует влияние температуры кальцинирования на deNOx-каталитическую активность материалов согласно настоящему изобретению. Эталонные катализаторы на основе DT-58™, имеющие содержание 2% по весу V2O5, описанные в Примере 8, были использованы в качестве эталонного образца. На композицию TiO2:SiO2:WO3 в соотношении 90:4:6 согласно настоящему изобретению, полученную как в Примере 13 (в периодическом режиме) и Примере 14 (в непрерывном режиме), нанесли V2O5 до содержания 2% по весу, как описано в этих Примерах. На композицию TiO2:SiO2:WO3 в соотношении 88:8:4 согласно настоящему изобретению, полученную как в Примере 9, также нанесли V2O5 до содержания 2% по весу, как здесь описано. Затем эти материалы подвергли воздействию высоких температур (кальцинированию), варьирующих от 500°C до 850°C, и степень deNOx-каталитической активности измеряли, как в Примере 17. Данные о результатах были аппроксимированы регрессией до полиномиальных функций, и согласованные кривые показаны в Фиг. 18. Фиг. 18 демонстрирует, что для получения максимальной активности для ванадийоксидных каталитических материалов согласно настоящему изобретению, в особенности активности, которая является большей, чем активность эталонного DT-58, каталитические материалы на основе оксида ванадия нужно сначала подвергать воздействию повышенных температур, то есть, температур, превышающих 650°C.
Применимость
Настоящее изобретение направлено, в одном варианте осуществления, на композиции, включающие анатазный диоксид титана, в котором диоксид титана стабилизирован диоксидом кремния, внесенным в форме с низкой молекулярной массой и/или в форме мелких наночастиц. Кроме того, изобретение направлено на применение этих кремнийоксид-титаноксидных композиций в качестве носителей катализаторов, в особенности в сочетании с добавленным оксидом вольфрама и оксидом ванадия, для основанного на оксиде ванадия селективного каталитического восстановления DeNOx из двигателей (дизельных), работающих на обедненных смесях. Кроме того, изобретение направлено на способы получения этих стабилизированных диоксидом кремния титаноксидных или титаноксид-вольфрамоксидных носителей, и катализаторы на основе оксида ванадия, которые включают стабилизированные диоксидом кремния титаноксидные или титаноксид-вольфрамоксидные носители, и способы получения ванадийоксидных катализаторов, и на каталитические устройства, включающие эти катализаторы на основе оксида ванадия.
Реальный конкретный состав кремнийоксид-титаноксидного или кремнийоксид-титаноксид-вольфрамоксидного носителя катализатора зависит от требований, предъявляемых для конкретных вариантов применения катализаторов. В одной предпочтительной композиции изобретение включает стабилизированный диоксидом кремния носитель катализатора на основе диоксида титана, который включает частицы, которые включают ≥90% по сухому весу TiO2 и ≤10% по сухому весу SiO2. В еще одной предпочтительной композиции изобретение включает стабилизированный диоксидом кремния носитель катализатора на основе диоксида титана и оксида вольфрама с ≥85% по сухому весу диоксида титана, 3%-10% по сухому весу SiO2 и 3%-10% по сухому весу WO3. Альтернативно, в одном варианте исполнения, где условия применения требуют особенно хорошей термической стабильности, носитель катализатора включает ≥85% по сухому весу TiO2, 5,0%-9,0% по сухому весу SiO2, и 3,0%-7,0% по сухому весу WO3. Более конкретно, этот стабильный носитель катализатора включает 87%-89% по сухому весу TiO2, 7%-9% по сухому весу SiO2, и 3%-5% по сухому весу WO3. В одном предпочтительном варианте исполнения носитель катализатора включает около 88% (±0,5%) по сухому весу TiO2, около 8% (±0,5%) по сухому весу SiO2, и около 4% (±0,5%) по сухому весу WO3. В одном варианте исполнения количество WO3 в весовых процентах является меньшим, чем количество SiO2 в весовых процентах. В одном варианте исполнения носитель катализатора в свежеприготовленном состоянии имеет удельную площадь поверхности по меньшей мере 80 м2/грамм, и более предпочтительно по меньшей мере 100 м2/грамм.
В еще одном варианте исполнения, где условия применения требуют особенно хорошей каталитической активности, носитель катализатора включает ≥85% по сухому весу TiO2, 3,0%-8,0% по сухому весу SiO2, и 4,0%-9,0% по сухому весу WO3. Более конкретно, этот носитель активного катализатора включает ≥87% по сухому весу TiO2, 3%-6% по сухому весу SiO2, и 4%-8% по сухому весу WO3. В одном предпочтительном варианте исполнения носитель катализатора включает около 90% (±0,5%) по сухому весу TiO2, около 4% (±0,5%) по сухому весу SiO2, и около 6% (±0,5%) по сухому весу WO3. В одном варианте исполнения количество WO3 в весовых процентах является большим, чем количество SiO2 в весовых процентах. В одном варианте исполнения носитель катализатора в свежеприготовленном состоянии имеет удельную площадь поверхности по меньшей мере 80 м2/грамм, и более предпочтительно по меньшей мере 100 м2/грамм.
В одном варианте осуществления изобретения TiO2-компонент используемого здесь материала носителя катализатора главным образом имеет удельную площадь поверхности <400 м2/г, и объем пор <0,40 см3/г.
В одном варианте осуществления изобретения суспензию диоксида титана и кремнийоксидный компонент, используемые здесь, смешивают при температуре <80°C и при значении pH<8,5. Альтернативно, используемые здесь суспензия диоксида титана и компонент диоксида кремния могут быть смешаны при температуре <70°C и при значении pH<7,0.
В еще одном варианте осуществления изобретение представляет катализатор на основе оксида ванадия, включающий новый, описанный здесь стабилизированный диоксидом кремния носитель катализатора на основе диоксида титана или диоксида титана и оксида вольфрама, на который нанесено некоторое количество оксида ванадия (V2O5). В ванадийоксидном катализаторе V2O5 предпочтительно составляет от 0,5% до 3% до 5% его сухого веса. Изобретение дополнительно направлено на каталитические устройства для нейтрализации выхлопа дизельного двигателя, которые содержат описанные здесь катализаторы на основе оксида ванадия. Материалы катализаторов на основе оксида ванадия согласно изобретению могут быть дополнительно обработаны кальцинированием (спеканием) при температуре ≥650°C для повышения их deNOx-каталитической активности.
Кроме того, эти новые каталитические устройства могут быть использованы выше по потоку или ниже по потоку относительно дизельного сажевого фильтра (DPF) в системе регулирования дизельного выхлопа. В системе с компоновкой выше по потоку каталитическое устройство находится между двигателем и DPF, и в системе с компоновкой ниже по потоку DPF находится между двигателем и каталитическим устройством.
Термин «кремнийоксид-титаноксидный носитель», везде, где он здесь используется, предполагается имеющим такое же значение, как «стабилизированный диоксидом кремния носитель на основе диоксида титана», и термин «кремнийоксид-титаноксид-вольфрамоксидный носитель» предполагается имеющим такое же значение, как «стабилизированный диоксидом кремния носитель на основе диоксида титана и оксида вольфрама».
Большинство частиц диоксида кремния в частицах носителя на основе стабилизированного диоксида титана предпочтительно имеет диаметры <5 нм, и более предпочтительно <4 нм, и более предпочтительно <3 нм, и еще более предпочтительно <2 нм, и/или имеет низкие молекулярные массы (например, MW <100000, имеют ли или не имеют частицы осажденный на них V2O5).
Там, где частицы кремнийоксид-титаноксидного носителя содержат V2O5, V2O5 преимущественно составляет от 0,5%-3% по сухому весу материала носителя.
Распределение частиц WO3 и SiO2 на поверхности носителя на основе диоксида титана также играет важную роль в оптимизации DeNOx-активности катализаторов на основе оксида ванадия. Таким образом, когда катализаторы являются свежеприготовленными, то есть, когда добавленные диоксид кремния и оксид вольфрама осаждают сначала и до высокотемпературной обработки, парциальное монослойное покрытие должно быть около 1,0 или менее.
Как отмечено выше, стабилизация материала носителя на основе диоксида титана диоксидом кремния включает обработку диоксида титана диоксидом кремния в форме с низкой молекулярной массой и/или в форме мелких наночастиц, таким как силикат тетра(алкил)аммония (например, силикат тетраметиламмония) или тетраэтилортосиликат (TEOS). Другие примеры прекурсоров диоксида кремния с низкой молекулярной массой и/или в виде мелких наночастиц, которые могут быть использованы в настоящем изобретении, включают, но не ограничиваются таковыми, водные растворы галогенидов кремния (то есть, безводные SiX4, где X=F, Cl, Br или I), алкоксиды кремния (то есть, Si(OR)4, где R=метил, этил, изопропил, пропил, бутил, изобутил, втор-бутил, трет-бутил, пентилы, гексилы, октилы, нонилы, децилы, ундецилы и додецилы, например), прочие кремнийорганические соединения, такие как гексаметилдисилазан, соли фторкремниевой кислоты, такие как гексафторсиликат аммония [(NH4)2SiF6], растворы четвертичных силикатов аммония (например, (NR4)n, (SiO2), где R=H, или алкилы, такие как перечислено выше, и где n=0,1-2, например), водные растворы силиката натрия и калия (Na2SiO3, K2SiO3, и MSiO3, в которых М представляет Na или К в разнообразных количествах относительно Si), кремниевую кислоту (Si(OH)4), образованную ионным обменом любой из катионных форм диоксида кремния, перечисленных здесь, с использованием кислотной ионообменной смолы (например, ионный обмен растворов силикатов щелочных металлов или растворов четвертичного силиката аммония). В предпочтительных вариантах исполнения используемый здесь диоксид титана не получали в присутствии мочевины.
Хотя настоящее изобретение и его преимущества были описаны подробно, должно быть понятно, что разнообразные изменения, замены и модификации могут быть сделаны здесь без выхода за пределы сути и объема изобретения, которые определены прилагаемыми пунктами патентной формулы. Более того, область настоящей заявки не предполагается быть ограниченной конкретными вариантами исполнения способа, изделиями производства, составами материала, средствами, методами и стадиями, приведенными в описании. Как будет без труда понятно специалисту с обычной квалификацией в этой области технологии из описания настоящего изобретения, способы, изделия производства, составы материала, средства, методы или стадии, существующие в данный момент или разработанные позднее, которые исполняют по существу те же функции или достигают по существу того же результата, что и соответствующие варианты исполнения, описанные здесь, могут быть применены согласно настоящему изобретению. Соответственно этому, прилагаемые пункты патентной формулы предполагаются включающими в пределы их объема такие способы, изделия производства, составы материала, средства, методы или стадии.
Каждые из литературных ссылок, патентов или публикаций, цитированных здесь, тем самым явным образом включены сюда ссылкой во всей своей полноте.
Цитированные литературные источники
1. Granger, Р. и Parvulescu, V.I., редакторы, ″Studies in Surface Science and Catalysis″ («Исследования в области поверхностных явлений и катализа»), том 171, Глава 9 (2007).
2. Ullmann. ″Encyclopedia of Industrial Chemistry″ («Энциклопедия промышленной химии»), пятое издание, том А23, стр.583-660 (1993).
3. Iler, R.K. ″The Chemistry of Silica″ («Химия кремнезема») (1979).
4. Fedeyko и др., ″Langmuir″, том 21, стр.5179-5206 (2005).
5. Engelhardt G. и D. Michel. ″High Resolution Solid-State NMR of Silicates and Zeolites″ («Твердофазный ЯМР высокого разрешения силикатов и цеолитов»), издательство John Wiley and Sons, Нью-Йорк (1987).
6. Wachs, I. и др., ″Catalysis Today″, том 78, стр.17 (2003).
7. Wachs, I. и др., ″Catalysis Today″, том 116, стр.162-168 (2008).
8. Bergna, H.E. и W.O. Roberts, редакторы, ″Colloidal Silica, Fundamentals and Applications″ («Коллоидальный кремнезем, основы и применение»), Surfactant Science Series, том 131, издательство CRC Press, Taylor and Francis (2006).
9. Wachs и др., ″J. Catalysis″, том 161, стр.211-221 (1996).
10. Bergna, H., редактор, ″The Colloid Chemistry of Silica″ («Коллоидная химия кремнезема»), ACS Series, том 234 (1994).
11. Brinker, С.J. и G.W. Scherer. ″Sol-Gel Science,″ Глава 3 (1990).
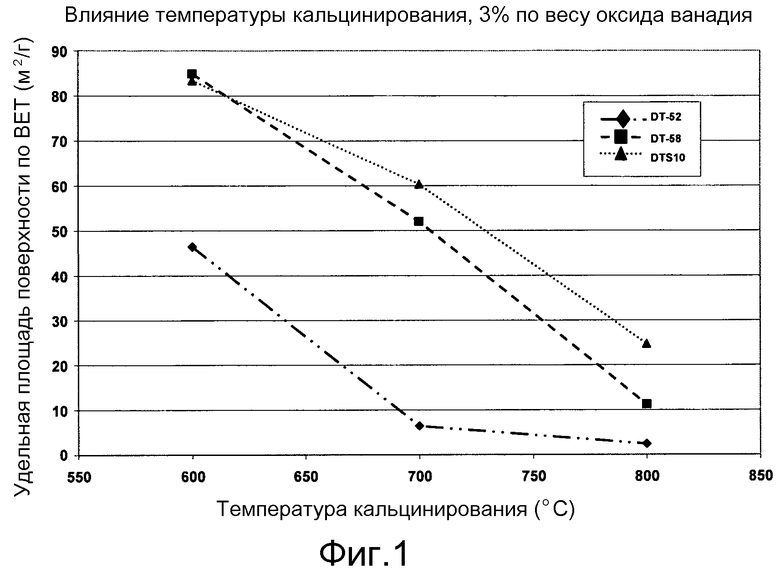
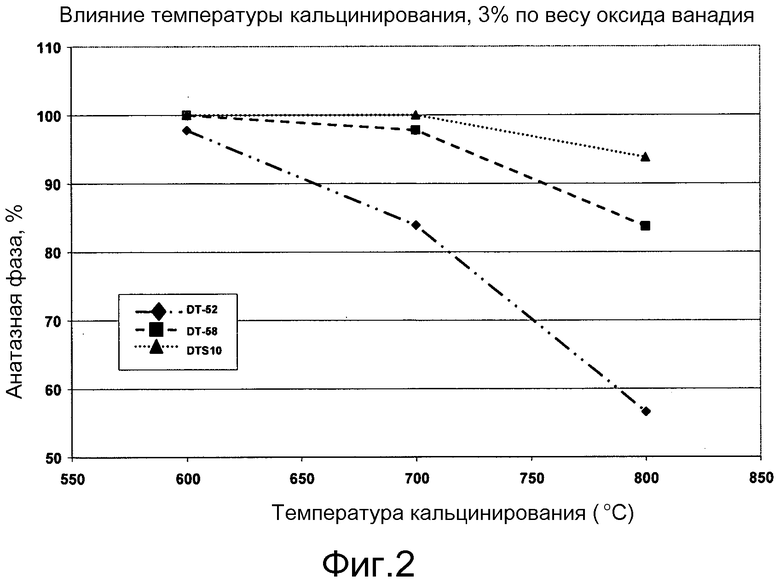
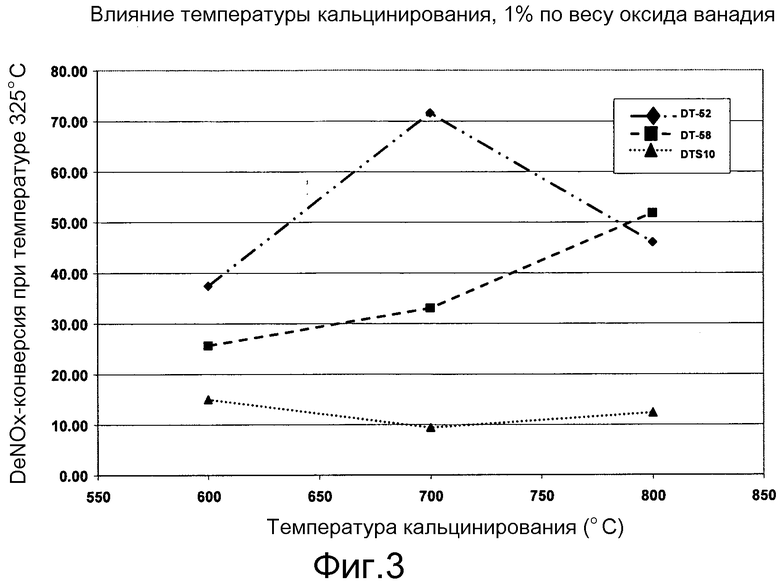
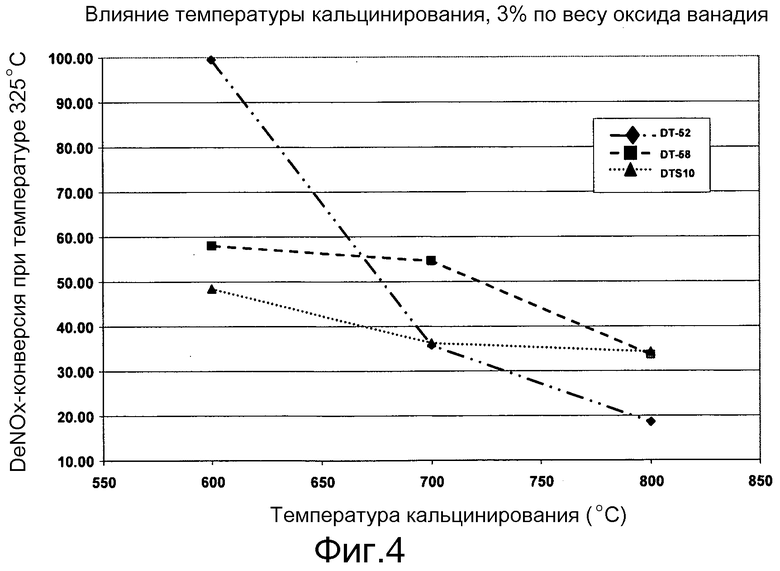

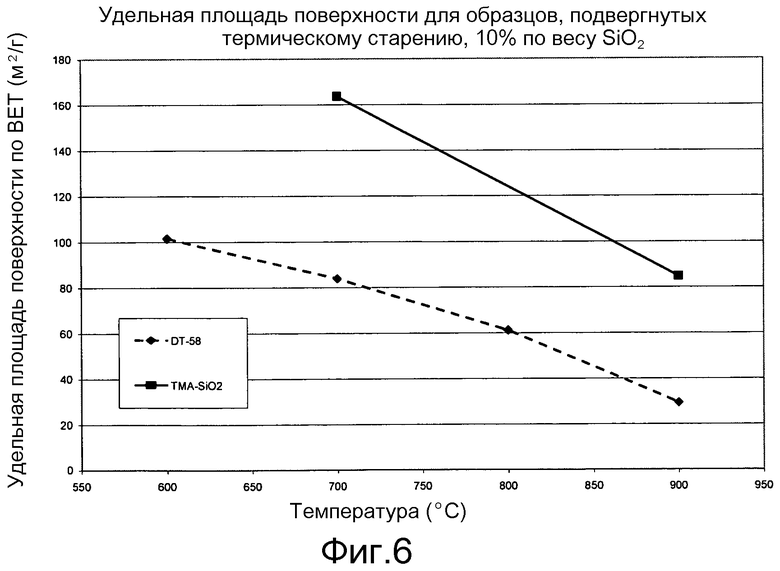


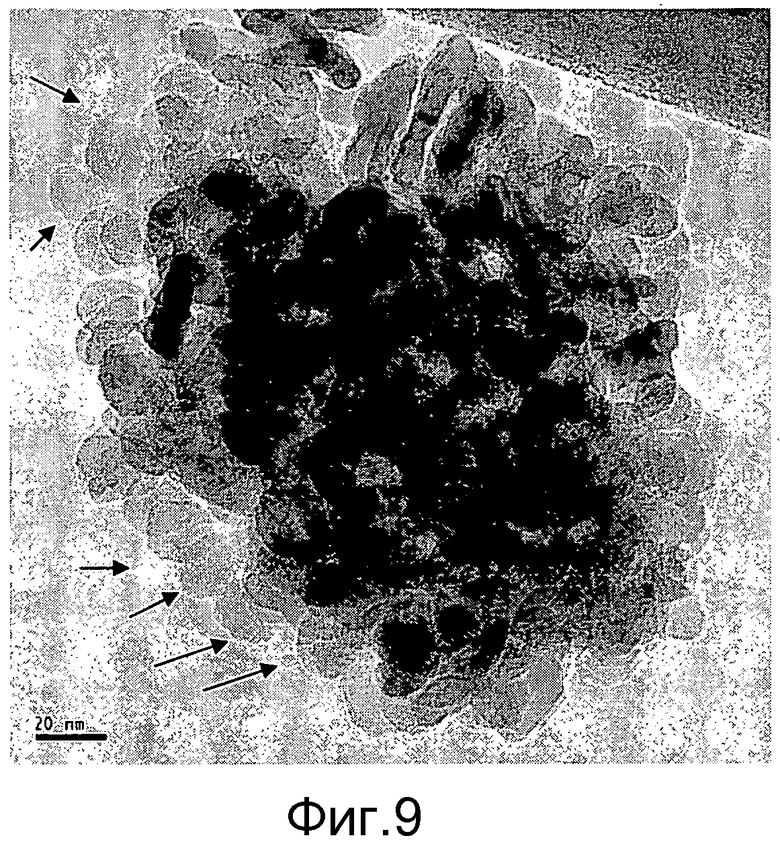
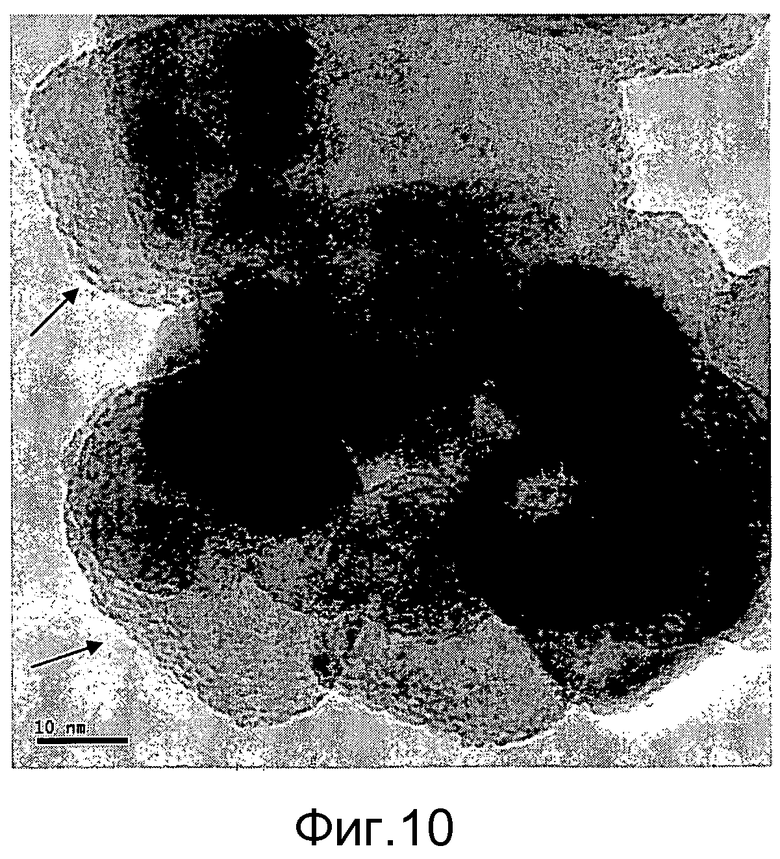

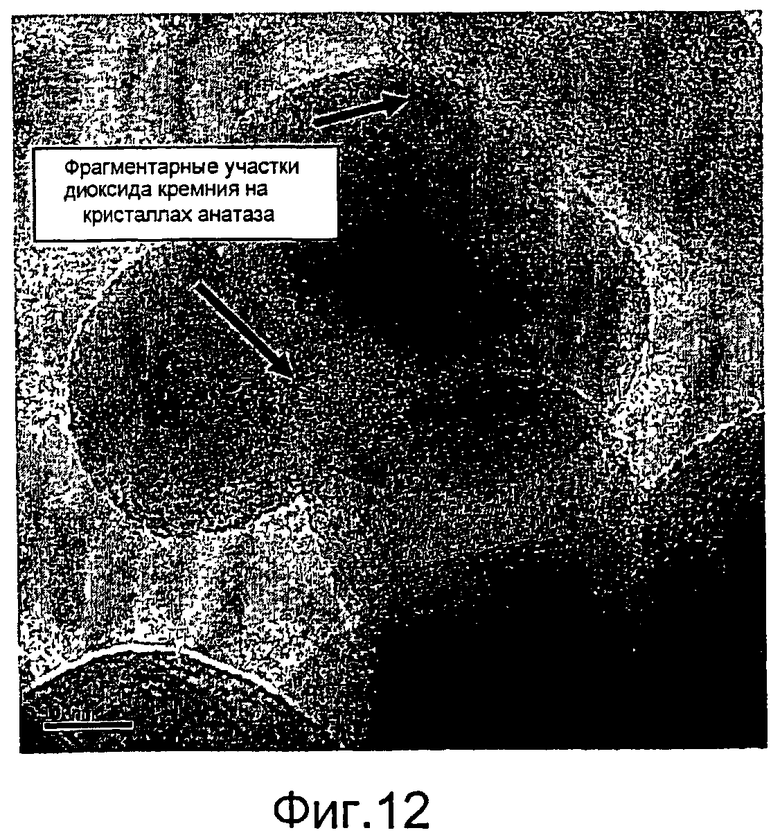
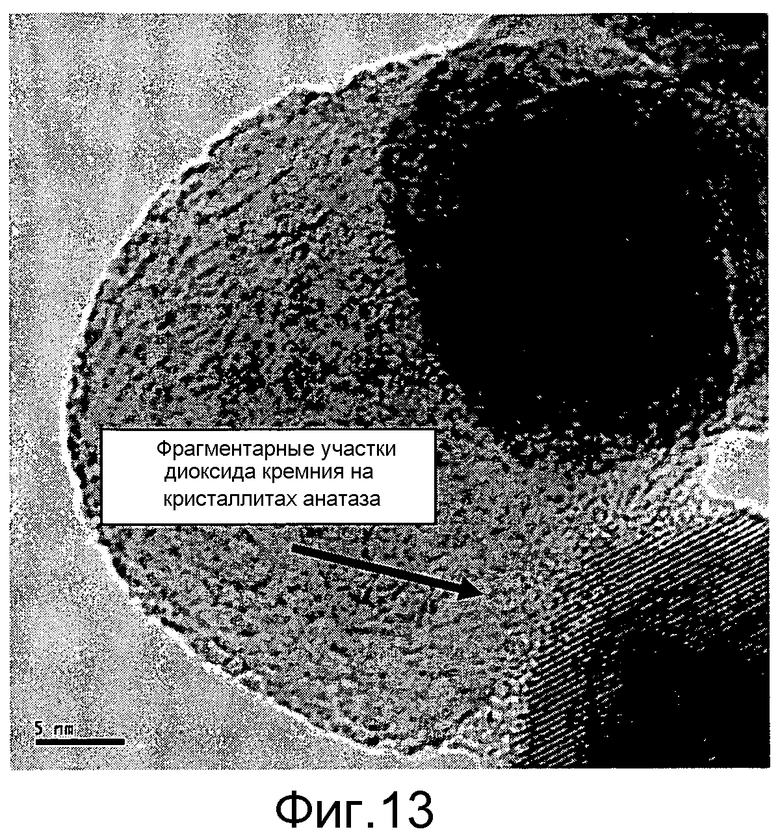
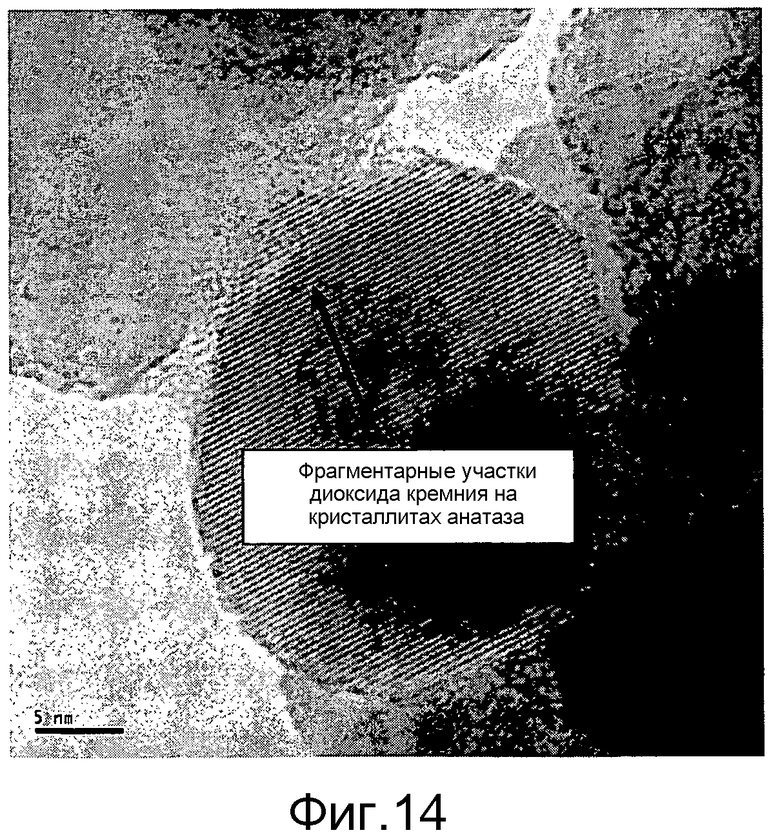
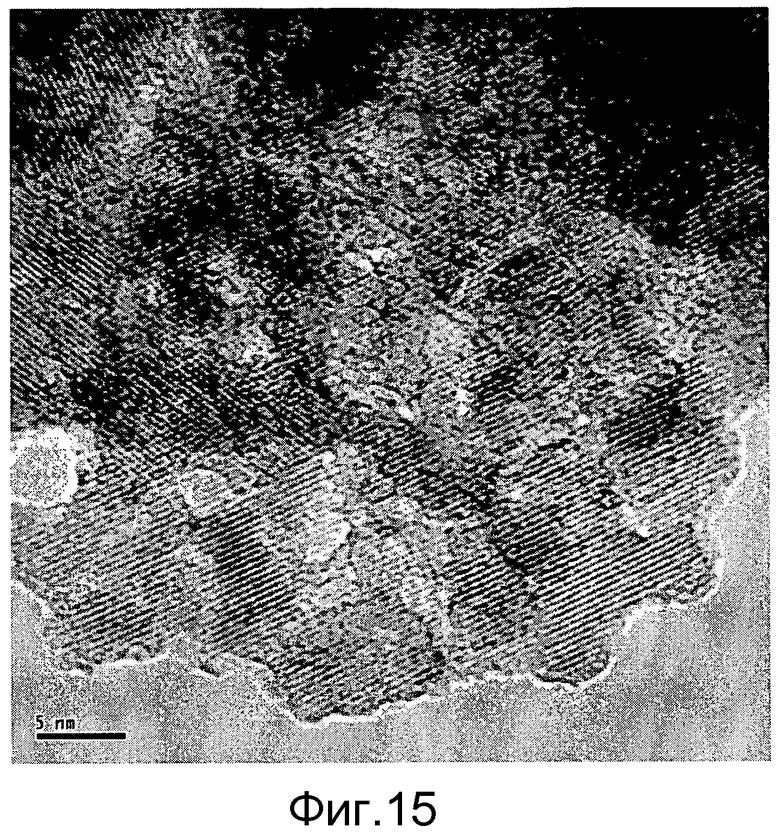
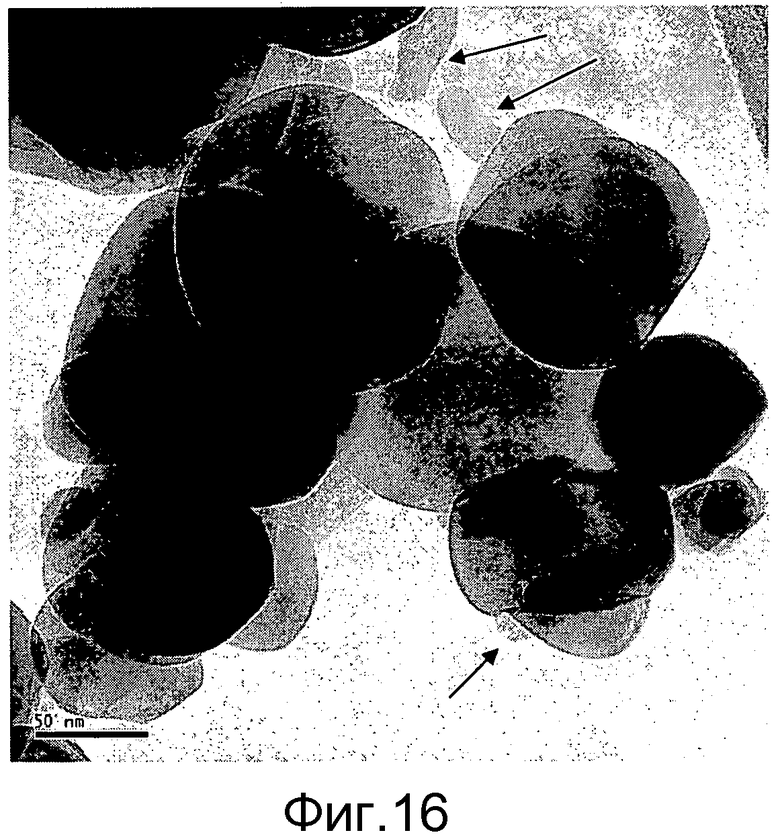
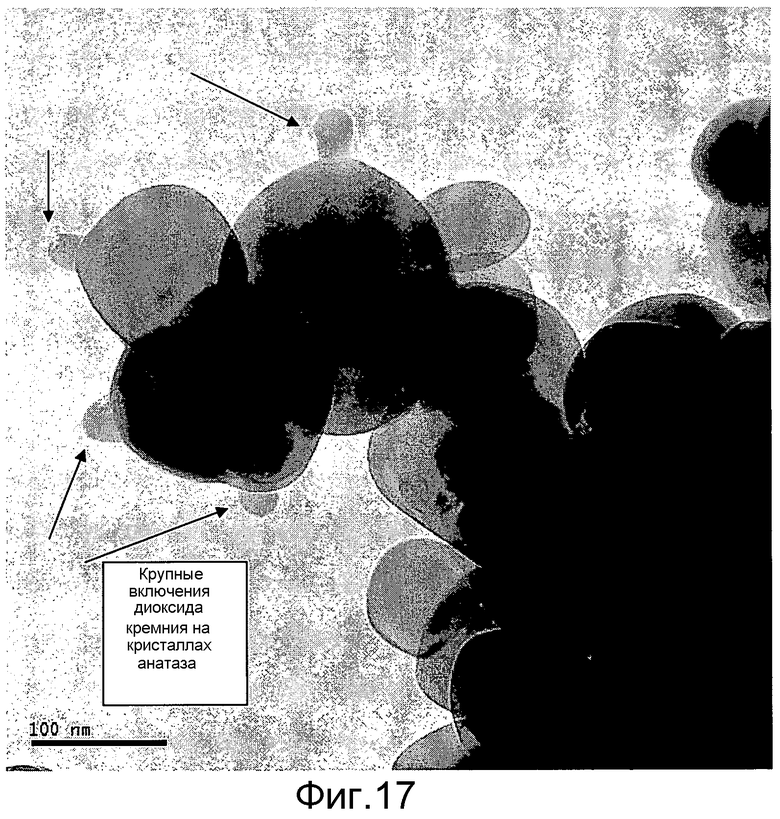

Изобретение относится к области селективного каталитического восстановления оксидов азота, а именно к материалу носителя для катализатора, используемого в этом процессе. Предложенный материал носителя представляет собой частицы анатазного диоксида титана, включающие ≥85% по сухому весу TiO2 и ≤10% по сухому весу SiO2. При этом (i) SiO2 находится главным образом в форме, выбранной из группы, состоящей из форм с низкой молекулярной массой, наночастиц и их комбинаций; и (ii) по меньшей мере 50% атомов кремния SiO2 находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения. Изобретение также относится к каталитическому устройству для нейтрализации дизельного выхлопа, включающему такие частицы, системе регулирования дизельного выхлопа, включающей данное каталитическое устройство, способу, в котором катализируют конверсию оксидов азота в присутствии предложенных частиц анатазного диоксида титана, а также способам получения таких частиц. Предлагаемые частицы позволяют повысить термическую стабильность конечного катализатора, с сохранением или повышением каталитической активности для селективного каталитического восстановления оксидов азота из мобильных устройств, работающих на обедненных смесях. 6 н. и 38 з.п. ф-лы, 18 ил., 15 табл., 18 пр.
1. Частицы анатазного диоксида титана в качестве материала для носителя катализатора для селективного восстановления оксидов азота, включающие ≥85% по сухому весу TiO2 и ≤10% по сухому весу SiO2, причем (i) SiO2 находится главным образом в форме, выбранной из группы, состоящей из форм с низкой молекулярной массой, наночастиц и их комбинаций; и (ii) по меньшей мере 50% атомов кремния SiO2 находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения.
2. Частицы анатазного диоксида титана по п.1, дополнительно включающие от 3% до 10% WO3.
3. Частицы анатазного диоксида титана по п.2, в которых удельная площадь поверхности по БЭТ составляет по меньшей мере 80 м2/г.
4. Частицы анатазного диоксида титана по п.2, включающие ≥85% по сухому весу TiO2, 3%-9% по сухому весу SiO2 и 3%-9% по сухому весу WO3.
5. Частицы анатазного диоксида титана по п.1, в которых SiO2 присутствует со значением парциального монослоя менее 1,0 до спекания частиц анатазного диоксида титана.
6. Частицы анатазного диоксида титана по п.1, в которых SiO2 в форме наночастиц имеет диаметр <5 нм.
7. Частицы анатазного диоксида титана по п.1, в которых SiO2 в форме с низкой молекулярной массой имеет молекулярную массу <100000.
8. Частицы анатазного диоксида титана по п.1, в которых SiO2 включает фрагментарные участки, которые имеют глубину, по существу, ≤5 нм после перераспределения, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии.
9. Частицы анатазного диоксида титана по п.1, в которых TiO2 не был получен в присутствии мочевины.
10. Частицы анатазного диоксида титана по п.2, дополнительно имеющие распределенный на них V2O5.
11. Частицы анатазного диоксида титана по п.10, включающие от 0,5% до 5% по сухому весу V2O5.
12. Частицы анатазного диоксида титана по п.10, в которых V2O5 присутствует на них со значением парциального монослоя менее 1,0 перед спеканием.
13. Частицы анатазного диоксида титана по п.10, которые были подвергнуты спеканию при температуре ≥650°С.
14. Каталитическое устройство для нейтрализации дизельного выхлопа, включающее частицы анатазного диоксида титана по п.10.
15. Система регулирования дизельного выхлопа, включающая:
каталитическое устройство для нейтрализации дизельного выхлопа по п.14; и
дизельный сажевый фильтр, и при этом каталитическое устройство для нейтрализации дизельного выхлопа размещают выше по потоку или ниже по потоку относительно дизельного сажевого фильтра.
16. Способ, в котором катализируют конверсию оксидов азота в газообразный N2, включающий:
воздействие на дизельные выхлопы, включающие NOx, частицами анатазного диоксида титана по п.10 с добавленным восстановителем для образования N2 и H2O.
17. Способ по п.16, в котором восстановитель представляет собой вещество, выбранное из группы, состоящей из NH3, мочевины и их комбинаций.
18. Способ по п.16, в котором частицы анатазного диоксида титана по п.10 включают 0,5%-3% по сухому весу V2O5.
19. Способ по п.16, в котором дизельные выхлопы пропускают через дизельный сажевый фильтр до или после воздействия частиц анатазного диоксида титана по п.10.
20. Способ получения частиц по п.2, включающий стадии, на которых:
готовят суспензию, содержащую TiO2;
объединяют TiO2-суспензию с (1) раствором прекурсора диоксида кремния, содержащим SiO2 главным образом в форме, выбранной из группы, состоящей из форм с низкой молекулярной массой, наночастиц и их комбинаций, и с (2) WO3 с образованием смеси TiO2-WO3-SiO2; причем раствор прекурсора диоксида кремния объединяют с ΤiO2-суспензией до, после или в то время, когда WO3 объединяют с TiO2-суспензией, и
промывают и подвергают спеканию смесь TiO2-WO3-SiO2 с образованием стабилизированного диоксидом кремния титаноксидного материала носителя.
21. Способ по п.20, в котором стабилизированный диоксидом кремния титаноксидный материал носителя включает
86%-94% по сухому весу TiO2, 3%-9% по сухому весу SiO2, и 3%-7% по сухому весу WO3; и в котором титаноксидный материал носителя первоначально имеет удельную площадь поверхности по меньшей мере 80 м2/г перед спеканием.
22. Способ по п.20, в котором ΤiO2 в суспензии включает материал, выбранный из группы, состоящей из предварительно сформированных частиц гидроксида титана, оксигидроксида титана, диоксида титана и их комбинаций.
23. Способ по п.20, в котором TiO2 в суспензии получен не в присутствии мочевины.
24. Способ по п.20, в котором SiO2 в форме наночастиц в растворе прекурсора диоксида кремния главным образом имеет диаметр <5 нм.
25. Способ по п.20, в котором SiO2 в форме с низкой молекулярной массой в растворе прекурсора диоксида кремния главным образом имеет MW <100000.
26. Способ по п.20, в котором SiO2 в растворе прекурсора диоксида кремния включает атомы кремния, которые главным образом находятся в состояниях Q3, Q2, Q1 и Q0 координационного окружения.
27. Способ по п.20, в котором раствор прекурсора диоксида кремния включает вещество, выбранное из группы, состоящей из раствора силиката тетра(алкил)аммония, кремниевой кислоты и их комбинаций.
28. Способ по п.20, в котором SiO2 главным образом включает фрагментарные участки, которые имеют глубину ≤5 нм после перераспределения, по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии.
29. Способ по п.20, включающий стадию, в которой объединяют смесь TiO2-WO3-SiO2 с V2O5 с образованием катализатора на основе оксида ванадия.
30. Способ по п.29, в котором катализатор на основе оксида ванадия включает 0,5%-3% по сухому весу V2O5.
31. Способ по п.29, в котором V2O5 в катализаторе на основе оксида ванадия присутствует со значением парциального монослоя менее 1,0 перед спеканием.
32. Способ по п.29, включающий дополнительную стадию, на которой катализатор на основе оксида ванадия подвергают спеканию при температуре ≥650°С.
33. Способ получения частиц по п.1, включающий стадии, на которых:
готовят TiO2-суспензию, содержащую частицы TiO2;
готовят источник дисперсного диоксида кремния;
объединяют TiO2-суспензию с источником дисперсного диоксида кремния с образованием TiO2-SiO2 - смеси; и
доводят значение рН TiO2-SiO2 - смеси до <8,5 и температуру до <80°С, причем источник дисперсного диоксида кремния растворяют и переосаждают на частицах TiO2 с образованием стабилизированного диоксидом кремния титаноксидного материала носителя катализатора.
34. Способ по п.33, дополнительно включающий стадию, на которой объединяют стабилизированный диоксидом кремния титаноксидный материал носителя катализатора с WO3 для получения стабилизированного диоксидом кремния титаноксид-вольфрамового материала носителя катализатора.
35. Способ по п.34, дополнительно включающий стадии, на которых стабилизированный диоксидом кремния титаноксид-вольфрамовый материал носителя катализатора промывают и подвергают спеканию.
36. Способ по п.34, в котором стабилизированный диоксидом кремния титаноксид-вольфрамовый материал носителя катализатора включает:
86%-94% по сухому весу TiO2, 3%-9% по сухому весу SiO2, и 3%-7% по сухому весу WO3; и в котором титаноксидный материал носителя первоначально имеет удельную площадь поверхности по меньшей мере 80 м2/г перед спеканием.
37. Способ по п.33, в котором частицы TiO2 в TiO2-суспензии включают материал, выбранный из группы, состоящей из предварительно сформированных частиц гидроксида титана, оксигидроксида титана, диоксида титана и их комбинаций.
38. Способ по п.33, в котором частицы TiO2 в TiO2-суспензии получены не в присутствии мочевины.
39. Способ по п.33, в котором SiO2 в TiO2-SiO2 - смеси после растворения включает атомы кремния, которые находятся главным образом в состояниях Q3, Q2, Q1 и Q0 координационного окружения.
40. Способ по п.33, в котором SiO2 на частицах TiO2 главным образом включает фрагментарные участки, которые имеют глубину ≤5 нм после перераспределения SiO2 по наблюдениям с помощью сканирующей электронной микроскопии или трансмиссионной электронной микроскопии.
41. Способ по п.34, включающий стадию, на которой объединяют смесь TiO2-WO3-SiO2 с V2O5 с образованием катализатора на основе оксида ванадия.
42. Способ по п.41, в котором катализатор на основе оксида ванадия включает 0,5%-3% по сухому весу V2O5.
43. Способ по п.41, в котором V2O5 катализатора на основе оксида ванадия присутствует со значением парциального монослоя менее 1,0 перед спеканием.
44. Способ по п.41, включающий дополнительную стадию, на которой катализатор на основе оксида ванадия подвергают спеканию при температуре ≥650°С.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| US 6956006 B1, 18.10.2005 | |||
| US 5198403 A, 30.03.1993 | |||
| ЧАСТИЦЫ ДИОКСИДА ТИТАНА | 1997 |
|
RU2162443C2 |
| R.J.DAVIS ET AL., Titania-Silica: A Model Binary Oxide Catalyst System, CHEMISTRY OF MATERIALS, 1997, vol.9, pp | |||
| Насадка для бунзеновской горелки лабораторного типа | 1923 |
|
SU2311A1 |
Авторы
Даты
2015-06-10—Публикация
2010-09-07—Подача