Изобретение относится к практическому здравоохранению, физиологии, может быть использовано в качестве способа медицинского обследования. Изобретение может быть также использовано в гинекологической и акушерской практике для прогнозирования риска возникновения патологических состояний, осложнения течения беременности, диагностике и мониторинге развития ряда заболеваний (например, синдрома Леша-Найхана, болезни Канавана и др.). Изобретение относится к химическому анализу биологических материалов, например крови, мочи, исследованию или анализу материалов путем разделения на составные части (компоненты) с использованием адсорбции, абсорбции или подобных процессов или с использованием ионного обмена, а также метаболомному анализу, который также называют анализом метаболического профиля. В основе изобретения лежит количественный анализ гипоксантина, ксантина и мочевой кислоты в сыворотке крови человека с последующим сравнением их значений с пороговыми для оценки риска возникновения нарушений течения беременности.
В настоящее время важным аспектом акушерской практики и наблюдения за беременностью является оценка риска беременности и перинатальной патологии.
На сегодняшний день существует ряд биомаркеров, измерение концентраций которых в крови, моче, амниотической жидкости используется для оценки возникновения нарушений гестационного процесса, а именно преэклампсии, гипоксии, преждевременных родах. Следует отметить некоторые белковые показатели, измеряемые в сыворотке крови матери и позволяющие проводить оценку риска возникновения преэклампсии не только во втором и третьем триместрах беременности, и на более ранних сроках гестации (плацентарный фактор роста (PLGF), сосудисто-эндотелиальный фактор роста (VEGF), fms-подобная тирозин киназа 1 (sFLT-1), эндотелии-1, 2). Оценку риска возникновения преждевременных родов осуществляют по результатам анализов крови на гормоны - прогестерон, пролактин, эстрогены и кортизол, а также назначают динамическое исследование в крови беременной уровня хорионического гонадотропина человека (ХГЧ).
Известен способ оценки риска возникновения патологии беременности, в частности преэклампсии, в основе которого лежит определения соотношения концентраций белков sFlt-1 / PLGF в кровотоке [1]. В случае преэклампсии уровень sFlt-1 в плазме крови беременных женщин повышен, а уровень PLGF понижен по сравнению с нормально протекающей беременностью. Таким образом, соотношение sFlt-1/PLGF позволяет выявить риск развивающейся преэклампсии.
В литературе описываются применения подобных вышеуказанному способов оценки риска возникновения нарушений течения беременности на основании определения концентраций VEGF, PLGF и sFlt-1, среди недостатков которых отмечается высокая длительность анализа, невысокая чувствительность при исследовании пациенток на ранних сроках гестации.
Известен способ неизвазивной оценки риска развития преэклампсии в I триместре беременности путем определения концентраций указанных белков методами иммуноферментного анализа (ИФА), в моче с использованием для диагностики коэффициента uFP=log(sFlt-1/PLGF*100). Метод гарантирует диагностическую точность 88.2% при uFP>2.1 [2].
Известен способ оценки риска возникновения преэклампсии и эклампсии на сроке не более 20 недель путем определения концентрации в биологическом образце, по крайней мере, одного из белков sFlt-1, PLGF, VEGF или любой их комбинации с использованием ИФА. В качестве образца могут быть использованы моча или сыворотка крови. Индикатором риска развития преэклампсии или эклампсии может быть, в частности, уровень sFlt-1>2 нг/мл или антиангиогенный индекс преэклампсии (PAAI): sFlt-1/VEGF+PLGF, превышающий 20 [3].
В литературе описаны также способы, позволяющие диагностировать преэклампсию на сроке беременности от 12 недель с использованием данных генотипирования и ИФА содержания различных форм VEGF и его рецепторов, а также PLGF [4-6].
Известен способ ранней оценки риска возникновения нарушений беременности, в частности преэклампсии, уже начиная с 5 недели (а также на сроке 6-12, 14, 16, 18, 20 или 24 недель) с использованием ангиогенных биомаркеров sFlt-1 и PLGF. Также описывается диагностика других нарушений течения беременности путем определения концентраций глобулина, связывающего половые гормоны (SHBG), цитокинов и интерлейкина 6 [7].
Известны также способы ранней оценки риска развития патологий беременности, основанные на измерении концентраций многих других белков, а также мониторинге уровня экспрессии кодирующих их генов в биологическом материале, взятом у беременных женщин. К таким белкам относятся плацентарный и сывороточный изоферритин [8], гемоглобин [9, 10], ингибин А [11], TGF [12], синцитин [13], а также специфический полипептид с молекулярной массой 26.6 кДа [14].
Известны способы, в которых наряду с PLGF отмечается возможность использования РАРР-А (pregnancy-associated plasma protein А) для диагностики как ранней (начиная с 11-13 недели), так и поздней (после 34 недели) преэклампсии. В тест-систему для диагностики преэклампсии и связанных с ней нарушений также включены реагенты для определения других биомаркеров (РР13, ММР3, TNFR1, ADAM12 и др.) [15].
Известен способ, описывающий процедуру скрининга гестационных нарушений, в том числе преэклампсии, на 6-24 неделях беременности и основанный на определении уровня PLGF, SHGB, а также группы цитокинов в составе крови, мочи, амниотической жидкости, плацентраной ткани и других биологических образцов, отобранных у беременных женщин [16]. Диагностическая система включает в себя биологический микрочип с иммобилизированными реагентами для упрощения детектирования интересующих белковых молекул.
Способ [17] предназначен для оценки риска возникновения преэклампсии в течение всей беременности, и включает определение экспрессии по крайней мере одного, двух или трех биомаркеров апоптических процессов трофобласта на основе иммуноферментного и других методов анализа цельной крови или сыворотки крови матери. В частности, для оценки риска в первом триместре беременности используется, по крайней мере, один биомаркер из группы: Ang, Leptin, RANTES, PDGF, ICAM I, VEGF, G-SCF, Fas, EGF, IGFBP 1, MCP 1, IL8, FasL, - а также связанных с ними ферментов и метаболитов.
Известен способ оценки риска развития преэклампсии на 9-11 или 10-14 неделях беременности с использованием тест-систем, позволяющих определять концентрации различных комбинаций белковых молекул (от 5 до 40 в каждой системе) в сыворотке материнской крови с помощью метода ИФА [18].
В способе [19] представлено более 150 генов, дифференциально экспрессируемых в случае преэклампсии по сравнению с нормально протекающей беременностью, а также различные методы диагностики, включающие исследование экспрессии генов с помощью гибридизационных чипов или ПЦР, а также определение концентраций кодируемых ими биомаркеров в биологических образцах методами ИФА, ВЭЖХ, ВЭЖХ-МС, блоттинга и др.
Способ [20] представляет собой метод ранней (начиная с 13 недели) диагностики риска преждевременных родов с помощью определения уровня экспрессии генов-биомаркеров (от 27 до 611 возможных биомаркеров в представленных тест-системах) в клетках крови матери.
Известен также способ, в котором предложен анализ комплекса (33) белковых биомаркеров для оценки риска развития преэклампсии, начиная с 5 недели беременности, однако наиболее оптимальным сроком для проведения диагностики является 22-24 неделя беременности [21].
Известен также способ, используемый для диагностики преэклампсии на сроке 12-14 недель. Способ заключается в хроматографическом разделении белков в составе сыворотки крови, мочи, амниотической жидкости, а также других биологических жидкостях и тканях, с последующим МС-детектированием. В роли биомаркеров преэклампсии используют интенсивности отдельных пиков (соответствующие определенным величинам m/z), диагностика проводится с использованием соотношений различных биомаркеров [22].
Способ, аналогичный описанному выше, но используемый для диагностики риска преждевременных родов, описан в [23].
Известен также способ, используемый для оценки риска возникновения преждевременных родов, начиная с 12 недели беременности. Способ основан на ИФА биологического материала, в качестве которого может быть использована как жидкость, так и твердая масса, отобранная в области заднего свода матки. Исследование материала включает анализ содержания 6 основных групп белковых продуктов локального воспаления (цитокины, простеноиды, коллагеназа, эластаза, фибронектин, церуллоплазмин, фибрин, интерфероны, иммуноглобулины, продукты жизнедеятельности мисцеллярных белых кровяных клеток и др.) [24].
Таким образом, большая часть способов оценки риска возникновения нарушений течения беременности, а именно преэклампсии, гипоксии, преждевременных родов, основаны на анализе ряда белков, измерение концентраций которых в сыворотке крови, моче, амниотической жидкости и другом биологическом материале на сегодняшний день используется для оценки риска возникновения патологии беременности. Однако данные заболевания являются многосистемными и маловероятно, что их обнаружение и оценка риска возникновения связаны с одним или группой белков (единичные маркеры имеют недостаточную чувствительность (от 30 до 60% в случае, например, преэклампсии)).
В биологических жидкостях человека следует оценивать также и присутствующие в значительном количестве другие вещества, метаболиты, которые могут быть значительно более важными биомаркерами и использование которых для диагностики позволит выявлять риск возникновения патологий уже в I триместре беременности, поскольку метаболиты наиболее тесно связаны с активностью клетки или организма на функциональном уровне.
В последние годы наблюдается рост исследований, в которых были получены данные, подтверждающие важность применения метаболомных исследований для оценки риска возникновения нарушений течения беременности. В этих работах были получены данные о взаимосвязи метаболических маркеров с различными видами нарушений, такими как ранние потери беременности, преэклампсия, нарушенное развитие плода, преждевременные роды [25-30].
Известен способ ранней оценки риска возникновения преэклампсии, в котором наряду с группой белковых молекул используют в качестве биомаркера уровень гликозаминогликанов (ГАГ) в образце биопсии плаценты, определяемый с помощью хромато графических методов [31]. Недостатком известного способа является необходимость биопсии плаценты, что создает предпосылки для осложнения беременности.
Известен способ прогноза развития преэклампсии, включающий забор биологической жидкости (кровь, моча, синовиальная жидкость, цереброспинальная жидкость), определение содержания в ней гистидина или его метиловых производных, а также липидов и кетоновых тел методами ЯМР-спектроскопии (предпочтительный метод) и/или ферментативного анализа и/или методами разделения и/или определения антител. При отклонении полученных показателей от известных для женщин на данных сроках с нормально протекающей беременностью делают заключение о риске развития преэклампсии [32].
Все перечисленные выше способы оценки риска возникновения патологии беременности не обладают необходимой чувствительностью, а применяемые методы исследования биологического материала с использованием иммуноферментного анализа, масспектрометрии, ядерно-магнитного резонанса являются длительными, при этом осуществление некоторых из них затруднено в условиях рутинного клинического анализа при отсутствии высококвалифицированного обслуживающего персонала. Другим недостатком является высокая стоимость оборудования для ЯМР.
Известен способ определения риска развития преэклампсии беременности, включающий забор биологического материала (кровь, сыворотка, плазма, моча, спиномозговая жидкость, синовиальная жидкость, амниотическая жидкость, вагинальная жидкость, жидкость, полученная при лаваже, ткань или их комбинация), разделение биомаркеров белковой природы методом капиллярной жидкостной хроматографии, идентификация хотя бы одного из 9 биомаркеров по времени их высвобождения Rf (аналог времени удерживания, определяющий расположение пика на хроматограмме относительно других пиков), проведение масс-спектрометрического анализа для количественного определения по предварительно построенным калибровочным кривым концентрации m/z хотя бы одного из предложенных девяти биомаркеров; определении количественного соотношения концентраций различных биомаркеров в исследуемом биологическом материале, причем количественные параметры, используемые для диагностики (линейные комбинации указанных соотношений), подобраны таким образом, что их отрицательное значение свидетельствует о риске развития преэклампсии, в то время как положительное значение говорит об отсутствии такого риска. Недостатком известного способа то, что он не позволяет одновременно определить риск развития преждевременных родов. Кроме того, способ является трудоемким и требует привлечения высококвалифицированного персонала (33).
Наиболее близким к заявленному является способ оценки риска развития преэклампсии, включающий определение в плазме крови или других биологических жидкостях беременной женщины концентрации асимметричной (АДМА) и симметричной (СДМА) форм диметиларгинина с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) или ИФА (предпочтительно на 10-25 неделях беременности), при концентрация АДМА>1.45 мкмоль/л и/или величине АДМА, по крайней мере, в 3 раза превышающей уровень АДМА у женщин, не испытавших преэклампсию и/или при соотношении концентраций АДМА/СДМА, по крайней мере, в 5 раз более высоком по сравнению с нормально протекающей беременностью, делают заключение о риске развития преэклампсии (34). Для реализации способа плазму в объеме 1,5 мл наносят на активированную катионообменную колонку, элюируют, элюент испаряют в среде жидкого азота, осадок растворяют, фильтруют и хроматографируют с помощью ВЭЖХ. Для идентификации биомаркеров в данном способе требуется их предварительная модификация реагентом офтальальдегид (o-phthalaldehyde, ОРА) Недостатком известного способа является то, что он не позволяет одновременно выявлять риск развития преждевременных родов. Кроме того, способ является трудоемким, т.к. включает длительную предварительную подготовку образцов до стадии хроматографии, включающую нанесение на катионообменную колонку, испарение элюента в среде жидкого азота, необходимость предварительной модификации биомаркеров для их идентификации. Кроме того, для осуществления способа требуется достаточно большой объем крови.
Задачей, на решение которой направлено изобретение, является дополнительное определение риска развития преждевременных родов, расширение арсенала средств для определения риска развития преэклампсии, снижение трудоемкости способа, уменьшение количества забираемой крови.
Решение поставленной задачи достигается тем, что в качестве биомаркеров риска развития патологии беременности используют концентрацию гипоксантина, ксантина, мочевой кислоты, для чего сыворотку крови разводят дистиллированной водой, освобождают от белков, маскирующих определение биомаркеров риска развития патологии беременности путем фильтрования и последующего центрифугирования; в осажденной фракции разделяют биомаркеры риска развития патологии беременности при помощи обращенно-фазовой жидкостной хроматографии с использованием буферного раствора, содержащего ион-парный реагент; одновременно регистрируют сигнал в ультрафиолетовой области спектра, соответствующий гипоксантину, ксантину, мочевой кислоте; вычисляют концентрацию гипоксантина, ксантина, мочевой кислоты по времени удерживания и площади пика поглощения в сравнении с аналогичными показателями стандартного раствора, содержащего заведомо известные концентрации гипоксантина, ксантина, мочевой кислоты; при концентрации мочевой кислоты более 600 мкмоль/л делают заключение о риске развития преэклампсии; при соотношении концентраций гипоксантин/ксантин более 0.9 - о риске развития преждевременных родов; сыворотку крови предварительно разводят дистиллированной водой в 2 раза; освобождение разведенной дистиллированной водой сыворотки крови от белков, маскирующих определение биомаркеров риска развития патологии беременности, осуществляют путем фильтрования через мембрану инертного фильтра с отсечкой по молекулярному весу разделяемых компонентов в 3 кДа и последующего центрифугирования в течение 30 мин при температуре 4°C со скоростью 10500 g; в качестве ион-парного реагента используют тетрабутиламмоний сульфат; регистрацию сигнала в ультрафиолетовой области спектра, соответствующего мочевой кислоте, ксантину, гипоксантину, осуществляют с помощью высокочувствительного диод-матричного детектора при длине волны 260 нм.
Раскрытие изобретения
Способ осуществляют следующим образом.
Выполняют забор венозной крови, получают сыворотку крови, разводят ее дистиллированной водой, освобождают полученный раствор от белков, маскирующих определение биомаркеров риска развития патологии беременности путем фильтрования и последующего центрифугирования. В осажденной фракции разделяют биомаркеры риска развития патологии беременности при помощи обращенно-фазовой жидкостной хроматографии с использованием буферного раствора, содержащего ион-парный реагент. Одновременно регистрируют сигнал в ультрафиолетовой области спектра, соответствующий гипоксантину, ксантину, мочевой кислоте. Вычисляют концентрацию гипоксантина (HYP), ксантина (XAN), мочевой кислоты (UA), по времени удерживания и площади пика поглощения в сравнении с аналогичными показателями стандартного раствора, содержащего заведомо известные концентрации гипоксантина, ксантина, мочевой кислоты. При концентрации мочевой кислоты более 600 мкмоль/л делают заключение о риске развития преэклампсии; при соотношении концентраций гипоксантин/ксантин более 0.9 - о риске развития преждевременных родов.
Венозную кровь объемом 250 мкл отбирают в вакуумные пробирки, с последующим выделением сыворотки крови согласно стандартному протоколу, аналогично описанному в [35]. Пробу сыворотки крови разводят в 2 раза дистиллированной водой (например, 250 мкл сыворотки и 250 мкл воды). Для освобождения от белков, маскирующих определение биомаркеров риска развития патологии беременности, полученный раствор фильтруют путем нанесения на мембрану инертного фильтра с отсечкой по молекулярному весу разделяемых компонентов в 3 кДа, затем центрифугируют в течение 30 мин при температуре 4°C и 10500×g оборотах. На дне пробирки собирают осажденную фракцию, не содержащую белков, маскирующих определение метаболитов.
В осажденной фракции объемом 100 мкл разделяют биомаркеры риска развития патологии беременности при помощи обращенно-фазовой жидкостной хроматографии с использованием буферного раствора, содержащего ион-парный реагент. В качестве ион-парного реагента используют тетрабутиламмоний сульфат.
В качестве подвижной фазы используют два буфера. Буфер А содержит 12 мМ тетрабутиламмоний сульфат, 10 мМ КН2РО4 и 0,125% метанола, pH 7.00. Буфер Б: 2.8 мМ тетрабутиламмоний сульфат, 100 мМ КН2РО4, 30% метанола, pH 5.50. Разделение смеси осуществляют градиентным элюированием в следующем режиме: 20 мин 100% буфера А, 8 мин 80% буфера А и 20% буфера Б, 10 мин 70% буфера А и 30% буфера Б, 12 мин 55% буфера А и 45% буфера Б, 11 мин 40% буфера А и 60% буфера Б, 9 мин 15% буфера А и 85% буфера Б, 10 мин 0% буфера А и 100% буфера Б, 10 мин 50% буфера А и 50% буфера Б, 15 мин 100% буфера А. Скорость потока 1.2 мл/мин, температура колонки 10°C. Разделение осуществляют с помощью обращенно-фазовой хроматографической колонки Hypersil С-18, размер частиц 5 мкм, размер колонки 250×4.6 мм. Колонку защищают предколонкой.
Регистрацию сигнала, соответствующего каждому биомаркеру в ультрафиолетовой области спектра, осуществляют с помощью высокочувствительного диод-матричного детектора при длине волны 260 нм.
Для определения концентраций веществ в сыворотке крови используют калибровочные кривые, получаемые посредством метода внутреннего стандарта при использовании соответствующего метаболита известной концентрации, при этом процедуру выполняют отдельно для каждого метаболита (гипоксантина, ксантина, мочевой кислоты) следующим образом. Биомаркер известной концентрации добавляют к аликвоте сыворотки крови, не используемой в анализе (обозначим Сыворотка А). Готовят стандартную навеску метаболита (например, гипоксантина) массой 1 мг, растворяют ее в 1 мл 1 М раствора NaOH до получения гомогенной смеси. Для нейтрализации pH к полученному раствору добавляют по каплям 1 М НСl до значения pH 6-7. Разбавляют полученный раствор в 2, 4, 8, 16 раз (четыре разведения). К 100 мкл дистиллированной воды и к 100 мкл каждого из полученных растворов добавляют 100 мкл Сыворотки А, тщательно перемешивают. Далее согласно заявленному способу освобождают полученные растворы для построения калибровочных кривых, а также образец Сыворотки А от белков, маскирующих определение биомаркеров риска развития патологии беременности путем фильтрования и последующего центрифугирования. В осажденной фракции разделяют биомаркеры риска развития патологии беременности при помощи обращенно-фазовой жидкостной хроматографии с использованием буферного раствора, содержащего ион-парный реагент.Одновременно регистрируют сигнал в ультрафиолетовой области спектра, соответствующий гипоксантину, ксантину, мочевой кислоте. Для растворов для построения калибровочных кривых вычисляют площади хроматографических пиков при известном времени удерживания, характерном для каждого из биомаркеров: 4.14±0.12 мин для гипоксантина; 5.43±0.10 мин - для ксантина; 10.66±0.21 мин - для мочевой кислоты (36). Калибровочные кривые строят в координатах зависимости концентрации метаболита от площади пика поглощения.
Концентрации биомаркеров в анализируемых пробах беременных женщин вычисляют согласно полученным калибровочным кривым с учетом времени удерживания и площади пика поглощения при длине волны 260 нм.
Вычисляют концентрацию мочевой кислоты, а также отношение концентраций гипоксанина и ксантина:
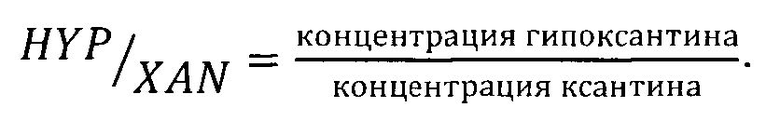
Полученные значения концентрации мочевой кислоты (UA), отношения концентраций 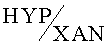

Данные критерии отражают особенности изменения метаболизма ксантина, гипоксантина, мочевой кислоты при риске возникновении преэклампсии или преждевременных родов. Заявленный способ обладает высокой чувствительностью, специфичностью и воспроизводимостью. В заявленном способе в сравнении с прототипом не требуется подготовка образца с помощью катионообменной колонки, предварительная модификация биомаркеров для их идентификации. Объем забираемой крови существенно ниже. Все это делает возможным широкое использование способа оценки риска возникновения патологии беременности в клинической практике.
Осуществление изобретения
Пациентка 1. Возраст: 23 года. Неделя беременности - 15. Индекс массы тела: 27.5 кг/м2. Систолическое артериальное давление: 113 мм рт.ст. Диастолическое артериальное давление: 67 мм рт.ст. Содержание белка в моче (суточное): 0,7 г (протеинурия). Повышенное содержание белка в моче, наличие артериальной гипертензии в семейном анамнезе. В связи с этим рекомендованы динамическое наблюдение артериального давления и хроматографический анализ сыворотки венозной крови на содержание метаболитов пуринового пути.
Определено следующее содержание метаболитов в сыворотке крови:
Гипоксантин - 7,9 мкМ
Ксантин - 3,11 мкМ
Мочевая кислота - 442,0 мкМ
HYP/XAN - 2,54
Согласно результатам динамического исследования артериального давления поставлен диагноз - артериальная гипертензия. Отношение HYP/XAN превышает 0.9, возможен риск преждевременных родов. На 23 неделе обнаружена повышенная сократительная деятельность матки, укорочение и размягчение шейки матки. Выбор выжидательной тактики ведения беременности с угрозой прерывания. В последствии преэклампсия не выявлена.
Пациентка 2. Возраст: 28 лет. Неделя беременности - 17. Индекс массы тела: 25,7 кг/м2. Систолическое артериальное давление: 137 мм рт.ст. Диастолическое артериальное давление: 92 мм рт.ст. Содержание белка в моче (суточное): 0,3 г. В связи с повышенным артериальным давлением рекомендован хроматографический анализ сыворотки венозной крови по заявленному способу на содержание метаболитов пуринового пути. Определено следующее содержание метаболитов в сыворотке крови:
Гипоксантин - 13,8 мкМ
Ксантин - 12,7 мкМ
Мочевая кислота - 739,0 мкМ
HYP/XAN - 1,086
Концентрация мочевой кислоты более 600 мкМ.
Согласно результатам хроматографического анализа сыворотки венозной крови пациентки во время беременности возможно развитие преэклампсии и повышен риск преждевременных родов.
На 18 неделе обнаружена повышенная сократительная деятельность матки, укорочение и размягчение шейки матки. Выбор выжидательной тактики ведения беременности с угрозой прерывания. В последствие выявлена преэклампсия на 28 неделе беременности.
Пациентка 3. Возраст: 22 года. Неделя беременности - 15. Индекс массы тела: 26 кг/м2. Систолическое артериальное давление: 140 мм рт.ст. Диастолическое артериальное давление: 89 мм рт.ст. Содержание белка в моче (суточное): 0,28 г. В связи с повышенным артериальным давлением рекомендован хроматографический анализ сыворотки венозной крови на содержание метаболитов пуринового пути.
Определено следующее содержание метаболитов в сыворотке крови:
Гипоксантин - 13,7 мкМ
Ксантин - 16,7 мкМ
Мочевая кислота - 824,9 мкМ
HYP/XAN-0,82.
Согласно результатам хроматографического анализа сыворотки венозной крови пациентки по заявленному способу во время беременности возможно развитие преэклампсии.
В последствии преэклампсия выявлена на 25 неделе.
Пациентка 4.
Возраст: 29 года. Неделя беременности - 19. Индекс массы тела: 28,1 кг/м2. Систолическое артериальное давление: 120 мм рт.ст. Диастолическое артериальное давление: 82 мм рт.ст. Содержание белка в моче (суточное): 0,2 г. Определено следующее содержание метаболитов в сыворотке крови согласно заявленному способу:
Гипоксантин - 13,4 мкМ
Ксантин - 19,1 мкМ
Мочевая кислота - 518,3 Мкм
HYP/XAN - 0,7
Согласно результатам хроматографического анализа сыворотки венозной крови пациентки по заявленному способу во время беременности не предполагается развитие патологии беременности. Впоследствии беременность протекала физиологически и завершилась нормальными родами.
Литература.
1. Muteins of placental growth factor type 1, preparation and application thereof. Maglione, D. US 7314734 B2, 19.05.2003.
2. Diagnosis of preeclampsia. Buhimschi, C., Buhimschi, I., Norwitz, E. US 2010/0227342, 17.05.2010
3. Methods of diagnosing pre-eclampsia or eclampsia. Karumanchi, S., Maynard, S., Sukhatme, V. 7947449, 4.08.2008.
4. Detection of risk of pre-eclampsia. Bates, D., Bills, V., Harper, S., Qiu, Y. US 2011/0076259, 24.09.2010.
5. Variants of VEGFR and their use in the diagnosis and treatment of pregnancy associated medical conditions. Keshet, E., Sela, S., Ithin, A., Yagel, S. US 2010/0136012, 20.12.2007.
6. Modulators of VEGF splicing as pro- and anti-angiogenic agents. Bates, D., Harper, S., James, N., Dawid, G. WO 2008/110777, 10.03.2008.
7. Screening for gestational disorders. Thadhani, R., Karumanchi, S. US 7344892, 23.09.2004.
8. Isoferritin as a marker for pathological pregnancy. Moroz; C. US 5871735, 12.06.1990.
9. Diagnosis and treatment of preeclampsia. Hansson, S., Akerstrom, B. US 2010/0105070 A1, 12.02.2008.
10. Diagnosis of preeclampsia in mammals. Olson; C, Peterson; C. US 5849474, 06.12.1995.
11. Inhibin-A: a marker for differentiation, diagnosing and screening abnormal pregnancies. Segal, S., Rivnay, B. US 2006/0046274 A1, 31.08.2004.
12. Methods for early diagnosing of an increased risk of preeclampsia. Caniggia, I., Post, M., Lye, S. US 7754495 B2, 16.10.2008.
13. Diagnosis and treatment of preeclampsia. Buhimschi, I., Norwitz, E., Buhimschi, C, Tsen, L. WO 2005/093413, 22.03.2005.
14. Method of diagnosing preeclampsia. Voroteliak, V. US 2010/0190192 A1, 15.09.2009.
15. Methods for determining the risk of prenatal complications. Cuckle, H., Ahola, Т., Poon, L. US 2010/0304412, 26.01.2009.
16. Compositions and methods for healthy pregnancy. Carter, D. US 2008/0213301 A1, 05.05.2008.
17. Methods of determining whether a pregnant woman is at risk of developing preeclampsia. Mor, G., Neale, D., Romero, R. US 7790463 B2, 02.02.2006.
18. Maternal serum biomarkers for detection of pre-eclampsia. Nagalla, S., Rasanen, J., Gravett, M. US 2010/0016173 A1, 30.01.2009.
19. Biomarkers for preeclampsia. Fisher, S., Winn, V., Haimov-Kochman, R. US 2008/0233583 A1, 20.02.2008.
20. Preterm delivery diagnostic assay. Williams, M., Enquobahrie, D. US 2011/0144076 A1, 01.05.2009.
21. Biomarkers for hypertensive disorders of pregnancy. Kas, K. US 2011/0251094 A1, 13.04.2011.
22. Identifying and quantifying biomarkers associated with preeclampsia. Graves, S., Esplin, M. US 2011/0247404 A1, 24.06.2009.
23. Identification and quantification of biomarkers for evaluating the risk of preterm birth. Graves, S., Esplin, M., Thulin, C. US 2010/0297679 A1, 17.07.2008.
24. Screening method for identifying women at increased risk for imminent delivery. Senyei; A., Casal; D. US 5516702, 29.06.1994.
25. Robust early pregnancy prediction of later preeclampsia using metabolomic biomarkers. Kenny LC, Broadhurst DI, Dunn W, Brown M, North RA, McCowan L, Roberts C, Cooper GJ, Kell DB, Baker PN. // Hypertension. 2010. V. 56(4), pp. 741-749.
26. Metabolomics in premature labor: a novel approach to identify patients at risk for preterm delivery. Romero R, Mazaki-Tovi S, Vaisbuch E, Kusanovic JP, Chaiworapongsa T, Gomez R, Nien JK, Yoon BH, Mazor M, Luo J, Banks D, Ryals J, Beecher C. // J Matern Fetal Neonatal Med. 2010. V. 23(12), pp. 1344-1359.
27. Changes in the metabolic footprint of placental explant-conditioned medium cultured in different oxygen tensions from placentas of small for gestational age and normal pregnancies. Horgan RP, Broadhurst DI, Dunn WB, Brown M, Heazell AE, Kell DB, Baker PN, Kenny LC. // Placenta. 2010. V. 31(10), pp. 893-901.
28. Changes in the metabolic footprint of placental explant-conditioned culture medium identifies metabolic disturbances related to hypoxia and pre-eclampsia. Dunn WB, Brown M, Worton SA, Crocker IP, Broadhurst D, Horgan R, Kenny LC, Baker PN, Kell DB, Heazell AE. // Placenta. 2009. V. 30(11), pp. 974-980.
29. Identification and quantification of preterm birth biomarkers in human cervicovaginal fluid by liquid chromatography/tandem mass spectrometry. Shah SJ, Yu KH, Sangar V, Parry SI, Blair IA. // J Proteome Res. 2009. V. 8(5), pp. 2407-2417.
30. Maternal-fetal metabolism in normal pregnancy and preeclampsia, von Versen-Hoeynck FM, Powers RW. // Front Biosci. 2007. V. 1, pp. 2457-2470.
31. Biomarker and composition for diagnosis of preeclampsia and method for using the same. Park, W., Kim, N., Warda, M., Han, J. US 2011/0269136 A1, 28.02.2011.
32. Biomarkers for preeclampsia. Fisher, J., Turner, E., Walker, J. US 2010/0190181 A1, 26.06.2007.
33. Screen for preeclampsia. Savvidou, M., Hingorani, A., Vallance, P., Nicolaides, K. US 2007/0185200 A1, 19.04.2004.
34. Identifying and quantifying biomarkers associated with preeclampsia. Graves, S., Esplin, M. US 2011/0247404 A1, 24.06.2009.
35. Применение метода молекулярной спектроскопии средней инфракрасной области для определения ряда биохимических показателей сыворотки крови. С.А. Хаустова, Я.И. Давыдов, Е.В. Трушкин, М.Ю. Шкурников, Р. Мюллер, Й. Бекхаус, А.Г. Тоневицкий // Бюллетень экспериментальной биологии и медицины. 2009. Т. 148, С. 707-711.
36. Simultaneous high performance liquid chromatographic separation of purines, pyrimidines, N-acetylated amino acids, and dicarboxylic acids for the chemical diagnosis of inborn errors of metabolism. B. Tavazzi, G. Lazzarino, P. Leone, A.M. Amorini, F. Bellia, C.G. Janson, V. Di Pietro, L. Ceccarelli, S. Donzelli, J.S. Francis, B. Giardina // Clin. Biochem. 2005. V. 38, pp. 997-1008.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития преэклампсии у женщин разных соматотипов | 2018 |
|
RU2679111C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С САХАРНЫМ ДИАБЕТОМ 1 ТИПА | 2022 |
|
RU2800717C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА | 2022 |
|
RU2800716C1 |
| Способ диагностики врастания плаценты в стенку матки у женщин с предлежанием плаценты | 2021 |
|
RU2771874C1 |
| Прогнозирование преэклампсии на основе определения внеклеточной ДНК плода в материнской крови при проведении скрининга первого триместра беременности | 2019 |
|
RU2697845C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПУРИНОВ И ПИРИМИДИНОВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ЧЕЛОВЕКА | 2012 |
|
RU2620155C2 |
| СПОСОБ ПРОЛОНГИРОВАНИЯ БЕРЕМЕННОСТИ ПРИ РАННЕЙ ПРЕЭКЛАМПСИИ | 2023 |
|
RU2803574C1 |
| Способ дифференциальной диагностики изолированной преэклампсии и преэклампсии, развившейся на фоне недиагностированной хронической артериальной гипертензии | 2019 |
|
RU2713436C1 |
| Способ прогнозирования развития гипертензивных расстройств при беременности в средней группе риска среди прошедших комбинированный скрининг 1 триместра | 2023 |
|
RU2803010C1 |
| Способ прогнозирования риска развития преэклампсии | 2023 |
|
RU2817206C1 |
Изобретение относится к медицине, а именно к способу оценки риска развития патологии беременности. Сущность способа состоит в том, что в качестве биомаркеров оценки риска развития патологии беременности используют концентрацию гипоксантина, ксантина, мочевой кислоты, для чего сыворотку крови разводят дистиллированной водой, освобождают от белков, маскирующих определение биомаркеров риска развития патологии беременности. В осажденной фракции разделяют биомаркеры риска развития патологии беременности при помощи обращенно-фазовой жидкостной хроматографии с использованием буферного раствора, содержащего ион-парный реагент, регистрируют сигнал в ультрафиолетовой области спектра, соответствующий гипоксантину, ксантину, мочевой кислоте. Вычисляют концентрации. При концентрации мочевой кислоты более 600 мкмоль/л делают заключение о риске развития преэклампсии, а при соотношении концентраций гипоксантин/ксантин более 0,9 - о риске развития преждевременных родов. Использование заявленного способа позволяет повысить эффективность оценки риска развития патологии беременности. 4 з.п. ф-лы, 1 табл., 4 пр.
1. Способ оценки риска развития патологии беременности, включающий забор венозной крови, выделение сыворотки крови, определение в ней содержания биологических маркеров риска развития преэклампсии методом жидкостной хроматографии, отличающийся тем, что в качестве биомаркеров риска развития патологии беременности используют концентрацию гипоксантина, ксантина, мочевой кислоты, для чего сыворотку крови разводят дистиллированной водой, освобождают от белков, маскирующих определение биомаркеров риска развития патологии беременности путем фильтрования и последующего центрифугирования; в осажденной фракции разделяют биомаркеры риска развития патологии беременности при помощи обращенно-фазовой жидкостной хроматографии с использованием буферного раствора, содержащего ион-парный реагент; одновременно регистрируют сигнал в ультрафиолетовой области спектра, соответствующий гипоксантину, ксантину, мочевой кислоте; вычисляют концентрацию гипоксантина, ксантина, мочевой кислоты по времени удерживания и площади пика поглощения в сравнении с аналогичными показателями стандартного раствора, содержащего заведомо известные концентрации гипоксантина, ксантина, мочевой кислоты; при концентрации мочевой кислоты более 600 мкмоль/л делают заключение о риске развития преэклампсии; при соотношении концентраций гипоксантин/ксантин более 0.9 - о риске развития преждевременных родов.
2. Способ по п. 1, отличающийся тем, что сыворотку крови предварительно разводят дистиллированной водой в 2 раза.
3. Способ по п. 1, отличающийся тем, что освобождение разведенной дистиллированной водой сыворотки крови от белков, маскирующих определение биомаркеров риска развития патологии беременности, осуществляют путем фильтрования через мембрану инертного фильтра с отсечкой по молекулярному весу разделяемых компонентов в 3 кДа и последующего центрифугирования в течение 30 мин при температуре 4°C со скоростью 10500 g.
4. Способ по п. 1, отличающийся тем, что в качестве ион-парного реагента используют тетрабутиламмоний сульфат.
5. Способ по п. 1, отличающийся тем, что регистрацию сигнала в ультрафиолетовой области спектра, соответствующего мочевой кислоте, ксантину, гипоксантину, осуществляют с помощью высокочувствительного диод-матричного детектора при длине волны 260 нм.
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕРАЗВИВАЮЩЕЙСЯ БЕРЕМЕННОСТИ | 2006 |
|
RU2313793C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УГРОЖАЮЩИХ ПРЕЖДЕВРЕМЕННЫХ РОДОВ У ЖЕНЩИН С УГРОЗОЙ НЕВЫНАШИВАНИЯ РАННИХ СРОКОВ | 2007 |
|
RU2344424C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПЕРИНАТАЛЬНОЙ ПАТОЛОГИИ У БЕРЕМЕННЫХ С ХРОНИЧЕСКИМИ ИНФЕКЦИОННО-ВОСПАЛИТЕЛЬНЫМИ ЗАБОЛЕВАНИЯМИ | 2003 |
|
RU2256914C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА БЕРЕМЕННОСТИ ПРИ УГРОЖАЮЩИХ ПРЕЖДЕВРЕМЕННЫХ РОДАХ | 2010 |
|
RU2437097C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ И ПРЕДРАСПОЛОЖЕННОСТИ К РАЗВИТИЮ ПАТОЛОГИИ, АССОЦИИРОВАННОЙ С ПРИСУТСТВИЕМ АУТОАНТИТЕЛ ПРОТИВ EPCR | 2005 |
|
RU2375716C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЭКЛАМПСИИ У БЕРЕМЕННЫХ | 2003 |
|
RU2243562C1 |
| Станок для фальцевания кровельных металлических листов | 1928 |
|
SU10322A1 |
Авторы
Даты
2016-06-10—Публикация
2012-06-09—Подача