Изобретение относится к катализаторам окисления сажи и способу его получения, так как выброс токсичных соединений их двигателей существенно угрожает экологии. Изобретение катализаторов относится к катализаторам окисления дизельных выбросов, в частности сажи.
Известен катализатор окисления и каталитически активное покрытие сажевого фильтра, содержат палладий и платину, причем соотношение между общим количеством палладия и общим количеством платины составляет от 8:1 до 1:15, при этом одновременно соотношение между количеством платины и количеством палладия в катализаторе окисления не превышает 6:1, а соотношение между количеством платины и количеством палладия в каталитически активном покрытии сажевого фильтра составляет не менее 10:1 [1].
Способ получения простой, так как включает смешивание компонентов в необходимом соотношении.
Недостатком данного катализатора являются, прежде всего, дорогостоящие компоненты, и в связи с тем, что с каждым днем увеличивается количество источников выброса веществ, засоряющих атмосферу и поверхность Земли, требуются активные катализаторы в большом количестве, стоимость таких катализаторов велика и применение их нерентабельно.
Известен катализатор окисления сажи, состав которого содержит металлический алюминий и оксидный композит, состоящий из оксида алюминия, оксидов переходных металлов и, дополнительно, оксидов редкоземельных элементов или их смеси и/или оксида фосфора и/или оксида кремния смесей оксидов переходных металлов. Катализатор также может содержать платиновые металлы или их смеси. Катализатор обладает термостойкостью [2].
Способ получения незначительно отличается от первого аналога.
Недостаток этого катализатора также состоит в том, что стоимость подобных катализаторов достаточно велика для широкого внедрения.
Известен катализатор, в состав которого входят алюминий и соль кобальта, предварительно прокаленные, после чего получается оксидный композит состава Al1,20-1,88Co0,05-0,05Oy в количестве 60,5-72,6 вес. %, металлический алюминий - остальное; либо катализаторы включают платиновый металл в количестве 0,05 вес. % без указания концентрации остальных компонентов катализатора [3].
Недостатком катализаторов на основе металлического алюминия является выплавление алюминия при температуре выше 660°C через трещины в оксидном керамическом слое, что приводит к разрушению и дезактивации катализаторов.
Известен катализатор и способ его получения, который включает введение неблагородного металла в виде гидроксида аммония или аммиачного комплекса, или в виде органического аминового комплекса, или в виде гидроксидного соединения в активный в окислительно-восстановительных реакциях кубический флюоритный CeZrOx материал при основных условиях. Катализатор окисления включает первичный каталитический активный металл из группы благородных металлов, нанесенный на носитель, а также вторичный каталитический активный компонент, который получен путем ионного обмена между поверхностью кубического флюоритного CeZrOx материала и раствором неблагородного металла и необязательно цеолита. Полученные катализаторы используют в каталитическом устройстве, располагая один из них на субстрате, вокруг которого расположен корпус [4].
Недостатком данного катализатора является многокомпонентность, использование благородных металлов и возможность потери дорогих составляющих.
Наиболее близким к заявляемому является катализатор молибдат меди CuMoO4 и способ получения медно-молибдатных катализаторов дожита сажи [5]. Способ получения катализатора дожига дизельной сажи включает смешивание экстракта меди в н-каприловой кислоте и экстракта молибдена в изоамиловом спирте в соотношении, обеспечивающем содержание металлов в получаемой смеси, соответствующее составу CuMoO4, последующее удаление растворителя из полученной смеси и ее пиролиз на воздухе, причем полученную смесь экстрактов доводят изоамиловым спиртом до суммарной концентрации металлов 1,5-2,0 мас. %, разбавленную смесь наносят на подложку из титана либо его сплава, обработанную путем плазменно-электролитического оксидирования в водном электролите, удаление растворителя осуществляют нагреванием титановой подложки с нанесенной смесью экстрактов до 150°C в течение не менее 1 часа, последующий пиролиз проводят при температуре 540-550°C в течение не менее 1 часа. Технический результат - упрощение способа получения катализатора на металлической подложке и повышение его производительности при одновременном повышении качества и эффективности получаемого катализатора.
Недостатком способа можно только считать многоступенчатость получения данного катализатора, экстрагирование меди и молибдена, применение изоамилового спирта, плазменно-электролитического оксидирования, что усложняет получить молибдат меди.
В состав заявляемых катализаторов входят висмут, магний, медь и кислород, а именно в состав катализаторов входят сложные оксидные системы на основе висмута, магния и меди, Bi12MgO19+MgO; Bi12MgO19+Cu4MgO5 и CuB2O4.
Образцы катализаторов получались в корундовом тигле с последующим полным растворением их в дистиллированной воде.
Раствор частично упаривался, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивалась температура до 973 К и масса отжигалась в течение 4 часов. Все перечисленные операции проводились в воздушной среде.
Для выяснения стабильности катализаторов Bi-Mg, Bi-Cu-Mg, Bi-Cu была проведена серия экспериментов. Эксперименты проводились в проточном кварцевом реакторе при температурах 713 К и 733 К в атмосфере воздуха. Объемный расход воздуха составлял 12 мл/мин.
Исходным объектом для исследований являлась дизельная сажа с удельной поверхностью 16 м2/г. В качестве катализаторов использовались сложные оксидные системы на основе висмута, магния, меди.
Образцы катализаторов получались путем смешивания определенных масс нитратов перечисленных элементов в корундовом тигле с последующим полным растворением их в дистиллированной воде. Раствор частично упаривался, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали в течение 4 часов. Все перечисленные операции проводили в воздушной среде.
Пример 1. Нитраты магния и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов, затем увеличивалась температура до 973 К и каталитическая смесь отжигалась в течение 4 часов. Все перечисленные операции проводились в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза являются тетрагональный висмутит магния B12MgO19 и кубический оксид магния MgO.
Пример 2. Нитраты меди, висмута и магния массами 0,2 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого остаток раствора упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были висмутит меди тетрагональный Bi12MgO19 и кубический купрат меди CuMgO5.
Пример 3. Нитраты меди и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктом синтеза был тетрагональный висмутит меди CuBi2O4.
Пример 4. Нитраты магния и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были тетрагональный висмутит магния Bi12MgO19 и кубический оксид магния MgO.
Пример 5. Нитраты меди, висмута и магния массами 0,2 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого остаток раствора упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были висмутит меди тетрагональный Bi12MgO19 и кубический купрат меди Cu4MgO5.
Пример 6. Нитраты меди и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктом синтеза был тетрагональный висмутит меди CuBi2O4.
Пример 7. Нитраты магния и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были тетрагональный висмутит магния Bi12MgO19 и кубический оксид магния MgO.
Пример 8. Нитраты меди, висмута и магния массами 0,2 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого остаток раствора упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были висмутит меди тетрагональный Bi12MgO19 и кубический купрат меди Cu4MgO5.
Пример 9. Нитраты меди и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктом синтеза был тетрагональный висмутит меди CuBi2O4.
Пример 10. Нитраты магния и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были тетрагональный висмутит магния Bi12MgO19 и кубический оксид магния MgO.
Пример 11. Нитраты меди, висмута и магния массами 0,2 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого остаток раствора упаривался. частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктами синтеза были висмутит меди тетрагональный Bi12MgO19 и кубический купрат меди Cu4MgO5.
Пример 12. Нитраты меди и висмута массами 0,3 г смешивались в корундовом тигле с полным растворением их в дистиллированной воде. После этого раствор упаривался частично, помещался в муфельную печь и прокаливался при 573 К в течение 3 часов. Затем увеличивали температуру до 973 К и отжигали состав в течение 4 часов. Все перечисленные операции проводили в воздушной среде. Согласно рентгенофазовому анализу продуктом синтеза был тетрагональный висмутит меди CuBi2O4.
Исходным объектом для исследований являлась дизельная сажа с удельной поверхностью 16 м2/г. В качестве катализаторов, увеличивающих адсорбцию кислорода на поверхности сажи, использовали сложные оксидные системы на основе висмута, магния и меди, взятых в соотношении: сажа: катализатор = 1:1.
Следует отметить, что многие каталитические системы проявляют высокую каталитическую активность в окислении сажи только в случае плотного контакта с ней. Действительно, изученные системы проявляют каталитическую активность даже при неплотном контакте с сажей, что проявляется в снижении температуры начала окисления сажи и увеличении удельной скорости окисления по сравнению с некаталитическим процессом.
В то же время при плотном контакте каталитическая активность всех систем значительно выше. Система Bi-Cu оказалась наименее активна в адсорбции кислорода на саже. Для систем Bi-Cu-Mg окисление проводилось в температурном интервале от 293 К до 873 К в соотношении сажа: катализатор 2:1. Для системы Bi-Mg при 733 К скорость окисления при плотном контакте почти в 6 раз выше, чем при неплотном, а для системы Bi-Cu-Mg при 733 К - в 4 раза выше. Учитывая такую зависимость каталитической активности от типа контакта, исследования проводились в условиях плотного контакта. Следует также отметить значительное увеличение активности для обеих систем и для обоих типов контакта катализатора с сажей.
Все катализаторы исследовали в окислении сажи.
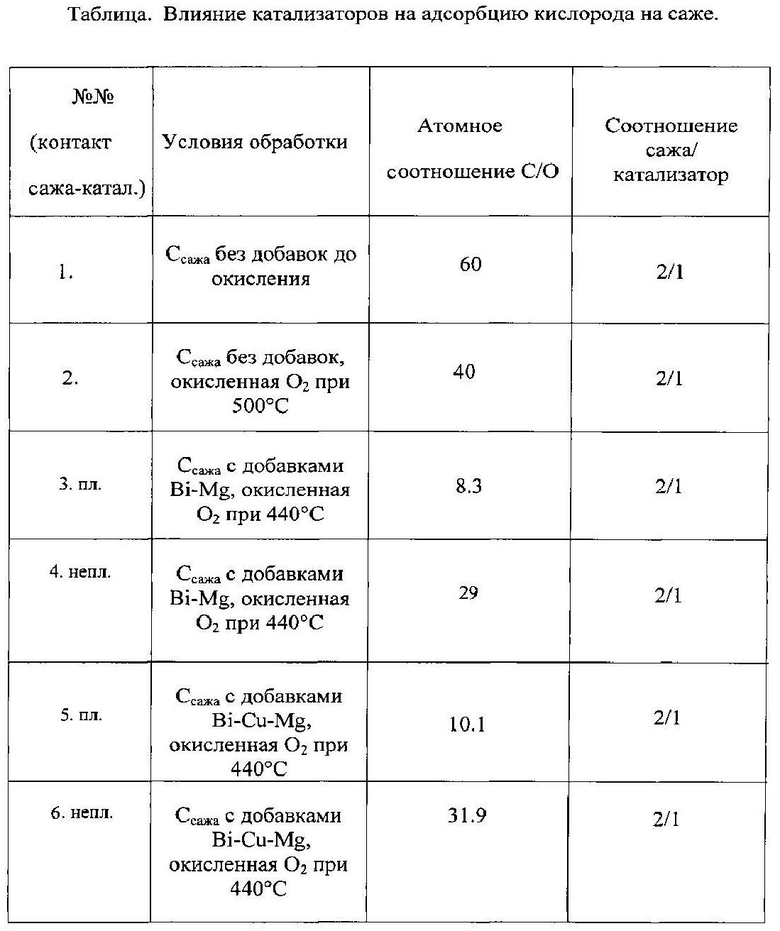
Рентгеновская фотоэлектронная спектроскопия (РФЭС) и смесей сажа-катализатор исследований поверхности образцов дизельной сажи (без добавок) и сажи с добавками, содержащими соединения Bi, Cu, Mg до и после окисления кислородом показала, что если до окисления с катализаторами, соотношение кислорода к углероду О/С (показатель адсорбции кислорода на саже) составляет двухзначное число, то после добавления катализатора к саже значение этого числа менее 10 (Таблица).
Исследования показали, что использование представленных катализаторов более эффективны по сравнению с применяемыми катализаторами на основе как благородных металлов, так и других катализаторов, включая прототип, кроме того, получение представленных катализаторов не представляет особых трудностей.
Использование в составе катализаторов окисления сажи соединений металлов: меди, висмута и магния при плотном контакте сажа-катализатор значительно увеличивают удаление сажи, очищая окружающую среду.
Источники информации
1. Патент RU №2479341, B01D 53/94, B01J 23/38, B01J 23/42, B01J 23/44, F01N 3/10, 2008.
2. Патент RU №2103057, B01J 27/185, B01J 27/182, B01J 23/70, B01J 23/10, B01J 21/04, B01J 21/02, B01J 103/54, B01D 53/72, B01D 53/72, B01D 53/48, 1998.
3. Авт. Св. СССР N 923588, В01J 37/02, Б.И. N 16, 1982.
4. Патент RU №2506996, B01J 23/00, 21/00, B01J 23/10, B01J 23/54, B01J 21/04, B01J 37/00, B01D 53/94, C01F 17/00.
5. RU 2455069, C1 B01J 37/025, C1 B01J 37/03, 2012.
6. Лебухова Н.В., Карпович Н.Ф., Макаревич К.С., Чигрин П.Г. «Каталитическое горение сажи в присутствии медно-молибдатных систем, полученных разными методами». Катализ в промышленности, 2008, №6, с. 35-40.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОРЫ ОКИСЛЕНИЯ САЖИ | 2017 |
|
RU2682248C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВИСМУТ-НАТРИЙ-КАЛЬЦИЙ ОКСОАПАТИТА | 2023 |
|
RU2829972C1 |
| КАТАЛИЗАТОР ДЛЯ ПАРОВОЙ КОНВЕРСИИ УГЛЕВОДОРОДОВ | 2017 |
|
RU2650495C1 |
| Способ получения ванадата металла | 2022 |
|
RU2794821C1 |
| КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ САЖИ | 2023 |
|
RU2832847C1 |
| Способ получения гетероструктуры, стекло, обогащенное Si/δ* - BiO/стекло, обогащенное Bi, в системе BiO - SiO | 2018 |
|
RU2693062C1 |
| Способ получения цирконата празеодима формулы PrZrO | 2021 |
|
RU2792641C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕГУЛИРУЕМОЙ ГЕТЕРОСТРУКТУРЫ СТЕКЛО/δ*-ВiO+BiSiO В СИСТЕМЕ BiO-SiO(Варианты) | 2018 |
|
RU2691334C1 |
| Ниобий-замещенный молибдат натрия-циркония и способ его получения | 2023 |
|
RU2814778C1 |
| Способ получения биосовместимых висмут-апатитов | 2021 |
|
RU2776293C1 |
Изобретение относится к катализаторам окисления сажи, включающим металлы и кислород. При этом в качестве металлов используются висмут, медь и магний, образующие висмутит меди CuBi2O4, купрат магния MgCu4O5, висмутит магния Bi12MgO19 и оксид магния MgO. Также изобретение относится к способу получения заявленных катализаторов, который заключается в том, что определенные массы нитратов перечисленных элементов смешивают в корундовом тигле с последующим полным растворением их в дистиллированной воде, раствор частично упаривают, помещают в муфельную печь и прокаливают при 300°C в течение 3 часов; затем увеличивают температуру до 700°C и отжигают в течение 4 часов, все перечисленные операции проводят в воздушной среде. Технический результат заключается в снижении выбросов токсичных соединений из двигателей. 2 н. и 1 з.п. ф-лы, 1 табл., 12 пр.
1. Катализаторы окисления сажи, включающие металлы и кислород, отличающиеся тем, что в качестве металлов используются металлы: висмут, медь и магний, образующих висмутит меди CuBi2O4, купрат магния MgCu4O5, висмутит магния Bi12MgO19 и оксид магния MgO.
2. Катализаторы по п. 1, отдичающиеся тем, что катализаторы имеют следующий состав: Bi12MgO19+MgO, Bi12MgO19+Cu4MgO5, CuBi2O4.
3. Способ получения катализаторов для окисления сажи, отличающийся тем, что определенные массы нитратов перечисленных элементов смешивали в корундовом тигле с последующим полным растворением их в дистиллированной воде, раствор частично упаривали, помещали в муфельную печь и прокаливали при 300°C в течение 3 часов; затем увеличивали температуру до 700°C и отжигали в течение 4 часов. Все перечисленные операции проводили в воздушной среде.
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДОЖИГА ДИЗЕЛЬНОЙ САЖИ | 2011 |
|
RU2455069C1 |
| ЗАБУГА В.Я | |||
| И ДР., ОКИСЛЕНИЕ САЖИ В ПРИСУТСТВИИ ОКСИДНОГО Cu-Co-Fe КАТАЛИЗАТОРА, Сверхтвердые материалы, 2009, 6, стр.9-14 | |||
| КАТАЛИЗАТОРЫ ОКИСЛЕНИЯ ДЛЯ ДИЗЕЛЬНЫХ ДВИГАТЕЛЕЙ НА ОСНОВЕ НЕБЛАГОРОДНЫХ МЕТАЛЛОВ И МОДИФИЦИРОВАННЫЕ НЕБЛАГОРОДНЫМИ МЕТАЛЛАМИ | 2009 |
|
RU2506996C2 |
| СПОСОБ ПРОИЗВОДСТВА ХЛЕБНОГО КВАСА | 2015 |
|
RU2590730C1 |
Авторы
Даты
2016-07-27—Публикация
2014-11-20—Подача