ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к области медицины, а именно к фармакологии и токсикологии, и может быть использовано для определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида в различных биологических средах, в том числе в плазме крови млекопитающих.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Производное 4-аминопиридина - 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорид является действующим веществом разрабатываемого лекарственного средства для коррекции когнитивных функций при сосудистых заболеваниях головного мозга.
Одной из актуальных задач при создании нового лекарственного средства является проведение исследований фармакокинетики с целью оценки всасывания, распределения, метаболизма и экскреции. Для проведения исследований фармакокинетики требуется разработать биоаналитическую методику количественного определения действующего вещества в биологических средах, в частности в плазме крови. Для количественного определения действующего вещества в плазме крови могут быть использованы различные методы - физико-химические, иммунологические, микробиологические и другие методы, обладающие специфичностью, высокой чувствительностью, точностью и воспроизводимостью.
Одним из самых распространенных для изучения фармакокинетики лекарственного средства является метод высокоэффективной жидкостной хроматографии (ВЭЖХ), который обладает рядом преимуществ по сравнению с другими методами, а именно: высокой чувствительностью, которая позволяет определять микроколичества вещества и высокой скоростью анализа.
Высокая чувствительность методики - ключевой критерий для разработки способа количественного определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида, поскольку его эффективная доза лежит в диапазоне 0,1-10 мг/кг в зависимости от способа введения, а при использовании таких низких доз концентрации действующего вещества в биологических средах, как правило, находятся в диапазоне очень низких концентраций от 10 до 1000 нг/мл.
В настоящее время не существует способов количественного определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида в биологических средах. Для поиска возможных прототипов проведен анализ сведений о методах определения 4-аминопиридина и его производных. Описаны методы определения 4-аминопиридина.
Известен способ определения 4-аминопиридина и его метаболитов в биологических средах организма (плазме крови и моче) с использованием радиоактивной метки 14С и высокоэффективной жидкостной хроматографии (ВЭЖХ) (заявка на патент US 2017035742, МПК А61К 31/4409 (2013.01), опуб. 09.02.2017; Caggiano А. и соавт., 2013). Однако для определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида данный способ не применим вследствие значительных отличий в химической структуре и сложности введения радиоактивной метки 14С в структуру молекулы.
В качестве прототипа использован ранее описанный оптимизированный способ определения 4-аминопиридина в плазме крови и моче с использованием метода ВЭЖХ (Gupta R.N., Hansebout R.R., 1996), который включает экстракцию определяемого вещества смесью 35% хлорной кислоты и метанола (1:100) с последующим определением его методом ВЭЖХ с использованием в качестве подвижной фазы смеси октансульфоновой кислоты в 10 мМ растворе натрия фосфорнокислого однозамещенного (рН=4,2) с ацетонитрилом. Однако для определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида данный способ не применим вследствие значительных отличий его химической структуры и физико-химических свойств от прототипа.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Предлагаемое изобретение решает задачу разработки нового высокоэффективного способа количественного определения лекарственного средства для коррекции когнитивных функций при сосудистых заболеваниях головного мозга в биологических средах - 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Поставленная задача решается способом количественного определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида в биологических средах, включающем экстракцию определяемого вещества ацетонитрилом при кислом значении рН среды с добавлением натрия хлорида, с последующим определением его методом высокоэффективной жидкостной хроматографии с градиентным режимом элюирования с использованием в качестве подвижной фазы смеси 0,5% раствора, содержащего калий фосфорнокислый однозамещенный (рН=4,0), и метанола при градиенте концентрации последнего от 5 до 75%.
Наиболее оптимальными, но не необходимыми режимами высокоэффективной жидкостной хроматографии при этом являются:
скорость подачи потока элюента - 0,1 мл/мин;
объем вводимой пробы - 20 мкл;
детектор - спектрофотометрический, 280 нм;
время анализа - 20 мин;
температура термостата колонки - 35°С.
Отсутствие источников информации, содержащих ту же совокупность признаков, что и в разработанном способе, сообщает ему соответствие критерию «новизна».
Та же совокупность признаков позволяет получить новый непредсказуемый эффект - разработка высокоэффективного способа количественного определения в биологических средах нового лекарственного средства - 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида (далее субстанция NL) и, таким образом, сообщает ему соответствие критерию «изобретательский уровень».
Проведение количественного определения нового лекарственного средства с использованием известного оборудования с помощью известных препаратов сообщает разработанному способу соответствие критерию «промышленная применимость».
Таким образом, разработанный способ соответствует всем 3 критериям охраноспособности изобретения и может быть квалифицирован как изобретение.
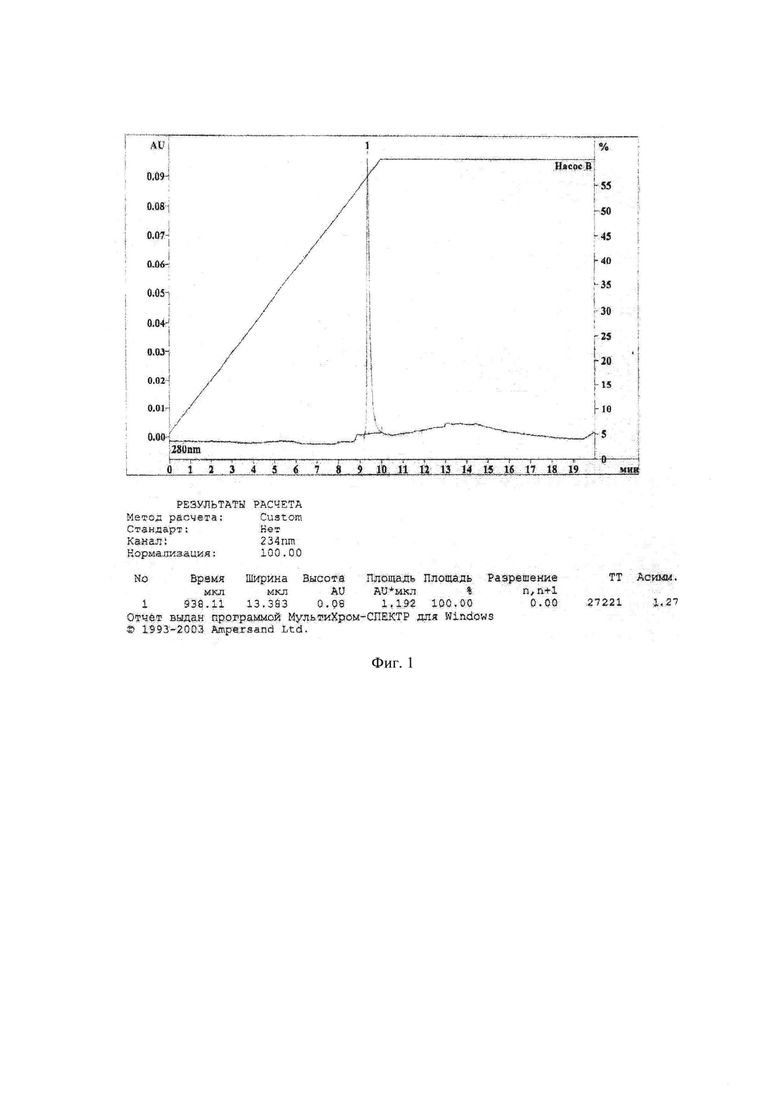
На Фиг. 1 представлена хроматограмма раствора субстанции NL с концентрацией 1000 нг/мл.
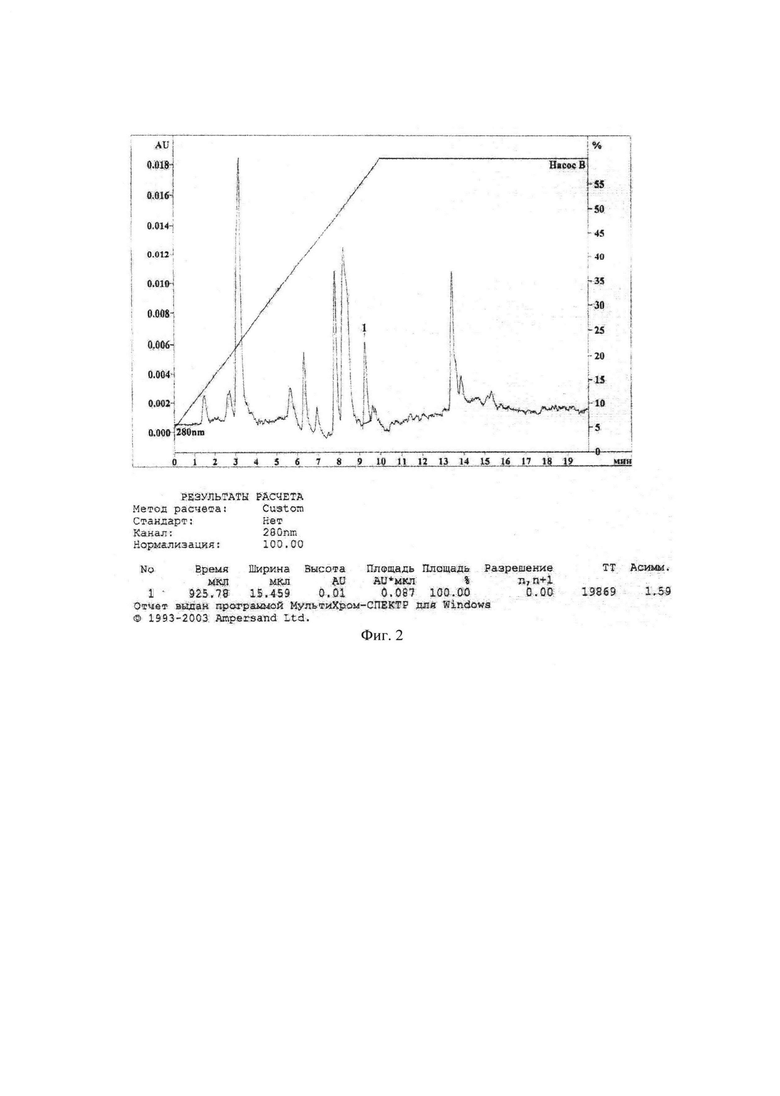
На Фиг. 2 представлена хроматограмма NL в плазме крови с концентрацией 1000 нг/мл при экстракции ацетонитрилом в нейтральной среде.
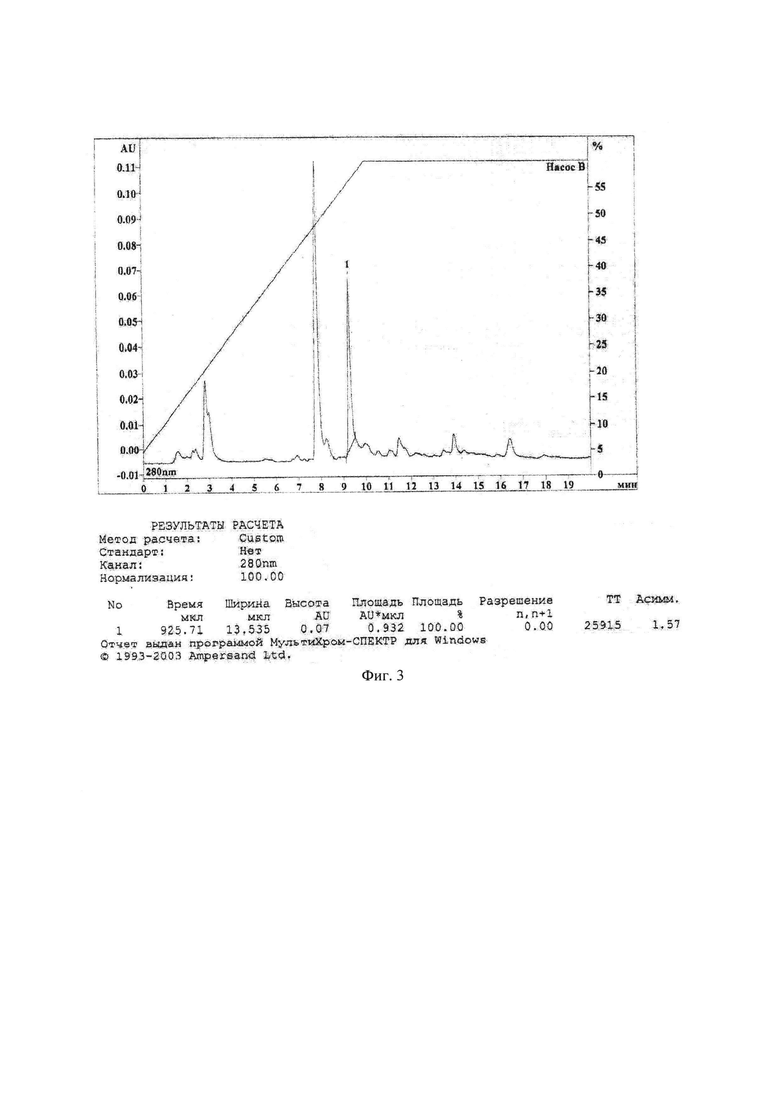
На Фиг. 3 представлена хроматограмма NL в плазме крови с концентрацией 1000 нг/мл при экстракции ацетонитрилом в кислой среде.
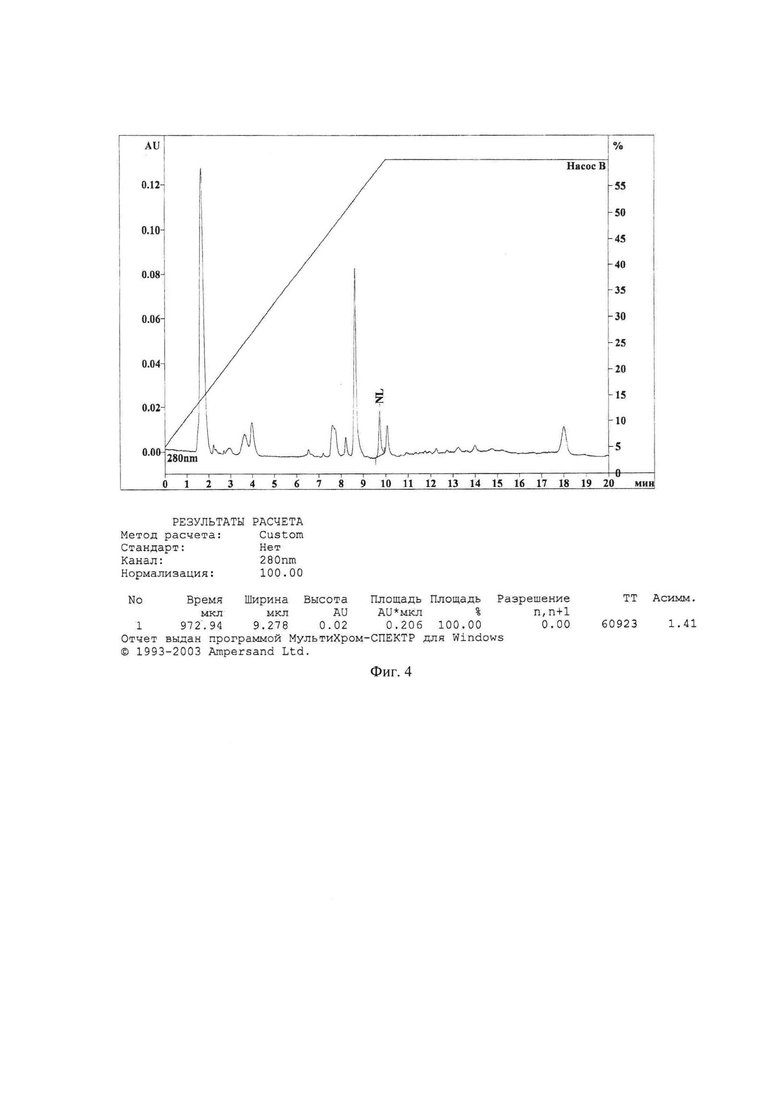
На Фиг. 4 представлена хроматограмма образца плазмы крови крысы, время забора крови 30 мин.
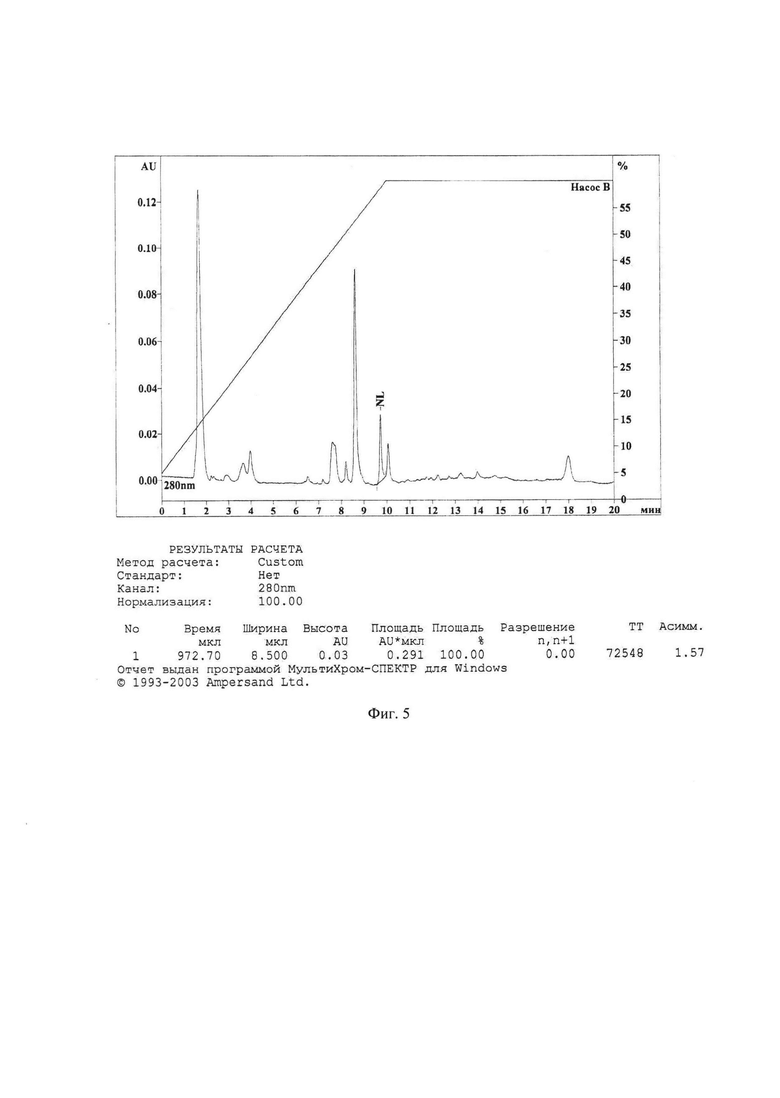
На Фиг. 5 представлена хроматограмма образца плазмы крови крысы, время забора крови 60 мин.
Пример 1. Подбор условий пробоподготовки
В качестве биологической среды использовали плазму крови крыс.В качестве метода извлечения NL из биологической матрицы использовали жидкостно-жидкостную экстракцию ацетонитрилом. Важнейшим и подлежащим оптимизации показателем при экстракции является степень извлечения. На степень извлечения может оказывать влияние множество внешних факторов: рН среды, температура, скорость, время перемешивания и т.д. Оптимизировали процедуру пробоподготовки по значению рН среды и времени перемешивания. При этом скорость перемешивания выбрана максимальной - 4000 об/мин, температура - комнатной. Определение степени извлечения при различных варьируемых внешних значениях осуществляли путем сравнения значений площадей пиков в растворе субстанции NL и в плазме крови аналогичных концентраций. Кислое значение рН среды создавали добавлением к плазме крови 20% раствора ортофосфорной кислоты, щелочное - 0,1 М раствора натрия гидроксида. Полученные хроматограммы представлены на фиг. 1-3, результаты подбора условий пробоподготовки представлены в таблице 1.
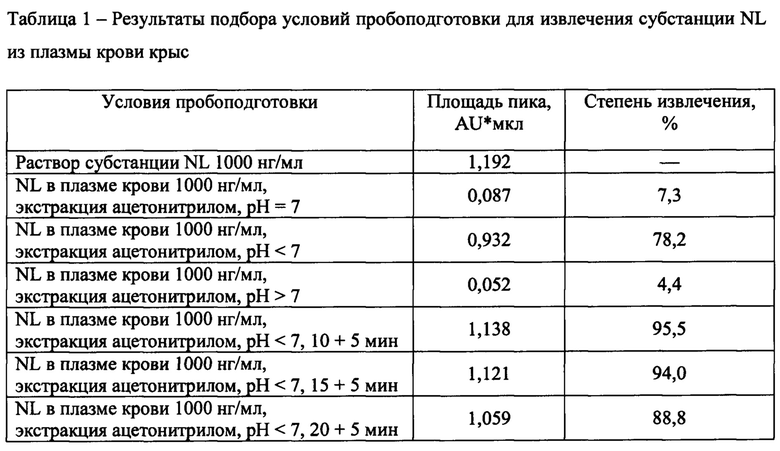
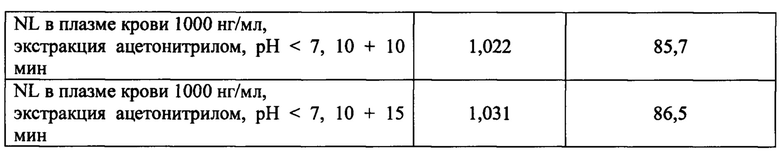
Из таблицы 1 видно, что наибольшая степень извлечения NL из плазмы крови крыс наблюдается при жидкостно-жидкостной экстракции ацетонитрилом при кислом значении рН среды. Также видно, что наибольшая степень извлечения наблюдается при времени перемешивания, равном 10 мин при экстракции и 5 мин при добавлении неорганической соли. Степень извлечения NL из плазмы крови животного составляет около 96%.
Для подтверждения возможности применения разработанных условий для определения NL в другой биологической среде (плазма крови кроликов) проводили исследование степени извлечения из данной матрицы методом жидкостно-жидкостной экстракции ацетонитрилом при кислом значении рН среды и времени перемешивания в течение 10 и 5 мин. Результаты исследования представлены в таблице 2.

Из таблицы 2 видно, что степень извлечения NL из плазмы крови кроликов составляет 96,4% и находится на одном уровне со степенью извлечения NL из плазмы крови крыс.Следовательно, в качестве биологической матрицы при определении NL в плазме крови животного можно использовать плазму крови как крыс, так и кроликов, ввиду одинаковой степени извлечения аналита.
Пример 2. Количественное определение субстанции NL в плазме крови.
Приготовление подвижной фазы А (ПФ А). 2,5 г калия фосфорнокислого однозамещенного помещают в мерную колбу вместимостью 500 мл, прибавляют 300 мл воды очищенной, перемешивают до полного растворения, прибавляют воду очищенную до метки и перемешивают. Доводят рН полученного раствора до 4,0 ортофосфорной кислотой.
Приготовление раствора субстанции NL с концентрацией 1 мг/мл
Около 0,01 г (точная навеска) субстанции NL помещают в мерную колбу вместимостью 10 мл, растворяют в 5 мл подвижной фазы А (ПФ А), доводят объем раствора тем же растворителем до метки и перемешивают.
Раствор хранят не более 3 суток при температуре 2-8°С.
Приготовление раствора субстанции NL с концентрацией 0,01 мг/мл
1 мл раствора субстанции NL с концентрацией 1 мг/мл помещают в мерную колбу вместимостью 10 мл, доводят объем раствора ПФ А до метки и перемешивают.1 мл полученного раствора помещают в мерную колбу вместимостью 10 мл, доводят объем раствора ПФ А до метки и перемешивают. Раствор используют свежеприготовленным.
Приготовление градуировочных растворов субстанции NL
Из раствора субстанции NL с концентрацией 0,01 мг/мл методом параллельно-последовательного разбавления готовят растворы субстанции NL с концентрациями: 20, 10, 7, 5, 2, 1, 0,5, 0,25 мкг/мл. Растворы используют свежеприготовленными.
Приготовление градуировочных образцов NL в плазме крови животных
В пластиковую центрифужную микропробирку типа «Эппендорф» вместимостью 2 мл помещают 450 мкл холостой плазмы крови крыс, не содержащей NL, прибавляют 50 мкл исходного калибровочного раствора субстанции соответствующей концентрации и перемешивают. Затем прибавляют 1 мл ацетонитрила и тщательно перемешивают на встряхивателе при 4000 об/мин в течение 10 мин. К полученной смеси прибавляют 0,1-0,2 г натрия хлорида и тщательно перемешивают на встряхивателе при 4000 об/мин в течение 5 мин. Полученный раствор центрифугируют при 13000 об/мин в течение 10 мин. Водную фазу отбрасывают, а органическую упаривают под вакуумом до сухого остатка при температуре 45°С в течение 90-100 мин. К сухому остатку прибавляют 500 мкл подвижной фазы А (ПФ А), перемешивают на встряхивателе в течение 5 мин и центрифугируют. Надосадочную жидкость используют для анализа.
Подготовка пробы
В пластиковую центрифужную микропробирку типа «Эппендорф» вместимостью 2 мл помещают 500 мкл плазмы крови крыс, содержащей NL, прибавляют 1 мл ацетонитрила и тщательно перемешивают на встряхивателе при 4000 об/мин в течение 10 мин. К полученной смеси прибавляют 0,1-0,2 г натрия хлорида и тщательно перемешивают на встряхивателе при 4000 об/мин в течение 5 мин. Полученный раствор центрифугируют при 13000 об/мин в течение 10 мин. Водную фазу отбрасывают, а органическую упаривают под вакуумом до сухого остатка при температуре 45°С в течение 90-100 мин. К сухому остатку прибавляют 500 мкл подвижной фазы А (ПФ А), перемешивают на встряхивателе в течение 5 мин и центрифугируют. Надосадочную жидкость используют для анализа.
Проверка пригодности хроматографической системы
Готовят модельный раствор NL в плазме крови животного с концентрацией 1000 нг/мл.
Время удерживания NL должно составлять около 9,6 мин, относительное стандартное отклонение времени удерживания не должно превышать 10%, соотношение сигнал/шум должно быть не менее 160/1, среднее квадратическое отклонение выходного сигнала не должно превышать 5%.

Анализируют раствор для проверки пригодности хроматографической системы. Далее анализируют градуировочные растворы. По результатам анализа градуировочных растворов строят градуировочный график зависимости площади пика анализируемого вещества от его концентрации в плазме крови животных. Концентрацию NL в исследуемых образцах определяют по градуировочному графику.
Хроматограммы, полученные при анализе образцов плазмы крови крыс после внутрижелудочного введения субстанции NL представлены на фиг. 4 и фиг. 5.
Как видно из приведенных примеров, предлагаемое изобретение позволяет получить необходимую и достоверную информацию о способе количественного определения субстанции 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида в биологических средах.
ИСТОЧНИКИ ИНФОРМАЦИИ
1 Caggiano A., Blight А., Рапу T.J. (2013) Identification of metabolites of dalfampridine (4-aminopyridine) in dog and rat. Journal of Drug Assessment, 2:1, 72-80, DOI: 10.3109/21556660.2013.794143.
2 Заявка на патент US 2017035742.
3 Gupta R.N., Hansebout R.R. Optimization of the determination of 4-aminopyridine in human serum and urine by column liquid chromatography. Journal of Chromatography B, 677 (1996) 183-189.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения 2,2,6,6-тетраметил-N-{ 1-[5-(4-метил-3-хлоранилино)-1,2,4-тиадиазол-3-ил]пропан-2-ил} пиперидин-4-амина дигидрохлорида в биологических средах | 2016 |
|
RU2636231C1 |
| 3,4-ДИГИДРО-2,7-НАФТИРИДИН-1,6(2H,7H)-ДИОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ MEK | 2022 |
|
RU2826000C1 |
| ЗАМЕЩЕННЫЕ 4-АРИЛ-1,4-ДИГИДРО-1,6-НАФТИРИДИНАМИДЫ И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2470932C9 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ N-[3-(4-НИТРОФЕНИЛАМИНО)-ИНДОЛ-2-ИЛМЕТИЛЕН]АМИНОГУАНИДИНА МЕТАНСУЛЬФОНАТА В ПЛАЗМЕ КРОВИ | 2018 |
|
RU2699550C1 |
| ПРОИЗВОДНОЕ ДИГИДРОИНДОЛИЗИНОНА | 2015 |
|
RU2707887C2 |
| НОВЫЕ АНТАГОНИСТЫ РЕЦЕПТОРОВ ДВОЙНОГО ДЕЙСТВИЯ (DARA) В ОТНОШЕНИИ РЕЦЕПТОРОВ AT1 И ETA | 2007 |
|
RU2425833C2 |
| ЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ 11БЕТА-ГИДРОКСИСТЕРОИД-ДЕГИДРОГЕНАЗЫ 1 | 2009 |
|
RU2531272C2 |
| ЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ 11БЕТА-ГИДРОКСИСТЕРОИД-ДЕГИДРОГЕНАЗЫ 1 | 2009 |
|
RU2539979C2 |
| ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ИНГИБИТОР JAK | 2015 |
|
RU2674262C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 8-(ТРИФТОРМЕТИЛ)БЕНЗО[F][1,2,3,4,5]ПЕНТАТИЕПИН-6-АМИНА ГИДРОХЛОРИДА В БИОЛОГИЧЕСКИХ СРЕДАХ | 2018 |
|
RU2676487C1 |
Изобретение относится к области медицины, а именно к фармакологии и токсикологии, может быть использовано для количественного определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида в биологических средах. Способ включает экстракцию определяемого вещества ацетонитрилом при кислом значении рН среды с добавлением натрия хлорида с последующим определением его методом высокоэффективной жидкостной хроматографии с градиентным режимом элюирования с использованием в качестве подвижной фазы смеси 0,5% раствора калия фосфорнокислого однозамещенного, подкисленного до рН 4,0 ортофосфорной кислотой, и метанола при градиенте концентрации последнего от 5 до 75%. 2 пр., 5 ил., 2 табл.
Способ количественного определения 4-амино-1-(3-нитро-2-оксо-1-фенил-1,2-дигидро-1,6-нафтиридин-5-ил)пиридиний хлорида в биологических средах, включающий экстракцию определяемого вещества ацетонитрилом при кислом значении рН среды с добавлением натрия хлорида с последующим определением его методом высокоэффективной жидкостной хроматографии с градиентным режимом элюирования с использованием в качестве подвижной фазы смеси 0,5% раствора калия фосфорнокислого однозамещенного, подкисленного до рН 4,0 ортофосфорной кислотой, и метанола при градиенте концентрации последнего от 5 до 75%.
| US 2017035742 A1, 09.02.2017 | |||
| Способ определения лекарственных препаратов-производных пиридина | 1979 |
|
SU941890A1 |
| КУЗНЕЦОВА А.В | |||
| Фармакопейный анализ производных фурана, пиррола, пиразола, имидазола, пиридина, хинолина // Учебное пособие для студентов IV курса специальности "Фармация", Пемза, 2013, ;[он-лайн], [найдено 24.10.2018] | |||
| Найдено из Интернет: URL: https://dep_oikf.pnzgu.ru/files/dep_oikf.pnzgu.ru/furany_posobie.pdf | |||
| GUPTA R.N | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2019-04-24—Публикация
2018-06-27—Подача