Область техники, к которой относится изобретение
[1] Настоящее изобретение относится к композиции для получения тагатозы и способу получения тагатозы из фруктозы, а более конкретно, к гену, кодирующему термофильную фруктозо-4-эпимеразу, полученному из термофильных микроорганизмов, и способу получения тагатозы из фруктозы с использованием указанного фермента.
Уровень техники
[2] Тагатоза представляет собой эпимер D-фруктозы и имеет естественный сладкий вкус почти не отличимый от сахарозы и физические свойства, подобные сахарозе. Тагатоза является натуральным подсластителем, который присутствует в небольшом количестве в таких пищевых продуктах, как молоко, сыр, какао и тому подобное, и в сладких фруктах, таких как яблоки и мандарины. Калорийность тагатоза - 1,5 ккал/г, что составляет одну треть от калорийности сахарозы, а гликемический индекс (ГИ) равен 3, что составляет 5% от ГИ сахарозы. Тагатоза имеет сладкий вкус, подобный сахарозе, и обеспечивает различные преимущества для здоровья. В этой связи, тагатоза может быть использована в самых разнообразных продуктах в качестве альтернативного подсластителя, удовлетворяющего вкусовым требованиям, полезного с точки зрения здоровья.
[3] Известно, что тагатоза может быть получена из галактозы химическим способом (каталитическая реакция) или биологическим способом (ферментативная реакция изомеризации) (выложенная публикация патента Кореи № 2009-0082774, опубликованная 31 июля 2009г.). Для обеспечения экономически целесообразного производства галактозы в качестве исходного материала для вышеуказанных реакций, были проведены исследования по разработке различных сырьевых материалов, содержащих галактозу, способа получения галактозы и способа получения тагатозы с использованием указанных сырьевых материалов. В качестве наиболее репрезентативного сырья для галактозы была использована лактоза. Однако цена лактозы или содержащих лактозу продуктов является нестабильной и зависит от объема выработки, спроса и предложения сырого молока и лактозы на мировом рынке и тому подобного. Такие колебания цен нарушают стабильные поставки сырья для получения тагатозы.
[4] В частности, примерно в 2012 году, резкий рост мировых цен на лактозу был в основном обусловлен быстрым ростом спроса на сухое обезжиренное молоко и сухое цельное молоко, содержащее лактозу, из-за быстрого экономического роста в Китае и снижения годового объема производства молока в странах-производителях молока, вызванного глобальным потеплением. Такие колебания цен на сырье препятствуют стабильному производству тагатозы. Соответственно, существует необходимость в создании нового способа получения тагатозы с использованием общих сахаридов (сахарозы, глюкозы, фруктозы и им подобных).
Описание
Техническая проблема
[5] В прошлом, тагатозу получали с использованием галактозы, получаемой при разложении различных биологических ресурсов, таких как сывороточный пермеат, который является растворимым побочным продуктом в качестве пищевого сырья, кроме лактозы, и древесина лиственницы, которая является растительной биомассой.
[6] Однако подходящее сырье, которое является коммерчески доступным или коммерциализация которого целесообразна с точки зрения наличия стабильных поставок сырья и эффективности инвестиций, отсутствует.
[7] Таким образом, одна из задач настоящего изобретения состоит в создании композиции для получения тагатозы из общих сахаридов, более подходящих для применения в промышленности по сравнению с предыдущими способами получения тагатозы из галактозы, а также к способу получения тагатозы.
[8] В частности, настоящее изобретение направлено на создание нового белка-фермента, функция которого не известна из уровня техники, и который имеет D-фруктозо-4-эпимеразную активность и обеспечивает возможность получения тагатозы из фруктозы с высоким выходом, гена, кодирующего указанный белок, композиции для получения тагатозы с использованием указанного белка, и к способ получения тагатозы из фруктозы.
Техническое решение
[9] В одном из вариантов осуществления настоящее изобретение относится к композиции для получения тагатозы из фруктозы, содержащей: белок, имеющий аминокислотную последовательность приведенную в SEQ ID NO:1 - SEQ ID NO:7, или микроорганизм, экспрессирующий указанный белок.
[10] Другой вариант осуществления настоящего изобретения относится к способу получения тагатозы из фруктозы, включающий: взаимодействие композиции по настоящему изобретению с фруктозой.
Благоприятные эффекты
[11] Настоящее изобретение может обеспечить способ получения тагатозы, который является экономичным и обеспечивает высокий выход, с использованием широко распространенного сырьевого материала, фруктозы, путем разработки новой D-фруктозо-4-эпимеразы, которая обладает активностью, обеспечивающей возможность получения тагатозы путем эпимеризации фруктозы по атому углерода 4.
[12] Кроме того, настоящее изобретение может обеспечить способ получения тагатозы, который является экономичным и обеспечивает высокий выход, с использованием широко распространенного сырьевого материала, фруктозы, вместо лактозы цена на которую колеблется в достаточно широком диапазоне, тем самым снижая затраты на производство.
[13] В общем случае, поскольку в данной области техники хорошо известно, что фруктозу можно получать в промышленных масштабах из глюкозы или сахарозы, сырьевые материалы, предлагаемые в настоящем изобретении, включают не только фруктозу, но и сырьевые материалы полностью или частично состоящие из фруктозы, что позволяет обеспечить более экономичное производство. А именно, настоящее изобретение охватывает получение тагатозы через ферментативную конверсию крахмала, сахара-сырца или сахарозы.
[14] Кроме того, настоящее изобретение позволяет получать тагатозу из фруктозы, что обеспечивает эффективное массовое производство тагатозы, которая рассматривается в настоящее время в качестве важного пищевого материала.
Описание чертежей
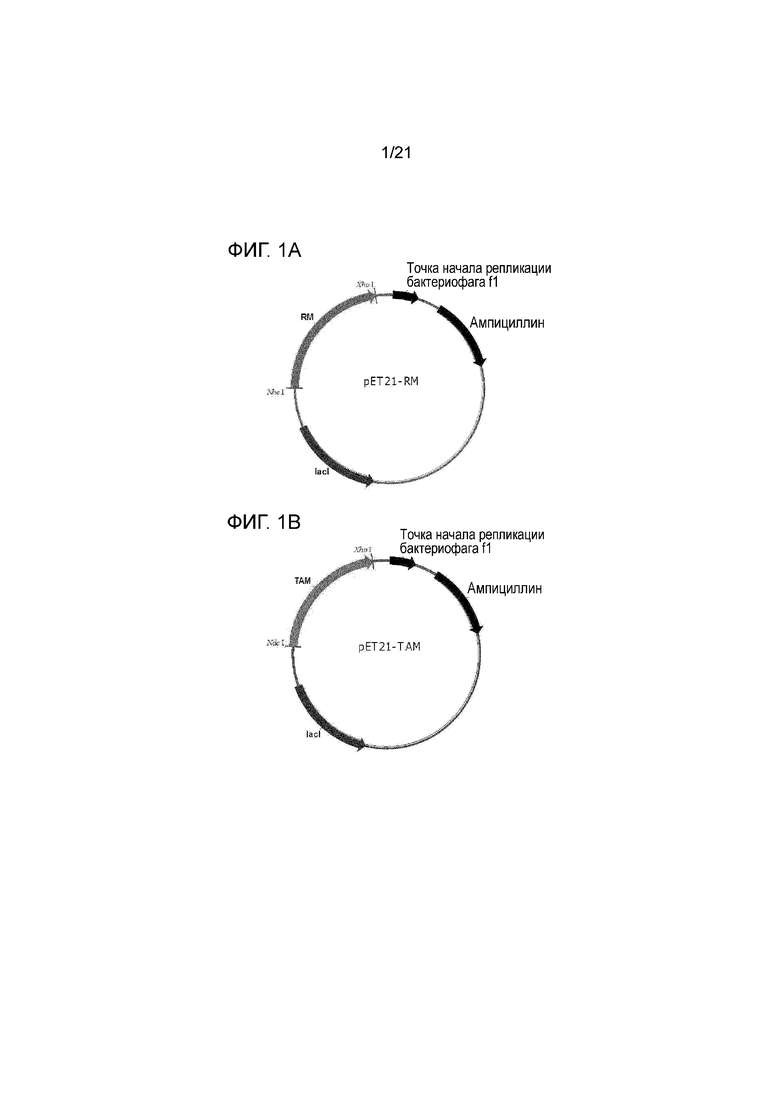
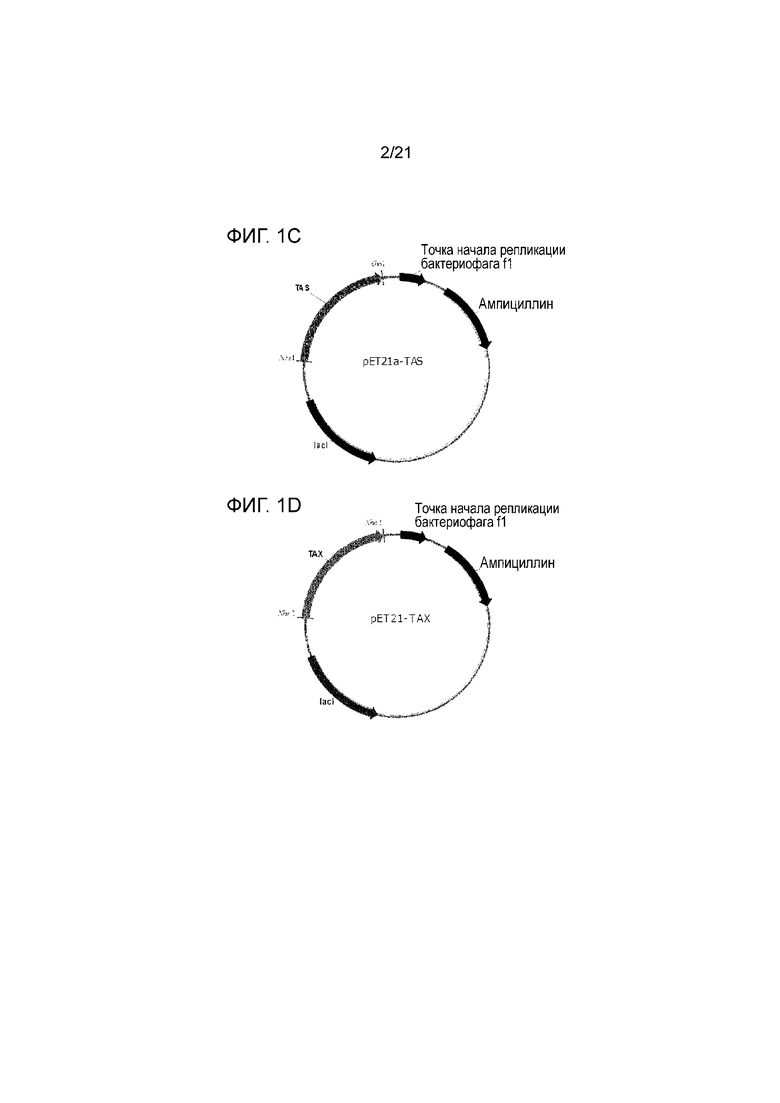
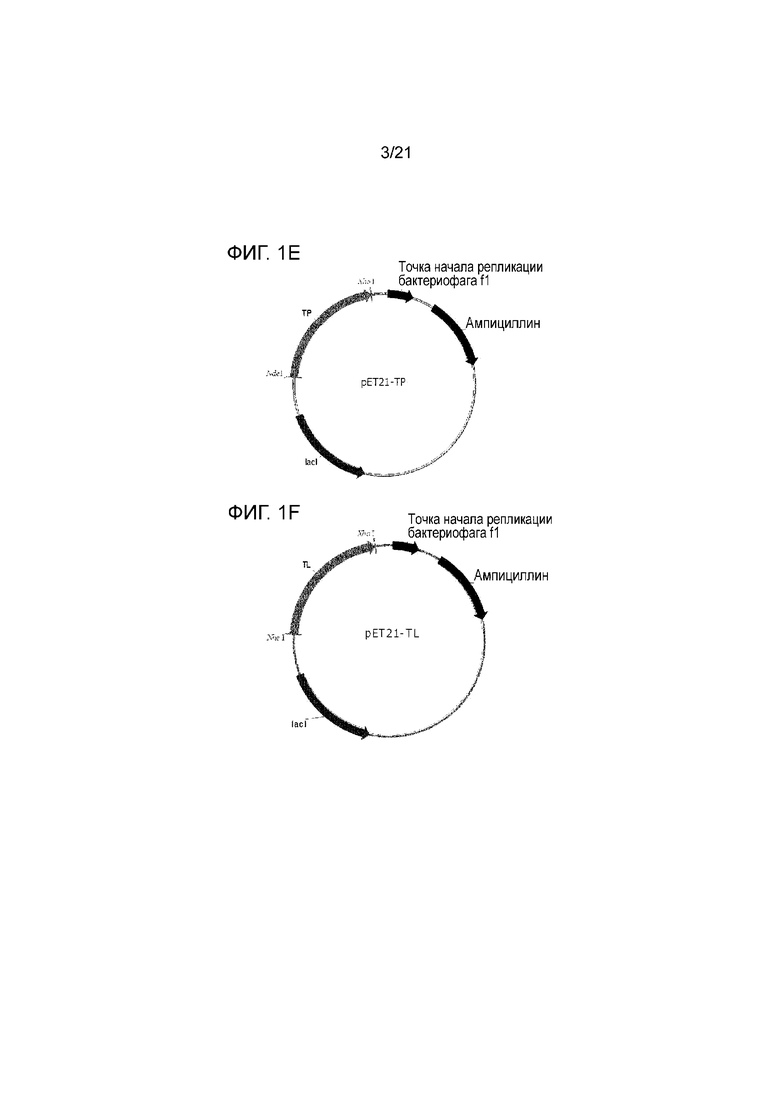
[15] На фиг. 1a-1g показаны карты расщепления рекомбинантных векторов для экспрессии семи D-фруктозо-4-эпимераз, полученных из каждого термофильного микроорганизма.
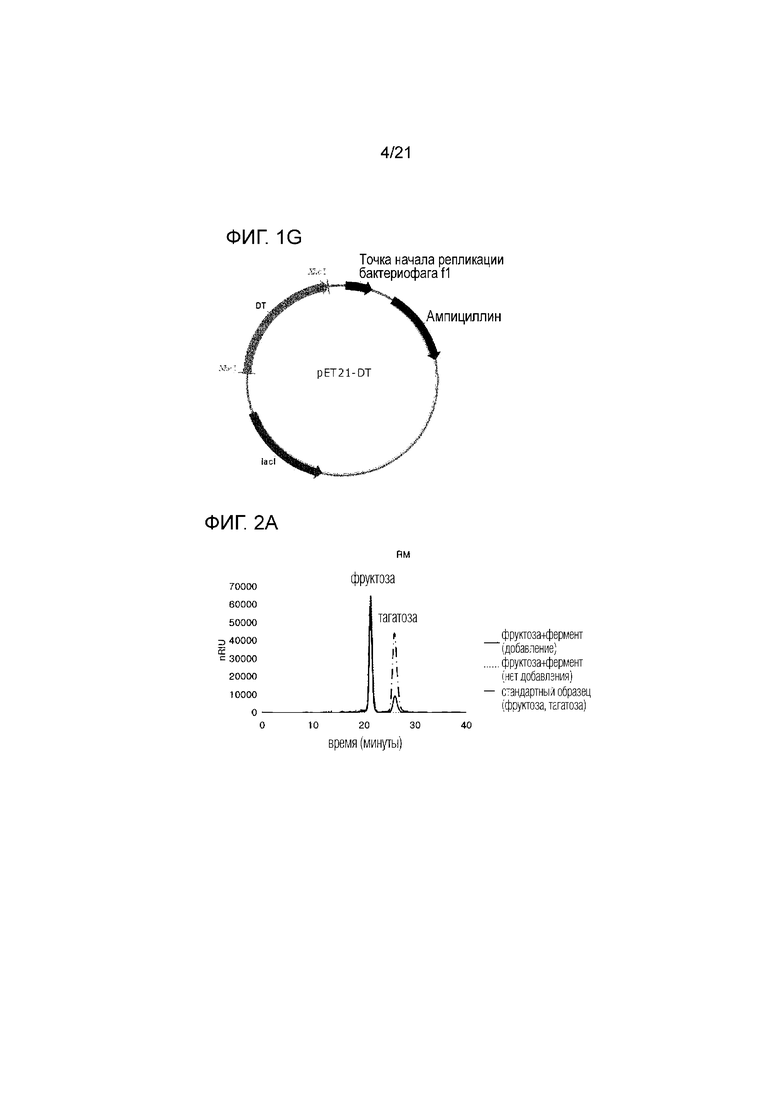
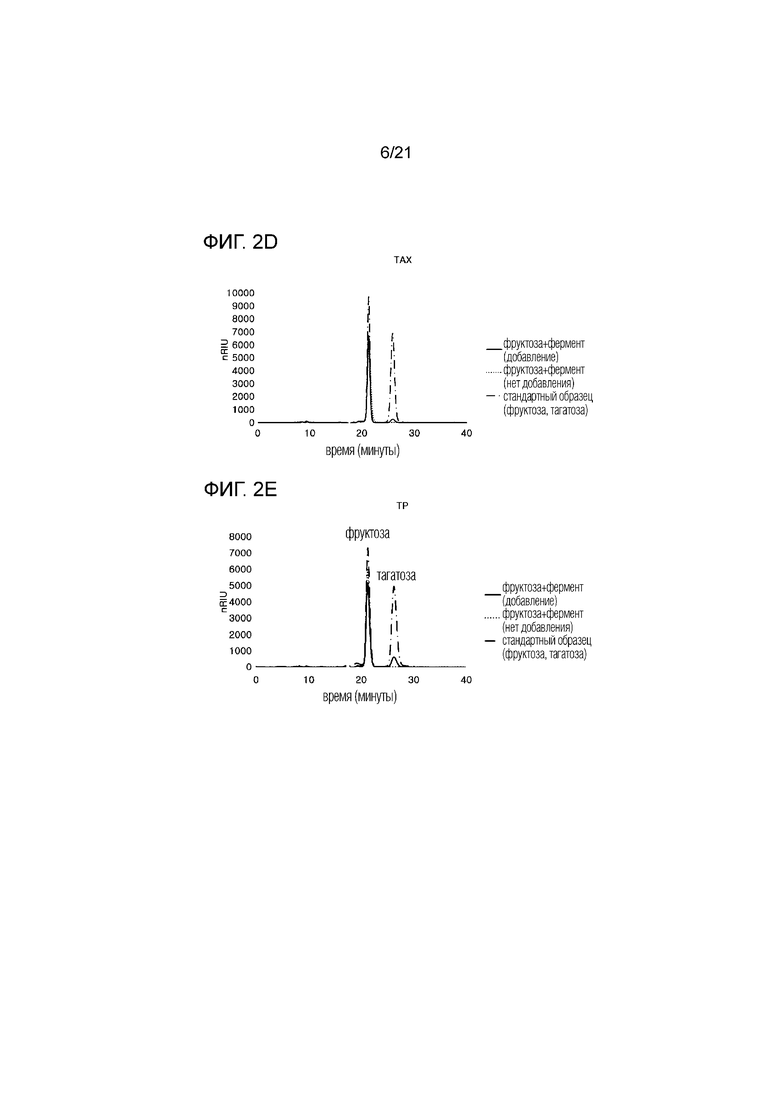
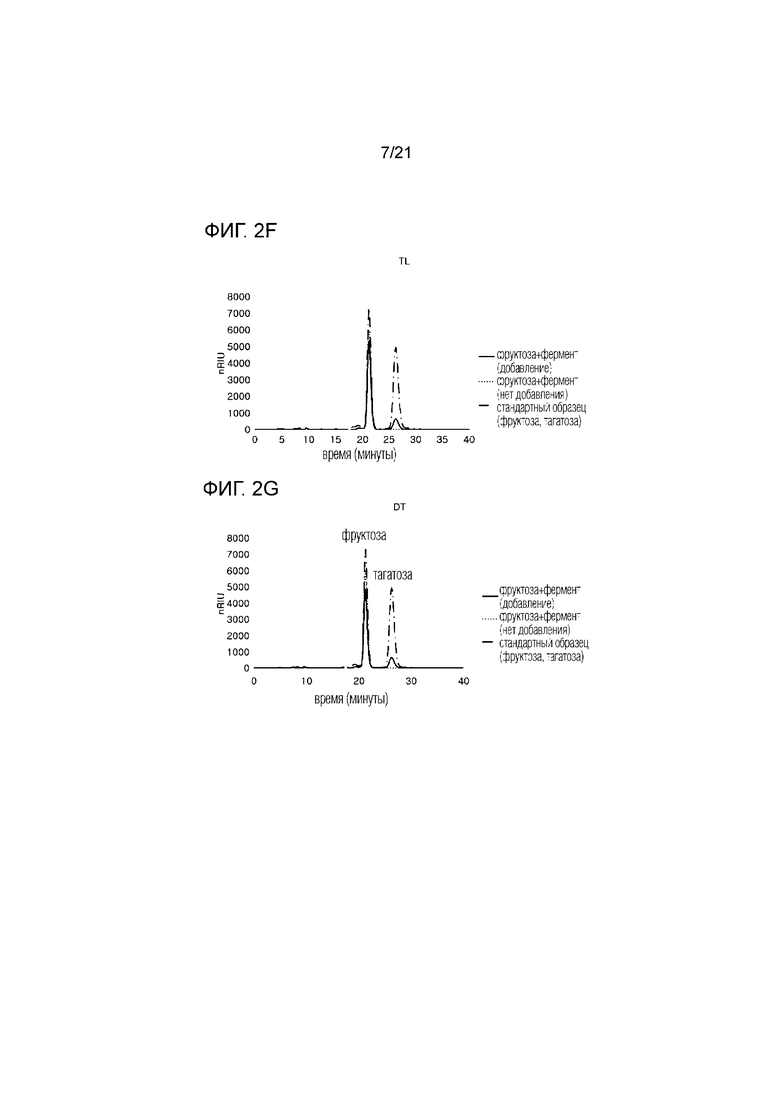
[16] На фиг. 2а-2g показаны диаграммы ВЭЖХ, отображающие семь путей получения тагатозы, полученной из термофильных микроорганизмов в результате взаимодействия D-фруктозо-4-эпимеразы с фруктозой, используемой в качестве субстрата.
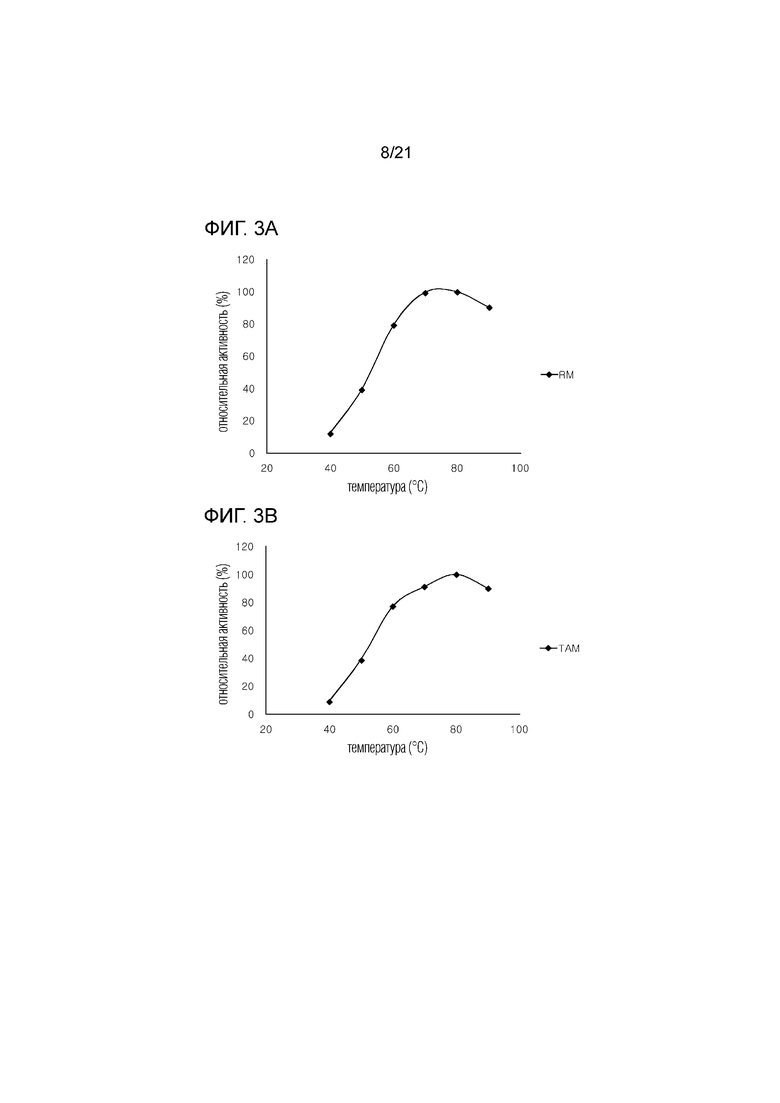
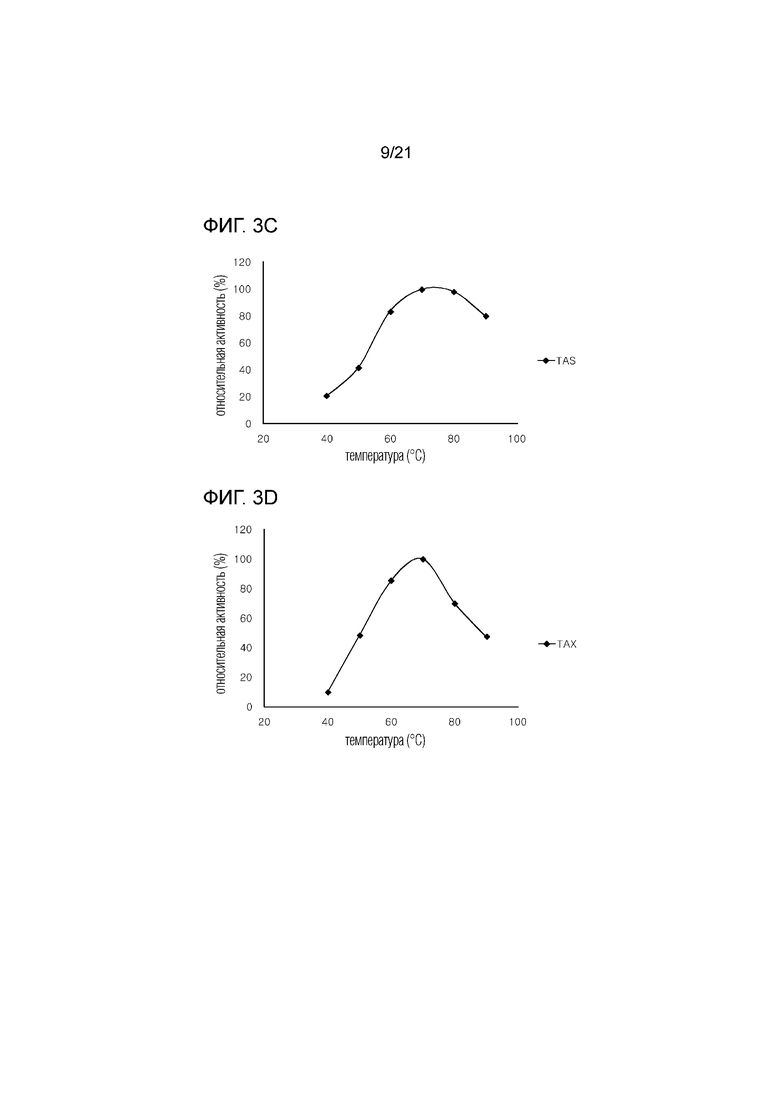
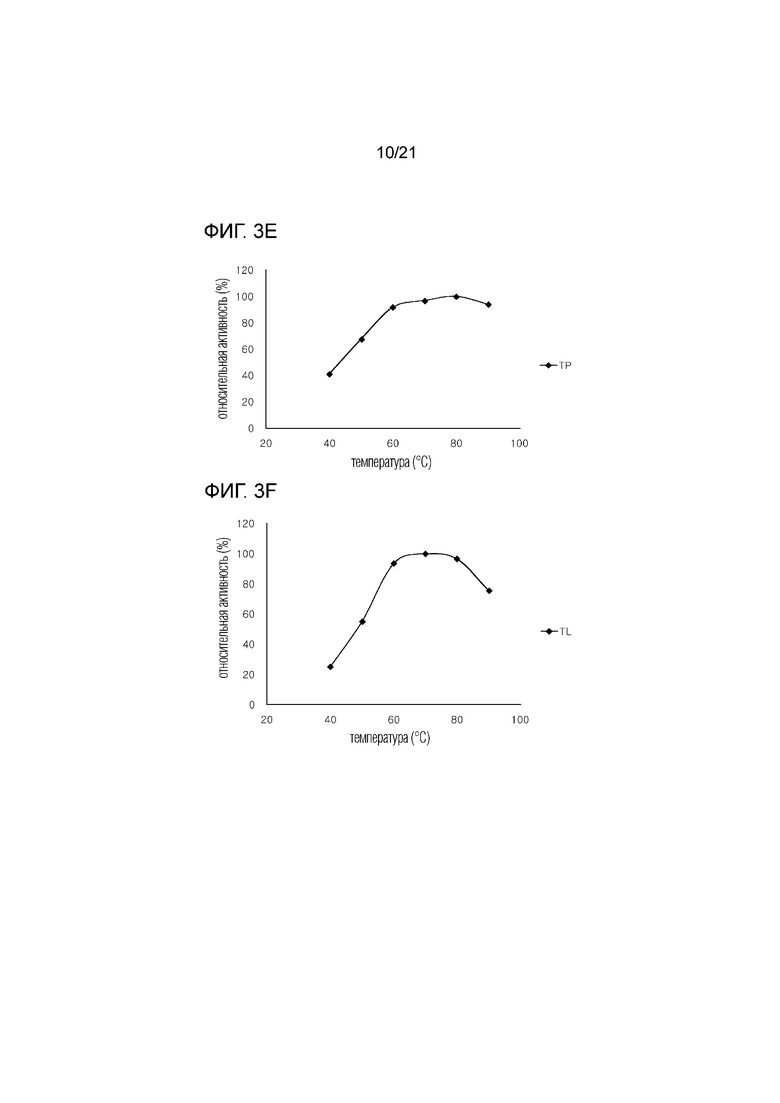
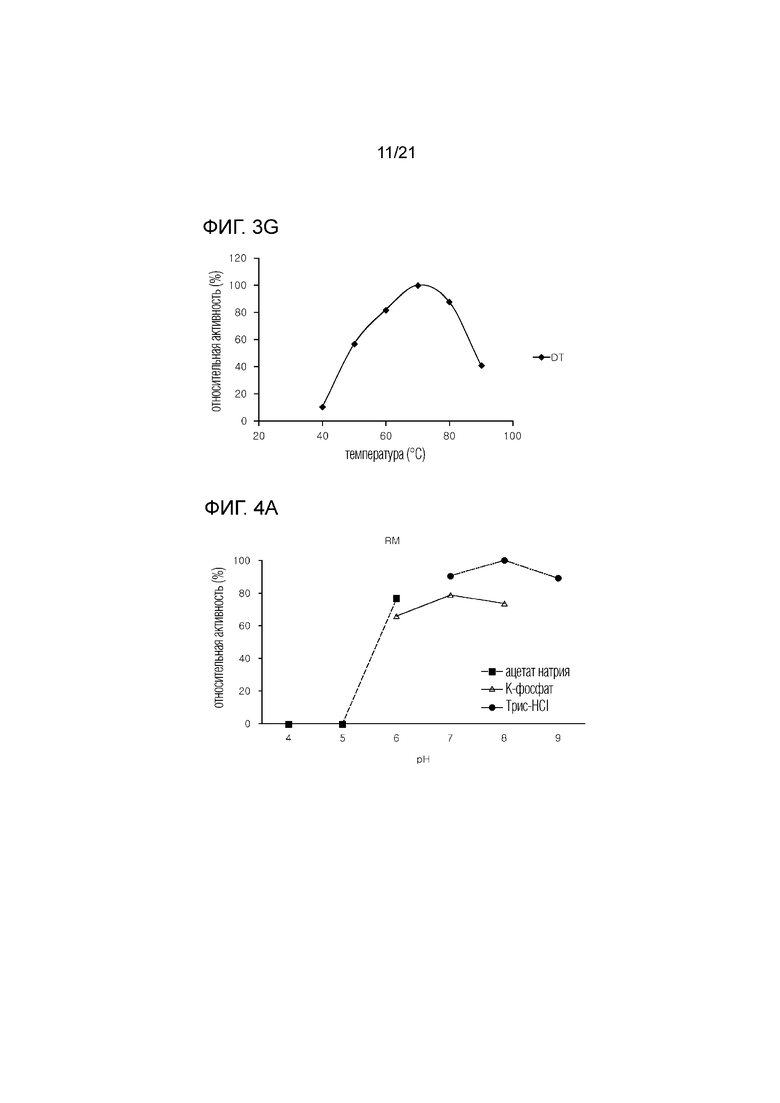
[17] На фиг. 3а-3g показаны графики активности семи D-фруктозо-4-эпимераз, полученных из термофильных микроорганизмов, в зависимости от температуры.
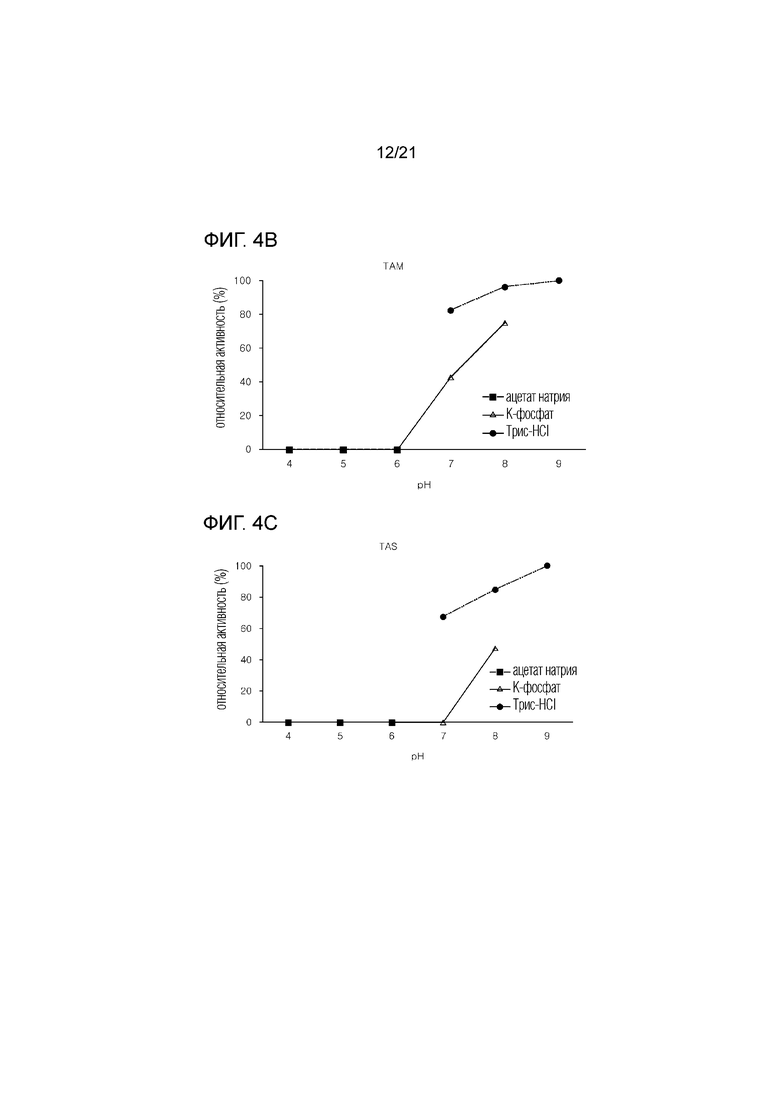
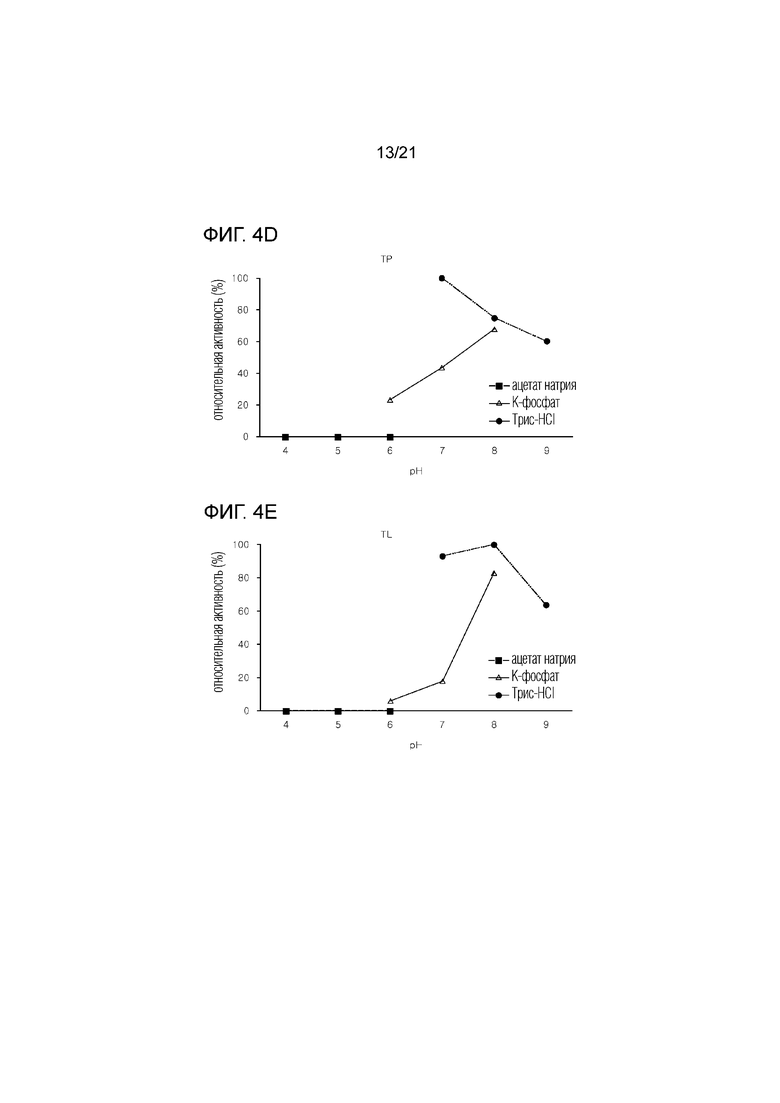
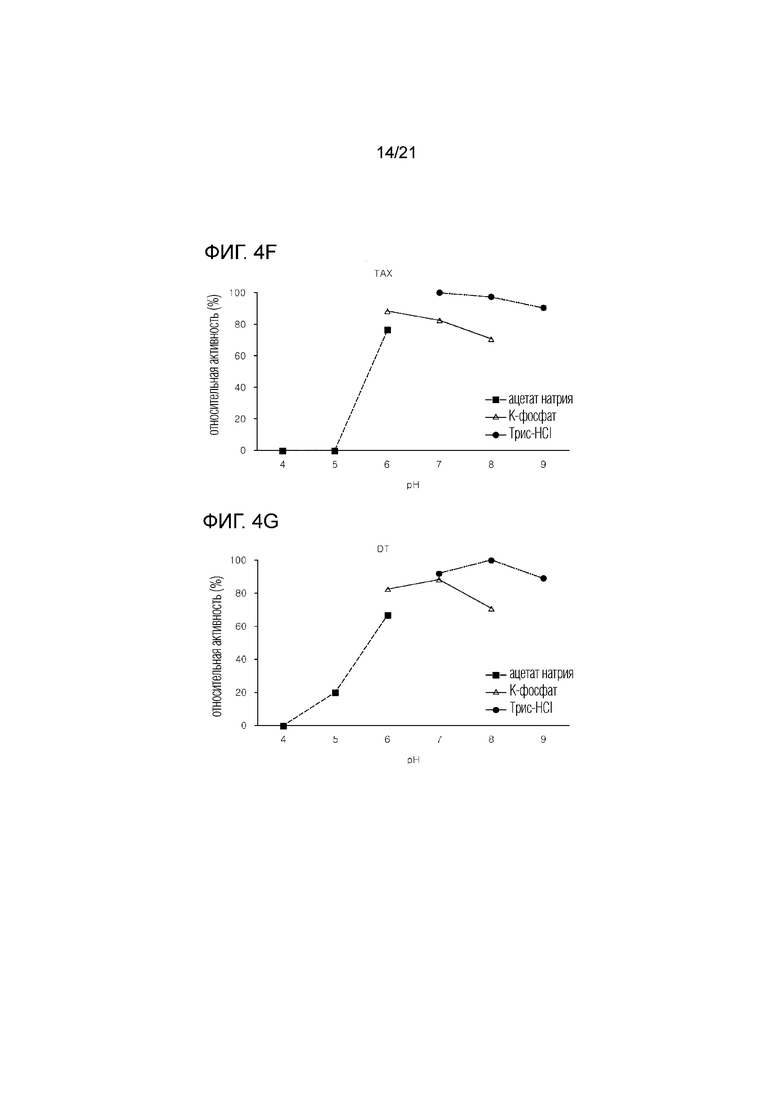
[18] На фиг. 4a-4g показаны графики активности семи D-фруктозо-4-эпимераз, полученных из термофильных микроорганизмов, в зависимости от изменения рН.
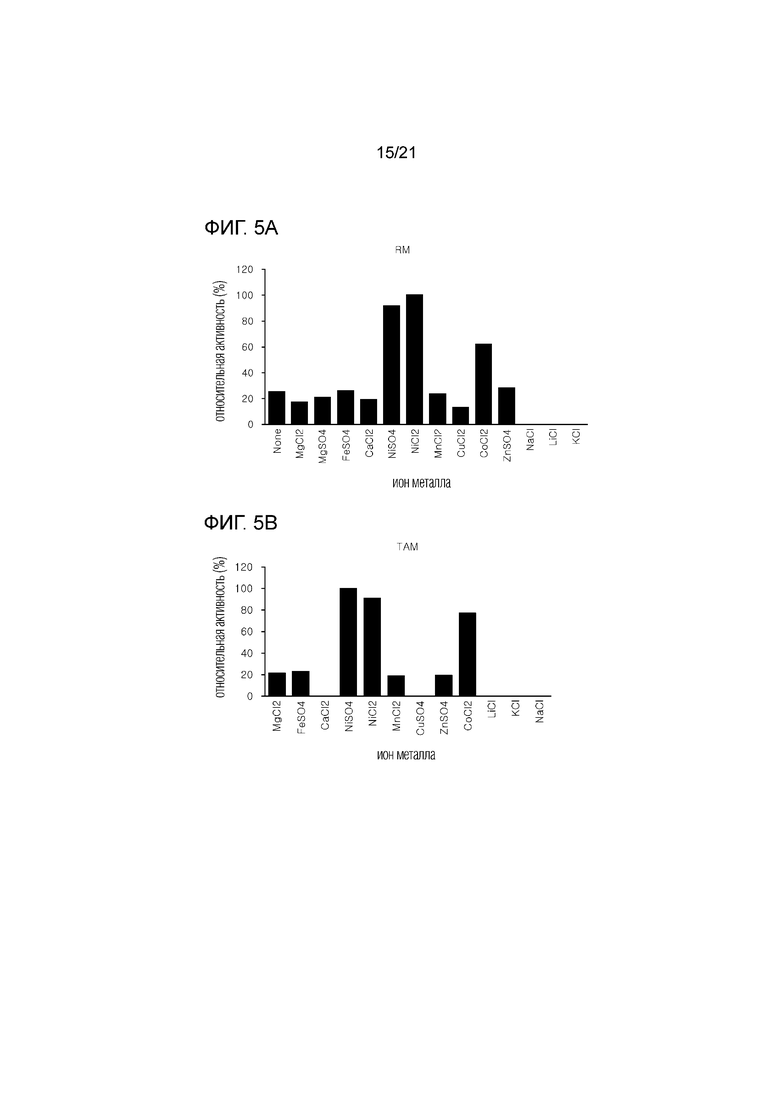
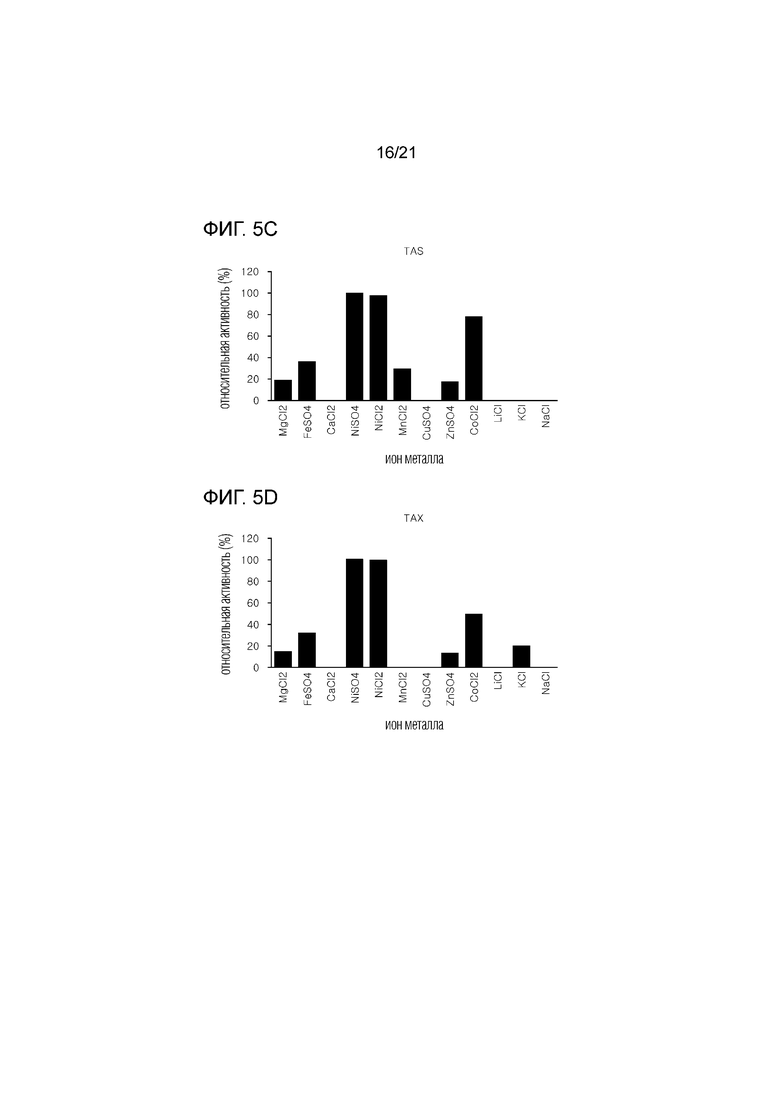
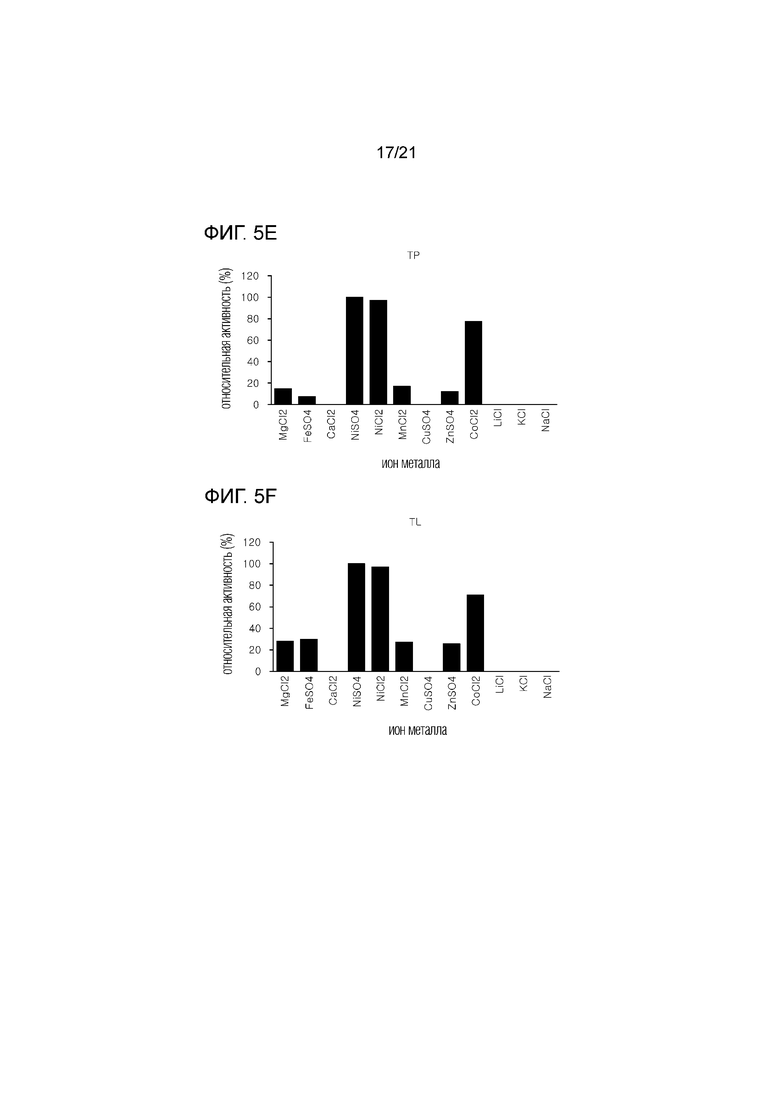
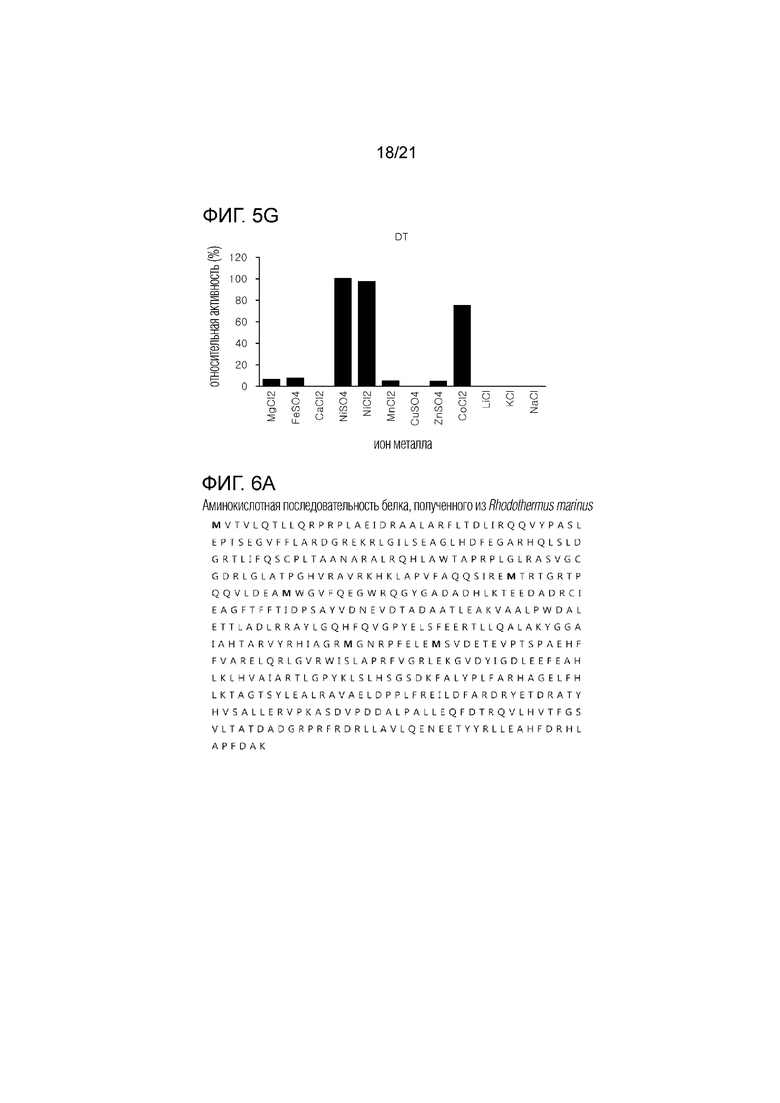
[19] На фиг. 5а-5g показаны графики активности семи D-фруктозо-4-эпимераз, полученных из термофильных микроорганизмов, в зависимости от видов ионов металлов.
[20] На фиг. 6а-6g показаны аминокислотные последовательности белков, приведенных в SEQ ID NO:1 - SEQ ID NO:7, полученных из каждого из семи термофильных микроорганизмов.
Наилучший вариант осуществления
[21] Далее приведено более подробное описание настоящего изобретения на основе конкретных вариантов осуществления. Настоящее изобретение не следует ограничивать указанными вариантами осуществления. Описания деталей, очевидных для специалистов в данной области техники, обладающих обычными знаниями в данной области техники или соответствующей области, в данном документе опущены.
[22] Как использовано в данном описании, термин ʺатом углерода в положении n (далее Cn)ʺ относится к положению углерода, определенному в соответствии с номенклатурой IUPAC, в которой n означает целое число, равное 1 или более. Например, ʺэпимеризация по атому углерода в 4-м положенииʺ выражаются как ʺC4-эпимеризацияʺ.
[23] Один из вариантов осуществления настоящего изобретения относится к композиции для получения тагатозы из фруктозы, которая содержит: белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:1 - SEQ ID NO:7, или микроорганизм, экспрессирующий указанный белок.
[24] Как правило, моносахариды могут быть классифицированы как относящиеся к альдогексозам и кетогексозам. Альдогексоза представляет собой альдозу, которая имеет шесть атомов углерода, и альдегидную группу на одном конце. Примеры альдогексоз включают глюкозу, галактозу, аллозу, гулозу, альтрозу, маннозу, талозу и идозу, но не ограничиваются ими.
[25] Кроме того, кетогексоза представляет собой моносахарид, имеющий шесть атомов углерода и кетогруппу. Примеры кетогексоз включают фруктозу, тагатозу, псикозу и сорбозу, но не ограничиваются ими. В частности, фруктоза используются в качестве кетогексозы. Как используется в настоящем документе, как фруктоза так и тагатоза представляют собой D-фруктозу и D-тагатозу, если не указано иное.
[26] В одном из вариантов осуществления настоящего изобретения, аминокислотная последовательности, представленная в SEQ ID NO:1 - SEQ ID NO:7 может, представлять собой фермент, который обладает активностью позволяющей получить тагатозу путем эпимеризации фруктозы по атому углерода 4.
[27] В частности, авторы настоящего изобретения использовали микроорганизмы, принадлежащие к термофильным родам Rhodothermus, Thermoanaerobacter, Thermotoga и Dictyoglomus. Так как ферменты, полученные из термофильных микроорганизмов, имеют ту же функцию, что и ферменты, полученные из мезофильных микроорганизмов, они могут стабильно взаимодействовать в экстремальных условиях (высокая температура или т.п.), что позволяет предотвратить загрязнение мезофильными микроорганизмами, повысить растворимость материалов, имеющих низкую растворимость в субстратах, и увеличить скорость реакции; ферменты, полученные из термофильных микроорганизмов, позволяют преодолеть недостатки мезофильных ферментов, связанные с их использованием в промышленных масштабах. Авторы настоящего изобретения выполнили скрининг фруктозо-4-эпимераз из вышеупомянутых термофильных микроорганизмов, а затем среди их нативных генов идентифицировали новые полинуклеотиды, которые экспрессируют ферменты, способные превращать фруктозу в тагатозу. Настоящее изобретение относится к ферменту, превращающему фруктозу в тагатозу, получаемому в результате синтеза полинуклеотидной последовательности, оптимизированной для эффективной повышенной экспрессии белка, посредством введения полинуклеотида в рекомбинантный вектор и экспрессии фермента.
[28] Аминокислотная последовательность, приведенная в SEQ ID NO:1 - SEQ ID NO:7, может быть трансформирована с помощью рекомбинантного вектора, включающего ген, который кодирут белок, имеющий указанную выше последовательность.
[29] Примеры используемых для трансформации микроорганизмов включают Escherichia coli BL21(DE3)-pET21a-RM (номер доступа: KCCM11576P), Escherichia coli BL21(DE3)-pET21a-TAM (номер доступа: KCCM11577P), Escherichia coli BL21(DE3)-pET21a-TAS (номер доступа: KCCM11578P), Escherichia coli BL21(DE3)-pET21a-TAX (номер доступа: KCCM11579P), Escherichia coli BL21(DE3)-pET21a-TP (номер доступа: KCCM11580P), Escherichia coli BL21(DE3)-pET21a-TL (номер доступа: KCCM11581P) и Escherichia coli BL21(DE3)-pET21a-DT (номер доступа: KCCM11582P), которые были депонированы в Корейском центре культур микроорганизмов (KCCM)(361-221 Hongje 1-dong, Seodaemun-gu, Seoul, Korea) 6 октября 2014г. под номерами доступа KCCM11576P, KCCM11577P, KCCM11578P, KCCM11579P, KCCM11580P, KCCM11581P и KCCM11582P, соответственно.
[30] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1, может представлять собой фермент, полученный из Rhodothermus marinus.
[31] Белок может иметь молекулярную массу от 55 кДа до 60 кДа, оптимальную температуру активности от 50°C до 90°C и оптимальный рН активности от 6,0 до 9,0.
[32] Более конкретно, оптимальная температура активности может составлять от 60°С до 80°С, а оптимальный рН активности может составлять от 7,0 до 9,0.
[33] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO:2, может представлять собой фермент, полученный из Thermotoga petrophila.
[34] Белок может иметь молекулярную массу от 55 кДа до 58 кДа, оптимальную температуру активности от 50°C до 90°C и оптимальный рН активности от 7,0 до 9,0.
[35] Более конкретно, оптимальная температура активности может составлять от 70°С до 90°С.
[36] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 3, может представлять собой фермент, полученный из Thermotoga lettingae.
[37] Белок может иметь молекулярную массу от 55 кДа до 58 кДа, оптимальную температуру активности от 50°C до 90°C и оптимальный рН активности от 7,0 до 9,0.
[38] Более конкретно, оптимальная температура активности может составлять от 60°С до 80°С.
[39] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 4, может представлять собой фермент, полученный из Thermoanaerobacter mathranii.
[40] Белок может иметь молекулярную массу от 55 кДа до 58 кДа, оптимальную температуру активности от 50°C до 90°C и оптимальный рН активности от 7,0 до 10,0.
[41] Более конкретно, оптимальная температура активности может составлять от 70°С до 90°С, а оптимальный рН активности может составлять от 8,0 до 10,0.
[42] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO:5, может представлять собой фермент, полученный из Dictyoglomus turgidum.
[43] Белок может иметь молекулярную массу от 55 кДа до 58 кДа, оптимальную температуру активности от 50°C до 90°C и оптимальный рН активности от 7,0 до 9,0.
[44] Более конкретно, оптимальная температура активности может составлять от 60°С до 80°С.
[45] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 6, может представлять собой фермент, полученный из Thermoanaerobacterium xylanolyticum.
[46] Белок может иметь молекулярную массу от 53 кДа до 58 кДа, оптимальную температуру активности от 50°C до 90°C и оптимальный рН активности от 6,0 до 9,0.
[47] Более конкретно, оптимальная температура активности может составлять от 60°С до 80°С, и оптимальный рН активности может составлять от 6,0 до 8,0.
[48] В частности, в одном из вариантов осуществления белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO:7 может представлять собой фермент, полученный из Thermoanaerobacter siderophilus.
[49] Белок может иметь молекулярную массу от 55 кДа до 58 кДа, оптимальную температуру активности от 50°C до 80°C и оптимальный рН активности от 7,0 до 10,0.
[50] Более конкретно, оптимальная температура активности может составлять от 60°С до 80°С, и оптимальный рН активностью может составлять от 8,0 до 10,0.
[51] Другой вариант осуществления настоящего изобретения относится к способу получения тагатозы из фруктозы, который включает: взаимодействие композиции по любому одному из вариантов осуществления настоящего изобретения с фруктозой.
[52] В частности, реакция может быть проведена при температуре от 50°С до 80°С.
[53] Кроме того, реакцию можно проводить при рН от 6,0 до 9,0.
[54] Помимо этого, реакция может быть выполнена путем дополнительного добавления ионов магния, ионов цинка, ионов никеля, ионов кобальта, ионов железа, ионов марганца или их смеси.
[55] Кроме того, в качестве субстрата может присутствовать фруктоза в концентрации от 5% (вес/объем) до 60% (вес/объем).
[56] В соответствии с одним из вариантов осуществления настоящего изобретения фруктоза может быть получена из сахарозы или глюкозы. В результате, настоящее изобретение может обеспечить способ получения тагатозы с высоким выходом с использованием распространенных и недорогих сырьевых материалов, таких как глюкоза, фруктоза, сахароза и т.п., что обеспечивает возможность серийного производства тагатозы.
[57] Соответственно, настоящее изобретение может дополнительно включать гидролиз сахарозы или изомеризацию глюкозы для получения фруктозы перед проведением реакции композиции по любому одному из вариантов осуществления настоящего изобретения с фруктозой.
[58] Ферменты, используемые в гидролизе, могут представлять собой по меньшей мере один, выбранный из группы, состоящей из β-D-фруктозидазы, включая β-фруктофуранозидазу, инвертазы, сахаразы и им подобных; сахаразы, α-глюкозидазы, и α-D-глюкогидролазы, но не ограничиваются ими.
[59] Примеры фермента, изомеризующего глюкозу, могут включать глюкозоизомеразу и фосфоглюкоизомеразу, но не ограничиваются ими.
[60] Пример
[61] Пример 1. Получение рекомбинантного микроорганизма, продуцирующего D-фруктозо-4-эпимеразу
[62] Полинуклеотиды, кодирующие аминокислотные последовательности, приведенные в SEQ ID NO:1 - SEQ ID NO:7 (Фиг 6а-6g), показанные в таблице 1, полученные из семи термофильных микроорганизмов, были вставлены в сайт рестрикции в векторе экспрессии pET21a (Novagen) с использованием ферментов рестрикции NdeI и XhoI, получая таким образом рекомбинантные векторы pET21a-RM, pET21a-TAM, pET21a-TAS, pET21a-TAX, pET21a-TP, pET21a-TL и pET21a-DT (Фиг. 1a-1g). Рекомбинантные векторы были обработаны методом теплового шока (Sambrook and Russell: Molecular Cloning) для трансформации E.coli BL21 (DE3) (Invitrogen), получая таким образом рекомбинантный микроорганизм.
[63] Таблица 1
Список термофильных микроорганизмов
[64] Трансформированный рекомбинантный микроорганизм инокулировали в 5 мл LB среды с ампициллином (Difco), культивировали при температуре 37°C при встряхивании при 180 об./мин до тех пор, пока поглощение (ОП) при 600 нм не достигло 1,5, а затем инокулировали в 500 мл LB среды с ампициллином. Затем к полученной массе добавляли 5 мМ лактозы для того, чтобы индуцировать повышенную экспрессию целевого фермента, с последующим культивированием в инкубаторе-качалке при температуре 37°С. Культивирование при температуре 37°С и 180 об./мин проводили в течение 16 часов. После этого полученную массу центрифугировали при 4000 об./мин в течение 20 минут для сбора только рекомбинантных микроорганизмов.
[65] Полученные таким образом рекомбинантные микроорганизмы обозначены следующим образом: Escherichia coli BL21(DE3)-pET21a-RM (номер доступа: KCCM11576P), Escherichia coli BL21(DE3)-pET21a-TAM (номер доступа: KCCM11577P), Escherichia coli BL21(DE3)-pET21a-TAS (номер доступа: KCCM11578P), Escherichia coli BL21(DE3)-pET21a-TAX (номер доступа: KCCM11579P), Escherichia coli BL21(DE3)-pET21a-TP (номер доступа: KCCM11580P), Escherichia coli BL21(DE3)-pET21a-TL (номер доступа: KCCM11581P) и Escherichia coli BL21(DE3)-pET21a-DT (номер доступа: KCCM11582P), которые были депонированы в Корейском центре культур микроорганизмов (KCCM)(361-221 Hongje 1-dong, Seodaemun-gu, Seoul, Korea) 6 октября 2014г. под номерами доступа KCCM11576P, KCCM11577P, KCCM11578P, KCCM11579P, KCCM11580P, KCCM11581P и KCCM11582P, соответственно.
[66] Пример 2. Очистка и идентификация свойств D-фруктозо-4-эпимеразы
[67] 2-1. Очистка D-фруктозо-4-эпимеразы
[68] Семь микроорганизмов, собранных в примере 1, растворяли в буфере для лизиса (50 мМ К-фосфат), а затем разрушали с помощьюультразвукового гомогенизатора при 4°С в течение 10 минут. Жидкость, полученную в результате разрушения, подвергали термической обработке в инкубаторе-качалке при температуре 60°С в течение 30 минут, а затем центрифугировали при 13000 об./мин в течение 10 минут с получением супернатантов. Полученные супернатанты наносили на Q-сефарозу DEAE, уравновешенную буфером для лизиса, затем последовательно промывали 50 мМ K-фосфатом и буферным раствором, содержащим 200 мМ NaCl, тем самым очищая искомые белки. Элюированные белки подвергали диализу против буферного растворам для оценки активности фермента (50 мМ K-фосфат, рН 7), который затем использовали в следующем эксперименте. Кроме того, семь очищенных D-фруктозо-4-эпимераз, RM, TAM, TAS, TAX, TP, TL и DT были подвергнуты электрофорезу в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE), при этом было установлено, что они имеют молекулярную массу примерно 58 кДа, 56кДа, 56кДа, 55кДа, 56кДа, 57кДа и 57кДа, соответственно.
[69] 2-2. Анализ активности D-фруктозо-4-эпимеразы в зависимости от изменений температуры и рН
[70] Для определения активности семи D-фруктозо-4-эпимераз, очищенных в примере 2-1, в зависимости от изменений рН и температуры ферменты подвергали взаимодействию с фруктозным субстратом при различных рН и температурах.
[71] Измерение активности проводили по результатам реакции 50 мМ фруктозы, 1 мг/мл ферментов и 0,1 мм NiSO4 при каждом значении рН и температуры диапазона, с последующим охлаждением продукта реакции льдом, а затем анализировали с помощью ВЭЖХ. ВЭЖХ-анализ проводили с использованием колонки SUGAR SP0810 (Shodex) при 80°C в потоке воды в качестве подвижной фазы при скорости потока 0,6 мл/мин, с последующим обнаружением тагатозы с помощью дифференциального детектора показателя преломления для анализа эффективности производства тагатозы.
[72] Во-первых, для оценки активности ферментов при рН 7 в зависимости от изменения температуры, эффективность производства тагатозы измеряли при 40°C - 90°C. В результате, из семи ферментов два фермента, TAM и TP, показали максимальную скорость конверсии при 80°С, в то время как пять ферментов RM, TAS, TAX, TL и DT показали максимальную скорость конверсии при 70°C (фиг. 3а - 3g).
[73] Кроме того, для оценки активности ферментов в зависимости от изменения рН, эффективности производства тагатозы измеряли при 70° C с использованием буферных растворов, состоящих из 50 мМ ацетата натрия, рН 4-6, 50 мМ К-фосфата, рН 6-8, и 50 мМ трис-HCl, рН 7 - рН 9, соответственно. В результате было подтверждено, что ферменты продемонстрировали максимальную активность при различных значениях рН, в частности, высокую активность при рН 7 - рН 9.
[74] В частности, TAX показал высокую активность при рН 7, TP, TL, RM и DT показали высокую активность при рН 8, а TAS и TAM показали высокую активность при рН 9. Кроме того, для буферных растворов с соответствующими вышеуказанными значениями рН было подтверждено, что буферный раствор трис-HCl показал максимальную активность (фиг. 4а - 4g).
[75] Как видно из фиг. 5а-5g, было подтверждено, что ферменты примера 2-1 обеспечивают возможность получения тагатозы из фруктозы.
[76] 2-3. Анализ ионов металлов, требуемых для D-фруктоза-4-эпимеразы
[77] Ранее известные эпимеразы (псикозо-3-эпимераза) и изомеразы (глюкозоизомераза, арабинозоизомераза), как известно, требуют присутствия ионов металлов. Была проведена оценка для определения, оказывают ли ионы металлов влияние на D-фруктозо-4-эпимеразы, полученные в примере 2-1.
[78] Семь белков, очищенных в примере 2-1, обрабатывали ионами металлов, используя 1 мМ NiSO4, NiCl2, CuCl2, MnCl2, CaCl2, ZnSO4, MgSO4, MgCl2, FeSO4, NaCl, LiCl, KCl или CoCl2, тем самым измеряя активность фермента. В качестве контрольной группы использовали семь ферментов, не обработанных ионами металлов. Сравнение ферментативной активности ферментов, обработанных различными ионами металлов, с необработанными ферментами показано на фиг. 5а-5g.
[79] Как показано на фиг. 5а-5g, было подтверждено, что ферменты примера 2-1 демонстрируют повышенную активность при добавлении ионов никеля и ионов кобальта, что указывают на необходимость присутствия ионов металла. В частности, было подтверждено, что NiSO4 обеспечивает максимальную активность.
[80] Пример 3. Получение тагатозы из фруктозы
[81] Эффективность производства тагатозы измеряли при оптимальных условиях для проведения ферментативной реакции, выбранных в примере 2. В частности, проводили реакцию между 1 мг/мл D-фруктозо-4-эпимеразы, очищенной в примере 2-1, и 20 г/л (в концентрации примерно 110 мМ) фруктозы при температуре реакции, например, 80°С для двух ферментов TAM и TP, 70°С для пяти ферментов RM, TAS, TAX, TL и DT в присутствии 0,1 мМ сульфата никеля, и при рН 7 для TAX, рН 8 для TP, TL, RM и DT и рН 9 для TAS и ТАМ с использованием буферного раствора 50 мМ Трис-HCl с каждым из соответствующих значений рН.
[82] Анализ методом ВЭЖХ проводили таким же способом, как и в примере 2-2 (фиг. 2а - фиг. 2g). Коэффициент конверсии фруктозы в тагатозу определялся по количеству тагатозы, полученной в результате реакции. Результаты представлены в таблице 2.
[83] Таблица 2
[84] Раствор, полученный в результате описанной выше реакции (смешанный раствор тагатозы и фруктозы), обесцвечивали (используя активированный уголь), очищали путем ионного обмена, хроматографии, и кристаллизации, получая таким образом кристаллическую тагатозу.




Группа изобретений относится к получению тагатозы из фруктозы. Предложен белок для получения тагатозы из фруктозы, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1-7. Предложен также рекомбинантный микроорганизм для получения тагатозы из фруктозы, экспрессирующий указанный белок. Предложен также способ получения тагатозы из фруктозы, включающий приведение в контакт вышеуказанных белка или микроорганизма с фруктозой и получение тагатозы. Изобретение обеспечивает получение тагатозы из фруктозы с высоким выходом. 3 н. и 18 з.п. ф-лы, 42 ил., 2 табл., 3 пр.
1. Белок для получения тагатозы из фруктозы, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1-7.
2. Белок по п.1, где белок представляет собой ферментативный белок, превращающий фруктозу в тагатозу путем эпимеризации фруктозы по углероду в положении 4.
3. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:1, получают из Rhodothermus marinus.
4. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:2, получают из Thermotoga petrophila.
5. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:3, получают из Thermotoga lettingae.
6. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:4, получают из Thermoanaerobacter mathranii.
7. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:5, получают из Dictyoglomu sturgidum.
8. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:6, получают из Thermoanaerobacterium xylanolyticum.
9. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:7, получают из Thermoanaerobacter siderophilus.
10. Белок по п.1, где белок, имеющий аминокислотную последовательность, описанную в SEQ ID NO:1, имеет молекулярную массу от 55 до 60 кДа, оптимальную температуру активности от 50 до 90°C и оптимальный рН активности 6,0-9,0.
11. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:2, имеет молекулярную массу от 55 до 58 кДа, оптимальную температуру активности от 50 до 90°С и оптимальный рН активности 7,0-9,0.
12. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:3, имеет молекулярную массу от 55 до 58 кДа, оптимальную температуру активности от 50 до 90°С и оптимальный рН активности 7,0-9,0.
13. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:4, имеет молекулярную массу от 55 до 58 кДа, оптимальную температуру активности от 50 до 80°С и оптимальный рН активности 7,0-10,0.
14. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:5, имеет молекулярную массу от 55 до 58 кДа, оптимальную температуру активности от 50 до 90°С и оптимальный рН активности рН 7,0-9,0.
15. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:6, имеет молекулярную массу от 55 до 58 кДа, оптимальную температуру активности от 50 до 90°С и оптимальный рН активности 6,0-9,0.
16. Белок по п.1, где белок, имеющий аминокислотную последовательность, приведенную в SEQ ID NO:7, имеет молекулярную массу от 55 до 58 кДа, оптимальную температуру активности от 50 до 80°С и оптимальный рН активности 7,0-10,0.
17. Рекомбинантный микроорганизм для получения тагатозы из фруктозы, экспрессирующий белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1-7.
18. Микроорганизм по п. 17, где микроорганизм трансформирован рекомбинантным вектором, содержащим ген, кодирующий белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1-7.
19. Способ получения тагатозы из фруктозы, включающий приведение в контакт белка по любому из пп.1-16 или микроорганизма по п. 17 или 18 с фруктозой и получение тагатозы.
20. Способ получения тагатозы из фруктозы по п.19, в котором приведение в контакт проводят в условиях, соответствующих одному из следующих условий:
а) температура от 50 до 80°С,
б) рН от 6,0 до 9,0 и
с) концентрация фруктозы от 5 до 60% (вес./об.).
21. Способ получения тагатозы из фруктозы по п.19, дополнительно включающий добавление ионов магния, ионов цинка, ионов никеля, ионов кобальта, ионов железа, ионов марганца или их смеси.
| NCBI Reference Sequence: WP_012844026.1, 18.05.2013 | |||
| NCBI Reference Sequence: WP_011943119.1, 16.05.2013 | |||
| NCBI Reference Sequence: WP_012002872.1, 16.05.2013 | |||
| NCBI Reference Sequence: WP_013150657, 18.05.2013 | |||
| NCBI Reference Sequence: WP_012582608.1, 17.05.2013 | |||
| NCBI Reference Sequence: WP_013788787.1, 18.05.2013 | |||
| NCBI Reference Sequence: WP_006569468.1, 28.05.2013 | |||
| KIM HJ ET AL | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Appl Biochem Biotechnol | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| WANARSKA M | |||
| A method for the production of D-tagatose using a recombinant Pichia pastoris strain secreting β-D-galactosidase from Arthrobacter chlorophenolicus and a recombinant L-arabinose isomerase from Arthrobacter sp | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Microbial Cell Factories, 2012, 11:113 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТАГАТОЗЫ С ИСПОЛЬЗОВАНИЕМ ОЛИГОСАХАРИДА СОИ | 2009 |
|
RU2451688C2 |
Авторы
Даты
2019-09-30—Публикация
2015-10-19—Подача