ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к катализатору синтеза оксалата посредством реакции связывания СО, а также к способу получения и применениям такого катализатора.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Диметилоксалат может быть использован в качестве важного химического сырья для получения щавелевой кислоты, этиленгликоля и т.д. либо в качестве промежуточного фармацевтического продукта. Этиленгликоль в качестве важного химического сырья в основном используется при получении полиэтилентерефталата (ПЭТФ). При получении этиленгликоля путем традиционного производства технологического маршрута из нефтяного этилена добывается окись этилена, которая затем подвергается гидрированию. Данный технологический маршрут относится к «нефтяному технологическому маршруту». Его преимущество заключается в сформированности этой технологии, но его недостатком является то, что энергопотребление является высоким, а на себестоимости получаемого продукта серьезно отражаются мировые цен на сырую нефть.
В среде известных на сегодняшний день различных технологий синтеза этиленгликоля постепенно сформировался технологический маршрут, предусматривающий синтез диэфира щавелевой кислоты из СО с последующим гидрированием такого диэфира щавелевой кислоты, в результате чего образуется этиленгликоль. На конец 2009 года в зоне разработки высоких технологий в городе Тунляо автономного региона Внутренняя Монголия была завершена промышленная демонстрационная установка мощностью 200000 тонн, которая осуществила успешный выпуск высококачественных этиленгликолевых продуктов, возвестив тем самым о том, что основанная на угле технология получения этиленгликоля официально перешла на уровень крупных промышленных масштабов.
Одной из ключевых технологий получения этиленгликоля из угольного синтез-газа является разработка катализатора, ускоряющего реакцию СО с метилнитритом, в результате которой образуется диметилоксалат. В патенте, выданном на территории Японии под №JP 8242656, представлена технология синтеза диметилоксалата из СО и метилнитрита с применением катализатора на основе металлов платиновой группы, которая имеет выход продукта за один проход в единицу времени на уровне 432 г/л-1⋅час-1. В патенте, выданном на территории США под №4,507,494, сообщается о выходе метилового эфира за один проход в единицу времени на уровне от 429 до 462 г/л-1⋅час-1, а также об избирательности в отношении полученного из СО диметилоксалата на уровне до 95% при использовании катализатора Pd-Ti/Al2O3. Существующие катализаторы карбонилирования СО, как правило, являются палладиевыми катализаторами на основе αAl2O3. С целью повышения выхода продукта за один проход в единицу времени в Китае исследовались такие вспомогательные вещества, как Zr (патент, выданный в КНР под №CN 1066070С), 1 г (патента, опубликованный в КНР под №CN 101279257А) и Се (патент, выданный в КНР под №CN 1141179С).
В последние годы в большом количестве патентов представлялись катализаторы, содержащие такие добавки, как Mo, Ni, Ti, Fe, Ga, Cu, Zn, Na2O и SiO2, которые добавляются в качестве вспомогательных веществ в катализаторы, используемые в синтезе оксалата из СО и метилнитрита.
Кроме того, исследователями были проведены обширные исследования на предмет модификации 01AI2O3 и новейших носителей.
В патенте, выданном на территории КНР под №CN 102649056 В, описана технология, в которой в качестве активного компонента используется палладий, в качестве вспомогательного вещества - рутений или осмий, а в качестве композитного носителя - оксид алюминия и диоксид кремния, в результате чего получается катализатор с высокой избирательностью и большой удельной площадью поверхности, но низким выходом продукта за один проход в единицу времени.
В патенте, опубликованном на территории КНР под №CN 106607024А, представлена технология, в которой в качестве активного компонента используется палладий, в качестве вспомогательного вещества - цинк, а в качестве носителя - редкоземельный элемент, модифицированный оксидом алюминия, в результате чего получается катализатор, имеющий удельную площадь поверхности от 3 до 40 м2/г, выход диметилоксалата за один проход в единицу времени на уровне выше 760 г/л-1⋅час-1 и стабильность работы на протяжении 3000 час.
В патенте, опубликованном на территории КНР под №CN 108187691, излагается способ получения катализатора, имеющего уплотненную композитную структуру, который предназначен для осуществления путем связывания газовой фазы СО синтеза оксалата, а также сфера его применения. Такой катализатор содержит каркас из оксида алюминия и носитель с наполненной композитной структурой, состоящей из наполнителя, которым изнутри заполнен каркас, а также выполняющий функцию активного компонента Pd и выполняющие функцию вспомогательных веществ Fe и Cu, которыми покрыта поверхность носителя. Выход продукта за один проход в единицу времени составлял до 1000 г/л-1⋅час-1.
В настоящее время в большинство катализаторов синтеза диметилоксалата в качестве активного компонента используется Pd, в качестве вспомогательного вещества используются Mo, Ni, Ti, Fe, Ga, Cu, Zn или подобные вещества, а в качестве композитного носителя используется α-оксид алюминия либо модифицированный оксид алюминия. При этом общий выход продукта за один проход в единицу времени является небольшим, площадь поверхности - малой, а содержание примесей в сырье - высоким. В промышленных установках для обеспечения целей очистки сырьевых газов зачастую требуется специальное дегидрогенизационное оборудование. В подобной промышленной установке в циркуляционной системе содержится NO, а присутствие NO, как правило, приводит к снижению коэффициента конверсии MN.
Поэтому остается потребность в эффективном катализаторе синтеза оксалата посредством реакции связывания СО.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В рамках настоящего изобретения предлагаются катализатор, а также способ получения и применения такого катализатора.
При этом предлагается катализатор синтеза оксалата посредством реакции связывания СО. Такой катализатор включает (а) активный компонент, содержащий палладий (Pd) либо его оксид; (b) вспомогательное вещество, содержащее вспомогательный элемент, выбранный из группы, состоящей из никеля, кобальта, марганца, циркония, церия, лантана, молибдена, бария, ванадия, титана, железа, иттрия, ниобия, вольфрама, олова и висмута; и (с) носитель, состоящий из полых микросфер α-Al2O3. Этот катализатор может обладать удельной площадью поверхности от 1 до 200 м2/г. Этот катализатор может состоять из активного компонента, содержание которого будет составлять от 0,005 до 1,000 вес. %, вспомогательного вещества, содержание которого будет составлять от 0,01 до 5,00 вес. %, и носителя. Вспомогательный элемент может быть выбран из группы, состоящей из марганца, циркония, церия, лантана, ванадия, титана, иттрия, ниобия, олова и висмута.
По каждому катализатору в рамках настоящего изобретения предлагается свой способ получения. Данный способ включает (а) дегидратацию углеводного раствора с получением твердого углеводного образца, причем указанный углеводный раствор содержит углевод, имеющий карбонильную группу, гидроксильную группу или их сочетание; (b) сушку твердого углеводного образца с получением структурного прекурсора; (с) добавление структурного прекурсора в раствор нитрата алюминия с получением алюминиевого образца; (d) дегидратацию алюминиевого образца с получением твердого алюминиевого образца; (е) сушку твердого алюминиевого образца с получением высушенного твердого алюминиевого образца; (f) прокаливание высушенного твердого алюминиевого образца с получением носителя, состоящего из полых микросфер из α-Al2O3; (g) пропитывание носителя пропиточным раствором, содержащим активный компонент и вспомогательное вещество с получением смеси; (h) сушку указанной смеси с получением высушенной смеси; и (i) прокаливание высушенной смеси.
Упомянутый углевод может быть выбран из группы, состоящей из глюкозы, фруктозы, сахарозы и мальтозы. Кроме того, данный способ может включать перед этапом (b) многократную промывку твердого углеводного образца деионизированной водой и этанолом.
Структурный прекурсор может быть добавлен в раствор нитрата алюминия при массовом соотношении структурный прекурсор/нитрат алюминия 1:(5-50).
Кроме того, данный способ может предусматривать на этапе (с) ультразвуковую обработку алюминиевого образца и выдерживание его на протяжении от 8 до 20 час.
Данный способ дополнительно включает растворение в деионизированной воде соли вспомогательного элемента и соли Pd с получением раствора активного компонента/вспомогательного вещества, и корректирование рН раствора активного компонента/вспомогательного вещества до значения от 1 до 5 с помощью разбавленной азотной кислоты, разбавленный соляной кислоты, щавелевой кислоты либо лимонной кислоты с получением пропиточного раствора, и распыление пропиточного раствора по носителю в объеме, равном объему носителя. Соль Pd может быть выбрана из группы, состоящей из галогенида, нитрата, ацетата и ацетилацетоната. Соль вспомогательного элемента может быть выбрана из группы, состоящей из хлорида, нитрата, ацетата, оксалата и аммониевой соли.
По каждому представленному в данном изобретении катализатору предлагается способ его восстановления для целей синтеза оксалата в происходящей в газовой фазе реакции между монооксидом углерода (СО) и метилнитритом (MN). Указанный способ восстановления включает подвергание катализатора воздействию восстановительного газа на протяжении от 3 до 8 часов при температуре от 130 до 220°С и при атмосферном давлении. Восстановительный газ представляет собой смесь водорода (H2) и азота (N2), которая имеет молярное содержание H2 от 5 до 30% и величину расхода от 40 до 80 мл/мин ⋅ г катализатора.
По каждому представленному в данном изобретении катализатору также предлагается способ синтеза оксалата в газофазной реакции между монооксидом углерода (СО) и метилнитритом (MN). Этот способ синтеза включает подвергание сырьевого газа воздействию представленного в настоящем изобретении катализатора при температуре от 100 до 160°С и под давлением от 0,1 до 0,5 МПа. Сырьевой газ представляет собой смесь метилнитрита (MN), монооксида углерода (СО) и азота (N2), которая имеет молярное отношение CO/MN на уровне (1-3):1, а объемно-пространственную скорость, также известную как часовая объемная скорость газа (GHSV), от 3000 до 10000 час-1, и из которой в итоге синтезируется оксалат.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В рамках настоящего изобретения предлагаются катализатор синтеза оксалата посредством реакции связывания СО, а также способ получения и применения такого катализатора. Указанный катализатор включает активный компонент, вспомогательное вещество и носитель. Настоящее изобретение предлагает решение технических проблем в части большой потребности в сырье, малого выхода продукта за один проход в единицу времени, а также низкой стабильности, которые сопряжены с существующими технологиями, путем предложения катализатора синтеза оксалата посредством реакции связывания СО. Авторы настоящего изобретения неожиданно обнаружили, что полые микросферы из a-Al2O3, обладающие большой удельной площадью поверхности, могут быть использованы в качестве носителя катализатора, обеспечивая при этом хорошую диспергируемость металла, низкую концентрацию драгоценного металла, высокую активность и селективность во время реакции СО и MN, происходящей в процессе синтеза диметилоксалата, сильное сопротивление водороду в сырьевом газе, высокий коэффициент конверсии MN под действием высокого содержания NO в сырьевом газе, а также высокую стабильность самого катализатора. Кроме того, предлагается способ получения указанного катализатора, а также его применение в реакции связывания СО, направленной на синтез оксалата, например, диметилоксалата.
Здесь предлагается катализатор синтеза оксалата посредством реакции связывания СО. Указанный катализатор содержит активный компонент, вспомогательное вещество и носитель. Оксалат может представлять собой диметилоксалат, диэтилоксалат или их сочетание.
Используемый в настоящем документе термин «активный компонент» относится к присутствующему в катализаторе веществу, которое катализирует один или несколько реагентов, задействованных в синтезе целевого продукта. Активный компонент может содержать палладий (Pd) либо его оксид. Активный компонент может составлять примерно от 0,005 до 1,000 вес. %, предпочтительно от 0,06 до 0,95 вес. %, а более предпочтительно от 0,2 до 0,6 вес. % катализатора. Для получения присутствующего в катализаторе активного компонента может быть использована соль Pd. Соль Pd может быть выбрана из группы, в которую входят галогенид, нитрат, ацетат и ацетилацетонат, предпочтительно галогенид, ацетат и нитрат, а более предпочтительно галогенид и нитрат.
Используемый в настоящем документе термин «вспомогательное вещество» относится к присутствующему в катализаторе веществу, которое способствует взаимодействию между присутствующими в таком катализаторе активным компонентом и носителем. Вспомогательное вещество может содержать элемент, выбранный из группы, в которую входят никель, кобальт, марганец, цирконий, церий, лантан, молибден, барий, ванадий, титан, железо, иттрий, ниобий, вольфрам, олово и висмут, предпочтительно элемент, выбранный из группы, в которую входят марганец, цирконий, церий, лантан, ванадий, титан, иттрий, ниобий, олово и висмут, а более предпочтительно элемент, выбранный из группы, в которую входят церий, лантан, иттрий, ниобий, олово и висмут. Вспомогательное вещество может составлять примерно от 0,01 до 5,00 вес. %, предпочтительно от 0,1 до 4,00 вес. %, а более предпочтительно от 0,15 до 2,00 вес. % катализатора. Для получения присутствующего в катализаторе вспомогательного вещества можно использовать соль вспомогательного элемента. Соль вспомогательного элемента может быть выбрана из группы, в которую входят хлорид, нитрат, ацетат, оксалат и аммониевая соль, предпочтительно хлорид, нитрат и ацетат, а более предпочтительно хлорид и нитрат.
Используемый в настоящем документ термин «носитель» относится к присутствующему в катализаторе веществу, которое обеспечивает основу для активного компонента и вспомогательного вещества. В зависимости от своей структуры носитель может изменить распределение активного компонента по носителю настолько, что может быть изменена каталитическая активность самого активного компонента. Носитель состоит из полых микросфер из оксида алюминия (например, α-Al2O3). Полые микросферы из оксида алюминия могут образоваться путем установления оксидом алюминия ковалентных связей. Такая микросфера имеет в своем составе оболочку, которая обволакивает собой полую структуру. Полая структура может составлять примерно от 1 до 90 об. %, предпочтительно от 3 до 85 об. %, а более предпочтительно от 5 до 75 об. % от общего объема микросферы.
Используемый в данном документе термин «удельная площадь поверхности» относится к свойству твердого вещества, определяемому как общая площадь поверхности материала на единицу массы. Присутствующий в представленном в настоящем изобретении катализаторе носитель может обладать удельной площадью поверхности от 1 до 200 м2/г, предпочтительно от 7 до 180 м2/г, а более предпочтительно от 10 до 150 м2/г.
По каждому катализатору в рамках настоящего изобретения предлагается свой способ получения. Такой способ предусматривает получение носителя, состоящего из полых микросфер из β-Al2O3, а также получение из такого носителя, активного компонента и вспомогательного вещества катализатора.
Носитель может быть получен по своему способу. Такой способ получения носителя предусматривает дегидратацию углеводного раствора, например, при температуре от 150 до 180°С на протяжении от 6 до 12 час, в результате чего получается твердый углеводный образец; сушку твердого углеводного образца, например, при температуре от 40 до 80°С на протяжении от 5 до 24 час, в результате чего получается структурный прекурсор; добавление структурного прекурсора в раствор нитрата алюминия, в результате чего получается алюминиевый образец; дегидратацию алюминиевого образца, например, при температуре от 6 до 80°С на протяжении от 10 до 20 час, в результате чего получается твердый алюминиевый образец; сушку твердого алюминиевого образца, например, при температуре от 6 до 80°С на протяжении от 10 до 20 час, в результате чего получается высушенный твердый алюминиевый образец; прокаливание высушенного твердого алюминиевого образца, например, по меньшей мере при температуре от 300 до 500°С на протяжении от 2 до 5 час в условиях газообразного азота, а затем при температуре от 1000 до 1200°С на протяжении от 1 до 6 час, в результате чего получается носитель, состоящий из полых микросфер из α-Al2O3.
Углеводный раствор может содержать углевод, имеющий карбонильную группу, гидроксильную группу либо их сочетание. Упомянутый углевод может быть выбран из группы, в которую входят глюкоза, фруктоза, сахароза и мальтоза, предпочтительно глюкоза и сахароза, а более предпочтительно глюкоза.
Кроме того, способ получения носителя может предусматривать перед переходом к сушке многократную промывку твердого углеводного образца деионизированной водой и этанолом. Также этот способ получения носителя может предусматривать перед переходом к дегидратации алюминиевого образца ультразвуковую обработку алюминиевого образца с дальнейшим выдерживанием его на протяжении от 8 до 20 час.
Катализатор может быть получен по способу получения катализатора. Такой способ получения катализатора предусматривает пропитку носителя пропиточным раствором, содержащим активный компонент и вспомогательное вещество, в результате чего получается смесь; сушку этой смеси, например, при температуре от 65 до 130°С на протяжении от 5 до 10 час, в результате чего получается высушенная смесь; а также прокаливание такой высушенной смеси, например, при температуре от 300 до 500°С на протяжении от 2 до 8 час, в результате чего и получается катализатор. Структурный прекурсор может быть добавлен в раствор нитрата алюминия при массовом соотношении структурный прекурсор/нитрат алюминия 1:(5-50), предпочтительно 1:(10-40), а более предпочтительно 1:(15-30).
Кроме того, способ получения катализатора может предусматривать растворение в деионизированной воде соли вспомогательного элемента и соли Pd, в результате чего получается раствор активного компонента/вспомогательного вещества, а также корректирование рН раствора активного компонента/вспомогательного вещества до уровня от 1 до 5 с помощью разбавленной азотной кислоты, разбавленный соляной кислоты, щавелевой кислоты либо лимонной кислоты, в результате чего получается пропиточный раствор, а также распыление пропиточного раствора по носителю в объеме, равном объему самого носителя.
В каждом из описанных в настоящем изобретении вариантов перед использованием для целей синтеза оксалата в происходящей в газовой фазе реакции между монооксидом углерода (СО) и метилнитритом (MN) катализатор подвергается восстановлению. Указанный способ предусматривает подвергание представленного в настоящем изобретении катализатора воздействию восстановительного газа в восстановительных условиях, например, при температуре от 130 до 220°С и при атмосферном давлении на протяжении от 3 до 8 час. Восстановительный газ может представлять собой смесь водорода (Н2) и азота (N2), которая имеет молярное содержание Н2 от 5 до 30% и величину расхода на уровне от 40 до 80 мл⋅мин-1⋅г-1 катализатора. В результате осуществляется восстановление катализатора.
По каждому представленному в данном изобретении катализатору предлагается способ синтеза оксалата в газофазной реакции между монооксидом углерода (СО) и метилнитритом (MN). Такой способ синтеза предусматривает подвергание сырьевого газа воздействию катализатора, описанного в п. 1 формулы изобретения. Взаимозаменяемо используемые в настоящем документе термины «сырьевой газ» и «исходный газ» относятся к газу, который вводится в химический технологический процесс. Температура реакции может составлять от 100 до 160°С, предпочтительно от 115 до 130°С. Давление реакции может составлять от 0,1 до 0,5 МПа, предпочтительно от 0,2 до 0,4 МПа. Сырьевой газ может представлять собой смесь метилнитрита (MN), монооксида углерода (СО) и азота (N2). Сырьевой газ может иметь молярное отношение CO/MN от 1:1 до 3:1, предпочтительно от 1,3 до 2,5. Сырьевой газ или исходный газ может содержать водород (Н2). Содержание Н2 может составлять до 500, 750, 1000, 1500 либо 2000 ч. на млн. Часовая объемная скорость газа (GHSV) [причем «часовая объемная скорость газа (GHSV)» идентична «объемно-пространственной скорости»] сырьевого газа может быть на уровне от 3000 до 10000 час-1, от 3200 до 8300 час-1 либо от 4000 до 6000 час-1. В результате осуществляется синтез оксалата.
Носитель, используемый в настоящем изобретении, состоит из полых микросфер из α-Al2O3. Данный носитель обладает большой удельной площадью поверхности, обеспечивающей равномерное распределение активного металла и вспомогательного металла по поверхности микросфер, а также эффектное снижение концентрации драгоценного металла и повышение активности и стабильности катализатора.
Органическое соединение активного металла, вспомогательного вещества и носителя может сделать катализатор устойчивым к присутствующему в исходном газе водороду без специального дегидрогенизационного устройства. Это благоприятно сказывается на сокращении инвестиций в подобное устройство и затрат на очистку исходного газа.
Во время направленной на синтез диметилоксалата реакции СО и метилнитрита (MN) представленный в данном изобретении катализатор обеспечивает высокий коэффициент конверсии MN, высокую селективность в отношении диметилоксалата, высокую стабильность и большой выход диметилоксалата.
Используемый в настоящем документе термин «коэффициент конверсии» относится к проценту метилнитрита (MN), превращающегося в продукт. Средний коэффициент конверсии MN представленного в соответствии с настоящим изобретением катализатора может составлять по меньшей мере примерно 90%, 95%, 96%, 97%, 98%, 99%, 99,5%, 99,9% или 100%, предпочтительно от 96 до 98%, на протяжении отрезка времени, например, по меньшей мере 500, 1000, 2000, 3000, 4000, 5000, 6000, 6000, 7000, 8000, 9000 или 10000 часов, предпочтительно по меньшей мере 6000 часов. При использованием представленного в настоящем изобретении катализатора вместо катализатора без полых микросфер из α-Al2O3 средний коэффициент конверсии MN может составлять по меньшей мере примерно 1%, 2%, 3%, 4% или 5% и выше на протяжении отрезка времени, например, по меньшей мере примерно 500, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000 или 10000 часов.
Используемый в настоящем документе термин «селективность» относится к проценту метилнитрита (MN), превращенного в целевой продукт, от общего объема метилнитрита (MN). Селективность представленного в соответствии с настоящим изобретением катализатора может составлять по меньшей мере примерно 95,0%, 96,0%, 97,0%, 98,0%, 99,0%, 99,5%, 99,9% или 100%, предпочтительно от 97,0 до 98,8%, на протяжении отрезка времени, например, по меньшей мере 500, 1000, 2000, 3000, 4000, 5000, 6000, 6000, 7000, 8000, 9000 или 10000 часов, предпочтительно по меньшей мере 6000 часов. При использованием представленного в настоящем изобретении катализатора вместо катализатора без полых микросфер из α-Al2O3 степень селективности катализатора в отношении диметилоксалата может составлять по меньшей мере примерно 1%, 2%, 3%, 4% или 5% и выше на протяжении отрезка времени, например, по меньшей мере 500, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000 или 10000 часов.
Используемый в настоящем документ термин «выход диметилоксалата за один проход в единицу времени» относится к получаемому количеству диметилоксалата на единицу объема (либо массы) катализатора на единицу времени. Выход диметилоксалата за один проход в единицу времени в результате синтеза, осуществляемого в соответствии с настоящим изобретением, может составлять по меньшей мере примерно 500, 1000 либо 2000 г⋅л-1⋅час-1. При использовании представленного в настоящем изобретении катализатор вместо катализатора без полых микросфер из α-Al2O3 выход диметилоксалата за один проход в единицу времени может составлять по меньшей мере 800, 1200 или 1600 г⋅л-1⋅час-1 и выше на протяжении отрезка времени, например, по меньшей мере 500, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000 или 10000 часов, предпочтительно, по меньшей мере 6000 часов.
В одном из вариантов осуществления содержание водорода в сырьевом газе составляло 1000 ч. на млн., а содержание NO - 12%. Температура реакции составляла от 115 до 128°С. Давление реакции составляло 0,3 МПа. Часовая объемная скорость газа (GHSV) может составлять 4000 час-1. Когда GHSV была увеличена до 6000 час-1, активность катализатора после 6000 часов стабильной работы не снизилась. Средний коэффициент конверсии MN составлял от 96 до 98%.
Термин «примерно», используемый в настоящем документе при упоминании измеряемого значения, например, количества, процента и тому подобного, предназначен для охвата отклонений в пределах ±20% либо ±10%, более предпочтительно - ±5%, еще более предпочтительно - ±1% и еще более предпочтительно - ±0,1% от указанного значения, поскольку такие отклонения соответствуют норме.
Образец 1. Катализатор 1
Был получен катализатор 1. С использованием глюкозы в качестве прекурсора был получен раствор глюкозы с концентрацией 1,2 моль/л. 2 л такого раствора глюкозы было на протяжении 10 часов выдержано при температуре 170°С. Полученная в итоге жидкость была подвергнута дегидратации, а также многократному промыванию деионизированной водой и этанолом. Полученное в результате твердое вещество было на протяжении 20 часов подвергнуто сушке при температуре 50°С, в результате чего был получен структурный прекурсор.
С использованием в качестве растворителя этанола был получен раствор нитрата алюминия с концентрацией 0,5 моль/л. 10,8 г такого структурного прекурсора было добавлено в 2 л раствора нитрата алюминия с последующей обработкой на протяжении 50 мин ультразвуком при температуре 25°С и с дальнейшим добавлением выдерживанием на протяжении 10 часов. Полученная в итоге жидкость была подвергнута дегидратации. Полученное в итоге твердое вещество было на протяжении 15 часов подвергнуто сушке при температуре 70°С и на протяжении 3,5 часов прокаливанию при температуре 380°С в азотной атмосфере, после чего она была подвергнута прокаливанию при 1150°С в воздушной атмосфере, в результате чего были получены используемые в качестве носителя полые микросферы из α-Al2O3.
Нитрат палладия и нитрат Bi в количествах, эквивалентных количествам, составляющим, соответственно, 0,25 вес. % и 0,60 вес. % катализатора, и 30 г носителя были растворены в деионизированной воде с дальнейшем использованием разведенной азотной кислоты для корректирования показателя рН получаемого в итоге раствора до уровня 2,3. Полученная в итоге жидкость при температуре 30°С была равномерно распылена по носителю. Затем полученный в итоге образец был на протяжении 9 часов подвергнут сушке при температуре 110°С с дальнейшим прокаливанием на протяжении 4 часов в воздушной среде при температуре 310°С, в результате чего был получен катализатор Pd-Bi/α-Al2CO3.
Методом МС ИСП было измерено содержание присутствующего в катализаторе активного компонента, а с помощью измерителя физико-химической адсорбции была измерена удельная площадь поверхности катализатора.
Перед оценкой катализатор был помещен в зону постоянной температуры в реакторе с неподвижным слоем из нержавеющей стали ϕ20 мм, где она был заполнена загрузкой катализатора в количестве 8,7 мл. При температуре восстановления 200°С при нормальном давлении была добавлена смесь водорода с азотом, молярное содержание водорода в которой составляло 15%, при этом величина расхода составляла 80 мл⋅мин-1⋅г-1 катализатора, а время восстановления - 8 часов, после чего катализатор был подвергнут продувке азотом и охлажден до температуры 120°С.
Как только в отходящих газах не осталось водорода, была запущена реакция. Реакция происходила в условиях исходного газа, который представлял собой газообразную смесь MN, СО и N2. Молярное отношение CO/MN составляло 1,8:1. Температура реакции составляла 120°С. Давление реакции составляло 0,3 МПа. Часовая объемная скорость газа (GHSV) составляла 6400 час-1.
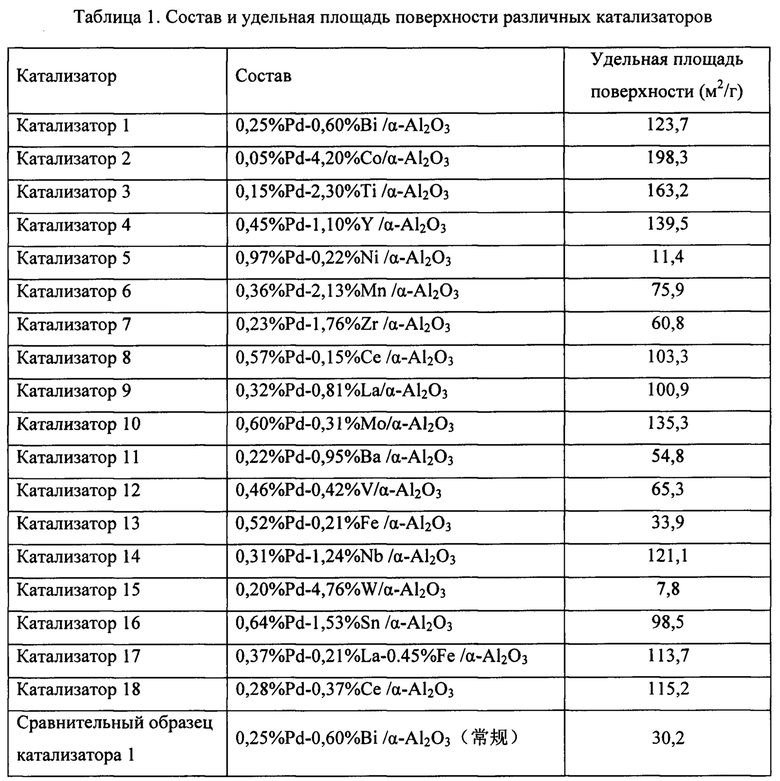
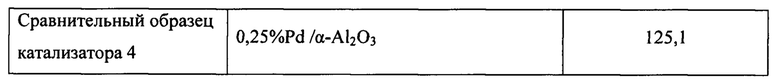
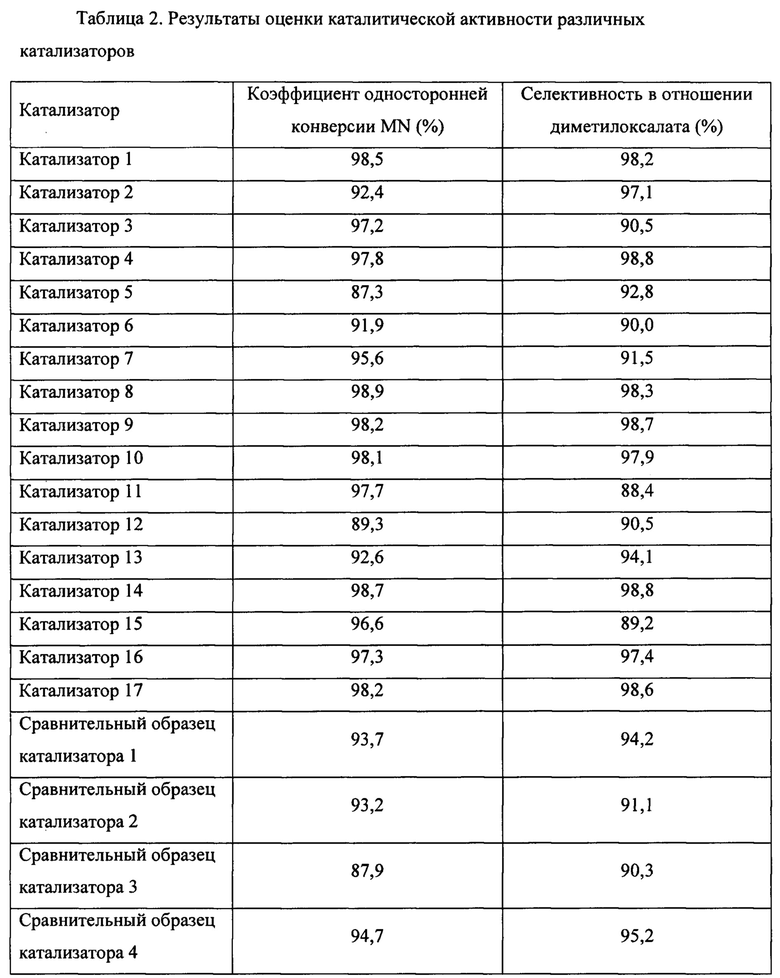
В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 2. Катализатор 2
Катализатор 2 был получен в соответствии со способом, описанным в образце 1, за исключением того, что глюкоза была заменена на мальтозу, а нитрат Bi был заменен на нитрат Со, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что давление реакции составляло 0,27 МПа, a GHSV - 4300 час-1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 3. Катализатор 3
Катализатор 3 был получен в соответствии со способом, описанным в образце 1, за исключением того, что глюкоза была заменена на фруктозу, а нитрат Bi был заменен на нитрат Ti, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что молярное отношение CO/MN составляло 1,25:1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 4. Катализатор 4
Катализатор 4 был получен в соответствии со способом, описанным в образце 1, за исключением того, что глюкоза была заменена на сахарозу, а нитрат Bi был заменен на нитрат Y, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что температура реакции составляла 128°С. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 5. Катализатор 5
Катализатор 5 был получен в соответствии со способом, описанным в образце 1, за исключением того, что глюкоза была заменена на фруктозу, а нитрат Bi был заменен на нитрат Ni, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что температура реакции составляла 103°С, a GHSV - 8100 час-1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 6. Катализатор 6
Катализатор 6 был получен в соответствии со способом, описанным в образце 1, за исключением того, что глюкоза была заменена на мальтозу, а нитрат Bi был заменен на нитрат Mn, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что давление реакции составляло 0,15 МПа, a GHSV - 3300 час-1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 7. Катализатор 7
Катализатор 7 был получен в соответствии со способом, описанным в образце 1, за исключением того, что глюкоза была заменена на сахарозу, а нитрат Bi был заменен на нитрат Zr, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что давление реакции составляло 0,35 МПа, a GHSV - 9700 час-1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 8. Катализатор 8
Катализатор 8 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на нитрат Се, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что молярное отношение CO/MN составляло 1,75:1, а температура реакции - 121°С. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 9. Катализатор 9
Катализатор 9 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на нитрат La, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что молярное отношение CO/MN составляло 1,75:1, a GHSV - 6900 час-1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 10. Катализатор 10
Катализатор 10 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на аммониевую соль Мо, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что давление реакции составляло 0,25 МПа, a GHSV - 5700 час-1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 11. Катализатор 11
Катализатор 11 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на нитрат Ва, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что температура восстановления составляла 175°С. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 12. Катализатор 12
Катализатор 12 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на нитрат V, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что время восстановления составляло 5 часов. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 13. Катализатор 13
Катализатор 13 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на нитрат Fe, а высушенное твердое вещество было на протяжении 2,8 часов подвергнуто прокаливанию при температуре 420°С в азотной атмосфере, а затем на протяжении 3,5 часов подвергнуто прокаливанию при температуре 1080°С в воздушной атмосфере, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что GHSV составляла 8400 час-1, давление реакции - 0,2 МПа, а температура реакции - 110°С. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 14. Катализатор 14
Катализатор 14 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на оксалат Nb, а используемая в получении катализатора разбавленная азотная кислота была заменена на лимонную кислоту, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что GHSV составляла 5500 час-1, давление реакции - 0,3 МПа, температура реакции - 148°С, а молярное отношение CO/MN - 1,6:1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 15. Катализатор 15
Катализатор 15 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на аммониевую соль W, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что GHSV составляла 4700 час-1, давление реакции - 0,5 МПа, температура реакции - 160°С, а молярное отношение СО/метилнитрат - 2,5:1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 16. Катализатор 16
Катализатор 16 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на хлорид Sn, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что GHSV составляла 7700 час-1, давление реакции - 0,18 МПа, температура реакции - 130°С, а молярное отношение СО/метилнитрат - 1,3:1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 17. Катализатор 17
Катализатор 17 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был заменен на нитрат La и ацетат Fe, а также был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что GHSV составляла 8300 час-1, давление реакции - 0,4 МПа, температура реакции - 115°С, а молярное отношение СО/метилнитрат - 1,3:1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 18. Катализатор 18
Катализатор 18 был получен в соответствии со способом, описанным в примере 1, за исключением того, что нитрат Bi был заменен на нитрат Се.
Перед оценкой катализатор был помещен в зону постоянной температуры в реакторе с неподвижным слоем из нержавеющей стали ϕ20 мм, где она был заполнена загрузкой катализатора в количестве 8,7 мл. При температуре восстановления 200°С при нормальном давлении была добавлена смесь водорода с азотом, молярное содержание водорода в которой составляло 15%, при этом величина расхода составляла 80 мл⋅мин-1⋅г-1 катализатора, а время восстановления - 8 часов, после чего катализатор был подвергнут продувке азотом и охлажден до температуры реакции.
Как только в отходящих газах не осталось водорода, была запущена реакция. Реакция происходила в условиях смеси MN, СО, N2 и Н2, обладающей молярным соотношением CO/MN на уровне 1,8:1. Содержание Н2 составляло 1000 ч. на млн. Содержание NO составляло 12%. Температура реакции составляла от 115 до 128°С, давление реакции - 0,3 МПа, a GHSV - от 4000 до 6000 час-1. Стабильная работа сохранялась на протяжении 6000 час, пока не снижалась активность катализатора. Средний коэффициент конверсии MN составлял от 96 до 98%. Средний выход диметилоксалата за один проход в единицу времени составлял не менее 1400 г на литр катализатора (L) в час (час).
Образец 19. Сравнительный образец катализатора 1
Сравнительный образец катализатора 1 был получен в соответствии со способом, описанным в образце 1, за исключением того, что носителем был выбран обычный альфа-оксид алюминия, а также был подвергнут оценке в соответствии со способом, описанным в образце 1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 20. Сравнительный образец катализатора 2
Сравнительный образец катализатора 2 идентичен сравнительному образцу катализатора 1, при этом он был подвергнут оценке в соответствии со способом, описанным в образце 1, за исключением того, что газообразная смесь дополнительно содержала Н2 в концентрации 1000 ч. на млн. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 21. Сравнительный образец катализатора 3
Сравнительный образец катализатора 3 идентичен сравнительному образцу катализатора 1, при этом он был подвергнут оценке в соответствии со способом, описанным в образце 20, за исключением того, что газообразная смесь дополнительно содержала NO в концентрации 10%. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 22. Сравнительный образец катализатора 4
Сравнительный образец катализатора 4 был получен в соответствии со способом, описанным в образце 1, за исключением того, что нитрат Bi был откинут, а также этот образец был подвергнут оценке в соответствии со способом, описанным в образце 1. В таблице 1 приведены данные по составу и удельной площади поверхности катализатора. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 23. Сравнительный образец катализатора 5
Сравнительный образец катализатора 5 идентичен сравнительному образцу катализатора 4, при этом он был подвергнут оценке в соответствии со способом, описанным в образце 20. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 24. Сравнительный образец катализатора 6
Сравнительный образец катализатора 6 идентичен сравнительному образцу катализатора 4, при этом он был подвергнут оценке в соответствии со способом, описанным в образце 21. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 25. Сравнительный образец катализатора 7
Сравнительный образец катализатора 7 идентичен катализатору 1, при этом он был подвергнут оценке в соответствии со способом, описанным в образце 20. В таблице 2 приведены данные по каталитической активности катализатора.
Образец 26. Сравнительный образец катализатора 8
Сравнительный образец катализатора 8 идентичен катализатору 1, при этом он был подвергнут оценке в соответствии со способом, описанным в образце 21. В таблице 2 приведены данные по каталитической активности катализатора.

Как показано в образцах 1-25, полые микросферы из a-Al2O3 в качестве носителя катализатора были получены в два этапа. Носитель обладал большой удельной площадью поверхности. Активный металл и вспомогательный металл могут быть равномерно распределены по поверхности микросфер. Таким образом можно эффективно снизить концентрацию драгоценного металла, а также повысить активность и стабильность катализатора. Органическое соединение активного металла, вспомогательного вещества и носителя могло бы сделать катализатор устойчивым к присутствующему в исходном газе водороду без необходимости в специальном дегидрогенизационном устройстве. Это благоприятно сказывается на сокращении инвестиций в такое оборудование и затрат на очистку исходного газа. Кроме того, катализатор обладает высоким коэффициентом конверсии MN при использования сырья с высоким содержанием NO, а также хорошей селективностью в отношении оксалата.
Представленный в данном изобретении катализатор может быть использован для ускорения реакции СО и метилнитрита, осуществляющейся в процессе синтеза диметилоксалата. Содержание водорода в сырьевом газе могло бы составлять 1000 ч. на млн., а содержание NO - 12%. Температура реакции могло бы составлять от 115 до 128°С, a GHSV - от 4000 до 6000 час-1. После 6000 часов стабильной работы активность катализатора не снижалась. Средний коэффициент конверсии MN составлял от 96 до 98%.
Хотя заявленное изобретение проиллюстрировано и описано в настоящем документе с упоминанием конкретных варианты осуществления, оно никак не ограничивается продемонстрированными характеристиками. Наоборот, в эти характеристики в пределах объема и диапазона эквивалентов формулы изобретения могут вноситься различные изменения без отступления от самого изобретения.
Изобретение относится к катализатору, предназначенному для синтеза оксалата посредством реакции связывания СО. Данный катализатор включает (a) активный компонент, содержащий палладий (Pd) либо его оксид; (b) вспомогательное вещество, содержащее вспомогательный элемент, выбранный из группы, состоящей из никеля, кобальта, марганца, циркония, церия, лантана, молибдена, бария, ванадия, титана, железа, иттрия, ниобия, вольфрама, олова и висмута; и (c) носитель, состоящий из полых микросфер из α-Al2O3. Также предлагаются способ получения указанного катализатора и способ его применения при синтезе оксалата в газфазной реакции между монооксидом углерода (СО) и метилнитритом (MN). Технический результат заключается в уменьшении концентрации драгоценного металла, увеличении активности и стабильности катализатора. 4 н. и 10 з.п. ф-лы, 2 табл.
1. Катализатор синтеза оксалата посредством реакции связывания СО, включающий:
(a) активный компонент, содержащий палладий (Pd) либо его оксид;
(b) вспомогательное вещество, содержащее вспомогательный элемент, выбранный из группы, состоящей из никеля, кобальта, марганца, циркония, церия, лантана, молибдена, бария, ванадия, титана, железа, иттрия, ниобия, вольфрама, олова и висмута; и
(c) носитель, состоящий из полых микросфер из α-Al2O3.
2. Катализатор по п. 1, в котором носитель обладает удельной площадью поверхности от 1 до 200 м2/г.
3. Катализатор по п. 1, где указанный катализатор состоит из активного компонента, содержание которого составляет от 0,005 до 1,000 вес. %, вспомогательного вещества, содержание которого составляет от 0,01 до 5,00 вес. %, и носителя.
4. Катализатор по п. 1, в котором вспомогательный элемент выбран из группы, состоящей из марганца, циркония, церия, лантана, ванадия, титана, иттрия, ниобия, олова и висмута.
5. Способ получения катализатора по п. 1, включающий:
(a) дегидратацию углеводного раствора с получением твердого углеводного образца, причем указанный углеводный раствор содержит углевод, имеющий карбонильную группу, гидроксильную группу или их сочетание;
(b) сушку твердого углеводного образца с получением структурного прекурсора;
(c) добавление структурного прекурсора в раствор нитрата алюминия с получением алюминиевого образца;
(d) дегидратацию алюминиевого образца с получением твердого алюминиевого образца;
(e) сушку твердого алюминиевого образца с получением высушенного твердого алюминиевого образца;
(f) прокаливание высушенного твердого алюминиевого образца с получением носителя, состоящего из полых микросфер из α-Al2O3;
(g) пропитывание носителя пропиточным раствором, содержащим активный компонент и вспомогательное вещество с получением смеси;
(h) сушку указанной смеси с получением высушенной смеси; и
(i) прокаливание указанной высушенной смеси с получением указанного катализатора.
6. Способ по п. 5, в котором углевод выбран из группы, состоящей из глюкозы, фруктозы, сахарозы и мальтозы.
7. Способ по п. 5, дополнительно включающий перед этапом (b) многократную промывку твердого углеводного образца деионизированной водой и этанолом.
8. Способ по п. 5, в котором структурный прекурсор добавляют в раствор нитрата алюминия при массовом соотношении структурный прекурсор/нитрат алюминия 1:(5-50).
9. Способ по п. 5, дополнительно включающий на этапе (с) ультразвуковую обработку алюминиевого образца и выдерживание его на протяжении от 8 до 20 час.
10. Способ по п. 5, дополнительно включающий растворение в деионизированной воде соли вспомогательного элемента и соли Pd с получением раствора активного компонента/вспомогательного вещества, и корректирование рН раствора активного компонента/вспомогательного вещества до значения от 1 до 5 с помощью разбавленной азотной кислоты, разбавленной соляной кислоты, щавелевой кислоты либо лимонной кислоты с получением пропиточного раствора, и распыление пропиточного раствора по носителю в объеме, равном объему носителя.
11. Способ по п. 10, в котором соль Pd выбрана из группы, состоящей из галогенида, нитрата, ацетата и ацетилацетоната.
12. Способ по п. 10, в котором соль вспомогательного элемента выбрана из группы, состоящей из хлорида, нитрата, ацетата, оксалата и аммониевой соли.
13. Способ восстановления катализатора синтеза оксалата в газофазной реакции между монооксидом углерода (СО) и метилнитритом (MN), включающий подвергание катализатора по п. 1 воздействию восстановительного газа на протяжении от 3 до 8 час при температуре от 130 до 220°С и при атмосферном давлении, причем восстановительный газ представляет собой смесь водорода (Н2) с азотом (N2), которая имеет молярное содержание Н2 от 5 до 30% и величину расхода от 40 до 80 мл/мин⋅г катализатора, в результате чего осуществляется восстановление катализатора.
14. Способ синтеза оксалата в газофазной реакции между монооксидом углерода (СО) и метилнитритом (MN), включающий подвергание сырьевого газа воздействию катализатора по п. 1 при температуре от 100 до 160°С и под давлением от 0,1 до 0,5 МПа, причем сырьевой газ представляет собой смесь метилнитрита (MN), монооксида углерода (СО) и азота (N2), которая имеет молярное соотношение CO/MN (1-3):1 и объемно-пространственную скорость от 3000 до 10000 час-1, в результате чего осуществляется синтез оксалата.
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЛАТА ГАЗОФАЗНЫМ СПОСОБОМ С УЧАСТИЕМ ОКСИДА УГЛЕРОДА | 2011 |
|
RU2554887C2 |
| US 20100197486 A1, 05.08.2010 | |||
| СПОСОБ СИНТЕЗА УГЛЕВОДОРОДОВ С5+ В ПРИСУТСТВИИ КАТАЛИЗАТОРА, ПОЛУЧЕННОГО ПРИ ПОМОЩИ ПО МЕНЬШЕЙ МЕРЕ ОДНОГО ЦИКЛИЧЕСКОГО ОЛИГОСАХАРИДА | 2011 |
|
RU2561112C2 |
| ПРОМОТИРОВАННЫЙ АЛЮМОСИЛИКАТНЫЙ КАТАЛИЗАТОР И УЛУЧШЕННЫЙ СПОСОБ ОБРАБОТКИ УГЛЕВОДОРОДНОГО СЫРЬЯ | 2005 |
|
RU2372984C2 |
Авторы
Даты
2019-10-04—Публикация
2018-10-22—Подача